-
植物化感作用是植物通过淋溶、挥发、残体分解和根系分泌等方式向环境释放化学物质,从而对周围植物产生直接或间接的、有害或有利的作用[1]。植物间的这种化学作用对作物增产、森林抚育、植物保护和生物防治等方面有着广泛的影响[2]。目前,植物化感作用已经成为一个十分活跃的研究领域,并且无论在广度还是深度上都取得了重要进展。在广度上,研究范围从集中于作物和入侵杂草不断向林木、园林绿化植物及水生植物拓展,以至几乎涵盖所以植物类群,植物与微生物间的化感作用也引起人们的广泛重视[3-8];在深度上经历了由化感现象的简单描述和证明到化感机制的阐释,再到初步应用于生产实践的过程[9]。虽然已经取得了许多成果,但植物化感作用领域依然存在大量空白,亟须开展更多更为系统深入的研究。园林植物是指具有一定观赏价值,适用于室内外布置,美化环境,改善环境,并丰富人们生活的植物。园林植物化感作用的研究对于园林植物配置的科学性和植物群落演替有着直接影响,同时也影响园林人工生态系统的稳定和功能发挥[10]。近年,园林植物化感作用逐渐引起人们的关注,白三叶Trifolium repens[2],百里香Thyme mandschuricus[11],小佛肚竹Bambusa ventricosa[12],火炬树Rhust typhina[8],万寿菊Tagetes erecta[13]等被报道具有较强化感作用。笔者曾筛选对44种常见园林植物的化感作用,发现红叶李Prunus ceraifera叶片水浸液具有较强的化感作用。红叶李为蔷薇科Rosaceae落叶乔木,又称紫叶李、樱桃李,其叶片常年紫红,是著名色叶树种。原产中亚及中国新疆天山一带,现作为园林植物栽培分布于北京以及山西、陕西、河南、江苏、山东等省的各大城市[14]。除用于园林绿化外,未见有关于红叶李其他用途的报道,这使得针对红叶李的研究和开发利用受到极大限制。红叶李化感作用的发现无疑有利于充分开发其应用潜力。本实验对红叶李的化感作用进行了更为全面的研究。以红叶李在园林中的伴生草坪植物白三叶,紫花苜蓿Medicago sativa,剪股颖Agrostis tenuis和黑麦草Lolium perenne等为受体,研究了红叶李不同器官及根际土壤水浸液的化感作用,旨在探究红叶李对伴生草坪植物的化感作用,为提高其园林配置水平提供可靠依据。
-
供体:红叶李的根、茎、叶及根际土壤,2013年9月采于郑州大学校园内。红叶李树高约3 m,胸径10 cm左右。受体:白三叶、紫花苜蓿、剪股颖和黑麦草。种子购于郑州陈寨花卉市场。
-
①不同器官水浸液置备。用清水将红叶李新鲜根、茎、叶冲洗干净,平铺晾干,剪成1 cm2小片(或1 cm小段),称取一定量并加入20倍蒸馏水,室温浸提24 h。4层纱布过滤得比例为50 g·L-1(鲜质量/体积)的浸提液,稀释为30,10,5 g·L-1。4 ℃冰箱保存备用。以上浸提液用于种子萌发实验,考虑到浸提液在土壤中作用可能减弱,将盆栽生长实验测试比例调整为100,50,30,10 g·L-1。②根际土壤水浸液置备。取适量红叶李根毛区的土壤,筛出杂质后风干,加入2倍于土样质量的蒸馏水室温浸提24 h,期间搅拌数次。双层滤纸过滤后比例定为500 g·L-1(质量/体积),梯度稀释为250,125 g·L-1,4 ℃冰箱保存备用。
-
①种子萌发实验。以滤纸为载体测试红叶李不同部位及根际土壤水浸液对4种草坪植物种子萌发的化感作用。将籽粒健康均一的受体种子冲洗干净,质量分数为10%次氯酸钠消毒2 min,再用蒸馏水洗5次,置于垫有2层滤纸的培养皿(直径d=9 cm)中。摆放种子30粒·皿-1,3次重复。加入浸提液6 mL·皿-1,用蒸馏水作对照。人工气候培养箱中25 ℃暗培养2~3 d(预实验确定白三叶2 d,其他3 d),每天记录发芽数,统计发芽率和发芽指数。②盆栽幼苗生长实验。以土壤为载体在光照培养室内测定红叶李鲜叶水浸液对4种草坪植物株高和生物量的影响。土壤选用砂性土壤,除杂风干,混匀后装于直径为8 cm的塑料盆中,播种一定量的种子,加适量清水培养。待幼苗出土后留长势一致的幼苗5株·盆-1,浇灌浸提液,清水为空白对照,重复4次。20 d后取10株·处理-1测量株高及鲜干质量。
-
采用Williamson等[15]的化感效应指数(IRI)来评价化感作用。计算公式为IRI=1-C/T(T>C);IRI=T/C-1(T≤C)。其中C为对照,是以蒸馏水培养的受体植物各项指标的平均值。T为处理值,是以浸提液培养的受体植物各项指标的平均值。当IRI>0时表示浸提液具有促进作用,IRI<0时具有抑制作用。IRI的绝对值代表作用强度的大小。另外,为了综合评价受体植物对红叶李的敏感效应,采取鲍根生等[16]的相加平均法。采用SPSS 16.0软件进行统计分析,用平均数和标准误表示测定结果,分别对各项测试结果进行单因素方差分析,并用Duncan法对各测定数据进行多重比较:采用Excel 2007作图。
-
由表 1可知:在测试比例下红叶李不同器官水浸液对白三叶种子萌发都具有极显著的抑制作用,且不同器官的抑制程度有所差异。发芽率和发芽指数能一致地反应出不同器官的强弱次序,但发芽指数更为敏感(落叶除外)。叶片的作用最强,综合效应(ESE)为-0.96,其次是根,茎的作用相对最弱,ESE值为-0.51。叶与根的化感活性间没有显著差异,但都极显著高于茎的化感活性。这反应出化感物质在红叶李体内的分布情况,可能叶片和根是化感物质合成或聚集的重要场所。红叶李落叶同样具有较高的化感作用,这说明落叶分解可能是红叶李化感物质释放的一种途径。
表 1 红叶李不同器官水浸液对白三叶种子萌发的影响
Table 1. Effect of 50 g·L-1 water extract from different organs of Prunus ceraifera on seed germination of Trifolium repens
供体 发芽率/% IRI值 发芽指数 IRI值 ESE值 对照 61.11±6.19 aA 18.17±1.48 aA 根 5.55±0.22 cC -0.91 0.83±0.33 cdC -0.95 -0.93 茎 37.78±1.11 bB -0.38 6.67±0.73 bB -0.63 -0.51 叶 3.33±0.93 cC -0.95 0.50±0.29 dC -0.97 -0.96 落叶 11.11±1.44 cC -0.82 4.67±0.19 bcBC -0.74 -0.78 说明:水浸液质量浓度为50 g·L-1。数据后小写字母分别表示在5#水平差异显著性,大写字母分别表示在1$水平差异显著性 -
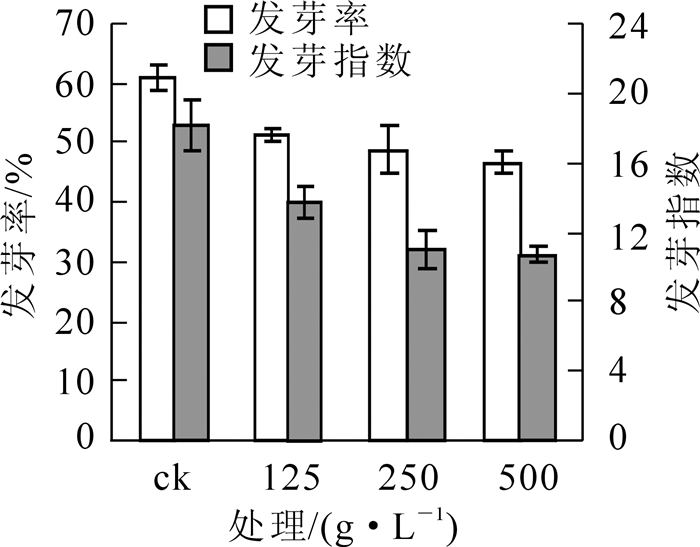
随着红叶李根际土壤水浸液浓度的增加,白三叶种子的发芽率和发芽指数呈现出逐渐下降的趋势(图 1),且发芽指数下降更明显,但对发芽率的抑制作用在各比例下都没有达到显著水平。发芽指数在125 g·L-1时即受到显著抑制,在250,500 g·L-1时抑制作用达到极显著水平,IRI值分别为-0.39,-0.41。这再次证明发芽指数对化感作用较发芽率敏感,说明红叶李化感物质延缓种子萌发的作用要强于遏止种子萌发。
-
结合表 2和表 3可知:红叶李叶片水浸液对不同植物种子萌发的作用不同,且在不同比例浸提液时的作用效果也存在较大差别。整体上可分为2种情况:对白三叶和紫花苜蓿的抑制作用及对剪股颖和黑麦草的“低促高抑”效应。白三叶和紫花苜蓿的发芽率及发芽指数随浸提液比例的升高而逐渐降低(但在10 g·L-1时抑制作用却异常降低甚至出现促进作用),对白三叶的影响明显比紫花苜蓿大。白三叶的发芽率在5 g·L-1时即受到显著的抑制,IRI值为-0.33;紫花苜蓿的发芽率只有在最高比例50 g·L-1时受到的抑制作用才达到显著水平,IRI值为-0.20。在5 g·L-1时,剪股颖和黑麦草种子萌发受到不同程度的促进作用,但都未达到显著水平;在50 g·L-1时,发芽率和发芽指数受到显著或极显著的抑制作用。这提示红叶李化感物质对单子叶植物和双子叶植物可能具有不同的作用机制。
表 2 红叶李叶片水浸液对4种草坪植物种子萌发的影响
Table 2. Effect of water extract from leaves of Prunus ceraifera on seed germination of four turfgrass plants
处理/(g·L-1) 发芽率/% 发芽指数 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 对照 61.11±6.19 60.00±3.85 44.44±4.84 85.56±2.94 18.17±1.48 16.33±0.82 5.61±0.36 17.78±1.46 aAB a abAB a bAB aA aAB aA 5 41.11±4.84 51.11±1.11 61.11±2.94 85.56±1.11 13.17±1.30 13.00±0.06 6.78±0.31 18.06±0.59 bBC ab aA a bcBD bcAB aA aA 10 65.56±4.44 57.78±2.94 45.56±4.84 82.22±4.01 22.50±2.85 13.28±0.58 7.00±0.55 13.34±2.19 aA ab abAB a aA bAB aA aAB 30 27.78±2.01 53.33±5.09 31.11±1.11 82.22±6.19 9.25±1.48 10.17±1.64 3.00±0.11 15.84±1.14 bC ab bcBC a cC cdBC bBC aAB 50 3.33±1.03cD 47.78±1.11
b20.00±3.82
cC60.00±5.00
b0.50±0.09
dD8.45±0.68
dC2.17±0.14
bC9.83±1.17
bB说明:数据后小写字母分别表示在5%水平差异显著性,大写字母分别表示在1%水平差异显著性。 表 3 红叶李叶片水浸液对4种草坪植物种子萌发的化感作用
Table 3. Allelopathic effects of water extract from leaves of Prunus ceraifera on seed germination of four turfgrass plant
处理/(g·L-1) 对发芽率的化感作用(IRI) 对发芽指数的化感作用(IRI) 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 5 -0.33 -0.15 0.38 0.00 -0.28 -0.20 0.21 0.01 10 0.07 -0.04 0.03 -0.04 0.24 -0.19 0.25 -0.25 30 -0.55 -0.11 -0.30 -0.04 -0.49 -0.38 -0.47 -0.11 50 -0.95 -0.20 -0.55 -0.30 -0.97 -0.48 -0.61 -0.45 -
由表 4和表 5可以看出:在测试比例范围内,红叶李对白三叶和紫花苜蓿幼苗的生长主要表现为促进作用,对剪股颖和黑麦草则主要表现为抑制作用,而这正好与对4种植物种子萌发的作用效果截然相反。这可能是由于红叶李化感物质对单子叶植物和双子叶植物幼苗生长的作用机制不同,且与对种子萌发的作用机制不同。白三叶幼苗的干质量随浸提液比例在升高受到的促进作用逐渐增强,在100 g·L-1时促进了101%,对株高的促进作用不明显。紫花苜蓿的株高、鲜质量和干质量随比例在升高受到的促进作用则都逐渐减弱,株高受到的促进作用由32%减为1%,干质量由127%减为18%。剪股颖和黑麦草的幼苗生长大体上随比例升高受到的抑制作用逐渐增强,剪股颖受到抑制程度较黑麦草高。
表 4 红叶李叶片水浸提对4种草坪植物幼苗生长的影响
Table 4. Effect of water extract from leaves of Prunus ceraifera on seeding growth of four turfgrass plants
处理/ (g·L-1) 株高/cm 鲜质量/(mg·株-1) 干质量/(mg·株-1 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 对照 2.96 5.38 4.13 18.51 11.90 25.20 1.30 36.50 1.30 2.22 0.24 4.05 10 3.21 7.08 3.60 17.88 13.40 37.70 1.30 40.30 1.51 5.03 0.17 3.74 30 3.50 6.89 4.01 16.00 15.80 35.70 1.20 36.40 1.63 4.11 2.10 3.22 50 3.18 4.96 3.62 17.67 14.90 27.60 0.90 32.80 1.81 3.06 0.27 2.92 100 3.13 5.41 3.53 17.16 15.40 25.70 0.70 34.60 2.61 2.63 0.22 3.11 表 5 红叶李叶片水浸提对4种草坪植物幼苗生长的化感作用
Table 5. Allelopathic effects of water extract from leaves of Prunus ceraifera on seeding growth of four turfgrass plants
处理/ (g·L-1) 对株高的化感作用(IRI) 对鲜质量的化感作用(IRI) 对干质量的化感作用(IRI) 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 10 0.08 0.32 -1.3 -0.3 1.3 5.0 0.0 1.0 1.6 12.7 -9.3 -0.8 30 0.18 0.28 -0.3 -1.4 3.3 4.2 -0.8 0.0 2.5 8.5 -1.3 -2.0 50 0.07 -0.08 -1.2 -0.5 2.5 1.0 -3.1 -1.0 3.9 3.8 -8.9 -2.8 100 0.06 0.01 -1.5 -0.7 2.9 0.2 -4.6 -0.5 10.1 1.8 -9.1 -2.3 -
一级敏感指数(M1)反应了4种植物不同测定指标对红叶李化感作用的敏感性,5项指标受抑制程度为萌发率>萌发指数>株高>株干质量>株鲜质量,其中株高、株干质量、株鲜质量表现为轻微的促进作用。4种植物发芽率受抑制程度强弱次序为剪股颖>白三叶>紫花苜蓿>黑麦草,其中剪股颖最敏感,敏感指数为-0.55;黑麦草最不敏感。敏感指数为-0.09。二级敏感指数(M2)反应了4种植物种子萌发期和幼苗生长期对红叶李水浸液化感作用的平均敏感指数,分别为-0.28,0.05。表明红叶李化感物质对种子萌发主要表现为强烈抑制作用,对幼苗生长表现为轻微促进作用。4种植物萌发期受抑制最强的是白三叶,平均敏感指数为-0.41,其次是剪股颖,黑麦草最弱。白三叶和紫花苜蓿在生长期受到强烈的促进作用,剪股颖和黑麦草则受到不同程度的抑制作用。值得注意的是,白三叶和紫花苜蓿在萌发期和生长期受到的作用恰好相反。三级敏感指数(M3)反应了4种植物在物种水平上对红叶李水浸液化感作用的综合敏感性,平均敏感指数为-0.12。说明红叶李的化感物质对4种植物主要表现为抑制作用。4种植物对红叶李化感作用的敏感性强弱顺序为剪股颖>黑麦草>白三叶>紫花苜蓿,其中紫花苜蓿的平均敏感指数为正值,其余均为负值(表 6)。
表 6 4种植物对红叶李水浸液化感作用的敏感指数
Table 6. Assessment of sensitivity of four turfgrass plants to allelopathy of water extract from leaves of Prunus ceraifera
植物 三级敏感指数M3 二级敏感指数M2 一级敏感指数M1 物种水平 萌发期 生长期 发芽率 发芽指数 株高 株鲜质量 株干质量 白三叶 -0.07 -0.41 0.27 -0.44 -0.38 0.10 0.25 0.45 紫花苜蓿 0.07 -0.22 0.35 -0.13 -0.31 0.13 0.26 0.67 剪股颖 -0.36 -0.36 -0.35 -0.55 -0.16 -0.11 -0.21 -0.72 黑麦草 -0.12 -0.15 -0.09 -0.09 -0.20 -0.07 -0.01 -0.20 平均 -0.12 -0.28 0.05 -0.30 -0.26 0.01 0.07 0.05 -
植物的化感物质几乎分布在各个部位,但主要存在于叶片和根内,这是与植物主要通过叶片和根系释放其化感物质相一致[17]。红叶李叶片和根水浸液的化感作用最强。根际土壤也具有一定的化感作用,这说明其化感物质确实释放到了环境中且能够抑制其他植物种子的萌发。化感作用对受体植物的影响是多方面的,能抑制或延缓种子萌发、影响幼苗正常生长发育。已有研究表明:化感物质首先作用于植物根细胞的细胞膜,通过细胞膜功能的改变进而影响植物的生理生化代谢活动,包括呼吸作用、光合作用、离子吸收、蛋白质合成、激素代谢、基因表达等,最终抑制(或促进)植物的生长发育。红叶李水浸液能延缓和抑制白三叶、紫花苜蓿、黑麦草和剪股颖种子的萌发,但其对4种植物生长的影响却不同。对白三叶和紫花苜蓿表现出促进作用,而抑制黑麦草和剪股颖幼苗的生长。这说明红叶李的化感物质对不同植物生长的影响存在较大差异,且对某些植物在其不同生长期的效应可能完全相反。化感作用对不同植物的影响不同与前人研究结果一致[18],但抑制种子萌发促进生长的现象比较少见,很值得注意。在园林配置中可以巧妙地利用这些关系;红叶李附近不宜播种这4种草坪植物,也不宜移栽黑麦草和剪股颖,但栽植白三叶和紫花苜蓿则会有利于幼苗生长。
本实验只测试了红叶李对受体萌发和生长影响的一些形态学指标,其化感作用的生理生化机制,尤其对萌发期和生长期不同作用的机制有待深入研究。红叶李的化感物质也需要进行分离鉴定。
Allelopathic effects of Prunus cerasifera on four turfgrass plants
-
摘要: 研究了园林植物红叶李Prunus ceraifera不同器官及根际土壤水浸液对白三叶Trifolium repens, 紫花苜蓿Medicago sativa, 剪股颖Agrostis tenuis和黑麦草Lolium perenne等种子萌发和幼苗生长的影响, 其中种子萌发实验采用培养皿滤纸法, 幼苗生长实验采用温室盆栽法。结果表明:在50 g·L-1浸提液质量浓度下, 红叶李根、茎、叶水浸液对白三叶种子萌发具有极显著的抑制作用, 强弱顺序为叶>根>茎; 红叶李落叶和根际土壤水浸液对白三叶种子萌发也具有较强抑制作用; 在测试质量浓度范围内, 红叶李叶片水浸液对白三叶和紫花苜蓿种子萌发表现为抑制作用, 对剪股颖和黑麦草则表现出"低促高抑"效应; 红叶李叶片水浸液对白三叶和紫花苜蓿幼苗的生长主要表现为促进作用, 对剪股颖和黑麦草则主要表现为抑制作用; 4种植物对红叶李化感作用的平均敏感性强弱顺序为剪股颖>黑麦草>白三叶>紫花苜蓿, 其中紫花苜蓿的平均敏感指数为正值, 其余均为负值。结果为从化感角度提高红叶李的园林配置水平提供了依据。Abstract: To understand the chemical relationships of Prunus cerasifera with others turfgrass plants, the allelopathic effects of an aqueous extract from different organs and rhizosphere soil of P. cerasifera on seed germination and seedling growth of four turfgrass plants:Trifolium repens, Medicago sativa, Agrostis tenuis, and Lolium perenne, were studied. Seed germination was tested indoors using a biological monitoring method, and seedling growth was tested in a pot experiment. Results indicated that the root, stem, and leaf aqueous extracts of P. cerasifera at 0.05 g·mL-1 concentration significantly inhibited (P < 0.01) seed germination of T. repens with leaf> root> stem. Leaf litter and rhizosphere soil extracts of P. cerasifera also had a strong inhibition on seed germination of T. Repens. Leaf extracts inhibited seed germination of T. repens and M. Sativa with A. tenuis and L. perenne being promoted at lower concentration and being inhibited at higher concentration. For seedling growth, leaf extracts promoted T. repens and M. sativa, and inhibited A. tenuis and L. perenne. Overall the allelopathic sensitivity was in the order of A. tenuis> L. perenne> T. repens> M. sativa. Additionally, the overall allelopathic sensitivity of M. sativa was positive, but the others were negative. These results provide a basis for allelopathic application of P. cerasifera.
-
Key words:
- botany /
- garden plants /
- Prunus cerasifera /
- turfgrass plants /
- allelopathy
-
表 1 红叶李不同器官水浸液对白三叶种子萌发的影响
Table 1. Effect of 50 g·L-1 water extract from different organs of Prunus ceraifera on seed germination of Trifolium repens
供体 发芽率/% IRI值 发芽指数 IRI值 ESE值 对照 61.11±6.19 aA 18.17±1.48 aA 根 5.55±0.22 cC -0.91 0.83±0.33 cdC -0.95 -0.93 茎 37.78±1.11 bB -0.38 6.67±0.73 bB -0.63 -0.51 叶 3.33±0.93 cC -0.95 0.50±0.29 dC -0.97 -0.96 落叶 11.11±1.44 cC -0.82 4.67±0.19 bcBC -0.74 -0.78 说明:水浸液质量浓度为50 g·L-1。数据后小写字母分别表示在5#水平差异显著性,大写字母分别表示在1$水平差异显著性 表 2 红叶李叶片水浸液对4种草坪植物种子萌发的影响
Table 2. Effect of water extract from leaves of Prunus ceraifera on seed germination of four turfgrass plants
处理/(g·L-1) 发芽率/% 发芽指数 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 对照 61.11±6.19 60.00±3.85 44.44±4.84 85.56±2.94 18.17±1.48 16.33±0.82 5.61±0.36 17.78±1.46 aAB a abAB a bAB aA aAB aA 5 41.11±4.84 51.11±1.11 61.11±2.94 85.56±1.11 13.17±1.30 13.00±0.06 6.78±0.31 18.06±0.59 bBC ab aA a bcBD bcAB aA aA 10 65.56±4.44 57.78±2.94 45.56±4.84 82.22±4.01 22.50±2.85 13.28±0.58 7.00±0.55 13.34±2.19 aA ab abAB a aA bAB aA aAB 30 27.78±2.01 53.33±5.09 31.11±1.11 82.22±6.19 9.25±1.48 10.17±1.64 3.00±0.11 15.84±1.14 bC ab bcBC a cC cdBC bBC aAB 50 3.33±1.03cD 47.78±1.11
b20.00±3.82
cC60.00±5.00
b0.50±0.09
dD8.45±0.68
dC2.17±0.14
bC9.83±1.17
bB说明:数据后小写字母分别表示在5%水平差异显著性,大写字母分别表示在1%水平差异显著性。 表 3 红叶李叶片水浸液对4种草坪植物种子萌发的化感作用
Table 3. Allelopathic effects of water extract from leaves of Prunus ceraifera on seed germination of four turfgrass plant
处理/(g·L-1) 对发芽率的化感作用(IRI) 对发芽指数的化感作用(IRI) 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 5 -0.33 -0.15 0.38 0.00 -0.28 -0.20 0.21 0.01 10 0.07 -0.04 0.03 -0.04 0.24 -0.19 0.25 -0.25 30 -0.55 -0.11 -0.30 -0.04 -0.49 -0.38 -0.47 -0.11 50 -0.95 -0.20 -0.55 -0.30 -0.97 -0.48 -0.61 -0.45 表 4 红叶李叶片水浸提对4种草坪植物幼苗生长的影响
Table 4. Effect of water extract from leaves of Prunus ceraifera on seeding growth of four turfgrass plants
处理/ (g·L-1) 株高/cm 鲜质量/(mg·株-1) 干质量/(mg·株-1 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 对照 2.96 5.38 4.13 18.51 11.90 25.20 1.30 36.50 1.30 2.22 0.24 4.05 10 3.21 7.08 3.60 17.88 13.40 37.70 1.30 40.30 1.51 5.03 0.17 3.74 30 3.50 6.89 4.01 16.00 15.80 35.70 1.20 36.40 1.63 4.11 2.10 3.22 50 3.18 4.96 3.62 17.67 14.90 27.60 0.90 32.80 1.81 3.06 0.27 2.92 100 3.13 5.41 3.53 17.16 15.40 25.70 0.70 34.60 2.61 2.63 0.22 3.11 表 5 红叶李叶片水浸提对4种草坪植物幼苗生长的化感作用
Table 5. Allelopathic effects of water extract from leaves of Prunus ceraifera on seeding growth of four turfgrass plants
处理/ (g·L-1) 对株高的化感作用(IRI) 对鲜质量的化感作用(IRI) 对干质量的化感作用(IRI) 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 白三叶 紫花苜宿 剪股颖 黑麦草 10 0.08 0.32 -1.3 -0.3 1.3 5.0 0.0 1.0 1.6 12.7 -9.3 -0.8 30 0.18 0.28 -0.3 -1.4 3.3 4.2 -0.8 0.0 2.5 8.5 -1.3 -2.0 50 0.07 -0.08 -1.2 -0.5 2.5 1.0 -3.1 -1.0 3.9 3.8 -8.9 -2.8 100 0.06 0.01 -1.5 -0.7 2.9 0.2 -4.6 -0.5 10.1 1.8 -9.1 -2.3 表 6 4种植物对红叶李水浸液化感作用的敏感指数
Table 6. Assessment of sensitivity of four turfgrass plants to allelopathy of water extract from leaves of Prunus ceraifera
植物 三级敏感指数M3 二级敏感指数M2 一级敏感指数M1 物种水平 萌发期 生长期 发芽率 发芽指数 株高 株鲜质量 株干质量 白三叶 -0.07 -0.41 0.27 -0.44 -0.38 0.10 0.25 0.45 紫花苜蓿 0.07 -0.22 0.35 -0.13 -0.31 0.13 0.26 0.67 剪股颖 -0.36 -0.36 -0.35 -0.55 -0.16 -0.11 -0.21 -0.72 黑麦草 -0.12 -0.15 -0.09 -0.09 -0.20 -0.07 -0.01 -0.20 平均 -0.12 -0.28 0.05 -0.30 -0.26 0.01 0.07 0.05 -
[1] RICE E L. Allelopathy[M]. New York:Academic Press Inc, 1984:1-5. [2] 郑洁, 刘芳, 吴兴波, 等.白三叶叶片水浸提液对几种园林植物的化感作用[J].浙江农林大学学报, 2014, 31(1):19-27. ZHENG Jie, LIU Fang, WU Xingbo, et al. Research of the aquatic extract from leaves of Trifolium repens to several garden plants[J]. J Zhejiang A & F Univ, 2014, 31(1):19-27. [3] WESTON L A. Utilization of allelopathy for weed management in agroecosystems[J]. Agron J, 1996, 88(6):860-866. [4] VIVANCO J M, BAIS H P, STERMITZ F R, et al. Biogeographical variation in community response to root allelochemistry:novel weapons and exotic invasion[J]. Ecol Lett, 2004, 7(4):285-292. [5] 吴秀华, 李羿桥, 胡庭兴, 等.巨桉凋落叶分解初期对菊苣生长和光合特性的影响[J].应用生态学报, 2013, 24(7):1817-1825. WU Xiuhua, LI Yiqiao, HU Tingxing, et al. Effects of Eucalyptus grandis leaf litter at its early stage of decomposition on the growth and photosynthetic characteristics of Cichorium intybus[J]. Chin J Appl Ecol, 2013, 24(7):1817-1825. [6] 王霞, 罗小勇.海桐不同器官除草活性的研究[J].中国生态农业学报, 2011, 19(4):982-984. WANG Xia, LUO Xiaoyong. Herbicidal activities of different organs of Pittosporum tobira (Thunb.) Ait[J]. Chin J Eco-Agric, 2011, 19(4):982-984. [7] ALAMSJAH M A, HIRAO S, ISHIBASHI F, et al. Isolation and structure determination of algicidal compounds from Ulva fasciata[J]. Biosci Biotechnol Biochem, 2005, 69(11):2186-2192. [8] 侯玉平, 柳林, 王信, 等.外来植物火炬树水浸液对土壤微生态系统的化感作用[J].生态学报, 2013, 33(13):4041-4049. HOU Yuping, LIU Lin, WANG Xin, et al. Allelopathic effects of aqueous extract of exotic plant Rhus typhina L. on soil microecosystem[J]. Acta Ecol Sin, 2013, 33(13):4041-4049. [9] CHEEMA Z A, KHALIQ A. Use of sorghum allelopathic properties tocontrol weeds in irrigated wheat in a semi arid region of Punjab[J]. Agric Ecos Environ, 2000, 79(7):105-112. [10] 张岚, 高素萍.园林植物化感作用研究现状与问题探讨[J].浙江林学院学报, 2007, 24(4):497-503. ZHANG Lan, GAO Suping. Review of researches on allelopathy of ornamental plants[J]. J Zhejiang For Coll, 2007, 24(4):497-503. [11] 王玲, 马喜娟, 张秀珍.东北百里香化感作用[J].东北林业大学学报, 2012, 40(7):41-44. WANG Ling, MA Xijuan, ZHANG Xiuzhen. Allelopathy of Thymus mandschuricus[J]. J Northeast For Univ, 2012, 40(7):41-44. [12] 王淑英.竹叶化感作用及小佛肚竹化感物质的分离[D].北京:中国林业科学研究院, 2010. WANG Shuying. Allelopathy on Bamboo Leaves and Isolation of Allelochemieals from Bambusa ventricosa Leaves[D]. Beijing:Chinese Aeademy of Forestry, 2010. [13] KIRAN K, KAUL K. Autotoxicity in Tagetes erecta L. on its own germination and seeding growth[J]. Allelopathy J, 2000, 7(1):109-113. [14] 丛志强, 侯潘杰.红叶李人工栽培丰产技术[J].中国林副特产, 2011(6):64-65. CONG Zhiqiang, HOU Panjie. High-yielding cultivation technique of Prunus ceraifera[J]. For By-Prod Spec China, 2011(6):64-65. [15] WILLIAMSON G B, RICHARDSON D. Bioassays for allelopathy:measuring treatment responses with independent controls[J]. J Chem Ecol, 1988, 14(1):181-187. [16] 鲍根生, 王宏生.甘肃马先蒿对高寒地区几种优良牧草的化感作用[J].中国草地学报, 2011, 33(3):88-94. BAO Gensheng, WANG Hongsheng. Allelopathic effects of Pedicularis kansuensis Maxim on several graminaceous grass species on alpine meadow[J]. Chin J Grassland, 2011, 33(3):88-94. [17] 张学文, 刘亦学, 刘万学, 等.植物化感物质及其释放途径[J].中国农学通报, 2007, 23(7):295-297. ZHANG Xuewen, LIU Yixue, LIU Wanxue, et al. Allelochemicals and its releasing modes[J]. Chin Agric Sci Bull, 2007, 23(7):295-297. [18] YANG Qinqin, MIAO Lihua. HONG Chuntao, et al. Allelopathic effects of Hydrocotyle vulgaris extract on seed germination and seeding growth[J]. J Zhejiang A & F Univ, 2013, 30(3):354-358. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.2014.05.008







 下载:
下载: