-
随着社会经济与城市化的快速发展,人类活动造成的水体污染已成为全球重要的环境污染问题之一。面源污染是水体污染的主要表现形式之一,而农业面源污染是面源污染的主要来源[1]。作为农业大国,中国化肥使用量逐年增长。据统计,2015年全年使用量已高达6 022.6万t,农用化肥单位面积平均施用量已达458.6 kg·hm-2,是安全上限(225 kg·hm-2)的2.04倍,但化肥利用率仅为30%~40%[2],导致化肥中大部分营养元素进入水体,造成水体氮、磷污染。因此,如何治理农业面源污染已成为目前环境治理的重难点问题。许多研究表明:位于水陆交界处的河岸植被缓冲带可以有效截留和清除面源污染中的氮磷[3-6],被认为是控制非点源污染的最佳管理措施之一[7]。河岸植被缓冲带通过沉积、土壤吸附、植物吸收、反硝化作用和微生物固定等途径,有效截留和清除氮等面源污染物质。目前,国内外学者在河岸缓冲带氮素截留方面已做了诸多研究。SPRUILL[8]对小流域的河岸植被缓冲带进行研究时,发现其能移除地表水中95%以上的氮元素,其中反硝化作用去除的氮元素占65%~70%;KOVACIC等[9]研究发现:森林和草地河岸缓冲带对浅层地下水中硝态氮的截留率达90%以上,其中森林河岸缓冲带对硝态氮的截留转化能力高于草地河岸缓冲带;WANG等[10]研究表明:林地和草地缓冲带主要通过显著减少土壤表面径流量有效去除水分和养分。国内研究起步虽然较晚,但也取得了一些成果。陈金林等[11]研究发现:农田与沟渠间的缓冲林带有利于截留和净化土壤径流中的氮、磷等物质,不同林带宽度对农业非点源污染的防治效果不同;王庆成等[12]研究表明:农田背景下的森林河岸带土壤反硝化强度最大,硝态氮消失率的变化范围为46.79%~91.13%,且河岸带表层土壤的反硝化强度大于底层;林晓晟[13]在流域尺度上利用有限元数值模技术构建了HYDRUS2D/3D模型,提出丘陵区河岸缓冲带的宽度为15~60 m,平原区河岸缓冲带宽度为5~20 m,可有效截留氮、磷污染物。总体而言,学者大多基于景观甚至流域尺度上研究河岸植被缓冲带的功能及其影响因素,很少在林分水平上开展缓冲带削减面源污染的研究。且在有关湖泊周围地势较为平坦的河岸缓冲带截留养分和沉积物的研究较少[14]。因此,本研究以太湖不同宽度的林地河岸缓冲带为对象,研究其对径流水及土壤中氮素截留效果的影响,以期为适宜河岸缓冲带宽度的设计提供参考。
-
研究区位于江苏省宜兴市周铁镇沙塘港村(31°07′~31°37′N,119°31′~120°03′E),该区紧邻太湖。气候类型为亚热带季风气候,温和湿润,雨水充沛,四季分明。主导风向为东南风,无霜期239 d,年平均气温为15.7 ℃,年均日照时数为1 924.2 h,作物生长季积温5 475.8 ℃。降水集中在春季和夏季,6和8月多暴雨。年均降水量为1 177.0 mm。地表、地下水丰富。研究区土壤为中性黄壤,土质均匀,土壤容积密度为1.38 g·cm-3,样地坡度比为1:250。周边居民主要以农业为主,主要种植水稻Oryza sativa,小麦Triticum aestivum和油菜Brassica napus等农作物。
-
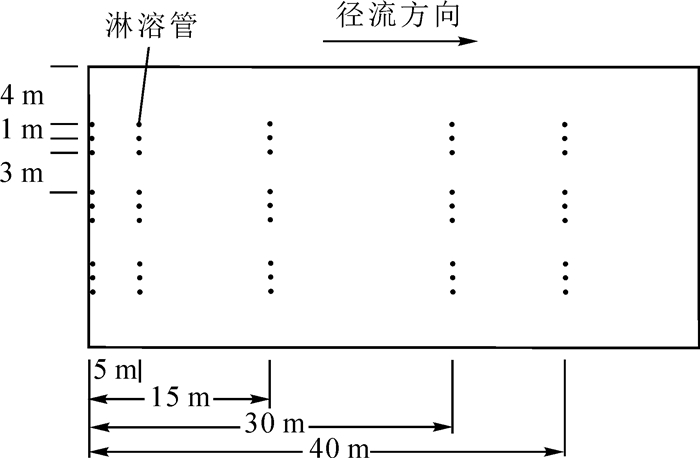
在样地设置4个20 m × 50 m的小区,小区之间间隔5 m,并用宽60 cm,厚1.5 cm的复合板分隔,避免相互干扰(图 1)。小区平行排列,依次为荒地、1 000株·hm-2的中山杉Taxodium hybrid ‘Zhongshanshan’-‘南林95’杨Populus × euramericana‘Nanlin 95’混交林、1 000株·hm-2的中山杉林和1 000株·hm-2的杨树林。所选树种为太湖流域常见树种,树龄均为5 a,杨树平均树高为4.0 m,胸径为5.0 cm,平均冠幅为135 cm,中山杉平均树高为3.0 m,胸径为4.0 cm,冠幅为105 cm。在每个样地小区距样地起始端(沿径流水方向)0,5,15,30,40 m宽度处分别埋设3组聚氯乙烯淋溶管,3个·组-1,深度分别为20,40和60 cm,用于径流水样的采集。
在每块样地小区前0至0.5 m处,参照当地农田施肥量进行施肥,模拟氮素流失状况。所施复合肥氮磷钾比例为16:8:16,施肥量为48 kg·hm-2。在降雨前施肥,降雨产流后采样,施肥与采样间隔1周。样品采集选择在当地的雨季(4-9月)进行采集,3次采样时间分别是2016年4月21-23日,7月9-11日以及9月23-24日。采样期间前1周平均降水量分别为57.7,87.7和72.6 mm。
-
用小型泵在各样地小区分别抽取不同宽度处20,40和60 cm深淋溶管内径流水样,装入250 mL塑料瓶中,带回实验室,放入-4~0 ℃冰箱内进行保存,及时测定水样中不同形态氮质量浓度。每次采样结束后,将淋溶管内的水抽空,方便下次采集,并在远离样地的地方倾倒。取水样后,在不同宽度的每组淋溶管所在区域,选取1 m × 1 m的范围,用土钻采集0~5,5~20和20~40 cm等3个不同深度的土样,分别装入塑料袋内,带回实验室检测。
水样总氮(TN)的测定采用GB 11894-1989《水质总氮的测定碱性过硫酸钾消解紫外分光光度法》测定;待测铵态氮(NH4+-N)和硝态氮(NO3--N)的水样先经过0.45 μm滤膜抽滤预处理,再分别使用HJ 535-2009《水质氨氮的测定纳氏试剂分光光度法》和HJ/T 346-2007《水质硝酸盐氮的测定紫外分光光度法(试行)》进行测定。土样铵态氮、硝态氮是利用鲜土分别采用HJ 535-2009《水质氨氮的测定纳氏试剂分光光度法》和HJ/T 346-2007《水质硝酸盐氮的测定紫外分光光度法(试行)》进行测定。土壤总氮(TN)是土样经风干、过筛后,用元素分析仪测定。
-
用Excel 2010对数据进行处理;用SPSS 20.0对数据进行单因素方差分析和Pearson相关性分析。取3次数据采样平均值进行分析。
-
随着河岸缓冲带宽度的增加,径流水中硝态氮、铵态氮和总氮质量浓度逐渐降低(图 2),截留率逐渐上升(图 3)。其中,对铵态氮的截留率最高,其次是硝态氮,对总氮的去除率最低。经过40 m的河岸缓冲带后,对径流水中硝态氮、铵态氮和总氮的平均截留率分别达68.69%,68.81%和66.01%。说明不同宽度的河岸缓冲带对径流水中的氮素有一定截留效果。对各深度径流水中氮质量浓度与缓冲带宽度进行单因素分析表明:前15 m径流水中硝态氮、铵态氮和总氮质量浓度随宽度变化差异显著(P<0.05),15 m后不显著(P>0.05)。说明15 m宽的河岸缓冲带能很好地截留径流水中的硝态氮、铵态氮和总氮。随着深度的增加,径流水中氮素质量浓度总体呈降低趋势,说明土壤吸附和植物吸收在径流水下渗过程中起到了一定的截留作用。对不同深度径流水中氮素质量浓度进行差异性分析表明:硝态氮质量浓度在5 m以后随深度变化差异不显著(P>0.05);各宽度铵态氮质量浓度在20与60 cm深度差异显著(P<0.05);总氮质量浓度在30 m之前20 cm与40,60 cm深度差异显著(P<0.05),30 m之后不显著。就截留率而言,不同深度径流水中硝态氮的截留率从高到低依次为20,40,60 cm;对铵态氮和总氮的截留率从高到低依次为40,20,60 cm。
-
从图 4可看出:乔木林河岸缓冲带对径流水中氮素的截留率均显著高于荒地(P<0.05);其中杨树林在前15 m对硝态氮的截留率最高(64.37%),15 m后混交林对硝态氮的去除率最高,并在40 m处达最大值(69.92%),但与杨树林、中山杉林截留率差异不显著(P>0.05)。不同宽度下,杨树林对铵态氮的截留率最高,且与中山杉林、混交林截留率差异显著(P<0.05),并在30 m处截留率达最大值(77.4%)。15 m及其以上的混交林对径流水总氮截留率最高,并在30 m处达最大值(73.0%)。在30 m宽度处混交林与杨树林和中山杉林对径流水中总氮的截留率之间差异显著(P<0.05)。
-
随着缓冲带宽度的增加,土壤氮素质量分数总体上呈增加趋势(图 5),表明随着缓冲带宽度的增加,氮素被更多地滞留在土壤中,起到了较好的截留作用。土壤中硝态氮、铵态氮和总氮的质量分数在前15 m随宽度变化差异性显著(P<0.05),15 m后差异不显著(P>0.05),说明缓冲带前15 m截留了大部分氮素。经过40 m河岸缓冲带后,土壤中硝态氮、铵态氮、总氮的平均截留率分别达37.75%,24.20%和28.53%(图 6)。在15 m及以后,0~5 cm深土壤中硝态氮质量分数较高,且在15和30 m处与5~20,20~40 cm深土壤硝态氮质量分数差异显著(P<0.05)。各宽度不同深度土壤中铵态氮质量分数从大到小依次为0~5,5~20,20~40 cm,但差异不显著(P>0.05)。0~5 cm深度土壤中总氮质量分数最高,且在15和30 m宽度处与20~40 cm深土壤中总氮质量分数差异显著(P<0.05)。就截留率而言,河岸植被缓冲带对硝态氮的截留效果最好,其次为总氮,铵态氮截留率最低。不同深度土壤中,3种氮素截留率随着河岸缓冲带宽度的增加均以15 m为节点,先上升后下降或缓慢上升,其中硝态氮和铵态氮截留率下降后在40 m处达最大值。可能是由于前15 m缓冲带截留了绝大部分氮素,导致径流水氮素质量分数大幅下降,从而被土壤吸附的量减少,截留率下降;在各宽度处,5~20 cm深土壤对硝态氮和铵态氮截留率较高,而土壤对总氮的截留率从大到小依次是0~5,20~40和5~20 cm。
-
从图 7可看出:乔木林(中山杉林、杨树林、混交林)对土壤中氮素的截留率均高于荒地,且随着缓冲带宽度的增加,截留率基本都呈上升趋势,说明林地对径流水中的氮素起到了很好的截留效果。不同宽度处,杨树林对硝态氮和铵态氮的截留率均高于中山杉和混交林,且均在40 m处达最大值(36.87%和29.71%),其中杨树林对硝态氮的截留率要高于对铵态氮的截留率。在各缓冲带宽度处杨树林对硝态氮的截留率与中山杉林差异显著(P<0.05),但与混交林差异不显著(P>0.05);杨树林在5和40 m处对铵态氮的截留率与中山杉林、混交林差异显著(P<0.05)。对于总氮来说,混交林对总氮的截留率最高,在40 m处达最大值(28.47%),但在各宽度处对总氮的截留率与中山杉林和杨树林差异不显著(P>0.05)。
-
相关分析表明:土壤中总氮质量分数与径流水中总氮质量浓度呈显著负相关(P<0.05,图 6),说明土壤对径流水中氮素的截留起到了积极的作用,有效降低了径流水中总氮质量浓度;植物叶片总氮与径流水中总氮的质量浓度相关性不显著,但呈一定负相关关系(图 8)。
-
本研究发现:随着河岸缓冲带宽度的增加,径流水中氮素的质量浓度不断降低,氮素截留率不断上升,但在15 m后氮素的截留效率上升不明显,且与40 m处氮素截留率相近,即随缓冲带宽度的增加,单位宽度缓冲带氮素截留率先升高后降低,15 m宽缓冲带即可显著降低经流水中氮素,这与SYVERSEN[15]研究中单位宽度缓冲带氮素截留率随宽度增加先升高后降低的结果一致。赵警卫等[16]、孟亦奇等[17]也认为:15 m后缓冲带氮素截留率上升不明显,但与汤家喜[18]提出的9 m缓冲带宽度即可显著减少经流水中氮素含量不同,主要因为其研究地土壤为砂质土壤,固氮能力较强的草本植物占优势,这从另一方面也说明了土壤物理性质对缓冲带功能的影响。土壤中氮素质量分数和截留率均呈现先升高后降低的趋势,并且在前15 m质量分数变化显著,在15 m后变化不显著,与郭鑫[19]研究中土壤氮素截留率随缓冲带宽度增加先升高后降低的结果一致,可能是由于前15 m缓冲带截留了绝大部分氮素,导致径流水氮素质量分数大幅下降,从而被土壤吸附的量减少,截留率下降。综上所述,15 m宽的河岸缓冲带能够有效截留氮素污染物,这与王敏等[20]、于红丽[21]认为的15 m宽河岸缓冲带即可有效截留氮素的结果一致。BORIN等[22]则认为6 m宽的河岸缓冲带即能有效去除径流水中的氮,而李怀恩等[23]认为缓冲带对氮素的截留作用主要发生在前10 m。植被组成、坡度、土壤理化性质、水文过程以及气候等因素的不同,均会导致有效截留氮素的宽度差异。因此,针对不同的地域环境,要综合考虑不同的影响因子,建立适宜的缓冲带宽度。
不同宽度缓冲带处径流水和土壤中氮素的含量随深度的加深呈降低趋势,说明土壤在径流水下渗的过程中起到了一定的截留作用,截留吸附了径流水中部分氮素。其中径流水中硝态氮质量浓度随深度变化差异不显著,铵态氮、总氮随深度变化差异显著,这与黄玲玲[24]研究中土层越深土壤总氮浓度越低的结果一致,主要是因为硝态氮极易溶于土壤水中而向更深层的土壤淋溶[25],在降雨过程中,在雨水的溶解下迅速向60 cm或更深的土层淋溶,而导致0~60 cm硝态氮含量差异不大。就去除率而言,缓冲带对40 cm深径流水中铵态氮、总氮的截留率较高,对20 cm深的硝态氮截留率较高;而缓冲带5~20 cm深土壤铵态氮和硝态氮的截留率较高,主要是因为铵态氮通过硝化作用,在0~5 cm深土壤总氮截留率较高,说明土壤对总氮的截留主要发生在土壤表层,而对硝态氮和铵态氮的截留主要发生在土壤中层。
有研究表明:缓冲带不同的植物配置对氮素污染的净化效果不同[26]。本研究中,3种河岸植被缓冲带对氮素的截留能力均高于对照,表明不同植被类型河岸缓冲带对径流水中氮素均起到较好的截留效果。杨树林缓冲带对径流水中铵态氮和硝态氮的截留率较高,其中对径流水中铵态氮的截留率与中山杉林和混交林差异显著(P<0.05),对径流水中硝态氮的截留率与中山杉林和混交林差异不显著;混交林缓冲带对总氮的截留率较高,但与杨树林和中山杉林的截留率差异不显著(P>0.05)。主要由于阔叶林可以显著增加土壤有机质的积累,而针叶林对土壤有机质积累的影响较弱,尤其是杉木Cunninghamia lanceolata纯林对土壤有机质的累积作用缓慢[11],同时,杨树根系比中山杉根系深[17],能够更多地吸收淋溶到深层土壤中的硝态氮,且样地树种处于幼龄阶段,杨树的生长速度较中山杉和混交林快,需要吸取更多的养分,这可能是造成杨树林缓冲带对径流水中铵态氮、硝态氮有较高截留率的主要原因。同时,不同缓冲带宽度处杨树林叶片全氮含量均高于中山杉林和混交林可能亦与此有关。
相关分析表明:土壤中总氮质量分数与径流水中总氮质量浓度呈显著负相关(P<0.05),且土壤中硝态氮的截留率最高,说明土壤吸附和反硝化作用是径流水中氮素截留去除的主要途径。从截留率来说,径流水中氮素截留率为66.01%~68.81%,土壤对氮素的截留率为24.20%~37.75%,占径流水中氮素截留率近一半,说明土壤对径流水中氮素的截留起到了积极的作用,有效降低了径流水中总氮质量浓度。
Removing nitrogen with trees planted in the riparian vegetation buffer strips of Taihu Lake
-
摘要: 为研究河岸植被缓冲带对氮素的截留效率,以太湖流域平缓坡地上人工林河岸缓冲带作为研究对象,分析了不同河岸缓冲带宽度(5,15,30,40 m),不同植物类型(‘南林95’杨Populus×euramericana ‘Nanlin 95’林、中山杉Taxodium hybrid ‘Zhongshanshan’林、南林杨95-中山杉混交林)对不同深度径流水及土壤中氮素的截留效果。结果表明:15 m宽的河岸缓冲带即能很好地截留各形态氮素,40 m缓冲带对径流水中硝态氮、铵态氮、总氮的截留率分别达68.8%,68.7%和66.0%;同一宽度条件下,缓冲带对40 cm深径流水中铵态氮、总氮的截留率较高,分别达71.4%和69.1%,对20 cm深径流水中硝态氮截留率较高,达70.6%;森林土壤对铵态氮和硝态氮的截留主要在中层土壤,对总氮截留主要在表层土壤;杨树林缓冲带对径流水中铵态氮和硝态氮的截留率较高(P < 0.05),达77.4%和66.3%;杨树-中山杉混交林缓冲带对总氮的截留率较高(P < 0.05),达73.0%;植物叶片(r=-0.53)全氮和土壤总氮(r=-0.59)均与径流水中总氮呈负相关关系。Abstract: In the Taihu Lake area many riparian vegetation buffer strips have been built to alleviate the input of eutrophic nutrients into the lake. To provide a scientific basis for determining a suitable width and components of these riparian buffer strips, the effects of riparian vegetation buffer strips with widths of 5, 15, 30, and 40 m and vegetation types of a Populus×euramericana 'Nanlin 95' plantation, an Taxodium hybrid 'Zhongshanshan' plantation, and a mixed plantation with the two tree species on total nitrogen, ammonia nitrogen, and nitrate nitrogen removal rates for different depths of runoff water and soil were studied. Results showed that the buffer strips of 15 m width effectively removed various fractions of N and removal rates in runoff water of 40 m width of 68.8% for NO3-, 68.7% for NH4+, and 66.0% for total N. Removal rates of NH4+ and total N in runoff water at 40 cm below ground level were higher, reached 71.4% and 69.1%, but NO3- removal rate in the 20 cm depth of runoff water was higher, reached 70.6%. The interceptions of NH4+ and NO3- in plantation soils were mainly in the middle soil layer, and total N was trapped mainly in surface soils. The poplar plantation had a higher removal rate of NH4+ and NO3- in runoff water(P < 0.05), reached 77.4% and 66.3%, but the mixed forests of the poplar plantation and Taxodium hybrid 'Zhongshanshan' plantation had a higher removal rate of total N(P < 0.05), reached 73.0%. Also, total N in runoff water was negatively correlated to total N in the soil (r=-0.59) and total N in the leaves (r=-0.53) of plants.
-
Key words:
- forest ecology /
- riparian vegetation buffer strip /
- width /
- vegetation type /
- nitrogen /
- removal rate
-
-
[1] 陈勇.陕西省农业非点源污染评价与控制研究[D].杨凌: 西北农林科技大学, 2010. CHEN Yong. Research on Evaluation and Controling Measure System of Agriculture Non-point Source Pollution in Shaanxi Province[D]. Yangling: Northwest A & F University, 2010. [2] 赵晓军, 翟超英, 赵明月.农业污染国内外研究进展及防控对策建议[J].农业环境与发展, 2013, 30(4):1-6. ZHAO Xiaojun, ZHAI Chaoying, ZHAO Mingyue. Agricultural pollution research progress in China and abroad and pollution control countermeasures[J]. Agro-Environ Dev, 2013, 30(4):1-6. [3] HICKEY M, BRIAN C, DORAN B. A review of the efficiency of buffer strips for the maintenance and enhancement of riparian ecosystems[J]. Water Qual Res J Can, 2004, 39(3):311-317. [4] MANKIN K R, NGANDU D M, BARDEN C J, et al. Grass-shrub riparian buffer removal of sediment phosphorus, and nitrogen from simulated runoff[J]. J Am Water Resour Association, 2007, 43(5):1108-1116. [5] DUCHEMIN M, HOGUE R. Reduction in agricultural non-point source pollution in the first year following establishment of an integrated grass/tree filter strip system in southern Quebec (Canada)[J]. Agric Ecol Environ, 2009, 131(1/2):85-97. [6] 王敏, 黄宇驰, 吴建强.植被缓冲带径流渗流水量分配及氮磷污染物去除定量化研究[J].环境科学, 2010, 31(11):2607-2612. WANG Min, HUANG Yuchi, WU Jianqiang. Quantification study on the runoff and seepage distribution and N, P pollutants removal of the vegetated buffer strips[J]. Environ Sci, 2010, 31(11):2607-2612. [7] LIU Xingmei, ZHANG Xuyang, ZHANG Minghua. Major factors influencing the efficacy of vegetated buffers on sediment trapping:a review and analysis[J]. J Envi Qual, 2008, 37(5):1667-1674. [8] SPRUILL T B. Statistical evaluation of effects of riparian buffers on nitrate and ground water quality[J]. J Environ Qual, 2000, 29(5):1523-1538. [9] KOVACIC D A, DAVID M B, GENTRY L E, et al. Effectiveness of constructed wetlands in reducing nitrogen and phosphorus export from agricultural tile drainage[J]. J Environ Qual, 2000, 29(4):1262-1274. [10] WANG L, DUGGIN J A, NIE D. Nitrate-nitrogen reduction by established tree and pasture buffer strips associated with a cattle feedlot effluent disposal area near Armidale, NSW Australia[J]. J Environ Manage, 2012, 99(5):1-9. [11] 陈金林, 潘根兴, 张爱国, 等.林带对太湖地区农业非点源污染的控制[J].南京林业大学学报(自然科学版), 2002, 26(6):17-20. CHEN Jinlin, PAN Genxing, ZHANG Aiguo, et al. The controlling effects of shelter forest on non-point source pollution of agricultural lands in Taihu Lake area[J]. J Nanjing For Univ Nat Sci Ed, 2002, 26(6):17-20. [12] 王庆成, 崔东海, 王新宇, 等.帽儿山地区不同类型河岸带土壤的反硝化效率[J].应用生态学报, 2007, 18(12):2681-2686. WANG Qingcheng, CUI Donghai, WANG Xinyu, et al. Soil denitrification rates in different type riparian zones in Maoershan mountainous region of China[J]. Chin J Appl Ecol, 2007, 18(12):2681-2686. [13] 林晓晟.吉林省辽河流域土壤涵水与缓冲带截污能力研究[D].长春: 吉林大学, 2017. LIN Xiaosheng. Research on Soil Water Conservation and Riparian Buffer Pollutant Retention in Liao River Basin, JilinProvince[D]. Changchun: Jilin University, 2017. [14] 吴永波.河岸植被缓冲带减缓农业面源污染研究进展[J].南京林业大学学报(自然科学版), 2015, 39(3):143-148. WU Yongbo. Research progress on the riparian vegetation buffer strip functions on agricultural nonpoint source pollution reduction[J]. J Nanjing For Univ Nat Sci Ed, 2015, 39(3):143-148. [15] SYVERSEN N. Effect and design of buffer zones in the Nordic climate:the influence of width, amount of surface runoff, seasonal variation and vegetation type on retention efficiency for nutrient and particle runoff[J]. Eco Eng, 2005, 24(5):483-490. [16] 赵警卫, 胡彬.河岸带植被对非点源氮、磷以及悬浮颗粒物的截留效应[J].水土保持通报, 2012, 32(4):51-55. ZHAO Jingwei, HU Bin. Interception of non-point source N and P and suspended solid matter by riparian vegetation[J]. Bull Soil Water Conserv, 2012, 32(4):51-55. [17] 孟亦奇, 吴永波, 朱颖, 等.利用河岸缓冲带去除径流水中氮的研究[J].湿地科学, 2016, 14(4):532-537. MENG Yiqi, WU Yongbo, ZHU Ying, et al. The study on removing nitrogen in runoff water by riparian buffer strips[J]. Wetland Sci, 2016, 14(4):532-537. [18] 汤家喜.河岸缓冲带对农业非点源污染的阻控作用研究[D].沈阳: 沈阳农业大学, 2014. TANG Jiaxi. Study on Control of Agricultural Non-point Source Pollutants by Riparian Vegetated Filter Strips[D].Shenyang: Shengyang Agricultural University, 2014. [19] 郭鑫.辽河保护区植被缓冲带对N、P污染的阻控作用研究[D].沈阳: 沈阳大学, 2016. GUO Xin. The Study on the Effect of Vegetation Buffer Zone about N and P Pollution in Liao River Protection Zone[D]. Shenyang: Shenyang Universiy, 2016. [20] 王敏, 吴建强, 黄沈发, 等.不同坡度缓冲带径流污染净化效果及其最佳宽度[J].生态学报, 2008, 28(10):4951-4956. WANG Min, WU Jianqiang, HUANG Shenfa, et al. Effects of slope and width of riparian buffer strips on runoff purification[J]. Acta Ecol Sin, 2008, 28(10):4951-4956. [21] 于红丽.不同类型河岸带对溪流氮素输入的截留转化效率研究[D].哈尔滨: 东北林业大学, 2005. YU Hongli. Nitrogen Attenuation Efficiency at Difference Types Stream Riparian Buffer Zones[D]. Harbin: Northeast Foretstry University, 2005. [22] BORIN M, PASSONI M, THIENE M, et al. Multiple functions of buffer strips in farming areas[J]. Eur J Agron, 2010, 32(1):103-111. [23] 李怀恩, 邓娜, 杨寅群, 等.植被过滤带对地表径流中污染物的净化效果[J].农业工程学报, 2010, 26(7):81-86. LI Huaien, DENG Na, YANG Yanqun, et al. Clarification efficiency of vegetative filter strips to several pollutants in surface runoff[J]. Trans CSAE, 2010, 26(7):81-86. [24] 黄玲玲.竹林河岸带对氮磷截留转化作用的研究[D].北京: 中国林业科学研究院, 2009. HUANG Lingling. Study on Retaining and Transformation of N and P in Bamboo Riparian Buffer Zone[D]. Beijing: Chinese Academy of Forestry, 2009. [25] 司友斌, 王慎强, 陈怀满.农田氮、磷的流失与水体富营养化[J].土壤, 2000, 32(4):188-193. SI Youbin, WANG Shenqiang, CHEN Huaiman. Loss of nitrogen and phosphorus in farmland and water Eutrophication[J]. Soils, 2000, 32(4):188-193. [26] 刘燕, 夏品华, 郑钧宁, 等.河岸缓冲带植物配置模式对面源污染物的净化效果[J].贵州农业科学, 2014, 42(10):248-251. LIU Yan, XIA Pinhua, ZHENG Junning, et al. Effects of different plant configuration modes of riparian buffer strips on runoff purification[J]. Guizhou Agric Sci, 2014, 42(10):248-251. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.2019.03.018







 下载:
下载: