-
竹材具有生长周期短、产量高和强度大等优点,是一种非常有潜力的可再生生物质原料[1]。通过热解技术将竹材等生物质原料制成高品质生物燃料和化学品,已成为生物质能源利用的研究热点[2-3]。综纤维素主要由纤维素和半纤维素组成,是生物质经过脱木质素和抽提物后得到的产物,其热分解机制研究有助于深入了解生物质原料的热解特性。热重红外联用技术(TG-FTIR)不仅可以掌握生物质组分的热解失重规律,还可以对挥发分气体的成分实现在线识别。Liu等[4-5]、Ren等[6]利用TG-FTIR分别对纤维素、综纤维素和木质素的热解特性进行研究,利用挥发分气体成分的特定官能团的红外特征吸收峰进行鉴定,发现其热解挥发分主要成分为一部分小分子物质如CO,CO2,CH4和H2O等,以及一些醛类、酮类、酚类和芳香族有机化合物。木材综纤维素已经得到了研究,而目前还没有竹材综纤维素热解研究报道。竹综纤维素热解过程涉及到复杂的链式反应,通过热解动力学分析,可以深入了解其热解反应机制[7]。因此,本研究以竹综纤维素为原料,采用不同的升温速率,利用TG-FTIR首先分析了竹综纤维素的热解失重规律以及挥发分气体析出特性;然后采用2种无模式函数积分法(model-free method)[8-9],即Flynn-Wall-Ozawa(FWO)法和kissinger-Akahira-Sunose(KAS)法,对其热解动力学进行研究,分析综纤维素热解活化能随转化率的变化规律。
HTML
-
竹综纤维素是通过毛竹Phyllostachys edulis脱木质素和抽提物自制获得。精确称取2.0 g毛竹粉末,用定性滤纸包好,按GB/T 2677.6-1994《造纸原料有机溶剂抽出物含量的测定》,先将原料通过苯醇抽提,抽出原料中抽提物。然后将试样包风干后,把里面的试样移入250.0 mL锥形瓶中,加入65.0 mL去离子水、0.5 mL冰醋酸和0.6 g亚氯酸钠,摇匀,扣上25.0 mL锥形瓶,置于75 ℃恒温水浴中加热1 h。之后重复上一步骤,直至试样变白,过滤、洗涤、干燥后得竹综纤维素。
-
采用元素分析仪(德国Elementar Vario EL Ⅲ)测定原料的碳、氢、氮和硫含量,氧元素采用差减法计算;采用GB/T 28731-2012《固体生物质燃料工业分析方法》对原料进行工业分析;采用微机量热仪(中国河南鹤壁仪器有限公司,ZDHW-8A)测定原料热值。采用高效液相色谱(美国安捷伦科技有限公司Agilent-1100)分析原料化学组成,测试标准为NREL 2007 Determination of Structural Carbohydrates and Lignin in Biomass。结果见表 1。
元素分析 工业分析 化学组分分析 元素 百分比/% 成分 百分比/% 成分 百分比/% C 42.12 挥发分 93.56 葡聚糖 62.60 H 6.12 固定碳 6.38 木聚糖 27.90 0# 51.07 灰分 0.06 果胶糖 5.40 N 0.47 S 0.13 低位热值/(MJ.kg-1) 11.43 说明:#氧元素采用差减法得到。 Table 1. Ultimate, proximate and chemical component analysis of bamboo holo-cellulose
热重红外联用(TG-FTIR)分析仪由热重分析仪TGA Q500(TA Instruments,美国)和傅里叶红外光谱仪Nicolet 6700(Thermo Fisher Scientific,美国)组成。实验用料约为15.0 mg·次-1,氮气流量为70.0 mL·min-1,红外光谱仪的扫描范围为4 000~400 cm-1,分辨率为4 cm-1,扫描时间约为8 s·次-1;升温速率分别为5.0,10.0,15.0,20.0和30.0 ℃·min-1,从室温升至850.0 ℃。
-
固体物质的非等温热反应速率方程(Arrhenius方程)可表示为:
式(1)中:α为热分解转化率,而α可根据公式(2)计算得到:
式(2)中:τ为热分解时间;m0为生物质初始质量;mτ为τ时刻对应的生物质质量;m∞为热分解终温时残余物质量;A为频率因子,min-1;E为生物质反应活化能,kJ·mol-1;R为摩尔气体常数,8.314×10-3 kJ·K-1·mol-1;T为热力学温度,K;f(α)为反应机制函数。而升温速率β定义为β=dT/dτ,代入式(1)可得热分解反应动力学方程式:
对(3)式求积分整理得:
式(4)中:G(α)为机制函数f(α)的积分形式。
-
根据公式(1)~式(4),可以采用不同的动力学模型对生物质的热解动力学进行研究,本研究采用FWO和KAS积分法对综纤维素的热解机制进行研究。活化能(E)是转化率(α)的函数。FWO和KAS积分法分别用式(5)和式(6)表示。
式(7)中:Tij为αij(i=1,2,…,L;j=1,2,…,ki)时相应的温度,ki为升温速率为βj时的取值数量。在不同的升温速率βj时,取相同的转化率αij为常数,因此G(αij)也是常数。所以,lg(βj)和1/Tij以及ln(βj /T2)和1/Tij为线性关系。经过线性拟合后,活化能E可以根据式(5)和式(6)的斜率-0.456 7E/R和E/R求解得到。本研究采用5个升温速率(5.0,10.0,15.0,2.0和30.0 ℃·min-1)来求解活化能,以期获得更加稳定可靠的活化能值。
1.1. 实验材料和制备方法
1.2. 实验方法
1.3. 热解动力学
1.3.1. 非等温动力学模型基础
1.3.2. 无机制函数积分法
-
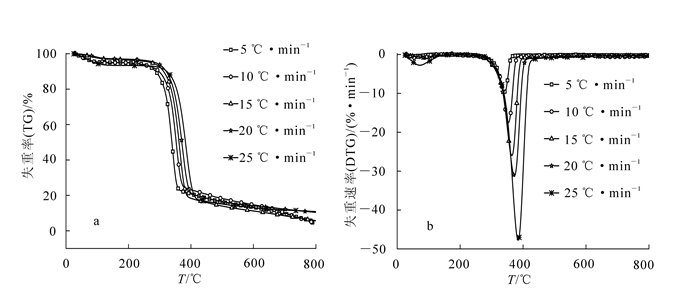
图 1为竹材综纤维素在不同升温速率条件下(5.0,10.0,15.0,20.0和30.0 ℃·min-1)的失重率TG(a)和失重速率DTG(b)曲线。从图 1可以看出:竹材综纤维素热解过程包括3个阶段。第1阶段为干燥阶段,温度范围为室温~150.0 ℃,失重率为2.8%~5.9%,这阶段主要是原料中自由水和结合水的蒸发[10]。第2阶段为快速裂解阶段,温度范围为150.0~452.0 ℃,主要是半纤维素和纤维素的降解,失重率为68.7%~76.2%,不同升温速率此阶段温度范围有所不同。第3阶段为慢速裂解阶段,温度范围为453.0~800.0 ℃,剩余的纤维素和第2阶段热解产生的炭发生进一步降解,失重率为5.5%~19.3%。
从图 1可以看出:随着升温速率增加,TG-DTG曲线往高温区域移动。原因是竹材原料试样的导热系数低,热重分析仪记录的坩埚的温度与试样本身的温度有偏差。另外,受试样传质传热的影响,试样颗粒会形成温度梯度,形成热滞后现象,升温速率越高,热滞后越明显[11]。
-
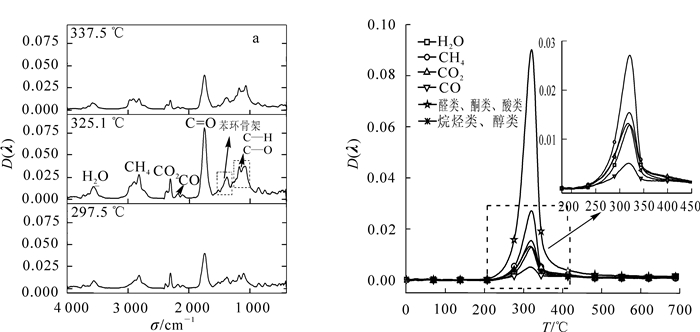
图 2为竹材综纤维素在升温速率10.0 ℃·min-1时的三维红外光谱图。从图 2可以看出:综纤维素热解过程中挥发分主要吸收峰出现在29~43 min时间范围内,与其TG/DTG曲线失重规律吻合,为快速热解阶段。
图 3a为3个典型温度点(热解起始点297.5 ℃,热解峰325.1 ℃和热解接近结束点337.5 ℃)时挥发分的成分分析,图 3b为一些典型热解产物随温度的变化趋势。从图 3可以看出:温度对热解挥发分有明显的影响。在初始热解温度297.5 °C时,所有挥发产物特征峰都已经开始出现,并且在325.1 °C时浓度达到最大值,之后逐渐下降。

Figure 3. FTIR spectra for validation of the volatile components and the evolution of the concentration in each component in pyrolysis process of bamboo holo-cellulose
以热解失重率最大处时(325.1 ℃)为例,对其挥发分成分进行分析。一些小分子的物质如H2O,CH4,CO2和CO,因其特征吸收峰特别明显,很容易进行判别。4 000~3 400 cm-1为羟基O—H伸缩振动,代表的物质是过氧化氢(H2O)[12]。3 000~2 700 cm-1为C—H键伸缩振动,主要是甲基(—CH3)和亚甲基团(—CH2—),代表的成分是CH4 [5]。2 400~2 250 cm-1区间为CO伸缩振动,代表的是二氧化碳(CO2)。紧靠2 400~2 250 cm-1右侧的波数为2 250~2 000 cm-1处的是一氧化碳(CO)的不显著的特征吸收峰[6]。
另一个显著的特征吸收峰在1 900~1 650 cm-1处,为羰基CO伸缩振动吸收峰,可能的化学物质为醛、酮、酸等。1 690~1 460 cm-1处主要为CC伸缩振动及苯环的骨架振动区。由于在1 600 cm-1,1 580 cm-1和1 500 cm-1处都有吸收峰,因此可判断此区域存在单核的芳环类化合物。1 475~1 000 cm-1为指纹区的一部分,包括C—H键面内弯曲和C—O键伸缩振动等,特征吸收峰相互重叠,很难分辨出单种物质具体成分。然而通过官能团对应的特征吸收峰,可以对其进行类别的分析,如1 460~1 365 cm-1主要是甲基(—CH3)和亚甲基团(—CH2—)的特征吸收峰,可能为烷烃类物质;其他部分,1 200~1 000 cm-1为醇类,1 300~1 200 cm-1为酚类物质,1 275~1 060 cm-1为醚类物质,1 300~1 050 cm-1为脂类物质[13]。
经过以上分析,对其挥发分成分进行分析后,单种挥发分成分随温度的变化趋势如图 3b所示。根据Lambert-Beer定律,处于特定波数物质吸光度数值的大小代表了该物质浓度的高低,因此,吸光度的变化反映出整个热解过程中挥发分气体的浓度变化趋势[12]。气体的产生主要在250.0~450.0 ℃范围内,297.0~325.0 ℃各类挥发分产物浓度随着温度升高而增加,325.0~337.0 ℃各类挥发分产物浓度随着温度升高而减少,之后逐渐降低至0。
-
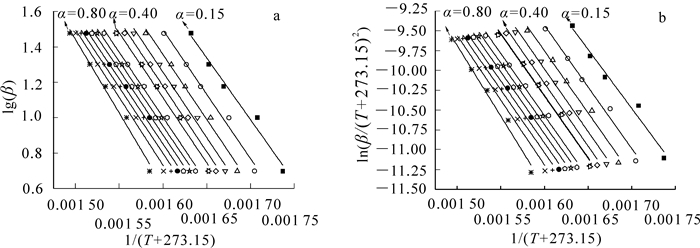
在1.3.2中说明了,竹综纤维素的活化能值的计算方法,即根据不同升温速率时,同一转化率(α)下对应的温度(T)与升温速率(β)的拟合曲线的斜率来计算。活化能代表的是化学反应发生所需的最低能量,因此活化能越高证明反应发生越困难或者反应速率越低。图 4为竹综纤维素转化率在0.15~0.80范围(间隔0.05)的线性拟曲线,可以看出线性拟合相关系数高于0.98。由于转化率在0.15~0.80范围以外的拟合曲线的线性相关系数太低,故本研究没有采用。
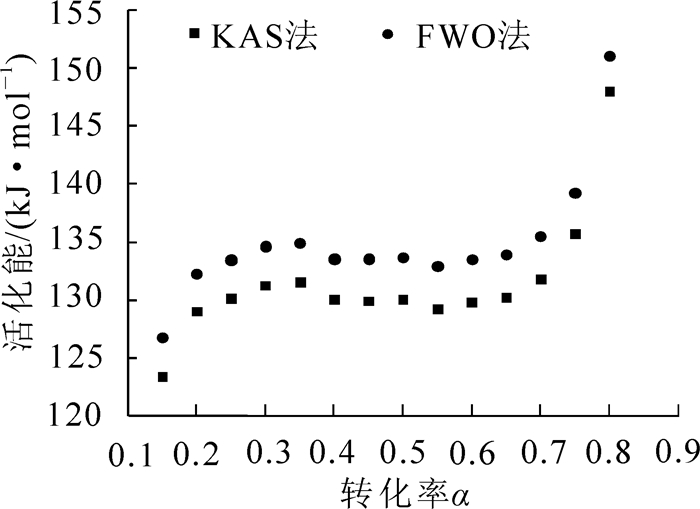
活化能随转化率的变化规律如图 5所示。从整体上看活化能值随着转化率的增加而上下浮动,说明竹综纤维素在热解过程中发生了复杂的化学反应,包括重叠、平行和连续反应等。因此,必须对其进行分段讨论,进一步解释其热解反应机制。另外,FWO法和KAS法计算得到的活化能变化趋势一样,两者偏差在5.0%以内。较小的偏差来自于2种方法采用了不同的近似解,FWO法采用的是Doyle近似解lg(P(u)≈-2.315+0.457u,而KAS法采用的近似解为P(u)≈u-2e-u。2种无函数模式法获得的活化能基本一致,说明获得的活化能可靠性。

Figure 5. Activation energy distribution dependence on the conversion rate using FWO and KAS methods
根据表 1可知:竹综纤维素主要由纤维素(葡聚糖为代表)和半纤维素(木聚糖和果胶糖为代表)组成,以纤维素为主,占62.5%,半纤维素含量为33.3%。由图 5可以看出:热解第1阶段,0.15<α<0.25,活化能逐渐升高,FWO法活化能为126~133 kJ·mol-1,KAS法活化能为123~130 kJ·mol-1。这一阶段主要是半纤维素的降解,键的断裂首先发生在键能较弱的支链部位,所需的能量较低,因此活化能值也较低;然后半纤维素主链开始发生自由断裂,使得活化能值增加[14]。热解第2阶段,0.25<α<0.80,活化能先出现轻微降低,最后突然快速增加,FWO法活化能为134~151 kJ·mol-1,KAS法活化能为129~148 kJ·mol-1。这一阶段主要是纤维素的降解,初始阶段活化能比中间段高,根据Broido-Shafizadeh提出的纤维素热解模型,纤维素热解首先产生中间产物活性纤维素,聚合度降低,分子链长度减少[15-16]。之后,随着温度升高,活性纤维素开始降解,但此时随着聚合度降低,热降解更易发生,因此活化能跟初始阶段比有所降低。临近纤维素热解结束时,活化能突然快速增加,可能是纤维素表面热解固体产物焦炭含量逐渐增加引起的[17]。一方面炭的反应活性较低,另一方面此时热降解反应主要取决于扩散反应区扩散速度,而随着可降解物质(挥发分)的减少,反应速率急剧降低,造成活化能快速增加[18]。
2.1. 热重分析
2.2. FTIR分析
2.3. 热解动力学分析
-
竹材综纤维素热分解可分为干燥、快速裂解和慢速裂解等3个阶段;随着升温速率增加,TG/DTG曲线往高温一侧移动;热解挥发分主要由小分子CO,H2O,CH4和CO2,以及一些醛类、酮类、酸类、烷烃、醇类和酚类等有机物组成。竹综纤维素热解过程发生复杂的化学反应,包括多重、平行和连续反应,使得FWO和KAS积分法计算得到的活化能随着转化率升高而变化。当0.15<α<0.25,活化能逐渐升高,主要是半纤维素的降解,热裂解首先发生在键能较弱的支链部位,然后半纤维素主链开始发生自由断裂;当0.25<α<0.80,此阶段主要是纤维素的降解,纤维素热解首先产生中间产物活性纤维素,活化能轻微降低,随着反应的进行,纤维素表面热解固体产物焦炭含量逐渐增加致使活化能迅速增加。












 DownLoad:
DownLoad: