-
近年来,庭院花卉、家庭菜园等农艺经营活动受到人们广泛的青睐,而快节奏的生活方式(不能及时灌水)导致植株遭受水分胁迫威胁的问题较为严重,因此,探索简便实用的盆栽植物水分管理技术具有重要的实用意义。土壤水分是植物生长的重要因子,研究表明:缺水时植物的形态生长和生理特性均会受到不同程度的影响[1]。水分胁迫下,植物细胞分裂和体积增长受到显著抑制,植株生长变缓;叶绿体结构破坏,叶绿素含量下降,造成植物光合作用和干物质的积累受阻[2]。叶片相对含水量(RWC)可表征植物组织水分的亏缺程度[3-4],过氧化物酶(POD)活性、丙二醛(MDA)质量摩尔浓度和脯氨酸(Pro)质量分数等3个指标分别表征植物抵御活性氧伤害的保护酶活性、细胞质膜过氧化最终分解产物含量和植物体内渗透调节物质的含量[5-8],研究中常用来表征植物水分胁迫状态,并以此为依据探索简便实用的水分管理技术。农业岩棉是一种由玄武岩类材料经高温熔融,离心喷吹等工序加工而成的矿物棉,孔隙度高,通气性好,质地较轻,浸水不易变形;具有很强的蓄水和保水性能,对外界环境湿度变化具有缓冲作用,可为植物根系生长创造良好稳定的生长环境,适用于工厂化立体育苗栽培,在现代农业生产领域,常被作为无土栽培的基质而广泛应用于花卉蔬菜等经济型作物的育苗栽培[9]。农业岩棉应用于室内盆栽植物栽培,一定程度上解决了盆栽浇水不及时引起的植物缺水问题,也为拓展农业岩棉的新的应用领域提供借鉴。本研究选取对水分较敏感的樱桃番茄Lycopersicone sculentum作为研究对象,分析水分胁迫下岩棉及其不同埋设方式对土壤含水量、番茄植株形态生长指标和生理生化指标的影响,揭示岩棉及其不同埋设方式对缓解盆栽植物水分胁迫的作用,以期为岩棉保水技术在盆栽植物水分管理应用方面提供指导。
-
供试岩棉由施可达岩棉股份有限公司(江苏宜兴)提供,容重约为70~100 kg·m−3,纤维直径≤50 μm,主要化学成分为氧化钙(CaO)、氧化镁(MgO)和二氧化硅(SiO2)等;岩棉加工过程中添加亲水性黏结剂,孔隙度大于95%,吸水性良好,最大容积持水量为64.64%。育苗基质由杭州锦海农业科技有限公司提供,主要成分为发酵牛粪和泥炭等。供试土壤取自浙江农林大学试验田,0~20 cm土层粉壤土,与育苗基质充分混合,控制土壤田间持水量为40%,pH 6.43,有机质为14.07 g·kg−1,碱解氮为89.78 mg·kg−1,速效磷为44.84 mg·kg−1,速效钾为435.65 mg·kg−1。供试盆栽植物为樱桃番茄。
-
2019年4月13日,选取长势一致的番茄幼苗进行盆栽试验。盆栽容器为直径24 cm、高27 cm的塑料盆,过2 mm筛的风干土6 kg·盆−1,育苗基质600 g·盆−1,装盆前混合均匀。容器内各材料自下而上布设如下:盆底填土约3 cm,岩棉约10 cm,覆土10 cm,并在距土表5 cm处埋设水分传感器。受长期水分胁迫影响,番茄成熟期提前,于2019年7月12日拉苗。
采用完全随机区组试验设计,设置植物根系下部埋设块状岩棉(BR)、环根周埋设片状岩棉(FR)2个处理,以埋设惰性不吸水材料为对照(ck);添加的岩棉或惰性材料总体积保持一致。各处理9次重复,1株·盆−1,共27盆,置于温室大棚内;栽培条件:昼/夜温度为28 ℃/20 ℃,空气相对湿度为75%,光照条件为自然光;每周交换花盆位置,保证各处理光照一致,利用水分传感器原位监测初苗期、开花期、结果初期和结果末期等4个生长时期的土壤容积含水量。
模拟水分胁迫盆栽试验设计参考李永胜等[10]方法,依据土壤田间持水量和土量等对灌水量适当改进。试验开始前各处理在1 d内等量(800 mL)灌水2次,使田间持水量保持在67%,之后进行水分胁迫试验。为预防因缺水导致的植株永久萎焉,待各处理植株出现临时萎焉时需少量灌水(200 mL·次−1)。
-
采用托普云农TZS-2X-G多参数水分记录仪原位测定土壤容积含水量。
-
生长指标测定。初苗期、开花期、结果初期和结果末期等4个生长时期,分别测定植株株高(卷尺测定植株基部距土表2 mm处到主茎顶部的高度),地茎(游标卡尺测定垂直距离土壤表面2 mm处的番茄植株横径),叶片数(选取长或宽大于2 mm的叶片),最大叶面积(选取3片·株−1最大叶片,测定长宽2个方向最大值的乘积);结果末期测定植株根长,拔苗前先用流水冲松盆土,轻取植株,洗净吸干水分后,测定植株主根根长;植株整株在105 ℃下杀青30 min,降温至70 ℃烘至恒量,称单株干质量[11]。生理指标测定。初苗期、开花期、结果初期和结果末期等4个生长时期,采集各处理植株相同叶位的成熟叶9片,经预处理后测定各生理指标,重复3次。参考高俊凤等[12]的方法,采用丙酮浸提紫外分光比色法测定叶绿素质量分数,采用磺基水杨酸提取茚三酮显色法测定脯氨酸质量分数,采用烘干法测定叶片相对含水量,采用硫代巴比妥酸法测定丙二醛质量摩尔浓度,采用愈创木酚显色法测定过氧化物酶活性。
-
利用Excel 2007初步统计数据,结果以平均值±标准误表示;通过Duncan’s新复极差法进行方差分析,显著性水平取0.05;用Origin Pro 8.5绘图。
-
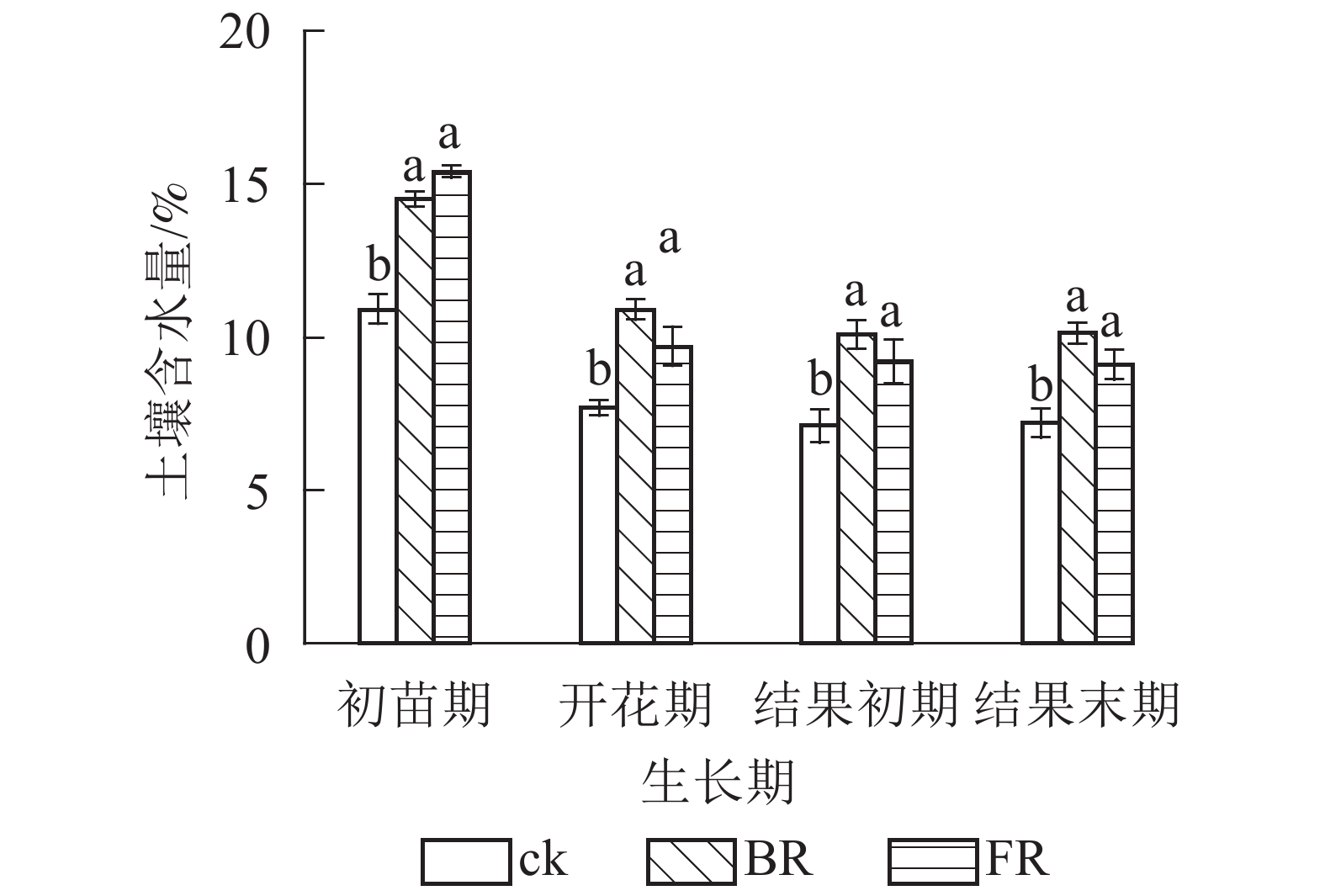
由图1可知:番茄整个生长期内不同处理的土壤容积含水量均呈现下降趋势,同一生长期内岩棉处理(BR和FR)土壤容积含水量均显著高于ck(P<0.05)。与ck相比,BR和FR处理初苗期土壤容积含水量分别增加32.96%和41.02%,开花期分别增加41.45%和26.01%,结果初期分别增加41.81%和29.61%,结果末期分别增加40.72%和26.61%。除初苗期外,BR处理的土壤容积含水量均略高于FR处理。
-
由表1可知:整个生长期内,同一处理番茄株高、地茎和叶片数均随时间增加而增加,最大叶面积先增加后减小。同一生长期番茄株高、地茎、叶片数、最大叶面积、根长和干质量等均表现为岩棉处理(BR和FR)高于ck,其中株高、叶片数、最大叶面积(除结果初期)和干质量等4个指标存在显著差异(P<0.05),结果末期BR和FR处理番茄株高分别显著增加9.77%和7.76%(P<0.05),叶片数分别显著增加17.52%和11.35%(P<0.05),最大叶面积分别显著增加33.64%和35.44%(P<0.05),干质量分别显著增加13.26%和4.69%(P<0.05)。
表 1 模拟水分胁迫条件下埋设岩棉对番茄植株生长的影响(n=9)
Table 1. Effects of embedded rock wool on tomato growth index under simulated water stress conditions (n=9)
生长期 处理 株高/cm 地茎/mm 叶片数/片 最大叶面积/cm2 根长/cm 干质量/g 初苗期 ck 35.17±1.49 b 5.99±0.18 a 75.00±3.21 b 14.05±1.10 b BR 38.67±0.35 a 6.03±0.21 a 84.55±2.76 a 18.47±0.68 a FR 38.72±0.39 a 6.16±0.24 a 83.2±0.39 ab 20.26±1.27 a 开花期 ck 51.95±1.04 b 7.18±0.13 a 132.89±8.73 b 18.77±0.63 b BR 57.83±1.93 a 7.30±0.24 a 153.67±1.35 a 21.48±1.64 a FR 57.22±1.47 a 7.77±0.31 a 180.89±11.95 ab 24.58±0.20 ab 结果初期 ck 63.44±0.69 b 8.03±0.09 a 206.78±13.13 b 19.37±1.44 a BR 70.67±0.58 a 8.01±0.21 a 233.22±8.55 a 23.05±1.42 a FR 69.61±0.94 a 8.42±0.36 a 256.44±5.67 ab 23.69±0.60 a 结果末期 ck 74.50±1.25 b 8.13±0.10 a 234.00±12.86 b 17.21±1.22 b 17.47±0.81 b 12.37±0.46 b BR 81.78±1.24 a 8.42±0.21 a 275.00±2.14 a 23.00±1.41 a 21.50±0.79 a 14.01±0.22 a FR 80.28±0.20 a 8.52±0.30 a 260.56±7.87 ab 23.31±1.05 a 18.61±0.39 b 12.95±0.39 ab 说明:同列不同字母表示同一生长期不同处理间差异显著(P<0.05) -
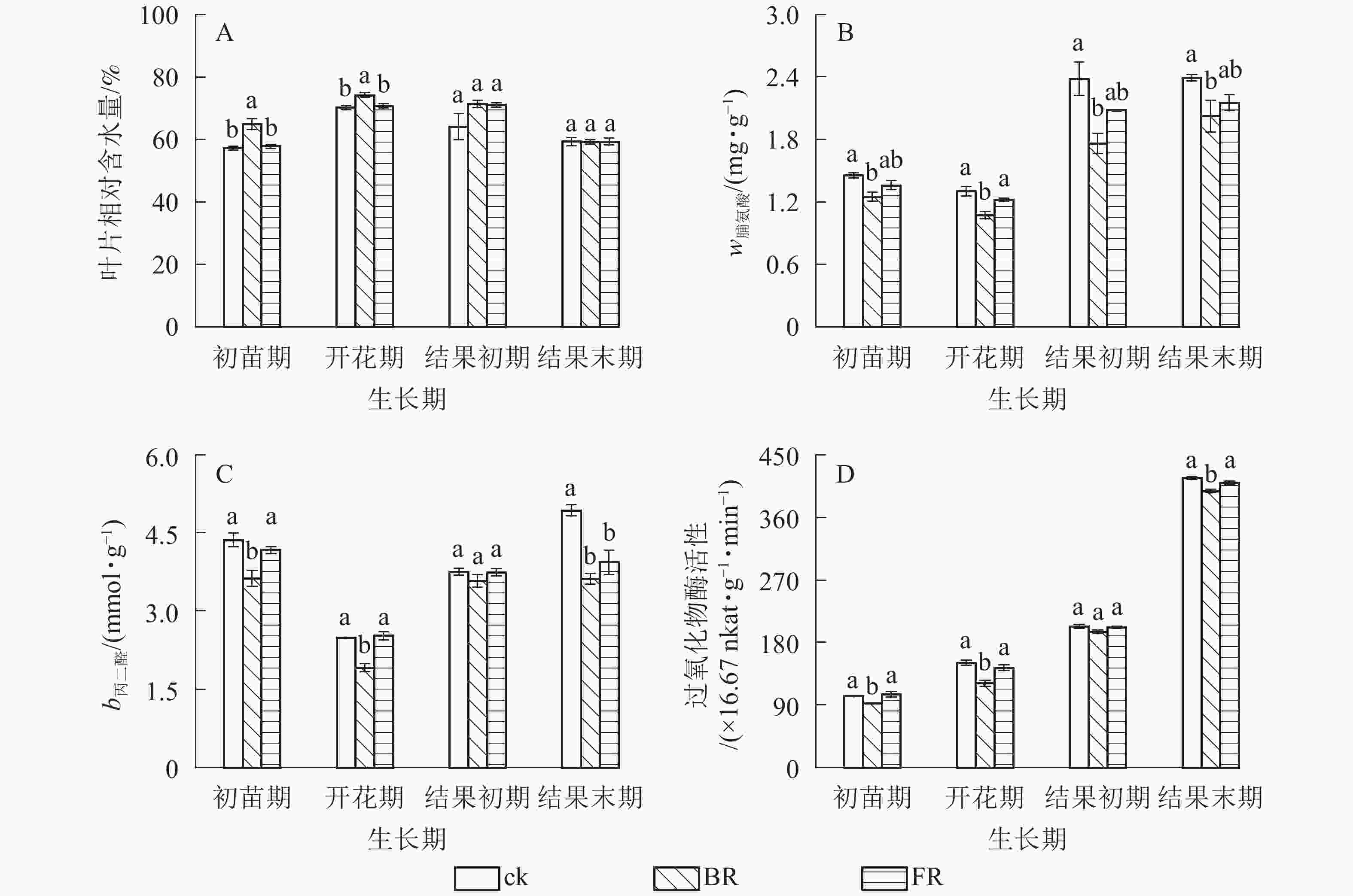
番茄叶片总叶绿素质量分数和叶绿素a质量分数均表现为岩棉处理(BR和FR)高于ck(图2A和图2B),开花期和结果初期差异显著(P<0.05);除结果初期外,同一生长期内叶片叶绿素b质量分数岩棉处理(BR和FR)与对照差异不显著,结果末期叶绿素b质量分数突增,其他时期相同处理下番茄叶片叶绿素b质量分数相对稳定(图2C);相同处理下叶绿素a/b在结果前期比较稳定,结果末期骤降,4个时期不同处理之间均无显著差异(图2D)。同一生长期内番茄叶片相对含水量总体表现为岩棉处理(BR和FR)高于ck,脯氨酸质量分数、丙二醛质量摩尔浓度和过氧化物酶活性等指标均表现为岩棉处理(BR和FR)低于ck。同一处理番茄叶片相对含水量呈现先升后降的趋势,初苗期和开花期BR处理叶片相对含水量比ck分别显著增加13.34%和5.64%(P<0.05) (图3A)。所有时期BR处理下叶片脯氨酸质量分数比ck分别显著降低14.09%、17.55%、26.19%和15.30%(P<0.05) (图3B)。初苗期、开花期和结果末期BR处理叶片丙二醛质量摩尔浓度比ck分别显著降低16.87%,23.07%和26.54%(P<0.05);结果末期FR处理丙二醛质量摩尔浓度比ck显著降低20.16%(P<0.05)(图3C)。初苗期、开花期和结果末期BR处理番茄叶片过氧化物酶活性比ck分别显著降低16.87%,10.15%和4.15% (P<0.05) (图3D)。
-
由表1可知:岩棉不同埋设方式处理后,番茄株高、地茎、叶片数和最大叶面积等生长指标无显著差异(P>0.05)。结果末期BR处理植株根长较FR处理显著增加15.53% (P<0.05),说明BR处理有利于植株根的伸长。
-
生长期内番茄叶片总叶绿素、叶绿素a和叶绿素b质量分数及叶绿素a/b,BR处理总体均高于FR处理(图2)。初苗期和开花期BR处理叶片相对含水量比FR处理分别显著增加12.41%和4.90%(P<0.05) (图3A);初苗期、开花期、结果初期和结果末期BR处理叶片脯氨酸质量分数比FR处理分别显著降低8.04%、12.07%、15.38%和5.87%(P<0.05)(图3B);初苗期和开花期叶片丙二醛质量摩尔浓度BR处理比FR处理分别显著降低12.95%和24.11%(P<0.05)(图3C);初苗期、开花期和结果末期叶片过氧化物酶活性BR处理比FR处理分别显著降低12.60%、15.57%和2.91% (P<0.05) (图3D)。
-
本研究中,模拟水分胁迫条件下番茄各生长期埋设岩棉处理(BR和FR)的土壤容积含水量明显高于ck,说明岩棉能够有效保蓄土壤水分,有利于缓解水分胁迫对植物生长和生理特性的影响。
-
土壤水分不足会抑制植物细胞的生长与扩展,进而影响植株株高、叶片和根系生长[13],株高、叶片数、叶面积、根长及生物量等均出现下降[14-15]。本研究发现:与ck相比,BR和FR处理提高了番茄株高、地茎、叶片数、最大叶面积、根长及生物量,说明在土壤中埋设岩棉有利于缓解水分胁迫对植物形态生长的抑制。结果期不同处理番茄植株最大叶面积均小于开花期,可能与植株新旧叶片更替有关;随水分胁迫时间的延长,新叶叶片细胞生长扩展受到抑制,生长变缓,最大叶面积减小。与RODIYATI等[16]、SINGH等[17]研究结果相似,即叶面积的减小有利于减少植物蒸腾失水量,提高植物抵御干旱的能力,维持植物生长代谢活动(如光合作用)必需的养分和水分的吸收运输均与根系的生长发育密切相关。任毛飞等[18]在利用岩棉育苗时发现,岩棉育苗更有利于幼苗根系的生长,与本研究结论一致;BR和FR处理植株根长均高于ck,体现了岩棉处理对植株根系生长的促进作用。
-
水分胁迫下植物叶片细胞内叶绿体结构遭到破坏,叶绿素合成受阻,分解加快,使得总叶绿素、叶绿素a、叶绿素b质量分数下降,叶绿素a/b发生变化,体现为植物光合作用能力下降,生物量积累受阻[2]。本研究中,相同生长期内叶片总叶绿素和叶绿素a质量分数BR和FR处理高于ck,说明岩棉处理可降低水分胁迫对植物叶片叶绿素含量的影响。结果末期叶绿素b质量分数突增,原因可能是该时期为防止强烈光照对植株造成永久损伤进行了遮光处理,而遮光有利于叶绿素b质量分数的增加[19-20]。有研究表明:表征植物组织水分亏缺程度的叶片相对含水量随胁迫程度或胁迫时间的增加而下降[3-4]。本研究中,初苗期、开花期和结果初期叶片相对含水量BR和FR处理高于ck,说明水分胁迫下岩棉处理的植物叶片细胞水分生理状况更好。有关研究表明:胁迫严重时植物体内大量活性氧基团积累,引发和加剧植物细胞质膜过氧化作用,其代表性产物丙二醛质量摩尔浓度增加[5-6, 21-22]。本研究中,相同生长期内叶片丙二醛质量摩尔浓度表现为ck高于BR和FR,说明岩棉处理减轻了水分胁迫对植物细胞膜的伤害。水分胁迫下植物自身会启动相应的保护机制来抵抗逆境伤害,如抗氧化保护酶系统中的过氧化物酶活性上升[4],清除有害自由基并降解有毒物质[23],脯氨酸等渗透调节物质的产生对活性氧基团(·OH)和氧气(O2)引发的丙二醛增生具有抑制作用[24],对维持自身细胞渗透势,提高叶片吸水、保水能力,维持植物体内正常的水环境具有积极作用[7-8]。本研究中,相同生长期内脯氨酸质量分数表现为ck高于BR和FR,说明岩棉处理植株受胁迫程度较ck低。相同生长期内岩棉处理植物叶片过氧化物酶活性低于ck,说明水分胁迫下岩棉处理植株所受逆境伤害程度较ck低。也有研究认为植物体内过氧化物酶具有两面性,胁迫前期丙二醛的积累诱导细胞过氧化物酶活性提高,用于清除过氧化氢(H2O2)等活性基团,维持膜系统稳定[25-27]。本研究中前3个时期各处理过氧化物酶活性随胁迫时间的延长而增加,过氧化物酶表现为保护效应;胁迫后期过氧化物酶活性升高,高水平的过氧化物酶活性促进了活性氧的生成,使得质膜过氧化作用加剧,造成丙二醛质量摩尔浓度上升,叶绿素a分解[28-30],与此同时,叶片相对含水量下降,植物衰老进程加块,伤害效应大于保护效应。综上,与ck相比,岩棉处理可以缓解干旱对植株生理特性的胁迫作用。
-
岩棉具有的灌水期吸水-旱期释水的特性为盆栽土壤起到水分微调控的作用。岩棉不同埋设方式(BR和FR)处理下,土壤含水量、株高、地茎、叶片数、最大叶面积和干质量等指标差异显著,但BR处理根长显著高于FR。室内模拟试验结果表明[31]:将吸水饱和岩棉埋入土壤中,当水分扩散达到稳定时,距岩棉垂直方向土壤含水量高于水平方向,说明岩棉吸持的水分在垂直方向比水平方向扩散更充分,BR处理相较于FR处理的片状岩棉和ck水分保持更加集中,同时岩棉的多孔结构可为植株根系提供生长通道,缓解土壤干旱环境对根系生长造成的不利影响,有利于植物根系伸长,促进根系有效利用水分,从而使植株所受逆境伤害程度降低。植物自身免疫系统对外界环境变化尤为敏感,生理特性的变化最终会影响植物的形态生长。本研究中,2种岩棉处理对叶绿素含量和叶片相对含水量无显著影响,但FR处理下植株脯氨酸质量分数、丙二醛质量摩尔浓度和过氧化物酶活性显著高于BR处理,说明FR处理的植物体内渗透调节和防御系统已敏感地感受到水分胁迫的影响,而BR处理对缓解植株水分胁迫的应用效果更好。从实际应用角度来分析,块状岩棉的生产工艺较片状岩棉工序少,节省人力物力;操作更方便快捷,易普及;在植物根系下部埋设块状岩棉,易于植物根系深扎入岩棉内部,更利于水分吸收。
-
本研究以农业岩棉为蓄水保水性材料,模拟水分胁迫测定土壤水分和植株生长生理指标的变化。在盆栽土壤中埋设岩棉材料可有效提高土壤含水量,促进植物生长,减少质膜过氧化产物丙二醛的积累,可缓解水分胁迫对植物生长生理特性的影响;相较于环根周埋设片状岩棉,盆栽植物根下部埋设块状岩棉的方式缓解效果更佳。因此,在盆栽植物底部埋入块状岩棉,不仅可以缓解水分胁迫对植物的伤害,也更有利于植物的定植与生长,是减少水资源浪费、提高盆栽植物水分管理效率的新型栽培方式。
Response of growth and physiological indicators of Lycopersicone sculentum to water stress relieved by rock wool
-
摘要:
目的 探索盆栽模式下,岩棉材料及其不同埋设方式对土壤水分保蓄能力和植物栽培的实用效果。 方法 以番茄Lycopersicone sculentum幼苗为研究对象,设置植根下部埋设块状岩棉(BR)、环根周埋设片状岩棉(FR)和埋设惰性不吸水材料(ck) 3个处理,模拟水分胁迫下的植株生长;监测土表下5 cm处土壤含水量、番茄生育期内生长和生理指标变化。 结果 等量灌水条件下,土壤容积含水量从大到小依次为BR、FR、ck,岩棉处理显著高于对照(P<0.05)。同一生长期内岩棉处理(BR和FR)番茄株高、地茎、叶片数、最大叶面积、根长和干质量等指标均高于ck;不同岩棉埋设方式对同期植物的生长指标影响不显著,结果末期BR处理根长显著高于FR处理(P<0.05),同期番茄叶片叶绿素a质量分数、总叶绿素质量分数和相对含水量等从大到小依次为BR、FR、ck,而丙二醛质量摩尔浓度、脯氨酸质量分数和过氧化物酶活性从大到小依次为ck、FR、BR。 结论 岩棉材料可以有效提高盆栽土壤蓄水保水能力,缓解水分胁迫对盆栽植物生长及生理特性的不利影响,其中植根下部埋设块状岩棉(BR)对缓解水分胁迫、促进植物根系定植效果更佳。图3表1参31 Abstract:Objective The purpose of this study is to explore the effects of rock wool and its different burying methods on improving soil water retention capacity as well as plant growth under pot culture mode. Method Lycopersicone sculentum seedlings were selected as the experimental objects. Three treatments were set up to simulate the plant growth under water stress, including burying block rock wool (BR) under the root, sheet rock wool (FR) around the root and inert nonabsorbent material (ck). The dynamic changes of soil water content at 5 cm below the soil surface, the growth and physiological indicators of L. sculentum were monitored. Result Under the condition of equal irrigation, the order of soil volume moisture content from large to small was BR, FR and ck, and the soil volume moisture content of rock wool treatment was significantly higher than that of ck (P<0.05), indicating that rock wool treatment could improve water retention and water storage capacity of potted soil. During the same growth period, the growth index such as plant height, base diameter, leaf number, maximum leaf area, root length and dry weight of L. sculentum treated with rock wool (BR and FR) were higher than those of ck, but there was no significant difference between two rock wool treatments, except that the root length of BR treatment was significantly higher than that of FR treatment (P<0.05). The order of the chlorophyll a content, total chlorophyll content and relative water content of L. sculentum leaf from large to small in the same period were BR, FR, and ck, while the contents of malondialdehyde (MDA), proline (Pro) and peroxidase (POD) were in the opposite order, indicating that BR was more beneficial to plant root elongation and capable of alleviating plants damage caused by soil water stress. Conclusion Rock wool materials can effectively improve water retention and storage capacity of potted soil, and alleviate adverse effects of water stress on the growth and physiological characteristics of potted plants. Burying block rock wool (BR) under the root is more effective in alleviating water stress and promoting plant root colonization. [Ch, 3 fig. 1 tab. 31 ref.] -
表 1 模拟水分胁迫条件下埋设岩棉对番茄植株生长的影响(n=9)
Table 1. Effects of embedded rock wool on tomato growth index under simulated water stress conditions (n=9)
生长期 处理 株高/cm 地茎/mm 叶片数/片 最大叶面积/cm2 根长/cm 干质量/g 初苗期 ck 35.17±1.49 b 5.99±0.18 a 75.00±3.21 b 14.05±1.10 b BR 38.67±0.35 a 6.03±0.21 a 84.55±2.76 a 18.47±0.68 a FR 38.72±0.39 a 6.16±0.24 a 83.2±0.39 ab 20.26±1.27 a 开花期 ck 51.95±1.04 b 7.18±0.13 a 132.89±8.73 b 18.77±0.63 b BR 57.83±1.93 a 7.30±0.24 a 153.67±1.35 a 21.48±1.64 a FR 57.22±1.47 a 7.77±0.31 a 180.89±11.95 ab 24.58±0.20 ab 结果初期 ck 63.44±0.69 b 8.03±0.09 a 206.78±13.13 b 19.37±1.44 a BR 70.67±0.58 a 8.01±0.21 a 233.22±8.55 a 23.05±1.42 a FR 69.61±0.94 a 8.42±0.36 a 256.44±5.67 ab 23.69±0.60 a 结果末期 ck 74.50±1.25 b 8.13±0.10 a 234.00±12.86 b 17.21±1.22 b 17.47±0.81 b 12.37±0.46 b BR 81.78±1.24 a 8.42±0.21 a 275.00±2.14 a 23.00±1.41 a 21.50±0.79 a 14.01±0.22 a FR 80.28±0.20 a 8.52±0.30 a 260.56±7.87 ab 23.31±1.05 a 18.61±0.39 b 12.95±0.39 ab 说明:同列不同字母表示同一生长期不同处理间差异显著(P<0.05) -
[1] 王天, 张舒涵, 闫士朋, 等. 干旱胁迫和磷肥用量对马铃薯根系形态及生理特征的影响[J]. 干旱地区农业研究, 2020, 38(1): 117 − 124. WANG Tian, ZHANG Shuhan, YAN Shipeng, et al. Effects of drought stress and application amount of phosphorus fertilizer on morphological and physiological characteristics of potato roots [J]. Agric Res Arid Areas, 2020, 38(1): 117 − 124. [2] 刘文瑜, 杨发荣, 黄杰, 等. 干旱胁迫对藜麦幼苗生长和叶绿素荧光特性的影响[J]. 干旱地区农业研究, 2019, 37(4): 171 − 177. LIU Wenyu, YANG Farong, HUANG Jie, et al. Effects of drought stresson chlorophyll fluorescence properties and seedling growth of quinoa seedlings [J]. Agric Res Arid Areas, 2019, 37(4): 171 − 177. [3] 周欢欢, 傅卢成, 马玲, 等. 干旱胁迫及复水对‘波叶金桂’生理特性的影响[J]. 浙江农林大学学报, 2019, 36(4): 687 − 696. ZHOU Huanhuan, FU Lucheng, MA Ling, et al. Physiological characteristics of Osmanthus fragrans ‘Boyejingui’ with drought stress and rewatering [J]. J Zhejiang A&F Univ, 2019, 36(4): 687 − 696. [4] 崔婷茹, 于慧敏, 李会彬, 等. 干旱胁迫及复水对狼尾草幼苗生理特性的影响[J]. 草业科学, 2017, 34(4): 788 − 793. CUI Tingru, YU Huimin, LI Huibin, et al. Effect of drought stress and rewatering on physiological characteristics of Pennisetum alopecuroides seedlings [J]. Pratacultural Sci, 2017, 34(4): 788 − 793. [5] 许馨露, 李丹丹, 马元丹, 等. 四季桂抗氧化防御系统对干旱、高温及协同胁迫的响应[J]. 植物学报, 2018, 53(1): 72 − 81. XU Xinlu, LI Dandan, MA Yuandan, et al. Responses of the antioxidant defense system of Osmanthus fragrans cv. ‘Tian Xiang TaiGe’ to drought, heat and the synergistic stress [J]. Chin Bull Bot, 2018, 53(1): 72 − 81. [6] 吴永波, 叶波. 高温干旱复合胁迫对构树幼苗抗氧化酶活性和活性氧代谢的影响[J]. 生态学报, 2016, 36(2): 403 − 410. WU Yongbo, YE Bo. Effects of combined elevated temperature and drought stress on anti-oxidative enzyme activities and reactive oxygen species metabolism of Broussonetia papyrifera seedlings [J]. Acta Ecol Sin, 2016, 36(2): 403 − 410. [7] 李涛龙, 胡笑涛, 王文娥, 等. 水分胁迫对玉米叶片脯氨酸和丙二醛含量的影响[J]. 节水灌溉, 2017(6): 34 − 37. LI Taolong, HU Xiaotao, WANG Wen’e, et al. Effects of water stress on proline and malonadialdehyde content in leaves of spring maize [J]. Water Saving Irrig, 2017(6): 34 − 37. [8] 丁玉梅, 马龙海, 周晓罡, 等. 干旱胁迫下马铃薯叶片脯氨酸、丙二醛含量变化及与耐旱性的相关性分析[J]. 西南农业 学报, 2013, 26(1): 106 − 110. DING Yumei, MA Longhai, ZHOU Xiaogang, et al. Effects of drought stress on free proline and malonaldedyde contents in potato leaves and correlation analysis of drought-tolerant level among different varieties [J]. Southwest China J Agric Sci, 2013, 26(1): 106 − 110. [9] 任少勇, 丁丽. 不同无土栽培基质对番茄产量和品质的影响[J]. 长江蔬菜, 2018(4): 62 − 64. REN Shaoyong, DING Li. Effects of different soilless culture substrates on yield and quality of tomato [J]. J Changjiang Veg, 2018(4): 62 − 64. [10] 李永胜, 苟春林, 杜建军, 等. 保水剂与磷肥的相互影响及节水保肥效果[J]. 水土保持研究, 2014, 21(6): 67 − 71. LI Yongsheng, GOU Chunlin, DU Jianjun, et al. Interaction between water retaining agent and phosphorus fertilizers and the effect of water and fertilizer conservation [J]. Res Soil Water Conserv, 2014, 21(6): 67 − 71. [11] 丁红, 张智猛, 戴良香, 等. 干旱胁迫对花生生育中后期根系生长特征的影响[J]. 中国生态农业学报, 2013, 21(12): 1477 − 1483. DING Hong, ZHANG Zhimeng, DAI Liangxiang, et al. Effects of drought stress on root growth characteristics of peanut during mid-to-late growth stages [J]. Chin J Eco-Agric, 2013, 21(12): 1477 − 1483. [12] 高俊凤. 植物生理学实验指导[M]. 北京: 高等教育出版社, 2006. [13] ZHAO Junbin, HARTMANN H, TRUMBORE S, et al. High temperature causes negative whole-plant carbon balance under mild drought [J]. New Phytol, 2013, 200(2): 330 − 339. [14] Mc DOWELL N G. Mechanisms linking drought, hydraulics, carbon metabolism, and vegetation mortality [J]. Plant Physiol, 2011, 155(3): 1051 − 1059. [15] 张凯, 王润元, 王鹤龄, 等. 温度升高和降水减少对半干旱区春小麦生长发育及产量的协同影响[J]. 中国生态农业学 报, 2019, 27(3): 413 − 421. ZHANG Kai, WANG Runyuan, WANG Heling, et al. Influence of climate warming and rainfall reduction on semi-arid wheat production [J]. Chin J Eco-Agric, 2019, 27(3): 413 − 421. [16] RODIYATI A, ARISOESILANINGSIH E, ISAGI Y, et al. Responses of Cyperus brevifolius (Rottb.) Hassk. and Cyperus kyllingia Endl. to varying soil water availability [J]. Environ Exp Bot, 2005, 53(3): 259 − 269. [17] SINGH B, SINGH G. Biomass partitioning and gas exchange in Dalbergia sissoo seedlings under water stress [J]. Photosynthetica, 2003, 41(3): 407 − 414. [18] 任毛飞, 王吉庆, 周燕, 等. 岩棉育苗块持水量对番茄幼苗生长的影响[J]. 北方园艺, 2016(9): 47 − 49. REN Maofei, WANG Jiqing, ZHOU Yan, et al. Effect of water capacity of rock wool block on the growth of tomato seedlings [J]. Northern Hortic, 2016(9): 47 − 49. [19] 孙小玲, 许岳飞, 马鲁沂, 等. 植株叶片的光合色素构成对遮阴的响应[J]. 植物生态学报, 2010, 34(8): 989 − 999. SUN Xiaoling, XU Yuefei, MA Luyi, et al. A review of acclimation of photosynthetic pigment composition in plant leaves to shade environment [J]. Chin J Plant Ecol, 2010, 34(8): 989 − 999. [20] 朱雨晴, 薛晓萍. 遮阴及复光对花果期番茄叶片光合特性的影响[J]. 中国农业气象, 2019, 40(2): 126 − 134. ZHU Yuqing, XUE Xiaoping. Effects of shading and light restoration on photosynthetic characteristics of tomato leaves during flowering and fruit period [J]. Chin J Agrometeorol, 2019, 40(2): 126 − 134. [21] 邵惠芳, 陈征, 许嘉阳, 等. 2种烟草幼苗叶片对不同强度干旱胁迫的生理响应比较[J]. 植物生理学报, 2016, 52(12): 1861 − 1871. SHAO Huifang, CHEN Zheng, XU Jiayang, et al. Physiological responses of two tobacco cultivar leaves to different drought stresses during seedling stage [J]. Plant Physiol J, 2016, 52(12): 1861 − 1871. [22] MA Xingli, XIN Zeyu, WANG Zhiqiang, et al. Identification and comparative analysis of differentially expressed miRNAs in leaves of two wheat (Triticum aestivum L.) genotypes during dehydration stress [J]. BMC Plant Biol, 2015, 15(1): 21. [23] 胡振兴, 刘灵, 陈丽萍, 等. 干旱胁迫下丛枝菌根对大豆抗氧化代谢及根围微生物的影响[J]. 中国生态农业学报, 2018, 26(4): 526 − 537. HU Zhenxing, LIU Ling, CHEN Liping, et al. Effects of arbuscular mycorrhizal fungi on antioxidant metabolism and rhizospheric micro-organism of soybean (Glycine max) under drought stress [J]. Chin J Eco-Agric, 2018, 26(4): 526 − 537. [24] 储凤丽, 刘亚军, 王文静, 等. 干旱胁迫对甘薯活性氧代谢、渗透调节物质、SPAD及叶绿素荧光特性的影响[J]. 中 国农学通报, 2019, 35(26): 29 − 34. CHU Fengli, LIU Yajun, WANG Wenjing, et al. Effects of drought stress on active oxygen metabolism, osmotic regulators, SPAD and chlorophyll fluorescence characteristics of sweet potato [J]. Chin Agric Sci Bull, 2019, 35(26): 29 − 34. [25] 顾建勤, 闫志利, 牛俊义, 等. 干旱胁迫及复水对豌豆苗期保护酶活性及膜脂过氧化的影响[J]. 干旱地区农业研究, 2012, 30(3): 159 − 164. GU Jianqin, YAN Zhili, NIU Junyi, et al. Effect of drought stress and rewater on protective enzyme activity and membrane lipid peroxidation in pea leaves during seedling stage [J]. Agric Res Arid Areas, 2012, 30(3): 159 − 164. [26] 范苏鲁, 苑兆和, 冯立娟, 等. 干旱胁迫对大丽花生理生化指标的影响[J]. 应用生态学报, 2011, 22(3): 651 − 657. FAN Sulu, YUAN Zhaohe, FENG Lijuan, et al. Effects of drought stress on physiological and biochemical parameters of Dahlia pinnata [J]. Chin J Appl Ecol, 2011, 22(3): 651 − 657. [27] 赵丽英, 邓西平, 山仑. 活性氧清除系统对干旱胁迫的响应机制[J]. 西北植物学报, 2005, 25(2): 413 − 418. ZHAO Liying, DENG Xiping, SHAN Lun. The response mechanism of active oxygen species removing system to drought stress [J]. Acta Bot Boreali-Occident Sin, 2005, 25(2): 413 − 418. [28] 闫成仕. 水分胁迫下植物叶片抗氧化系统的响应研究进展[J]. 烟台师范学院学报(自然科学版), 2002, 18(3): 220 − 225. YAN Chengshi. Antioxidant responses to water stress in plant leaves [J]. Yantai Norm Univ J Nat Sci, 2002, 18(3): 220 − 225. [29] 尹永强, 胡建斌, 邓明军. 植物叶片抗氧化系统及其对逆境胁迫的响应研究进展[J]. 中国农学通报, 2007, 23(1): 105 − 110. YIN Yongqiang, HU Jianbin, DENG Mingjun. Latest development of antioxidant system and responses to stress in plant leaves [J]. Chin Agric Sci Bull, 2007, 23(1): 105 − 110. [30] ZHANG Jingxian, KIRKHAM M B. Drought-stress-induced changes in activities of superoxide dismutase, catalase, and peroxidase in wheat species [J]. Plant Cell Physiol, 1994, 35(5): 785 − 791. [31] 顾佳悦, 方伟, 高竞, 等. 应用岩棉材料提高丘陵区经济林土壤水分保蓄能力[J]. 干旱地区农业研究, 2020, 38(3): 10 − 18. GU Jiayue, FANG Wei, GAO Jing, et al. Improving soil water retention capacity of economic forest using rock wool in hilly area [J]. Agric Res Arid Areas, 2020, 38(3): 10 − 18. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20200221







 下载:
下载: