-
赭曲霉毒素(ochratoxin)是曲霉属Aspergillus和青霉属Penicillium一些产毒菌株的次级代谢产物,包括赭曲霉毒素A,B,C,D和a等7种结构类似化合物[1];其中赭曲霉毒素A(ochratoxin A,OTA)毒性最大,在自然界分布最广泛,对农产品的污染也最严重,是严重危害人类健康的毒素之一。OTA在食物中较稳定且不易分解,在霉变谷物、饲料等中最常见,现已被证明具有弱诱变性、免疫毒性,能引起免疫抑制,并具有致癌、致畸、致突变作用。世界卫生组织建议,谷物、豆类及其产品中的OTA限量标准为5.0 μg·kg-1,而牛奶中OTA是“零容忍”毒素之一。目前中国对OTA的检测主要依靠薄层层析法(TLC),高效液相色谱法(HPLC),酶联免疫吸附法(ELISA)等仪器分析技术。这些方法虽然具有特异性强、灵敏度高的特点,但由于使用的仪器与试剂相对比较昂贵,样品处理过程繁琐,不适宜用来进行快速检测。胶体金免疫层析技术是20世纪80年代初期开发的一种免疫分析方法,它是在单克隆抗体技术、胶体金免疫技术和新材料技术基础上发展起来的快速检测技术[2-4]。该技术以微孔膜为固相载体,将已知的特异性抗原固定于硝酸纤维素(NC)膜上作为检测线。当加入待测样品后,样品经毛细管的扩散作用首先与胶体金标记物相结合,并继续在扩散作用下泳动至检测线,标记物与待测物的复合物被检测线的抗原或抗体截获,从而呈现红色的可见条带[5]。本法具有快速、灵敏度高、特异性强、稳定性好、操作简单等优点,结果判断直观可靠,容易被基层单位人员掌握,适合现场快速筛查和基层大面积推广,现在已广泛应用于临床诊断及药物检测等领域[6]。本研究应用胶体金免疫层析技术,将OTA单抗与胶体金偶联物固化在结合垫上,OTA-BSA(BSA,Bovine serum albumin,牛血清白蛋白)偶联物固化在检测线,羊抗鼠IgG固化在质控线,以制备一种快速检测食品和饲料中赭曲霉毒素A的方法。
-
赭曲霉毒素A(OTA)标准品购自美国Sigma公司;抗赭曲霉毒素单克隆抗体(monoclonal OTA antibody)和OTA-BSA由本实验室制备;羊抗鼠IgG、氯金酸、柠檬酸三钠、碳酸钾购自生工生物工程上海股份有限公司;硝酸纤维素膜(NC膜)、结合垫、样品垫、吸水纸、胶体金储存液、抗原稀释液购自上海杰一生物技术有限公司。
-
采用柠檬酸三钠法,取100.0 mL质量分数为0.01%的氯金酸溶液到300.0 mL锥形瓶中,将锥形瓶置于恒温磁力搅拌器上,搅拌加热至沸腾,持续搅拌加入质量分数为1%的柠檬酸三钠溶液2.5 mL,继续搅拌加热10 min,当溶液颜色逐渐变至透亮红色并不再改变后,停止加热。适当速度搅拌至室温,用去离子水定容至100.0 mL保存备用。
-
①标记前先将抗赭曲霉毒素A单克隆抗体溶液在转速15 000 r·min-1,温度4 ℃条件下离心30 min,取上清液用于标记。②量取制备好的胶体金溶液50.0 mL,用0.1 mol·L-1的碳酸钾(K2CO3)调节胶体金溶液pH 8.0。③用磁力搅拌器充分搅拌,并逐滴加入200.0 μL抗赭曲霉毒素A单克隆抗体溶液,达终质量浓度56.0 mg·L-1,混匀搅拌45 min。④取质量分数为10%BSA溶液逐滴加入至胶体金中至终质量分数为1%,继续搅拌15 min。⑤4 ℃,8 500 r·min-1离心15 min。⑥小心弃去上清液。⑦沉淀利用胶体金储存液悬浮至4 ℃冰箱备用。
-
样品垫筛选:样品垫作为样品的载体,其滤过性、吸水性、强度等性质对于试纸条的“跑板”有重要影响。参考文献[7]对4种样品垫(JY-BX108,JY-BX109,JY-BX110,JY-BX111)进行筛选,其方法为:在4批样品垫中随机抽检,分别编号为D1~D4,每张裁下10 mm×300 mm规格,组装成试纸条。取20条试纸条,通过检测样品的缓释速度、样品流动的均一性、过滤效果选择最佳样品垫。硝酸纤维素(NC)膜筛选:不同公司生产的NC膜对样品的检测时间、灵敏度等会产生重要影响,选择合适的NC膜对试纸条的研发尤为重要[8]。对2种规格NC膜分别编号为N1和N2,喷上相同质量浓度的OTA偶联抗原,组装成试纸条,取20条试纸条以NC膜的爬速、NC膜背景的洁净度、阴性显色强度等指标进行检测。吸水纸、结合垫的型号也按照相似方法进行筛选,选择最佳的型号备用。
-
NC膜的包被质量浓度影响试纸条的敏感度,因此选用2种方案测试OTA-BSA的包被质量浓度。1号方案:利用抗原稀释液稀释OTA-BSA,配制终质量浓度为3.22 g·L-1(原7.60 g·L-1)。2号方案:利用抗原稀释液稀释OTA-BSA,配制终质量浓度4.80 g·L-1(原15.60 g·L-1)。质控线利用抗原稀释液稀释羊抗鼠IgG,配制成终质量浓度为1.00 g·L-1和1.50 g·L-1(原10.00 g·L-1)。利用划膜喷金一体机以1.0 μL·cm-1和2.0 μL·cm-1的量分别包被到NC膜上。最终通过条带颜色的均匀和清晰程度选择最佳方案。
-
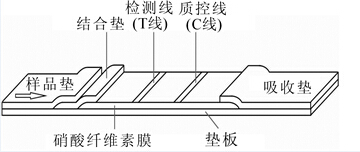
试纸条是在底板上粘接NC膜、结合垫、样品垫和吸水纸而成的。在底板中部粘贴NC膜,底板左侧粘贴样品垫,样品垫之下放置结合垫,结合垫上固化胶体金和抗OTA单抗偶联物,结合垫一端与NC膜紧密相连,在底板右侧粘贴吸收垫,吸收垫左侧与NC膜相连(图 1)。NC膜上有2条分开的显示印记带,分别喷上OTA-BSA偶联物和羊抗鼠IgG,作为检测线(T线)和质控线(C线),置于37 ℃干燥箱烘干15 min。利用点膜仪将抗赭曲霉毒素A单克隆抗体标记胶体金探针溶液均匀喷到结合垫上,真空冷冻干燥。最后将喷好T线和C线的NC膜、结合垫、样品垫和吸水纸按图 1所示组装并装入外壳中(图 2),以用于样品检测,样品垫正对加样孔,NC膜正对检测窗。
-
将试纸条检测卡平放,用加样管吸取制备好的检测样品,加入至样品孔(S孔,图 3C~D),样品在毛细管的扩散作用下沿着NC膜泳动至T线和C线,5 min内观察检测结果。如果试纸条失效,C线不呈现红色条带(图 3B),需重新检测。样品中没有OTA,试纸条的T线和C线均呈现红色条带。结合垫上的胶体金-OTA单抗在毛细管的扩散作用下泳动至T线,与T线的OTA-BSA相结合,呈现红色条带,多余的胶体金-OTA单抗泳动至C线,与羊抗鼠IgG相结合,呈现红色条带(图 3C)。样品中含有OTA,即可与结合垫上的胶体金-OTA单抗结合,并在毛细管的扩散作用下泳动至T线。由于胶体金-OTA单抗与样品中的OTA相结合,形成胶体金-OTA单抗-OTA复合物,因此T线的OTA-BSA无法与胶体金-OTA单抗相结合,不呈现红色条带或呈现微弱的红色条带,多余的胶体金-OTA单抗泳动至C线,与羊抗鼠IgG相结合,呈现红色条带(图 3D)。
-
将OTA标准品利用pH 7.4,0.01 mol·L-1的PBS溶液配制成质量浓度为0,1.0,5.0,10.0 μg·L-1的标准液,分别取70.0 μL加入到试纸条检测孔中,每个质量浓度重复检测3次,5 min后观察检测结果。检测结果通过试纸条呈现的红色条带颜色的深浅判断。样品中含有OTA,即可与结合垫上的胶体金-OTA单抗结合,并在毛细管的扩散作用下泳动至T线。形成胶体金-OTA单抗-OTA复合物,因此,T线的OTA-BSA无法与胶体金-OTA单抗相结合,不呈现红色条带或呈现微弱的红色条带,多余的胶体金-OTA单抗泳动至C线,与羊抗鼠IgG相结合,呈现红色条带。通过颜色的深浅即可判定肉眼可视检测限和肉眼可视的消线质量浓度。
-
将桔毒素、伏马毒素B1、玉米赤霉烯酮标准品利用pH 7.4,0.01 mol·L-1的PBS溶液配制成质量浓度为1.0,10.0,100.0 μg·L-1的标准液,分别取70 μL加入到试纸条检测孔中,每个质量浓度重复检测3次,5 min后观察检测结果。检测结果通过试纸条呈现的红色条带颜色的深浅判断。桔毒素、伏马毒素B1、玉米赤霉烯酮如果发生非特异性反应,形成胶体金-OTA单抗-桔毒素(伏马毒素B1/玉米赤霉烯酮)复合物,因此T线的OTA-BSA无法与胶体金-OTA单抗相结合,不呈现红色条带或呈现微弱的红色条带,多余的胶体金-OTA单抗泳动至C线,与羊抗鼠IgG相结合,C线呈现红色条带。桔毒素、伏马毒素B1、玉米赤霉烯酮如果不发生非特异性反应,结合垫上的胶体金-OTA单抗在毛细管的扩散作用下泳动至T线,与T线的OTA-BSA相结合,呈现红色条带,多余的胶体金-OTA单抗泳动至C线,与羊抗鼠IgG相结合,呈现红色条带。
-
利用已制备的胶体金标记抗体,匹配Pall vivid 90 NC膜和Pall vivid 170 NC膜测试。试验结果如图 4所示,Pall vivid 170 NC膜的条带更清晰,所以选择Pall vivid 170 NC膜。
-
检测结果显示:当OTA-BSA终质量浓度为4.8 g·L-1(原15.6 g·L-1),质控线用羊抗鼠IgG配制终质量浓度为1.5 g·L-1(原10.0 g·L-1),NC膜的包被量为1.0 μL·cm-1的时候所呈现的条带最清晰、最均匀,因此选择此方案为最佳包被方案。
-
当用PBS检测试纸条时,检测线与质控线均出现红色条带,随着加入的OTA样品质量浓度的增加,检测线的红色条带颜色逐渐变浅,当OTA标准品质量浓度达到1.0 μg·L-1的时候,检测线的红色条带与对照组相比显著变浅。质量浓度达到10.0 μg·L-1检测线未出现红色条带(图 5),其中质控线出现红色条带,因此判断该OTA试纸条的肉眼可视检测限为1.0 μg·L-1,肉眼可视的消线质量浓度为10.0 μg·L-1。
-
由于桔毒素、伏马毒素B1、玉米赤霉烯酮与胶体金-OTA单抗不发生非特异性反应,因此结合垫上的胶体金-OTA单抗在毛细管的扩散作用下泳动至T线,与T线的OTA-BSA相结合,试纸条均呈现2条红色条带。以上毒素不同质量浓度下特异性检测结果如表 1所示,表明本研究所制备的试纸条与桔毒素、伏马毒素B1、玉米赤霉烯酮均无交叉反应,特异性良好。
表 1 赭曲霉毒素A检测试纸条特异性试验结果
Table 1. Specificial results of the OTA test strip
毒素种类 不同质量浓度下特异性试验结果 1 10 10.0 μg·L-1 桔毒素 阴性 阴性 阴性 伏马毒素B1 阴性 阴性 阴性 玉米赤霉烯酮 阴性 阴性 阴性 -
食品安全问题一直是世界关注的焦点,其中霉菌毒素污染最为常见[9]。本研究应用胶体金免疫层析技术研制OTA检测试纸条,胶体金在弱碱环境下带负电荷,可与蛋白质分子的正电荷基团形成牢固的结合。由于这种结合是静电结合,所以不影响蛋白质的生物学特性。利用低速搅拌的方法将胶体金与抗OTA单克隆抗体进行偶联,结果表明:OTA单抗与胶体金通过非共价结合的方式牢固结合,在NC膜上移动顺畅,无任何滞留。当OTA-BSA配制终质量浓度为4.8 g·L-1(原15.6 g·L-1),质控线用羊抗鼠IgG配制终质量浓度为1.5 g·L-1(原10.0 g·L-1),NC膜的包被量为1.0 μL·cm-1时呈现最清晰、最均匀的条带。
本研究对试纸条的组成材料也做了严格筛选,通过比较分析不同类型的NC膜、结合垫、吸收垫、吸水纸、胶体金的喷金量、抗原点样位置以及T线、C线的划线位置等多种因素对试纸条检测特性的影响,确定最佳条件,并组装试纸条。本研究通过优化,最终选择Pall Vivid 170 NC膜和JY-BX108样品垫。
中国对OTA的限量标准是谷物、豆类及其产品中不能超过5.0 μg·kg-1(5.0 μg·L-1)。本研究所制备的试纸条的检测灵敏度可达1.0 μg·L-1,可满足国家检测标准。检测样品时,与对照组相比即可判定谷物、豆类及其产品被OTA污染与否。国外对OTA的检测也采用高效液相色谱法(HPLC)[10]、酶联免疫吸附法(ELISA)[11]等仪器分析技术,也有利用胶体金检测OTA的报道[12]。但检测下限仅为10.0 μg·L-1,而且耗时。本研究制备的OTA检测试纸条的肉眼可视检测限为1.0 μg·L-1,检测时间仅为5 min,时间短、灵敏度高,可广泛应用于大量样品的快速筛查。
An Ochratoxin A test strip based on a lateral-flow immunochromatographic assay
-
摘要: 针对霉菌毒素精准检测技术的开发对于保障食品安全至关重要。利用胶体金与赭曲霉毒素A单抗偶联物和赭曲霉毒素A-BSA偶联物(OTA-BSA),开发了一种快速检测赭曲霉毒素A的方法。研究结果表明:①当OTA-BSA配制终质量浓度为4.8 g·L-1,质控线用羊抗鼠IgG配制终质量浓度为1.5 g·L-1,硝酸纤维素(NC)膜的包被量为1.0 μL·cm-1时呈现最清晰、最均匀的条带。②赭曲霉毒素A胶体金快速检测试纸条的灵敏度达到1.0 μg·L-1,检测时间仅为5 min,非常适合现场快速检测。该检测试纸条具有携带方便、灵敏度高、特异性强等优点。由于本方法检测时间短,灵敏度高,与传统的仪器和酶联免疫检测方法相比,在野外和临床检测中更具有推广应用价值。图5表1参12Abstract: To develop an accurate and precise detection method to screen Ochratoxin A (OTA) contaminants for food safety concerns, a lateral-flow immunochromatographic assay for OTA detection was developed using colloidal nanoparticles, monoclonal OTA antibodies, and the OTA-BSA (bovine serum albumin) conjugate. The test strip was treated with PBS for negative control and OTA standard samples (ranging from 1 to 10 μg·L-1) for measurement, and 4 replications. Results over the entire growth period showed that (1) the optimized concentration of OTA-BSA was 4.8 g·L-1 and goat-anti mouse (IgG) concentration was 1.5 g·L-1. The suitable coating volume of OTA-BSA and IgG in Nitrocellulose (NC) membranes was 1.0 μL·cm-1 with (2) a sensitivity for this test strip of 1.0 μg·L-1. The entire detection procedure for OTA was completed within 5 min. This test strip provided advantages of easy carrying, high sensitivity, and specificity, thereby serving as a suitable and valuable screening tool for field and clinical detection compared to traditional equipment and to the enzyme-linked immunosorbent assay (ELISA)-based method. [Ch, 5 fig. 1 tab. 12 ref.]
-
表 1 赭曲霉毒素A检测试纸条特异性试验结果
Table 1. Specificial results of the OTA test strip
毒素种类 不同质量浓度下特异性试验结果 1 10 10.0 μg·L-1 桔毒素 阴性 阴性 阴性 伏马毒素B1 阴性 阴性 阴性 玉米赤霉烯酮 阴性 阴性 阴性 -
[1] 孙亚宁, 胡骄飞, 邓瑞广, 等. 赭曲霉毒素A人工抗原的合成与鉴定[J]. 食品工业科技, 2011, 32(5): 172 - 175. SUN Yaning, HU Jiaofei, DENG Ruiguang, et al. Synthesis and identification of ochratoxin A artificial immunogen[J]. Sci Technol Food Ind, 2011, 32(5): 172 - 175. [2] SHYU R H, SHYU H F, LIU H W, et al. Colloidal gold-based immunochromatographic assay for detection of ricin [J]. Toxicon, 2002, 40(3): 255 - 258. [3] 赖卫华, 熊勇华, 陈高明, 等. 应用胶体金试纸条快速检测赭曲霉毒素A 的研究[J]. 食品科学, 2005, 26(5): 204 - 207. LAI Weihua, XIONG Yonghua, CHEN Gaoming, et al. Preparation of colloidal gold strip for rapid detection of ochratoxin A [J]. Food Sci, 2005, 26(5): 204 - 207. [4] 邓省亮, 赖卫华, 许杨. 胶体金标记免疫层析法快速检测黄曲霉毒素B1的研究[J]. 食品科学, 2007, 28(2): 232 - 236. DENG Shengliang, LAI Weihua, XU Yang. Study on gold immunochromatography assay for rapid detection of aflatoxin B1 [J]. Food Sci, 2007, 28(2): 232 - 236. [5] 林彤, 独军政, 丛国政, 等. 胶体金标记免疫层析技术的最新应用进展[J]. 安徽农业科学, 2010, 38(16): 8429 - 8431. LIN Tong, DU Junzheng, CONG Guozheng, et al. Latest application of gold immunochromatographic assay [J]. J Anhui Agric Sci, 2010, 38(16): 8429 - 8431. [6] 舒文祥, 徐炜, 李艳, 等. 胶体金免疫层析法快速检测赭曲霉毒素A研究[J]. 粮食与油脂, 2011(10): 20 - 22. SHU Wenxiang, XU Wei, LI Yan, et al. Study on gold immunochromatography assay for rapid detection of ochratoxin A [J]. J Cereals Oils, 2011(10): 20 - 22. [7] 夏骏. 三聚氰胺胶体金免疫层析方法的建立[D]. 南昌: 南昌大学, 2013. XIA Jun. Development Colloidal Gold Lateral Flow Assay for Detection of Melamine [D]. Nanchang: Nanchang University, 2013. [8] 韦素梅, 李炜, 刘云龙. 影响赭曲霉毒素A免疫层析试纸条最低检出限的因素[J]. 粮食与食品工业, 2013, 20(2): 55 - 58. WEI Sumei, LI Wei, LIU Yunlong. Affections of the minimum detection limit of OTA colloidal gold strip[J]. Cereal Food Ind, 2013, 20(2): 55 - 58. [9] 李鑫, 李培武, 张奇, 等. 农产品中赭曲霉毒素A免疫层析试纸条快速检测技术研究[J]. 中国油料作物学报, 2014, 36(5): 648 - 652. LI Xin, LI Peiwu, ZHANG Qi, et al. Development of an immunochromatographic assay for ochratoxin A in agro-products [J]. Chin J Oil Crop Sci, 2014, 36(5): 648 - 652. [10] ZIMMERLI B, DICK R. Determination of ochratoxin A at the ppt level in human blood, serum, milk and some foodstuffs by high-performance liquid chromatography with enhanced fluorescence detection and immunoaffinity column cleanup: methodology and Swiss data [J]. J Chromatogr B Biomed Sci Appl, 1995, 666(1): 85 - 99. [11] SCOTT P M. Methods of analysis for ochratoxin A [G]// de VRIES J W, TRUCKSESS M W, JACKSOW L S. Mycotoxins and Food Safety. New York: Springer, 2002: 117 - 134. [12] MOON J, KIM G, LEE S. Development of nanogold-based lateral flow immunoassay for the detection of ochratoxin A in buffer systems [J]. J Nanosci Nanotechnol, 2013, 13(11): 7245 - 7249. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.2016.03.023







 下载:
下载: