-
凋落物是森林生态系统内由生物组分产生并归还到林地表面的所有有机物质的总称[1],也是种子落地后最先接触到的物理环境,对种子萌发、幼苗存活和生长等天然更新关键环节具有重要作用[2-4]。凋落物的存在会改变种子萌发和生长的微环境,同时其物理阻隔作用也对天然更新产生一定障碍[5-6],并且这种作用因凋落物类型、厚度和覆盖方式的不同而对幼苗出土及早期生长产生不同程度的影响[4, 6-8]。
水杉Metasequoia glyptostroboides为中国特有的杉科Taxodiaceae水杉属Metasequoia孑遗植物,属国家Ⅰ级保护树种,有植物界“活化石”之称。现仅存原生母树5 696株,集中分布于湖北利川、湖南龙山和重庆石柱之间狭窄的三角区域内,林下鲜见其天然更新的幼苗及幼树,天然更新困难[9-10]。天然更新是指植物从其种子成熟、萌发、生长到幼苗建成的连续过程[11]。它不仅是种群得以繁衍和恢复的重要方式[12],也是维持天然林动态稳定和可持续发展的基础[13]。有许多研究已对水杉天然更新障碍因素及机制进行了探讨,但主要集中在生物学特性[14]、遗传、种群结构[15, 10]、人为干扰[10]等方面。徐来仙等[8]研究发现:凋落物对水杉自身种子萌发和生长具有化感抑制作用,且不同类型凋落物的化感作用存在差异,而关于凋落物对水杉更新幼苗出土和生长的影响还未见报道。基于野外调查发现水杉母树林内有大量凋落物,凋落物质量一般达145.60~9 775.36 g·m−2,而水杉种子极小极轻(千粒重为2.57 g)[8],因此提出假设:水杉凋落物对水杉幼苗出土及早期生长是否具有物理阻隔作用?其影响程度是否与凋落物类型、覆盖方式及质量的多少紧密相关?鉴于此,本研究模拟种子成熟脱落后位于凋落物下方和上方的情况,通过野外模拟试验,采用不同类型、不同质量凋落物对种子进行覆盖或铺垫,探讨凋落物物理阻隔对水杉幼苗出土和早期生长的影响,旨在为解除水杉种群天然更新障碍提供科学依据。
-
为保证凋落物收集具有代表性,在湖北省利川市林业科学研究所水杉母树林内按东南西北中5个方向分30个区域随机布设凋落物收集框。于2020年10月末收集水杉母树上自然脱落的当季凋落物为新鲜凋落物[即尚未进入分解过程的混合物,其中各组成部分依据凋落物实际组成设定比例,为m(叶)∶m(枝)∶m(果皮等)=11.0∶8.0∶1.0];2020年11月末收集水杉母树林内地表的凋落物为自然凋落物[包括各分解层的枝叶果皮等混合物,其中各分解层同样依据凋落物实际组成设定比例,为m(未分解层)∶m(半分解层)∶m(全分解层)=1.2∶1.2∶1.0]。考虑到烘干可能会改变凋落物的化学成分,因此采集的凋落物置于室温风干后储藏于信封备用。
水杉种子为2020年11月从水杉原生母树1076号(树龄118 a,树高31 m,胸径87.6 cm,生长地理位置为30°07′21″N,108°35′45″E,海拔为1 114 m)采集。种子含水量为(9.78±1.13)%,千粒重为(2.57±0.17) g,储藏于4 ℃冰箱备用。
-
采用野外大田模拟试验,选取凋落物类型、凋落物覆盖方式、凋落物质量为控制因子,其中凋落物类型包括2种:新鲜凋落物和自然凋落物;覆盖方式设置2个水平:种子下层铺垫凋落物(即种子播种在凋落物上方,简称上方)、种子上层覆盖凋落物(即种子播种在凋落物下方,简称下方);凋落物质量设置6个梯度:0 (对照)、100、300、500、700、900 g·m−2。
于2021年4月初在湖北省利川市林业科学研究所基地(30°16′01″N,108°57′12″E)开展试验,试验地海拔为1 112.5 m,土壤为山地黄壤。播种前将试验田除草、整地、杀菌,起垄(宽100 cm),留沟(宽30 cm),将垄面划分成1 m×1 m的小样块。按试验设计将种子和凋落物均匀撒播,播种密度为300粒·m−2,每个处理3个重复,采用称量法控制各个处理的凋落物质量。吴漫玲[16]研究发现:3针遮阳网(遮光率为62.21%)更适于水杉幼苗早期生长,故本研究在3针遮阳网条件下进行。播种完成后,浇水使土壤湿透,每隔30 d记录幼苗出土和存活的数量(种子上层覆盖凋落物时以子叶穿过凋落物为出苗成功[17]),且在小样块内随机抽取10株幼苗并挂牌测量苗高。水杉幼苗经历150 d (1个生长季)后收苗,量取苗高、地径、主根长度和叶片数,并采用扫描仪结合Image J软件测量叶面积,随后将幼苗从基部分成地上和地下2个部分,分别置于信封中在80 ℃下烘干至恒量(48 h),用天平称取幼苗生物量。根据种子萌发和存活计算出苗率、存活率。出苗率=(穿过凋落物表面的幼苗数/播种种子总数)×100%[18];存活率=(试验结束后存活的幼苗数/播种种子总数)×100%[18]。
-
利用SPSS对各指标进行凋落物类型、覆盖方式、质量的多因素方差分析和单因素方差分析,采用Duncan法判断差异显著性(P=0.05)。采用Origin绘图。
-
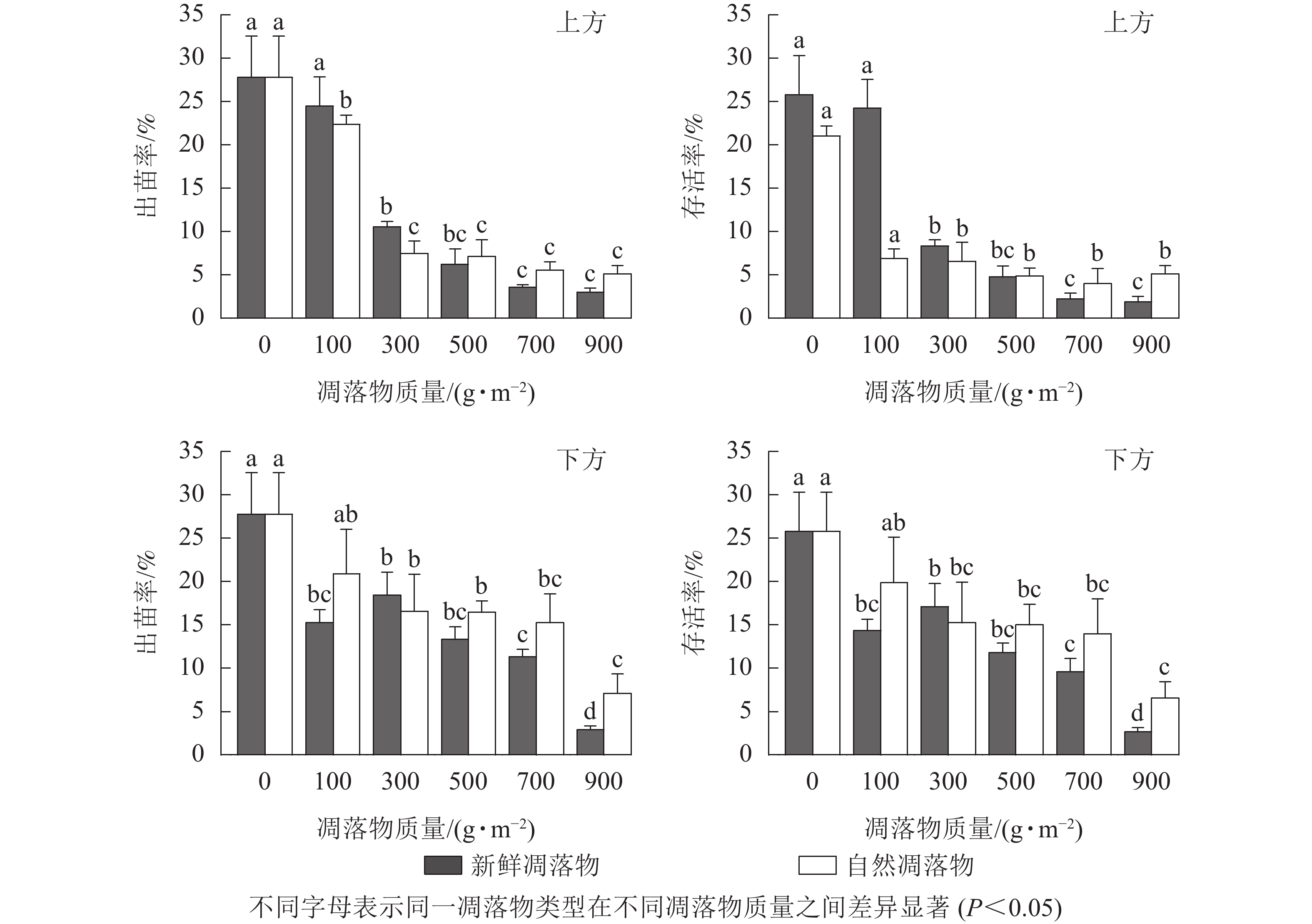
由表1可知:水杉种子出苗率和幼苗存活率均在不同质量新鲜和自然凋落物的2种覆盖方式间存在极显著差异(P<0.01),对照达最高值。由图1可知:处理为上方时,随着新鲜和自然凋落物质量的增加,出苗率和存活率随之降低;当凋落物质量高于100 g·m−2时,出苗率和存活率都显著小于对照 (P<0.05)。处理为下方时,不同凋落物类型则表现出一定差异:新鲜凋落物处理后随着凋落物质量增加,出苗率和存活率呈先上升后下降的变化趋势,且各处理均显著低于对照(P<0.05),在凋落物质量为300 g·m−2时达到第2个峰值;自然凋落物处理后,凋落物质量越大,出苗率和存活率越低,且凋落物质量为300~900 g·m−2时显著低于对照 (P<0.05)。
表 1 凋落物类型、质量、覆盖方式对水杉幼苗早期生长的单因素方差分析
Table 1. One-way ANOVA of of litter type, mass and mulching method on early growth of M. glyptostroboides seedlings
影响因子 出苗率 存活率 苗高 地径 根长 叶片数 叶面积 地上生物量 地下生物量 上方新鲜凋落物质量 0.000** 0.000** 0.003** 0.002** 0.002** 0.031* 0.004** 0.012* 0.001** 上方自然凋落物质量 0.000** 0.000** 0.517 0.280 0.001** 0.086 0.007** 0.005** 0.000** 下方新鲜凋落物质量 0.000** 0.000** 0.001** 0.020* 0.017* 0.019* 0.504 0.008** 0.002** 下方自然凋落物质量 0.004** 0.009** 0.005** 0.002** 0.017* 0.069 0.199 0.019* 0.000** 说明:数据为检验性P值。*表示差异显著(P<0.05),**表示差异极显著(P<0.01) 
图 1 凋落物类型、质量、覆盖方式对水杉种子出苗率和幼苗存活率的影响
Figure 1. Effect of litter type, mass and mulching method on seed emergence rate and survival rate of M. glyptostroboides seedling
多因素方差分析结果(表2)显示:只有凋落物覆盖方式与凋落物质量的交互作用对水杉种子出苗率和幼苗存活率有极显著影响(P<0.01)。当凋落物质量高于100 g·m−2时,水杉种子出苗率和幼苗存活率均表现为下方处理高于上方处理。2种凋落物覆盖方式均在凋落物质量为500~900 g·m−2呈现出:新鲜凋落物处理比自然凋落物处理的种子出苗率和幼苗存活率低。总的来说,凋落物的存在降低了水杉种子出苗率和幼苗存活率,尤其是当凋落物质量大于100 g·m−2时,明显阻碍幼苗出土和存活。
表 2 凋落物类型、质量、覆盖方式对水杉幼苗早期生长的多因素方差分析
Table 2. Multivariate analysis of variance of litter type, mass and mulching method on early growth of M. glyptostroboides seedlings
因子间交互作用 出苗率 存活率 苗高 地径 根长 叶片数 叶面积 地上生物量 地下生物量 凋落物质量×覆盖方式 0.000** 0.000** 0.528 0.233 0.158 0.965 0.676 0.812 0.995 凋落物质量×凋落物类型 0.140 0.258 0.090 0.069 0.367 0.224 0.275 0.265 0.955 凋落物类型×覆盖方式 0.052 0.101 0.441 0.985 0.002** 0.017* 0.049* 0.001** 0.008** 凋落物质量×覆盖方式×凋落物类型 0.652 0.423 0.281 0.507 0.260 0.143 0.396 0.035* 0.023* 说明:数据为检验性P值。*表示差异显著(P<0.05),**表示差异极显著(P<0.01) -
由表1可知:水杉幼苗苗高、地径、根长在不同质量新鲜和自然凋落物的2种覆盖方式间呈现出一定差异。在上方处理后,不同质量自然凋落物对水杉幼苗根长有极显著影响(P<0.01),对幼苗苗高和地径无显著影响(P>0.05),而不同质量新鲜凋落物对水杉幼苗苗高、地径和根长有极显著影响(P<0.01);在下方处理后,不同质量新鲜凋落物对水杉幼苗苗高有极显著影响(P<0.01),对地径和根长有显著影响(P<0.05),而不同质量自然凋落物对水杉幼苗苗高和地径有极显著影响(P<0.01),对根长有显著影响(P<0.05)。由图2可知:上方处理时,水杉幼苗苗高随着不同质量新鲜和自然凋落物增加呈先上升后下降的趋势,且均在凋落物质量为300 g·m−2时达峰值,但300 g·m−2处理与对照差异不显著(P>0.05)。下方处理时,新鲜和自然凋落物处理后的水杉幼苗苗高均在凋落物质量为300 g·m−2时达最高值,比对照分别增加了6.69%、15.25%;当凋落物质量超过100 g·m−2时,凋落物质量越大,幼苗苗高越小。在上方处理时,随新鲜凋落物质量的增加,水杉幼苗地径先在凋落物质量为100~300 g·m−2时逐渐上升,随后在凋落物质量为500~900 g·m−2时逐渐下降;当自然凋落物质量大于100 g·m−2时,水杉幼苗地径随凋落物质量增加而逐渐下降。在下方处理时,不同质量新鲜和自然凋落物对水杉幼苗地径生长表现出相同的变化规律,同时,当凋落物质量超过500 g·m−2时,地径显著低于对照(P<0.05)。不同质量新鲜和自然凋落物处理后的水杉幼苗根长与苗高和地径变化规律有一定差异,在下方处理时,幼苗根长均在对照达到最大值(14.11 mm),且随着新鲜和自然凋落物质量的增加而降低;在上方处理时,不同质量新鲜凋落物处理后,幼苗根长在凋落物质量为100 g·m−2时达最高值,比对照高了7.51%,但在凋落物质量为700、900 g·m−2时显著小于对照(P<0.05);自然凋落物处理后,幼苗根长均显著小于对照(P<0.05),且凋落物质量越高,幼苗根长越短。
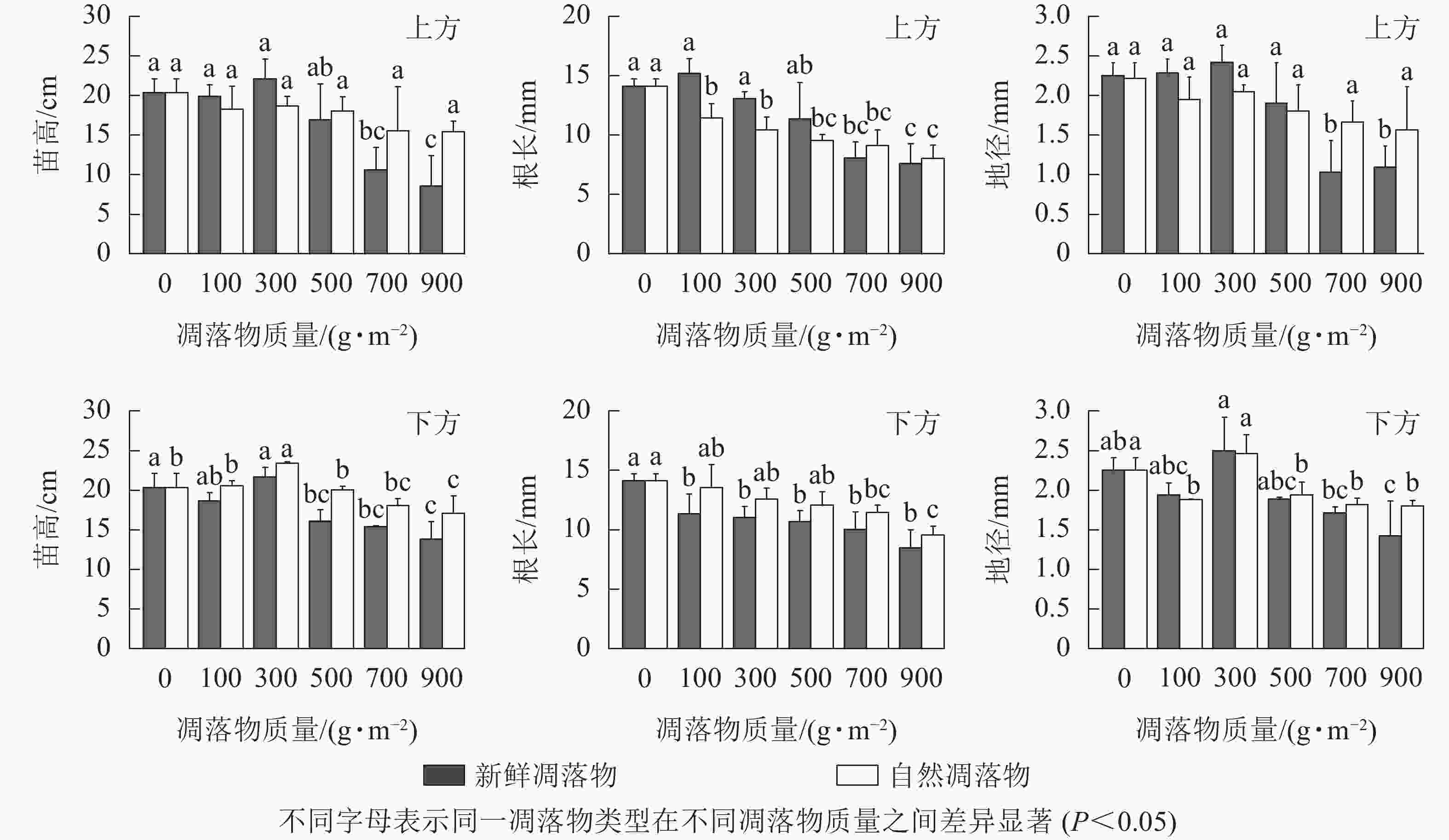
图 2 凋落物类型、质量、覆盖方式对水杉幼苗苗高、地径和根长的影响
Figure 2. Effect of litter type, mass and mulching method on seedling height, base diameter and root length of M. glyptostroboides seedlings
多因素分析结果(表2)显示:凋落物类型、凋落物质量和覆盖方式对幼苗苗高和地径的交互作用均不显著(P>0.05)。同一凋落物质量下,水杉幼苗苗高和地径呈现相似规律,即上方处理<下方处理;在凋落物质量为500~900 g·m−2时,水杉幼苗苗高和地径为自然凋落物处理>新鲜凋落物处理。只有凋落物覆盖方式和凋落物类型对幼苗根长有极显著交互作用(P<0.01)。当凋落物质量为300~900 g·m−2时,各处理的幼苗根长均小于对照,且上方处理小于下方处理;除新鲜和自然凋落物质量为100、300 g·m−2外,其余处理的幼苗根长表现为新鲜凋落物小于自然凋落物。综合来看,凋落物质量为300 g·m−2时促进幼苗苗高和地径生长,但未达显著水平(P>0.05);凋落物质量高于300 g·m−2时,明显抑制幼苗生长。同时,凋落物质量越大,幼苗根长越短。
-
由表1可知:在上方处理时,不同质量新鲜凋落物对水杉幼苗叶片数有显著影响(P<0.05),对幼苗叶面积有极显著影响(P<0.01),不同质量自然凋落物对水杉幼苗叶片数无显著影响(P>0.05),但对幼苗叶面积影响极显著(P<0.01);在下方处理时,不同质量新鲜凋落物对水杉幼苗叶片数有显著影响(P<0.05),但对叶面积无显著影响(P>0.05),不同质量自然凋落物对水杉幼苗叶片数和叶面积均无显著影响(P>0.05)。由图3可知:在上方处理时,自然凋落物质量越高,幼苗叶片数越少,所有处理显著小于对照(P<0.05);不同质量新鲜凋落物处理后,幼苗叶片数在凋落物质量为300 g·m−2时最高,但与对照差异不显著(P>0.05),对照的幼苗叶片数显著比凋落物质量为700、900 g·m−2处理的增加了31.42%、56.73%(P<0.05)。在下方处理时,随着新鲜和自然凋落物质量增加,幼苗叶片数逐渐减少,且幼苗叶片数在凋落物质量为900 g·m−2时比对照显著减少了29.67%、22.50%(P<0.05)。
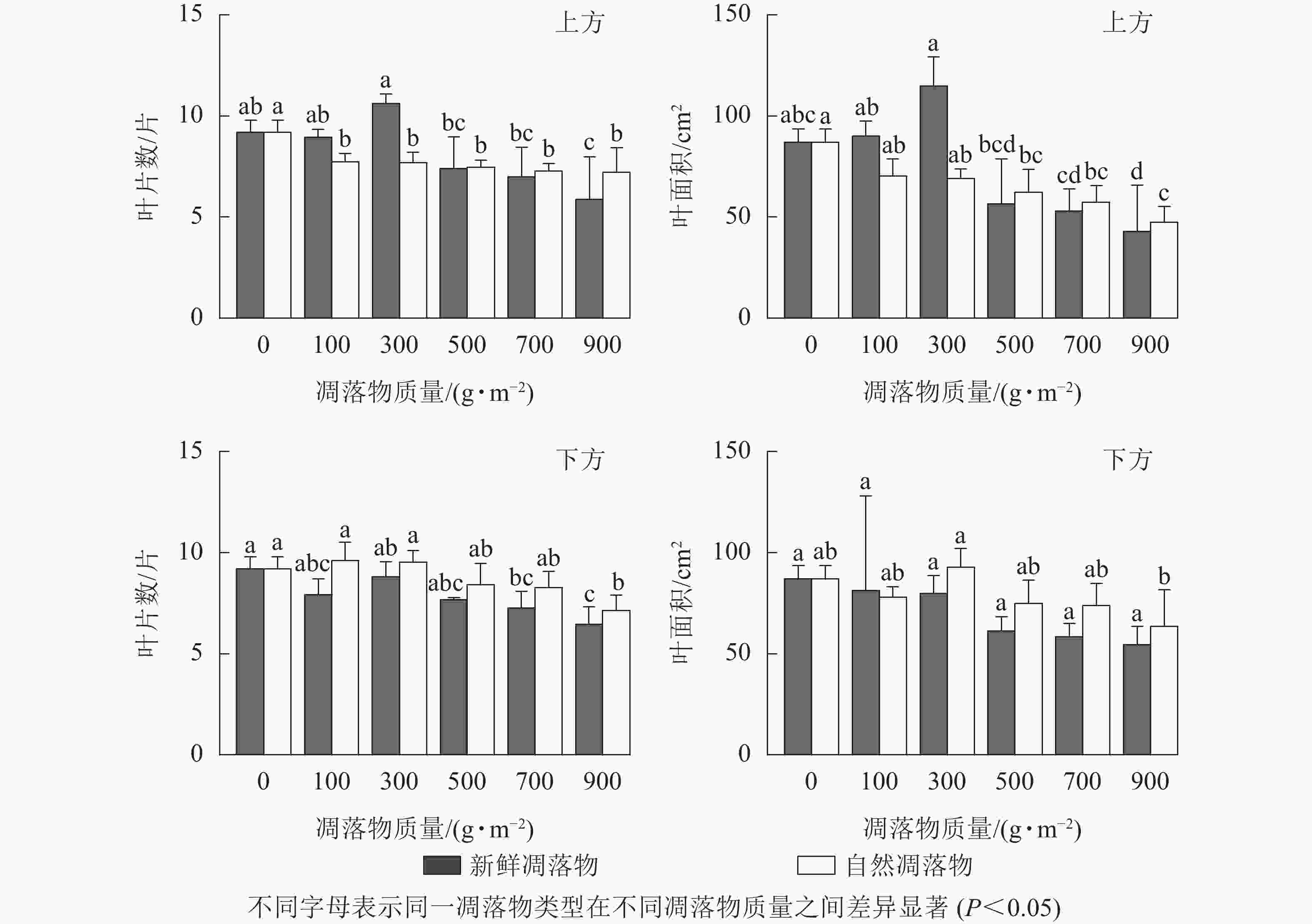
图 3 凋落物类型、质量、覆盖方式对水杉幼苗叶片数和叶面积的影响
Figure 3. Effect of litter type, mass and mulching method on leaf number and leaf area of M. glyptostroboides seedlings
在上方处理时,经新鲜凋落物处理后,幼苗叶面积在凋落物质量为300 g·m−2时达最高,比对照处理增加了3.30%;当凋落物质量高于300 g·m−2时,各处理幼苗叶面积均小于对照,且凋落物质量越大,幼苗叶面积越小;而不同质量自然凋落物处理后,幼苗叶面积随凋落物质量增加而逐渐减小,且对照处理显著比凋落物质量为900 g·m−2时高了83.37%(P<0.0.5)。在下方处理时,新鲜凋落物质量越大,幼苗叶面积越小,但均与对照差异不显著(P>0.05);随着自然凋落物质量的增加,幼苗叶面积表现为增加—下降—增加—再逐渐下降的变化。
只有凋落物覆盖方式和凋落物类型在水杉幼苗叶片数和叶面积上存在显著交互作用(表2,P<0.05)。同一凋落物质量下(>300 g·m−2),水杉幼苗叶片数和叶面积均小于对照,且新鲜凋落物处理小于自然凋落物处理,上方处理小于下方处理。总之,与对照相比,水杉幼苗叶片数和叶面积在“上方+新鲜凋落物+100、300 g·m−2”处理和“下方+自然凋落物+100、300 g·m−2”处理时不显著增加(P>0.05),其余处理均抑制了幼苗叶片数和叶面积。当凋落物质量高于300 g·m−2时,水杉幼苗叶片数和叶面积随凋落物质量的增加而减少。
-
由表1可知:2种凋落物覆盖方式下,不同质量新鲜和自然凋落物对水杉幼苗地上生物量有显著影响(P<0.05),而对幼苗地下生物量表现为极显著影响(P<0.01)。由图4可知:在上方处理时,幼苗地上生物量随着新鲜凋落物质量增加表现为在100、300 g·m−2时先上升,高于300 g·m−2后逐渐下降,且凋落物质量为300 g·m−2时,幼苗地上生物量比对照高了24.75%(P>0.05);经不同质量自然凋落物处理后,幼苗地上生物量均显著低于对照(P<0.05),且随凋落物质量增加而减少。在下方处理时,新鲜凋落物处理后,幼苗地上生物量均小于对照,且在凋落物质量高于300 g·m−2时达到显著水平;不同质量自然凋落物处理后,幼苗地上生物量的变化规律与上方处理时的新鲜凋落物相同。
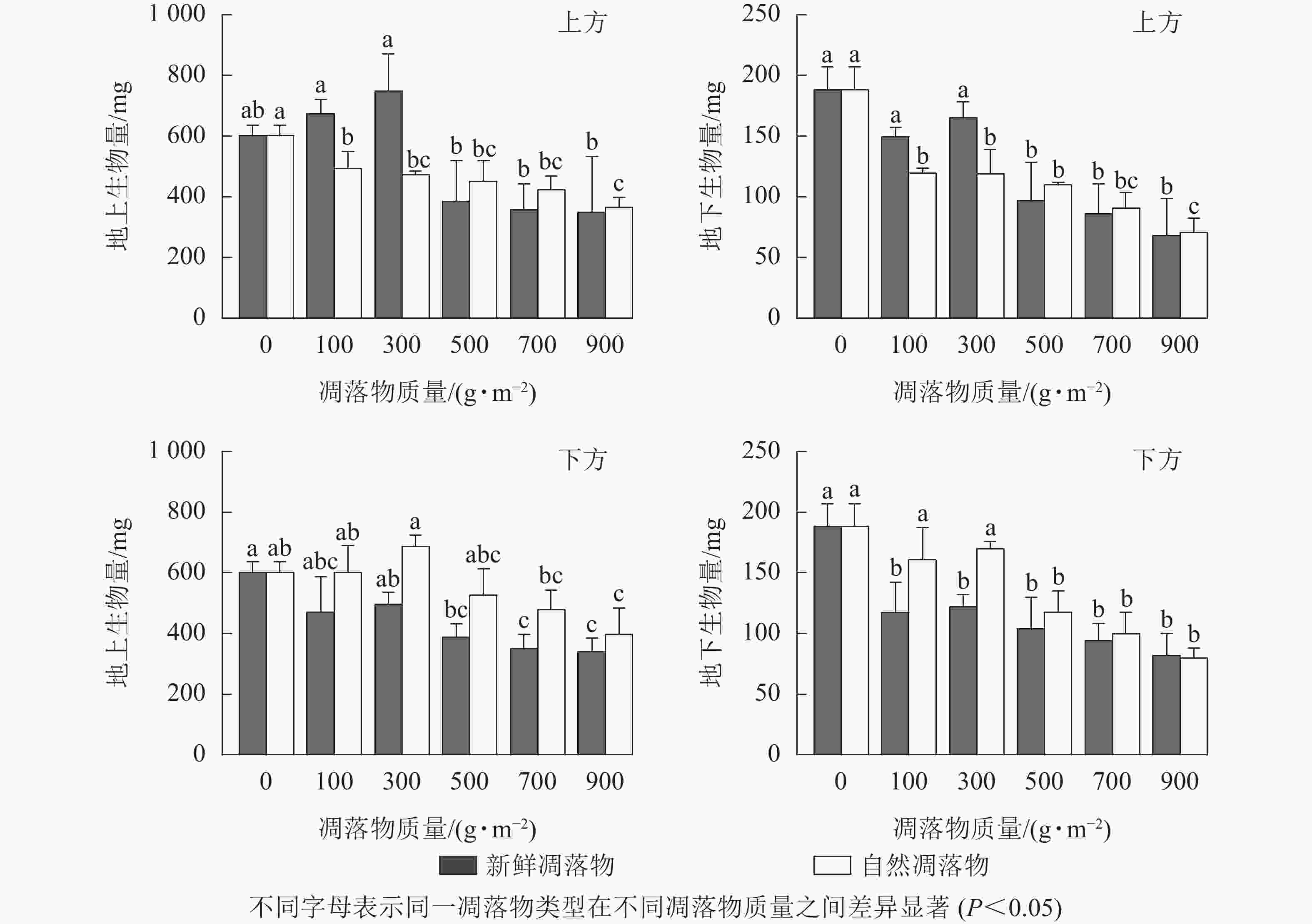
图 4 凋落物类型、质量、覆盖方式对水杉幼苗地上和地下生物量的影响
Figure 4. Effect of litter type, mass and mulching method on aboveground biomass and belowground biomass of M. glyptostroboides seedlings
在上方处理时,不同质量新鲜凋落物处理后的幼苗地下生物量均小于对照,且对照处理的幼苗地下生物量是凋落物质量为500、700、900 g·m−2时的1.94、2.19、2.76倍;与对照相比,自然凋落物均显著抑制幼苗地下生物量累积(P<0.05),且凋落物质量越大,地下生物量越低。在下方处理时,新鲜和自然凋落物不同程度地抑制幼苗地下生物量,当凋落物质量高于300 g·m−2时抑制作用达到显著水平(P<0.05)。
如表2所示:不同凋落物覆盖方式和凋落物类型对水杉幼苗地上和地下生物量有极显著的交互作用(P<0.01),凋落物质量、覆盖方式和类型对幼苗地上和地下生物量有显著的交互作用(P<0.05)。同一凋落物质量下,除凋落物质量为100、300 g·m−2外,幼苗地上生物量和地下生物量均表现为上方处理小于下方处理,新鲜凋落物处理小于自然凋落物处理。总之,当凋落物质量高于300 g·m−2时,凋落物对水杉幼苗地上和地下生物量均起显著的抑制作用(P<0.05)。
-
种子萌发和幼苗生长是植物天然更新中最脆弱、最敏感和最关键的阶段,凋落物对其有重要影响。不同质量水杉母树凋落物均降低了水杉种子出苗率和幼苗存活率,当凋落物质量高于100 g·m−2时阻碍作用达显著水平(P<0.05)。除种子上层覆盖300 g·m−2新鲜凋落物稍有波动外,其余处理的水杉种子出苗率和幼苗存活率均随着凋落物质量增加而逐渐降低,这与李根柱等[19]、RUPRECHT等[20]的研究结果一致。凋落物的存在会降低气温日较差,减少水分,且随着凋落物质量的增加,种子发生霉变和虫蛀等概率也逐渐增大。同时,凋落物的消光作用使幼苗的光合作用无法与呼吸作用的需求相匹配[21],从而对幼苗生长造成一定的损伤。本研究结果中水杉凋落物阻碍了水杉幼苗的出土和存活,故建议在种子萌发阶段适当清除林下地表凋落物,为种子接触土壤创造条件,以促进种子出苗率。
植物幼苗形态生长具有一定的可塑性,可以根据环境变化而改变自身生长,凋落物对其起到关键作用。随凋落物质量的增加,水杉幼苗苗高、地径、叶片数、叶面积和地上生物量表现为先上升后下降。这与赵冲等[22]对杉木Cunninghamia lanceolata幼苗生长的研究结果一致,也与杉木幼苗生物量随着凋落物厚度的增加呈先增加后减少的规律相同[4]。浅层凋落物对幼苗生长可能表现无影响甚至会有促进现象,但随着凋落物、物种以及微生境不同而存在差异[20, 23]。适量凋落物铺垫或覆盖激活植物体内产生抗逆蛋白[8],故分配更多能量来促进幼苗建成[24],同时适量凋落物覆盖也能减少土壤水分及温度的急剧变化,为幼苗快速生长提供良好的微环境[25],因此凋落物质量为300 g·m−2时,凋落物对水杉幼苗生长起到促进作用(P>0.05)。所以,在幼苗生长阶段,建议避免过多干扰而伤害幼苗,可以保留少量凋落物促进幼苗快速生长。然而,大量凋落物可能超过植物自身的调节阈值,导致凋落物质量超过300 g·m−2时,水杉幼苗生长明显受阻。此外,凋落物质量越大,幼苗根长越短。这与徐来仙等[8]的研究结论一致,凋落物的存在使植物能量物质分配时选择以减少根长来促进苗高[26]。
本研究表明:同一凋落物质量(>300 g·m−2)下,自然和新鲜凋落物类型处理后的水杉幼苗各指标均小于对照,其中自然凋落物类型在水杉种子出苗率、存活率、苗高、地径、根长、叶片数、叶面积、地上和地下生物量均高于新鲜凋落物类型,进一步证实了新鲜水杉母树凋落物对水杉种子萌发和生长的抑制作用大于自然凋落物[8]。可能因为不同分解阶段的2种水杉凋落物类型拥有不同的化感物质,其中水杉新鲜凋落物中化感自毒物质数量和种类比自然凋落物多,加之自然凋落物包括经过分解的混合物,受到土壤中微生物影响较大[27],导致自然凋落物对水杉种子萌发和生长的抑制小于新鲜凋落物。
同一凋落物质量下(>300 g·m−2),不同凋落物覆盖方式对水杉幼苗出土和早期生长的影响表现为:水杉种子出苗率、存活率、苗高、地径、根长、叶片数、叶面积、地上和地下生物量从大到小依次为对照、下方、上方。这与ELLWORTH等[26]发现上方处理的南蛇藤Celastrus orbiculatus种子出苗率和存活率低于下方的结论相同,也与朱静等[28]发现上方处理对格氏栲Castanopsis kawakamii种子萌发和胚根生长的抑制强于下方处理的结果一致,同样与王大洋等[18]发现杉木种子着生在凋落物表层比种子着生在凋落物下方的杉木幼苗生物量低的结果相似。种子在凋落物下方时,种子与土壤密切接触,有利于种子吸收养分和水分,加之适量凋落物覆盖保持了种子萌发所需的土壤温度和湿度,降低了土壤水分蒸发速度,而上方处理的种子则出现吸水缓慢,甚至接触不到土壤,种子水分蒸发快,从而导致种子出苗和幼苗生长时受到更明显的抑制。相对于上方处理而言,下方处理有利于种子出苗和幼苗快速生长[28-29]。
然而,在凋落物质量为100、300 g·m−2处理时,凋落物类型和覆盖方式的变化规律存在一定波动,可能因为在田间1 m×1 m的样框里,300 g·m−2的凋落物质量太少,导致凋落物覆盖方式对幼苗的影响不突出。此外,造成天然更新困难的原因是多重、复杂的,如何有效促进水杉天然更新还需进一步综合研究。
-
水杉母树凋落物类型、覆盖方式和质量均对水杉幼苗出土和早期生长产生一定的物理阻隔作用。凋落物质量是阻碍水杉幼苗出土和早期生长的主要影响因子,新鲜凋落物阻隔作用大于自然凋落物,且种子下层铺垫凋落物比上层覆盖凋落物更加阻碍幼苗出土和生长。水杉林下大量凋落物所形成的物理阻隔是导致林下幼苗天然更新困难的重要原因之一。建议在种子雨高峰期前,对不同类型的水杉凋落物进行及时清除,保证种子与土壤接触,获得较高的种子出苗率;同时,在幼苗生长阶段清理部分凋落物时避免过多干扰幼苗,为幼苗生长提供适宜环境,促进水杉天然更新。
Effect of litter physical barrier on emergence and early growth of Metasequoia glyptostroboides seedlings
-
摘要:
目的 探讨水杉Metasequoia glyptostroboides母树凋落物物理阻隔对水杉天然更新的影响,为解除水杉天然更新障碍及保护水杉种群提供科学依据。 方法 通过野外模拟试验,对不同类型凋落物(新鲜凋落物和自然凋落物)采用0(对照)、100、300、500、700、900 g·m−2的质量梯度,分别在种子下层和上层覆盖凋落物来探究凋落物对水杉幼苗出土及早期生长的影响。 结果 ①凋落物对水杉种子出苗率和幼苗存活率产生抑制作用,在凋落物质量为300~900 g·m−2时抑制作用显著增强(P<0.05)。②除在种子下层铺垫自然凋落物外,其余处理在凋落物质量为300 g·m−2时促进水杉幼苗苗高和地径生长,但与对照差异不显著(P>0.05);当凋落物质量高于300 g·m−2时,全部处理均抑制幼苗生长。随着凋落物质量的增加,对水杉幼苗根长的抑制作用逐渐增强。③随凋落物质量增加,水杉幼苗地上生物量和地下生物量呈先上升后下降的变化趋势,只有在种子下层铺垫300 g·m−2的自然凋落物处理后有一定波动,其余各处理均抑制幼苗地下生物量累积;当凋落物质量达500 g·m−2以上时,凋落物显著阻碍幼苗地上和地下生物量的累积(P<0.05)。④同一凋落物质量下(>300 g·m−2),新鲜凋落物对水杉幼苗出土和早期生长的抑制作用大于自然凋落物,种子下层铺垫凋落物比种子上层覆盖凋落物的抑制作用更强。 结论 水杉母树凋落物对水杉幼苗出土和早期生长具有明显的物理阻隔作用,进而影响水杉更新生长。因此,建议在种子雨高峰期前,对水杉林下不同类型的凋落物进行及时清理,以促进水杉天然更新。图4表2参29 Abstract:Objective This study aims to explore the effect of physical barrier of litter from Metasequoia glyptostroboides mother tree on its natural regeneration, so as to provide scientific basis for removing obstacles of M. glyptostroboides natural regeneration and protecting its population. Method Through field simulation experiments, different types of litter (fresh litter and natural litter) with different mass gradients (0, 100, 300, 500, 700 and 900 g·m−2) were used to investigate the effect of litter on emergence and early growth of M. glyptostroboides seedlings by spreading litter on the lower layer of seeds and covering litter on the upper layer of seeds. Result (1) Litter inhibited the seed emergence rate and seedling survival rate of M. glyptostroboides, and the inhibitory effect was significantly enhanced when the litter mass was 300−900 g·m−2 (P<0.05). (2) Except for spreading natural litter on the lower layer of seeds, the other treatments promoted the growth of seedling height and ground diameter M. glyptostroboides seedlings when the litter mass was 300 g·m−2 (P>0.05), but the difference with the control was not significant. When the litter mass was higher than 300 g·m−2, all treatments inhibited seedling growth. With the increase of litter mass, the inhibitory effect on the root length of M. glyptostroboides seedlings enhanced gradually. (3) With the increase of litter mass, the aboveground biomass and underground biomass of M. glyptostroboides seedlings first increased and then decreased. There was a certain fluctuation only after 300 g·m−2 natural litter treatment on the low layer of seeds, and the other treatments inhibited the underground biomass accumulation of seedlings. The accumulation of aboveground and underground biomass of seedlings was significantly hindered when the litter mass was above 500 g·m−2 (P<0.05). (4) Under the same litter mass (>300 g·m−2), the inhibitory effect of fresh litter on the emergence and early growth of M. glyptostroboides seedling was greater than that of natural litter, and the inhibitory effect of litter on the lower layer of seeds was stronger than that on the upper layer of seeds. Conclusion The litter of M. glyptostroboides mother tree has an obvious physical barrier effect on the emergence and early growth of M. glyptostroboides seedlings, which affects the natural regeneration of M. glyptostroboides. Therefore, it is suggested to treat the litter of different types under M. glyptostroboides forests in time before the peak of seed rain, so as to promote the natural regeneration of M. glyptostroboides. [Ch, 4 fig. 2 tab. 29 ref.] -
Key words:
- natural regeneration /
- Metasequoia glyptostroboides /
- physical barrier /
- biomass /
- litter /
- seedling growth
-
表 1 凋落物类型、质量、覆盖方式对水杉幼苗早期生长的单因素方差分析
Table 1. One-way ANOVA of of litter type, mass and mulching method on early growth of M. glyptostroboides seedlings
影响因子 出苗率 存活率 苗高 地径 根长 叶片数 叶面积 地上生物量 地下生物量 上方新鲜凋落物质量 0.000** 0.000** 0.003** 0.002** 0.002** 0.031* 0.004** 0.012* 0.001** 上方自然凋落物质量 0.000** 0.000** 0.517 0.280 0.001** 0.086 0.007** 0.005** 0.000** 下方新鲜凋落物质量 0.000** 0.000** 0.001** 0.020* 0.017* 0.019* 0.504 0.008** 0.002** 下方自然凋落物质量 0.004** 0.009** 0.005** 0.002** 0.017* 0.069 0.199 0.019* 0.000** 说明:数据为检验性P值。*表示差异显著(P<0.05),**表示差异极显著(P<0.01) 表 2 凋落物类型、质量、覆盖方式对水杉幼苗早期生长的多因素方差分析
Table 2. Multivariate analysis of variance of litter type, mass and mulching method on early growth of M. glyptostroboides seedlings
因子间交互作用 出苗率 存活率 苗高 地径 根长 叶片数 叶面积 地上生物量 地下生物量 凋落物质量×覆盖方式 0.000** 0.000** 0.528 0.233 0.158 0.965 0.676 0.812 0.995 凋落物质量×凋落物类型 0.140 0.258 0.090 0.069 0.367 0.224 0.275 0.265 0.955 凋落物类型×覆盖方式 0.052 0.101 0.441 0.985 0.002** 0.017* 0.049* 0.001** 0.008** 凋落物质量×覆盖方式×凋落物类型 0.652 0.423 0.281 0.507 0.260 0.143 0.396 0.035* 0.023* 说明:数据为检验性P值。*表示差异显著(P<0.05),**表示差异极显著(P<0.01) -
[1] 吴承祯, 洪伟, 姜志林, 等. 我国森林凋落物研究进展[J]. 江西农业大学学报, 2000, 22(3): 405 − 410. WU Chengzhen, HONG Wei, JIANG Zhilin, et al. Advances in research of forest litter-fall in China [J]. Acta Agric Univ Jiangxi, 2000, 22(3): 405 − 410. [2] 胡飞, 孔垂华. 胜红蓟化感作用研究(Ⅰ)水溶物的化感作用及其化感物质分离鉴定[J]. 应用生态学报, 1997, 8(3): 304 − 308. HU Fei, KONG Chuihua. Allelopathy of Ageratum conyzoides (Ⅰ) aqueous extract and isolation and identification of its allelochemicals [J]. Chin J Appl Ecol, 1997, 8(3): 304 − 308. [3] YUAN Jianli, LIANG Defei, ZHANG Shiting. Litter and its interaction with standing vegetation affectseedling recruitment in Tibetan alpine grasslands[J/OL]. Plant Ecol Diversity, 2015 [2021-10-08]. doi: 10.1080/17550874.2015.1073400. [4] 赵冲, 王正宁, 蔡一冰, 等. 凋落物类型及覆盖厚度对杉木幼苗出土与早期生长的影响[J]. 福建农林大学学报(自然科学版), 2019, 48(3): 350 − 358. ZHAO Chong, WANG Zhengning, CAI Yibing, et al. Effects of litter type and amount on seedling emergence and early growth of Chinese fir [J]. J Fujian Agric For Univ Nat Sci Ed, 2019, 48(3): 350 − 358. [5] ASPLUND J, HUSTOFT E, NYBAKKEN L, et al. Litter impair spruce seedling emergence in beech forests: a litter manipulation experiment[J/OL]. Scand J For Res, 2017 [2021-10-10]. doi: 10.1080/02827581.2017.1388440. [6] 王贺新, 李根柱, 于冬梅, 等. 枯枝落叶层对森林天然更新的障碍[J]. 生态学杂志, 2008, 27(1): 83 − 88. WANG Hexin, LI Genzhu, YU Dongmei, et al. Barrier effect of litter layer on natural regeneration of forests: a review [J]. Chin J Ecol, 2008, 27(1): 83 − 88. [7] KOOREM K, PRICE J N, MOORA M. Species-specific effects of woody litter on seedling emergence and growth of Herbaceous plants[J/OL]. PLoS One, 2011, 6(10): e26505[2021-10-18]. doi: 10.1371/journal.pone.0026505. [8] 徐来仙, 姚兰, 周大寨, 等. 水杉凋落物水浸提液对其种子萌发和生长的化感作用[J/OL]. 广西植物, 2021 [2022-04-30]. doi: 10.11931/guihaia.gxzw202104032. XU Laixian, YAO Lan, ZHOU Dazhai, et al. Allelopathy of aqueous extract from Metasequoia glyptostroboides litter on its seed germination and growth[J/OL]. Guihaia, 2021 [2022-04-30]. doi: 10.11931/guihaia.gxzw202104032. [9] LI Yuanyuan, TSANG E P K, CUI Minyan, et al. Too early to call it success: an evaluation of the natural regeneration of the endangered Metasequoia glyptostroboides [J]. Biol Conserv, 2012, 150(1): 1 − 4. [10] 林勇, 艾训儒, 姚兰, 等. 水杉原生母树种群结构与动态[J]. 生态学杂志, 2017, 36(6): 1531 − 1538. LIN Yong, AI Xunru, YAO Lan, et al. Population structure and dynamics of Metasequoia glyptostroboides parent trees [J]. Chin J Ecol, 2017, 36(6): 1531 − 1538. [11] 潘开文, 何静, 吴宁. 森林凋落物对林地微生境的影响[J]. 应用生态学报, 2004, 15(1): 153 − 158. PAN Kaiwen, HE Jing, WU Ning. Effect of forest litter on microenvironment conditions of forestland [J]. Chin J Appl Ecol, 2004, 15(1): 153 − 158. [12] WIEGAND T, MARTĺNEZ I, HUTH A. Recruitment in tropical tree species: revealing complex spatial patterns [J]. Am Nat, 2009, 174(4): 106 − 140. [13] D’AMATO A W, ORWIG D A, FOSTER D R. Understory vegetation in old-growth and second-growth Tsuga canadensis forests in western Massachusetts [J]. For Ecol Manage, 2009, 57(3): 1043 − 1052. [14] 吴漫玲, 姚兰, 艾训儒, 等. 水杉原生种群核心种质资源的繁殖特性[J]. 生物多样性, 2020, 28(3): 303 − 313. WU Manling, YAO Lan, AI Xunru, et al. The reproductive characteristics of core germplasm in a native Metasequoia glyptostroboides population [J]. Biodiversity Sci, 2020, 28(3): 303 − 313. [15] 刘小红. 水杉长链非编码RNA分析[J]. 分子植物育种, 2020, 18(3): 853 − 857. LIU Xiaohong. Analysis on long non-coding RNAs in Metasequoia glyptostroboides [J]. Mol Plant Breed, 2020, 18(3): 853 − 857. [16] 吴漫玲. 水杉原生种群天然更新种子繁殖障碍与调控研究[D]. 恩施: 湖北民族大学, 2020. WU Manling. The Study on Seed Propagation Obstacles and Regulation of Natural Regeneration for Metasequoia glyptostroboides [D]. Enshi: Hubei Minzu University, 2020. [17] ECKSTEIN R L, DONATH T W. Interactions between litter and water availability affect seedling emergence in four familial pairs of floodplain species [J]. J Ecol, 2005, 93(4): 807 − 816. [18] 王大洋, 刘青青, 陈艳芳, 等. 种子所处凋落物位置对杉木幼苗出土和早期生长的影响[J]. 福建农林大学学报(自然科学版), 2010, 49(6): 782 − 788. WANG Dayang, LIU Qingqing, CHEN Yanfang, et al. Effects of seeds and litter position on seedling emergence and early growth of Chinese fir [J]. J Fujian Agric For Univ Nat Sci Ed, 2010, 49(6): 782 − 788. [19] 李根柱, 王贺新, 朱书全, 等. 东北次生林区枯落物对天然更新的障碍作用[J]. 辽宁工程技术大学学报(自然科学版), 2008, 27(2): 295 − 298. LI Genzhu, WANG Hexin, ZHU Shuquan, et al. Barrier effect of litter on natural regeneration in northeast secondary forest [J]. J Liaoning Tech Univ Nat Sci, 2008, 27(2): 295 − 298. [20] RUPRECHT E, JÓZSA J, ÖLVEDI T B, et al. Differential effects of several “litter” types on the germination of dry grassland species [J]. J Veg Sci, 2010, 21(6): 1069 − 1081. [21] DONATH T W, EEKSTEIN R L. Grass and oak litter exert different effects on seedling emergence of herbaceous perennials from grasslands and woodlands [J]. J Ecol, 2008, 96(2): 272 − 280. [22] 赵冲, 蔡一冰, 黄晓, 等. 杉木凋落物覆盖对自身幼苗出土和早期生长的影响[J]. 应用生态学报, 2019, 30(2): 481 − 488. ZHAO Chong, CAI Yibing, HUANG Xiao, et al. Effects of Chinese fir litter cover on its seedling emergence and early growth [J]. Chin J Appl Ecol, 2019, 30(2): 481 − 488. [23] 郭晓燕, 张露, 梁跃龙, 等. 枯枝落叶物厚度影响毛红椿种子出苗的模拟研究[J]. 江西农业大学学报, 2014, 36(2): 332 − 337. GUO Xiaoyan, ZHANG Lu, LIANG Yuelong, et al. Simulation study on the effects of litter layer thickness on seedling emergence of Toona ciliata var. pubescens [J]. Acta Agric Univ Jiangxi, 2014, 36(2): 332 − 337. [24] 郑文辉, 林开敏, 徐昪, 等. 7 种不同树种凋落叶持水性能的比较研究[J]. 水土保持学报, 2014, 28(1): 88 − 91. ZHENG Wenhui, LIN Kaimin, XU Bian, et al. Comparative study of water-holding capacity of litter in seven different trees’ species [J]. J Soil Water Conserv, 2014, 28(1): 88 − 91. [25] CHEN Baoming, D’ANTONIO C M, MOLINARI N, et al. Mechanisms of influence of invasive grass litter on germination and growth of coexisting species in Califonia [J]. Biol Invasions, 2018, 20(7): 1881 − 1897. [26] ELLWORTH J W, HARRINGTON R A, FOWNES J H. Seedling emergence, growth, and allocation of oriental bittersweet: effects of seed input, seed bank, and forest floor litter [J]. For Ecol Manage, 2004, 190(2): 255 − 264. [27] ARANITI F, GULLÌ T, MARRELLI M, et al. Artemisia arborescens L. leaf litter: phytotoxic activity and phytochemical characterization[J/OL]. Acta Physiol Plant, 2016, 38(5): 128[2021-10-13]. doi: 10.1007/s11738-016-2141-7. [28] 朱静, 刘金福, 何中声, 等. 凋落物物理阻隔对格氏栲种子萌发及胚根生长的影响[J]. 生态学报, 2020, 40(16): 5630 − 5637. ZHU Jing, LIU Jinfu, HE Zhongsheng, et al. Effects of physical barrier of litter on the seed germination and radicle growth of Castanopsis kawakamii [J]. Acta Ecol Sin, 2020, 40(16): 5630 − 5637. [29] LI Yuan, NIU Wenquan, CAO Xiaoshu, et al. Effect of soil aeration on root morphology and photosynthetic characteristics of potted tomato plants (Solanum lycopersicum) at different NaCl salinity levels[J/OL]. BMC Plant Biol, 2019, 19(1): 331[2021-10-18]. doi: 10.1186/s12870-019-1927-3. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20210704






 下载:
下载: