-
物种多样性的形成和维持机制是生物多样性保护的基础,长期以来,生态学家针对植物物种多样性形成和维持的潜在机制先后提出了地质历史过程、水热动态假说、能量假说、寒冷忍耐假说及生境异质性假说等数十项假说[1]。森林群落的物种分布受多种因素影响,主要包括非生物环境因子、群落类型和空间距离等[2],而林下物种又是人工林森林生态系统的重要组成部分,深入揭示环境因素对林下物种分布的影响,是解读人工林森林生态系统物种多样性的形成和维持的有效途径之一。油松Pinus tabuliformis林是华北地区地带性植被,也是华北地区顶级群落松栎针阔混交林的重要组成部分。但由于人为活动干扰,该区域油松林以人工林为主,相比天然林,人工林存在病虫害严重,生物多样性、生产力、天然更新和生态稳定性下降等问题,森林生态系统健康面临挑战,系统原有的组成和结构被破坏,进而影响到生态过程和生态系统功能[3-4]。所以,开展环境因子对油松人工林下物种分布影响的研究,对于区域人工林生物多样性保护和经营管理具有重要的意义。大量研究[5]表明:地形、海拔、土壤、光照、植被类型等均对林下物种分布产生影响。对太岳山[6]与关帝山[7]油松林下物种分布研究表明:油松林下物种分布主要受非生物因子影响,受生物因子影响较小,且受地形因子的影响大于林分因子和土壤因子。以上2个研究地气候类型为暖温带半干旱气候区,而中条山处于暖温带半湿润气候区[8],不同的气候和土壤条件势必会影响研究结果,对油松人工林经营管理带来不确定性。基于此,本研究以山西中条山油松人工林为研究对象,基于植物和土壤调查数据,分析环境因子对影响油松人工林下物种分布的影响,为该地区油松人工林生物多样性保护和经营管理提供数据支撑。
-
中条山位于山西省南部,是中国黄土高原向华北平原过渡的东南边缘区,在气候区划上属暖温带半湿润季风气候区。油松人工林分布区土壤为山地褐土及淋溶褐土,植被区划上属暖温带落叶阔叶林地带,森林植被垂直分布明显[9]。林下物种主要有连翘Forsythia suspensa、土庄绣线菊Spiraea pubescens、披针薹草Carex lancifolia、早开堇菜Viola prionantha、茜草Rubia cordifolia和金线草R. membranace等。
-
2018年6—8月,在对中条山油松人工林进行全面踏查的基础上,根据海拔、林龄、密度、坡度、坡向、混交等选择具有代表性的12个油松人工林样地(表1),每个样地3个重复,共计36个乔木样方。除2号样地受条件限制,乔木样方面积为15 m×15 m,其他各样方面积为20 m×20 m,记录样方内出现的全部乔木种,并测定胸径≥5 cm乔木树种的名称、胸径、树高。将2号样地划分为9个、其他样地划分为16个5 m×5 m的灌木样方,并于每个灌木样方中心设置1个1 m×1 m的草本样方,灌木、草本样方数量合计均为555个,分别记录灌木和草本样方内的灌木、草本植物的种类、数量,并记录灌木样方内藤本的种类、数量。共记录178种植物,其中灌木47种,草本112种,藤本19种,分属56科124属,以36个乔木样方的物种多度数据建立物种矩阵(Z47×36、Z112×36、Z19×36)。记录每个样地的经纬度、海拔、坡度、坡向,根据中条山森林二类调查数据获取林龄和间伐时间,采用树冠投影法测定大样方郁闭度。
表 1 样地概况
Table 1. Overview of the sample sites
样地 林龄/a 坡度/(°) 坡向 海拔/m 密度/(株∙ hm−2) 平均胸径/cm 平均树高/m 1 40 22 西南 1 916 808 24.08 14.89 2 46 34 东南 1 924 1511 17.56 9.31 3 28 19 西 1 880 1600 14.77 12.43 4 38 35 西南 1 750 925 18.66 11.20 5 48 21 东 1 722 508 25.64 15.46 6 48 13 东北 1 933 583 27.84 16.31 7 41 20 西南 1 917 500 27.79 14.74 8 36 26 南 1 509 1383 17.39 11.60 9 39 25 西南 1 997 2475 14.79 9.07 10 32 11 东南 1 872 1250 17.39 12.95 11 48 8 西 1 928 467 29.32 15.94 12 46 23 西南 1 960 558 21.76 10.90 -
在每个乔木样地内沿对角线随机选择3个点为土壤样品采集点,在每个采样点挖掘1个土壤剖面,按0~10 、10~20、20~40 cm划分土壤层次。在每个土壤层次上,用100 cm3的环刀取样。采用土壤袋采集各层土样200 g,挑出侵入物质,带回实验室自然风干、研磨、过筛后进行化学分析和测定。
测定土壤质量含水量、最大持水量、毛管持水量、田间持水量、毛管孔隙、非毛管孔隙和总孔隙度等土壤物理性质,测定方法按照LY/T 1215—1999《森林土壤水分-物理性质的测定》[10]进行。pH采用pH酸度计法(HANNA pH 211 )测定;土壤有机质采用重铬酸钾氧化-外加热法测定;全氮采用凯氏定氮法测定;速效氮采用碱解扩散法测定;全磷和速效磷采用等离子发射光谱法(IRIS Intrepid Ⅱ XSP)测定。每个样地土壤理化性质以所有测定值的平均值表征。
-
生物因子数据选取乔木样方林分平均胸径、平均树高、胸高断面积、油松相对优势度、株树密度、林龄、疏密度、郁闭度、乔木公顷蓄积、乔木公顷生物量、乔木平均蓄积、乔木平均生物量,蓄积量采用一元材积表计算[11],生物量采用方精云等[12]生物量/材积转换系数计算。非生物因子数据包括土壤理化性质、坡度、坡向、海拔、间伐间隔。其中坡向为无序分类变量,按方位划分为北、东北、东、东南、南、西南、西、西北,分析时按1~8依次赋值。将以上因子构成环境矩阵(Z36×29)。
-
采用主成分分析(PCA)法对环境数据降维;采用除趋势对应分析(DCA)法去除“弓形效应”;采用典范对应分析(CCA)对物种进行排序。数据整理采用Excel 2016完成;物种多样性分析、作图及环境因子PCA分析均采用R 4.0.3软件中“vegan”程序包完成;DCA和CCA采用Canoco 5软件完成。
-
由于环境因子较多,且因子间存在多重共线性,需降低数据维度。因土壤pH对物种丰富度及空间分布影响较大[13],故将除土壤pH以外的28个环境因子进行主成分分析(表2)。根据因子载荷矩阵,第1主成分主要反映土壤水分;第2主成分主要反映林分密度;第3主成分主要反映土壤养分;第4主成分主要反映土壤通气性;第5主成分主要反映生物量;第6主成分主要反映林冠郁闭度;第7主成分为海拔。将以上7个主成分与土壤pH共同建立生境矩阵(Z36×8)。将土壤水分、养分、通气性、pH、海拔归为非生物环境因子,将林分密度、生物量、林冠郁闭度归为生物环境因子。基于主成分分析结果构建环境矩阵,分析环境因子对林下物种分布的影响。
表 2 环境因子主成分分析因子旋转载荷矩阵
Table 2. Rotated component matrix for principal component analysis of environmental factors
环境因子 主成分 1 2 3 4 5 6 7 土壤毛管持水量 0.93 0.05 0.23 0.18 0.06 −0.04 −0.06 田间持水量 0.93 0.12 0.18 −0.03 0.07 0.14 0.08 土壤毛管孔隙度 0.91 0.13 0.21 −0.19 0.01 −0.01 0.07 土壤总孔隙度 0.87 0.08 0.21 0.37 −0.08 0.05 −0.01 土壤最大持水量 0.81 −0.01 0.20 0.49 0.02 0.00 −0.10 土壤质量含水量 0.80 0.09 0.22 −0.34 0.16 0.00 0.32 株树密度 −0.10 −0.92 0.15 0.03 0.17 0.08 0.10 平均胸径 0.15 0.90 −0.02 −0.23 0.24 0.06 0.02 乔木平均蓄积 0.10 0.88 0.08 −0.19 0.31 −0.02 0.12 疏密度 −0.05 0.80 −0.06 −0.33 0.31 −0.11 0.03 平均树高 0.06 0.73 −0.23 −0.46 0.30 −0.05 −0.05 林龄 0.47 0.61 −0.01 0.34 0.06 0.37 0.14 土壤有机质 0.18 0.02 0.95 0.12 −0.03 −0.13 −0.03 土壤全氮 0.22 −0.11 0.92 0.20 −0.03 −0.16 0.06 土壤速效氮 0.21 −0.11 0.90 −0.05 0.11 −0.02 0.12 土壤全磷 0.41 0.09 0.67 −0.30 −0.06 0.06 0.26 土壤有效磷 0.29 −0.21 0.61 −0.03 0.04 0.01 −0.44 土壤非毛管孔隙度 0.13 −0.06 0.05 0.86 −0.14 0.10 −0.12 坡度 −0.06 −0.31 0.10 0.81 −0.28 −0.15 −0.19 油松相对优势度 0.05 0.21 0.11 −0.77 0.04 −0.26 −0.19 乔木平均生物量 0.40 −0.20 0.02 0.62 0.22 −0.09 −0.03 乔木公顷蓄积 0.04 0.29 0.04 −0.08 0.91 0.14 0.09 乔木公顷生物量 0.04 0.29 0.04 −0.08 0.91 0.14 0.09 胸高断面积 0.26 −0.51 −0.11 −0.33 0.63 0.02 −0.25 郁闭度 −0.12 0.00 −0.27 0.26 0.18 0.83 0.04 坡向 −0.30 −0.08 0.17 0.03 −0.03 −0.78 0.29 间伐间隔 −0.05 −0.46 0.27 −0.10 0.16 0.66 0.17 海拔 0.46 −0.02 0.20 −0.14 0.20 −0.13 0.73 贡献率/% 26.91 22.96 12.55 9.65 6.78 4.90 4.00 累计贡献率/% 26.91 49.88 62.43 72.07 78.85 83.75 87.74 说明:表中加粗字体表示指标在该主成分上有较高载荷 -
为排除冗余变量共轭效应对排序结果的影响,在CCA排序前先使用前向选择,并进行蒙特卡罗显著性检验(表3),综合检验结果确定可以进入CCA排序分析的环境因子。由表3可知:所有环境因子均可以进入CCA排序分析,且环境因子对灌木、草本、藤本物种的解释率(校正解释率)分别为45.7% (34.5%)、37.0% (20.4%)、43.4% (30.6%),因此分析中很大一部分的物种信息可能会丢失。
表 3 环境因子前向选择结果
Table 3. Forward selection results of environmental factors
环境因子 灌木 草本 藤本 解释率/% P 解释率/% P 解释率/% P 土壤水分 1.7 0.690 4.2 0.012 5.4 0.034 林分密度 6.6 0.002 5.1 0.002 4.8 0.046 土壤养分 4.6 0.002 3.3 0.112 6.3 0.044 土壤通气性 7.6 0.002 9.9 0.002 6.1 0.004 生物量 5.0 0.002 4.2 0.008 1.9 0.440 林冠郁闭度 5.8 0.002 4.2 0.014 4.6 0.038 海拔 10.7 0.002 3.5 0.068 8.7 0.002 pH 3.7 0.034 2.6 0.322 5.5 0.016 累计解释率/% 45.7 37.0 43.4 校正解释率/% 34.5 20.4 30.6 物种与环境变量CCA分析模型变量的方差膨胀因子分别为8.91、7.98、9.32,均小于10,说明模型可靠。由不同环境要素对油松人工林下物种分布的解释率可知(表4):油松林下物种分布主要受非生物环境影响。由生境因子与物种分布的相关显著性检验可知(表5):灌木、草本、藤本分布与环境因子极显著相关(P<0.001),前两轴的方差贡献率分别为53.63%、49.12%、63.93%,排序的大部分信息被反映。
表 4 生物与非生物环境因子对物种分布的校正解释率
Table 4. Adjusted explanation rates of biotic and abiotic environmental factors for species distribution
校正解释率/% 未解释率/% 非生物 生物 交互 灌木 19.6 11.1 3.8 65.5 草本 12.8 6.5 4.8 75.9 藤本 20.6 8.0 7.4 69.4 表 5 油松人工林下物种分布与环境因子在前4排序轴上的相关系数
Table 5. Correlation coefficients between distribution of species and environmental factors at the first fourth canonical correspondence analysis ordination axes under P. tabuliformis plantation
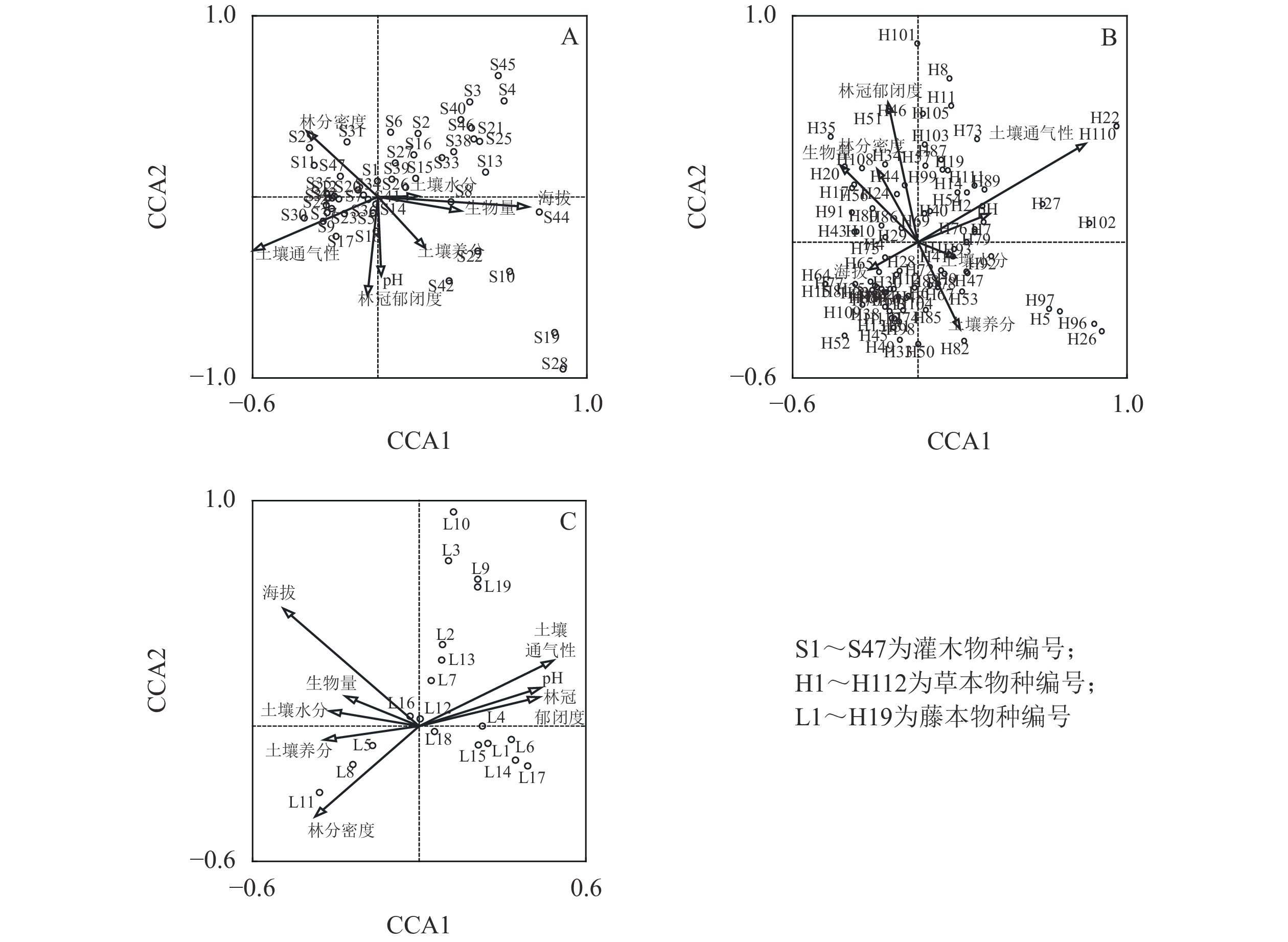
环境因子 排序轴 R2 P CCA1 CCA2 CCA3 CCA4 灌木 土壤水分 0.25 0.01 0.86 −0.44 0.59 0.001*** 林分密度 −0.37 0.40 0.73 0.41 0.83 0.001*** 土壤养分 0.37 −0.46 0.26 −0.77 0.37 0.051 土壤通气性 −0.85 −0.42 0.13 −0.28 0.48 0.007** 生物量 0.69 −0.13 −0.71 −0.10 0.33 0.099 林冠郁闭度 −0.06 −0.62 −0.01 0.78 0.76 0.001*** 海拔 0.90 −0.07 0.31 0.29 0.61 0.001*** pH −0.02 0.58 −0.81 0.00 0.55 0.004** 特征值 0.57*** 0.26*** 0.23*** 0.17*** 累计解释率/% 36.95 53.63 68.68 79.87 草本 土壤水分 0.38 −0.14 0.11 0.91 0.22 0.124 林分密度 −0.21 0.35 0.89 0.21 0.86 0.001*** 土壤养分 0.37 −0.70 0.42 −0.44 0.30 0.032* 土壤通气性 0.85 0.46 0.16 −0.18 0.88 0.001*** 生物量 −0.50 0.45 −0.39 0.63 0.56 0.001*** 林冠郁闭度 −0.18 0.77 −0.04 −0.60 0.63 0.001*** 海拔 −0.36 −0.19 0.31 −0.86 0.41 0.004** pH 0.56 0.21 −0.72 −0.34 0.37 0.004** 特征值 0.63*** 0.23*** 0.23*** 0.19*** 累计解释率/% 35.72 49.12 62.27 73.35 藤本 土壤水分 −0.39 0.08 0.76 0.51 0.68 0.001*** 林分密度 −0.66 −0.71 −0.26 0.06 0.32 0.053 土壤养分 −0.61 −0.11 0.67 −0.41 0.31 0.052 土壤通气性 0.69 0.42 −0.20 0.55 0.48 0.002** 生物量 −0.54 0.27 −0.79 −0.04 0.24 0.162 林冠郁闭度 0.65 0.19 −0.36 −0.64 0.44 0.005** 海拔 −0.59 0.62 −0.45 −0.25 0.70 0.001*** pH 0.64 0.25 0.72 0.13 0.47 0.006** 特征值 0.48*** 0.26*** 0.19*** 0.14*** 累计解释率/% 41.38 63.90 79.80 91.65 说明:*表示P<0.05,**表示P<0.01,***表示P<0.001 基于油松人工林下灌木、草本、藤本与环境因子的CCA二维排序结果可知(表5和图1):油松人工林下灌木、藤本分布主要受海拔影响,其次是土壤通气性,而草本分布主要受土壤通气性影响,其次是林冠郁闭度,即随着海拔、土壤通气性的升高油松人工林下物种多样性下降。
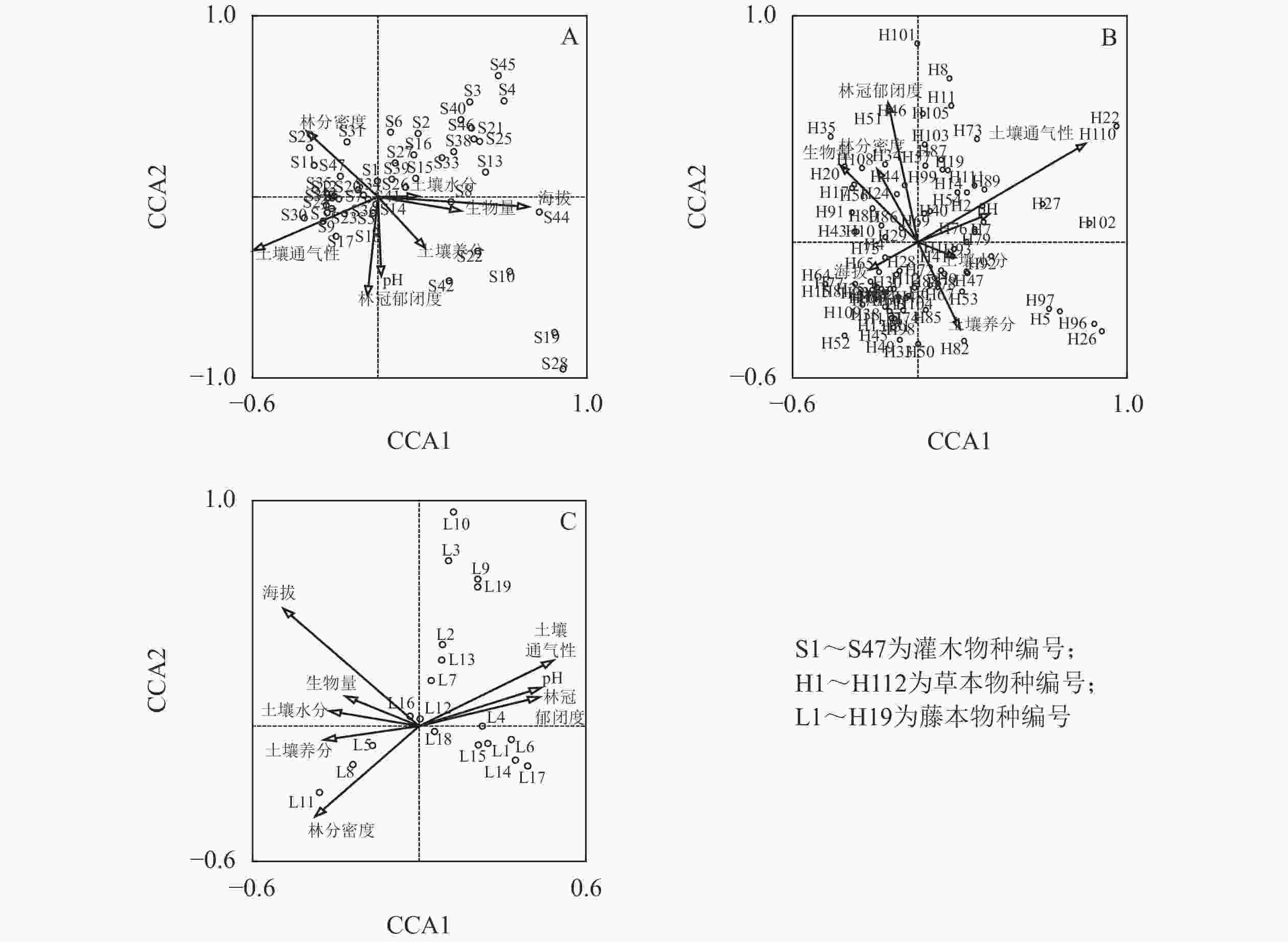
图 1 油松人工林下物种分布与环境因子典范对应分析二维排序图
Figure 1. Two-dimensional ordination diagram of canonical correspondence analysis between distribution of species and environmental factors under P. tabuliformis plantation
林下灌木物种分布除与土壤养分和生物量无显著相关关系外,与其他环境因子均显著相关,且灌木主要分布在海拔相对较低、土壤通气条件较好的油松人工林下,而偶见种黄芦木Berberis amurensis(S19)、美蔷薇Rosa bella (S28)主要分布在海拔较高的区域。林下草本物种分布除与土壤水分无显著相关关系外,与其他环境因子均显著相关,且草本主要分布在土壤条件较好、林内郁闭度较低油松人工林下,而偶见种中华秋海棠Begonia grandis subsp. sinensis (H22)、大油芒Spodiopogon sibiricus (H110)主要分布在土壤通气条件较差的区域,小花灯心草Juncus articulatus (H26)、独活Heracleum hemsleyanum (H96)主要分布在土壤养分较好的区域,羊齿天门冬Asparagus filicinus (H101)主要分布在郁闭度较高的区域。林下藤本物种分布除与林分密度、土壤养分、生物量无显著相关关系外,与其他环境因子均显著相关,且藤本主要分布在低海拔、土壤通气性良好、林分密度相对较低的油松人工林下,而偶见种粉绿铁线莲Clematis glauca (L10)主要分布在土壤通气条件较好的高海拔区域。
-
物种分布受多种因素影响。一般认为大尺度下,气候差异是物种多样性变化的最主要原因[1, 14-16],其中寒冷地区非生物因子对物种分布影响较大,温暖地区生物因子影响相对较大[17-18];随着纬度升高,物种多样性降低[19]。而在小尺度区域内,地形、土壤、生物等因素是物种多样性变化的主要驱动因素[2, 20-21]。中条山油松人工林下物种主要受非生物环境因子影响,由非生物环境因子(海拔)和土壤理化性质形成的局域尺度上的环境异质性,是影响局域内植物物种分布的关键因子,即非生物因子形成的环境筛(environmental filtering)作用是影响该区域林下物种的扩散和生存[22-24]。
海拔和土壤通气性是影响油松林下物种分布的关键性因子,其中灌木和藤本分布主要受海拔影响,草本分布主要受土壤通气性影响。研究[25]表明:海拔是影响植物物种分布的关键性因子之一,是反映温度、湿度、光照等因素的综合环境因素,对物种多样性的影响较复杂。一般认为海拔升高,水热条件将变差,物种多样性将下降;但在某些特殊环境中,海拔升高后水分条件会有所改善,人为干扰活动下降,物种多样性将升高[26];当上升到水热条件限制植物生存的海拔,物种多样性又下降[27];此外,植物物种多样性随海拔升高还呈现其他更复杂变化[28]。本研究发现:中条山物种分布与海拔显著负相关,即海拔升高,林下物种多样性下降。KRAFT等[29]研究发现:生态策略趋同的物种主要受地形环境筛控制,而生态策略趋异的物种主要受生物因素(竞争或密度制约过程)的影响。海拔是中条山油松人工林下灌木和藤本物种分布的重要影响因子之一,说明该地区林下物种生态策略存在趋同性。
在局域范围内,除海拔外,土壤是主导植物物种分布格局的另一个关键非生物环境因子[30-32]。本研究发现:土壤通气性对林下灌木和藤本物种分布的影响仅次于海拔,但对草本物种分布的影响大于海拔,即土壤因素对草本的影响大于地形因素,而对灌木和藤本的影响小于地形因素。该结论与前人研究结果相反,之前研究结果认为,在局域范围内,地形因素是影响植物物种分布最关键的因素,而土壤因素次之[26],其主要原因是,海拔升高导致温度、土壤肥力、土层厚度下降,辐射增加[33-36],即海拔是主导环境改变的关键因子。本研究的土壤通气性是土壤非毛管孔隙度、坡度、油松相对优势度、乔木平均生物量等4个环境因子的集合体,且土壤非毛管孔隙度是影响该综合指标的关键环境因子,此外,本研究区域各海拔土壤厚度变化不大,且海拔越高林分密度越大,辐射对林下植物影响较小,所以当土壤通气性增大时,土壤的保水能力下降,甚至消失,土壤孔隙被空气占据,植物根系无法吸收水分与养分,进而导致植物物种无法生存,所以当其值增大时植物分布将受到限制。
光照也是影响物种分布的主要环境因子之一[37]。本研究发现:林冠郁闭度对林下灌草藤物种分布均存在显著影响,说明光照是限制该区域林下物种多样性的另一个关键环境因子。刘浩栋等[38]研究发现:冠层郁闭度坡向是解释海南岛霸王岭陆均松Dacrydium petinatum天然群落物种分布的主要驱动因素。本研究中,林冠郁闭度是郁闭度、坡向、间伐间隔的等3个环境要素的综合体,所以在今后的森林经营活动中,可以通过开林窗的方式改变林下光照环境,增加林下物种多样性。
油松人工林下物种分布主要受非生物环境因子影响,其中地形(海拔)和土壤(土壤通气性)是影响中条山油松人工林下物种分布的关键环境因子。由于山地生态系统的水热主要受海拔影响,海拔对物种的分布的影响占主导地位,因此随着海拔和土壤通气性的升高,林下物种多样性下降,即地形和土壤因子形成的非生物环境筛作用影响区域群落植物物种的扩散和生存,使物种广泛分布于适宜其自身生存的环境中。
本研究校正解释率较低,说明分析中很大一部分的物种信息可能丢失。造成解释率较低的原因可能是未考虑一些生物、非生物环境要素的结果,如非生物因素中的温度、降水量、光照等,生物因素中的植物功能性状、竞争、人类活动等[39]。所以为了增加环境因子对中条山油松人工林下物种多样性的解释率,今后的研究需增加相应的环境因子。
Influence of environmental factors on distribution of undergrowth species of Pinus tabuliformis plantation in Zhongtiao Mountain
-
摘要:
目的 量化环境要素对山西省中条山油松Pinus tabuliformis人工林下物种分布影响,为进一步揭示中条山油松人工林下物种多样性维持机制提供理论依据。 方法 基于中条山油松人工林样地植物和土壤调查数据,分析环境因子对油松人工林下物种分布的影响。 结果 环境因子对灌木、草本、藤本物种分布的解释率(校正解释率)分别为45.7% (34.5%)、37.0% (20.4%)、43.4% (30.6%);油松林下物种分布主要受非生物环境影响,海拔和土壤通气性是影响该地区物种分布的关键环境因子;灌木和藤本分布主要受海拔影响,草本分布主要受土壤通气性影响,且随着海拔、土壤通气性的升高油松人工林下物种多样性下降。 结论 地形(海拔)和土壤(土壤通气性)因子对区域群落生境的关键塑造作用所形成的环境筛是影响中条山油松人工林下物种分布的关键性因子。图1表5参39 Abstract:Objective This study is aimed to quantify the impact of environmental factors on the distribution of species under the Pinus tabuliformis plantation in Zhongtiao Mountain, Shanxi Province so as to provide a theoretical basis for further revealing the maintenance mechanism of species diversity under the P. tabuliformis plantation in Zhongtiao Mountain. Method With survey data collected of the plant and soil of different types of P. tabuliformis plantation in Zhongtiao Mountain, an analysis was conducted of the influence of environmental factors on the distribution of species under the planted P. tabuliformis plantation. Result The interpretation rates (adjusted explanation rates) of environmental factors on the distribution of shrubs, herbs, and liana species were 45.7% (34.5%), 37.0% (20.4%), and 43.4% (30.6%), respectively. The distribution of species under the P. tabuliformis plantation is mainly affected by abiotic environment. Altitude and soil aeration are the key environmental factors that affect the distribution of species in this area. The distribution of shrubs and lianas under the P. tabuliformis plantation are mainly affected by altitude whereas the distribution of herbs was mainly affected by soil aeration, and the species diversity of the P. tabuliformis plantation declined with the increase of altitude and soil aeration. Conclusion The environmental filtering formed by the key shaping effects of topography (altitude) and soil (soil aeration) factors on the regional community habitat are the key factors that affect the distribution of understory species of P. tabuliformis plantation in Zhongtiao Mountain. [Ch, 1 fig. 5 tab. 39 ref.] -
表 1 样地概况
Table 1. Overview of the sample sites
样地 林龄/a 坡度/(°) 坡向 海拔/m 密度/(株∙ hm−2) 平均胸径/cm 平均树高/m 1 40 22 西南 1 916 808 24.08 14.89 2 46 34 东南 1 924 1511 17.56 9.31 3 28 19 西 1 880 1600 14.77 12.43 4 38 35 西南 1 750 925 18.66 11.20 5 48 21 东 1 722 508 25.64 15.46 6 48 13 东北 1 933 583 27.84 16.31 7 41 20 西南 1 917 500 27.79 14.74 8 36 26 南 1 509 1383 17.39 11.60 9 39 25 西南 1 997 2475 14.79 9.07 10 32 11 东南 1 872 1250 17.39 12.95 11 48 8 西 1 928 467 29.32 15.94 12 46 23 西南 1 960 558 21.76 10.90 表 2 环境因子主成分分析因子旋转载荷矩阵
Table 2. Rotated component matrix for principal component analysis of environmental factors
环境因子 主成分 1 2 3 4 5 6 7 土壤毛管持水量 0.93 0.05 0.23 0.18 0.06 −0.04 −0.06 田间持水量 0.93 0.12 0.18 −0.03 0.07 0.14 0.08 土壤毛管孔隙度 0.91 0.13 0.21 −0.19 0.01 −0.01 0.07 土壤总孔隙度 0.87 0.08 0.21 0.37 −0.08 0.05 −0.01 土壤最大持水量 0.81 −0.01 0.20 0.49 0.02 0.00 −0.10 土壤质量含水量 0.80 0.09 0.22 −0.34 0.16 0.00 0.32 株树密度 −0.10 −0.92 0.15 0.03 0.17 0.08 0.10 平均胸径 0.15 0.90 −0.02 −0.23 0.24 0.06 0.02 乔木平均蓄积 0.10 0.88 0.08 −0.19 0.31 −0.02 0.12 疏密度 −0.05 0.80 −0.06 −0.33 0.31 −0.11 0.03 平均树高 0.06 0.73 −0.23 −0.46 0.30 −0.05 −0.05 林龄 0.47 0.61 −0.01 0.34 0.06 0.37 0.14 土壤有机质 0.18 0.02 0.95 0.12 −0.03 −0.13 −0.03 土壤全氮 0.22 −0.11 0.92 0.20 −0.03 −0.16 0.06 土壤速效氮 0.21 −0.11 0.90 −0.05 0.11 −0.02 0.12 土壤全磷 0.41 0.09 0.67 −0.30 −0.06 0.06 0.26 土壤有效磷 0.29 −0.21 0.61 −0.03 0.04 0.01 −0.44 土壤非毛管孔隙度 0.13 −0.06 0.05 0.86 −0.14 0.10 −0.12 坡度 −0.06 −0.31 0.10 0.81 −0.28 −0.15 −0.19 油松相对优势度 0.05 0.21 0.11 −0.77 0.04 −0.26 −0.19 乔木平均生物量 0.40 −0.20 0.02 0.62 0.22 −0.09 −0.03 乔木公顷蓄积 0.04 0.29 0.04 −0.08 0.91 0.14 0.09 乔木公顷生物量 0.04 0.29 0.04 −0.08 0.91 0.14 0.09 胸高断面积 0.26 −0.51 −0.11 −0.33 0.63 0.02 −0.25 郁闭度 −0.12 0.00 −0.27 0.26 0.18 0.83 0.04 坡向 −0.30 −0.08 0.17 0.03 −0.03 −0.78 0.29 间伐间隔 −0.05 −0.46 0.27 −0.10 0.16 0.66 0.17 海拔 0.46 −0.02 0.20 −0.14 0.20 −0.13 0.73 贡献率/% 26.91 22.96 12.55 9.65 6.78 4.90 4.00 累计贡献率/% 26.91 49.88 62.43 72.07 78.85 83.75 87.74 说明:表中加粗字体表示指标在该主成分上有较高载荷 表 3 环境因子前向选择结果
Table 3. Forward selection results of environmental factors
环境因子 灌木 草本 藤本 解释率/% P 解释率/% P 解释率/% P 土壤水分 1.7 0.690 4.2 0.012 5.4 0.034 林分密度 6.6 0.002 5.1 0.002 4.8 0.046 土壤养分 4.6 0.002 3.3 0.112 6.3 0.044 土壤通气性 7.6 0.002 9.9 0.002 6.1 0.004 生物量 5.0 0.002 4.2 0.008 1.9 0.440 林冠郁闭度 5.8 0.002 4.2 0.014 4.6 0.038 海拔 10.7 0.002 3.5 0.068 8.7 0.002 pH 3.7 0.034 2.6 0.322 5.5 0.016 累计解释率/% 45.7 37.0 43.4 校正解释率/% 34.5 20.4 30.6 表 4 生物与非生物环境因子对物种分布的校正解释率
Table 4. Adjusted explanation rates of biotic and abiotic environmental factors for species distribution
校正解释率/% 未解释率/% 非生物 生物 交互 灌木 19.6 11.1 3.8 65.5 草本 12.8 6.5 4.8 75.9 藤本 20.6 8.0 7.4 69.4 表 5 油松人工林下物种分布与环境因子在前4排序轴上的相关系数
Table 5. Correlation coefficients between distribution of species and environmental factors at the first fourth canonical correspondence analysis ordination axes under P. tabuliformis plantation
环境因子 排序轴 R2 P CCA1 CCA2 CCA3 CCA4 灌木 土壤水分 0.25 0.01 0.86 −0.44 0.59 0.001*** 林分密度 −0.37 0.40 0.73 0.41 0.83 0.001*** 土壤养分 0.37 −0.46 0.26 −0.77 0.37 0.051 土壤通气性 −0.85 −0.42 0.13 −0.28 0.48 0.007** 生物量 0.69 −0.13 −0.71 −0.10 0.33 0.099 林冠郁闭度 −0.06 −0.62 −0.01 0.78 0.76 0.001*** 海拔 0.90 −0.07 0.31 0.29 0.61 0.001*** pH −0.02 0.58 −0.81 0.00 0.55 0.004** 特征值 0.57*** 0.26*** 0.23*** 0.17*** 累计解释率/% 36.95 53.63 68.68 79.87 草本 土壤水分 0.38 −0.14 0.11 0.91 0.22 0.124 林分密度 −0.21 0.35 0.89 0.21 0.86 0.001*** 土壤养分 0.37 −0.70 0.42 −0.44 0.30 0.032* 土壤通气性 0.85 0.46 0.16 −0.18 0.88 0.001*** 生物量 −0.50 0.45 −0.39 0.63 0.56 0.001*** 林冠郁闭度 −0.18 0.77 −0.04 −0.60 0.63 0.001*** 海拔 −0.36 −0.19 0.31 −0.86 0.41 0.004** pH 0.56 0.21 −0.72 −0.34 0.37 0.004** 特征值 0.63*** 0.23*** 0.23*** 0.19*** 累计解释率/% 35.72 49.12 62.27 73.35 藤本 土壤水分 −0.39 0.08 0.76 0.51 0.68 0.001*** 林分密度 −0.66 −0.71 −0.26 0.06 0.32 0.053 土壤养分 −0.61 −0.11 0.67 −0.41 0.31 0.052 土壤通气性 0.69 0.42 −0.20 0.55 0.48 0.002** 生物量 −0.54 0.27 −0.79 −0.04 0.24 0.162 林冠郁闭度 0.65 0.19 −0.36 −0.64 0.44 0.005** 海拔 −0.59 0.62 −0.45 −0.25 0.70 0.001*** pH 0.64 0.25 0.72 0.13 0.47 0.006** 特征值 0.48*** 0.26*** 0.19*** 0.14*** 累计解释率/% 41.38 63.90 79.80 91.65 说明:*表示P<0.05,**表示P<0.01,***表示P<0.001 -
[1] 王健铭, 崔盼杰, 钟悦鸣, 等. 阿拉善高原植物区域物种丰富度格局及其环境解释[J]. 北京林业大学学报, 2019, 41(3): 14 − 23. WANG Jianming, CUI Panjie, ZHONG Yueming, et al. Biogeographic patterns and environmental interpretation of plant regional species richness in Alxa Plateau of northern China [J]. J Beijing For Univ, 2019, 41(3): 14 − 23. [2] 翁昌露, 张田田, 巫东豪, 等. 古田山10种主要森林群落类型的α和β多样性格局及影响因素[J]. 生物多样性, 2019, 27(1): 33 − 41. WENG Changlu, ZHANG Tiantian, WU Donghao, et al. Drivers and patterns of α- and β-diversity in ten main forest community types in Gutianshan, eastern China [J]. Biodiversity Sci, 2019, 27(1): 33 − 41. [3] 刘世荣, 代力民, 温远光, 等. 面向生态系统服务的森林生态系统经营: 现状、挑战与展望[J]. 生态学报, 2015, 35(1): 1 − 9. LIU Shirong, DAI Limin, WEN Yuanguang, et al. A review on forest ecosystem management towards ecosystem services: status, challenges, and future perspectives [J]. Acta Ecol Sin, 2015, 35(1): 1 − 9. [4] PENNEKAMP F, PONTART M, TABI A, et al. Biodiversity increases and decreases ecosystem stability [J]. Nature, 2018, 563(7729): 109 − 112. [5] 朱强, 艾训儒, 吴漫玲, 等. 七姊妹山常绿落叶阔叶混交林物种多样性格局及其环境解释[J]. 西北植物学报, 2019, 39(8): 1491 − 1502. ZHU Qiang, AI Xunru, WU Manling, et al. Species diversity pattern and environmental explanation of evergreen deciduous broad-leaved mixed forest in Qizimei Mountains [J]. Acta Bot Boreal-Occident Sin, 2019, 39(8): 1491 − 1502. [6] 刘宏文, 程小琴, 康峰峰. 油松人工林林下植物群落变化及其环境解释[J]. 生态学杂志, 2014, 33(2): 290 − 295. LIU Hongwen, CHENG Xiaoqin, KANG Fengfeng. Changes of understory plant community in Pinus tabuliformis plantation and associated environmental explanations [J]. Chin J Ecol, 2014, 33(2): 290 − 295. [7] 王慧, 南宏伟, 刘宁. 关帝山油松天然林林下植物组成及环境解释[J]. 生态环境学报, 2017, 26(1): 13 − 19. WANG Hui, NAN Hongwei, LIU Ning. Species composition and environmental factors of understory plant communities in Pinus tabuliformis Garr. natural forest of Guandi Mountain [J]. Ecol Environ Sci, 2017, 26(1): 13 − 19. [8] 秦浩, 董刚, 张峰. 山西植物功能型划分及其空间格局[J]. 生态学报, 2015, 35(2): 396 − 408. QIN Hao, DONG Gang, ZHANG Feng. Classification of plant functional types and spatial pattern in Shanxi Province [J]. Acta Ecol Sin, 2015, 35(2): 396 − 408. [9] 傅志军, 郑雪婷. 山西中条山植物区系的特征[J]. 西北植物学报, 1994, 14(2): 148 − 152. FU Zhijun, ZHENG Xueting. The characteristics of flora in the Zhongtiao Mountain [J]. Acta Bot Boreal-Occident Sin, 1994, 14(2): 148 − 152. [10] 国家林业局. 森林土壤水分-物理性质的测定: LY/T 1215—1999[S]. 北京: 中国标准出版社, 2000. State Forestry Administration. Determination of Forest Soil Water-physical Properties: LY/T 1215−1999 [S]. Beijing: China Standard Press, 2000. [11] 刘琪璟, 孟盛旺, 周华, 等. 中国立木调查表[M]. 北京: 中国林业出版社, 2017. LIU Qijing, MENG Shengwang, ZHOU Hua, et al. Tree Volume Tables of China [M]. Beijing: China Forestry Publishing House, 2017. [12] 方精云, 刘国华, 徐嵩龄. 我国森林植被的生物量和净生产量[J]. 生态学报, 1996, 16(5): 497 − 508. FANG Jingyun, LIU Guohua, XU Songling. Biomass and net production of forest vegetation in China [J]. Acta Ecol Sin, 1996, 16(5): 497 − 508. [13] 黄庆阳, 曹宏杰, 谢立红, 等. 五大连池火山熔岩台地草本层物种多样性及环境解释[J]. 生物多样性, 2020, 28(6): 658 − 667. HUANG Qingyang, CAO Hongjie, XIE Lihong, et al. Species diversity and environmental interpretation of herb layer in lava platform of Wudalianchi, China [J]. Biodiversity Sci, 2020, 28(6): 658 − 667. [14] WOODWARD F I, MCKEE I F. Vegetation and climate [J]. Environ Int, 1991, 17(6): 535 − 546. [15] XU Manhou, MA Li, JIA Yanyan, et al. Integrating the effects of latitude and altitude on the spatial differentiation of plant community diversity in a mountainous ecosystem in China [J/OL]. PLoS One, 2017, 12(3): e0174231[2021-03-14]. doi: 10.1371/journal.pone.0174231. [16] 董雪蕊, 张红, 张明罡. 基于系统发育的黄土高原地区木本植物多样性及特有性格局[J]. 生物多样性, 2019, 27(12): 1269 − 1278. DONG Xuerui, ZHANG Hong, ZHANG Minggang. Explaining the diversity and endemic patterns based on phylogenetic approach for woody plants of the Loess Plateau [J]. Biodiversity Sci, 2019, 27(12): 1269 − 1278. [17] LAUGHLIN D C, ABELLA S R. Abiotic and biotic factors explain independent gradients of plant community composition in ponderosa pine forests [J]. Ecol Modelling, 2007, 205(1/2): 231 − 240. [18] KLANDERUD K, VANDVIK V, GOLDERG D. The importance of biotic vs. abiotic drivers of local plant community composition along regional bioclimatic gradients [J/OL]. PLoS One, 2015, 10(6): e0130205[2021-03-14]. doi: 10.1371/journal.pone.0130205. [19] 李林, 魏识广, 练琚愉, 等. 亚热带不同纬度植物群落物种多样性分布规律[J]. 生态学报, 2020, 40(4): 1249 − 1257. LI Lin, WEI Shiguang, LIAN Juyu, et al. Distributional regularity of species diversity in plant community at different latitudes in subtropics [J]. Acta Ecol Sin, 2020, 40(4): 1249 − 1257. [20] 张树斌, 王襄平, 吴鹏, 等. 吉林灌木群落物种多样性与气候和局域环境因子的关系[J]. 生态学报, 2018, 38(22): 7990 − 8000. ZHANG Shubin, WANG Xiangping, WU Peng, et al. Relationship between shrub species diversity and climate and local environmental factors across Jilin [J]. Acta Ecol Sin, 2018, 38(22): 7990 − 8000. [21] 唐丽丽, 杨彤, 刘鸿雁, 等. 华北地区荆条灌丛分布及物种多样性空间分异规律[J]. 植物生态学报, 2019, 43(9): 825 − 833. TANG Lili, YANG Tong, LIU Hongyan, et al. Distribution and species diversity patterns of Vitex negundo var. heterophylla shrublands in North China [J]. Chin J Plant Ecol, 2019, 43(9): 825 − 833. [22] KLUGE J, WORM S, LANGE S, et al. Elevational seed plants richness patterns in Bhutan, Eastern Himalaya [J]. J Biogeogr, 2017, 44(8): 1711 − 1722. [23] ZELLWEGER F, BALTENSWEILER A, GINZLER C, et al. Environmental predictors of species richness in forest land scapes: abiotic factors versus vegetation structure [J]. J Biogeogr, 2016, 43(6): 1080 − 1090. [24] PETERS M K, HEMP A, APPELHANS T, et al. Predictors of elevational biodiversity gradients change from single taxa to the multi-taxa community level [J/OL]. Nat Commun, 2016, 7: 13736[2021-03-14]. doi: 10.1038/ncomms13736. [25] GALLARDO-CRUZ J A, PÉREZ-GARCÍA E A, MEAVE J A. β-diversity and vegetation structure as influenced by slope aspect and altitude in a seasonally dry tropical landscape [J]. Landscape Ecol, 2009, 24(4): 473 − 482. [26] SUBEDI C K, ROKAYA M B, MÜNZBERGOVÁ Z, et al. Vascular plant diversity along an elevational gradient in the Central Himalayas, western Nepal [J]. Folia Geobot, 2020, 55: 127 − 140. [27] 沈泽昊, 张新时, 金义兴. 三峡大老岭森林物种多样性的空间格局分析及其地形解释[J]. 植物学报, 2000, 42(6): 620 − 627. SHEN Zehao, ZHANG Xinshi, JIN Yixing. Spatial pattern analysis and topographical interpretation of species diversity in the forests of Dalaoling in the region of the Three Gorges [J]. Acta Bot Sin, 2000, 42(6): 620 − 627. [28] ITOW S. Species turnover and diversity patterns along an elevation broad-leaved forest coenocline [J]. J Veg Sci, 1991, 2(4): 477 − 484. [29] KRAFT N J B, VALENCIA R, ACKERLY D D. Functional traits and niche-based tree community assembly in an Amazonia forest [J]. Science, 2008, 322(5901): 580 − 582. [30] RODRIGUES P M S, SCHAEFER C E G R, SILVA J D O, et al. The influence of soil on vegetation structure and plant diversity in different tropical savannic and forest habitats [J]. J Plant Ecol, 2018, 11(2): 226 − 236. [31] 谭一波, 申文辉, 付孜, 等. 环境因子对桂西南蚬木林下植被物种多样性变异的解释[J]. 生物多样性, 2019, 27(9): 970 − 983. TAN Yibo, SHEN Wenhui, FU Zi, et al. Effect of environmental factors on understory species diversity in Southwest Guangxi Excentrodendron tonkinense forests [J]. Biodiversity Sci, 2019, 27(9): 970 − 983. [32] SIEFERT A, RAVENSCROFT C, ALTHOFF D, et al. Scale dependence of vegetation-environment relationships: a meta-analysis of multivariate data [J]. J Veg Sci, 2012, 23(5): 942 − 951. [33] DROLLINGER S, MÜLLER M, KOBL T, et al. Decreasing nutrient concentrations in soils and trees with increasing elevation across a treeline ecotone in Rolwaling Himal, Nepal [J]. J Mt Sci, 2017, 14(5): 843 − 858. [34] HALBRITTER A H, FIOR S, KELLER I, et al. Trait differentiation and adaptation of plants along elevation gradients [J]. J Evol Biol, 2018, 31(6): 784 − 800. [35] KÖRNER C. The use of ‘altitude’ in ecological research [J]. Trends Ecol Evol, 2007, 22(11): 569 − 574. [36] MIEHE G, PENDRY C A, CHAUDHARY R. Nepal: An Introduction to the Natural History, Ecology and Human Environment in the Himalayas [M]. Edinburgh: Royal Botanic Garden Edinburgh, 2015. [37] MARDARI C, TĂNASE C. Plant diversity-environment relationships in xeric grasslands of North-Eastern Romania [J]. Appl Ecol Environ Res, 2016, 14(1): 111 − 127. [38] 刘浩栋, 陈巧, 徐志扬, 等. 海南岛霸王岭陆均松天然群落物种多样性及地形因子的解释[J]. 生态学杂志, 2020, 39(2): 394 − 403. LIU Haodong, CHEN Qiao, XU Zhiyang, et al. Effects of topographical factors on species diversity across Dacrydium pectinatum natural community in Hainan Island [J]. Chin J Ecol, 2020, 39(2): 394 − 403. [39] LI Ting, XIONG Qinli, LUO Peng, et al. Direct and indirect effects of environmental factors, spatial constraints, and functional traits on shaping the plant diversity of montane forests [J]. Ecol Evol, 2020, 10(1): 557 − 568. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20210323






 下载:
下载: