-
花型花色单一、花期短、花叶均赏品种稀缺是木兰科Magnoliaceae植物杂交育种的主要问题[1]。目前有关含笑属Michelia杂交亲和性的研究较少,而了解物种间亲和性关系是培育新品种的关键。有研究认为:在含笑属远缘杂交过程中存在不亲和现象[2−3]。王亚玲等[4]则发现含笑属内种间杂交大多表现亲和,而紫花含笑M. crassipes×金叶含笑M. foveolata则不亲和,但未对不亲和原因进行探究。金叶含笑隶属木兰科含笑属,其花淡黄白色,花被片内扣形成独特花型,叶背密被红褐色柔毛,是木兰科中珍稀的花叶共赏树种,也是木兰科优良的杂交亲本材料。紫花含笑是含笑属珍稀的紫色花色植物,含笑M. figo的花被片边缘有紫色条纹。本研究通过金叶含笑与紫花含笑和含笑的杂交育种研究,以期将三者的优良性状相结合,培育出花叶共赏新品种,提高金叶含笑利用价值,丰富含笑属种质资源,并探究不亲和的原因,以期提高含笑属杂交成功率,为含笑属远缘杂交育种提供理论依据。
-
金叶含笑和紫花含笑来自湖南省长沙市湖南省科技示范园,含笑来自中南林业科技大学校园。
-
于2021年和2022年4—5月,收集金叶含笑、含笑、紫花含笑的花粉,置于−20 ℃的冰箱保存。在授粉前进行花粉活力测定,确保各亲本的花粉活力在60%以上。培养基配方参考柴弋霞等[5]并改良,采用固体培养基。紫花含笑花粉活力测定所用培养基的配制方法:150 g·L−1 蔗糖 + 300 mg·L−1硼酸 + 300 mg·L−1氯化钙+ 8 g·L−1琼脂;含笑花粉活力测定所用培养基的配制方法:100 g·L−1 蔗糖 + 200 mg·L−1硼酸 + 300 mg·L−1氯化钙 + 8 g·L−1琼脂;作者通过预实验已筛选出金叶含笑花粉活力测定的最适培养基为50 g·L−1蔗糖 +200 mg·L−1硼酸 + 300 mg·L−1氯化钙 + 8 g·L−1琼脂。杂交组合 (♀×♂) :含笑×金叶含笑、紫花含笑×金叶含笑、金叶含笑×含笑、金叶含笑×紫花含笑。每个组合授粉30~34朵花。
-
授粉后,在当年9—12月,采集各杂交组合的果实,统计坐果率、结籽率、单个果序上的蓇葖膨大率、种子数、单个蓇葖内含种子数、形态异常种子占比和千粒重。
-
用洗涤剂将杂交种子富含油脂的外种皮搓洗掉,经质量浓度为0.3%的高锰酸钾溶液消毒30 min,再用双蒸水(ddH2O)反复清洗,随后播种,统计各杂交组合种子的出苗率。
-
参考柴弋霞等[5]的方法并改良,在母本花蕾期去除花被片及雄蕊,授予父本花粉并套袋,在授粉后2 h、4 h、6 h、8 h、10 h、12 h、1 d、2 d、4 d、6 d、8 d取下雌蕊放入FAA固定液中,待固定48 h以上后,用解剖针将雌蕊从雌蕊群柄上取下,进行体积分数为50%、30%、10%乙醇和蒸馏水逐级复水,每级复水15 min。复水后将雌蕊置于1 mol·L−1 氢氧化钠溶液中,60 ℃水浴软化3 h,随后用蒸馏水重复清洗3次,用质量分数为0.1%苯胺蓝避光染色12 h。由于金叶含笑花柱从中部至子房基部均密被银灰色短绒毛,采用常规压片时花粉管会被绒毛所覆盖,很难观察到花粉管的生长情况,因此在本研究中,将授粉12 h前的花柱切下,再将授粉12 h后各时间点的子房壁沿心皮背缝线和腹缝线方向削去直至漏出胚珠,软化后使截面呈透明。将上述处理后的材料常规压片后置于莱卡(Leica)荧光倒置显微镜下观察花粉管的生长情况。
-
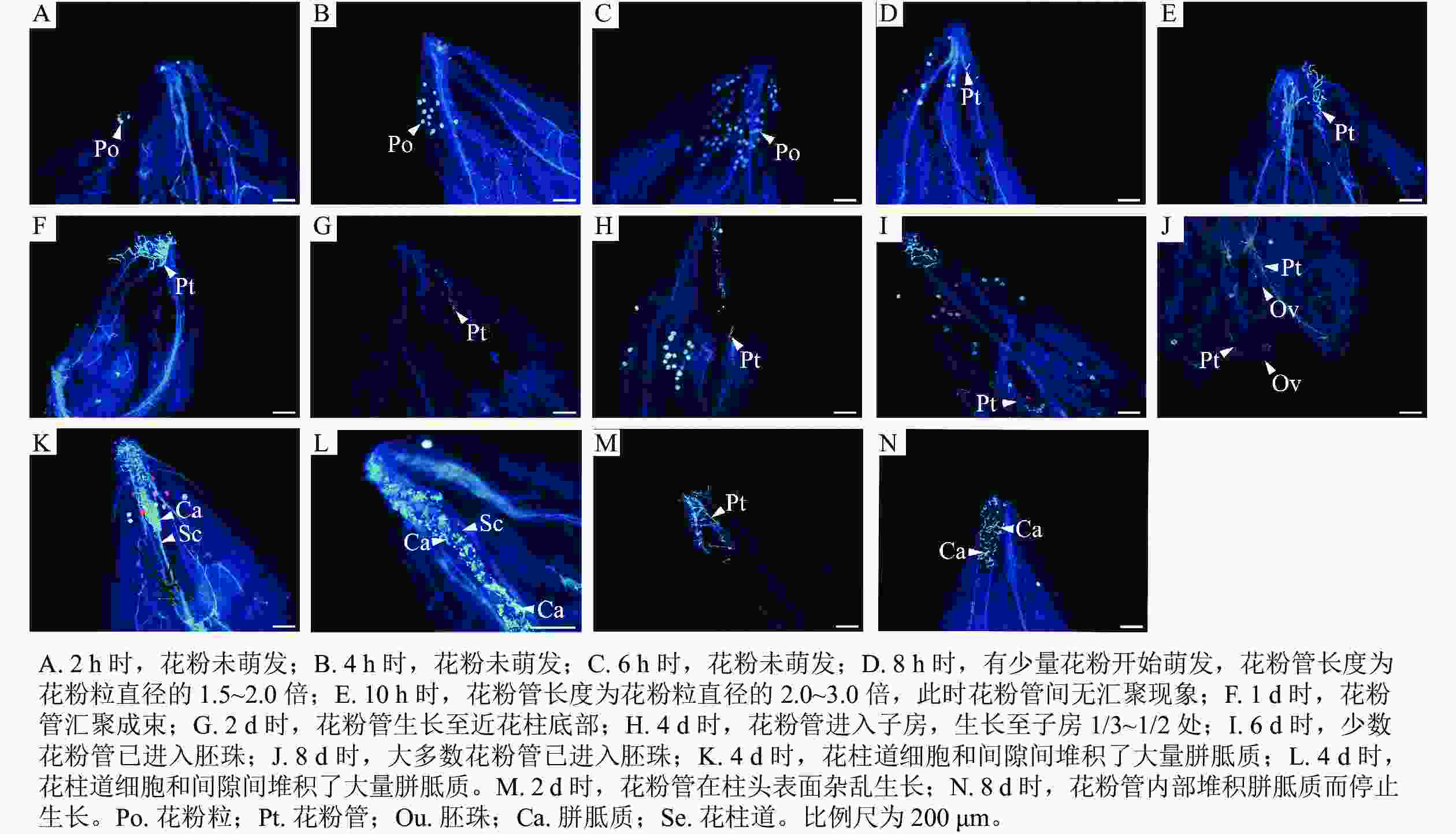
如图1所示:授粉2 h时,仅有极少量的花粉附着在含笑柱头表面且花粉未萌发(图1A);4、6 h时,附着在含笑柱头表面的花粉数量逐渐增多,但同样未萌发(图1B和C);8 h时,有少量花粉开始萌发,花粉管长度为花粉粒直径的1.5~2.0倍(图1D);10 h时,萌发的花粉数量增加,花粉管长度为花粉粒直径的2.0~3.0倍,此时花粉管无汇聚现象(图1E);1 d时,花粉大量萌发,花粉管长度生长至花粉粒直径的3.0倍以上,花粉管出现了明显的汇聚现象(图1F);2 d时,花粉管生长至近花柱底部,即将进入子房(图1G);4 d时,花粉管进入子房,生长至子房1/3~1/2处(图1H);6 d时,有少数生长较快的花粉管进入胚珠(图1I);8 d时,大多数花粉管在此时已进入胚珠(图1J)。但同时也出现了花粉管生长异常的现象:授粉4 d时,发现花柱道细胞和间隙间堆积了大量胼胝质(图1K和L),阻碍了花粉管生长,这一现象也在4、8 d时出现;2 d时,花粉管应汇聚成束进入花柱,但有些花粉管在柱头表面生长杂乱无章(图1M)。在8 d时发现,花粉管在柱头表面萌发,但因花粉管内部堆积胼胝质而停止生长(图1N)。
-
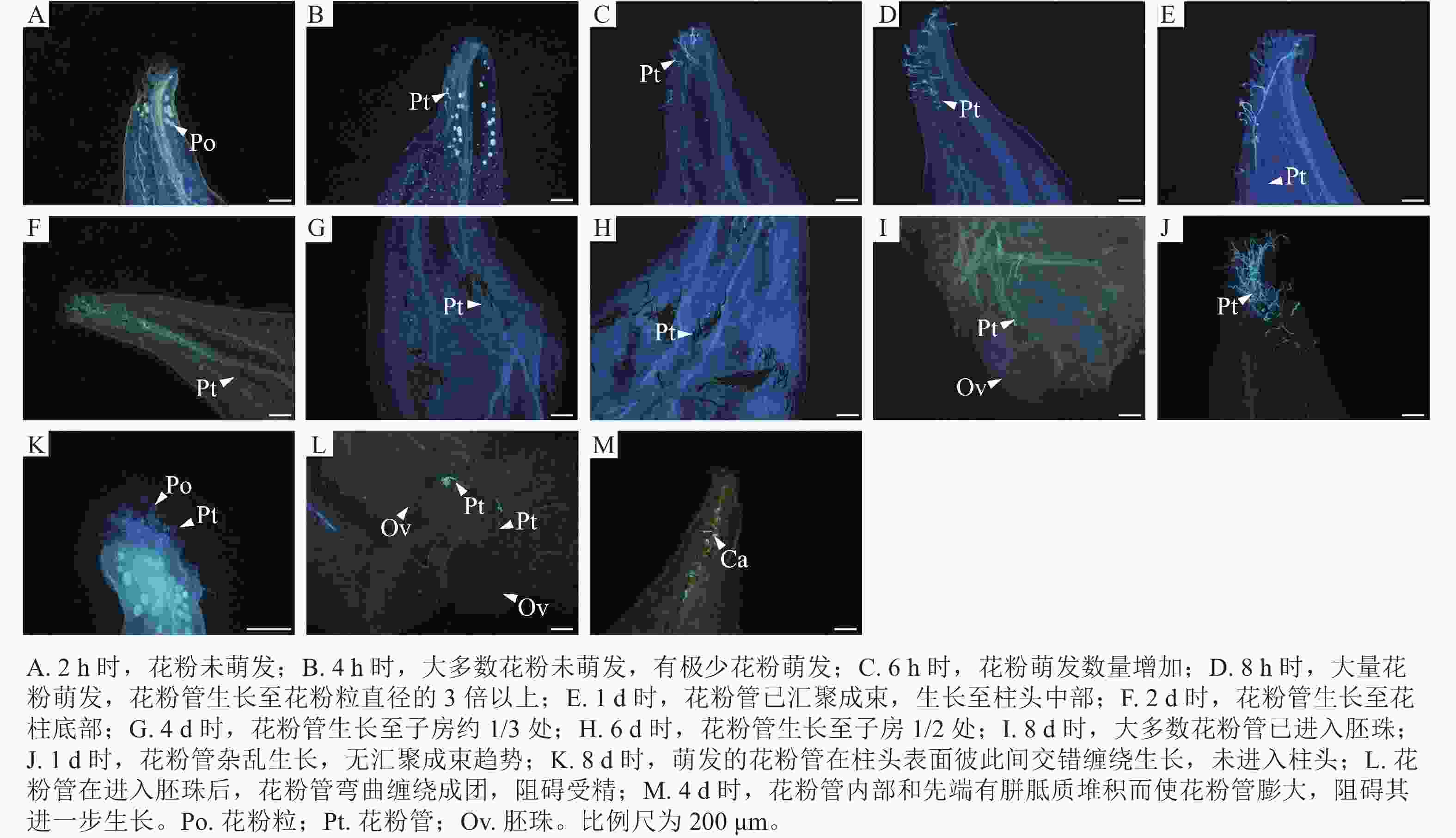
如图2所示:授粉2 h时,花粉未萌发(图2A);4 h时,柱头表面的花粉数量增多,有极少数花粉在此时开始萌发(图2B);6 h时,花粉萌发数量逐渐增多(图2C);在8 h时,大量花粉萌发,花粉管生长至花粉粒直径的3倍以上,此时花粉管存在汇聚的趋势但还没有开始汇聚(图2D);授粉后1 d,花粉管已汇聚成束,生长至柱头中部(图2E);2 d时,花粉管生长至花柱底部(图2F);4 d时,花粉管生长至子房约1/3处(图2G);6 d时,花粉管生长至子房1/2处(图2H);8 d时,大多数花粉管已进入胚珠(图2I)。该组合出现以下受精前障碍:授粉1 d时,出现花粉管生长杂乱且无汇聚现象。有的花粉萌发后,花粉管朝反方向生长(图2J);8 d时,发现有的花粉粒仍未萌发、萌发的花粉管在柱头表面彼此间交错缠绕生长,未进入柱头(图2K);花粉管在进入胚珠后,花粉管弯曲缠绕成团,阻碍受精(图2L);4 d时,花粉管内部和先端有胼胝质堆积而使花粉管膨大,阻碍其进一步生长(图2M)。
-
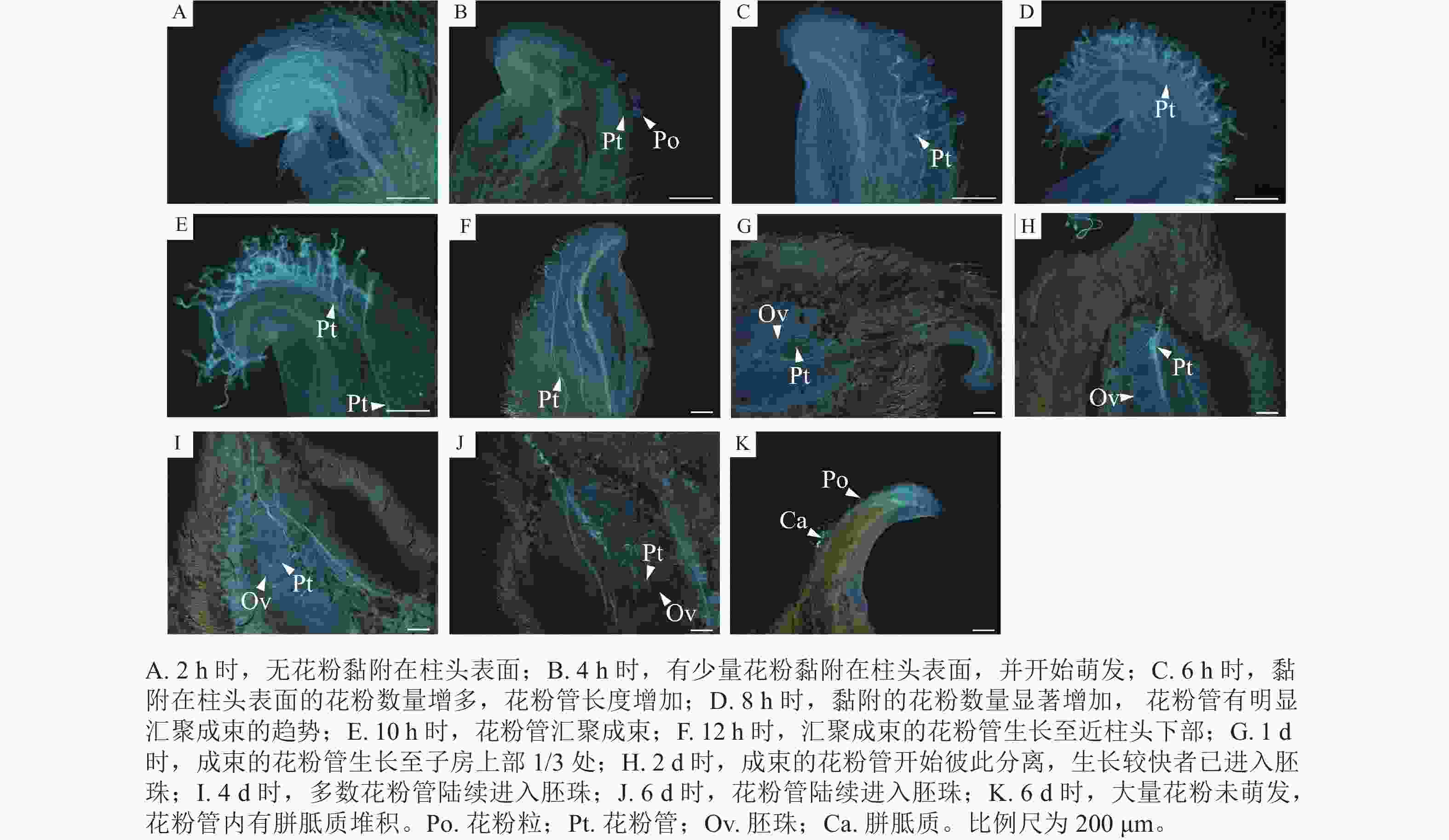
如图3所示:授粉2 h时,无花粉黏附在柱头表面(图3A);4 h时,有少量花粉黏附在柱头表面,并开始萌发,花粉管长度为花粉粒直径的2~3倍(图3B);6 h时,萌发的花粉数量增加,花粉管生长至花粉粒直径的4倍以上,生长较快的花粉管已开始汇聚成束(图3C);8 h时,萌发的花粉数量显著增加,花粉管有明显汇聚成束的趋势(图3D);10 h时,花粉管汇聚成束(图3E);12 h时,汇聚成束的花粉管生长至近柱头下部(图3F);1 d时,成束的花粉管生长至子房上部1/3处(图3G);2 d时,成束的花粉管开始彼此分离,生长较快者已进入胚珠(图3H);4 d时,多数花粉管已进入胚珠(图3I);6 d时,花粉管逐渐向下生长,进入底部的胚珠(图3J)。6 d时,极个别的柱头表面仍存在大量未萌发的花粉,少数已萌发花粉的花粉管内存在胼胝质堆积(图3K)。
-
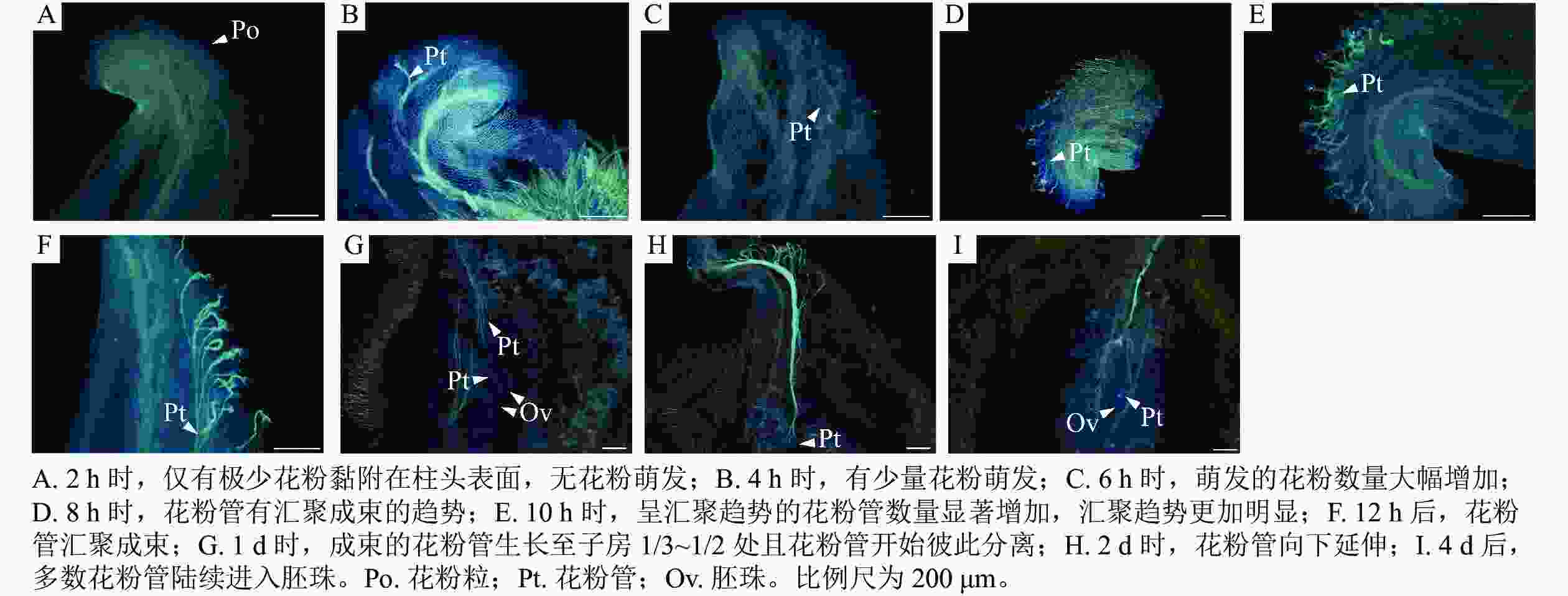
如图4所示:授粉2 h后,仅有极少花粉黏附在柱头表面,无花粉萌发(图4A);4 h时,黏附的花粉数量增加,已有少量花粉萌发,花粉管生长至花粉粒直径的2~3倍,少数生长较快的花粉管生长至花粉粒直径的4倍以上(图4B);6 h时,黏附及萌发花粉数量大幅增加,花粉管生长至花粉粒直径的4倍以上(图4C);8 h时,花粉管有汇聚成束的趋势(图4D);10 h时,呈汇聚趋势的花粉管数量显著增加,汇聚趋势更加明显(图4E);12 h时,花粉管汇聚成束(图4F);1 d时,成束的花粉管生长至子房1/3~1/2处且花粉管开始彼此分离(图4G);2 d时,花粉管继续向下延伸(图4H);4 d时,多数花粉管已进入胚珠(图4I)。
-
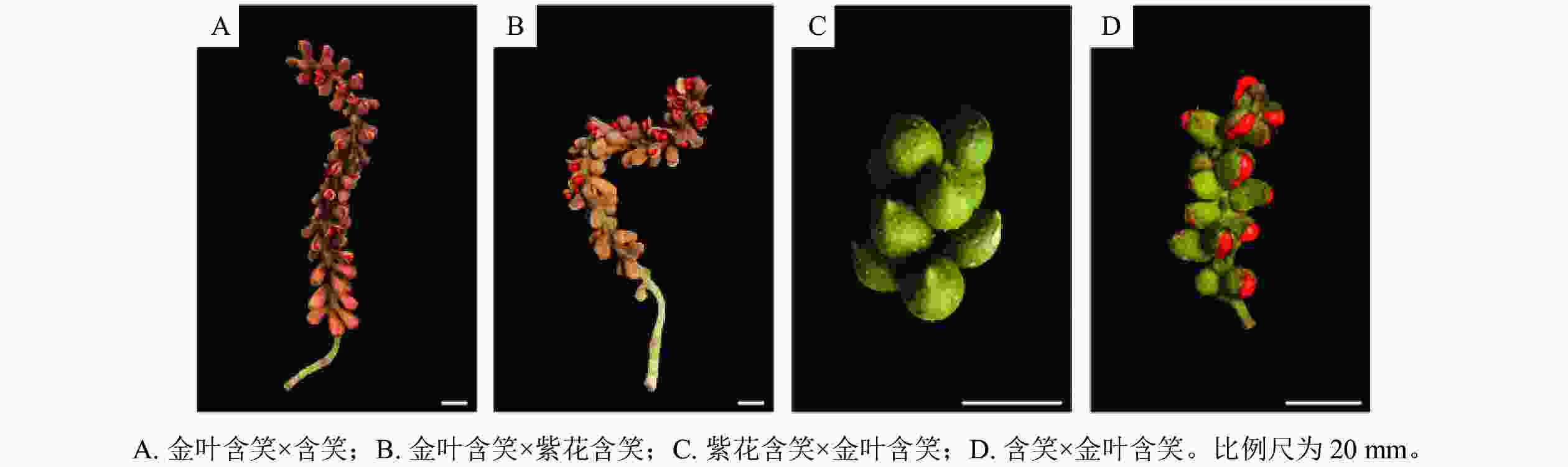
如表1和图5所示:金叶含笑与含笑正反交的坐果率均较高,分别为75.0%和78.8%。金叶含笑与紫花含笑正反交坐果率相差极大,正交的坐果率很高,达80.0%,而反交则极低,只有6.7%。金叶含笑×紫花含笑与金叶含笑×含笑的果实在坐果率、蓇葖膨大率与种子数上无显著差异,金叶含笑×含笑的种子较金叶含笑×紫花含笑略大而饱满。含笑×金叶含笑的坐果率显著高于紫花含笑×金叶含笑,蓇葖膨大率与种子数同样高于紫花含笑×金叶含笑。
表 1 金叶含笑在不同杂交组合中的结实情况
Table 1. Fruit and seed setting status of M. foveolata in different cross combinations
杂交组合 (♀×♂) 坐果率/% 结籽率/% 单个果序蓇葖
膨大率/%种子数/粒 单个蓇葖内
含种子数/粒形态异常
种子占比/%千粒重/g 种子萌发率/% 金叶含笑×含笑 75.0 a 50.3±13.4 a 90.5±8.8 a 300.7±79.2 a 4.8±1.1 a 9.6±5.8 a 25.1 90.6 金叶含笑×紫花含笑 80.0 a 36.6±9.6 b 87.6±7.1 a 287.5±47.9 a 4.4±0.6 a 16.1±9.2 a 21.8 78.1 含笑×金叶含笑 78.8 a 27.3±9.0 bc 49.4±15.7 b 24.1±9.7 b 1.1±0.2 b 0.0±0.0 b 107.7 87.5 紫花含笑×金叶含笑 6.7 b 18.4±1.4 c 27.3±4.6 c 13.0±1.4 b 1.1±0.0 b 0.0±0.0 b 113.3 92.9 说明:不同字母表示不同杂交组合间差异显著(P<0.05)。 -
于2021年和2022年9—12月采集各杂交组合的种子。含笑×金叶含笑与紫花含笑×金叶含笑的种子经低温沙藏处理后于翌年1月播种,种子在3月初至4月初开始陆续萌发。金叶含笑×含笑与金叶含笑×紫花含笑的种子属于薄皮种子,很容易因失水、氧化而失去活性,因此采用即采即播的方式,种子在翌年2月中旬陆续萌发。由表1所示:各杂交组合的种子出苗情况良好,萌发率较高,均在75.0%以上,其中最高的为紫花含笑×金叶含笑杂交组合的种子,萌发率高达92.9%。
-
杂交障碍分为受精前障碍与受精后障碍。受精前障碍主要表现为:花粉在柱头上不能萌发;即使花粉在柱头表面萌发,但花粉管不能伸入柱头;花粉管可以穿过柱头在花柱中生长但生长受阻,不能进入子房到达胚囊;花粉管虽能达到胚囊,但不能完成双受精[6]。受精后障碍主要表现为受精后的合子不分裂或原胚发育异常或早期发育停止;胚乳发育异常或胚乳与胚发育不协调,最终导致胚体发育异常而降解;可获得种子但种子不能发芽或发芽后成株前夭亡或不能正常开花和结果[7]。
本研究中含笑×金叶含笑杂交的坐果率较高,达78.8%。平均每个果序上有49.4%的蓇葖膨大,当果序上有极少数蓇葖膨大时依然可以实现坐果。然而结籽率却较低,仅为27.3%,平均单个蓇葖内含种子数为1.1个,含笑的每心皮内含2枚胚珠,有近一半的胚珠没有成功受精或受精后胚发育异常。综合分析,在荧光显微观察中发现的花柱道细胞和间隙间堆积了大量胼胝质,阻碍了花粉管的生长;花粉管在柱头表面杂乱生长,导致花粉管无法汇聚成束进入花柱道,最终停止生长;花粉管内部和先端有胼胝质堆积,形成胼胝质塞,使花粉管生长受阻等障碍与结实情况,认为上述杂交障碍并不影响坐果,而是影响结籽。王亚玲[8]发现花粉管两型性在木兰科植物中广泛存在,绝大多数花粉是短花粉管型,极少数是长花粉管型,而只有长花粉管能完成受精。香港木兰M. championii的花粉大量萌发,在花柱道汇聚成束后,随着花粉管生长,越靠近胚珠的花粉管neng数量越少,仅有少数花粉管能到达胚珠。这种现象与本研究中含笑和紫花含笑的胚珠附近未见明显的花粉管分离现象相似。因此推测:可能是由于花粉的生理特性加上胼胝质阻碍花粉管进入胚珠完成受精,进而影响结籽率。也有研究发现木兰科植物存在大孢子发生和雌配子体发育异常的现象[9−11],这会对木兰科植物结实产生影响。
金叶含笑×紫花含笑坐果率与结籽率显著高于紫花含笑×金叶含笑,可见金叶含笑作母本时表现亲和,而作父本时亲和性较差。目前已有许多学者发现杂交亲和性具有单向性[12−14]。在王亚玲[8]研究中,紫花含笑×金叶含笑的坐果率为0,判定紫花含笑和金叶含笑杂交不亲和。本研究证实该杂交组合坐果率虽然很低,但仍可以结实。产生差异的原因可能是由于王亚玲仅对7朵花进行杂交试验,样本量过少。虽然在紫花含笑×金叶含笑中出现花粉在柱头表面未萌发,花粉管在柱头表面盘旋生长,未进入柱头,花粉管内部、先端堆积胼胝质而变得膨大,生长受阻,花粉管在胚珠内弯曲缠绕成团,阻碍受精等不亲和现象,但经观察发现绝大多数金叶含笑的花粉管已到达紫花含笑胚珠部位。杨占辉等[15]在鸢尾Iris spp.杂交试验中发现鸢尾花粉在柱头表面缠绕扭曲,但对花粉管伸长影响不大,最终都可见花粉管进入胚珠。何兴波等[16]发现‘风味玫瑰’Prunus domestica × P. armeniaca ‘Fengweimeigui’自交的花粉管在胚珠附近时,花粉管先端出现团状胼胝质,阻碍花粉管进入胚珠。张赛阳等[17]发现杂交石竹Dianthus hybridus的花粉管即使可以从珠孔进入胚囊,但在珠孔附近卷曲盘绕生长,并堆积胼胝质,阻碍双受精。在紫花含笑×金叶含笑杂交1个月后,紫花含笑的雌蕊群上仅有极少数雌蕊膨大,但未落果。在2个月时大多数雌蕊的颜色由绿色转为黄色,随后脱落。当下层雌蕊脱落时会连带上层膨大的雌蕊一起脱落,果实脱落率高达93.34%。王亚玲[8]发现没有完成双受精的香港木兰雌蕊会在授粉后10 d左右开始凋落。也有学者认为:在授粉后子房生长停滞并大量落果,是胚胎发育不良引起的[18−19]。吴美娇等[20]发现百合Lilium spp.花粉管在受精前无明显障碍,但在受精和胚胎发育过程中出现不同程度的胚败育现象。综合分析,推测紫花含笑×金叶含笑杂交不亲和主要是由受精后障碍引起的,因此,需要对受精情况和胚胎发育进一步研究。
在金叶含笑×含笑与金叶含笑×紫花含笑中均存在形态异常的种子,大多数为空瘪的种子。在2个组合中形态异常种子占比分别为9.6%和16.1%,而反交则均为饱满的种子,王亚玲[8]发现:在香港木兰授粉后部分合子出现败育,如果胚乳核继续发育,最后可以形成无胚种子。同时也存在受精胚乳核败育,胚乳没有形成营养丰富的胚乳核细胞,而是形成海绵状物质。目前已有许多方法用于克服受精前障碍,如蒙导法、重复授粉法等。贺丹等[21]研究发现:延迟授粉法可以减缓甚至克服母本柱头或花柱对异源花粉萌发及花粉管生长的抑制,克服受精前障碍,提高育种效率。对于杂交胚早期败育可采用胚抢救的方法[22−23]。因此,在今后研究中可对紫花含笑×金叶含笑的杂交胚采取胚抢救的方法克服不亲和障碍。
-
金叶含笑与含笑正反交均亲和,金叶含笑花粉管与含笑花柱道内的胼胝质堆积,但不影响坐果率,只对结籽率有一定影响。金叶含笑与紫花含笑表现为单向杂交亲和,金叶含笑×紫花含笑亲和性较强,紫花含笑×金叶含笑亲和性较差是由受精后障碍所引起的。
Compatibility between Michelia foveolata and two Michelia species
-
摘要:
目的 探明金叶含笑Michelia foveolata与含笑M. figo和紫花含笑M. crassipes的杂交亲和性。 方法 以金叶含笑与含笑和紫花含笑作正反交授粉,于授粉2 h、4 h、6 h、8 h、10 h、12 h、1 d、2 d、4 d、6 d、8 d后,通过荧光显微镜观察花粉管的生长情况。同时展开金叶含笑与含笑和紫花含笑的正反交杂交试验,统计结实情况。 结果 ①金叶含笑与含笑正反交的坐果率分别为75.0%和78.8%;②金叶含笑×紫花含笑坐果率(80.0%)显著高于紫花含笑×金叶含笑坐果率(6.7%);③含笑×金叶含笑花粉萌发较紫花含笑×金叶含笑晚2 h,花粉管在生长速度上无明显差异,均在8 d时进入胚珠;④以金叶含笑作母本的组合无明显杂交障碍,花粉管均在2~6 d内进入胚珠,种实发育良好;⑤含笑×金叶含笑存在花粉管在柱头表面杂乱生长、花粉管内部和先端有胼胝质堆积、花柱道细胞及间隙有大量胼胝质堆积等受精前障碍,虽不影响坐果,但对结籽有影响;⑥紫花含笑×金叶含笑存在受精前障碍和受精后障碍,受精前障碍包括花粉在柱头表面未萌发、花粉管在柱头表面盘旋生长未进入柱头、花粉管内部和先端堆积胼胝质而变得膨大,使花粉管生长受阻、花粉管在胚珠内弯曲缠绕成团,阻碍受精作用。但受精后障碍可能是影响落果的重要原因。 结论 金叶含笑与含笑正反交均表现亲和;金叶含笑×紫花含笑的亲和性程度高,紫花含笑×金叶含笑亲和性程度低。图5表1参23 Abstract:Objective This study is aimed to investigate the compatibility of Michelia foveolata with M. figo and M. crassipes. Method On the one hand, fluorescence microscope was used to observe the pollen tube growth after 2 h, 4 h, 6 h, 8 h, 10 h, 12 h, 1 d, 2 d, 4 d, 6 d and 8 d. On the other hand, the reciprocal cross test was carried out of M. foveolata with M. figo and M. crassipes respectively to calculate the fruit and seed setting status. Result (1) The fruit setting rates of the reciprocal cross of M. foveolata and M. figo were 75.0% and 78.8% respectively. (2) The fruit setting rate of M. foveolata × M. crassipes (80.0%) was significantly higher than that of M. crassipes × M. foveolata (6.7%). (3) The pollen germination of M. figo × M. foveolata was 2 h later than that of M. crasspies × M. foveolata and pollen tubes entered ovule on 8 d with no significant difference in growth rate. (4) There was no obvious hybridization barriers in the combination of M. foveolata as mother, and the pollen tube entered the ovule successively within 2 to 6 days with well developed fruit and seeds. (5) There were some pre-fertilization barriers, such as disarranged growth of pollen tube on stigma surface, callose accumulation in pollen tube, and callose accumulation in style channel cells and interstitial space and it was speculated that callose accumulation in style channel as the main cause of pre-fertilization barriers does not affect fruit setting, but has an effect on seed setting. (6) There were pre-fertilization and post-fertilization barriers in M. crassipes×M. foveolata. Pre-fertilization barriers include the failure of pollen to germinate on the stigma surface, the growth of pollen tubes in circles on the stigma surface, without entering the stigma, the expansion of pollen tubes due to the accumulation of callose inside and at the apex and the pollen tube becoming twisted and entangled within the ovule. However, post-fertilization barriers may be an important factor affecting fruit fall. Conclusion The reciprocal cross of M. foveolata and M. figo shows good compatibility with the compatibility degree of M. foveolata × M. crassipes being high, while the compatibility degree of M. crassipes×M. foveolata being low. [Ch. 5 fig. 1 tab. 23 ref.] -
Key words:
- Michelia foveolata /
- cross-compatibility /
- pollen tube /
- fruit setting rate /
- seed setting rate
-
表 1 金叶含笑在不同杂交组合中的结实情况
Table 1. Fruit and seed setting status of M. foveolata in different cross combinations
杂交组合 (♀×♂) 坐果率/% 结籽率/% 单个果序蓇葖
膨大率/%种子数/粒 单个蓇葖内
含种子数/粒形态异常
种子占比/%千粒重/g 种子萌发率/% 金叶含笑×含笑 75.0 a 50.3±13.4 a 90.5±8.8 a 300.7±79.2 a 4.8±1.1 a 9.6±5.8 a 25.1 90.6 金叶含笑×紫花含笑 80.0 a 36.6±9.6 b 87.6±7.1 a 287.5±47.9 a 4.4±0.6 a 16.1±9.2 a 21.8 78.1 含笑×金叶含笑 78.8 a 27.3±9.0 bc 49.4±15.7 b 24.1±9.7 b 1.1±0.2 b 0.0±0.0 b 107.7 87.5 紫花含笑×金叶含笑 6.7 b 18.4±1.4 c 27.3±4.6 c 13.0±1.4 b 1.1±0.0 b 0.0±0.0 b 113.3 92.9 说明:不同字母表示不同杂交组合间差异显著(P<0.05)。 -
[1] 王晶, 王先磊, 赵强民, 等. 木兰科植物杂交育种研究进展[J]. 安徽农业科学, 2014, 42(16): 5084 − 5087. WANG Jing, WANG Xianlei, ZHAO Qiangmin, et al. Research advance in Magnoliaceae crossbreeding [J]. Journal of Anhui Agricultural Sciences, 2014, 42(16): 5084 − 5087. [2] 粟莉圆. 火力楠种子园开花动态与繁育系统研究[D]. 南宁: 广西大学, 2021. SU Liyuan. Study on the Flowering Dynamics and Breeding System in Seed Orchard of Michelia macclurei [D]. Nanning: Guangxi University, 2021. [3] 刘向东, 殷云龙. 不同固体培养基配方对台湾含笑花粉萌发的影响及台湾含笑杂交亲和性分析[J]. 植物资源与环境学报, 2022, 31(2): 49 − 56. LIU Xiangdong, YIN Yunlong. Effects of different solid medium formulas on pollen germination of Michelia compressa and analysis on cross-compatibility of M. compressa [J]. Journal of Plant Resources and Environment, 2022, 31(2): 49 − 56. [4] 王亚玲, 李勇, 张寿洲, 等. 木兰科植物的人工杂交[J]. 武汉植物学研究, 2003, 21(6): 508 − 514. WANG Yaling, LI Yong, ZHANG Shouzhou, et al. The crossing result of Magnoliaceae [J]. Journal of Wuhan Botanical Research, 2003, 21(6): 508 − 514. [5] 柴弋霞, 胡希军, 张冬林, 等. 紫花含笑与含笑、深山含笑和阔瓣含笑杂交亲和性分析[J]. 园艺学报, 2018, 45(10): 1970 − 1978. CHAI Yixia, HU Xijun, ZHANG Donglin, et al. Studies on compatibility of interspecific hybridization between Michelia crassipes and M. figo, M. maudiae, M. platypetala [J]. Acta Horticulturae Sinica, 2018, 45(10): 1970 − 1978. [6] 邓衍明, 叶晓青. 园艺作物远缘杂交受精前生殖障碍及其克服方法[J]. 华北农学报, 2012, 27(增刊 1): 81 − 86. DENG Yanming, YE Xiaoqing. The prefertilization reproductive barriers and overcoming methods of horticultural crops distant hybridization [J]. Acta Agriculturae Boreali-Sinica, 2012, 27(suppl 1): 81 − 86. [7] 邓衍明, 叶晓青. 植物远缘杂交受精后生殖障碍及其克服方法[J]. 华北农学报, 2013, 28(增刊 1): 120 − 124. DENG Yanming, YE Xiaoqing. The post-fertilization eproductive barriers and overcoming methods of horticultural crops distant hybridization [J]. Acta Agriculturae Boreali-Sinica, 2013, 28(suppl 1): 120 − 124. [8] 王亚玲. 香港木兰Magnolia championii Benth的保护生物学研究[D]. 杨凌: 西北农林科技大学, 2006. WANG Yaling. Study on the Conservation Biology of Magnolia championii Benth [D]. Yangling: Northwest A&F University, 2006. [9] 赵兴峰, 孙卫邦, 杨华斌, 等. 极度濒危植物西畴含笑的大小孢子发生及雌雄配子体发育[J]. 云南植物研究, 2008, 30(5): 549 − 556. ZHAO Xingfeng, SUN Weibang, YANG Huabin, et al. Mega- and microsporogenesis and development of female and male gametophytes of Michelia coriacea (Magnoliaceae), a globally critical endangered plant in South-East Yunnan of China [J]. Acta Botanica Yunnanica, 2008, 30(5): 549 − 556. [10] 熊海燕, 刘志雄. 深山含笑大、小孢子发生和雌、雄配子体发育研究[J]. 植物研究, 2018, 38(2): 212 − 217. XIONG Haiyan, LIU Zhixiong. Mega- and microsporogenesis and development of female and male gametophytes in Michelia maudiae Dunn [J]. Bulletin of Botanical Research, 2018, 38(2): 212 − 217. [11] 王姗, 沈永宝, 鲍华鹏, 等. 宝华玉兰大小孢子发生和雌雄配子体发育过程中解剖结构的变化[J]. 植物资源与环境学报, 2021, 30(3): 46 − 53. WANG Shan, SHEN Yongbao, BAO Huafeng, et al. Change of anatomical structure in the process of mega- and microsporogenesis and female and male gametophyte development of Yulania zenii [J]. Journal of Plant Resources and Environment, 2021, 30(3): 46 − 53. [12] 李娜, 邓童, 罗乐, 等. 榆叶梅的远缘杂交亲和性和花粉管行为[J]. 分子植物育种, 2022, 20(17): 5754 − 5762. LI Na, DENG Tong, LUO Le, et al. Distant hybridization compatibility and pollen tube behavior of Prunus triloba [J]. Molecular Plant Breeding, 2022, 20(17): 5754 − 5762. [13] 田青兰, 吴艳艳, 张英俊, 等. 西番莲自交和异交的花粉管荧光显微观察及授粉亲和性分析[J]. 果树学报, 2023, 40(1): 98 − 110. TIAN Qinglan, WU Yanyan, ZHANG Yingjun, et al. Pollen tube fluorescence microscopic observation and pollination compatibility analysis of self and cross- pollination in passion fruit (Passiflora edulis) [J]. Journal of Fruit Science, 2023, 40(1): 98 − 110. [14] 王文鹏, 周莉花, 赵宏波, 等. 蜡梅与光叶红蜡梅和夏蜡梅属间杂交亲和性初步研究[J]. 浙江农林大学学报, 2015, 32(5): 756 − 762. WANG Wenpeng, ZHOU Lihua, ZHAO Hongbo, et al. Intergeneric cross-compatibility from pollen-pistil interactions of three Calycanthaceae species [J]. Journal of Zhejiang A&F University, 2015, 32(5): 756 − 762. [15] 杨占辉, 高亦珂, 史言妍, 等. 无髯鸢尾远缘杂交障碍[J]. 中国农业大学学报, 2013, 18(4): 71 − 76. YANG Zhanhui, GAO Yike, SHI Yanyan, et al. Crossbreeding barriers of distant hybridization in beardless irises [J]. Journal of China Agricultural University, 2013, 18(4): 71 − 76. [16] 何兴波, 雷莉莉, 李芳东, 等. 杏李杂交种‘风味玫瑰’花柱类型与花粉管的生长观察[J]. 热带作物学报, 2014, 35(4): 655 − 661. HE Xingbo, LEI Lili, LI Fangdong, et al. Pistil variability and pollen tube growth of Prunus domestica × P. armeniaca ‘Fengweimeigui’ [J]. Chinese Journal of Tropical Crops, 2014, 35(4): 655 − 661. [17] 张赛阳, 栗燕, 郝鹏博, 等. 杂交石竹授粉受精及其胚胎发育过程的观察[J]. 西北植物学报, 2016, 36(10): 1984 − 1989. ZHANG Saiyang, LI Yan, HAO Pengbo, et al. Pollination fertilization and embryonid development of Dianthus hybridus [J]. Acta Botanica Boreali-Occidentalia Sinica, 2016, 36(10): 1984 − 1989. [18] 王虹妍, 孙英, 孙婉仪, 等. 梅与桃、山桃杂交亲和性和花粉管行为研究[C]// 张启翔. 中国观赏园艺研究进展2017, 北京: 中国林业出版社, 2017: 239 − 245. WANG Hongyan, SUN Ying, SUN Wanyi, et al. Study on compatibility and pollen tube growth after pollination of distant hybridization between Prunus mume and P. persica, P. davidiana [C]// ZHANG Qixiang. Advances in Ornamental Horticulture of China 2017. Beijing: China Forestry Publishing House, 2017: 239 − 245. [19] 任海燕, 李登科, 王永康, 等. 迎秋红枣的柱头形态变化及早期胚胎发育研究[J]. 果树学报, 2022, 39(4): 602 − 609. REN Haiyan, LI Dengke, WANG Yongkang, et al. Stigma morphological changes and early embryogenesis development of Yingqiuhong Chinese jujube (Ziziphus jujuba Mill. ) [J]. Journal of Fruit Science, 2022, 39(4): 602 − 609. [20] 吴美娇, 张亚明, 王雪倩, 等. 无花粉污染百合的杂交育种研究[J]. 南京农业大学学报, 2019, 42(6): 1030 − 1039. WU Meijiao, ZHANG Yaming, WANG Xueqian, et al. Study on hybrid breeding of pollen-free lily [J]. Journal of Nanjing Agricultural University, 2019, 42(6): 1030 − 1039. [21] 贺丹, 张佼蕊, 何松林, 等. 授粉方式对牡丹和芍药远缘杂交受精前障碍的影响[J]. 西北农林科技大学学报(自然科学版), 2020, 48(3): 99 − 106. HE Dan, ZHANG Jiaorui, HE Songlin, et al. Effects of pollination method on pre-fertilization barriers in Paeonia latiflora × Paeonia suffruticosa crosses [J]. Journal of Northwest A&F University (Natural Science Edition), 2020, 48(3): 99 − 106. [22] 杨莹, 于淑霞, 杨林毅, 等. 紫荆属种间杂交胚拯救研究[J]. 植物生理学报, 2022, 58(11): 2173 − 2180. YANG Ying, YU Shuxia, YANG Linyi, et al. Study on embryo rescue of interspecific hybridization in Cercis Linn. [J]. Plant Physiology Journal, 2022, 58(11): 2173 − 2180. [23] 苏晓倩, 鲍仁蕾, 胡凤荣. 不同风信子品种杂交亲和性及胚拯救[J]. 东北林业大学学报, 2019, 47(3): 27 − 30. SU Xiaoqian, BAO Renlei, HU Fengrong. Hybrid affinity and embryo rescue of different hyacinth varieties [J]. Journal of Northeast Forestry University, 2019, 47(3): 27 − 30. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20230021






 下载:
下载: