-
植物悬浮细胞培养是快速获得次生代谢产物特别是天然药物的新技术。近年来,尽管通过构建微生物底盘细胞,进行工业微生物生产的合成生物学技术快速发展[1−2],但植物细胞具备高效的催化酶表达、后修饰能力以及精细的代谢区隔,是天然产物合成的理想底盘,因此植物细胞大规模培养具有代谢独特、可持续和生物安全等特性,符合“绿色制造”的理念,仍然是极具发展潜力的生物合成平台, 是次生代谢产物生产不可替代的技术手段[3] 。目前,多种植物的离体细胞系已经建立,有的已经实现工厂化生产,展现出了巨大的生产潜力 [4−7]。
多胺(polyamines,PAs)是一类广泛存在于原核及真核生物中,具有强烈生物活性,具有3~15个直链碳原子,2个及以上氨基的低分子量脂肪族含氮碱。常见的多胺包括腐胺(putrescine, Put)、精胺(spermine,Spm)、亚精胺(spermidine,Spd)等[8]。多胺在植物生长发育、离体再生、生物和非生物应激源的响应中都起着重要的作用[9−11],如多胺可刺激细胞分裂,促进荔枝Litchi chinensis、云杉Picea abies 等植物体细胞胚的发生和龙葵Solanum nigrum等不定芽的形成[12−14]。多胺在刺激次生代谢物合成方面具有更重要的调控作用,如多胺诱导了印度马兜铃Aristolochia elegans无性系马兜铃酸的产生[15];0.5 mg·L−1精胺处理马槟榔属Capparis植物的愈伤组织,其槲皮素和芦丁积累量最高[16]。1.0 mmol·L−1 亚精胺处理假马齿苋Bacopa monnieri,显著提高了马齿苋苷、总酚和类黄酮的含量[17];外源施用多胺可提高丹参Salvia miltiorrhiza丹酚酸的含量[18];亚精胺和精胺对刺山柑Capparis sp.愈伤组织的培养效果优于腐胺,且使用低剂量多胺效果显著[19];在生物反应器中,添加腐胺增强了西洋参Panax quinquefolius根中人参皂苷的生物合成[20]。
银杏Ginkgo biloba是中国特有的,集食用、药用、生态、木材生产和装饰等用途于一体的重要经济树种[21],其叶中具有较高的类黄酮、萜内酯等药用活性成分,因此银杏叶提取物(EGB)具有抗氧化、抗炎、降血压等功效,还能改善大脑功能、增强记忆能力,对阿尔兹海默症及帕金森病等疑难杂症具有较高的疗效[22−23]。可见,提高银杏叶或细胞中类黄酮和萜内酯的产量是银杏产业发展的重要目标,通过细胞培养生产银杏类黄酮和萜内酯,是实现银杏细胞工厂化生产的重要技术手段。鉴于多胺作为诱导剂对植物悬浮细胞的分化和次生代谢有重要的调控作用,本研究以不同浓度的多胺,包括腐胺、亚精胺、精胺处理银杏悬浮细胞,探究多胺对银杏悬浮细胞生长,类黄酮和萜内酯质量分数及关键酶的调控作用,为提高银杏细胞工厂化生产类黄酮、萜内酯等次生代谢物的能力,酶活性底盘的控制,建立和优化遗传转化体系提供理论和技术支持。
-
叶片来源于40年生生长状态良好的银杏树。4月下旬采集银杏树基部萌芽条的叶片,参照CHEN等[24]的方法建立银杏叶片愈伤组织诱导、增殖及悬浮细胞的培养体系。以继代4次以上的愈伤组织作为悬浮细胞的起始材料,按每瓶100 mL的液体培养基 (250 mL锥形瓶)中放入10 g鲜质量愈伤组织的接种量,将愈伤组织接种到 MS+1.0 mg·L−1 NAA+0.5 mg·L−1 KT+30 g·L−1蔗糖(不含琼脂)的液体培养基中进行培养,建立悬浮培养细胞系。此后每隔12 d将50 mL悬浮细胞液转接到含有100 mL液体培养基的新鲜培养基中,进行扩大培养。锥形瓶放置在100 r·min−1的往复式振荡器上进行震荡培养,获得增殖的悬浮细胞。
-
根据前期多胺研究文献及本课题组前期对多胺浓度的预试验,设定腐胺(Put)、精胺(Spm)、亚精胺(Spd)等3种多胺在悬浮培养液中的终浓度分别均为0.5、1.0、3.0 mmol·L−1。将各多胺母液经0.22 µm微孔滤膜过滤后,根据培养液所要求的浓度计算出相应的体积,分别添加到相应的悬浮培养液中至所需的浓度, 以不添加多胺为对照 (ck)。各多胺处理分别标记为Put 0.5、Put 1.0、Put 3.0;Spm 0.5、Spm 1.0、Spm 3.0;Spd 0.5、Spd 1.0、Spd 3.0。将等量的培养7 d的悬浮细胞(参照文献[23])接种到上述添加多胺的培养基中,再培养7 d后,收获细胞,每个处理设置7瓶,重复3次。
参照CHEN等[24]的方法,将培养的细胞进行抽滤,一部分样品称取鲜质量后,再在80 ℃ 烘干至恒量,获得干质量,用于总类黄酮(total flavonoids, Fla)和总萜内酯(total terpenoid lactones, Lac)质量分数的测定。另一部分鲜样品储存在−80 ℃超低温冰箱中,进行其他生理指标的测定。过滤后的细胞液进行培养液的pH (pH酸度计测定)和电导率(EC)的测定。
调节上述所有培养基的pH为5.80左右,培养室光照强度55 μmol·m−2·s−1,光周期14 h /10 h (光/暗),温度(25±1) ℃。
-
叶绿素质量分数、电导率、苯丙氨酸解氨酶(PAL)活性参照CHEN等[24]方法测定。4-香豆酸辅酶A连接酶 (4-coumarate-coenzyme a ligase, 4CL)、肉桂酰辅酶A还原酶(cinnamoyl-coenzyme a reductase, CCR)、查尔酮合成酶(chalcone synthase, CHS)、肉桂醛脱氢酶(cinnamyl alcohol dehydrogenase, CAD)、二氢黄酮醇还原酶 (dihydroflavonol 4-reductase, DFR)等采用ELISA试剂盒(上海酶联生物科技有限公司)说明书进行测定。参照PEREZ-AMBROCIO等[25]方法测定总类黄酮质量分数。总萜内酯测定方法如下:将干燥的细胞样品研磨成粉末并通过400目筛,在70 ℃下在体积分数为70%乙醇中孵育1 h,随后,将上述溶液在冰浴中冷却,然后在8 000×g下离心15 min。将上清液与质量分数13.9%碱性羟胺混合,放置5 min,依次加入3 mol·L−1盐酸和质量分数6.0% 氯化铁,最后补充体积分数70%乙醇至所需体积。用分光光度计在517 nm处测定吸光度[D(517)],根据标准曲线计算总萜内酯质量分数。
-
采用SPSS 22.0对数据进行单因素方差分析(ANOVA)和Duncan多重分析(DMRT),采用Excel 2016软件作图。
-
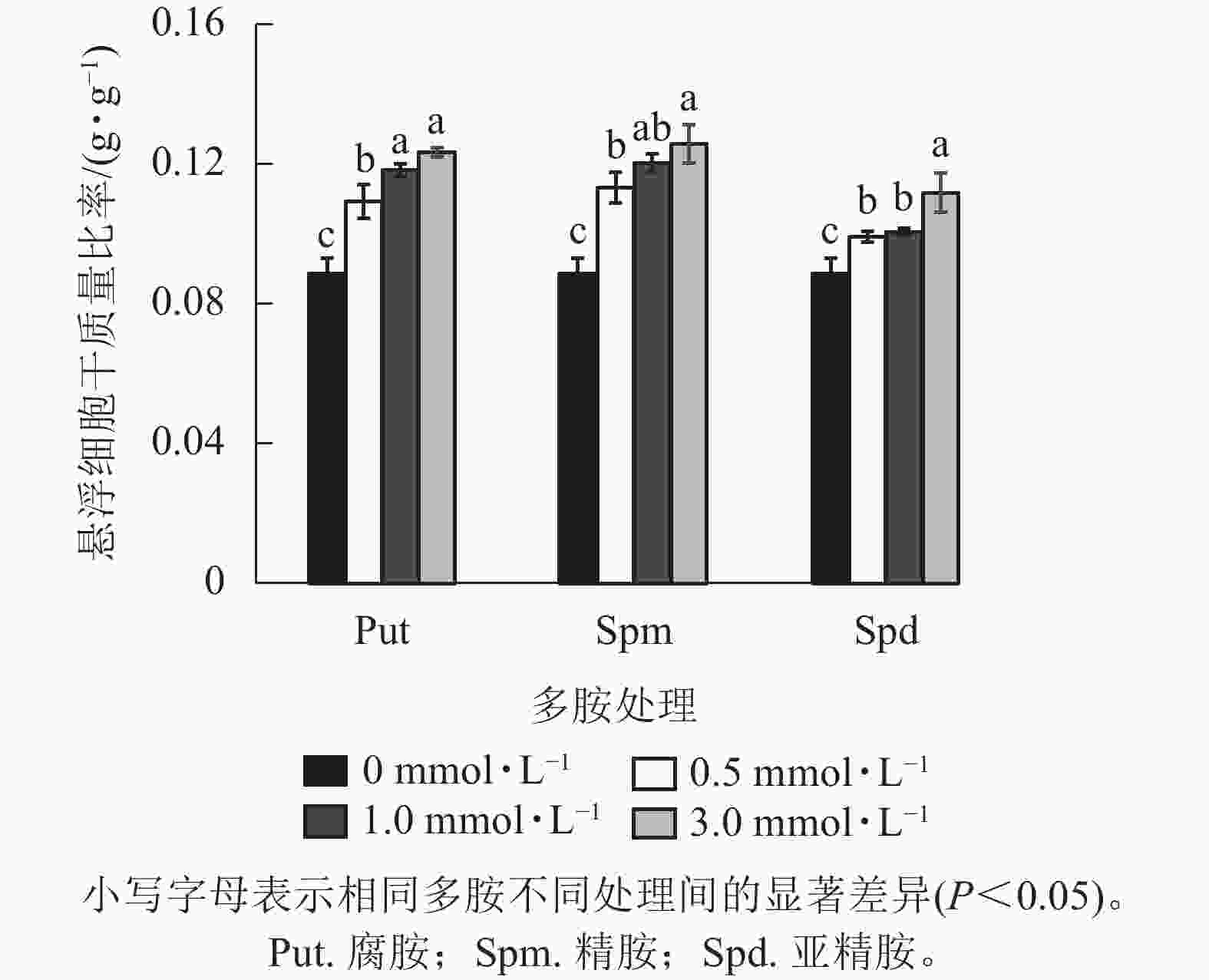
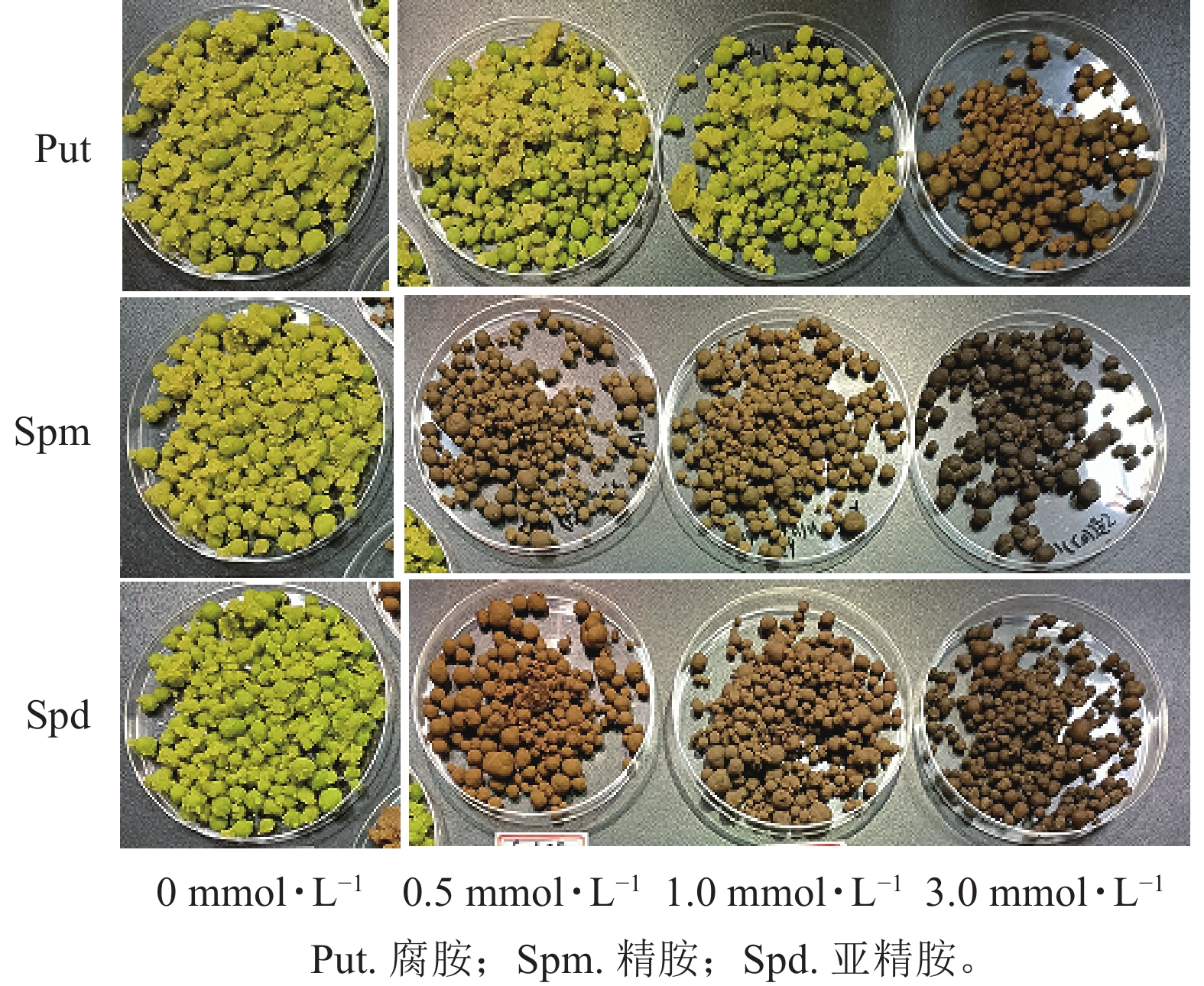
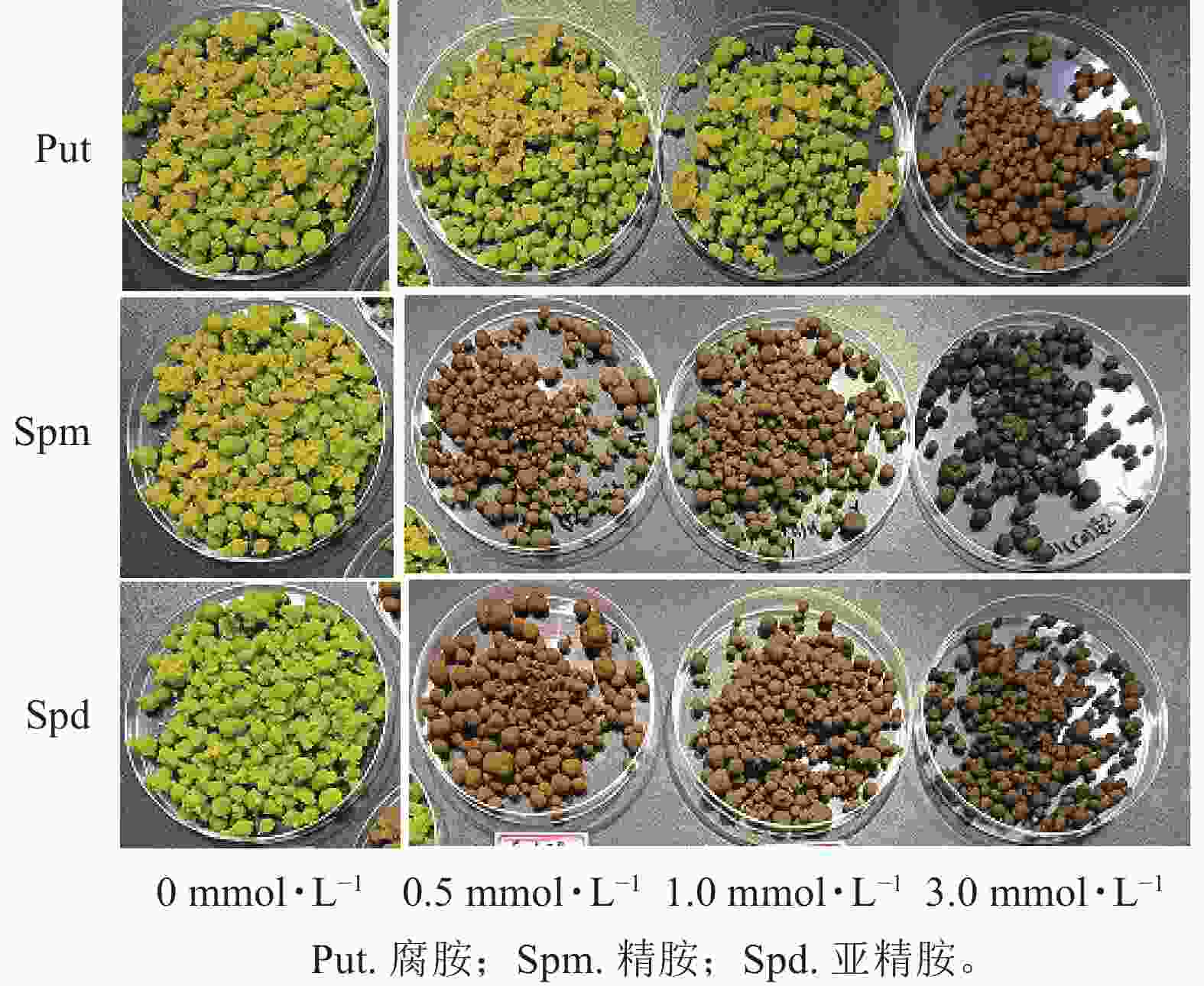
将培养7 d的银杏悬浮细胞接种到0.5、1.0、3.0 mmol·L−1的Put、Spm和Spd的液体培养基后再培养7 d,发现银杏细胞的生长与颜色发生显著变化(图1)。低浓度的 Put 0.5~ Put 1.0处理的细胞团表面呈现黄绿色,颜色较对照绿,细胞团颗粒分明且紧实,富有光泽,但浓度较高的Put 3.0处理的细胞呈黄褐色,细胞团大。经Spm 0.5~Spm 1.0处理后的细胞团表面部分出现黄褐色,部分带有绿色,较Put 3.0褐化程度低,而Spm 3.0的细胞呈黑绿色。Spd 0.5的细胞团表面呈土黄色,细胞团大,但不及Spm处理的绿,Spd 1.0、Spd 3.0处理的细胞团颜色呈灰黄色。总之,浓度为3.0 mmol·L−1的3种多胺处理的细胞团都呈黄褐色或灰褐色,生长严重受抑(图1)。从细胞的干质量比率来看,3种多胺处理后银杏悬浮细胞干质量比率(每克鲜质量细胞的干质量)都随着多胺处理浓度的加大而增加,其中Put 1.0、Put 3.0、Spm 1.0、Spm 3.0处理的比对照分别增加了33.3%、39.1%、34.5%、41.7% (P<0.05)。Spd处理增加的相对较小,在Spd 3.0时比对照增加了26.0%(P<0.05,图2)。
-
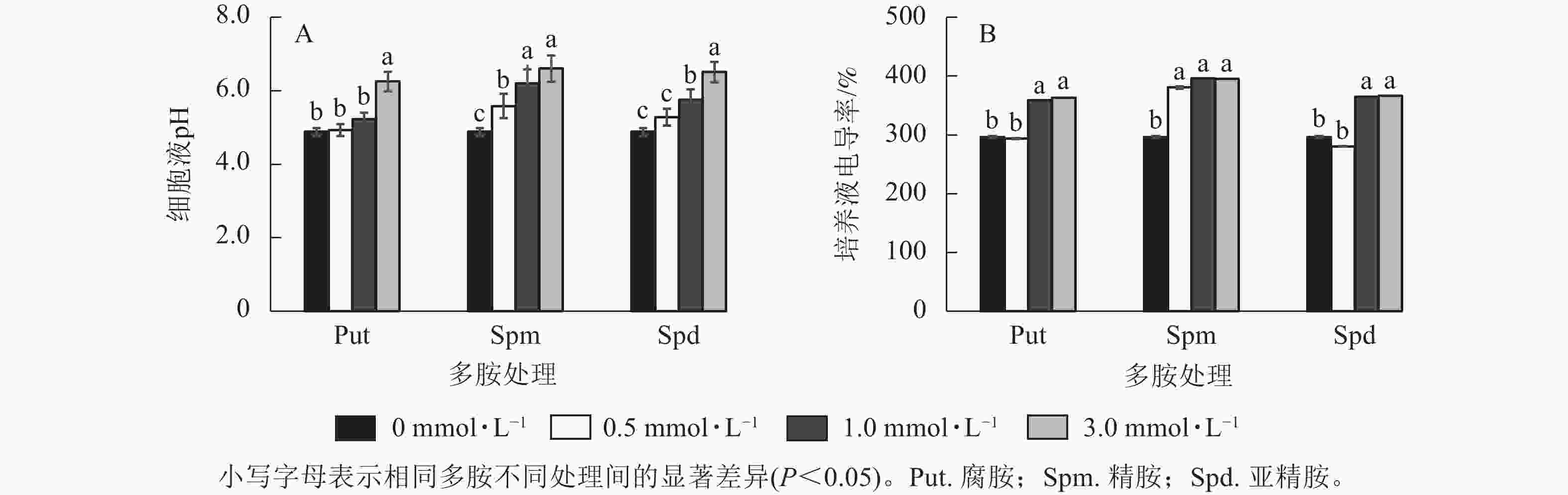
将银杏悬浮细胞分别采用不同浓度的Put、Spm和Spd处理后,细胞培养液的电导率及pH变化如图3所示。从细胞的培养液pH变化来看,Put 3.0、Spm 0.5~Spm 3.0、Spd 1.0~Spd 3.0培养液的pH都显著高于对照(P<0.05),特别是3.0 mmol·L−1多胺处理的细胞液pH最高达6.60 (偏中性),说明多胺处理提高了细胞液的pH,其余处理组的培养液pH与对照无显著差异(图3A)。除Put 0.5与Spd 0.5处理的电导率与对照无显著差异外,其他处理,如Put 1.0~Put 3.0、Spm 0.5~Spm 3.0、Spd 1.0~Spd 3.0都显著高于对照(P<0.05,图3B)。
-
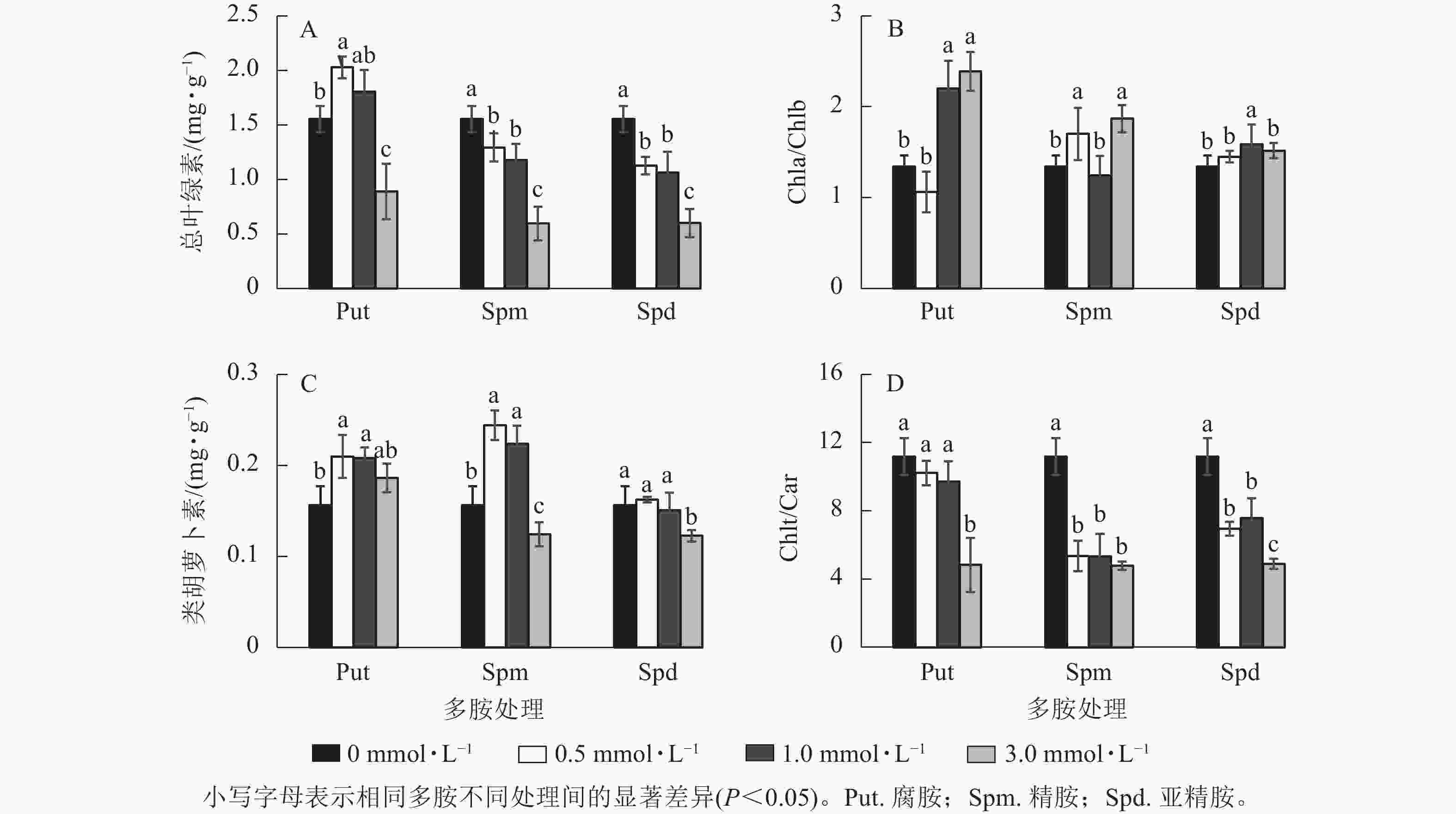
银杏悬浮细胞分别经不同浓度的Put、Spm和Spd处理培养7 d 后,其光合色素变化如图4所示。Put 0.5处理的总叶绿素(Chlt)质量分数显著高于对照(P<0.05),比对照提高了30.5%,Put 3.0处理却下降了42.6%。Spm和Spd 的3个处理浓度都显著降低了总叶绿素质量分数(P<0.05),特别是Spm 3.0和Spd 3.0处理的悬浮细胞总叶绿素质量分数分别下降了61.6%和61.3% (图4A)。Put 1.0~Put 3.0、Spm 0.5、Spm 3.0、Spd 1.0处理后细胞的叶绿素a/叶绿素b (Chla/Chlb)比值都显著高于对照(P<0.05),如Put 1.0~Put 3.0处理的分别比对照提高了63.7%和77.7%(图4B)。Put 0.5~Put 1.0与Spm 0.5~Spm 1.0 处理都显著提高了类胡萝卜素(Car)质量分数(P<0.05),如Put 0.5和Spm 0.5处理分别比对照提高了34.2%和56.3%,Put 3.0、Spd 0.5~Spd 1.0处理与对照之间都没有显著差异,但Spm 3.0与Spd 3.0处理的类胡萝卜素都显著低于对照(P<0.05,图4C)。多胺处理也显著影响了Chlt/Car的比值,Put 0.5~Put 1.0的比值与对照没有显著差异,而Put 3.0、Spm 0.5~Spm 3.0与Spd 0.5~Spd 3.0处理的Chlt/Car比值都显著低于对照(P<0.05,图4D)。
-
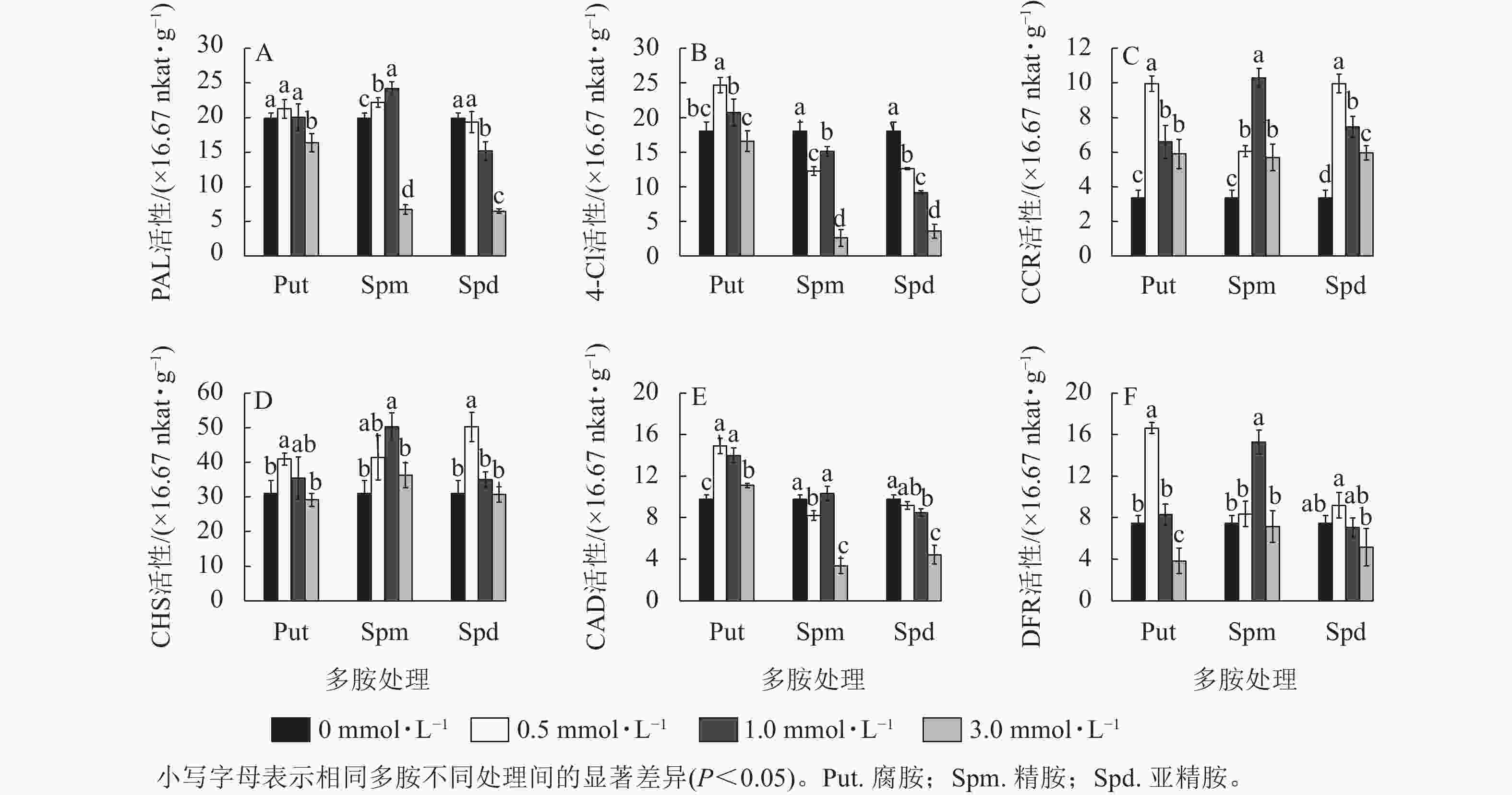
3种不同浓度多胺处理也显著影响黄酮代谢关键酶的活性。对PAL活性来说,只有Spm 0.5~Spm 1.0 处理的酶活性显著高于对照(P<0.05),如Spm 1.0处理的比对照提高了21.5%;Put 0.5~Put 1.0、Spd 0.5处理与对照无显著差异,而3.0 mmol·L−1的3种多胺处理都显著抑制了PAL的活性(P<0.05),如Spm 3.0与Spd 3.0处理的分别下降了66.1%和 67.4% (图5A)。从4CL活性来看,Put 0.5~Put 1.0处理提高了4CL活性,如Put 1.0处理的比对照提高了36.8%;而Spm和Spd处理的都显著低于对照(P<0.05),其中3.0 mg·L−1的下降最明显,分别下降了85.4%和80.0% (图5B)。CCR活性变化不同于前两者,多胺处理都显著提高了该酶的活性(P<0.05),且Put 0.5、Spm 1.0与 Spd 0.5处理都显著高于各自其他2个浓度处理的活性,三者分别比对照提高了196.3%、206.5%和196.3% (图5C)。 对CHS酶来说,Put 0.5、Spm 0.5~Spm 1.0、Spd 0.5处理的都显著高于对照(P<0.05),如Spm 1.0处理的比对照提高了61.9%,其他处理均与对照无显著差异 (图5D)。3个浓度的Put 处理都显著提高了CAD的活性(P<0.05),如Put 0.5处理的比对照提高了52.6%;Spm 3.0与Spd 3.0都显著抑制了CAD活性(P<0.05),分别降低了65.5%和54.6%,其他处理的与对照差异不大(图5E)。对DFR来说,Put 0.5和Spm 1.0处理的DFR活性都显著高于对照 (P<0.05),分别比对照提高了123.2%和105.2%。Put 3.0处理的则出现显著抑制,降低了48.7% (P<0.05,图5F)。
-
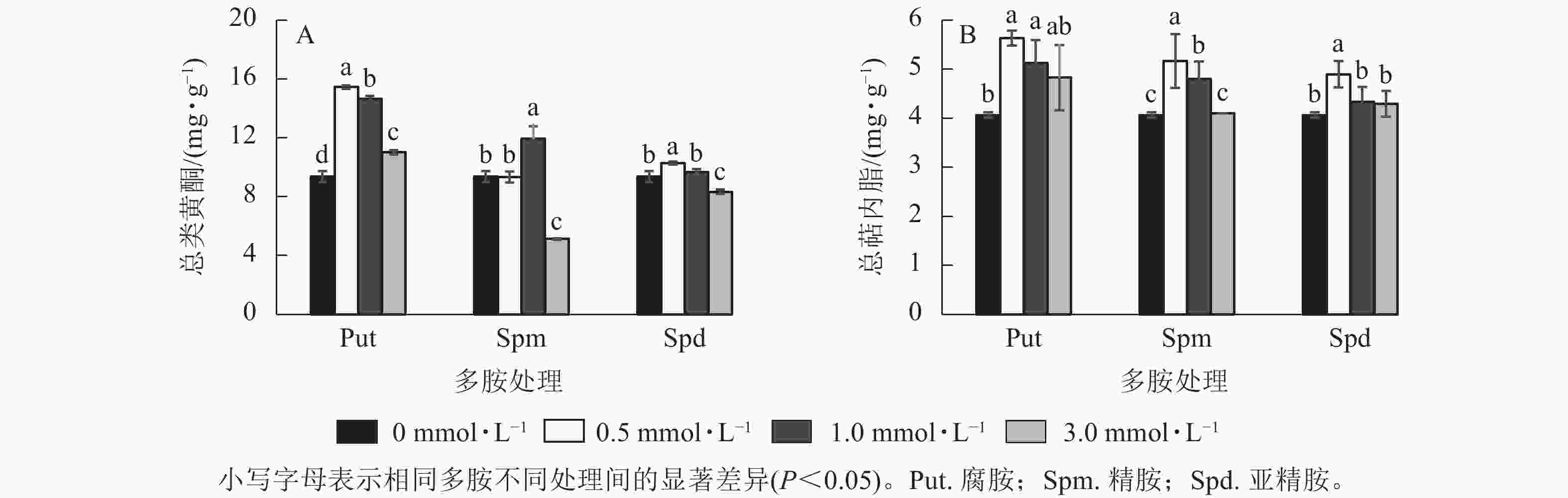
将0.5~3.0 mmol·L−1的Put、Spm和Spd处理悬浮细胞7 d 后,总类黄酮和总萜内酯变化见图6。由图6可见:Put 0.5~Put 3.0和Spd 1.0处理的悬浮细胞总类黄酮质量分数均显著高于对照(P<0.05),分别比对照提高了65.1%、56.6%、17.8 %和27.4%。Spm 3.0与Spd 3.0处理都显著抑制了细胞总类黄酮的积累(P<0.05,图6A), 如Spm 3.0处理的总类黄酮质量分数比对照的降低了82.5%。悬浮细胞的总萜内酯质量分数变化如图6B所示:Put 0.5~Put 1.0、Spm 0.5~Spm 1.0、Spd 0.5处理的总萜内酯质量分数都显著高于对照(P<0.05),其中Put 0.5~Put 1.0比对照提高了38.5%和26.2%,Spm 0.5~Spm 1.0及Spd 0.5处理的总萜内酯分别比对照提高了27.1%、18.0% 和20.1%,其他浓度处理与对照都无显著性差异。
-
多胺是生物代谢过程中产生的一类具有重要生理活性的植物生长调节物质[26]。腐胺(Put)是多胺合成的中心产物,属于二胺,它是亚精氨 (Spd, 三胺)和精氨 (Spm, 四胺)的直接底物。多胺处理下,培养液的pH和电导率影响着悬浮细胞的生长和次生代谢物的积累[27]。本研究中低浓度Put 0.5~Put 1.0和Spd 0.5处理的悬浮细胞液pH与对照没有显著差异,而3.0 mmol·L−1的3种多胺处理使得培养液的pH显著增高,偏向碱化。前人研究表明:培养液适度的碱化是悬浮细胞感受胁迫、产生防卫反应的标志[28−29],此时细胞会释放出一些代谢产物,如生物碱、类黄酮等化合物,有利于次生代谢物的生产。另外,本研究中1.0~3.0 mmol·L−1的3种多胺处理后,银杏悬浮细胞液的电导率也明显提高,这说明pH的升高增强了悬浮细胞质膜的通透性,改善细胞内外环境,因此适宜浓度多胺对银杏类黄酮化合物的积累是有利的。这些研究结果与白桦Betula platyphylla、长叶点地梅Androsace longifolia的结果一致[28, 30]。
本研究发现:3种多胺对细胞生长、颜色、光合色素存在不同的浓度效应。3种多胺都能提高细胞的干质量比率,而低浓度Put 0.5~Put 1.0处理有利于细胞团的生长,细胞颜色黄绿色,总叶绿素和类胡萝卜素质量分数都显著提高,说明Put 处理有利于细胞的生长和光合色素的合成,有利于光合作用。这与多胺能够影响玫瑰Rosa hybrida的形态变化、提高光合色素的结果是一致的[31−32]。Put 3.0、Spm 0.5~Spm 1.0及Spd 0.5处理的细胞颜色都偏黄褐色, 总叶绿素质量分数下降,Chlt/Car比值显著低于对照,而Chla/Chlb比值显著提高,说明Put 3.0及中低浓度的Spm、Spd处理可能使悬浮细胞受到了一定的胁迫,因而抑制了其生长,但这对次生代谢物如类黄酮和萜内酯的合成是有利的。高浓度(Spm 3.0 及Spd 3.0)处理,光合色素大比例地下降,细胞生长受逆严重,反而影响了次生代谢物的合成。本研究结果与多胺处理促进金盏花Calendula officinalis、藏红花Crocus sativus的光合色素变化的结果一致,其原因可能是多胺与类囊体膜中的酶相互作用,保护光合色素免受破坏[33−34]。
3种多胺对总类黄酮质量分数及关键酶活性的调控作用也不同。Put 0.5~Put 1.0及Spd 0.5处理都能够显著促进悬浮细胞类黄酮的积累,而相关酶如4CL、CCR、CHS、CAD、DFR活性都显著增强,特别是Put 0.5处理促进效果最明显。这些结果说明:不同浓度多胺对细胞的影响可分为2种情况:一种是间接作用,如低浓度(如Put 0.5)的多胺通过促进细胞生长、增强光合作用、增加生物量积累来提高类黄酮和萜内酯的产量;一种是直接作用,中等浓度多胺处理 (Put 1.0、Spm 0.5~Spm 1.0、Spd 0.5)可能通过使细胞生长受到适度的胁迫,从而诱导次生代谢物的合成。有研究表明:多胺可以作为诱导子,参入调节次生代谢合成的上游信号,如一氧化氮 (NO)、γ-氨基丁酸 (GABA)、脯氨酸 (Pro)和植物激素等信号分子,并与它们相互作用,启动植物防御反应,调控细胞的次生代谢途径,增强其对环境胁迫的耐受性[9, 20, 35]。本研究结果与 Put 促进刺山柑Capparis spinosa胚芽中槲皮素和芦丁的积累[19],多胺促进金盏花酚类、类黄酮合成[33],促进白桦悬浮细胞中多酚、黄酮和三萜积累,促进火龙果Hylocereus undatus中类黄酮和总萜内酯累积的结果一致[36−37]。
一些研究表明:多胺促进次生代谢物产生的机制与其化学性质有关。在生理pH下,多胺呈游离状态,且带有正电荷,这种性质使其能够与羟基肉桂酸,如咖啡酸、对香豆酸和阿魏酸以共轭形式的存在[38];多胺与酚类化合物的这种偶联改变了它们的极性和亲水性,进而促进了它们的易位、区隔和稳定性,促进了酚类特别是苯丙烷途径物质的合成代谢[39]。类黄酮含有多酚结构,是苯丙烷合成途径中的一条支路,其中PAL、CAD、CCR、4CL、CHS、DFR等6种酶是苯丙素类及黄酮类化合物代谢途径的关键酶。PAL、4CL、CAD处于类黄酮合成途径的上游。查尔酮是黄酮类化合物合成途径中的第1个产物,而CHS是催化查尔酮形成的关键酶,也是促进下游各种类黄酮化合物合成的必由之路[23, 40]。在本研究中, Put 0.5~Put 1.0、Spm 0.5~Spm 1.0,及 Spd 0.5处理都促进了4CL、CAD、CHS酶的活性,与多胺促进黄酮的积累结果是一致的,说明多胺参与了银杏细胞类黄酮化合物代谢的调控。
3种多胺对类黄酮代谢酶活性和类黄酮质量分数的调控出现不同的浓度效应。银杏悬浮细胞对Put的耐受性高于Spm和Spd,对Spd耐受性最低,大部分指标只有在多胺浓度为0.5 mmol·L−1时出现较好的促进效果,而Put在3.0 mmol·L−1仍然有正向的调控作用,这可能与细胞中游离多胺库的动态变化有关。多胺通过Put→Spd→Spm进行正向生物合成,Spm→Spd→Put进行多胺的反向分解代谢[34, 41]。植物细胞中存在着合成和分解多胺的精细、复杂调节机制,控制着游离多胺库的比例、分布和运输,形成了植物细胞内多胺的稳态,调控着细胞的发育和应激[42]。3种多胺对银杏悬浮细胞类黄酮代谢的不同效应,可能与3种多胺合成的先后有关,Put是合成的第1个多胺,外源Put的进入改变了细胞内源游离多胺库的比例,有利于Put合成Spd 和Spm,因而外源加入的Spd 和Spm 就不需要高的浓度。高浓度的Spd 和Spm反而出现负向调节,因此银杏细胞可能存在对3种多胺浓度适应的特异性。有关多胺在银杏细胞内的比例、质量分数的变化、相互协调调控类黄酮代谢的机制等还需要进一步深入研究。
-
多胺处理对银杏细胞的生长、形态及总类黄酮的合成存在不同的浓度效应。低浓度Put 0.5~Put 1.0处理有利于细胞团的生长,而Put 3.0处理的细胞颜色偏黄褐色,细胞生长缓慢。Spm 0.5~Spm 1.0及Spd 0.5处理的细胞呈黄褐色,细胞生长受到抑制。Put 0.5~Put 3.0及Spd 1.0处理对银杏细胞总类黄酮和总萜内酯的积累是有利的;Spm 0.5和Spd 0.5处理更有利于总萜内酯的积累,而Spm 3.0和Spd 3.0处理对银杏细胞生长和类黄酮的合成都不利。另外,多胺还促进了4CL、CAD、CHS酶的活性。多胺,特别是腐胺能够显著促进总类黄酮和总萜内酯化合物的合成。
Effects of exogenous polyamines on the growth and flavonoid synthesis of Ginkgo biloba suspension cells
-
摘要:
目的 探究多胺对银杏Ginkgo biloba悬浮细胞生长和类黄酮代谢的调控作用,为构建和优化银杏遗传转化体系、酶活性底盘控制、规模化生物合成有用药物提供理论和技术支持。 方法 以银杏悬浮细胞为材料,分别将不同浓度(0.5、1.0、3.0 mmol·L−1)的腐胺(Put)、亚精胺(Spd)和精胺(Spm)加入到悬浮细胞培养液中,分别标记为Put 0.5、Put 1.0、Put 3.0,Spm 0.5、Spm 1.0、Spm 3.0,Spd 0.5、Spd 1.0和Spd 3.0,以不添加多胺的处理为对照,培养7 d后,研究多胺对细胞液pH、电导率、细胞光合色素、总类黄酮及总萜内酯质量分数及黄酮合成关键酶活性的影响。 结果 多胺处理的浓度越大,细胞液的电导率和pH越高;低浓度的腐胺处理(Put 0.5~Put 1.0)有利于细胞团的生长,细胞颜色呈黄绿色,总叶绿素、类胡萝卜素、类黄酮和萜内酯质量分数提高,如Put 0.5处理的总类黄酮和总萜内酯分别比对照增加了65.1%和38.5% (P<0.05);Spm 0.5~Spm 1.0 及Spd 0.5处理的细胞呈黄褐色,类胡萝卜素、总类黄酮和总萜内酯的积累也显著提高,如Spm 1.0处理的总类黄酮、 Spm 0.5及Spd 0.5处理的总萜内酯分别比对照提高了27.4%、27.1%和 20.1% (P<0.05)。3种多胺对悬浮细胞类黄酮合成关键酶活性的影响也表现出浓度效应,Put 1.0 处理的4-香豆酸辅酶A连接酶、Spm 1.0处理的苯丙氨酸解氨酶和查尔酮合成酶活性比对照提高的程度最大,分别达36.8%、21.5%和61.9% (P<0.05);Put 0.5、Spm 1.0与Spd 0.5处理的肉桂酰辅酶A还原酶的活性分别比对照提高2.0倍左右;Put 0.5处理的肉桂醛脱氢酶及Put 0.5、Spm 1.0 处理的二氢黄酮醇还原酶分别比对照提高了52.6%、123.2%和105.2% (P<0.05)。 结论 Put 0.5~Put 1.0、Spm 1.0处理对细胞生长和总类黄酮、总萜内酯的积累都是最有利的。多胺,特别是腐胺能够促进类黄酮的生物合成,但Spd 3.0和Spm 3.0处理对细胞生长、总类黄酮和总萜内酯的积累不利。图6参42 Abstract:Objective The objective is to explore the regulatory effects of polyamines (PAs) on the growth and flavonoid (Fla) metabolism in Ginkgo biloba suspension cells, so as to provide theoretical and technical support for constructing and optimizing the genetic transformation system of G. biloba, enzyme activity chassis control, and the large-scale biosynthesis of useful drugs. Method Using suspension cells of G. biloba as the material, different concentrations (0.5,1.0, 3.0 mmol·L−1) of putrescine (Put), spermidine (Spd), and spermine (Spm) were added into the suspension cell culture medium (CCM), labeled as Put 0.5, Put 1.0, Put 3.0, Spm 0.5, Spm 1.0, Spm 3.0, Spd 0.5, Spd 1.0, and Spd 3.0 respectively. A treatment without polyamine addition (0 mmol·L−1 ) was served as the control. After 7 days of cultivation, the effects of PAs on pH and electrical conductivity (EC) of CCM, the contents of photosynthetic pigments, total Fla, total terpenoid lactones (Lac), and the activity of key Fla biosynthesis enzymes were investigated. Result The higher the concentration of PAs was, the higher EC and pH were in CCM. Low concentration of Put treatment (0.5−1.0) was beneficial to the growth of cell clusters, resulting in a yellow-green color of the cells and an increase in the contents of total chlorophyll (Chlt) and carotenoids (Car), Fla and Lac, compared with the control. For example, Fla and Lac contents under Put 0.5 treatment increased by 65.1% and 38.5%, respectively, compared with the control group (P<0.05). The cells treated with Spm 0.5−1.0 and Spd 0.5 turned yellowish brown, and the accumulation of Car, Fla and Lac in suspension cells significantly increased. For example, the content of Fla treated with Spm 1.0, Lac treated with Spm 0.5 and Spd 0.5 increased by 27.4%, 27.1%, and 20.1%, respectively, compared with the control (P<0.05). The effects of 3 PAs treatments on the activity of key enzymes involved in Fla synthesis in suspension cells also showed concentration effects. The activities of 4-coumaric acid coenzyme A ligase (4CL) treated with Put 1.0, phenylalanine ammonia-lyase treated with Spm 1.0, and chalcone synthase treated with Spd 1.0 showed the highest increase compared with the control, reaching 36.8%, 21.5%, and 61.9%, respectively (P<0.05). The activity of cinnamoyl coenzyme A reductase treated with Put 0.5, Spm 1.0, and Spd 0.5 increased by about 2.0 times compared with the control. The cinnamaldehyde dehydrogenase (CAD) treated with Put 0.5, and the dihydroflavonol reductase treated with Put 0.5 and Spm 1.0 increased by 52.6%, 123.2% or 105.2%, respectively, compared with the control (P< 0.05). Conclusion The optimal treatments for suspension cell growth and the accumulation of Fla and Lac are Put 0.5−1.0 and Spm 1.0. Polyamines, especially Put, can promote the biosynthesis of Fla, but Spd 3.0 and Spm 3.0 treatments are detrimental to cell growth, Fla and Lac accumulation. [Ch, 6 fig. 42 ref.] -
Key words:
- Ginkgo biloba /
- polyamines /
- suspension cells /
- flavonoid regulation
-
-
[1] DZIURKA K, DZIURKA M, CZYCZYŁO-MYSZA I, et al. Insight into primary and secondary metabolites of 21-day-old haploid oat embryos[J]. Journal of Plant Growth Regulation, 2025, 44(8): 4396−4407. DOI: 10.1007/s00344-025-11694-8. [2] 孙天丽, 黄明珠, 刘斌, 等. 基于合成生物学微生物底盘细胞构建与优化的研究进展[J]. 食品工业科技, 2025, 46(1): 394−402. SUN Tianli, HUANG Mingzhu, LIU Bin, et al. Research progress in the construction and optimization of microbial chassis cells based on synthetic biology[J]. Science and Technology of Food Industry, 2025, 46(1): 394−402. DOI: 10.13386/j.issn1002-0306.2023120354. [3] 颜钊涛, 周鹏飞, 汪阳忠, 等. 植物合成生物学: 植物细胞大规模培养的新机遇[J]. 合成生物学, 2025(5): 1107−1125. YAN Zhaotao, ZHOU Pengfei, WANG Yangzhong, et al. Plant synthetic biology: a new opportunity for large-scale culture of plant cells[J]. Synthetic Biology Journal, 2025(5): 1107−1125. DOI: 10.12211/2096-8280.2024-095. [4] ARYA S S, ROOKES J E, CAHILL D M, et al. Next-generation metabolic engineering approaches towards development of plant cell suspension cultures as specialized metabolite producing biofactories[J]. Biotechnology Advances, 2020, 45: 107635. DOI: 10.1016/j.biotechadv.2020.107635. [5] 王沐兰, 杨生超, 郁步竹, 等. 红豆杉高产悬浮细胞系建立及其紫杉醇诱导的研究进展[J]. 广西植物, 2016, 36(9): 1137−1146. WANG Mulan, YANG Shengchao, YU Buzhu, et al. Research progress on establishment of high-yield suspension cell line of Taxus chinensis and its taxol induction[J]. Guihaia, 2016, 36(9): 1137−1146. DOI: 10.11931/guihaia.gxzw201412021. [6] LIANG Chuxin, CHEN Chang, ZHOU Pengfei, et al. Effect of Aspergillus flavus fungal elicitor on the production of terpenoid indole alkaloids in Catharanthus roseus cambial meristematic cells[J]. Molecules, 2018, 23(12): 3276. DOI: 10.3390/molecules23123276. [7] PRASHANT S P, BHAWANA M. An update on biotechnological intervention mediated by plant tissue culture to boost secondary metabolite production in medicinal and aromatic plants[J]. Physiologia Plantarum, 2024, 176(4): e14400. DOI: 10.1111/ppl.14400. [8] NANDY S, DAS T, TUDU C K, et al. Unravelling the multi-faceted regulatory role of polyamines in plant biotechnology, transgenics and secondary metabolomics[J]. Applied Microbiology and Biotechnology, 2022, 106(3): 905−929. DOI: 10.1007/s00253-021-11748-3. [9] MUSTAFAVI S H, NAGHDI BADI H, SĘKARA A, et al. Polyamines and their possible mechanisms involved in plant physiological processes and elicitation of secondary metabolites[J]. Acta Physiologiae Plantarum, 2018, 40(6): 102. DOI: 10.1007/s11738-018-2671-2. [10] CHEN Dandan, SHAO Qingsong, YIN Lianghong, et al. Polyamine function in plants: metabolism, regulation on development, and roles in abiotic stress responses[J]. Frontiers in Plant Science, 2019, 9: 1945. DOI: 10.3389/fpls.2018.01945. [11] 杨硕知, 刘球, 吴际友, 等. 外源多胺对红椿S-腺苷甲硫氨酸脱羧酶基因表达的调节作用[J]. 中南林业科技大学学报, 2019, 39(1): 116−123. YANG Shuozhi, LIU Qiu, WU Jiyou, et al. Regulation of exogenous polyamines on S- adenosylmethionine decarboxylase gene expression in Toona sinensis[J]. Journal of Central South University of Forestry & Technology, 2019, 39(1): 116−123. DOI: 10.14067/j.cnki.1673-923x.2019.01.018. [12] 王果, 刘耀婷, 李焕苓, 等. 多胺对荔枝胚性愈伤组织增殖与体胚发生的影响[J]. 广西植物, 2024, 44(7): 1307−1318. WANG Guo, LIU Yaoting, LI Huanling, et al. Influences of polyamines on embryogenic callus proliferation and somatic embryogenesis in Litchi chinensis[J]. Guihaia, 2024, 44(7): 1307−1318. DOI: 10.11931/guihaia.gxzw202308066. [13] VONDRÁKOVÁ Z, ELIÁŠOVÁ K, VÁGNER M, et al. Exogenous putrescine affects endogenous polyamine levels and the development of Picea abies somatic embryos[J]. Plant Growth Regulation, 2015, 75(2): 405−414. DOI: 10.1007/s10725-014-0001-2. [14] BISWAS D, TARUN HALDER T, BISWAJIT GHOSH B. Enhancing secondary metabolite biosynthesis from ethnomedicinal plant Solanum nigrum L. through cytogenetically stable mass propagation, transgenic hairy root induction, and using different LED light and culture vessels for hairy root culture [J]. Journal of Biotechnology, 2025, 404: 63−82. [15] BISWAS D, HALDER T, GHOSH B. Enhancing secondary metabolite biosynthesis from ethnomedicinal plant Solanum nigrum L. through cytogenetically stable mass propagation, transgenic hairy root induction, and using different LED light and culture vessels for hairy root culture[J]. Journal of Biotechnology, 2025, 404: 63−82. DOI: 10.1016/j.jbiotec.2025.04.003. [16] DEY A, HAZRA A K, NONGDAM P, et al. Enhanced bacoside content in polyamine treated in-vitro raised Bacopa monnieri (L. ) Wettst[J]. South African Journal of Botany, 2019, 123: 259−269. DOI: 10.1016/j.sajb.2019.03.012. [17] YASEMIN C, VILDAN Y. Polyamine elicitation of quercetin and rutin production in callus cultures of caper and impact to regeneration[J]. Journal of Scientific and Industrial Research, 2022, 81(5): 475−481. DOI: 10.56042/jsir.v81i05.58826. [18] DEY A, NONGDAM P, NANDY S, et al. Polyamine elicited aristolochic acid production in in vitro clonally fidel Aristolochia indica L. : an ISSR and RAPD markers and HPTLC based study[J]. South African Journal of Botany, 2021, 140: 326−335. DOI: 10.1016/j.sajb.2020.06.018. [19] HAO Gangping, JI Haiwei, LI Yanlin, et al. Exogenous ABA and polyamines enhanced salvianolic acids contents in hairy root cultures of Salvia miltiorrhiza Bge. F. alba[J]. Plant Omics Journal, 2012, 5(5): 446−452. [20] COSKUN Y, YAMAN V. Enhancing phenolic compounds in caper through the incorporation of polyamines in in vitro cultures from various explant sources[J]. South African Journal of Botany, 2024, 165: 43−48. DOI: 10.1016/j.sajb.2023.12.017. [21] YU Yao, ZHANG Wanbo, LI Xiying, et al. Pathogenic fungal elicitors enhance ginsenoside biosynthesis of adventitious roots in Panax quinquefolius during bioreactor culture[J]. Industrial Crops and Products, 2016, 94: 729−735. DOI: 10.1016/j.indcrop.2016.09.058. [22] CHEN Ying, HU Yuchen, WANG Ruimin, et al. Transcriptome and physiological analysis highlights the hormone, phenylpropanoid, and photosynthesis effects on early somatic embryogenesis in Ginkgo biloba[J]. Industrial Crops and Products, 2023, 203: 117176. DOI: 10.1016/j.indcrop.2023.117176. [23] ABDEL SALAM S, GEORGE C S, AL ABDULSALAM N K, et al. Ginkgo biloba attenuates complete Freund’s adjuvant-induced inflammatory pain by suppressing the NF-κB-CXCL1/CXCR2 signaling cascade in the rat spinal cord[J]. Redox Report, 2025, 30(1): 2447778. DOI: 10.1080/13510002.2024.2447778. [24] CHEN Ying, LIN Fangzhi, YANG Hua, et al. Effect of varying NaCl doses on flavonoid production in suspension cells of Ginkgo biloba: relationship to chlorophyll fluorescence, ion homeostasis, antioxidant system and ultrastructure[J]. Acta Physiologiae Plantarum, 2014, 36(12): 3173−3187. DOI: 10.1007/s11738-014-1684-8. [25] PÉREZ-AMBROCIO A, GUERRERO-BELTRÁN J A, APARICIO-FERNÁNDEZ X, et al. Effect of blue and ultraviolet-C light irradiation on bioactive compounds and antioxidant capacity of Habanero pepper (Capsicum chinense) during refrigeration storage[J]. Postharvest Biology and Technology, 2018, 135: 19−26. DOI: 10.1016/j.postharvbio.2017.08.023. [26] 张妍妍, 卢玉, 史保争, 等. 植物中多胺的代谢及生理功能研究进展[J]. 北方园艺, 2023(15): 122−127. ZHANG Yanyan, LU Yu, SHI Baozheng, et al. Research progress on metabolism and physiological function of polyamines in plants[J]. Northern Horticulture, 2023(15): 122−127. DOI: 10.11937/bfyy.20224477. [27] 杨正宇, 周佳君, 胡恒康, 等. 香榧胚性愈伤组织的悬浮培养动力学及对赤霉素的响应[J]. 浙江农林大学学报, 2025, 42(1): 103−111. YANG Zhengyu, ZHOU Jiajun, HU Hengkang, et al. Suspension culture dynamics of embryogenic callus from Torreya grandis ‘Merrillii’ and its response to gibberellin[J]. Journal of Zhejiang A&F University, 2025, 42(1): 103−111. DOI: 10.11833/j.issn.2095-0756.20240291. [28] 翟俏丽, 范桂枝, 詹亚光. 真菌诱导子促进白桦悬浮细胞三萜的积累[J]. 林业科学, 2011, 47(6): 42−47. ZHAI Qiaoli, FAN Guizhi, ZHAN Yaguang. Fungal elicitors promote triterpenoids accumulation in suspension cells of Betula platyphylla[J]. Scientia Silvae Sinicae, 2011, 47(6): 42−47. DOI: 10.11707/j.1001-7488.20110607. [29] BOLLER T. Chemoperception of microbial signals in plant cells[J]. Annual Review of Plant Physiology and Plant Molecular Biology, 1995, 46: 189−214. DOI: 10.1146/annurev.pp.46.060195.001201. [30] 张彦妮, 陈素波. 长叶点地梅的细胞悬浮培养条件[J]. 草业科学, 2014, 31(8): 1481−1486. ZHANG Yanni, CHEN Subo. Cell suspension culture conditions of Dianthus longifolia[J]. Pratacultural Science, 2014, 31(8): 1481−1486. DOI: 10.11829/j.issn.1001-0629.2013-0359. [31] YOUSEFI F, JABBARZADEH Z, AMIRI J, et al. Response of roses (Rosa hybrida L. ‘Herbert stevens’) to foliar application of polyamines on root development, flowering, photosynthetic pigments, antioxidant enzymes activity and NPK[J]. Scientific Reports, 2019, 9(1): 16025. DOI: 10.1038/s41598-019-52547-1. [32] YOUSEFI F, JABBARZADEH Z, AMIRI J, et al. Foliar application of polyamines improve some morphological and physiological characteristics of rose[J]. Folia Horticulturae, 2021, 33(1): 147−156. DOI: 10.2478/fhort-2021-0012. [33] TAVALLALI V, ALHAVI N, GHOLAMI H, et al. Developmental and phytochemical changes in pot marigold (Calendula officinalis L. ) using exogenous application of polyamines[J]. Plant Physiology and Biochemistry, 2022, 183: 128−137. DOI: 10.1016/j.plaphy.2022.05.011. [34] BADIHI L, GERAMI M, AKBARINODEH D, et al. Physio-chemical responses of exogenous calcium nanoparticle and putrescine polyamine in Saffron (Crocus sativus L. )[J]. Physiology and Molecular Biology of Plants, 2021, 27(1): 119−133. DOI: 10.1007/s12298-020-00923-x. [35] NAVAKOUDIS E, KOTZABASIS K. Polyamines: Α bioenergetic smart switch for plant protection and development[J]. Journal of Plant Physiology, 2022, 270: 153618. DOI: 10.1016/j.jplph.2022.153618. [36] 王紫晴, 李飞洁, 郭玉婷, 等. 硫化氢对白桦悬浮细胞中多胺和次生代谢物积累的影响[J]. 南京林业大学学报(自然科学版), 2017, 41(6): 26−32. WANG Ziqing, LI Feijie, GUO Yuting, et al. Effects of hydrogen sulfide on the accumulation of polyamines and secondary metabolites in suspension cells of Betula platyphylla[J]. Journal of Nanjing Forestry University (Natural Sciences Edition), 2017, 41(6): 26−32. DOI: 10.3969/j.issn.1000-2006.201610011. [37] DU Xiaoji, WANG Xiaogang, CHEN Jianye, et al. Putrescine maintains postharvest pitaya quality by regulating polyamine and reactive oxygen homeostasis and energy metabolism[J]. LWT, 2025, 220: 117573. DOI: 10.1016/j.lwt.2025.117573. [38] TIBURCIO A F, ALTABELLA T, BITRIÁN M, et al. The roles of polyamines during the lifespan of plants: from development to stress[J]. Planta, 2014, 240(1): 1−18. DOI: 10.1007/s00425-014-2055-9. [39] BASSARD J E, ULLMANN P, BERNIER F, et al. Phenolamides: bridging polyamines to the phenolic metabolism[J]. Phytochemistry, 2010, 71(16): 1808−1824. DOI: 10.1016/j.phytochem.2010.08.003. [40] GE Xiaomin, ZHAO Aiguo, LI Shasha, et al. ACC treatment induced alterations in flavonoid accumulation in Toxicodendron vernicifluum[J]. Plant Physiology and Biochemistry, 2025, 220: 109491. DOI: 10.1016/j.plaphy.2025.109491. [41] PÁL M, SZALAI G, GONDOR O K, et al. Unfinished story of polyamines: role of conjugation, transport and light-related regulation in the polyamine metabolism in plants[J]. Plant Science, 2021, 308: 110923. DOI: 10.1016/j.plantsci.2021.110923. [42] AUGUSTYNIAK B, WOJTASIK W, SAWUŁA A, et al. The effect of spermidine supplementation on polyamine metabolism and Fusarium infection in Linum usitatissimum[J]. Physiological and Molecular Plant Pathology, 2024, 134: 102453. DOI: 10.1016/j.pmpp.2024.102453. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20250518






 下载:
下载: