-
香榧Torreya grandis ‘Merrillii’是红豆杉科Taxaceae榧树属Torreya中的优良栽培类型,其种仁风味香酥,余味浓郁,营养丰富,深受消费者喜爱,是干果中的珍品[1]。香榧果实(实为裸露的种子。为了便于理解,本研究统称为果实)发育历时17个月,即每年4月上旬授粉,9月底完成受精,次年4月幼果突破种鳞开始膨大,9月成熟[2],但有部分幼果未能突破种鳞,内部珠心呈现褐化萎缩,称为僵果,比例高达89%[3]。大量研究表明:植物僵果的形成常与病原微生物侵染密切相关。例如,佛罗里达炭疽菌Colletotrichum fioriniae侵染桃Prunus persica幼果或膨大果实,导致果实软腐、萎缩、硬化,并引发大量落果[4];伯氏镰刀菌Fusarium pernambucanum侵染荔枝Litchi chinensis幼果,抑制果实膨大并形成僵果[5]。研究表明:苹果Malus pumila霉心病是由花期枝孢属Cladosporium spp.、链格孢菌属Alternaria spp.和粉红聚端孢Trichothecium roseum等病菌通过合生花柱顶缝—萼心间组织—萼窦路径侵染所致,在果实期显现症状,导致僵果、落果或果实腐烂[6−8]。前期研究发现:在授粉期,香榧雌球花因珠孔裸露,枝孢属真菌可随花粉通过传粉滴进入储粉室,进而侵染珠心,严重时导致珠心褐腐、萎缩,雌球花脱落[5],表明授粉期是珠心这一核心部位面临病原侵染风险的关键时期[9]。完成授粉后,雌球花需约24 d发育,使假种皮完全包被裸露珠孔[9],此后进入长达约11个月的缓生期,直至次年4月僵果病症显现[1]。鉴于授粉期是珠心可被直接侵染的唯一阶段,且僵果的内部特征是珠心褐化、皱缩,由此推测,授粉期的病菌侵染及后续的潜伏性发展可能是导致香榧僵果的关键诱因。然而,在缓生期内,花期定殖的枝孢属等病原菌的动态变化及如何导致珠心褐化萎缩尚不清楚。因此,系统分析从缓生期至病症显现期香榧幼果珠心中的病原菌动态,对明确导致僵果的主要致病菌及致病机制至关重要。
组织分离法是果实病原菌鉴定的经典方法。通过病原菌分离纯化,结合形态学(如菌落特征)和分子生物学(如ITS、act、tef1多基因位点)分析,可精准鉴定病原菌种类[9−11]。研究表明:枝孢属包含多个致病种,包括枝状枝孢菌C. cladosporioides、极细枝孢菌C. tenuissimum等[12−15]。此外,病原菌生物学特性是研究其生长条件、预测流行趋势以及评估环境与宿主适应性的重要基础。这些研究结果可为制定有效的防控策略提供理论依据[14−15]。
在过去几十年,香榧种植面积呈现指数型增长,但这种扩张主要依赖于毁坏现有林分,并将其转变为结构单一的人工林,因此,现有的香榧多以纯林形式存在,且栽培品种较为单一,导致其在面对病原菌侵袭时更为脆弱,容易受到病害影响。此外,从香榧缓生期(9月至翌年4月)至病症发生期(翌年4月至5月)历经8个多月,期间环境温度、光照时长等因子均发生了剧烈变化,表明病原菌需适应剧烈变化的环境条件才能完成侵染过程。本研究旨在明确导致香榧僵果形成的优势病原真菌,解析其从缓生期至显症期的动态,并探究其生物学特性,为致病机制研究和防控策略制定提供依据。
-
试验地点位于浙江省杭州市临安区太湖源镇潘母岗香榧基地(30°10′N,119°22′E)。该香榧林地于2012年采用“2+1”嫁接苗(砧木为2年生榧树T. grandis,穗条为1年生‘细榧’‘Xi Fei’)造林,2016年开始结实,林分密度为500株·hm−2。香榧果实发育成熟需历时17个月,其正常果实和僵果的主要外观区别在于果实是否突破种鳞,因此,为精确界定果实发育过程,本研究以距香榧果实突破种鳞的时间(D)作为记录发育进程的指标,突破种鳞当天记为D=0。
本研究于2023年9月,选取15株生长状态和树冠形态较为一致的香榧树,平均地径和树高分别为10.2 cm和2.0 m。每5株树为1个重复,共设3个重复。参照历年香榧突破种鳞时间,于2023年9月15日(D≈−210 d)挂牌标记,并自此每间隔20 d采集香榧种实珠心样品。采样时间根据2024年香榧实际突破种鳞日期(4月20日)进行修正,分别在D=−207、−177、−147、−117、−92、−56、−35、0、21 d时采集样品。每次采样时,从每株样本树上采集1簇结果枝(每簇含12~14个果实),每个重复5簇,3个重复共计15簇。样品采回后立即带回实验室,进行后续分离。
-
马铃薯葡萄糖琼脂培养基(PDA)、马铃薯蔗糖琼脂培养基(PSA)、燕麦培养基(OMA)、麦芽汁琼脂培养基(MEA)和合成低营养琼脂(SNA)。
-
采用组织分离法对所采集的样本进行病原菌分离。具体步骤:从每次采样获得的15簇结果枝中,每簇随机选取2个幼果,共30个幼果。去除种鳞后,取出内部小果(带假种皮),用无菌水洗净并风干。随后进行表面消毒:将小果置于体积分数为75%乙醇中浸泡30 s,用无菌水冲洗3次;再转入质量分数为2%次氯酸钠溶液中浸泡3 min,最后无菌水冲洗3次。用无菌滤纸吸干表面水分后,风干备用。最后,用灭菌手术刀沿小果纵切,取内部珠心组织接种至PDA培养基上。每个平板接种3块组织,每个采样点接种10个平板,即每个采样点共接种30块组织。将所有平板置于25 ℃恒温避光培养。待菌丝长出后,用接种针挑取菌落边缘菌丝,在PDA培养基上培养,连续纯化3代。在最后纯化的PDA板上,加入5 mL无菌水,用涂布棒刮取菌丝和孢子制成菌悬液,再与等体积的体积分数为50%甘油混合,保存于−80 ℃冰箱中,用于后续实验。
结合菌落与孢子的形态特征(形态学鉴定)和使用核糖体DNA内转录间隔区(ITS)序列分析(分子鉴定),对所有分离菌株进行初步属级鉴定。各真菌属的分离率和分离频率计算公式[13]:分离率=(同一属的菌株数/鉴定出的菌株总数)×100%;分离频率=(某一属的菌株数/培养出菌落的组织块总数)×100%。
-
基于不同发育时期果实珠心的分离率结果,枝孢属真菌是香榧幼果缓生期和病症显现期的优势菌群。为明确其致病性,本研究采用离体接种法,对5种主要枝孢属真菌(TGZX1、TGZX2、TGZX3、TGZX4、TGZX5)进行科赫法则验证。具体步骤如下:①枝孢属分生孢子悬浮液的制备。分别制备5种枝孢属的代表菌株(TGZX1-1、TGZX2-1、TGZX3-1、TGZX4-1、TGZX5-1)的分生孢子悬浮液。具体方法:刮取PDA平板上培养7 d的菌落,用无菌水悬浮后,经纱布过滤并离心,沉淀用无菌水重悬,最后用血球计数板将比例调整至1×106个·mL−1。同时,将等体积的上述5种悬浮液混合,配制成总孢子比例为1×106个·mL−1的混合孢子悬浮液(MIX,每种孢子的比例为2 × 105个·mL−1)。②采用分生孢子悬浮液进行离体接种。前期观察表明,缓生期(D=−207~−117 d)的果实珠心组织尚未褐变,因此,选取更早期的健康果实(D=−230 d)作为接种对象。采集21个结果枝组(每个枝组约含3簇结果枝),依次用体积分数为75%乙醇浸泡30 s、质量分数为2%次氯酸钠溶液浸泡5 min进行表面消毒,随后用无菌水冲洗3次,风干备用。③使用1 mL注射器从香榧幼果顶部注入10 μL单一或混合孢子悬浮液,并以注射等量无菌水作为对照(ck)。每个菌种设置3个重复,每个重复包含3个结果枝组(共9个结果枝,108~126个果实)。接种后的结果枝组置于锥形瓶中,在25 ℃恒温培养箱中光暗交替培养并保持湿度。接种7 d后,通过体视荧光显微镜观察珠心组织发病情况。每个处理随机选取15个接种果实,利用ImageJ软件测量疾病面积与珠心组织面积,计算病害严重度=(病斑面积/珠心组织面积)×100%。同时,从典型病斑组织重新分离病原菌,纯化后观察其菌落和孢子形态特征,并与原接种菌株进行比对。
-
①形态学鉴定。将纯化后的分离菌株接种在PDA平板上25 ℃黑暗培养7 d,观察菌落特征。在荧光显微镜(OLYMPUS BX53)下观察记录各菌株分生孢子的形态特征,并测量分生孢子大小。按BENSCH等[11]的方法进行形态鉴定。②分子生物学鉴定。EF-728F(5′-CATCGAGAAGTTCGAGAAGG-3′)/EF-986R (5′-TACTTGAAGGAACCCTTAC-3′)、ACT-512F (5′-ATGTGCAAGGCCGGTTTCGC-3′)/ACT-512R (5′-TACGAGTCCTTCTGGCCCAT-3′)分别扩增菌株的翻译延伸因子 (tef1)和肌动蛋白 (act)基因片段,同时结合ITS rDNA区域(内转录间隔区)[16−17]。扩增产物送至杭州有康生物技术有限公司进行测序。获得的菌株序列在美国生物技术信息中心(NCBI)的GenBank数据库 (https://www.ncbi.nlm.nih.gov/)中进行比对,将相似性较高的序列和模式菌株以FASTA的格式下载,相关序列见表1。以Cercospora beticola作为外群,使用MEGA 11.0软件对序列进行比对修剪,并使用PhyloSuite v 1.2.3软件对待测菌株和模式菌株ITS、tef1和act的序列进行最大似然法(ML)和贝叶斯推断(BI)系统发育树分析,确定菌株的具体分类地位。
表 1 系统发育分析所用的菌株和基因序列
Table 1. Strains and gene sequences used for phylogenetic analysis
病原菌 菌株 Genbank 登录号 ITS tef1 act Cercospora beticola CBS 116456 *AY840527 AY840494 AY840458 Cladosporium cladosporioides CBS 101367 HM148002 HM148243 HM148489 Cladosporium cladosporioides CBS 112388 *HM148003 HM148244 HM148490 Cladosporium cladosporioides CBS 113738 HM148004 HM148245 HM148491 Cladosporium funiculosum CBS 122129 HM148094 HM148338 HM148583 Cladosporium funiculosum CBS 122128 *HM148093 HM148337 HM148582 Cladosporium funiculosum CPC 22247 MF472980 MF473407 MF473830 Cladosporium guizhouense GUCC 401.8* ON334728 ON383470 ON383338 Cladosporium guizhouense GUCC 21227.4 OP852663 OP859048 OP863100 Cladosporium maltirimosum SFC20230103-M51* OQ186147 OQ185155 OQ185195 Cladosporium maltirimosum SFC20230103-M52 OQ186148 OQ185156 OQ185196 Cladosporium oxysporum CBS 125991 *HM148118 HM148362 HM148607 Cladosporium pseudocladosporioides CBS 117134 HM148156 HM148400 HM148645 Cladosporium pseudocladosporioides CBS 125993 *HM148158 HM148402 HM148647 Cladosporium rectoides CBS 125994 *HM148193 HM148438 HM148683 Cladosporium rectoides CBS 126357 HM148194 HM148439 HM148684 Cladosporium scabrellum CBS 126358 *HM148195 HM148440 HM148685 Cladosporium subuliforme CBS 126500 *HM148196 HM148441 HM148686 Cladosporium subuliforme DTO 130-H8 KP701938 KP701815 KP702060 Cladosporium tenuissimum CBS 125995 *HM148197 HM148442 HM148687 Cladosporium tenuissimum CBS 262.80 HM148201 HM148446 HM148691 Cladosporium tenuissimum CPC 14196 HM148218 HM148463 HM148708 Cladosporium varians CBS 126361 HM148223 HM148469 HM148714 Cladosporium varians CBS 126362 *HM148224 HM148470 HM148715 说明:*为模式菌株。 -
将培养7 d的7 mm病原菌菌饼接种在PDA平板中央,分别置于5、10、15、20、25、30和35 ℃的培养箱中黑暗培养7 d。随后采用十字交叉法使用钢直尺测量菌落直径,并观察病原菌在培养基上的菌落特征。采用相同接种方法将菌饼接种至PDA培养基,分别置于全光照(光照24 h)、光暗交替(光照和黑暗各12 h)和完全黑暗(光照0 h)等3种光照条件下培养7 d (28 ℃),以分析病原菌的最适光照条件。此外,将菌饼分别接种至PSA、PDA、SNA、OMA和MEA培养基,在25 ℃黑暗条件下培养7 d,通过十字交叉法测量菌落直径,筛选最适病原菌生长的培养基。以察氏培养基为基础培养基,分别用等摩尔碳质量的可溶性淀粉、乳糖、麦芽糖、甘露醇、山梨醇、葡萄糖、蔗糖和果糖替代其中的蔗糖,并用等摩尔氮质量的氯化铵、牛肉浸粉、硫酸铵、硝酸钠、甘氨酸、胰蛋白胨、丙氨酸和酵母提取物替代其中的硝酸钠。同时设置无碳无氮源作为对照,在28 ℃黑暗条件下培养7 d后,采用十字交叉法测量菌落直径并观察菌落特征。
-
采用Excel 2021和SPSS 27.0软件进行统计分析。利用PhyloSuite_v1.2.3进行系统发育树分析。图表中数据以平均值±标准误表示,并利用GraphPad Prism 8.0绘图。
-
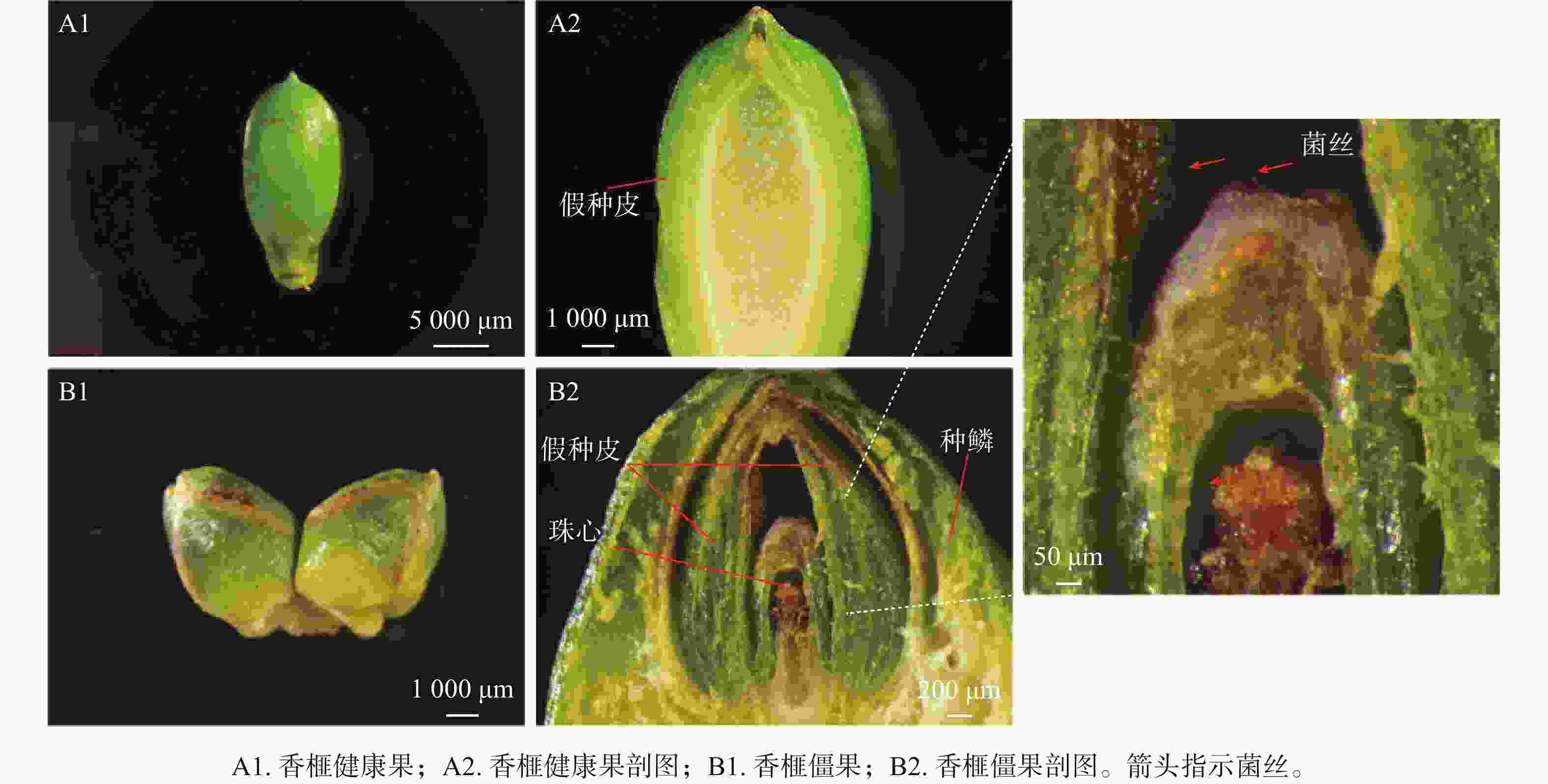
香榧膨大果的假种皮正常突破种鳞(图1A1),珠心组织则正常生长发育,内部呈凝胶透明状(图1A2)。香榧僵果的假种皮仍被种鳞包被(图1B1),其珠心顶端则已褐化腐烂,皱缩停止发育(图1B2),在珠孔和珠心出现菌丝。
-
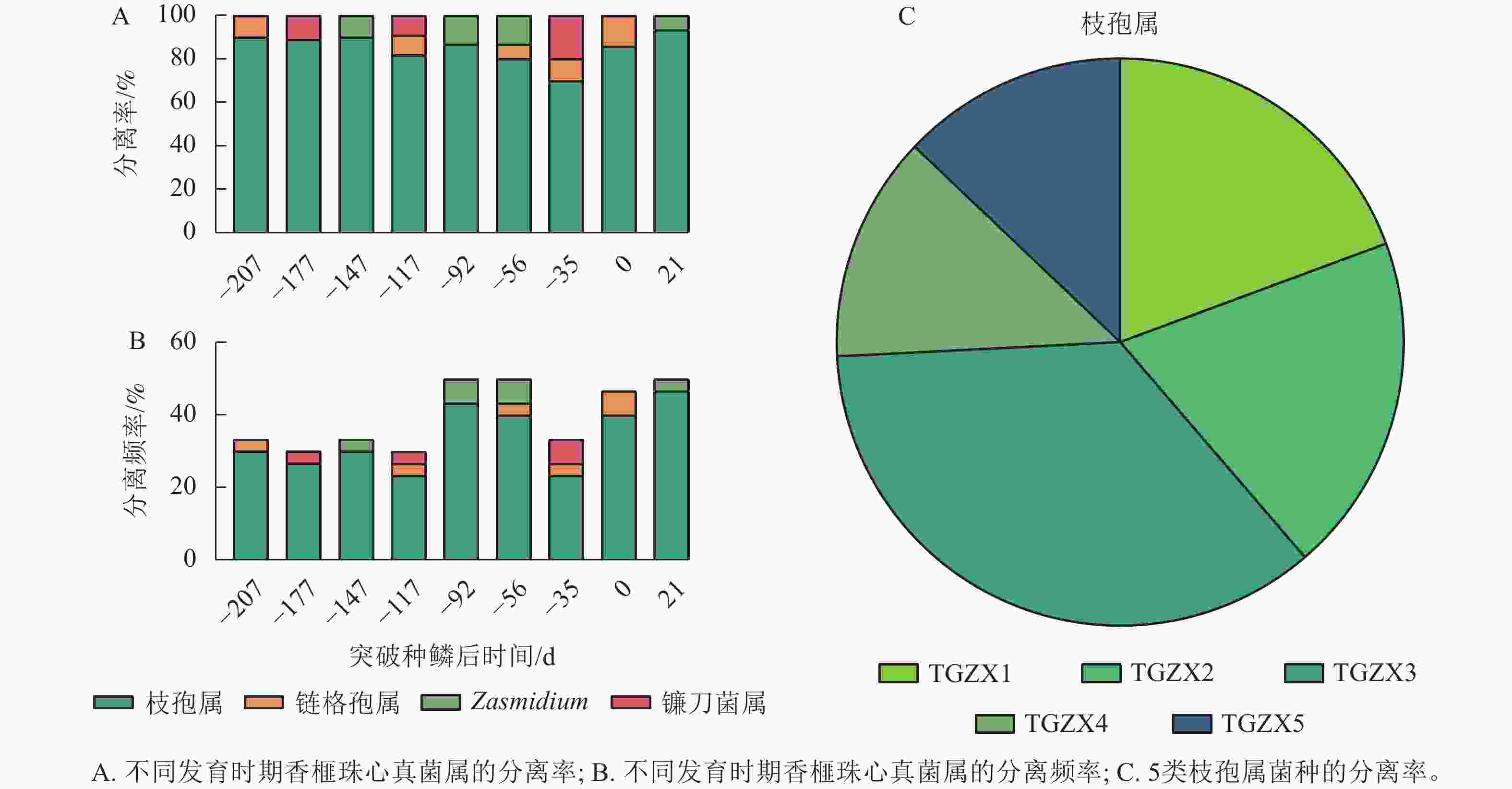
从缓生期(D=−207 d)至僵果病症显现期(D=21 d),采集香榧果实的珠心组织进行病原菌分离,共分离得到109个菌株。根据形态特征,这些菌株可初步分为4种菌属,分别为镰刀菌属Fusarium、链格孢属、枝孢属和 Zasmidium。值得注意的是,分离得到的真菌以枝孢属为主,其分离率在各个时期均在70%以上,分离频率均在20.0%以上,其他3个菌属的分离率很低(图2A~B)。进一步通过形态特征、菌落生长速率等初步将分离得到的枝孢属真菌分为5类,分别命名为TGZX1、TGZX2、TGZX3、TGZX4、TGZX5,其中,TGZX3分离频率最高,为35.5% (图2C)。
-
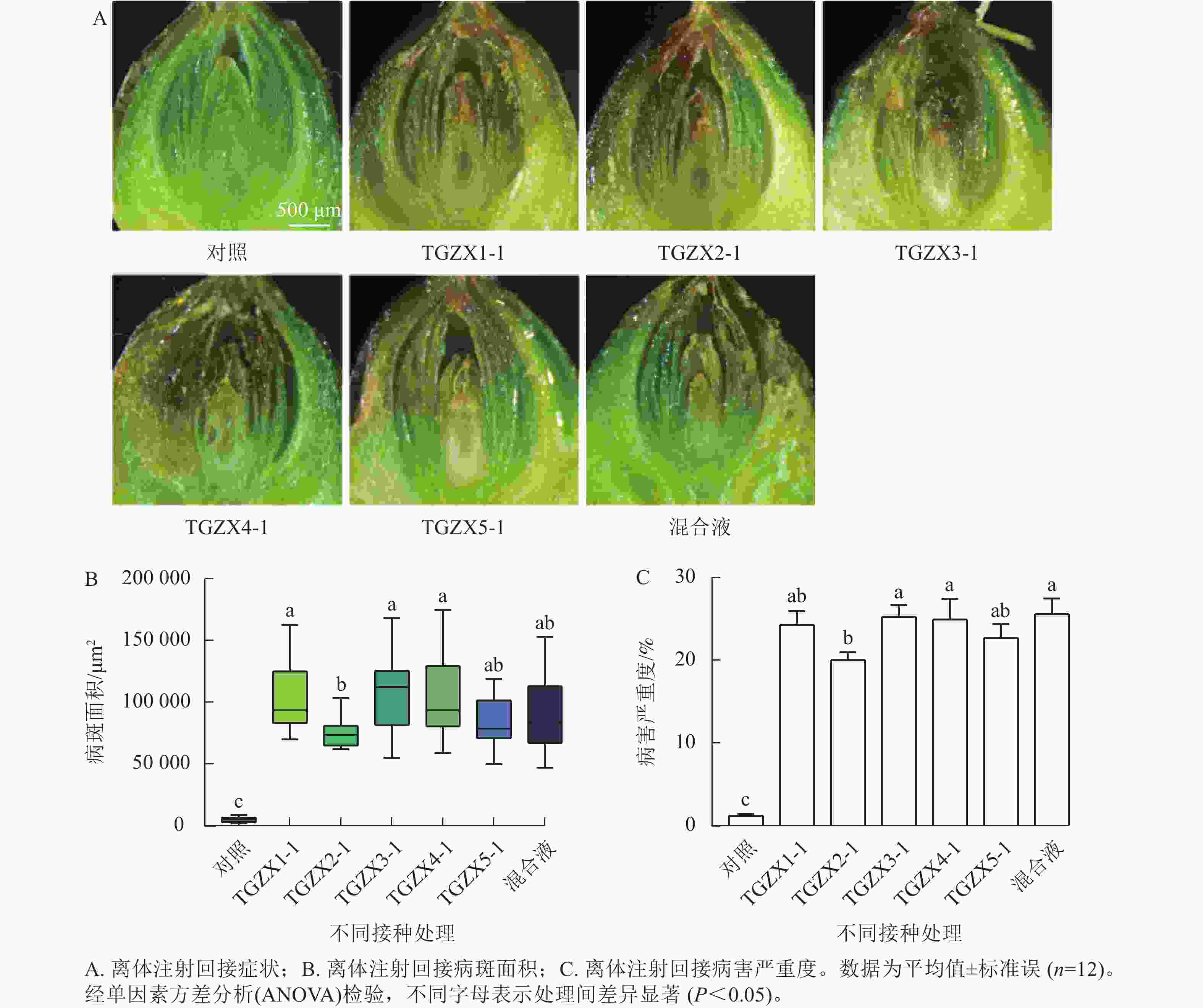
为明确香榧僵果的病原菌,本研究选取在病果中分离率和分离频率最高、关联最密切的5种枝孢属的代表菌株(TGZX1-1、TGZX2-1、TGZX3-1、TGZX4-1、TGZX5-1)进行致病性测定。依据科赫法则,对健康的香榧果实接种其孢子悬浮液(图3)。接种7 d后,发现5种菌及混合菌液回接的果实珠心均出现褐变坏死,发病率100%;病斑面积和病害严重度均显著高于注射无菌水的对照组(P<0.05),表明这5种枝孢属菌对香榧珠心均具有致病性。5种菌株的致病力存在差异,其中,TGZX1-1、TGZX3-1和TGZX4-1回接的病斑面积显著大于TGZX2-1 (P<0.05);TGZX3-1和TGZX4-1回接的病害严重度也显著高于TGZX2-1 (P<0.05)。值得注意的是,采用5种菌株的混合液接种时,其病害严重度显著高于TGZX2-1单独接种(P<0.05),且病斑面积虽与TGZX2-1接种无显著差异,但引发了珠心明显的皱缩现象,此症状与田间观察到的僵果症状最为相似。对照组未出现明显症状。通过对回接病原菌的患病样本进行重新分离培养,均可再次分离鉴定出原接种菌株,从而完成了科赫法则验证。可见,TGZX1-1、TGZX2-1、TGZX3-1、TGZX4-1和TGZX5-1这5种枝孢属真菌均为香榧僵果的病原真菌,能够引起珠心褐变、萎缩坏死,是导致僵果形成的重要病原菌。
-
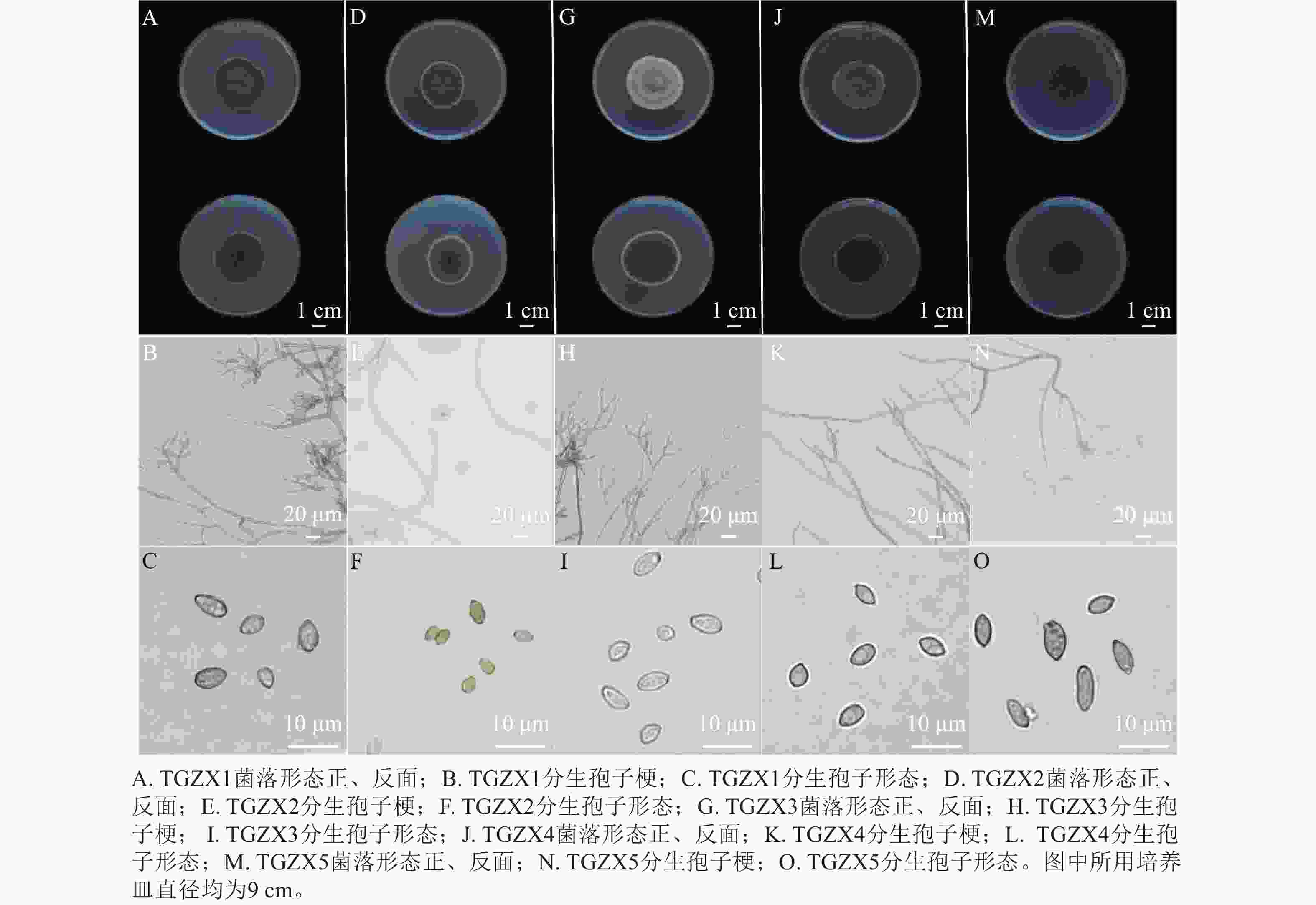
由图4可知:TGZX1菌落呈圆形,菌丝絮状,菌落中间呈灰黑色至深绿色,边缘呈白色,菌落背面呈深黑色。分生孢子梗,具隔膜,透明浅色,直立或弯曲,分枝,大小为76.07~121.74 μm×3.67~4.93 μm (n=10)。分生孢子卵圆形或柠檬形,大小为5.18~8.37 μm×2.68~6.04 μm (n=50),平均为(6.77±0.22) μm× (4.46±0.14) μm (图4A~C)。TGZX2菌落呈圆形,菌落中央灰黑色,外圈呈橄榄绿,边缘为白色,背面呈深黑色,表面有辐射状沟壑,菌丝密集呈絮状。分生孢子梗,具隔膜,透明浅色,细长,直立或弯曲,分枝,大小为29.70~187.35 μm×1.60~4.56 μm (n=10)。分生孢子卵圆形或椭圆形,大小为3.01~5.91 μm×2.11~3.79 μm (n=50),平均为(4.45±0.16) μm× (2.81±0.09) μm (图4D~F)。TGZX3菌落圆形,呈灰白色,气生菌丝密集呈绒毛状,菌落背面呈深橄榄色,边缘白色。分生孢子梗,具隔膜,浅橄榄绿色,直立分枝光滑,大小为42.49~166.12 μm×3.11~4.64 μm (n=10)。分生孢子椭圆形,大小为4.04~7.11 μm×3.03~4.92 μm (n=50),平均为(5.84±0.17) μm× (3.95±0.10) μm (图4G~I)。TGZX4菌落呈橄榄绿,粉末状,菌落背面呈深黑色。分生孢子梗具隔膜,淡棕色,单生或簇生,直立分枝,大小为67.18~119.90 μm×2.82~4.79 μm (n=10)。分生孢子卵圆形或柠檬形,大小为4.32~8.52 μm×2.49~4.71 μm (n=50),平均为(6.29±0.21) μm× (3.77±0.14) μm (图4J~L)。TGZX5菌落呈深绿色,菌落背面深黑色。分生孢子梗具隔膜,透明浅色,直立分枝,大小为32.50~136.51 μm×1.60~3.54 μm (n=10)。分生孢子卵圆形或椭圆形,大小为4.28~10.48 μm×2.41~5.02 μm (n=50),平均为(7.32±0.34) μm× (3.85±0.13) μm (图4M~O)。参考BENSCH等[11]对枝孢属真菌的形态特征描述,初步鉴定TGZX1、TGZX2、TGZX3、TGZX4、TGZX5为枝孢属真菌。
-
为进一步准确鉴定病原菌种类,分别选取5种枝孢属菌TGZX1、TGZX2、TGZX3、TGZX4、TGZX5 各2株代表性菌株基于多位点序列(ITS、tef1和act)进行系统发育分析,以Cercospora beticola CBS
116456 作为外群,利用最大似然法和贝叶斯推断法进行进化树的构建。由图5可知:2株TGZX1代表株与模式菌株Cladosporium funiculosum CBS122128 聚在一枝,具有较高的支持率(96/1.00);2株TGZX2代表株与模式菌株C. oxysporum CBS125991 聚在一枝,具有高支持率(99/1.00);2株TGZX3代表株与模式菌株C. guizhouense GUCC 401.8聚在一枝,具有较高的支持率(97/1.00);2株TGZX4代表株与模式菌株C. tenuissimum CBS125995 聚在一枝,具有较高的支持率(98/0.90);2株TGZX5代表株与模式菌株C. scabrellum CBS126358 聚在一枝,具有较高的支持率(96/1.00)。综上所述,结合形态学与分子生物学鉴定,将10株Cladosporium代表菌株鉴定为5个已知种,分别确定为C. funiculosum、C. oxysporum、C. guizhouense、C. tenuissimum和C. scabrellum。 -
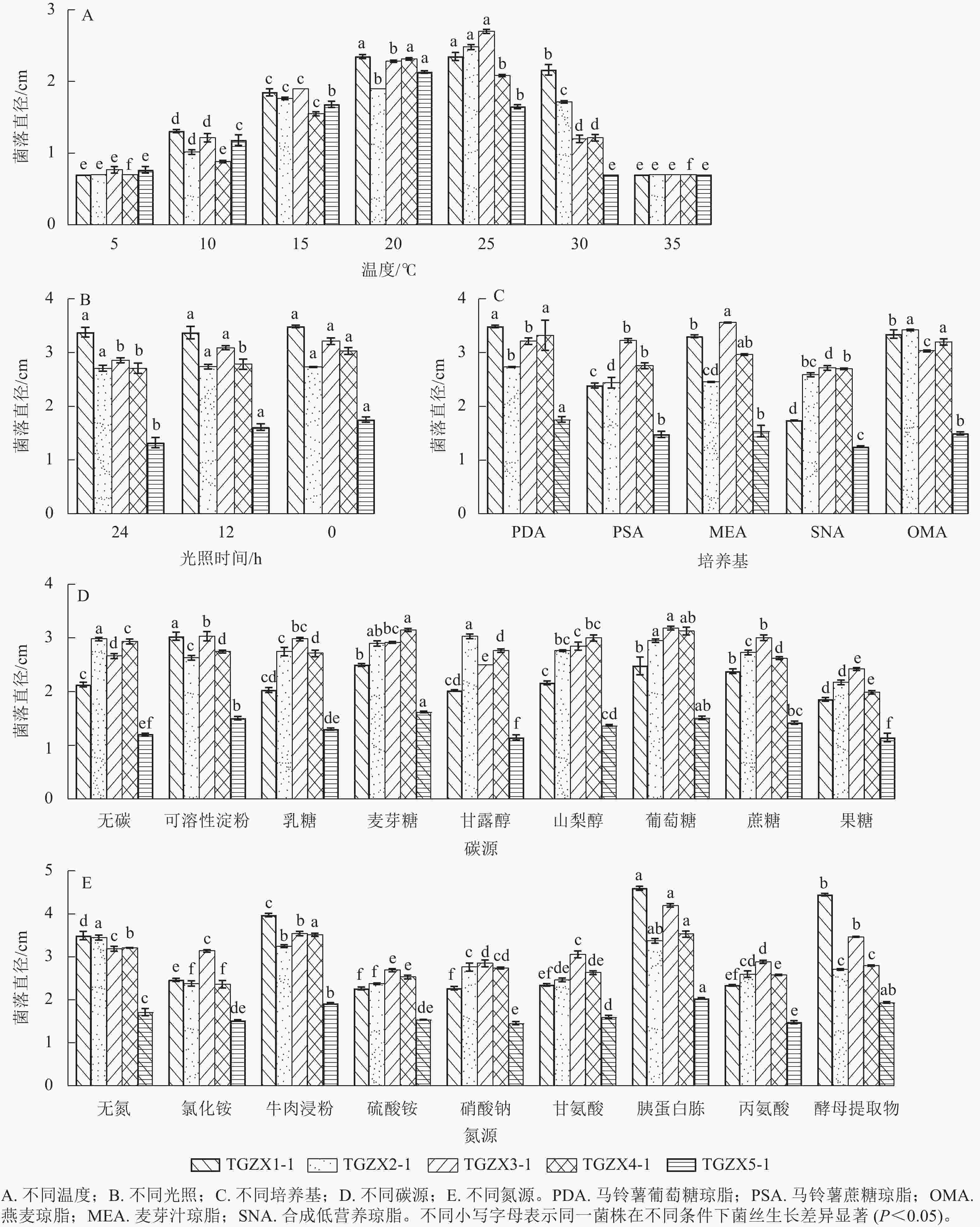
由图6A可知:5种枝孢属真菌的最佳生长温度均为20~25 ℃,其中,TGZX1-1的菌丝适宜在20~25 ℃下生长;TGZX2-1和TGZX3-1的菌丝在25 ℃下生长最快,均显著高于其他温度处理(P<0.05);TGZX4-1和TGZX5-1的菌丝则在20 ℃下生长最快,均显著高于其他温度处理(P<0.05)。根据不同光照条件下5种菌丝生长的差异(图6B),总体上可分为3种类型:①TGZX1-1和TGZX2-1为光照不敏感型,其菌丝生长不受光照影响;②TGZX3-1和TGZX5-1为厌光型,其菌丝在光暗交替(光照和黑暗各12 h)和全黑暗(光照0 h)条件下的生长速度显著高于全光照(光照24 h)条件(P<0.05);③TGZX4-1为严格厌光型,其菌丝在全黑暗(光照0 h)条件下生长最快(P<0.05)。5种菌株在供试培养基上均可生长,但其最适培养基存在差异(图6C),其中,TGZX1-1和TGZX5-1的最适培养基均为PDA培养基,其菌丝生长速度显著快于其他培养基(P<0.05);TGZX2-1和TGZX3-1分别在OMA和MEA培养基上生长最佳,且显著优于其他培养基;TGZX4-1对培养基的适应性较广,在PDA、MEA和OMA培养基上均生长良好,且无显著差异。不同菌种在碳源偏好上表现出差异,但麦芽糖和葡萄糖是多数菌种的良好碳源(图6D),其中,TGZX1-1和TGZX3-1菌丝生长的最适碳源分别为可溶性淀粉和葡萄糖,其菌丝生长速度均显著高于其他碳源培养基(P<0.05);TGZX2-1在甘露醇、麦芽糖和葡萄糖多种碳源上生长良好;TGZX4-1和TGZX5-1均在麦芽糖和葡萄糖培养基上生长最佳,显著优于其他碳源培养基(P<0.05)。胰蛋白胨是5株菌株的良好氮源(6E),其中,TGZX1-1、TGZX3-1、TGZX4-1和TGZX5-1的最适氮源均为胰蛋白胨,显著优于其他氮源培养基(P<0.05)。与其他菌株不同,TGZX2-1在无氮源培养基中的生长情况与含胰蛋白胨的培养基相当,表现出独特的氮素利用特性。
-
果实的主要病原菌会因不同发育时期而发生改变[6, 18]。本研究结果显示:从缓生期至僵果发病期(D=−207~21 d),枝孢属始终是香榧幼果珠心中的优势菌属。由于枝孢属真菌种类丰富,且部分种在形态上极其相似,难以分辨,通常需结合分子生物学手段才能确认具体种类[11−13]。本研究基于act和tef1基因序列构建多基因系统发育树,鉴定出5种枝孢属真菌,包括绳状枝孢菌TGZX1-1、尖孢枝孢菌TGZX2-1、贵州枝孢菌TGZX3-1、极细枝孢菌TGZX4-1和微糙枝孢菌TGZX5-1。其中,贵州枝孢菌TGZX3-1的分离率最高。研究表明:这5种枝孢属真菌可导致多种植物病害,例如,尖孢枝孢菌能引起辣椒Capsicum annuum叶片和果实病斑发霉[19]及尼泊尔李Prunus nepalensis叶斑病[20];贵州枝孢菌可导致蓝莓Eucommia ulmoides幼果发霉腐烂[21];极细枝孢菌与绣球Hydrangea macrophylla花叶斑病[22]和醋栗Physalis pruinosa黑斑病[23]相关;微糙枝孢菌可引起羊肚菌Morchella importuna子实体腐烂[24]。为排除外界环境干扰,本研究采用离体接种法测定致病性。结果显示:5类枝孢属真菌代表株及混合株的孢子液均可诱发香榧珠心褐化。其中,接种5种菌株混合孢子液的香榧珠心表现出明显皱缩褐化的表型,与香榧僵果的珠心症状最为相似,表明香榧僵果是由多种枝孢属真菌复合侵染所致。本研究还发现:在漫长的缓生期中,除了枝孢属优势菌外,还分离到其他3个菌属(链格孢属、镰刀菌属和Zasmidium)。研究表明:这些菌属同样具有致病性,如链格孢属菌A. alternata和A. arborescens可引起柑橘Citrus落果[25];尖孢镰刀菌Fusarium oxysporum和链格孢菌会导致核桃Juglans regia顶端坏死[26];Z. mangiferae则能引发芒果Mangifera indica叶锈病[27]。本研究仅明确了优势病原菌枝孢属对香榧珠心的致病性,后续研究需进一步验证不同菌属之间是否存在协同互作关系。
枝孢属真菌属于弱寄生菌或腐生菌,需通过自然开口或伤口侵入宿主[14, 16]。本研究结果显示:香榧僵果症状仅表现为内部珠心皱缩褐化,假种皮未见破损病征,表明病害并非由外部侵入,而是从内部开始发病。前人研究表明:在授粉等待期,香榧雌球花的珠心因珠孔裸露而易受枝孢属侵染,导致雌球花黄化、皱缩和脱落[9]。值得注意的是,本研究中从缓生期香榧幼果珠心分离出的优势菌属(枝孢属)及其他常见菌属(链格孢菌和Zasmidium),与叶浩杰[9]在香榧雌球花中分离出的菌属高度相似,表明花期可能是一个重要的共同侵染窗口期。因其珠孔裸露,授粉期可能是珠心受外部病原菌侵染的关键时期,结合僵果珠心具有顶端褐化、皱缩的特征,推测枝孢属菌对香榧僵果的侵染过程可能始于花期,部分病原菌在珠心中长期存活,直至条件适宜时引发症状。这与苹果霉心病相似,其实质是病原菌在花期侵染心室[7]。此外,戴蓬博[8]通过绿色荧光蛋白(GFP)标记菌株证实花期受粉时红聚端孢Trichothecium roseum侵染会导致苹果霉心病的发生。本研究已证实枝孢属菌从授粉期至缓生期持续存在于香榧幼果中,这在一定程度上可说明枝孢属真菌侵染具有连续性。后续研究可结合荧光标记菌株进一步明确具体的侵染与潜伏时期。
温度、光照和养分等环境条件对病原菌的侵染具有重要影响[14−15],明确病原菌的生物学特性对探索病原菌致病机制具有关键意义[28]。研究表明:枝孢属真菌对温度响应存在种间差异。例如,尖孢枝孢菌菌丝的最适生长温度为20~25 ℃[19],而极细枝孢菌菌丝的适宜生长温度为20 ℃[29]。本研究结果与之相符,5种枝孢属菌丝的适宜生长温度均为20~25 ℃,3—5月气温的快速上升(12.8~22.4 ℃)为幼果中枝孢属的定殖提供了适宜的环境温度。此外,研究发现光照对TGZX1-1和TGZX2-1菌丝生长无显著影响,而其他3种菌株(TGZX3-1、TGZX5-1和TGZX4-1)在半光照和黑暗条件下的菌丝生长优于全光照条件,表明这5种枝孢属真菌均能在黑暗条件下正常生长,这与香榧珠孔等组织长期被假种皮包被形成的低光照微环境高度契合,进一步解释了病原菌在宿主体内的定殖优势。
碳源和氮源等养分是影响病原菌菌丝生长和侵染能力的关键因素[30−31]。研究表明:尖孢枝孢菌菌丝生长的最适碳源和氮源分别为山梨醇和麦芽浸膏,以V8果汁为菌丝最适宜生长的培养基[19]。此外,研究发现极细枝孢菌菌丝生长的最适碳源为葡萄糖和木糖,最适氮源为天门冬素和蛋白胨[29]。前人研究表明:枝孢属真菌具有丰富的碳水化合物酶和植物细胞壁降解酶,可增强对碳水化合物的降解和利用的能力[32]。香榧雌球花及果实内部组织均含有丰富的淀粉和葡萄糖等碳水化合物[33−34]。本研究结果显示:TGZX1-1、TGZX2-1、TGZX3-1、TGZX4-1和TGZX5-1的最适碳源分别为可溶性淀粉、甘露醇、葡萄糖、麦芽糖和麦芽糖,而5种枝孢属真菌的最适氮源均为胰蛋白胨,表明香榧幼果内部组织可为枝孢属真菌提供充足的碳源,从而增强其侵染和定殖能力。
由于香榧雌球花裸露的珠孔在授粉期易受枝孢属真菌侵染,因此,应将传统保果期的防治重心前移至授粉期,未来需评估内吸性杀菌剂或针对枝孢属真菌的生防菌剂在花期的精准防控效果。此外,病原菌适宜在黑暗湿润环境中生长,可通过合理修剪以增强通风透光。
-
引起香榧僵果病害的病原菌为枝孢属菌,包括绳状枝孢菌、尖孢枝孢菌、贵州枝孢菌、极细枝孢菌和微糙枝孢菌;这些枝孢属真菌的最适宜生长温度为20~25 ℃,能够在黑暗条件下生长,它们的最佳碳源分别为可溶性淀粉、甘露醇、葡萄糖、麦芽糖和麦芽糖,最佳氮源为胰蛋白胨。
Isolation, identification and biological characteristics of major pathogenic fungi in stiff fruits of Torreya grandis
-
摘要:
目的 每年4月,香榧Torreya grandis ‘Merrillii’结果枝上有89%的果实为僵果,其假种皮未突破种鳞,内部珠心褐化萎缩。目前关于香榧僵果形成的机制仍不清楚。研究香榧僵果的发生机制,可为制定有效的防治措施提供理论依据。 方法 以距香榧果实突破种鳞的时间(D)作为记录发育进程指标,突破种鳞当天记为D=0,隔一定时间采集香榧种实珠心样品,采用组织分离法对不同发育时期的香榧果实珠心组织进行病原菌分离和纯化,结合形态学、多基因联合系统发育分析及科赫法则验证,鉴定香榧僵果的优势致病菌种类,并分析其生物学特性。 结果 ①在D为−207~21 d时,从香榧果实珠心组织分离出的病原菌中,枝孢属Cladosporium的分离率和分离频率均最高。根据菌落形态,这些枝孢属真菌可分为5种类型。接种这5种枝孢属真菌的代表菌株及混合菌株的孢子液均可诱发香榧珠心褐化,其中回接混合菌株孢子液后的香榧珠心褐化表型与僵果的褐化珠心最为相似。②通过形态学鉴定及多基因序列分析,鉴定出5种主要枝孢属致病菌株分别为绳状枝孢菌C. funiculosum TGZX1、尖孢枝孢菌C. oxysporum TGZX2、贵州枝孢菌C. guizhouense TGZX3、极细枝孢菌C. tenuissimum TGZX4和微糙枝孢菌C. scabrellum TGZX5。③5种枝孢属真菌生长的最适温度均为20~25 ℃。TGZX1-1、TGZX2-1、TGZX3-1、TGZX4-1和TGZX5-1的最适碳源分别为可溶性淀粉、甘露醇、葡萄糖、麦芽糖和麦芽糖,最适氮源均为胰蛋白胨,且这些菌株均能在黑暗条件下生长。 结论 香榧僵果是由5种枝孢属真菌复合侵染所致。这与雌球花在授粉期易受枝孢属真菌侵染密切相关。在香榧雌花期采取防控措施是有效防治僵果形成的关键。图6表1参34 Abstract:Objective In April each year, 89% of the fruits on the bearing branches of Torreya grandis ‘Merrillii’ are stiff fruits characterized by unruptured arils and internal nucellus browning and shrinking. The aim of this study is to investigate the occurrence mechanism of stiff fruits, so as to provide a theoretical basis for developing effective prevention and control measures. Method The number of days after seed protrusion (D) was used as an indicator to record the developmental progression of T. grandis ‘Merrillii’ fruits, with the day of protrusion recorded as D=0. Nucellar tissue samples were collected at regular intervals. The tissue separation method was employed to isolate and purify pathogenic bacteria from the nucellar tissues at various developmental stages. By combining morphological analysis, multi-gene joint phylogenetic analysis and Koch’s postulates verification, the dominant pathogenic bacteria species of stiff fruits were identified and their biological characteristics were analyzed. Result (1) When D was within the range of −207 to 21 days, Cladosporium exhibited the highest isolation rate and frequency among the pathogens isolated from the nucellar tissues. Based on colony morphology, these Cladosporium isolates were classified into 5 types. Vaccination with representative strains and mixed strains of these 5 species of bacteria consistently induced browning of the T. grandis ‘Merrillii’ nucellus. The browning phenotype after inoculation with the mixed spore suspension was similar to that of stiff fruits. (2) Through morphological identification and multi-gene sequence analysis, the 5 major pathogenic strains of Cladosporium were identified as C. funiculosum TGZX1, C. oxysporum TGZX2, C. guizhouense TGZX3, C. tenuissimum TGZX4, and C. scabrellum TGZX5. (3) The optimal growth temperature for the 5 species of Cladosporium was 20−25 ℃. The optimal carbon sources for TGZX1-1, TGZX2-1, TGZX3-1, TGZX4-1, and TGZX5-1 were soluble starch, mannitol, glucose, maltose, and maltose, respectively. The optimal nitrogen source for all strains was tryptone. Moreover, these strains grew well under dark conditions. Conclusion The stiff fruits of T. grandis ‘Merrillii’ are caused by the combined infection of 5 species of Cladosporium, which is closely linked to the susceptibility of the female cone to Cladosporium infection during pollination. Therefore, the key to effectively preventing the formation of stiff fruits is to take control measures during the female flowering stage of T. grandis ‘Merrillii’. [Ch, 6 fig. 1 tab. 34 ref.] -
Key words:
- Torreya grandis ‘Merrillii’ /
- stiff fruit /
- Cladosporium /
- biological characteristics
-
表 1 系统发育分析所用的菌株和基因序列
Table 1. Strains and gene sequences used for phylogenetic analysis
病原菌 菌株 Genbank 登录号 ITS tef1 act Cercospora beticola CBS 116456 *AY840527 AY840494 AY840458 Cladosporium cladosporioides CBS 101367 HM148002 HM148243 HM148489 Cladosporium cladosporioides CBS 112388 *HM148003 HM148244 HM148490 Cladosporium cladosporioides CBS 113738 HM148004 HM148245 HM148491 Cladosporium funiculosum CBS 122129 HM148094 HM148338 HM148583 Cladosporium funiculosum CBS 122128 *HM148093 HM148337 HM148582 Cladosporium funiculosum CPC 22247 MF472980 MF473407 MF473830 Cladosporium guizhouense GUCC 401.8* ON334728 ON383470 ON383338 Cladosporium guizhouense GUCC 21227.4 OP852663 OP859048 OP863100 Cladosporium maltirimosum SFC20230103-M51* OQ186147 OQ185155 OQ185195 Cladosporium maltirimosum SFC20230103-M52 OQ186148 OQ185156 OQ185196 Cladosporium oxysporum CBS 125991 *HM148118 HM148362 HM148607 Cladosporium pseudocladosporioides CBS 117134 HM148156 HM148400 HM148645 Cladosporium pseudocladosporioides CBS 125993 *HM148158 HM148402 HM148647 Cladosporium rectoides CBS 125994 *HM148193 HM148438 HM148683 Cladosporium rectoides CBS 126357 HM148194 HM148439 HM148684 Cladosporium scabrellum CBS 126358 *HM148195 HM148440 HM148685 Cladosporium subuliforme CBS 126500 *HM148196 HM148441 HM148686 Cladosporium subuliforme DTO 130-H8 KP701938 KP701815 KP702060 Cladosporium tenuissimum CBS 125995 *HM148197 HM148442 HM148687 Cladosporium tenuissimum CBS 262.80 HM148201 HM148446 HM148691 Cladosporium tenuissimum CPC 14196 HM148218 HM148463 HM148708 Cladosporium varians CBS 126361 HM148223 HM148469 HM148714 Cladosporium varians CBS 126362 *HM148224 HM148470 HM148715 说明:*为模式菌株。 -
[1] 黎章矩, 戴文圣. 中国香榧[M]. 北京: 科学出版社, 2007. LI Zhangju, DAI Wensheng. Torreya grandis of China[M]. Beijing: Science Press, 2007. [2] 王哲, 吴诗涵, 索金伟, 等. 香榧僵果调查与解剖学观察[J]. 浙江农业科学, 2021, 62(10): 1950−1952, 2026. WANG Zhe, WU Shihan, SUO Jinwei, et al. Investigation and anatomic observation of Torreya grandis aborted seeds[J]. Journal of Zhejiang Agricultural Sciences, 2021, 62(10): 1950−1952, 2026. DOI: 10.16178/j.issn.0528-9017.20211016. [3] 成豪, 吴家胜, 马爽, 等. 树形调整对香榧成花和坐果的影响[J]. 林业科学, 2023, 59(11): 49−58. CHENG Hao, WU Jiasheng, MA Shuang, et al. Effects of tree shape adjustment on flower formation and fruit setting of Torreya grandis cv. Merrillii[J]. Scientia Silvae Sinicae, 2023, 59(11): 49−58. DOI: 10.11707/j.1001-7488.LYKX20230104. [4] 孙前军. 北京平谷区桃细菌性黑斑病与炭疽病病原鉴定及生防菌初筛[D]. 南阳: 南阳师范学院, 2024. SUN Qianjun. Identification of Peach Bacterial Black Spot and Anthracnose Pathogens in Pinggu District, Beijing, and Initial Screening of Biocontrol Fungi [D]. Nanyang: Nanyang Normal Unisersity, 2024. DOI: 10.27850/d.cnki.gnysf.2024.000009. [5] 王伟博, 李松刚, 胡美姣, 等. 无核荔枝僵果病的病原菌鉴定、入侵途径及快速检测技术[J]. 热带作物学报, 2024, 45(3): 602−608. WANG Weibo, LI Songgang, HU Meijiao, et al. Identification, invasion pathway and rapid detection technology of new mummy fruit pathogen of seedless Litchi[J]. Chinese Journal of Tropical Crops, 2024, 45(3): 602−608. DOI: 10.3969/j.issn.1000-2561.2024.03.017. [6] 王冬, 梁鹏, 刘晓菊. 苹果花腐病发病规律及防治措施[J]. 河北果树, 2009(1): 36. WANG Dong, LIANG Peng, LIU Xiaoju. Occurrence regularity and control measures of apple flower rot[J]. Hebei Fruits, 2009(1): 36. DOI: 10.3969/j.issn.1006-9402.2009.01.022. [7] 张强. 富士苹果霉心病病原菌侵染特性研究[D]. 杨凌: 西北农林科技大学, 2012. ZHANG Qiang. Infection Characteristics of Pathogens Associated with Moldy Core of Fuji Apple[D]. Yangling: Northwest A&F University, 2012. [8] 戴蓬博. 粉红聚端孢引致富士苹果心腐病的侵染特征及致病机制[D]. 杨凌: 西北农林科技大学, 2019. DAI Pengbo. Infection Characteristics and Pathogenic Mechanisms of Apple Core Rot Caused by Trichothecium Roseum[D]. Yangling: Northwest A&F University, 2019. [9] 叶浩杰. 香榧雌球花花腐病主要病原菌鉴定及其发生规律初探[D]. 杭州: 浙江农林大学, 2024. Ye Haojie. Identification and Occurrence Regularity of the Main Pathogen for Female Cone Blight in Torreya grandis [D]. Hangzhou: Zhejiang A&F University, 2024. [10] ZHANG Yuan, NAN Mina, XUE Huali. Isolating, identifying, and analyzing the biological characteristics of pathogens causing postharvest disease in fresh Radix Astragali[J]. Horticulturae, 2023, 9(9): 1019. DOI: 10.3390/horticulturae9091019. [11] BENSCH K, GROENEWALD J Z, MEIJER M, et al. Cladosporium species in indoor environments[J]. Studies in Mycology, 2018, 89: 177−301. DOI:10.1016/j.simyco.2018.03.002. [12] PRASANNATH K, SHIVAS R G, GALEA V J, et al. Novel Botrytis and Cladosporium species associated with flower diseases of Macadamia in Australia[J]. Journal of Fungi, 2021, 7(11): 898. DOI: 10.3390/jof7110898. [13] PRASANNATH K, GALEA V J, AKINSANMI O A. Diversity and pathogenicity of species of Botrytis, Cladosporium, Neopestalotiopsis and Pestalotiopsis causing flower diseases of Macadamia in Australia[J]. Plant Pathology, 2023, 72(5): 881−899. DOI: 10.1111/ppa.13707. [14] 陈思颖, 焦瑞莲, 李志强, 等. 新疆葡萄枝孢果腐病病原菌的鉴定及生物学特性[J]. 植物保护, 2022, 48(4): 180−187, 202. CHEN Siying, JIAO Ruilian, LI Zhiqiang, et al. Identification and biological characteristics of Cladosporium pathogens causing grape fruits rot in Xinjiang[J]. Plant Protection, 2022, 48(4): 180−187, 202. DOI: 10.16688/j.zwbh.2021243. [15] 龙安琪, 朱泽, 李强, 等. 浙贝母芽枝霉斑病病原菌鉴定、生物学特性及生物药剂防治效果研究[J]. 植物病理学报, 2023, 53(6): 1047−1055. LONG Anqi, ZHU Ze, LI Qiang, et al. Identification biological characteristics, and inhibition efficacy of plant-derived antifungal agents of pathogen Cladosporium spp. causing mildew spot of Fritillaria thunbergii[J]. Acta Phytopathologica Sinica, 2023, 53(6): 1047−1055. DOI: 10.13926/j.cnki.apps.000838. [16] BENSCH K, BRAUN U, GROENEWALD J Z, et al. The genus Cladosporium[J]. Studies in Mycology, 2012, 72: 1−401. DOI: 10.3114/sim0003. [17] CARBONE I, KOHN L M. A method for designing primer sets for speciation studies in filamentous ascomycetes[J]. Mycologia, 1999, 91(3): 553−556. DOI: 10.1080/00275514.1999.12061051. [18] 马文平, 倪志婧, 任贤, 等. ‘玉金香’甜瓜采后真菌病原物鉴定及侵染规律的研究[J]. 北方园艺, 2011(17): 36−40. MA Wenping, NI Zhijing, REN Xian, et al. Study on latent infection pattern and identification of postharvest fungal diseases on ‘Yujinxiang’ melon fruit[J]. Northern Horticulture, 2011(17): 36−40. [19] 黄欣阳. 中国辣椒叶斑病病原学及分子检测研究[D]. 沈阳: 沈阳农业大学, 2013. HUANG Xinyang. The Etiology and Molecular Detection of a Leaf Spot on Pepper in China[D]. Shenyang: Shenyang Agricultural University, 2013. [20] BAISWAR P, CHANDRA S, BAG T K, et al. Cladosporium oxysporum on Prunus nepalensis in India[J]. Australasian Plant Disease Notes, 2011, 6(1): 3−6. DOI: 10.1007/s13314-011-0002-1. [21] WANG Siyao, WANG Yong, LI Yan. Cladosporium spp. (Cladosporiaceae) isolated from Eucommia ulmoides in China[J]. MycoKeys, 2022, 91: 151−168. DOI: 10.3897/mycokeys.91.87841. [22] GU Xin, LIU Wei, JI Kewen, et al. First reports of Cladosporium tenuissimum causing leaf spots on Hydrangea macrophylla in Anhui Province in China[J]. Plant Disease, 2024, 108(5): 1392. DOI: 10.1094/pdis-10-23-2261-pdn. [23] MIYAKE N, TSUKASA M, KOUNO T, et al. First report of sooty spot caused by Cladosporium tenuissimum on mature calyces of Cape gooseberry grown in greenhouse[J]. Journal of General Plant Pathology, 2022, 88(4): 282−284. DOI: 10.1007/s10327-022-01070-9. [24] ZHANG Yuanyuan, XU Hongyan, DING Jian, et al. First report of Cladosporium scabrellum causing stipe spot disease of Morchella importuna in China[J]. Plant Disease, 2024, 108(1): 225. DOI: 10.1094/pdis-09-22-2152-pdn. [25] CAMILETTI B X, LICHTEMBERG P S F, PAREDES J A, et al. Characterization, pathogenicity, and fungicide sensitivity of Alternaria isolates associated with preharvest fruit drop in California Citrus[J]. Fungal Biology, 2022, 126(4): 277−289. DOI: 10.1016/j.funbio.2022.02.003. [26] SAN MARTÍN J, LAGOS M J, RUIZ B, et al. Understanding the association of apical necrosis in flowers and fruits of walnut (Juglans regia L. ) with causal microorganisms under field conditions[J]. European Journal of Plant Pathology, 2023, 166(4): 445−462. DOI: 10.1007/s10658-023-02673-4. [27] ARMAND A, FALLAHI M, ABSALAN S, et al. Mango microcosm: unveiling the species diversity and pathogenic potential of fungi isolated from mango (Mangifera indica) in northern Thailand[J]. Fungal Biology, 2025, 129(3): 101552. DOI: 10.1016/j.funbio.2025.101552. [28] 武崇高, 朱桐, 崔云龙, 等. 月季枯枝病病原物鉴定、生物学特性与防治药剂筛选[J/OL]. 浙江农林大学学报, 2025-07-14. https: //link.cnki.net/urlid/33.1370.s.20250711.1951.002. WU Chonggao, ZHU Tong, CUI Yunlong, et al. Identification, characterization and fungicide screening of the causal pathogen of branch blight in Rosa chinensis[J/OL]. Journal of Zhejiang A&F University, 2025-07-14. https://link.cnki.net/urlid/33.1370.s.20250711.1951.002 [29] 项存悌, 常国彬, 赵海峰, 等. 极细枝孢生物学特性的研究[J]. 东北林业大学学报, 1989, 17(3): 38−41. XIANG Cunti, CHANG Guobin, ZHAO Haifeng, et al. Study on biological characters of Cladosporium tenuissimum Cook[J]. Journal of Northeast Forestry University, 1989, 17(3): 38−41. DOI: 10.13759/j.cnki.dlxb.1989.03.006. [30] 王树和, 周彩勤, 张奎望, 等. 金叶女贞棒孢叶斑病菌的生物学特性、致病性及系统发育[J]. 浙江农林大学学报, 2019, 36(6): 1174−1181. WANG Shuhe, ZHOU Caiqin, ZHANG Kuiwang, et al. Characterization of Corynespora cassiicola from golden vicary privet based on phylogeny, biology, and pathogenicity[J]. Journal of Zhejiang A&F University, 2019, 36(6): 1174−1181. DOI: 10.11833/j.issn.2095-0756.2019.06.015. [31] 周洁璐, 吴天昊, 巨云为, 等. 薄壳山核桃叶斑病病原菌生物学特性及室内药剂毒力测定[J]. 浙江农林大学学报, 2023, 40(5): 1018−1025. ZHOU Jielu, WU Tianhao, JU Yunwei, et al. Biological characteristics and toxicity test of the pathogen of Carya illinoinensis leaf spot[J]. Journal of Zhejiang A&F University, 2023, 40(5): 1018−1025. DOI: 10.11833/j.issn.2095-0756.20230029. [32] ZHENG Fang, LI Lei, XIAO Xiaoe, et al. Species diversity of Cladosporium in Citrus and the genetic mechanisms for C. cladosporioides complex to adapt broad host plants[J]. Fungal Diversity, 2025, 133(1): 1−22. DOI: 10.1007/s13225-025-00559-w. [33] LIU Tao, ZHAO Xiaolong, ZHU Guangxia, et al. Shortage of storage carbohydrates mainly determines seed abscission in Torreya grandis ‘Merrillii’[J]. Horticultural Plant Journal, 2025, 11(2): 619−632. DOI: 10.1016/j.hpj.2023.10.007. [34] 郝琪淳, 谢吉全, 戴文圣, 等. 香榧种实充实期叶面施肥对种实品质的影响[J]. 浙江农林大学学报, 2024, 41(3): 457−466. HAO Qichun, XIE Jiquan, DAI Wensheng, et al. Effect of foliar fertilization on seed quality of Torreya grandis ‘Merrillii’ during seed filling period[J]. Journal of Zhejiang A& F University, 2024, 41(3): 457−466. DOI: 10.11833/j.issn.2095-0756.20230194. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20250575






 下载:
下载: