-
二氧化碳(CO2)浓度升高导致的全球气候变暖已成为人类生存面临的重要生态问题[1],覆盖陆地表面约31%的森林固定了约1/3的CO2排放量[2],是陆地上主要的碳汇生态系统[3],能在一定程度上缓解温室效应[4]。森林固碳是指森林植被通过光合作用将碳转化为有机质储存于树干、根系及凋落物等[5],其中,树木木质部生长是对环境变化较敏感的固碳过程,生长过程中的木质部特征对环境因子的响应存在种间差异[6]。因此对木质部形成进行季节动态监测,有助于了解环境因子对树木生长的影响,可为预估和评价森林碳储量变化提供科学依据。
通过微树芯法可以对木质部生长季节动态进行高时间分辨率监测(天或旬),目前相关的研究主要针对针叶树,如青杄Picea wilsorii[7]、欧洲落叶松Larix decidua[8]、祁连圆柏Juniperus przewalskii[9]、欧洲赤松Pinus sylvestris[10],也有少数阔叶树,如夏栎Quercus robur[11]、欧洲山毛榉Fagus sylvatica[12]等。这些研究集中在高纬度或高海拔地区,径向生长持续期主要在春末至秋初,不超过6个月。有研究发现:在受气温限制的湿润地区,气温升高有利于树木生长季延长[13]。在受水分限制的温带地区,气温升高加剧树木蒸腾作用,引起水分亏缺,部分树木出现生长短期停滞现象[14]。此外,同一树种,受年龄、海拔等因素的影响,对气候变化的响应存在一定差异[15]。
同一生境下,不同树种的径向生长动态存在差异。楸树Catalpa bungei、樟树Cinnamomum camphora、白蜡Fraxinus chinensis和栾树Koelreuteria paniculata是中国温带、亚热带重要的园林绿化树种,在维护城市生态系统稳定性上有较高的生态学价值。这4个树种属于环孔材树种,目前对它们的年内木质部生长仍缺乏相关研究,因此探索其木质部形成动态有助于加深对环孔材树种木质部生长的理解。本研究用微树芯技术监测了4个树种木质部径向生长的季节性动态变化,并分析了它们与气候因子的关系,以期掌握这4个树种的木质部生长规律,为评估和提高本地区森林的固碳能力提供基础数据。
-
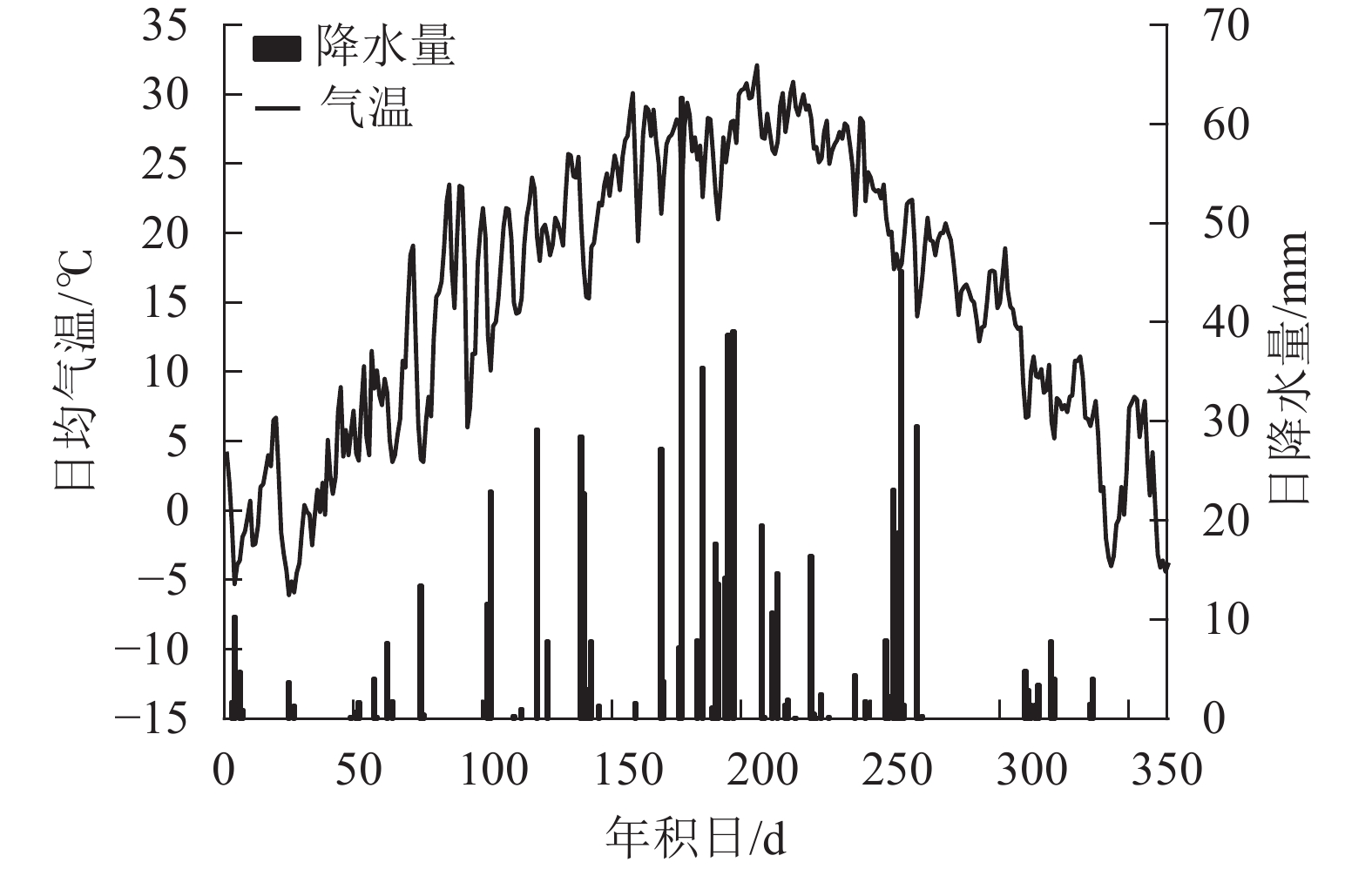
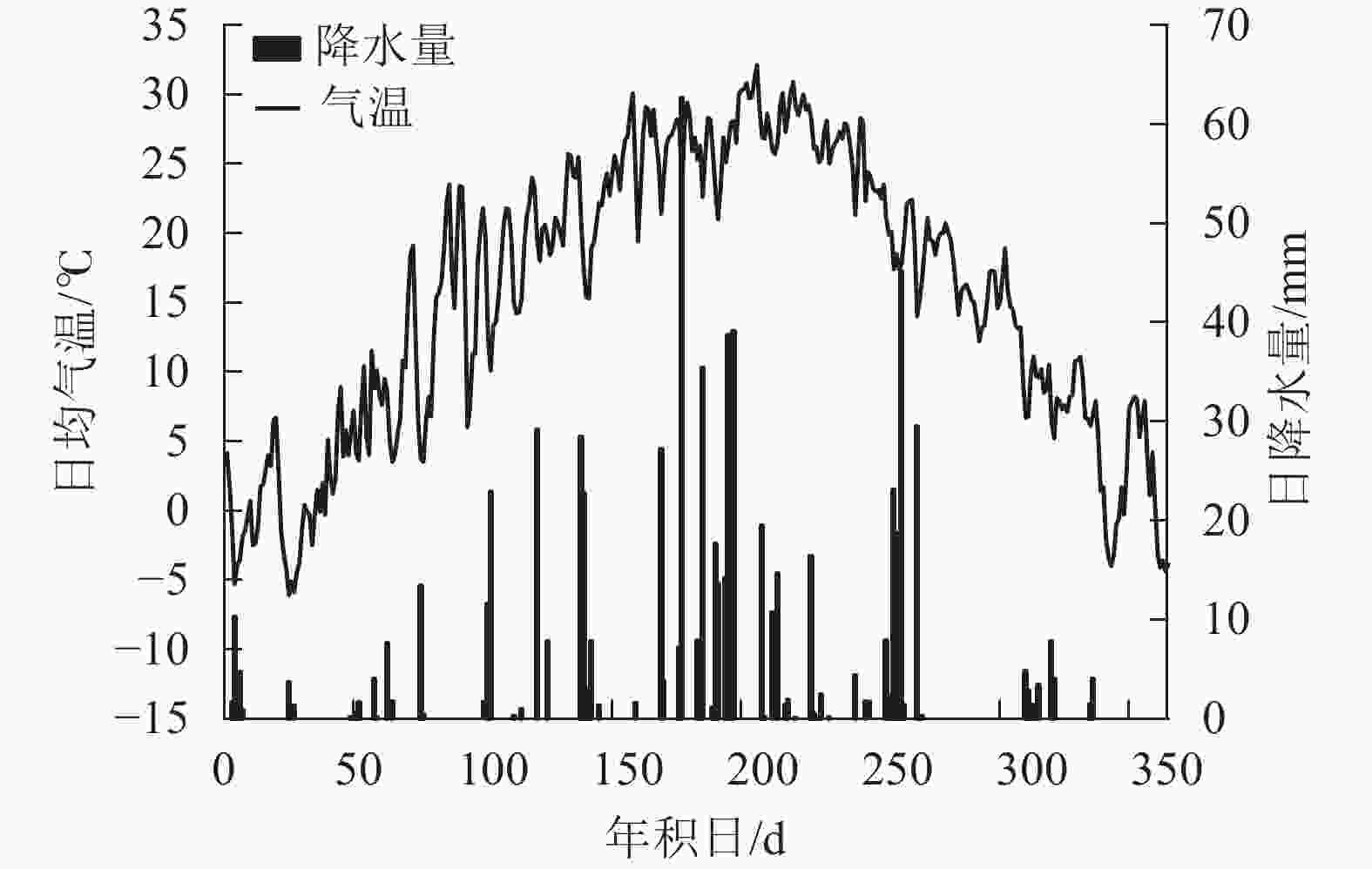
研究地位于河南省洛阳市河南科技大学。该区域属于北亚热带向暖温带过渡带的大陆性季风气候[16]。根据国家气象局数据,2018年洛阳市年均气温为15.3℃,年降水量为821.2 mm(图1),比多年同期(1960—2017年)的年均气温高1.1 ℃,降水量多223.2 mm。样地地势平坦,林下土壤以黄褐土为主[17],灌木层与草本层植被有紫叶李Prunus cerasifera、羊茅Festuca ovina等。
-
在样地选取长势良好、健康的楸树、樟树和白蜡样树各3株。受样树数量较少的影响,栾树为2株。样树基本信息:楸树平均胸径为17 cm,平均树高为9 m,平均树龄为13 a;樟树平均胸径为28 cm,平均树高为12 m,平均树龄为20 a;白蜡平均胸径为14 cm,平均树高为6 m,平均树龄为15 a;栾树平均胸径为23 cm,平均树高为9 m,平均树龄为20 a。
从2018年3—12月,对选定的样树进行监测,每隔7~10 d用Trephor微生长锥(Costruzioni Meccaniche Carabin C,专利号PD2004A000324,直径2 mm)在样树胸高处南北向轮流采集微树芯[18],共采样30次。取好的样芯立即放入软化液中,软化后样芯经自动脱水机(Leica ASP200S)脱水,组织包埋机(Leica EG1150H)包埋,轮转切片机(Leica RM2235)切片,复合染色剂(质量浓度为1%的番红水溶液,含质量浓度为0.5%固绿的体积分数为95%的乙醇溶液)染色,得到木材切片,用莱卡显微镜(Leica DM2500)观察[19]。
-
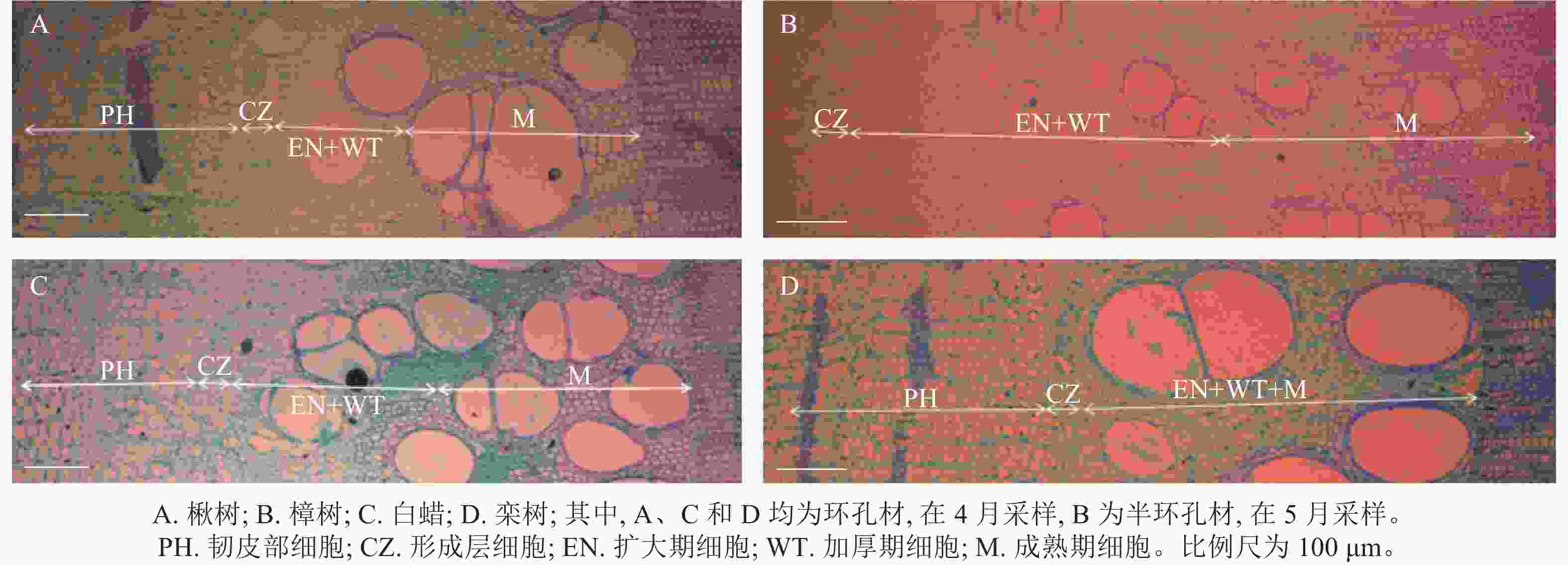
根据木质部细胞形态不同,木质部径向生长可划分为细胞扩大期、细胞壁加厚期和细胞成熟期[20]。在树木休眠期,形成层细胞扁长,排列紧密,细胞壁薄,直径小,染色后呈蓝绿色[21]。在树木生长初期,形成层细胞开始分裂、分化,当细胞体积增大至原细胞2倍时,称为扩大期细胞,细胞染色后呈蓝绿色。随后细胞壁加厚,直至细胞呈现紫红色,此时细胞完全成熟(图2)[22]。
根据ROSSI等[23]、ČUFAR等[24]的研究,以首次出现扩大期细胞作为形成层细胞活动开始(即径向生长开始)的标志。以形成层细胞不再分裂形成新的扩大期细胞作为形成层细胞活动结束的标志。以木质部细胞全部进入成熟阶段作为径向生长结束的标志。形成层活动持续期指形成层细胞活动开始到形成层细胞活动结束所持续的时间;径向生长持续期指形成层细胞活动开始到径向生长结束所持续的时间。
-
每个样芯随机选取3列径向细胞,统计形成层细胞数量并测量当年生木质部长度。每个样树选取2~3个生长末期的样芯,在当年生的第1轮导管环中选择具有代表性的3个导管,测量其直径和面积,并求得平均值。所有量测用Image J完成。使用Gompertz函数对木质部径向生长累积量进行拟合,得到年内径向生长拟合曲线,对其进行一阶求导可以得到径向生长速率[25]。数据分析用Origin 9.0[26]完成。采用Pearson相关分析树木生长与气候因子的相关性。树木生长采用相邻2次采样间的径向生长增量拟合值,环境因子为同期的日尺度气象因子均值,包括气温、地表温度、降水量、相对湿度和日照时长[27]。
-
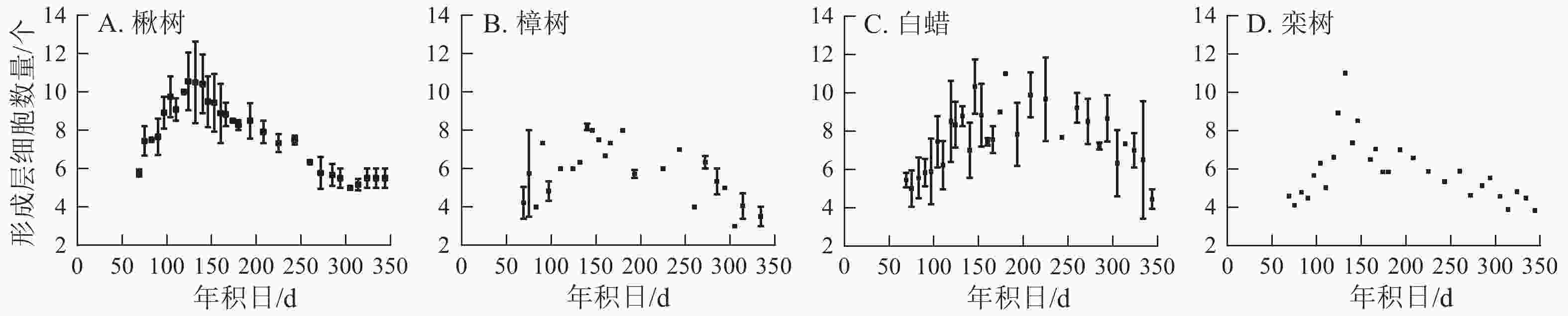
4个树种的形成层细胞数量呈先上升后下降的单峰曲线(图3)。楸树的形成层最早开始活动,在3月10日,年积日为69 d。栾树形成层活动开始时间与楸树基本一致,且最早达到形成层细胞数量最大值,在5月4日。樟树形成层细胞数量最少,仅9个,其余3个树种为11~12个。楸树形成层活动结束最早,在9月中旬,樟树最晚,在10月中旬。
-
4个树种年内径向生长在持续时间上略有差异。径向生长结束时间最早的是栾树,在10月中旬,樟树最晚,在11月初。木质部生长持续期栾树最短为220 d,樟树最长为236 d (表1)。
表 1 4个环孔材树种的形成层活动和木质部分化动态
Table 1. Phenology of cambial activity and xylem differentiation of four ring-porous tree species
树种 形成层活动启动时间/d 形成层活动停止时间/d 径向生长结束时间/d 形成层活动持续期/d 径向生长持续期/d 楸树 69.0±0.0 258.0±14.6 301.0±12.1 189.0±14.6 232.0±14.8 樟树 71.0±3.5 287.0±14.0 311.0±4.2 216.0±10.1 236.0±5.2 白蜡 80.0±4.6 280.0±17.6 301.0±6.4 199.0±13.0 221.0±9.5 栾树 69.0 273.0 289.0 204.0 220.0 说明:数值为平均值±标准差。栾树仅2个植株,未列标准差。 -
各树种的年内径向生长曲线基本一致,呈S型(图4),Gompertz函数拟合效果较好(表2),R2=0.58~0.95,P<0.000 1。年内总径向生长拟合量以楸树最大,为(8 276.0±1 744.2) μm,其次是栾树、樟树和白蜡,分别为6 727.0、(6 399.0±1 241.7)和(5 807.0±2 191.9) μm。
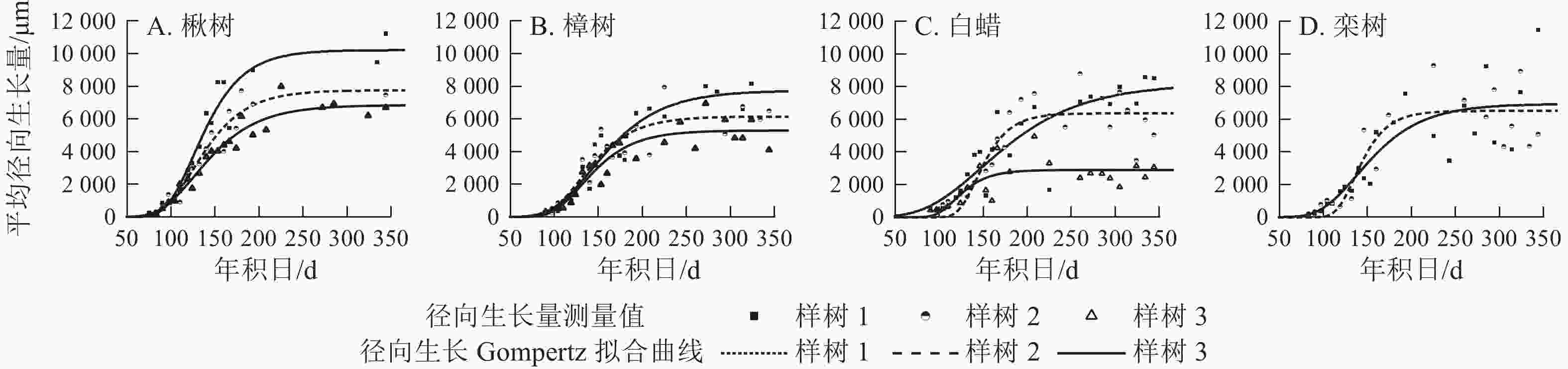
图 4 不同树种径向生长年内累积量实测值及其Gompertz拟合曲线
Figure 4. Seasonal cumulative radial growth and its model prediction from the microcore measurements
表 2 4个树种的木质部径向生长动态
Table 2. Phenology of xylem for four ring-porous species
树种 木质部径向生长
实测值/μm木质部径向生长
拟合值/μmR2 P 平均生长速率/
(μm·d−1)最大生长速率/
(μm·d−1)最大生长速率
出现的时间/d楸树 8 467.0±2 423.7 8 276.0±1 744.2 0.93~0.95 <0.000 1 55.0±17.7 90.0±28.9 126.0±1.5 樟树 5 869.0±1 548.7 6 399.0±1 241.7 0.84.0~0.91 <0.000 1 39.0±2.7 64.0±4.4 134.0±6.4 白蜡 5 541.0±2 260.1 5 807.0±2 191.9 0.58~0.80 <0.000 1 41.0±19.5 68.0±39.0 136.0±15.5 栾树 8 281.0 6 727.0 0.70~0.77 <0.000 1 54.3 88.8 137.0 说明:数值为平均值±标准差。栾树仅2个植株,未列标准差。 -
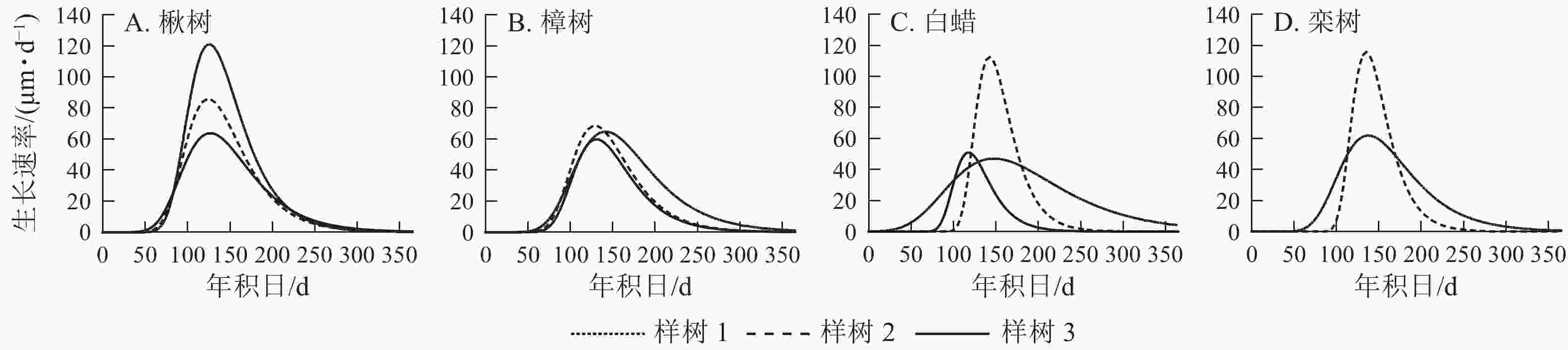
4个树种的生长速率呈先上升后下降的单峰曲线(图5),均在5月中旬达到峰值。由表2可见:楸树的峰值最高,为(90.0±28.9) μm·d−1,樟树最低,为(64.0±4.4) μm·d−1。楸树最早达到峰值,在5月6日(年积日126 d),比樟树、白蜡和栾树分别早8、10和11 d。
-
由表3可见:4个树种的年内径向生长量与气温和地表温度均呈极显著正相关(P<0.01),降水量仅与樟树树木年内径向生长的显著正相关(P<0.05)。
表 3 径向生长与同期气候因子相关性分析
Table 3. Correlation analysis between radial growth and contemporaneous environmental factors
树种 气温/℃ 地表温度/℃ 降水量/mm 相对湿度/% 日照时长/h 楸树 0.519** 0.523** 0.272 0.186 0.266 樟树 0.669** 0.663** 0.389* 0.286 0.260 白蜡 0.636** 0.629** 0.345 0.258 0.207 栾树 0.595** 0.587** 0.316 0.252 0.197 说明:**表示P<0.01;*表示P<0.05。 -
4个树种中栾树的导管直径最大(表4),为(243.0±19.2) μm,其次是楸树和白蜡,樟树的导管直径最小,为(137.0±24.0) μm。
表 4 4个环孔材树种的导管直径与横截面积
Table 4. Diameter and area of vessels in four ring-porous species
树种 导管直径/μm 导管面积/μm2 楸树 240.0±14.7 46 123.0±5 278.6 樟树 137.0±24.0 15 734.0±4 919.8 白蜡 216.0±5.8 38 370.0±1 381.9 栾树 243.0±19.2 48 125.0±8 475.7 说明:数值为平均值±标准差。 -
本研究中4个树种的形成层活动从3月开始,在9月中旬到10月中旬结束,活动持续期约200 d。木质部径向生长在10月底或11月初完成,持续时间约230 d。随着纬度升高,温度降低,树木的形成层活动推迟,径向生长结束提前,生长季缩短[28]。反之,在低纬度地区,树木生长季通常较长[29]。在高纬度芬兰(60°~70°N),欧洲云杉Picea abies的形成层细胞活动持续期约100 d[30],比本研究区持续期短。在中低纬度西双版纳(21°N),楝树Melia azedarach形成层细胞活动持续期更长,可达280 d以上[31]。在寒冷地区,树木常采用“集约化策略”,即在较短时间以较高的生长速率完成年内生长。在温暖地区,树木木质部生长表现为“广泛策略”,即生长季较长,平均生长速率较低[25],尤其是热带、亚热带地区,树木几乎全年生长[32]。本研究区树木生长虽未持续至全年,但较长(3月上旬至11月初),且平均生长速率为39~55 μm·d−1,采用的生长策略偏向于“广泛策略”。
树木的生长速率最大值出现时间通常受日照时长的影响,一般在日照时间最大值的夏至附近出现[33]。在一定范围内,随着纬度升高,日照时长加长,树木最大生长速率出现的时间延后[34]。本研究中4个树种最大生长速率出现时间均在5月中旬,可能与地处中纬度有关。除日照时长外,树木的生长速率还受降水的影响[35],因降水减少引起的干旱可能会导致生长速率减缓甚至停止[36]。这会导致树木生长速率呈双峰型曲线[37],通常发生在夏季降水较少或由高温引起植物强蒸腾作用,出现干旱胁迫的地区[38]。分布在适宜气候下的树种,其生长速率主要表现为单峰曲线[39]。本研究中4个树种的生长速率均呈单峰曲线,这说明4个树种生长旺盛时降水充足,温度适宜,未造成干旱胁迫使生长减缓这一现象。
-
树木的径向生长受树种本身(遗传基因等)和外界环境因子(温度等)的共同影响[40−41]。本研究中,气温是影响树木径向生长的主要气候因子,降水与树木径向生长的正相关关系只存在于樟树中。这可能与研究区的地理位置有关。研究区地处北亚热带与暖温带的过渡区。已有研究表明:在较寒冷的温带区域,气温是控制树木生长的主导气候因子[42]。而在亚热带,气温对树木生长的影响作用逐渐减弱[43]。此外,研究区位于半湿润向半干旱过渡区,降水对树木生长有一定影响。但降水对楸树、白蜡和栾树影响不显著,这可能是由于研究年份降水远高于多年平均水平。樟树主分布区位于南方,喜湿,对水分的需求量远高于其他3个树种[44]。因此,在樟树分布的北缘,樟树径向生长与降水的正相关关系高于其他3个树种。此外,这可能也与樟树的半环孔材木材特性有关[45]。有研究发现:与湿润年分相比,具有大导管的环孔材树种(欧梣Fraxinus excelsior等)在干旱年份时液流速率变化平缓,仅降低12%左右。而同一生境下的散孔材树种(欧洲甜樱桃Prunus avium等),在干旱年份液流速率下降幅度达15%~50%[46]。较强的树体水分调节能力使得环孔材树种在干旱时应对水分亏缺(土壤和大气)的敏感性低于散孔材树种[47−48]。这有助于解释介于散孔材和环孔材之间的半环孔材树种——樟树对水分的敏感性高于其他3个环孔材树种。此外,木质部解剖结构特征、木质部水力功能性状等多种因素均会影响植物对水分的敏感性[49]。根系特征也会影响树木生长对气候因子响应的差异性,有研究发现樟树的须根较细较少,根系在地下分布也较浅[50],而其他3个树种的根系都极为发达[51]。较发达的根系有助于促进树木获得更多土壤水分[52],这可能也是除樟树外其余3个树种与降水不具相关性的原因之一。
-
本研究使用2018年河南省洛阳市的气候数据与当地的4个环孔材树种的微树芯数据,分析了楸树、樟树、白蜡和栾树的年内径向生长动态及其对气候因子的响应。主要得到以下结论:4个树种的生长集中在3—11月,生长季内只有1个生长高峰,它们的径向生长都与气温呈极显著正相关;半环孔材樟树对气候因子的响应要强于其他3个环孔材树种,在降水这一因子上尤为明显。该研究结果有助于掌握本地区环孔材树种的木质部生长规律,为评估和提高本地区森林的固碳能力提供基础数据,加深对洛阳市环孔材树木生长-环境响应机制的认识和理解。
Intra-annual growth and its response to climatic factors in four ring-porous wood species
-
摘要:
目的 树木茎干木质部生长动态被认为是对环境变化敏感的指标之一,因此明确木质部年内形成过程对于阐明树木与气候的关系具有重要意义。 方法 利用微树芯技术,对茎干周期性采样(7~10 d),通过切片观察河南洛阳市4种环孔材树种楸树Catalpa bungei、樟树Cinnamomum camphora、白蜡Fraxinus chinensis和栾树Koelreuteria paniculata的木质部年内径向生长动态,并利用Gompertz模型对测量的木质部径向生长累积量进行拟合。 结果 ①4个树种形成层活动时间集中在3月上旬至10中旬,其中楸树最短,为(189.0±14.6) d,樟树最长,为(216.0±17.4) d。②4个树种木质部形成动态相似,均呈S型生长曲线,在11月初完成径向生长,最大生长速率出现在5月中旬。但不同树种的年内径向生长量差异较大,其中白蜡最短,为(5 807.0±2 192.9) μm,楸树最长,为(8 276.0±1 744.2) μm。③气温可能是影响本地区树木径向生长的主要气候因子,气温和地表温度与树木径向生长均呈极显著正相关(P<0.01)。降水量只与樟树生长呈显著正相关(P<0.05),这可能是因为樟树的导管直径与导管面积均最小,对水分条件较敏感。 结论 洛阳市4个树种的径向生长都与气温呈极显著正相关,并且半环孔材樟树对气候因子的响应要强于其他3个环孔材树种。图5表4参52 Abstract:Objective The radial growth dynamics of xylem is considered one of the indicators of sensitivity to environmental change. Investigating the xylem formation is crucial to elucidate the relationship between trees growth and the climate. Method Microcore sampling and paraffin sections technology were used to monitor the intra-annual growth dynamics of xylem formation. We collected the microcores of Catalpa bungei, Cinnamomum camphora, Fraxinus chinensis and Koelreuteria paniculata every 7−10 d, and Gompertz model was used to fit the modeled value of cumulative radial growth. Result (1) Cambial activity began in early March and ended in mid-October. The duration of cambial activity was shortest for C. bungei [(189.0±14.6) d], and longest for C. camphora [(216.0±17.4) d]. (2) Four species finished the xylem differentiation in early November, and their maximum growth rate occurred in the middle of May. However, the widths of cumulative radial growth showed great variations among four ring-porous species which were from (5 807.0±2 192.9) μm for F. chinensis to (8 276.0±1 744.2) μm for C. bungei. (3) Additionally, temperature may be the main climatic factor influence the radial growth in study area. Both air temperature and surface ground temperature had a significantly positive correlation on the xylem growth increment for four ring-porous wood species (P<0.01). The positive correlation between precipitation and xylem growth was only in C. camphora (P<0.05). It may explained by the smallest diameter and area of vessel of C. camphora, which led to the trees were more sensitive to precipitation. Conclusion The radial growth of the four tree species in the local area is highly significantly positively correlated with air temperature. The response of the C. camphora plants to climatic factors is stronger than the other three ring-porous porous tree species. [Ch, 5 fig. 4 tab. 52 ref.] -
Key words:
- ring-porous wood /
- cambium /
- Gompertz model /
- intra-annual radial growth dynamics /
- microcore /
- Pearson correlation
-
表 1 4个环孔材树种的形成层活动和木质部分化动态
Table 1. Phenology of cambial activity and xylem differentiation of four ring-porous tree species
树种 形成层活动启动时间/d 形成层活动停止时间/d 径向生长结束时间/d 形成层活动持续期/d 径向生长持续期/d 楸树 69.0±0.0 258.0±14.6 301.0±12.1 189.0±14.6 232.0±14.8 樟树 71.0±3.5 287.0±14.0 311.0±4.2 216.0±10.1 236.0±5.2 白蜡 80.0±4.6 280.0±17.6 301.0±6.4 199.0±13.0 221.0±9.5 栾树 69.0 273.0 289.0 204.0 220.0 说明:数值为平均值±标准差。栾树仅2个植株,未列标准差。 表 2 4个树种的木质部径向生长动态
Table 2. Phenology of xylem for four ring-porous species
树种 木质部径向生长
实测值/μm木质部径向生长
拟合值/μmR2 P 平均生长速率/
(μm·d−1)最大生长速率/
(μm·d−1)最大生长速率
出现的时间/d楸树 8 467.0±2 423.7 8 276.0±1 744.2 0.93~0.95 <0.000 1 55.0±17.7 90.0±28.9 126.0±1.5 樟树 5 869.0±1 548.7 6 399.0±1 241.7 0.84.0~0.91 <0.000 1 39.0±2.7 64.0±4.4 134.0±6.4 白蜡 5 541.0±2 260.1 5 807.0±2 191.9 0.58~0.80 <0.000 1 41.0±19.5 68.0±39.0 136.0±15.5 栾树 8 281.0 6 727.0 0.70~0.77 <0.000 1 54.3 88.8 137.0 说明:数值为平均值±标准差。栾树仅2个植株,未列标准差。 表 3 径向生长与同期气候因子相关性分析
Table 3. Correlation analysis between radial growth and contemporaneous environmental factors
树种 气温/℃ 地表温度/℃ 降水量/mm 相对湿度/% 日照时长/h 楸树 0.519** 0.523** 0.272 0.186 0.266 樟树 0.669** 0.663** 0.389* 0.286 0.260 白蜡 0.636** 0.629** 0.345 0.258 0.207 栾树 0.595** 0.587** 0.316 0.252 0.197 说明:**表示P<0.01;*表示P<0.05。 表 4 4个环孔材树种的导管直径与横截面积
Table 4. Diameter and area of vessels in four ring-porous species
树种 导管直径/μm 导管面积/μm2 楸树 240.0±14.7 46 123.0±5 278.6 樟树 137.0±24.0 15 734.0±4 919.8 白蜡 216.0±5.8 38 370.0±1 381.9 栾树 243.0±19.2 48 125.0±8 475.7 说明:数值为平均值±标准差。 -
[1] 竹万宽, 许宇星, 王志超, 等. 尾巨桉人工林土壤呼吸对林下植被管理措施的响应[J]. 浙江农林大学学报, 2023, 40(1): 164 − 175. ZHU Wankuan, XU Yuxing, WANG Zhichao, et al. Response of soil respiration to understory vegetation management in Eucalyptus urophylla × E. grandis plantation [J]. Journal of Zhejiang A&F University, 2023, 40(1): 164 − 175. [2] RICHARDSON A D, KEENAN T F, MIGLIAVACCA M, et al. Climate change, phenology, and phenological control of vegetation feedbacks to the climate system [J]. Agricultural and Forest Meteorology, 2013, 169: 156 − 173. [3] HUANG Jianguo, MA Qianqian, ROSSI S, et al. Photoperiod and temperature as dominant environmental drivers triggering secondary growth resumption in Northern Hemisphere conifers [J]. Proceedings of the National Academy of Sciences, 2020, 117(34): 20645 − 20652. [4] NJANA M A, MBILINYI B, ELIAKIMU Z. The role of forests in the mitigation of global climate change: Emprical evidence from Tanzania [J/OL]. Environmental Challenges, 2021, 4: 100170[2023-10-20]. doi: 10.1016/j.envc.2021.100170. [5] KOLO H, KINDU M, KNOKE T. Optimizing forest management for timber production, carbon sequestration and groundwater recharge [J/OL]. Ecosystem Services, 2020, 44: 101147[2023-10-20]. doi: 10.1016/j.ecoser.2020.101147. [6] 郭霞丽, 余碧云, 梁寒雪, 等. 结合微树芯方法的树木生长生理生态学研究进展[J]. 植物生态学报, 2017, 41(7): 795 − 804. GUO Xiali, YU Biyun, LIANG Hanxue, et al. Advancement in studies of tree growth and ecophysiology incorporating micro-sampling approach [J]. Chinese Journal of Plant Ecology, 2017, 41(7): 795 − 804. [7] 牛豪阁, 张芬, 于爱灵, 等. 祁连山东部青杄年内径向生长动态对气候的响应[J]. 生态学报, 2018, 38(20): 7412 − 7420. NIU Haoge, ZHANG Fen, YU Ailing, et al. Intra-annual stem radial growth dynamics of Picea wilsorii in response to climate in the eastern Qilian Mountains [J]. Acta Ecologica Sinica, 2018, 38(20): 7412 − 7420. [8] MOSER L, FONTI P, BÜNTGEN U, et al. Timing and duration of European larch growing season along altitudinal gradients in the Swiss Alps [J]. Tree Physiology, 2010, 30(2): 225 − 233. [9] REN Ping, ZIACO E, ROSSI S, et al. Growth rate rather than growing season length determines wood biomass in dry environments [J]. Agricultural and Forest Meteorology, 2019, 271: 46 − 53. [10] JYSKE T, MÄKINEN H, KALLIOKOSKI T, et al. Intra-annual tracheid production of Norway spruce and Scots pine across a latitudinal gradient in Finland [J]. Agricultural and Forest Meteorology, 2014, 194: 241 − 254. [11] GONZÁLEZ-GONZÁLEZ B D, GARCÍA-GONZÁLEZ I, VÁZQUEZ-RUIZ R A. Comparative cambial dynamics and phenology of Quercus robur L. and Q. pyrenaica Willd. in an Atlantic forest of the northwestern Iberian Peninsula [J]. Trees, 2013, 27(6): 1571 − 1585. [12] GIAGLI K, VETEŠKA O, VAVRČÍK H, et al. Monitoring of seasonal dynamics in two age-different European beech stands [J]. Wood Research, 2015, 60(6): 1005 − 1016. [13] PEREZ-DE-LIS G, ROSSI S, VAZQUEZ-RUIZ R A, et al. Do changes in spring phenology affect earlywood vessels? Perspective from the xylogenesis monitoring of two sympatric ring-porous oaks [J]. New Phytologist, 2016, 209(2): 521 − 530. [14] GAO Jiani, YANG Bao, PENG Xiaomei, et al. Tracheid development under a drought event producing intra-annual density fluctuations in the semi-arid China [J/OL]. Agricultural and Forest Meteorology, 2021, 308 − 309: 108572[2023-10-20]. doi: 10.1016/j.agrformet.2021.108572. [15] ROSSI S, GIRARD M J, MORIN H. Lengthening of the duration of xylogenesis engenders disproportionate increases in xylem production [J]. Global Change Biology, 2014, 20(7): 2261 − 2271. [16] 朱华. 中国热带生物地理北界的建议[J]. 植物科学学报, 2018, 36(6): 893 − 898. ZHU Hua. Suggestions for the northern boundary of the tropical zone in China [J]. Plant Science Journal, 2018, 36(6): 893 − 898. [17] 张俊洁, 高宾永, 雪原, 等. 近46年洛阳地区气候变化特征分析[J]. 气象与环境科学, 2008, 31(增刊1): 138 − 141. ZHANG Junjie, GAO Binyong, XUE Yuan, et al. Analysis of characteristics of climate change over last 46 years in Luoyang [J]. Meteorological and Environmental Sciences, 2008, 31(suppl 1): 138 − 141. [18] PARK J H, CHOI E B, PARK H C, et al. Intra-annual dynamics of cambial and xylem phenology in subalpine conifers at Deogyusan National Park in the Republic of Korea [J]. Journal of Wood Science, 2021, 67(1): 1 − 10. [19] ROSSI S, DESLAURIERS A, MORIN H. Application of the Gompertz equation for the study of xylem cell development [J]. Dendrochronologia, 2003, 21(1): 33 − 39. [20] DICKSON A, NANAYAKKARA B, SELLIER D, et al. Fluorescence imaging of cambial zones to study wood formation in Pinus radiata D. Don [J]. Trees, 2016, 31(2): 479 − 490. [21] DU Juan, WANG Yichen, CHEN Weifan, et al. High-resolution anatomical and spatial transcriptome analyses reveal two types of meristematic cell pools within the secondary vascular tissue of poplar stem [J]. Molecular Plant, 2023, 16(5): 809 − 828. [22] 刘伟韬, 李俊霞, 赵莹, 等. 水热耦合对沈阳地区油松木质部生长的影响[J]. 应用生态学报, 2021, 32(10): 3468 − 3476. LIU Weitao, LI Junxia, ZHAO Ying, et al. Effects of moisture and heat coupling on xylem growth of Pinus tabuliformis in Shenyang, China [J]. Chinese Journal of Applied Ecology, 2021, 32(10): 3468 − 3476. [23] ROSSI S, DESLAURIERS A, ANFODILLO T, et al. Conifers in cold environments synchronize maximum growth rate of tree-ring formation with day length [J]. New Phytologist, 2006, 170(2): 301 − 310. [24] ČUFAR K, CHERUBINI M, GRIČAR J, et al. Xylem and phloem formation in chestnut (Castanea sativa Mill. ) during the 2008 growing season [J]. Dendrochronologia, 2011, 29(3): 127 − 134. [25] JIANG Yuan, ZHANG Yiping, GUO Yuanyuan, et al. Intra-annual xylem growth of Larix principis-rupprechtii at its upper and lower distribution limits on the Luyashan Mountain in north-central China [J]. Forests, 2015, 6(12): 3809 − 3827. [26] TJORVE K M C, TJORVE E. The use of Gompertz models in growth analyses, and new Gompertz-model approach: an addition to the Unified-Richards family [J/OL]. PLoS One, 2017, 12(6): e0178691[2023-10-20]. doi: 10.1371/journal.pone.0178691. [27] ZHANG Yiping, JIANG Yuan, WEN Yan, et al. Comparing primary and secondary growth of co-occurring deciduous and evergreen conifers in an alpine habitat [J/OL]. Forests, 2019, 10(7): 574[2023-10-20]. doi: 10.3390/f10070574. [28] LIANG E, REN Ping, ZHANG Shengbang, et al. How can Populus euphratica cope with extremely dry growth conditions at 2, 800 ma. s. l. on the northern Tibetan Plateau? [J]. Trees, 2012, 27(2): 447 − 453. [29] MENG Shengwang, FU Xiaoli, ZHAO Bo, et al. Intra-annual radial growth and its climate response for Masson pine and Chinese fir in subtropical China [J]. Trees, 2021, 35(6): 1817 − 1830. [30] MÄKINEN H, JYSKE T, NÖJD P. Dynamics of diameter and height increment of Norway spruce and Scots pine in southern Finland [J]. Annals of Forest Science, 2018, 75(1): 1 − 11. [31] 陈礼敏, 韦小练, 范泽鑫, 等. 西双版纳地区楝径向生长和木质部发生季节动态及其对环境因子的响应[J]. 生态学报, 2023, 43(8): 1 − 11. CHEN Limin, WEI Xiaolian, FAN Zexin, et al. Seasonal radial growth and xylogenesis of Melia azedarach and its response to environmental factors in Xishuangbanna, southwest China [J]. Acta Ecologica Sinica, 2023, 43(8): 1 − 11. [32] LI Xiaoxia, ROSSI S, SIGDEL S R, et al. Warming menaces high-altitude Himalayan birch forests: Evidence from cambial phenology and wood anatomy [J/OL]. Agricultural and Forest Meteorology, 2021, 308/309: 108577[2023-10-20]. doi: 10.1016/j.agrformet.2021.108577. [33] KULMALA L, READ J, NÖJD P, et al. Identifying the main drivers for the production and maturation of scots pine tracheids along a temperature gradient [J]. Agricultural and Forest Meteorology, 2017, 232: 210 − 224. [34] RATHGEBER C B, ROSSI S, BONTEMPS J D. Cambial activity related to tree size in a mature silver-fir plantation [J]. Annals of Botany, 2011, 108(3): 429 − 438. [35] ANTONUCCI S, ROSSI S, LOMBARDI F, et al. Influence of climatic factors on silver fir xylogenesis along the Italian Peninsula [J]. IAWA Journal, 2019, 40(2): 259 − 275. [36] SALOMON R L, PETERS R L, ZWEIFEL R, et al. The 2018 European heatwave led to stem dehydration but not to consistent growth reductions in forests [J/OL]. Nature Communications, 2022, 13(1): 28[2023-10-20]. doi: 10.1038/s41467-021-27579-9. [37] KIYOMI M. Bimodal cambial activity and false-ring formation in conifers under a monsoon climate [J]. Tree Physiology, 2021, 41(10): 1893 − 1905. [38] ZHENG Zhuangpeng, ZHOU Feifei, FONTI P, et al. Intra-annual wood formation of Cryptomeria fortunei and Cunninghamia lanceolata in humid subtropical China [J]. Frontiers in Ecology and Evolution, 2021, 38(9): 1225 − 1236. [39] 陈佳佳, 周梅, 赵鹏武, 等. 内蒙古大兴安岭南段山杨径向变化特征[J]. 东北林业大学学报, 2022, 50(12): 25 − 30. CHEN Jiajia, ZHOU Mei, ZHAO Pengwu, et al. Radial growth characteristics of Populus davidiana in the southern section of the Daxing’an Mountains in Inner Mongolia [J]. Journal of Northeast Forestry University, 2022, 50(12): 25 − 30. [40] 谭灿灿, 聂稳, 刘逸夫, 等. 3种栎属树种单木生长模型及树皮厚度模型研究[J]. 浙江农林大学学报, 2023, 40(3): 589 − 597. TAN Cancan, NIE Wen, LIU Yifu, et al. Tree growth model and bark thickness model of three Quercus species based on trunk analysis [J]. Journal of Zhejiang A&F University, 2023, 40(3): 589 − 597. [41] 窦啸文, 吴登瑜, 张笑菁, 等. 天目山常绿阔叶林胸高断面积生长量影响因子研究[J]. 浙江农林大学学报, 2023, 40(5): 1063 − 1072. DOU Xiaowen, WU Dengyu, ZHANG Xiaojing, et al. Study on the factors affecting breast-height basal area increment of evergreenbroad-leaved forest in Mount Tianmu [J]. Journal of Zhejiang A&F University, 2023, 40(5): 1063 − 1072. [42] 李文超, 张秋良, 郝帅, 等. 大兴安岭温度梯度下兴安落叶松径向生长对气候的响应差异[J]. 内蒙古林业科技, 2023, 49(1): 1 − 8. LI Wenchao, ZHANG Qiuliang, HAO Shuai, et al. Response difference for radial growth of Larix gmelinii to climate factors under temperature gradient in the greater Xing’an mountains [J]. Journal of Inner Mongolia Forestry Science &Technology, 2023, 49(1): 1 − 8. [43] 刘士玲, 杨保国, 姚建峰, 等. 广西红椎树干径向生长研究[J]. 华南农业大学学报, 2020, 41(5): 82 − 90. LIU Shiling, YANG Baoguo, YAO Jianfeng, et al. Study on stem radial growth of Castanopsis hystrix in Guangxi [J]. Journal of South China Agricultural University, 2020, 41(5): 82 − 90. [44] 牛牧, 陈俊华, 周大松, 等. 川中丘陵区4种乡土阔叶树根系拓扑结构特征[J]. 南京林业大学学报(自然科学版), 2020, 44(2): 125 − 132. NIU Mu, CHEN Junhua, ZHOU Dasong, et al. Topological characteristics of the root systems of four native broad-leaved trees in the central Sichuan hilly region [J]. Journal of Nanjing Forestry University (Natural Sciences Edition), 2020, 44(2): 125 − 132. [45] VAVRČÍK H, GRYC V, VICHROVÁ G. Xylem formation in young Norway spruce trees in Drahany highland, Czech Republic [J]. IAWA Journal, 2013, 34(3): 231 − 244. [46] BADER M K F, SCHERRER D, ZWEIFEL R, et al. Less pronounced drought responses in ring-porous than in diffuse-porous temperate tree species [J/OL]. Agricultural and Forest Meteorology, 2022, 327: 109184[2023-10-20]. doi: 10.1016/j.agrformet.2022.109184. [47] BRINKMANN N, EUGSTER W, ZWEIFEL R, et al. Temperate tree species show identical response in tree water deficit but different sensitivities in sap flow to summer soil drying [J]. Tree Physiology, 2016, 36(12): 1508 − 1519. [48] TUMAJER J, SCHARNWEBER T, SMILJANIC M, et al. Limitation by vapour pressure deficit shapes different intra‐annual growth patterns of diffuse- and ring-porous temperate broad leaves [J]. New Phytologist, 2022, 233(6): 2429 − 2441. [49] WU Min, TIAN Yu, FAN Dayong, et al. Hydraulic regulation of Populus tomentosa and Acer truncatum under drought stress [J]. Chinese Journal of Plant Ecology, 2022, 46(9): 1086 − 1097. [50] 陈宏基. 川南五种典型植物根系分布及其对输气管道3PE防腐层的影响研究[D]. 雅安: 四川农业大学, 2020. CHEN Hongji. Root Distribution of Five Typical Plants in South Sichuan and Their Influence on Gas Pipeline 3PE Coating [D]. Ya’an: Sichuan Agricultural University, 2020. [51] 王奕丹, 李亮, 刘琪璟, 等. 亚热带6个典型树种吸收细根寿命与形态属性格局[J]. 植物生态学报, 2021, 45(4): 383 − 393. WANG Yidan, LI Liang, LIU Qijing, et al. Lifespan and morphological traits of absorptive fine roots across six typical tree species in subtropical China [J]. Chinese Journal of Plant Ecology, 2021, 45(4): 383 − 393. [52] 常云妮, 李宝银, 钟全林, 等. 3种功能型林木幼苗生物量分配及其与细根和叶片养分关系[J]. 生态学杂志, 2022, 41(11): 2090 − 2097. CHANG Yunni, LI Baoyin, ZHONG Quanlin, et al. Biomass allocation of three functional types of forest tree seedlings and their relationships with nutrients in fine roots and leaves [J]. Chinese Journal of Ecology, 2022, 41(11): 2090 − 2097. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20240574






 下载:
下载: