-
竹材作为低碳环保材料,在室内外家具、装饰和建筑等领域得到了广泛应用。然而竹材较于木材更易开裂和霉变,也成为消费者选择竹材的最大顾虑[1]。现有的竹材防裂和防霉主要通过表面涂饰、高温炭化和药剂浸渍等方式进行[2-3],虽然能够延缓竹材因尺寸和含水率变化而造成的开裂和霉变,但是尚未实现长效保护。也有研究者对竹材进行乙酰化、糠醇改性或树脂浸渍改性等处理[4-5],但由于竹材缺乏横向木射线、内部孔隙和通道大小不一、液体药剂表面张力大等原因,药剂不能均匀分散于竹材内部,导致改性难以达到预期效果。竹材的气相处理主要使用熏蒸灭杀菌虫,常采用硫化合物、溴甲烷和气相硼化合物等[6-7]。虽然能消灭菌虫,但是由于这些处理剂未与竹材的相关基团发生反应,因而不持久或抗流失性较差。因此,需要寻找一种既能够与竹材化学组分发生反应、又具有疏水和抗菌元素的气体改性剂。氟气具有优异的反应活性,氟化处理改性材料已得到广泛应用,如氟化聚合物用于防污防水涂层等[8-9]。氟(F)不仅能与碳(C)的SP2轨道发生加成反应形成C—F键,而且能取代碳SP3轨道上的氢原子形成C—F键,从而使材料具有憎水和疏油等特性[10-11]。基于氟碳化合物具有的疏水性质[12],本研究以活性较高的氟气对竹材进行气相反应,以期得到具有一定的疏水性能和抗菌性能的改性竹材。
-
以浙江省4年生新鲜毛竹Phyllostachys edulis为试材,取竹材中段,去青去黄后,加工成50 mm × 17 mm × 4.5 mm的竹块,每处理取8个重复试样。另取上述毛竹试样,置入烘箱105 ℃干燥8 h,粉碎并研磨至150~200目备用。
-
取方法1.1中的竹块和竹粉,按照表 1竹材的处理方案进行编号和改性处理。硫酸预处理采用20、200、400和800 g·kg-1的硫酸水溶液浸渍处理试样15 min,然后用去离子水洗涤至pH=7。处理好的试块先在烘箱中以(60±2)℃干燥4 h,再以(103±2)℃干燥8 h[13]。
表 1 竹材的处理方案
Table 1. Processing scheme of bamboo
编号 硫酸预处理
质量分数/(g·kg-1)氟化处理 150 ℃热处理 对照(ck) - - - 热处理(H) - - + 热氟化(HF) - + + 2AHF 20 + + 20AHF 200 + + 40AHF 400 + + 80AHF 800 + + 说明:“+”表示处理过程中包含该项步骤,“-”表示处理过程中不包含该项步骤 氟化处理在带有加热套的管式反应器中进行,温度控制在150 ℃。先通入30 min氮气以排出可挥发性杂质,再通入氟气(质量分数为25%,与氮气混合)常压反应4 h。用质量分数为25%的氢氧化钠溶液处理尾气。反应结束后,再次充入氮气,排出反应器和试块中的游离氟气。待冷却后取出样品。同时制备1组仅进行150 ℃热处理的样品作为对照。
-
取1 mg样品,加入200 mg溴化钾(KBr)进行研磨,在16 MPa下压缩成片。采用岛津IRPrestige-21型傅立叶变换红外分光光度计(32次扫描,分辨率4 cm-1,波数范围4 000~400 cm-1)进行红外光谱测试。
-
将处理好的竹粉放入离心管中,加水浸泡8 h,用离心机离心(3 000 r·min-1),倒掉上清液,重复该程序3次,共浸泡24 h。样品经干燥并在玛瑙研钵中轻轻研磨后用X射线光电子能谱(XPS)检测。XPS使用Thermo ESCALAB 250Xi光电子能谱仪分析。样品用单色化的铝(Al)的Kα射线(1 486.6 eV)激发,射线源的电压为15 kV。通过50 eV、步长为1 eV的透射能量扫描测量。高分辨率谱扫描在透射能30 eV、步长0.05 eV的条件下运行。电荷使用电子溢流枪中和,用不定型碳C1s(284.8 eV)做样品结合能(EB)荷电校正。
-
竹材的尺寸稳定性测试采用3次浸水-干燥循环试验,模拟竹材在户外晴雨环境中的尺寸变化[14],并采用3次吸湿-干燥循环,模拟干湿交替下的竹材尺寸稳定性。具体方法如下:①吸湿-干燥循环。取处理材和未处理材,先以(60±2)℃干燥4 h,再以(103±2)℃干燥8 h。用游标卡尺测量长度、宽度和厚度,精确到0.01 mm,计算体积。然后将试块置于温度为(25±2)℃,相对湿度为(85±5)%的环境中,3 d后再次测量,此为1个干燥-加湿循环,重复3次。②吸水-干燥循环。取处理材和未处理材,按照上述干燥程序进行干燥并测量尺寸。然后,将试块置于试验(25±2)℃的水浴中浸泡3 d,再次测量尺寸和干燥。循环3次。
尺寸稳定性参数包括体积膨胀率(Sw)、体积收缩率(Sh)和抗缩率(ASE),按照公式进行计算:${S_{\rm{w}}} = \frac{{\left( {{V_{{\rm{t}}n}} - {V_{{\rm{o}}n}}} \right)}}{{{V_{{\rm{o}}n}}}} \times 100\% ;\quad {S_{\rm{h}}} = \frac{{\left( {{V_{{\rm{o}}n}} - {V_{{\rm{t}}n}}} \right)}}{{{V_{{\rm{t}}n}}}} \times 100\% ;\;{A_{{\rm{SE}}}} = \frac{{\left( {{S_{\rm{u}}} - {S_{{\rm{h}}n}}} \right)}}{{{S_{\rm{u}}}}} \times 100\% $。其中:Vtn为第n次吸湿或浸水后试块的体积;Von为第n次干燥后试块的体积;Su为未处理试块的体积收缩率;Shn为第n次处理后试块的体积收缩率。
-
按照标准[15],将竹材样品置于接有木霉Trichoderma viride、青霉Penicillium citrinum和黑曲霉Aspergillus niger的混合霉菌培养基(PDA)中。在温度为25 ℃,相对湿度为85%的环境中进行防霉性能测试,培养30 d。防霉性能以目视评价方法表征:表面无菌丝和霉斑的试样感染值为0;表面感染面积<25%的试样感染值为1;表面感染面积25%~50%的试样感染值为2;表面感染面积50%~75%的试样感染值为3;表面感染面积75%~100%的试样感染值为4。培养结束后计算每组试块感染值的平均值为平均感染值。
-
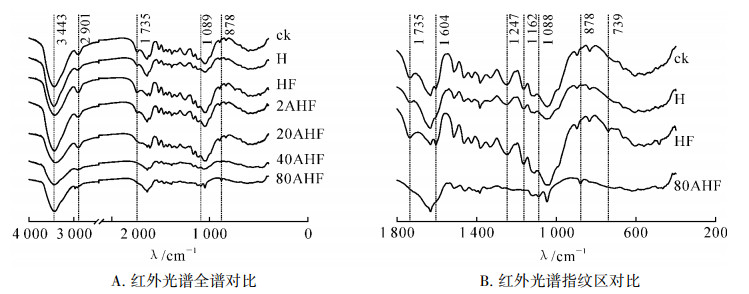
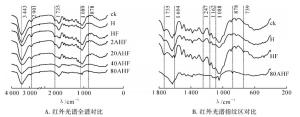
氟气化学性质活泼,具有极强的氧化性,能取代有机物中的氢元素,形成碳氟键(C—F)。氟化后的有机物对水、热和光等具有较高的稳定性。竹材主要由纤维素、半纤维素和木质素组成,也能在氟气的作用下发生反应,将氟元素接到竹材上。图 1为未处理材、热处理材、热氟化处理材和硫酸预处理后热氟化材的红外谱图。表征木质素的1 604 cm-1吸收峰在热氟化后发生了较大的变化。硫酸预处理热氟化竹材在1 514、1 464和1 424 cm-1处的木质素苯环骨架结构的峰随着预处理质量分数的增加而减弱。1 332和1 248 cm-1处的峰分别反映了愈创木基和紫丁香基的状况,该位置的峰平缓,说明木质素中部分甲氧基(—OCH)被脱去,并且1 162 cm-1处紫丁香基特征峰消失也证实了这个结果。直接氟化处理试材在739 cm-1出现了新的峰,可能由苯环上的碳氟单取代键(C—F)引起。832 cm-1处的峰是木质素芳核的弯曲振动,在800 g·kg-1硫酸处理样品中,该峰基本消失,说明木质素芳环结构发生变化。该组试样在878 cm-1处形成了强度较强的单峰,说明氟在苯环上由单取代变为了多取代,另外在1 088 cm-1有强度较弱的峰产生,进一步说明由于氟取代了竹材木质素苯环上的羟基生成了碳氟多取代(C—Fn)。
-
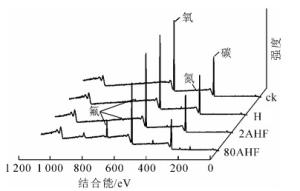
为了进一步分析热氟化对竹材化学成分的影响及氟在竹材中的存在状态,采用XPS测定氟化竹粉的碳(C)、氧(O)和氟(F)的组成及存在状态,计算竹粉的氧碳比(O/C)和氟碳比(F/C),结果如图 2和表 2。参照木材碳元素的不同化学状态[16-17],对氟化处理材XPS图进行分峰解析。氟化处理后的竹材中代表木素中苯丙烷和脂肪酸的C1(284.8 eV)含量显著减少,代表纤维素和半纤维素中羟基的C2(286.6 eV)含量略有增加,代表木素中的酮基和醛基的C3(288.1 eV)含量显著增加。竹材热氟化处理后O/C升高。这一现象表明热氟化处理后竹材表面氧化程度增加。
表 2 处理竹材元素的原子百分含量和比例变化
Table 2. Changes in the elemental composition of treated bamboo
试块名称 元素的原子百分含量/% 元素比例 O C F O/C C1/C2 F/C ck 32.27 66.31 0.15 0.49 0.80 0.00 HF 33.98 63.58 0.90 0.53 0.57 0.01 2AHF 36.62 61.21 0.75 0.60 0.52 0.01 80AHF 33.15 56.28 7.23 0.59 0.53 0.13 从表 2处理竹材元素的原子百分含量和比例变化可以看出:氟化处理竹材中均出现F,且硫酸预处理竹材F高于直接氟化竹材,氟随着预处理质量分数的提高呈增加趋势。800 g·kg-1硫酸预处理(80AHF)能显著提高热氟化材的含氟量,F/C达0.13。为了更加清晰地了解氟化竹材中氟的状态,对氟化材中的F进行XPS分峰分析,发现热氟化处理竹材均出现结合能为687.8 eV的碳氟键(—CHF—CH2—),随着氟化程度加深,80AHF试样出现了结合能为689.2 eV的碳氟多取代(—CF2—CH2—)。
-
含碳氟化物与水之间范德华作用较弱,具有一定憎水效果。为了得到氟化处理竹材受水和空气湿度的影响,采用循环吸湿或吸水试验对处理材进行测试(图 3)。直接热氟化竹材在3次吸湿-干燥过程中抗缩率达19.1%,略高于直接热处理竹材。低浓度硫酸预处理能够进一步提高氟化材的尺寸稳定性,其中20 g·kg-1硫酸预处理后的热氟化材(2AHF)抗缩率达31.0%,但是随着硫酸预处理质量分数的增加,抗缩率有所下降。在3次吸水-干燥过程中氟化处理材和热处理材尺寸变化率均减小,其中2AHF样品的抗缩率最大,达15.8%。
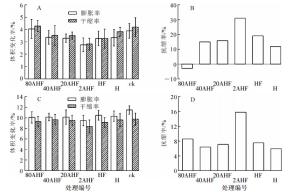
图 3 处理材在吸湿-干燥(A和B)和吸水-千燥(C和D)循环中的平均体积变化率和抗缩率
Figure 3. Volume variable rate and anti-shrink efficiency of bamboo under moistening-drying (A and B)and soaking-drying cycles(C and D)
综上所述,直接氟化处理能提高竹材的尺寸稳定性,使抗缩率略高于热处理材。根据FTIR和XPS分析,氟化处理后竹材中形成具有疏水性的碳氟键(C—F),对尺寸稳定性的提高有一定作用,但由于直接氟化(HF)试块的C—F转化率低,不能大幅提升竹材的抗胀性,需要通过工艺优化提高氟化程度和处理材的性能。低质量分数硫酸预处理热氟化材(2AHF)的尺寸稳定性大幅度提高,原因可能在于竹材中易吸水和吸湿的半纤维素降解,同时形成的C—F键使疏水性进一步提升。硫酸质量分数提高,试块虽然形成更多C—F,但同时造成了竹材表面疏松、粗糙,纤维发生部分降解,所以相较于2AHF尺寸稳定性反而逐步下降。
-
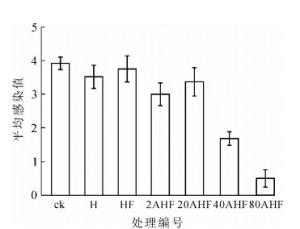
氟或含氟化合物作为一种抗菌防虫剂应用于木竹材、皮革、医学和农业领域[18-19]。热氟化竹材能将氟反应于竹材上,可能会提高竹材的抗菌性。从图 4可见:在经过1个月的室内防霉试验后,热处理和直接氟化处理试样的平均感染值分别为3.9和3.5,与未处理竹材相当。热处理和直接氟化对竹材的防霉性能没有明显改进作用。硫酸预处理再氟化能提高竹材的防霉效果,且随着硫酸预处理质量分数的提高防霉性能有增加趋势。400和800 g·kg-1硫酸预处理明显改善竹材防霉性能,平均感染值分别为1.7和0.5,原因可能是硫酸预处理并进行高温氟化,使试材发生一定程度的炭化和氟取代,氟化和炭化的协同作用提高了防霉性能。糖和淀粉的减少(图 5)也增加了防霉效果。
-
利用液相试剂处理木竹材,是目前国内外普遍使用的改性方法。但是对于难渗透的材料如竹材,处理工艺要求高,效果可能不理想,也存在药剂易流失的问题。由于氟作为氧化性极强的卤族元素具有与竹材反应的可能性,而且气相改性剂比传统液相试剂渗透性强。本研究利用氟气作为改性剂,用碱性溶液收集反应剩余尾气,可以有效避免二次污染。为了提高氟化程度,对竹材进行硫酸预处理,促进其在热氟化过程中炭化和氟取代,提高氟化效果。
根据氟与含碳化合物的反应规律,氟气与竹材的反应很可能取代竹材中的羟基(—OH)或甲基(C—Hn)生成碳氟键(C—F)[20]。通过对热氟化处理材的分析,证实了处理材化学结构发生了变化。较为明显的是硫酸预处理试样中—OH被取代,随着硫酸预处理质量分数增加,竹材中半纤维素的降解增加,木质素上的甲氧基被氧化,苯环骨架结构发生了较大变化,形成更多C—F键,这与POUZET等[21]氟化纤维的结论一致。以氟化石墨的XPS图谱分析为参考[22],氟化竹材的XPS图谱进一步证实了竹材C—F键的生成,且随着硫酸预处理质量分数的提高,竹材中氟元素逐渐增加。经过氟化处理的试块尺寸稳定性均有不同程度的提高,其中以20 g·kg-1硫酸预处理的试块效果最好,在吸湿-干燥循环中抗缩率为29.4%,吸水-干燥循环中抗缩率为17.4%。由于C—F键生成量较少或硫酸预处理质量分数过高造成竹材结构疏松等原因,尺寸稳定性提高幅度不明显,需要进一步完善热氟化处理工艺。氟化物是较好的抗菌防虫剂,由于处理竹材中含量较少,防霉效果也没有得到大幅度提高。20 g·kg-1硫酸预处理氟化材平均感染值为3.4,低于对照组(3.9)和仅热处理竹材(3.5)。800 g·kg-1的硫酸预处理氟化材防霉性能进一步提升,平均感染值为0.5。以上结果表明热氟化处理对于提高竹材的尺寸稳定性和防霉性能具有一定的效果,能够为竹材气相改性研究提供参考。
Dimensional stability and mold resistance to bamboo treated in gaseous phase fluorination
-
摘要:
目的 以氟气作为改性剂,利用其较强的渗透性和反应活性与木材细胞形成化学键,达到长效存留和改性竹材的目的。 方法 将4年生的毛竹Phyllostachys edulis置于管式反应器中,通入质量百分比为25%的氟气,在150℃下反应4 h。为了进一步提高氟化效果,先用不同质量分数硫酸预处理竹材,再进行高温氟化处理。 结果 氟化反应主要发生在木质素上。氟化材红外光谱说明氟化处理材在739 cm-1处产生了表征碳氟键(C-F)的新峰,浓硫酸预处理氟化竹材在878和1 088 cm-1出现木质素苯环氟多取代(C-Fn)吸收峰。X射线光电子能谱中结合能为687.8 eV的C-F特征峰和689.2 eV的C-F2特征峰证实了氟化处理竹材中C-Fn键的生成。热氟化试块在3次吸湿-干燥和吸水-干燥循环中平均抗胀率分别为19.1%和7.5%。硫酸预处理能进一步提高氟化材的尺寸稳定性,其中20 g·kg-1的硫酸预处理氟化材效果最为显著,平均抗胀率分别达31.0%和15.8%。防霉测试显示氟化处理材对木霉Trichoderma viride、青霉Penicillium citrinum和黑曲霉Aspergillus niger混合霉菌的抑制效果不明显,硫酸预处理后的氟化材防霉性能有所增加。 结论 竹材气相热氟化能对竹材内部进行改性,处理后的竹材尺寸稳定性和防霉性能均优于未处理竹材。利用氟气对竹材进行气相改性是一种渗透性强、反应活性高的竹材改性新技术。 Abstract:Objective The strong permeability and reactivity of gaseous fluorine supposedly helps form chemical bonds between fluorine and bamboo. This aim is to increase the leaching resistance of gaseous fluorine Method The four-year-old bamboo (Phyllostachys edulis) was heated in a tubular reactor at 150℃ and treated with 25% fluorine for 4 h. To improve the fluorination effect, bamboo was pretreated with sulfuric acid at different concentrations before the fluorine thermo treatment. Analysis included fourier transformed infrared spectra and X-ray photoelectron spectroscopy. Tests on mold resistance for fluorinated bamboo with mixed fungi of Trichoderma viride, Penicillium citrinum, and Aspergillus niger were conducted. Result The chemical analysis and testing of fluoride bamboo showed obvious changes in lignin. Fourier transformed infrared spectra demonstrated that the new peaks at 739 cm-1 were C-F (carbon-fluorine) monosubstituted bonds; whereas, concentrated sulfuric acid pretreated fluorinated bamboo showed double C-F peaks at 878 and 1 088 cm-1 caused by the polysubstitution of C-F bonds on the benzene ring of lignin. Binding energies of 687.8 eV (C-F) and 689.2 eV (C-F2) in X-ray photoelectron spectroscopy confirmed the presence of the C-F bond in fluorinated bamboo. The dimensional stability of treated bamboo was tested under three moistening-drying cycles and water soaking-drying cycles, respectively. The average anti-shrink efficiency (ASE) for three cycles of thermo fluorinated bamboo was 19.1% for moistening-drying and 7.5% for water soaking-drying. Sulfuric acid pretreatment further improved dimensional stability of thermo fluorinated bamboo where 20 g·kg-1 sulfuric acid pretreatment behaved the best with a corresponding ASE of 31.0% for moistening-drying and 15.8% for water soaking-drying. Tests on mold resistance for fluorinated bamboo with mixed fungi of T. viride, P. citrinum, and A. niger, showed no obvious anti-mold efficacy; whereas, for fluorinated bamboo pretreated with sulfuric acid there was slight improvement. Conclusion Thus, with gaseous-phase thermo fluorination, a new way of bamboo modification with strong permeability and high reactivity, dimensional stability and mold resistances of treated bamboo were better than the controls making them effective for inner modification of bamboo. -
表 1 竹材的处理方案
Table 1. Processing scheme of bamboo
编号 硫酸预处理
质量分数/(g·kg-1)氟化处理 150 ℃热处理 对照(ck) - - - 热处理(H) - - + 热氟化(HF) - + + 2AHF 20 + + 20AHF 200 + + 40AHF 400 + + 80AHF 800 + + 说明:“+”表示处理过程中包含该项步骤,“-”表示处理过程中不包含该项步骤 表 2 处理竹材元素的原子百分含量和比例变化
Table 2. Changes in the elemental composition of treated bamboo
试块名称 元素的原子百分含量/% 元素比例 O C F O/C C1/C2 F/C ck 32.27 66.31 0.15 0.49 0.80 0.00 HF 33.98 63.58 0.90 0.53 0.57 0.01 2AHF 36.62 61.21 0.75 0.60 0.52 0.01 80AHF 33.15 56.28 7.23 0.59 0.53 0.13 -
[1] 孙芳利, PROSPER N K, 吴华平, 等.木竹材防腐技术研究概述[J].林业工程学报, 2017, 2(5):1 - 8. SUN Fangli, PROSPER N K, WU Huaping, et al. A review on the development of wood and bamboo preservation[J]. China For Sci Technol, 2017, 2(5): 1 - 8. [2] LIU Yadi, LIU Wenjin. Research progress on the bamboo timber preservation[J]. Adv Mater Res, 2010, 159: 216 - 221. [3] 邹怡佳, 陈玉和, 吴再兴, 等.竹材防开裂研究进展[J].浙江林业科技, 32(5): 85 - 88. ZOU Yijia, CHEN Yuhe, WU Zaixing, et al. Advance of research on bamboo cracking prevention[J]. J Zhejiang For Sci Technol, 32(5): 85 - 88. [4] CHEN Hongyan, MIAO Menghe, DING Xin. Chemical treatments of bamboo to modify its moisture absorption and adhesion to vinyl ester resin in humid environment[J]. J Compos Mater, 2011, 45(14): 1533 - 1542. [5] 李万菊.木竹材糠醇树脂改性技术及其机理研究[D].北京: 中国林业科学研究院, 2016. LI Wanju. The Study on the Modification Technology and Mechanism of Fururylation of Wood and Bamboo [D]. Beijing: Chinese Academy of Forestry, 2016. [6] REMADEVI O K, GUNASEKARAN N. Phosphine fumigation for control of bamboo borer, Dinoderus minutus Fab. infesting bamboo culms and products[J]. J Indian Acad Wood Sci, 2013, 10(1): 68 - 71. [7] TSUNODA K. Preservative properties of vapor-boron-treated wood and wood-based composites[J]. J Wood Sci, 2001, 47(2): 149 - 153. [8] AL-AMODI A O, AL-MUBAIYEDH U A, SULTAN A S, et al. Novel fluorinated surfactants for enhanced oil recovery in carbonate reservoirs[J]. Can J Chem Eng, 2016, 94(3): 454 - 460. [9] CAI Lu, LI Zhanxiong. Preparation of fluoroalkylsilyl polymethacrylates and their waterproof application on cotton fabrics[J]. Fibers Polym, 2015, 16(10): 2094 - 2105. [10] MATSUO Y, NAKAJIMA T. Carbon-Fluorine bondings of fluorinated fullerene and graphite[J]. Zeitschrift Für Anorganische Chemie, 1995, 621(11): 1943 - 1950. [11] HAMWI A. Fluorine reactivity with graphite and fullerenes. fluoride derivatives and some practical electrochemical applications[J]. J Phys Chem Solids, 1996, 57(6/8): 677 - 688. [12] DALVI V H, WEEKS R J D. Molecular origins of fluorocarbon hydrophobicity[J]. Proc Nat Acad Sci United States Am, 2010, 107(31): 13603 - 13607. [13] 中华人民共和国国家林业局.木材干缩性测定方法:GB/T 1932-2009[S].北京:中国标准出版社, 2009. [14] 刘彬彬, 孙芳利, 吴华平, 等.载药聚丙烯酸/聚乙二醇半互穿聚合物网络在木材中的原位构建及其性能[J].林业科学, 2016, 52(11):134 - 141. LIU Binbin, SUN Fangli, WU Huaping, et al. Construction of drug-loaded polyacrylate/polyethylene glycol semi-interpenetrating network structure in wood and its performances[J]. Sci Silv Sin, 2016, 52(11): 134 - 141. [15] 中华人民共和国国家林业局.防霉剂对木材霉菌及变色菌防治效力的试验方法: GB/T 18261-2013[S].北京: 中国标准出版社, 2014. [16] 杨喜昆, 杜官本, 钱天才, 等.木材表面改性的XPS分析[J].分析测试学报, 2003, 22(4):5 - 8. YANG Xikun, DU Guanben, QIAN Tiancai, et al. Analysis of the surface modification of wood by X-ray photoelectron spectroscopy [J]. J Instrum Anal, 2003, 22(4): 5 - 8. [17] 侯伦灯, 张齐生, 苏团, 等.竹重组材的X射线光电子能谱分析[J].林业科技开发, 2012, 26(1): 47 - 49. HOU Lundeng, ZHANG Qisheng, SU Tuan, et al. X-ray photoelectron spectroscopy analysis of reconstituted bamboo lumber[J]. China For Sci Technol, 2012, 26(1): 47 - 49. [18] 刘慧颖, 伊哲, 王学金, 等.氟离子注入钛表面改性抗菌性能的研究[J].口腔医学, 2008, 28(6): 287 - 290. LIU Huiying, YI Zhe, WANG Xuejin, et al. XRD and FTIR analysis on bamboo culm treated by high-temperature hot water extraction[J]. Stomatology, 2008, 28(6): 287 - 290. [19] 杨平, 邵宇, 宋新建.含噻二唑环吡唑并[3, 4-d]嘧啶类含氟衍生物的合成及抗菌活性[J].精细化工, 2013, 30(8):856 - 859, 952. YANG Ping, SHAO Yu, SONG Xinjian. Synthesis and antibacterial activity of fluorinated pyrazolo[3, 4-d] pyrimidine derivatives containin[J]. Fine Chem, 2013, 30(8): 856 - 859, 952. [20] BORTHAKUR R D, GOGOI P K. Studies of dimensional stability, thermal stability and biodegradation resistance capacity of chemically treated bamboo[J]. Asian J Biochem, 1980, 9(1): 16 - 29. [21] POUZET M, DUBOIS M, CHARLET K, et al. The effect of lignin on the reactivity of natural fibres towards molecular fluorine[J]. Mater Des, 2017, 120: 66 - 74. [22] NIKOLENKO Y M, ZIATDINOV A M. XPS studies of graphite compounds with fluorine and pentafluorides[J]. Chem Prepr Arch, 2002, 2002(1): 145 - 149. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.2020.02.021






 下载:
下载: