-
土壤养分异质性在自然界中普遍存在,主要表现在土壤中包含许多大小不同、形状各异的养分富集区域,且养分含量各不相同[1]。引起养分异质性分布的因素很多,除了土壤自身的异质理化性质外,还包括动物的排泄物、植物凋落物理化性质的差异以及微生物活动等[2]。由于不同植物对养分异质性的响应不同,土壤养分异质性可能会对植物间的竞争关系造成一定的影响[3−5]。研究表明:与本地植物间的竞争关系是决定外来植物能否成功入侵的关键因素之一[6]。与本地植物相比,入侵植物更能从环境异质性中获益[7−8],因此,土壤养分异质性可能会促进外来植物的入侵[9−10]。
节节麦Aegilops tauschii属于禾本科Poaceae山羊草属Aegilops植物,为世界十大恶性杂草之一。野生节节麦种群广泛分布于欧亚大陆中部的干旱及半干旱地区[11],在长期的传播及适应过程中,该物种已经扩散至从叙利亚、土耳其北部到中国西部等欧亚大陆中部广泛的地理区域[12]。节节麦作为小麦Triticum aestivum的野生近缘种之一,在出苗时间、苗期特征及生长习性等方面均与小麦接近,不仅会竞争光照、水及肥等资源,还是小麦条锈病的替代宿主,因此极易造成小麦的减产甚至绝收。自1955年在河南省新乡地区首次采集到其标本至今,节节麦已入侵扩散至中国的陕西、河南及山东等小麦主产省[13],并已严重威胁到小麦的生产安全[13−14]。节节麦具有较强的生存能力,且对土壤养分条件的适应性强[15−16]。目前,有关养分异质性对节节麦和小麦生长及竞争影响的研究尚未见有报道。为此,本研究探讨土壤养分异质性对节节麦与小麦竞争关系的影响,以期为节节麦入侵危害机制研究提供参考。
-
2021年6月,供试节节麦及小麦种子来源于河南省新乡农业科学院试验田(35°18′N,113°52′E),种子晒干后室内保存。试验在河南科技大学科教试验园内进行,该试验园位于河南省洛阳市洛龙区(34°59′N,112°16′E)。该地区属温带季风气候,海拔高度为209 m。年均气温为14.86 ℃,年均降水量为578.2 mm。
-
2021年9月,将经过筛选的节节麦及小麦种子播种至营养钵内进行育苗,基质为V(珍珠岩)∶V(蛭石)∶V(草炭)=1∶1∶1。待幼苗生长至“两叶一心”时,选取高度及长势基本一致的节节麦和小麦幼苗移栽至种植箱(60 cm×40 cm×20 cm)内。
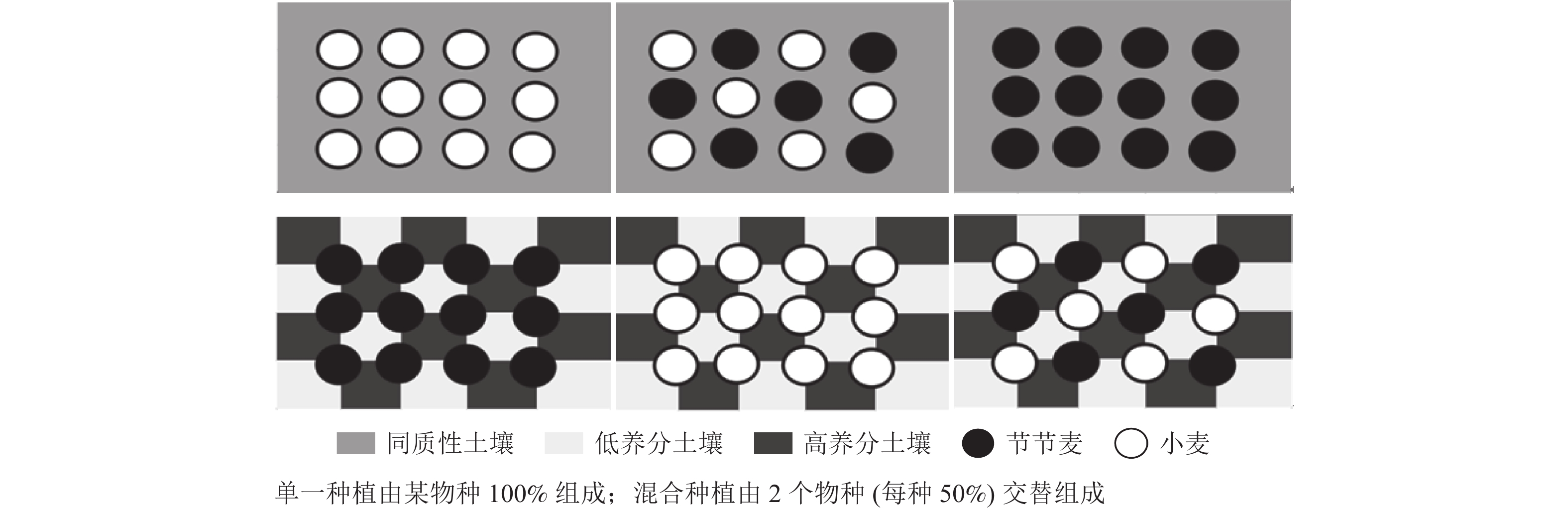
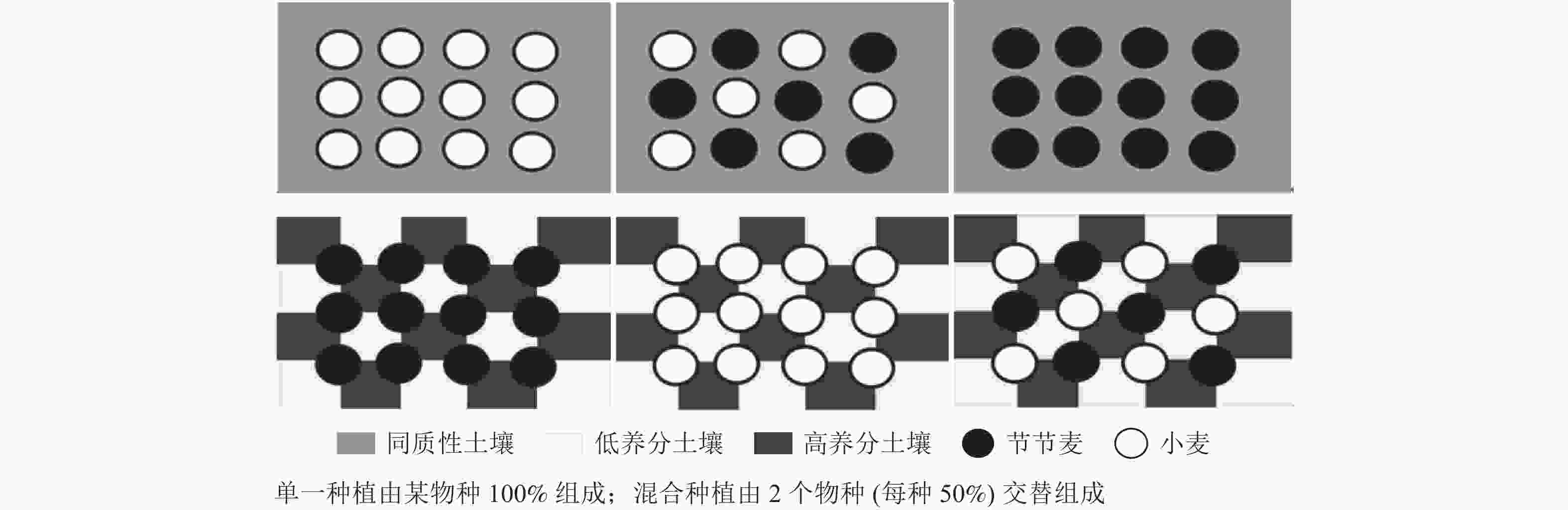
在种植箱内填入人工制备的均质或异质土壤,为了便于排水,容器底部均铺设约2 cm的略大颗粒砂土。基质填充前,利用聚氯乙烯(PVC)板在种植箱内隔离出所需空间,填充基质后移除PVC板。参照文献[17−18]的处理方式对土壤养分进行定性控制。设置包括高养分[V(草炭土)∶V(砂土)=3∶1]、低养分[V(草炭土)∶V(砂土)=1∶3]及异质性土壤(将种植容器均匀分隔为若干部分,交叉应用等量的高、低养分土壤)3种养分条件。异质养分处理设置20个营养斑块,其中高、低养分斑块各10个(图1)。同质养分处理则是用与异质养分处理中相同数量的高、低养分土壤混合而成。各个处理是由富含营养的草炭土和砂土的不同混合物代表的。因此,同质与异质养分处理中总体营养供应是相同的。此外,结合种植箱面积及大田小麦的种植密度,设计3种种植模式:①12株节节麦均匀种植;②12株小麦均匀种植;③6株节节麦和6株小麦交替均匀种植。异质养分模式中,植株均定植在异质性斑块的交叉点,与同质养分模式中植株定植的位置完全相同,如图1所示。共6个处理,每处理设置4个重复,所有种植箱均随机排列。养护期间维持土壤水分以保证植物正常生长。
试验于2021年10月开始,持续120 d。试验结束时,在单种及混种条件下,从每个处理中随机抽取10株植株。先测量每株植株高度,随后用水冲刷的方法将植株根部从土壤中小心分离出来,并尽量减少细根的损失。使用扫描仪和Photoshop软件来确定叶面积[19]。最后,将植物的叶、茎和根分开,保存在纸袋中。然后将样品在80 ℃的烘箱中烘干至恒量,并测定生物量(精确至0.000 1 g)。
-
采用单因素方差分析(one-way ANOVA)分析土壤养分异质性对节节麦和小麦单株指标的影响。利用SPSS 19.0进行数据统计分析,Excel软件作图。
根冠比=根生物量/地上部分生物量[20]。
采用相对产量(R)、相对产量总和(T)及竞争平衡指数(Ca)测度节节麦与小麦间的竞争能力强弱[21−23]。公式为:Ra=Yab/Ya;T=(Ra+Rb)/2;Ca=ln(Ra/Rb)。其中,a、b分别表示2个供试物种;Ya表示单种时物种a的单株产量;Ra、Rb分别表示混种时物种a、b的相对产量;Yab表示混种时物种a的单种产量。计算时单株产量为单个植株的干物质量。Ra=1.0,表明物种a与b的种内及种间竞争强度相同,即2个物种的竞争力相同;Ra>1.0,表明种内竞争力大于种间,即物种a对物种b的竞争力大于其对自身的竞争强度;Ra<1.0,表明种内竞争力小于种间,即物种a对物种b的竞争力小于其对自身的竞争强度。T=1.0,表明物种a与b需要相同的营养资源,且一种物种可以通过竞争作用将另一物种排除出去;T>1.0,表明a与b不存在竞争作用;T<1.0,表明a与b存在竞争作用。Ca=0,表明物种a和b的竞争力相等;Ca<0,表明物种a的竞争力小于物种b;Ca>0,表明物种a的竞争力大于物种b,Ca越大,表明物种a的竞争力越强。
-
与同质性土壤相比,无论种内还是种间竞争,土壤养分异质性均明显促进了小麦和节节麦株高及叶面积的增加(图2)。其中,种内竞争条件下,异质性土壤中小麦的株高和叶面积分别较同质性土壤中增加了29.80%、20.09%,明显小于节节麦的39.29%、39.37%;而种间竞争条件下,异质性土壤中小麦的株高及叶面积分别较同质性土壤中增加了23.88%、21.63%,同样明显小于节节麦的26.58%、25.35%。此外,仅有在种内竞争条件下,异质性土壤中节节麦株高的增加与同质性土壤差异显著(P<0.05)。
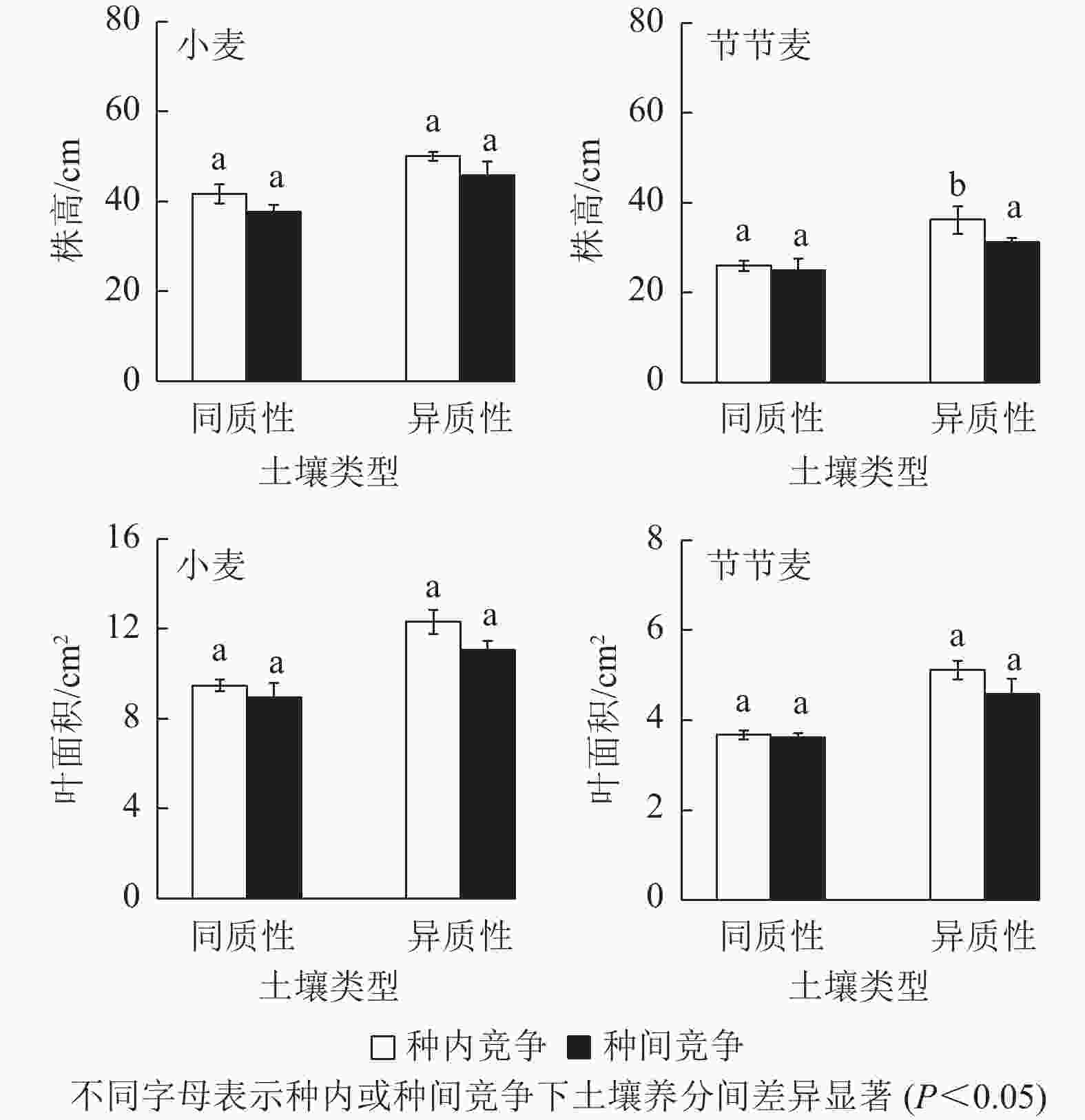
图 2 土壤养分异质性与种间竞争对小麦和节节麦株高及叶面积的影响
Figure 2. Effect of soil nutrient heterogeneous and interspecific competition on the plant height and leaf area of T. aestivum and A. tauschii
无论是种内竞争还是种间竞争,土壤养分异质性均促进了小麦和节节麦单株分蘖数的增加,但均未达到显著水平(图3)。其中,在种内和种间竞争条件下,异质性土壤中小麦的单株分蘖数分别较同质性土壤中增加了27.78%、24.39%,小于节节麦的41.43%、30.00%。

图 3 土壤养分异质性与种间竞争对小麦和节节麦单株分蘖数的影响
Figure 3. Effect of soil nutrient heterogeneous and interspecific competition on the tillers per plant of T. aestivum and A. tauschii
如图4所示:无论是种内竞争还是种间竞争,土壤养分异质性促进了小麦和节节麦总生物量的增加,且与同质性土壤相比,均达到了显著水平(P<0.05)。其中,在种内和种间竞争条件下,土壤养分异质性促使小麦的总生物量分别增加了132.51%、123.81%,小于节节麦的133.06%、131.42%。
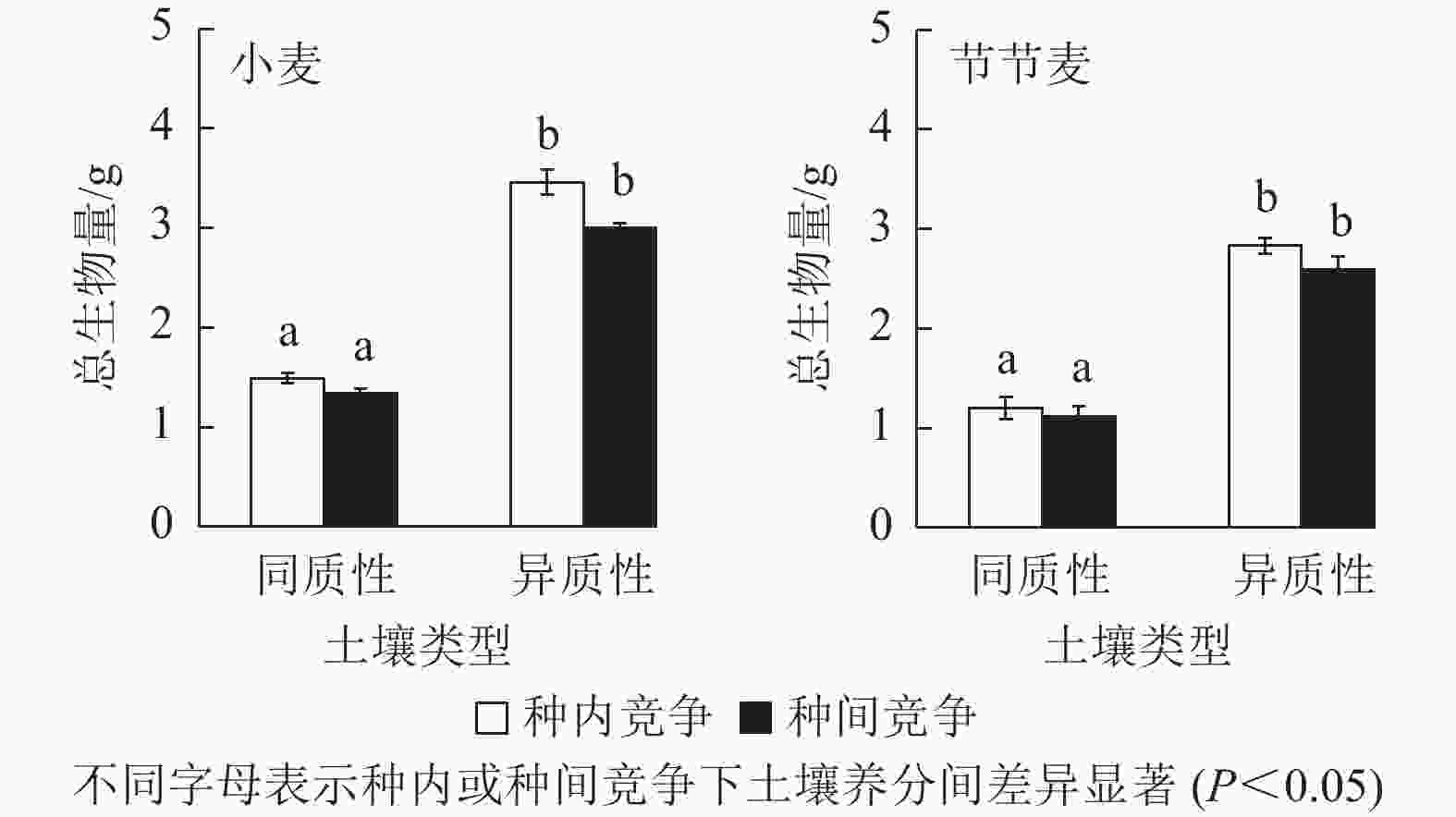
图 4 土壤养分异质性与种间竞争对小麦和节节麦总生物量的影响
Figure 4. Effect of soil nutrient heterogeneous and interspecific competition on total biomass of T. aestivum and A. tauschii
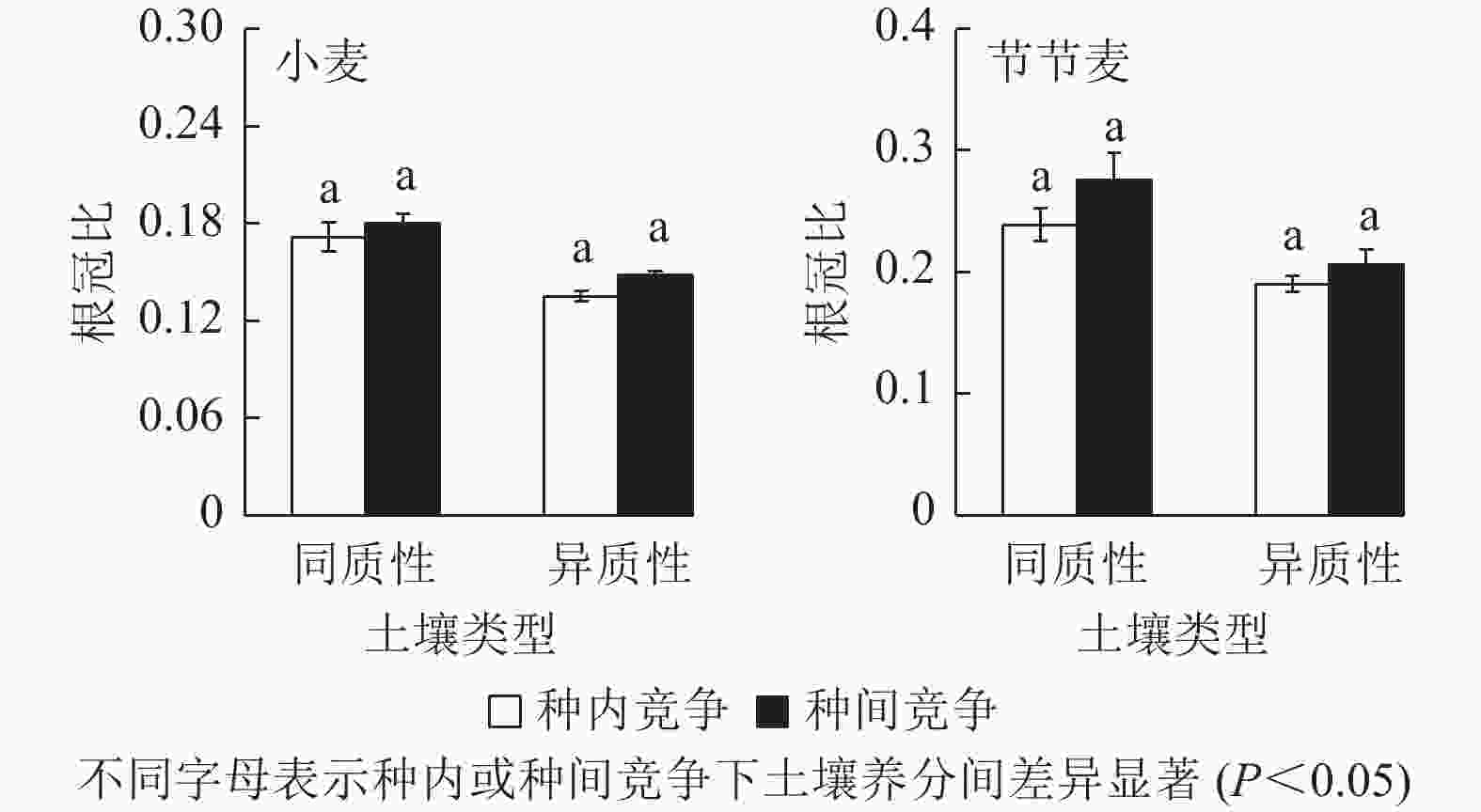
无论是种内还是种间竞争,与同质性土壤相比,异质性土壤中小麦和节节麦的根冠比均略有下降,但均未达到显著水平(图5)。其中,在种内和种间竞争下,土壤养分异质性促使小麦的根冠比分别下降了21.17%、17.74%,大于节节麦的20.53%、25.11%。
-
从表1可知:无论是在同质性土壤还是异质性土壤中,节节麦和小麦的相对产量及节节麦的相对产量总和均小于1。节节麦的竞争平衡指数值均大于0,且异质性土壤中的竞争平衡指数较同质性土壤中有所增加,但未达到显著水平。
表 1 不同土壤类型下节节麦与小麦的竞争关系
Table 1. Competitive relationship between A. tauschii and T. aestivum under soil nutrient heterogeneity
土壤类型 Ra Rb 相对产量总和 竞争平衡指数 同质性 0.921±0.022 a 0.901±0.016 a 0.911±0.011 a 0.022±0.001 a 异质性 0.914±0.041 a 0.867±0.014 a 0.891±0.022 a 0.053±0.015 a 说明:数值为平均值±标准误,同列不同小写字母表示不同土壤养分间差异显著(P<0.05) -
为了最大限度地获取土壤养分资源,植物会通过形态或生理上的调节来适应异质性的土壤斑块环境[24]。也有研究显示:土壤养分异质性对植物生长的影响是由植物自身属性及土壤养分异质性斑块的属性共同决定的[25]。当异质性土壤斑块间差异不明显或斑块较小时,土壤养分异质性并不会对植物生长造成显著影响[26],这可能是由于养分的空间异质性分布对植物的影响不足以抵消光照、空间或竞争等因素对生长特征的影响[24]。本研究中,土壤养分异质性一定程度促进了节节麦和小麦幼苗的生长发育,并提高了节节麦对小麦的竞争抑制作用。
-
株高和叶面积是植物获取光合作用空间及更多光照条件的重要保障,也是决定植物个体间光照资源竞争成功的关键因素之一[27],对环境变化敏感且可塑性强,并与植物生长发育紧密相关,因此,常被用于植物响应环境变化研究的评价指标[28]。本研究中,无论是种内还是种间竞争,异质性土壤中小麦和节节麦幼苗株高及叶面积均有所增加,表明土壤养分异质性促进了小麦和节节麦地上部分的生长发育。而此结果也证实之前的研究结论,即植物在异质性土壤养分供应的环境中经常表现出较同质土壤养分供应的环境更好,即使2种环境中的养分总量相同[29],而这可能与其在异质环境中能从资源丰富的斑块中获取更多养分有关[30]。从株高及叶面积的增幅可以看出,土壤养分异质性对节节麦的促进作用较为明显。
外界环境因素通常不会影响植物分蘖芽的分化,但分蘖芽是否会发育成为分蘖则与环境因素密切相关[31]。本研究发现:土壤养分异质性促进了小麦和节节麦单株分蘖数的增加,其中种内竞争条件下节节麦的增幅最大。相同条件下(即竞争模式及土壤状态),节节麦的单株分蘖数明显高于小麦。而这也证实了房锋[32]的研究结论,即节节麦的分蘖能力与土壤条件等因素有关,且通常情况下多于小麦。此结果再次证实了节节麦具有分蘖能力强、繁殖系数高的特征,而这也可能是节节麦得以大面积入侵扩散并对小麦造成危害的重要原因之一。
生物量是反映植物相对竞争能力的重要性状[33]。研究表明:在可用养分总含量相当的情况,一些植物在异质条件下比在均质条件下积累的生物量更大[34]。无论是否与本土植物莲子草Alternanthera sessilis共生,入侵植物空心莲子草A. philoxeroides的生物量在异质养分处理中明显高于同质养分处理[35]。袁伟影等[36]研究表明:土壤养分异质性增加了南美蟛蜞菊Sphagneticola trilobata和蟛蜞菊S. calendulacea的总生物量。与土壤均匀性相比,土壤异质性明显增加了入侵物种鬼针草Bidens pilosa和薇甘菊Mikania micrantha在竞争条件下的生物量[37]。本研究中,与同质性土壤相比,小麦和节节麦的总生物量均显著提高,其中又以节节麦的增幅最大,表明土壤养分异质性对节节麦幼苗生长的促进作用相对较大。
生物量分配格局的改变被认为是植物应对可变生境的重要策略[38]。植物会通过调节分配地上及地下器官的生物量对资源做出竞争反应,从而保证自身能够最大化的吸收受限资源[39]。在土壤养分充足条件下,植物会通过增加叶面积等形式将更多的生物量分配至碳同化器官[40];而当养分有限时,植物则会通过增加根冠比的形式加大对根部的投入,从而能更有效地捕获限制性的土壤养分[41]。本研究中,土壤养分异质性造成了小麦和节节麦根冠比的下降,这表明土壤养分并不是两者生长的限制因素,因此,两者均通过增加地上部分的投入以占领资源丰富斑块获得更多资源。其中,种间竞争条件下,节节麦根冠比的降幅较大,表明节节麦将更多的生物量投入至地上部分以加大对小麦的竞争抑制作用。
-
竞争能力会影响到群落的组成及结构,同时也是决定外来植物入侵的重要因素之一[42],正确选择判定指标对解释植物间的竞争结果至关重要[43]。生物量是种间竞争的重要衡量指标之一,因此,多数竞争指标均依据混种条件下的生物量变化来反映入侵植物的竞争能力[44]。有研究认为:相邻植物的根系会在营养丰富的区域增殖,因此,土壤养分异质性会增加入侵植物的竞争强度[45]。但也有不同的研究结果,如官玉婷等[1]研究发现:土壤养分异质性削弱了互花米草Spartina alterniflora对芦苇Phragmites australis的竞争优势。本研究中,无论是同质性还是异质性土壤,节节麦的相对产量总和均小于1,表明节节麦和小麦之间存在竞争关系,而节节麦与小麦的相对产量均小于1,表明两者的种内竞争小于其种间竞争。与同质性土壤相比,异质性土壤中节节麦的竞争平衡指数值同样大于0,并呈增加态势,表明土壤养分异质性增强了节节麦对小麦的竞争能力。
土壤养分异质性在较小尺度下可能会通过改变本地植物与入侵植物间的竞争平衡,从而有利外来植物的成功入侵[36]。但GAO等[46]研究认为:土壤养分异质性对入侵植物的生长一般具有积极影响,但不支持土壤养分异质性有利于外来植物在本地植物群落中成功入侵的观点。而本研究结果表明:土壤养分异质性一定程度上促进了节节麦的生长发育,并提高其对小麦的竞争作用,因此认为土壤养分异质性会进一步加剧节节麦对小麦的危害程度。
Effects of soil nutrient heterogeneity on competition between Aegilops tauschii and Triticum aestivum
-
摘要:
目的 土壤养分异质性在自然界中广泛存在,会对植物间的竞争关系造成影响。分析土壤养分异质性对入侵植物竞争能力的影响,可为其入侵危害研究提供参考。 方法 以入侵杂草节节麦Aegilops tauschii及其主要危害作物小麦Triticum aestivum为试材,设置同质性及异质性养分条件,结合de Wit取代实验方法,依据株高、叶面积及生物量等指标,探讨了土壤养分异质性对节节麦生长发育及其与小麦竞争关系的影响。 结果 ①土壤养分异质性促进了小麦和节节麦幼苗株高、叶面积及单株分蘖数的增加,2种植物总生物量增加显著(P<0.05)。②种间竞争条件下,异质性土壤中节节麦的根冠比降幅最大,表明节节麦通过将更多的生物量分配至地上以加大对小麦的竞争抑制作用。③从竞争平衡指数可知:异质性土壤中节节麦的竞争平衡指数大于0,并较同质性土壤中略有增加,表明土壤养分异质性一定程度上促进了节节麦对小麦的竞争作用。 结论 土壤养分异质性促进了节节麦幼苗的生长发育,并提高了其对小麦的竞争抑制作用。因此认为,土壤养分异质性会进一步加剧节节麦对小麦的危害程度。图5表1参46 Abstract:Objective Soil nutrient heterogeneity widely exists in nature, and affects competition among different plant species. This study aims to explore the effects of soil nutrient heterogeneity on competitiveness of invasive plants, so as to provide reference for the study of invasion hazards. Method The invasive plant Aegilops tauschii and its main endangered crop Triticum aestivum were used as test materials. Under the conditions of homogenous and heterogeneous nutrients, de Wit substitution experiment was carried out to investigate the impact of soil nutrient heterogeneity on the growth and development of A. tauschii and its competition with T. aestivum, based on plant height, leaf area and biomass. Result (1) Soil nutrient heterogeneity promoted the increase of plant height, leaf area and tiller number per plant of A. tauschii and T. aestivum seedlings. In particular, the total biomass of the two plants increased significantly (P<0.05). (2) Under the condition of interspecific competition, the root-shoot ratio of A. tauschii in heterogeneous soil decreased the most, indicating that A. tauschii increased its inhibition on T. aestivum competition by allocating more biomass to the ground surface. (3) Competition balance index showed that the competitiveness of A. tauschii in heterogeneous soil was above 0, and slightly increased compared with that in homogeneous soil, indicating that soil nutrient heterogeneity enhanced the competition of A. tauschii on T. aestivum. Conclusion Soil nutrient heterogeneity promotes the growth of A. tauschii seedling, and enhances its competitive inhibition on T. aestivum. [Ch, 5 fig. 1 tab. 46 ref.] -
Key words:
- heterogeneity /
- soil nutrient /
- Aegilops tauschii /
- competition /
- Triticum aestivum
-
表 1 不同土壤类型下节节麦与小麦的竞争关系
Table 1. Competitive relationship between A. tauschii and T. aestivum under soil nutrient heterogeneity
土壤类型 Ra Rb 相对产量总和 竞争平衡指数 同质性 0.921±0.022 a 0.901±0.016 a 0.911±0.011 a 0.022±0.001 a 异质性 0.914±0.041 a 0.867±0.014 a 0.891±0.022 a 0.053±0.015 a 说明:数值为平均值±标准误,同列不同小写字母表示不同土壤养分间差异显著(P<0.05) -
[1] 官玉婷, 秦天健, 牛雨欣, 等. 土壤养分异质性和种间竞争对互花米草和芦苇生长繁殖特性的影响[J]. 生态学杂志, 2018, 37(10): 2896 − 2904. GUAN Yuting, QIN Tianjian, NIU Yuxin, et al. Effects of soil nutrient heterogeneity and interspecific competition on growth and reproductive traits of Spartina alterniflora and Phragmites australis [J]. Chinese Journal of Ecology, 2018, 37(10): 2896 − 2904. [2] HODGE A. The plastic plant: root responses to heterogeneous supplies of nutrients [J]. New Phytologist, 2004, 162(1): 9 − 24. [3] HUTCHINGS M J, JOHN E A, WIJESINGHE D K. Toward understanding the consequences of soil heterogeneity for plant populations and communities [J]. Ecology, 2003, 84(9): 2322 − 2334. [4] van der WAAL C, de KROON H, HEITKÖNIG I M A, et al. Scale of nutrient patchiness mediates resource partitioning between trees and grasses in a semi-arid savanna [J]. Journal of Ecology, 2011, 99(5): 1124 − 1133. [5] MOMMER L, van RUIJVEN J, JANSEN C, et al. Interactive effects of nutrient heterogeneity and competition: implications for root foraging theory? [J]. Functional Ecology, 2012, 26(1): 66 − 73. [6] GOLIVETS M, WALLIN K F. Neighbour tolerance, not suppression, provides competitive advantage to non-native plants [J]. Ecology Letters, 2018, 21(5): 745 − 759. [7] WANG Yongjian, MÜLLER-SCHÄRER H, van KLEUNEN M, et al. Invasive alien plants benefit more from clonal integration in heterogeneous environments than natives [J]. New Phytologist, 2017, 216(4): 1072 − 1078. [8] CHEN Duo, ALI A, YONG Xiaohui, et al. A multi-species comparison of selective placement patterns of ramets in invasive alien and native clonal plants to light, soil nutrient and water heterogeneity [J]. Science of the Total Environment, 2019, 657: 1568 − 1577. [9] DAVIS M A, PELSOR M. Experimental support for a resource-based mechanistic model of invisibility [J]. Ecology Letters, 2001, 4(5): 421 − 428. [10] MELBOURNE B A, CORNELL H V, DAVIES K F, et al. Invasion in a heterogeneous world: resistance, coexistence or hostile takeover? [J]. Ecology Letters, 2007, 10(1): 77 − 94. [11] van SLAGEREN M W. Wild Wheats: a Monograph of Aegilops L. and Amblyopyrum (Jaub. & Spach) Eig (Poaceae) [M]. Wageningen: Wageningen Agricultural University, 1994. [12] MATSUOKA Y, TAKUMI S, KAWAHARA T. Intraspecific lineage divergence and its association with reproductive trait change during species range expansion in central Eurasian wild wheat Aegilops tauschii Coss. (Poaceae) [J/OL]. BMC Evolutionary Biology, 2015, 15: 213[2022-05-20]. doi: 10.1186/s12862-015-0496-9. [13] 张朝贤, 李香菊, 黄红娟, 等. 警惕麦田恶性杂草节节麦蔓延危害[J]. 植物保护学报, 2007, 34(1): 103 − 106. ZHANG Chaoxian, LI Xiangju, HUANG Hongjuan, et al. Alert and prevention of the spreading of Aegilops tauschii, a worst weed in wheat field [J]. Journal of Plant Protection, 2007, 34(1): 103 − 106. [14] ZHAO Bin, WU Tingting, MA Shanshan, et al. TaD27-B gene controls the tiller number in hexaploid wheat [J]. Plant Biotechnology Journal, 2020, 18(2): 513 − 525. [15] WANG Ning, CHEN Hao. Increased nitrogen deposition increased the competitive effects of the invasive plant Aegilops tauschii on wheat [J/OL]. Acta Physiologiae Plantarum, 2019, 41: 176[2022-05-20]. doi: 10.1007/s11738-019-2968-9. [16] 王宁, 袁美丽, 陈浩. 增施氮肥对节节麦与小麦苗期竞争的影响[J]. 中国土壤与肥料, 2018(5): 57 − 63. WANG Ning, YUAN Meili, CHEN Hao, et al. Effects of increased nitrogen application on the competitive performance of Aegilops tauschii and wheat at seedling stage [J]. Soils and Fertilizers Sciences in China, 2018(5): 57 − 63. [17] GENG Yupeng, PAN Xiaoyun, XU Chengyuan, et al. Phenotypic plasticity of invasive Alternanthera philoxeroides in relation to different water availability, compared to its native congener [J]. Acta Oecologica, 2006, 30(3): 380 − 385. [18] CAHILL Jr J F, MCNICKLE G G, HAAG J J, et al. Plants integrate information about nutrients and neighbors [J/OL]. Science, 2010, 328(5986): 1657[2022-05-18]. doi: 10.1126/science.1189736. [19] 肖强, 叶文景, 朱珠, 等. 利用数码相机和Photoshop软件非破坏性测定叶面积的简便方法[J]. 生态学杂志, 2005, 24(6): 711 − 714. XIAO Qiang, YE Wenjing, ZHU Zhu, et al. A simple non-destructive method to measure leaf area using digital camera and Photoshop software [J]. Chinese Journal of Ecology, 2005, 24(6): 711 − 714. [20] 王俊峰, 冯玉龙. 光强对两种入侵植物生物量分配、叶片形态和相对生长速率的影响[J]. 植物生态学报, 2004, 28(6): 781 − 786. WANG Junfeng, FENG Yulong. The effect of light intensity on biomass allocation, leaf morphology and relative growth rate of two invasive plants [J]. Chinese Journal of Plant Ecology, 2004, 28(6): 781 − 786. [21] de WIT C T. On competition [J]. Verslagen van Landouwkundige Onderzoekingen, 1960, 66: 1 − 82. [22] FOWLER N. Competition and coexistence in a North Carolina grassland: Ⅱ. the effects of the experimental removal of species [J]. The Journal of Ecology, 1981, 69(3): 843 − 854. [23] WILSON J B. Shoot competition and root competition [J]. Journal of Applied Ecology, 1988, 25(1): 279 − 296. [24] QIAN Yongqiang, LUO Dong, GONG Gu, et al. Effects of spatial scale of soil heterogeneity on the growth of a clonal plant producing both spreading and clumping ramets [J]. Journal of Plant Growth Regulation, 2014, 33(2): 214 − 221. [25] HE Weiming, ALPERT P, YU Feihai, et al. Reciprocal and coincident patchiness of multiple resources differentially affect benefits of clonal integration in two perennial plants [J]. Journal of Ecology, 2011, 99(5): 1202 − 1210. [26] WANG Zhengwen, van KLEUNEN M, DURING H J, et al. Root foraging increases performance of the clonal plant Potentilla reptans in heterogeneous nutrient environments [J/OL]. PLoS One, 2013, 8(3): e58602[2022-05-20]. doi: 10.1371/journal.pone.0058602. [27] GORCHOV D L, TRISEL D E. Competitive effects of the invasive shrub, Lonicera maackii (Rupr. ) Herder (Caprifoliaceae), on the growth and survival of native tree seedlings [J]. Plant Ecology, 2003, 166(1): 13 − 24. [28] 朱鹏锦, 杨莉, 师生波, 等. 模拟氮沉降对青藏高原地区油菜幼苗期生长和生理特性的影响[J]. 生物学杂志, 2012, 29(5): 56 − 59. ZHU Pengjin, YANG Li, SHI Shengbo, et al. Morphological and physiological responses of Brassica napus L. to mimic nitrogen deposition in the Tibetan Plateau [J]. Journal of Biology, 2012, 29(5): 56 − 59. [29] ZHOU Jian, DONG Bicheng, ALPERT P, et al. Effects of soil nutrient heterogeneity on intraspecific competition in the invasive, clonal plant Alternanthera philoxeroides [J]. Annals of Botany, 2012, 109(4): 813 − 818. [30] GAO Ying, XING Fu, JIN Yongjun, et al. Foraging responses of clonal plants to multi-patch environmental heterogeneity: spatial preference and temporal reversibility [J]. Plant and Soil, 2012, 359(1/2): 137 − 147. [31] 彭恒, 桂富荣, 李正跃, 等. 白茅对紫茎泽兰的竞争效应[J]. 生态学杂志, 2010, 29(10): 1931 − 1936. PENG Heng, GUI Furong, LI Zhengyue, et al. Competition effect of Imperata cylindrica to Ageratina adenophora [J]. Chinese Journal of Ecology, 2010, 29(10): 1931 − 1936. [32] 房锋. 节节麦(Aegilops tauschii Coss. )生态适应性[D]. 北京: 中国农业科学院, 2012. FANG Feng. Ecological Adaptability of Tausch’sgoatrass (Aegilops tauschii Coss. ) [D]. Beijing: Chinese Academy of Agricultural Science, 2012. [33] 王宁, 袁美丽, 王磊, 等. 入侵植物节节麦表型可塑性及竞争能力对模拟氮沉降的响应[J]. 草地学报, 2018, 26(6): 1428 − 1434. WANG Ning, YUAN Meili, WANG Lei, et al. The response of phenotypic plasticity and competitive ability of Aegilops tauschii Coss. to simulated nitrogen deposition [J]. Acta Agrestia Sinica, 2018, 26(6): 1428 − 1434. [34] HUTCHINGS M J, WIJESINGHE D K. Performance of a clonal species in patchy environments: effects of environmental context on yield at local and whole-plant scales [J]. Evolutionary Ecology, 2008, 22(3): 313 − 324. [35] LIANG Jinfeng, YUAN Weiying, GAO Junqin, et al. Soil resource heterogeneity competitively favors an invasive clonal plant over a native one [J]. Oecologia, 2020, 193(1): 155 − 165. [36] 袁伟影, 冯进, 张晓雅, 等. 入侵植物南美蟛蜞菊和本土蟛蜞菊生长对土壤养分的响应[J]. 生态学杂志, 2017, 36(4): 962 − 970. YUAN Weiying, FENG Jin, ZHANG Xiaoya, et al. Reponses of growth of Wedelia trilobata and W. chinensis to soil nutrients [J]. Chinese Journal of Ecology, 2017, 36(4): 962 − 970. [37] CHEN Baoming, SU Jinquan, LIAO Huixuan, et al. A greater foraging scale, not a higher foraging precision, may facilitate invasion by exotic plants in nutrient-heterogeneous conditions [J]. Annals of Botany, 2018, 121(3): 561 − 569. [38] AERTS R, CHAPIN III F S. The mineral nutrition of wild plants revisited: a re-evaluation of processes and patterns [J]. Advances in Ecological Research, 1999, 30: 1 − 67. [39] BLOOM R G, MALLIK A U. Indirect effects of black spruce (Piceamariana) cover on community structure and function in sheep laurel (Kalmia angustifolia) dominated heath of eastern Canada [J]. Plant and Soil, 2004, 265(1/2): 279 − 293. [40] AIKIO S, MARKKOLA A M. Optimality and phenotypic plasticity of shoot-to-root ratio under variable light and nutrient availabilities [J]. Evolutionary Ecology, 2002, 16(1): 67 − 76. [41] SHIPLEY B, MEZIANE D. The balanced-growth hypothesis and the allometry of leaf and root biomass allocation [J]. Functional Ecology, 2002, 16(3): 326 − 331. [42] SIEMANN E, ROGERS W E. Changes in light and nitrogen availability under pioneer trees may indirectly facilitate tree invasions of grasslands [J]. Journal of Ecology, 2003, 91(6): 923 − 931. [43] WEIGELT A, JOLLIFFE P. Indices of plant competition [J]. Journal of Ecologoy, 2010, 91(5): 707 − 720. [44] GIBSON D J, CONNOLLY J, HARTNETT D C, et al. Designs for greenhouse studies of interactions between plants [J]. Journal of Ecology, 1999, 87(1): 1 − 16. [45] FRANSEN B, de KROON H, BERENDSE F. Soil nutrient heterogeneity alters competition between two perennial grass species [J]. Ecology, 2001, 82(9): 2534 − 2546. [46] GAO Fanglei, HE Qiaosheng, ZHANG Yidan, et al. Effects of soil nutrient heterogeneity on the growth and invasion success of alien plants: a multi-species study [J/OL]. Frontiers in Ecology and Evolution, 2021, 8: 619861[2022-05-20]. doi: 10.3389/fevo.2020.619861. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20220370






 下载:
下载: