-
随着工业和城市化加速发展,矿产资源大量开采,以及化学产品(农药、化肥等)大量使用,使得各种重金属元素进入土壤造成严重的污染[1]。全球土壤都存在着不同程度上的重金属污染,目前全球平均排放汞、铅、铜、镍和锰的量分别为1.5×104,5.0×106,3.4×106,1.0×106和1.5×107 t[1]。2014年,国家环境保护部对中国土壤重金属污染的调查报告显示,中国有将近1/5的耕地,面积约为2×105 km2已经遭受到不同程度的重金属污染,而且因重金属污染而损失的粮食多达2.2×107 t·a-1[1],直接产生经济损失多达2×105万元·a-1[2]。在2014年全国土壤污染状况调查的14 278个点位中,铅、锌、汞、铜、铬、镍、砷等8种主要重金属污染源的超标率分别为7.0%,1.5%,0.9%,1.6%,2.1%,1.1%,4.8%和2.7%[2],8种重金属的超标率从大到小依次是镉、镍、砷、铜、汞、铅、铬和锌[2]。另外,土壤重金属污染具有隐蔽性、滞后性、积累性和多样性等特点,如有机氯农药“六六六”虽然在1992年就已经被禁用了,然而有些土壤中现在还能被检测出来[3]。
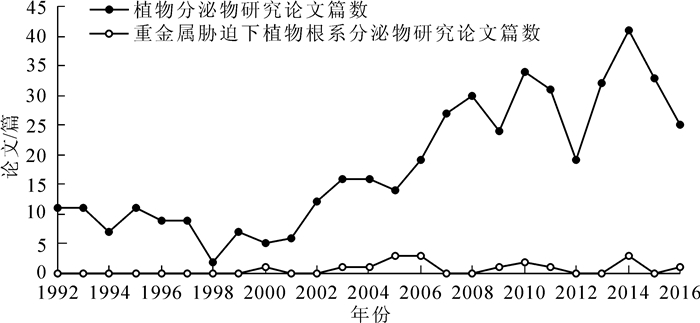
目前,土壤重金属污染的修复方法主要有传统修复和植物修复2类,但是传统修复存在着易产生二次污染和工艺复杂等问题,而植物修复显得更加的绿色环保。其中植物修复包括:①植物提取[4]。BAKER等[5]利用阿尔卑斯新蓂Thlaspi caerulesences修复了污泥导致的土壤的重金属污染证实了该方法的有效性[6]。②植物固定[7]。DUSHENKOV等[8]发现根系物分泌的磷酸盐能与铅发生反应生成难溶的磷酸铅固定在根部。③植物挥发。SOLODUCHO等[9]实验结果显示:洋麻Hibiscus cannabinus可以把根际土壤中的硒离子(Se3+)转化为甲基硒挥发掉,但是这些修复过程的修复时间长,2~3 a后它的修复效率还只有15%左右[9],而且一种植物只能修复一种重金属污染[10-11]。为了提高植物修复的效率,我们必须对植物根系分泌物进行深入探究。在中国知网收录的科学引文索引(SCI)期刊和核心期刊中通过主题检索“植物”+“分泌物”得到1992-2016年中国在植物分泌物中的研究论文发表篇数;我们同样通过主题检索“植物”+“根系分泌物”+“重金属”+“污染”得到中国在植物根系分泌物修复土壤重金属污染方面的研究论文数量。进行筛选整理后得到了1992-2016年中国知网上关于植物分泌物研究发表的论文篇数变化趋势图(图 1)。1992年至今有关植物分泌物研究论文的发表量整体呈现波动性增长趋势。从图 1可以明显发现:国内对植物分泌物的研究大致可以分为2个阶段。第1阶段是2000年以前,科学家们在这方面的研究成果甚少。第2阶段,在21世纪初,由于新研究设备和研究技术的开发,促进植物分泌物研究迅猛发展,呈现一个巨大跳跃阶段。从图 1我们还可以明显的看出:在国内对于植物根系分泌物领域的研究还处于比较年轻阶段[12],而且每年在这方面的研究论文发表量较低,可见此领域的研究在今后研究中需要更进一步的深入。
-
根系分泌物是指某些植物在其生长发育过程通过根系向根际环境释放的有机化合物总称[13]。在1795年时PLENK首次发现植物根系在其生活史内能不断的向根际土壤释放一些化学物质。在19世纪初科学家HARTMANN等[14]曾提出根际定义促进了植物根系分泌物的研究发展,而且他也曾指出根际土壤存在的理化性质差异是由这些根系分泌物质的性质所引起[15]。在20世纪50年代,ROVIRA等[16]对根土界面根系分泌物做了系统研究,在这之后现代仪器分析技术行业迅速崛起,尤其是高效液相色谱和气相色谱的研发和普及,各大实验室都具备了系统性研究根系分泌物的能力[17]。在最近几年里,在环境科学、植物营养学、土壤学等领域对植物根系分泌物展开广泛性地研究,使得植物根系分泌物成为各国科研人员研究热点[18]。
-
在学术界,科学家们对于植物根系分泌物分类依据一直有不同的见解。第1种分类方法根据分泌物来源来划分(表 1),包括渗出物、脱落物与分解物、黏胶质和分泌物[13]。第2种为广大学者所接受的分类方法,是根据分泌物的不同性质和分子量大小来划分(表 1),其中包括大分子量有机化合物和小分子有机化合物[19]。其中小分子有机化合物主要包括有机酸、氨基酸以及可溶性糖类,它们具备相当强的络合、鳌合能力;另外大分子量有机化合物,主要指凝胶类物质,包括胞外酶等。它们是一种吸附性强、黏性强以及有润湿作用的大分子有机物质[20]。这2种分类依据从学术性上面来说不存在哪种方法更准确之说,而需要根据我们实验的具体需求来选择,甚至有些科研项目需要同时使用这2个分类方法。
表 1 根系分泌物的种类及特点
Table 1. Types and characteristics of root exudates
分类 种类 特点 1 分泌物 在植物细胞新陈代谢过程中根系细胞主动分泌到外界的有机物质 黏胶质 根冠细胞、植物细胞中未形成次生壁的那些表皮细胞和根毛部位释放出来的黏胶状物质 脱落物与分解物 从死亡或者破裂的细胞向外界释放的有机物质 渗出物 细胞主动扩散出来的一类低分子量的化合物 2 小分子量有机化合物 有机酸、各种氨基酸以及可溶性糖类 大分子量有机化合物 主要是指凝胶类物质,包括胞外酶等 -
根据研究资料统计,植物根系不同部位向土壤环境中释放的根系分泌物种类有200多种[21]。其中有包括糖类、有机酸、酶、生长素和氨基酸等(表 2)。其中根系分泌的有机酸可以影响土壤中有毒金属形态。可溶性糖、有机酸和氨基酸是目前研究较多的根系分泌物组分。在重金属胁迫条件下,植物一般能够分泌出大量低分子量有机酸,如柠檬酸、苹果酸、草酸等[22]。如铅胁迫下秋茄树Kandelia obovata分泌的有机酸主要是草酸[23]。在铝胁迫条件下不同植物分泌的有机酸种类有草酸(荞麦Fagopyrum esculentum),苹果酸(麦Triticum aestivum,油菜Brassica campestris)和柠檬酸(油菜)等[24]。这些有机化合物可以活化土壤中难溶态重金属化合物,继而促进超级累植物对其吸收富集作用[25-26]。
表 2 根系分泌物分泌的有机质组分
Table 2. Organic components of root exudates
有机物类别 各类有机物的组成 糖类 葡萄糖,果糖,半乳糖,核糖,木糖,蔗糖,阿拉伯糖,棉籽糖,多糖,麦芽糖 有机酸 酒石酸,草酸,乙酸,丙二酸,马来酸,苹果酸,乙醛酸,延胡索酸,水杨酸,乳酸 氨基酸 甲梳氨酸,络氨酸,脯氨酸,组氨酸,α-丙氨酸,天冬氨酸,精氨酸 酶类 蛋白酶,RNA酶,转化酶,磷酸酶,DNA酶,硝酸酶,淀粉酶 生长素 生物素,植物生长素,维生素 固醇类 胆固醇,豆留醇 -
植物根系分泌物收集根据植物种类和实验的需求分为以下3种方法[27-28]:①基质培养收集法,②水培收集法,③土培收集法。
-
以石英砂等作为基质,把植物培养于基质中一段时间,取出基质用蒸馏水洗去基质表面吸附的培养液,再用有机溶液浸泡,提取出基质表面吸附的有机物质便是根系分泌物[29]。该方法的培养基质(石英砂和珍珠岩等)不易与根系分泌物反应,便于我们后期的实验处理,用试剂处理过的固体容易吸附根系分泌物中的某些极性物质,如芳香族化合物等。KUDOYAROVA等[30]曾通过分根的方式把小麦的幼苗培养在砂子基质中来进行小麦根系分泌物的收集。
-
主要以BENZARTI的方法为依据,根据不同种植物做略微调整来对植物根系分泌物进行收集。先将植物在营养液中培养一定时间后,把植株取出用蒸馏水洗去植物根系表面吸附的养分离子,再把它放入含微生物抑制剂的清水中培养一段时间,最后用树脂除去溶液中营养元素,剩下的便是根系分泌物溶液[31]。CIMMINO等[32]在研究黑麦Secale cereale根系分泌物的组分时也采用了该种方法进行收集。该法适用于在实验条件下根系分泌物的收集,它既有效地避免植物根系损伤,便于单因子调控;也确保了所收集到根系分泌物的组分更完整,含量更准确,避免了土壤微生物的分解作用[33]。但通过该法收集到的分泌物种类较多,分泌物之间易发生化学反应;而且它是在实验条件下收集的,和自然条件下收集的结果存在着误差[34],而且植物根系长时间浸泡在培养液中易发生缺氧使得根系腐烂。
-
将植物幼苗种植于事先准备好的土壤中,使其地上部分生长在含有标记放射性同位素环境中,培养数天后取其根际土壤进行过滤,检测其滤出物中标记同位素便可确定该植物根系分泌物的组成[35]。使用该种方法对植物根系分泌物的收集,完全模拟了自然条件下植物生长环境,所以它收集到的根系分泌物组分和含量变化与自然状况下的基本上一致,使得检测数据更加准确。此法还是存在着许多不足之处[36]:植物根系分泌物易与土壤微生物发生化学反应,从而使得鉴定结果不准确;土壤微生物在自身代谢过程中向外分泌的一些酸类、有机化合物等也会对实验结果产生一定的影响。综上所述,虽然各种收集方法都有自己的适用性,但它们都存在着一个共性问题,通过以上方法收集到根系分泌物都不包括微生物作用后而分泌的那些分泌物,不能代表植物在田间环境下根系所分泌的物质[37]。为此,随着科学技术飞速发展,我们需要不断地研究出几种更加完整、准确、先进的收集方法。
-
植物根系分泌物收集完成后,需要对它们进行分离和提纯,分离提纯方法的选取得根据待测组分性质来确定。常用的方法主要有衍生法和萃取法等2类[38]。其中萃取法又可细分为3类[39](表 3):①树脂法(细分为吸附法和离子交换法);②固相根区萃取法;③溶剂萃取法。我们可以根据实验的实际要求来合理的选择分离提纯方法,尽可能地将实验误差降到最低。
表 3 常见的几种分离提纯方法各自的特点
Table 3. Several common methods of separation and purification of their respective characteristics
方法 特点 衍生法 衍生化法对于现在的研究者来说较实用,它主要通过生成衍生化合物使待测部分更容易被分离检测,而且不含杂质[38]离子交换法虽然分离再生容易、吸附量大以及二次污染小[49],但这个方法有一个较大的缺陷,即:样品试剂 离子交换法 浪费量大(样品的需求量和有机洗脱试剂的需求量也比一般的方法要大的多),实验耗时较长,因此并没有被研究者广泛使用[50] 吸附法 吸附法是充分利用吸附树脂具有吸附效果好、脱附再生容易、性能稳定、适用范围宽和实用性好的优点,对根系分泌物进行一个吸附以及分离提纯的作用,该方法对于研究者来说具有良好选择性[39]固相根区萃取法是一种用于植物根际土壤中分泌物检测的新方法。该方法是以聚二甲硅氧烷作为分泌物的吸 固相根区萃取法 附材料。相比于树脂管萃取法,虽然聚二甲硅氧烷材料吸附效果更好,但是由于它的特殊性不能广泛地被采用,而且易产生交叉污染,应用范围小[51] 溶剂萃取法 溶剂萃取法是目前被研究者采纳最多的一种方法。虽然该方法操作简单、所用的设备廉价,但也存在着许多不足之处:对样品和有机试剂的需求量大、实验步骤繁琐,耗时长、试验试剂容易浪费污染环境以及该种方法一次只能对根系分泌物中的一种组分进行分离鉴定,为此不能准确地推断出该组分在根系分泌物中所有的组分中的含量[52] -
植物根系分泌物的种类多,迄今为止已被检测出来的分泌物种类有200种左右[40],其中含量高的有可溶性糖、有机酸、氨基酸、酶类等,但是对于植物根系分泌物的组分和含量的鉴定仍然是难点之一[41]。目前,最常用的鉴定方法是采用先进仪器技术——核磁共振种技术和气相色谱-质谱技术[42]。核磁共振除了得到大量信息,还可以精确测定某些分泌化合物的分子空间构型,但是测试成本较高[43]。气相色谱-质谱联用技术具有高灵敏度,拥有较为广阔的数据检索库的特点,这有助于根系分泌物的组分鉴定[44]。罗庆等[45]利用该技术对超积累东南景天Sedum alfredii的根系分泌物进行鉴定,检测出根系分泌物中的58种化合物,其中检测出含量最多的便是有机酸类物质。
目前,对于根系分泌物中含量最多的有机酸鉴定常用以下5种[46-47]:①气相色谱法;②高效液相色谱法;③离子色谱法;④光谱鉴;⑤液相色谱-质谱联用法。前3种可以合并为1种:色谱法。在目前的研究中,采用最多的是第2种和第5种,其中高效液相色谱法主要对于那些已知分泌物组分条件下的定性化以及定量化鉴定,该种检测方法的操作简单,成本低,适用性广[48];而色谱-质谱联用技术主要是对于哪些含量极低且分泌物组分还不确定的化合物鉴定,该种鉴定方法不仅分离度好,操作容易,而且对于根系分泌物组分鉴定的准确度高[53]。
以上这些鉴定方法都只是对于根系分泌物中提纯出来的那部分物质进行鉴定,无法对根系分泌物整体进行准确鉴定,鉴定结果还受到鉴定方法等的影响。为此开发更完善、更准确、适用性更广的根系分泌物鉴定方法,对于在根系分泌物的研究领域起着极为重要的作用。
-
前面已经阐述植物根系分泌物组分有机酸、可溶性糖、酶类以及黏胶质等,这些化学物质反应植物与土壤,植物与植物之间,植物与根际微生物之间的化学、物理、生物关系,也参与它们之间的各种反应。因此,我们可以利用植物根系分泌物来进行土壤质量改良,作物自身耐性提高等,尤其在土壤污染方面(重金属污染、有机污染)发挥着巨大作用。为此,笔者整理分析了近几年在土壤污染植物修复方面的研究成果,绘制根系分泌物在土壤环境中的化学物理生物反应过程图(图 2)。
-
植物根系分泌物大部分属于有机化合物,如许多金属蛋白[54],它能与土壤中重金属元素进行螯合反应[55],使得重金属元素在根际环境中形成一种相对稳定的难溶化合物,从而使重金属元素在土壤中移动性能降低,得到的一定的固定作用[56]。张汝民等[57]通过实验证实超积累植物可以分泌金属结合蛋白与土壤中重金属离子进行螯合反应。INSKEEP等[58]研究发现植物根系分泌的有些有机酸对铁离子,锌离子结合有促进作用。
-
研究表明:现在已知的超积累植物能够向根际土壤分泌一些特殊有机化合物来活化重金属[59],其中氨基酸和有机酸这2种分泌物的络合重金属能力最强。氨基酸和有机酸主要与根际土壤环境中的铅、砷、锌、铬等重金属元素进行活化反应[59],使它们的生物有效性增加,便于植物对其吸收、转运和富集,使根际土壤中各类或者某一类重金属含量得以下降[60],植物根系分泌物活化土壤重金属的途径如图 3。另外,有研究显示:2种生态型东南景天的根系分泌物都具有活化土壤中难溶化合物的能力,而且超积累生态型东南景天活化能力更强[61]。KRISHNAMURTI等[62]研究报道一些低分子量的有机酸能促进土壤对镉的释放,增加它的有效性。HUANG等[63]研究发现荠菜Capsella bursa-pastoris分泌的有机酸含量与它体内吸收的铀含量呈正相关。
-
植物根系分泌物清除有机污染物主要通过间接降解和直接降解这2种途径来实现,即促进微生物繁殖提高其活性的间接降解[64]和通过其分泌酶组成酶系统直接降解[65]。第2种途径已有研究证实,在外酶作用下能将高毒的有机化合物降解为低毒形态的有机化合物。根系向土壤中释放的酶系统以直接降解途径对土壤环境中的有机污染物如三氯乙烯(TCE),三硝基甲苯(TNT)等进行分解,从而降低它们的毒性[66]。有研究证实硝酸盐还原酶能降解TNT等有机废弃物。另外,旷远文等[67]对小麦和玉米Zea mays幼苗产生的分泌物进行研究表明,它们促进土壤中二二三(DDT)等有机物降解。TOYAMA等[68]研究表明:芦苇Phragmites australis根系分泌物中酚类化合物提高了苯并芘的生物降解能力。GAO等[69]通过向菲和萘污染的土壤中添加人工合成根系分泌物(ARE),发现ARE对土壤中多环芳烃具有显著的解吸附作用。YOSHITOMI等[70]研究表明,玉米根系产生的分泌物对多环芳烃的降解有促进作用。也有研究证实土壤环境中有机磷的降解主要靠植物根系分泌物中的酸性磷酸酶以及真菌产生的酸性(碱性)磷酸酶等[71]。
-
有研究表明当植物组织内某一营养元素缺乏时,植物会过量分泌某种根分泌物到根际土壤中,使土壤中含有该种营养元素的难溶态化合物得到活化[72],从而大大提高了植物对该种营养元素的吸收利用率,缓解植物对该种营养元素的缺乏症状,达到自身营养调节的目的[73]。苗欣宇等[74]研究显示:在缺铁逆境中,植物根系会增加麦根酸类物质的分泌应对缺铁环境。李德华等[75]和章爱群等[76]的研究发现:植物在缺磷土壤环境中植物会通过增加草酸、苹果酸等的分泌来活化难溶态磷。在低钾环境胁迫下,富钾基因型根系分泌可溶性糖、氨基酸和有机酸的能力强于一般基因型,促进土壤中难溶态钾活化[77]。
-
植物根系能够不停地向根际释放出大量的含碳物质[78],该类化合物为根基微生物生长、繁殖提供充足碳源,对微生物生存代谢起到了促进作用[79]。根际微生物能和根系本身都能够向外分泌许多有机化合物,其中包括有机酸、铁载体、溶磷等化合物,该类化合物有利于根际环境中的某些特定重金属的降解[80]。也有研究显示,大部分对植物生长发育有着促进作用的根际微生物,均能向外分泌有机酸、铁载体等有机化合物,降低铁、锌等重金属对植物产生的毒害作用[81],增加植物体内可溶性糖含量,提升植物在铁、锌胁迫环境下的耐性。
-
根系分泌物对稳定性高的团聚体形成有促进作用[82-83]。VYMAZAL等[84]认为植物根系分泌产生的高分子黏胶质对土壤颗粒有很强黏着力。有科学家对玉米根际土壤稳定性团聚体含量进行调查发现:玉米根际环境中的稳定性团聚体量远远大于其在非根际土壤中的量。这是由于黏胶质中所含的多糖物质与黏土矿物共同形成了一个有机—无机联结体。BAETZ等[85]的研究证实:种植过黑麦和小麦的土壤中,直径大于9.50 mm的团聚体明显下降,直径为0.25~9.50 mm的团聚体却显著增加。
-
在以上的介绍中我们对根系分泌物的研究进程和研究创新点都有了比较明确的认识。研究显示:根系分泌物在消除土壤有机污染,减缓重金属污染,改善土壤的理化性质以及在逆境中调节植物本身的生长状况等方面已经有相当大的研究成果,然而对于毛竹Phyllostachys edulis的根系分泌物在这些方面的研究成果甚少,为此我们开展毛竹根系分泌物作用机制以及作用效果的研究具有重要的理论价值和实践意义[86]。若毛竹根系分泌物能有效的解决以上问题,再加上其自身拥有的生物量大生长快的优点,有望成为土壤重金属污染修复的候选植物之一。
Research progress of soil plant root exudates in heavy metal contaminated soil
-
摘要: 根系分泌物不仅是植物与根际进行物质交换的载体,还参与植物修复污染土壤的各个环节。通过查阅1992-2016年国内外关于根系分泌物的研究成果,对根系分泌物分类的依据、常用收集鉴定方法的适用性,及其在土壤修复中的作用方面等进行了综述。通过植物根系分泌物的提取鉴定方法以及对污染土壤修复机理影响等方面的系统梳理,揭示了目前中国在植物根系分泌物研究的研究体系以及在今后的研究中所需要突破的方向。植物修复作为典型的绿色、环保的修复技术近年来应用广泛,但修复效率低、耗时长等一系列现实问题,一直是困扰该技术大面积应用的重要瓶颈,而加强根系分泌物在植物修复中作用的研究是解决这一问题的关键。通过对以往该领域的研究文献的分析,系统阐明了根系分泌物在土壤中的物理、化学、生物作用,为重金属污染土壤的植物修复工程的研究提供理论支撑和技术指导。Abstract: Root exudates are the carrier of material exchange between plant and rhizosphere, which are also involved in phytoremediation of contaminated soil links. The classification basis, methods applicability and remediation effects of root exudates in soil were reviewed among the literature of China and abroad in 1992-2016 in present paper. Through the systematic analysis on the extraction and identification methods of plant root exudates and its effect on contaminated soil remediation mechanism, the present research system and breakthrough in the future was revealed. Phytoremediation is a green and environmental remediation technology, and which was used widely in recent years. However, low efficiency and long time-consuming were its important bottleneck. The key to solving these problems is to accelerate the study of the role of root exudates in phytoremediation. Through the analysis of the previous research literature in this field, the physical, chemical and biological effects of root exudates were clarified systematically, which provide theoretical support technical guidance for the study of phytoremediation of heavy metal contaminated soil in the future.
-
Key words:
- soil science /
- phytoremediation /
- root exudates /
- soil heavy metal /
- review
-
表 1 根系分泌物的种类及特点
Table 1. Types and characteristics of root exudates
分类 种类 特点 1 分泌物 在植物细胞新陈代谢过程中根系细胞主动分泌到外界的有机物质 黏胶质 根冠细胞、植物细胞中未形成次生壁的那些表皮细胞和根毛部位释放出来的黏胶状物质 脱落物与分解物 从死亡或者破裂的细胞向外界释放的有机物质 渗出物 细胞主动扩散出来的一类低分子量的化合物 2 小分子量有机化合物 有机酸、各种氨基酸以及可溶性糖类 大分子量有机化合物 主要是指凝胶类物质,包括胞外酶等 表 2 根系分泌物分泌的有机质组分
Table 2. Organic components of root exudates
有机物类别 各类有机物的组成 糖类 葡萄糖,果糖,半乳糖,核糖,木糖,蔗糖,阿拉伯糖,棉籽糖,多糖,麦芽糖 有机酸 酒石酸,草酸,乙酸,丙二酸,马来酸,苹果酸,乙醛酸,延胡索酸,水杨酸,乳酸 氨基酸 甲梳氨酸,络氨酸,脯氨酸,组氨酸,α-丙氨酸,天冬氨酸,精氨酸 酶类 蛋白酶,RNA酶,转化酶,磷酸酶,DNA酶,硝酸酶,淀粉酶 生长素 生物素,植物生长素,维生素 固醇类 胆固醇,豆留醇 表 3 常见的几种分离提纯方法各自的特点
Table 3. Several common methods of separation and purification of their respective characteristics
方法 特点 衍生法 衍生化法对于现在的研究者来说较实用,它主要通过生成衍生化合物使待测部分更容易被分离检测,而且不含杂质[38]离子交换法虽然分离再生容易、吸附量大以及二次污染小[49],但这个方法有一个较大的缺陷,即:样品试剂 离子交换法 浪费量大(样品的需求量和有机洗脱试剂的需求量也比一般的方法要大的多),实验耗时较长,因此并没有被研究者广泛使用[50] 吸附法 吸附法是充分利用吸附树脂具有吸附效果好、脱附再生容易、性能稳定、适用范围宽和实用性好的优点,对根系分泌物进行一个吸附以及分离提纯的作用,该方法对于研究者来说具有良好选择性[39]固相根区萃取法是一种用于植物根际土壤中分泌物检测的新方法。该方法是以聚二甲硅氧烷作为分泌物的吸 固相根区萃取法 附材料。相比于树脂管萃取法,虽然聚二甲硅氧烷材料吸附效果更好,但是由于它的特殊性不能广泛地被采用,而且易产生交叉污染,应用范围小[51] 溶剂萃取法 溶剂萃取法是目前被研究者采纳最多的一种方法。虽然该方法操作简单、所用的设备廉价,但也存在着许多不足之处:对样品和有机试剂的需求量大、实验步骤繁琐,耗时长、试验试剂容易浪费污染环境以及该种方法一次只能对根系分泌物中的一种组分进行分离鉴定,为此不能准确地推断出该组分在根系分泌物中所有的组分中的含量[52] -
[1] 樊霆, 叶文玲, 陈海燕, 等.农田土壤重金属污染状况及修复技术研究[J].生态环境学报, 2013, 22(10):1727-1736. FAN Ting, YE Wenling, CHEN Haiyan, et al. Review on contamination and remediation technology of heavy metal in agricultural soil[J]. Ecol Environ Sci, 2013, 22(10):1727-1736. [2] 环境保护部, 国土资源部. 全国土壤污染状况调查公报[R/OL]//http://www.gov.cn/foot/site1/20140417/782bcb88840814ba158d01.pdf. [3] 邢艳帅, 乔冬梅, 朱桂芬, 等.土壤重金属污染及植物修复技术研究进展[J].中国农学通报, 2014, 30(17):208-214. XING Yanshuai, QIAO Dongmei, ZHU guifen, et al. Research progress of heavy pollution in soil and phytoremediation technology[J]. Chin Agric Sci Bull, 2014, 30(17):208-214. [4] 陈靖, 林振景, 孟媛媛, 等.土壤重金属污染的植物修复及超富集植物的研究进展[J].中国环境管理干部学院学报, 2011, 21(1):69-71. CHEN Jing, LIN Zhenjing, MENG Yuanyuan, et al. Research progress on phytoremediation for heavy metal contamination in soil and hyperaccumulators[J]. J Environ Manage Coll China, 2011, 21(1):69-71. [5] BAKER A J M, MCGRATH S P, SIDOLI C M D, et al. The possibility of in situ heavy metal decontamination of polluted soils using crops of metal-accumulating plants[J]. Resour Conserv Recycl, 1994, 11(1/4):41-49. [6] 张知贵, 王明贤, 杨华, 等.植物根系分泌物研究进展[J].广东农业科学, 2013(2):219-222. ZHANG Zhigui, WANG Mingxian, YANG Hua, et al. The research status of plant root exudates[J]. Guangdong Agric Sci, 2013(2):219-222. [7] PILON-SMITS E. Phytoremediation[J]. Annu Rev Plant Biol, 2005, 56(1):15-39. [8] DUSHENKOV V, KUMAR P B, MOTTO H, et al. Rhizofiltration:the use of plants to remove heavy metals from aqueous stream[J]. Environ Sci Technol, 1995, 29(5):1239-1245. [9] SOLODUCHO J, CABAJ J. Phenolic compounds hybrid detectors[J]. J Biomater Nanobiotechnol, 2013, 4(3):17-27. [10] 钟斌, 陈俊任, 彭丹莉, 等.速生林木对重金属污染土壤植物修复技术研究进展[J].浙江农林大学学报, 2016, 33(5):899-909. ZHONG Bin, CHEN Junren, PENG Danli, et al. Research progress of heavy metal phyteremediation technology of fast-growing forest tree in soil[J]. J Zhejiang A & F Univ, 2016, 33(5):899-909. [11] HARRISON S J, LEPP N W, PHIPPS D A. Uptake of copper by excised roots:(Ⅳ) copper uptake from complexed sources[J]. Z Pflanzenphysiol, 1984, 113(5):445-450. [12] 李汛, 段增强.植物根系分泌物的研究方法[J].基因组学与应用生物学, 2013, 32(4):540-547. LI Xun, DUAN Zengqiang. Progress on the research methods for root exudates[J]. Genom Appl Biol, 2013, 32(4):540-547. [13] 郭晓方, 卫泽斌, 许田芬, 等.不同pH值混合螯合剂对土壤重金属淋洗及植物提取的影响[J].农业工程学报, 2011, 27(7):96-100. GUO Xiaofang, WEI Zebin, XU Tianfen, et al. Effects of mixture of chelating agents with different pH values on phytoextraction and heavy metals removal[J]. Trans Chin Soc Agric Eng, 2011, 27(7):96-100. [14] HARTMANN A, ROTHBALLER M, SCHMID M. Lorenz Hiltner, a pioneer in rhizosphere microbial ecology and soil bacteriology research[J]. Plant Soil, 2008, 312(1):7-14. [15] 朱丽霞, 章家恩, 刘文高.根系分泌物与根际微生物相互作用研究综述[J].生态环境, 2003, 12(1):102-105. ZHU Lixia, ZHANG Jiaen, LIU Wengao. Review of studies on interactions between root exudates and rhizopheric microorganisms[J]. Ecol Environ, 2003, 12(1):102-105. [16] ROVIRA A D, FOSTER R C, MARTIN J K. Note on terminology:origin, nature and nomenclature of the organic material in the rhizosphere[G]//HARLEY J L, RUSSELL R S. The Soil-Root Interface. London:Academic Press, 1979:1-4. [17] GUO Wei, ZHANG Huayong, HUO Shouliang. Organochlorine pesticides in aquatic hydrophyte tissues and surrounding sediments in Baiyangdian wetland, China[J]. Ecol Eng, 2014, 67(2):150-155. [18] 徐卫红, 王宏信, 刘怀, 等. Zn, Cd单一及复合污染对黑麦草根分泌物及根际Zn, Cd形态的影响[J].环境科学, 2007, 28(9):2089-2095. XU Weihong, WANG Hongxin, LIU Huai, et al. Effects of individual and combined pollution of Cd and Zn on root exudates and rhizosphere Zn and Cd fractions in ryegrass (Loliurn perenne L.)[J]. Environ Sci, 2007, 28(9):2089-2095. [19] 姜海燕, 袁秀英, 樊石磊.胡杨根际土壤化感物质成分分析[J].内蒙古农业大学学报(自然科学版), 2011, 32(2):48-51. JIANG Haiyan, YUAN Xiuying, FAN Shilei. Composition analysis of soil allelochemicals in Populus euphratica rhizosphere[J]. J Inner Mongolia Agric Univ Nat Sci Ed, 2011, 32(2):48-51. [20] BESSONBARD A, GRAVOT A, RICHAUD P, et al. Nitric oxide contributes to cadmium toxicity in Arabidopsis by promoting cadmium accumulation in roots and by up-regulating genes related to iron uptake[J]. Plant Physiol, 2009, 149(3):1302-1315. [21] ZENG Fanrong, CHEN Song, MIAO Ying, et al. Changes of organic acid exudation and rhizosphere pH in rice plants under chromium stress[J]. Environ Poll, 2008, 155(2):284-289. [22] CARBALLEIRA T, RUIZ I, SOTO M. Effect of plants and surface loading rate on the treatment efficiency of shallow subsurface constructed wetlands[J]. Ecol Eng, 2016, 90(1):203-214. [23] XIE Xiangyu, WEISS D J, WENG Bosen, et al. The short-term effect of cadmium on low molecular weight organic acid and amino acid exudation from mangrove (Kandelia obovata Yong) roots[J]. Environ Sci Poll Res, 2013, 20(2):997-1008. [24] 潘声旺, 袁馨, 刘灿, 等.苯并[α]芘对不同修复潜力羊茅属植物的根系分泌物中几种低分子量有机物的影响[J].植物生态学报, 2016, 40(6):604-614. PAN Shengwang, YUAN Xin, LIU Can, et al. Effects of benzo[α] pyrene on the organic compounds of low molecule weight excreted by root systems in five Festuca species with different remediation potentials[J]. Chin J Plant Ecol, 2016, 40(6):604-614. [25] NAIDU R, HARTER R D. Effect of different organic ligands on cadmium sorption by and extractability from soils[J]. Soil Sci Soc Am J, 1998, 62(3):644-650. [26] LU Lingli, TIAN Shengke, YANG Xiao'e, et al. Improved cadmium uptake and accumulation in the hyperaccumulator Sedum alfredii:the impact of citric acid and tartaric acid[J]. J Zhejiang Univ Sci B BiomBiotechnol, 2013, 14(2):106-114. [27] KRUMINS J A, GOODEY N M, FGALLAGHER F. Plant soil interactions in metal contaminated soils[J]. Soil Biol Biochem, 2015, 80:224-231. [28] LI Xiaopang, DING Changfeng, HUA Ke, et al. Soil sickness of peanuts is attributable to modifications in soil microbes induced by peanut root exudates rather than to direct allelopathy[J]. Soil Biol Biochem, 2014, 78:149-159. [29] BOEUF-TREMBLAY V, PLANTUREUX S, GUCKERT A. Influence of mechanical impedance on root exudation of maize seedlings at two development stages[J]. Plant Soil, 172(2):279-287. [30] KUDOYAROVA G R, MELENTⅡEV A I, MARTYNENKO E V, et al. Cytokinin producing bacteria stimulate amino acid deposition by wheat roots[J]. Plant Physiol Biochem, 2014, 83:285-291. [31] DIEZ J A, DUSENBERY D B. Repellent of root-knot nematodes from exudate of host roots[J]. J Chem Ecol, 15(10):2445-2455. [32] CIMMINO A, FERNÁNDEZ-APARICIO M, AVOLIO F, et al. Ryecyanatines A and B and ryecarbonitrilines A and B, substituted cyanatophenol, cyanatobenzodioxple, and benzodiox-olecarbonitriles from rye(Secale cereale L.)root exudates:novel metabolites with allelopathic activity on Orobanche seed germination and radicle growth[J]. Phytochemistry, 2015, 109:57-65. [33] 杨瑞吉, 牛俊义.磷胁迫对油菜根系分泌物的影响[J].西南农业大学学报(自然科学版), 2006, 6(6):895-899. YANG Ruiji, NIU Junyi. Effects of phosphorus deficiency on root exudation of rape (Brassica campestris L.)[J]. J Southwest Agric Univ Nat Sci, 2006, 6(6):895-899. [34] HORCHHANI F, GALLUSCI P, BALDET P, et al. Prolonged root hypoxia induces ammonium accumulation and decreases the nutritional quality of tomato fruits[J]. J Plant Physiol, 2008, 165(13):1352-1359. [35] ZHANG Fusuo, TREEBY M, RÖMHELD V, et al. Mobilization of iron by phytosiderophore as affected by other micronutrients[J]. Plant Soil, 1991, 130(1/2):173-178. [36] 张文明, 邱慧珍, 张春红, 等.马铃薯根系分泌物成分鉴别及其对立枯丝核菌的影响[J].应用生态学报, 2015, 26(3):859-866. ZHANG Wenming, QIU Huizhen, ZHANG Chunhong, et al. Identification of chemicals in root exudates of potato and their effects on Rhizoctonia solani[J]. Chin J Appl Ecol, 2015, 26(3):859-866. [37] LUO Yongming, CHRISTIE P. Alkaline sewage sludge solidsaffectthe chemical speciation and bio availability of Cu and Zn in the rhizosphere soil solution[J]. Soil Scid Plant Nutr, 1997, 43(special issue):1041-1046. [38] 陶波, 赵微, 韩玉军, 等.假苍耳根系分泌物对土壤中微生物的影响[J].东北农业大学学报, 2010, 41(2):15-19. TAO Bo, ZHAO Wei, HAN Yujun, et al. Effect of Iva xanthifolia root secretion on soil microorganisms amount[J]. J Northeast Agric Univ, 2010, 41(2):15-19. [39] 孙海燕. 基于微萃取技术的根系分泌物分析及其化感作用研究[D]. 哈尔滨: 哈尔滨工业大学, 2014. SUN Haiyan. Research on Root Exudate Analysis Based on Microextraction and Allellopathic Effect[D]. Harbin:Harbin Institute of Technology, 2014. [40] 马凤鸣, 王安娜, 吴蕾, 等.大豆根系分泌物的鉴定及PAL1, PAL2, C4H的克隆[J].作物杂志, 2011(2):65-71. MA Fengming, WANG Anna, WU Lei, et al. Identification of soybean root exudates and cloning of the PAL1, PAL2, C4H genes[J]. Crops, 2011(2):65-71. [41] 杨先国, 刘塔斯, 陈斌, 等.丹参根际土壤浸提物的GC-MS分析[J].中国农学通报, 2013, 29(10):173-177. YANG Xianguo, LIU Tasi, CHEN Bin, et al. GC-MS analysis of rhizosphere-soil extract of Salvia miltiorrhiza Bge[J]. Chin Agric Sci Bull, 2013, 29(10):173-177. [42] SOROABELL M R, HERNÁNDEZFERNÁNDEZ A, SOTOCARREÑO F, et al. Inoculation responses with beneficial microorganisms in gerbera taking into account rhizosphere characterization[J]. Rev Chap Ser Hortic, 2009, 15(2):41-48. [43] 谢明吉, 严重玲, 叶菁.菲对黑麦草根系几种低分子量分泌物的影响[J].生态环境, 2008, 17(2):576-579. XIE Mingji, YAN Chongling, YE Jing. Effect of phenanthrene on the secretion of low molecule weight organic compounds by ryegrass root[J]. Ecol Environ, 2008, 17(2):576-579. [44] 杜茜, 卢迪, 马琨.马铃薯连作对土壤生物群落结构和功能的影响[J].生态环境学报, 2012, 12(7):1252-1256. DU Qian, LU Di, MA Kun. Effect of potato continuous cropping on soil microbial community structure and function[J]. Ecol Environ Sci, 2012, 21(7):1252-1256. [45] 罗庆, 孙丽娜, 胡筱敏.镉超富集植物东南景天根系分泌物的代谢组学研究[J].分析化学, 2015, 43(1):7-12. LUO Qing, SUN Lina, HU Xiaomin. Metabonomics study on root exudates of Cd hyperaccumulator Sedum alfredii[J]. Chin J Analyt Chem, 2015, 43(1):7-12. [46] DINKCI N, AKALIN A S, GÖNC S, et al. Isocratic reverse-phase HPLC for determination of organic acids in Kargí tulum cheese[J]. Chromatographia, 2007, 66(1):45-49. [47] EHLING S, COLE S. Analysis of organic acids in fruit juices by liquid chromatography-mass spectrometry:an enhanced tool for authenticity testing[J]. J Agric Food Chem, 2011, 59(6):2229-2234. [48] 胡蓉, 乙引, 伍庆. RP-HPLC法测定植物根系中有机酸含量[J].贵州农业科学, 2007, 35(2):20-21. HU Rong, YI Yin, WU Qing. Determination of organic acids with low molecular weight in plant roots by RP-HPLC[J]. Guizhou Agric Sci, 2007, 35(2):20-21. [49] HAO Zhengping, WANG Qing, CHRISTIEP P, et al. Allelopathic potential of watermelon tissues and root exudates[J]. Sci Hortic, 2007, 112(3):315-320. [50] CANVIN D T, BEEVER H. Sucrose synthesis from ac-etate in the germinating castor bean kinetics and pathway[J]. J Biol Chem, 1998, 236(4):988-995. [51] YU Jingquan, MATSUI Y. Phytotoxic substances in root exu-dates of cucumber(Cucumis sativus L.)[J]. J Chem Ecol, 1994, 20(1):21-31. [52] BLARI A C, HANSON B D, BRUNK G R, et al. New techniques and findings in the study of a candidate allelochemical implicated in invasion success[J]. Ecol Lett, 2005, 8(10):1039-1047. [53] 涂书新, 吴佳.植物根系分泌物研究方法评述[J].生态环境学报, 2010, 19(9):2493-2500. TU Shuxin, WU Jia. A review on research methods of root exudates[J]. Ecol Environ Sci, 2010, 19(9):2493-2500. [54] 唐新莲, 韦进进, 李耀燕, 等.在铝胁迫下黑麦根系分泌的柠檬酸和苹果酸的解毒机制的研究[J].广西农业科学, 2006, 25(4):325-340. TANG Xinlian, WEI Jinjin, LI Yaoyan. Studies on Al-detoxification mechanism of both citrate and malate secreted from roots of rye under Al stress[J]. J Guangxi Agric Biol Sci, 2006, 25(4):325-340. [55] PIÑEROS M A, MAGALHAES J V, CARVALHO ALVES V M, et al. The physiology and biophysics of an aluminum tolerance mechanism based on root citrate exudation in maize[J]. Plant Physiol, 2002, 129(3):1194-1206. [56] LI Xiaofeng, MA Jianfeng, MATSUMOTO H. Pattern of Al-induced secretion of organic acids differs between rye and wheat[J]. Plant Physiol, 2000, 123(4):1537-1543. [57] 张汝民, 张丹, 陈宏伟, 等.梭梭幼苗根系分泌物提取方法的研究[J].干旱区资源与环境, 2007, 21(3):153-157. ZHANG Rumin, ZHANG Dan, CHEN Hongwei, et al. Study on the extracts methods of the root exudates from the seedling of Haloxylon ammodendron (C. A. Mey.) Bunge[J]. J Arid Land Resour Environ, 2007, 21(3):153-157. [58] INSKEEP W P, COMFORT S D. Thermodynamic prediction for the effect of root exudates on mental speciation in the rhizosphere[J]. Plant, 1986, 9(3):567-586. [59] ZENG Fanrong, CHEN Song, MIAO Ying, et al. Changes of organic acid exudation and rhizosphere pH in rice plants under chromium stress[J]. Environ Poll, 2008, 155(2):284-289. [60] 陈英旭, 林琦, 陆芳, 等.有机酸对铅、镉植株危害的解毒作用研究[J].环境科学学报, 2000, 20(4):467-472. CHEN Yingxu, LIN Qi, LU Fang, et al. Study on detoxication of organic acid to raddish under the stress of Pb and Cd[J]. Acta Sci Circumst, 2000, 20(4):467-472. [61] 王紫娟, 刘万学, 蔡静萍, 等.紫茎泽兰根系分泌物对旱稻的化感作用[J].现代农业科技, 2007(16):71-72. WANG Zijuan, LIU Wanxue, CAI Jingping, et al. Eupatorium upland rice root exudates on Allelopathy[J]. Mod Agric Sci Technol, 2007(16):71-72. [62] KRISHNAMURTI G S R, CIESLINSKI G, HUANG P M, et al. Kinetic of cadmium release from soils as influenced by organic acids:implication in cadmium avail-ability[J]. J Environ Qual, 1997, 26:271-277. [63] HUANG Jianwei, BLAYLOCK M J, KAPULNIKY, et al. Phytoremediation of uranium-contaminated soils:role of organic acids in triggering uranium hyperaccumulation in plants[J]. Environ Sci Technol, 1998, 32(13):2004-2008. [64] SANDAMANN E R I C, LOOS M A. Enumeration of 2, 4-D-Degrading microorganisms in soils and crop plant rhizospherws using indication media:high populations associated with sugarcane (Saccharum officinarum)[J]. Chemosphere, 1984, 13(9):1073-1084. [65] MACEK T, MACKOVÁM, J KÁŠ J. Exploitation of plantsforthe removal of organics in environmental remediation[J]. Biotechnol Adv, 2000, 18(1):23-34. [66] KANEKO M, YOSHIMURA E, NISHIZAWA N K, et al. Time course study of aluminum-induced callose formation roots as observed digital microscopy and low-vacuum scanning electron microscopy[J]. Soil Sci Plant Nutr, 2002, 45(3):701-712. [67] 旷远文, 温达志, 钟传文, 等.根系分泌物及其在植物修复中的作用[J].植物生态学报, 2003, 27(5):709-717. KUANG Yuanwen, WEN Dazhi, ZHONG Chuanwen, et al. Root exudates and their roles in phytoremediation[J]. Acta Phytoecol Sin, 2003, 27(5):709-717. [68] TOYAMA T, FURUKAWA T, MAEDA N, et al. Accelerated biodegradation of pyrene and benzo[a] pyrene in the Phragmites australis rhizosphere by bacteria-root exudate interactions[J]. Water Res, 2012, 45(4):1629-1638. [69] GAO Yanzheng, REN Lili, LING Wanting, et al. Desorption of phenanthrene and pyrene in soils by root exudates[J]. Bioresour Technol, 2010, 101(4):1159-1165. [70] YOSHITOMI K J, SHANN J R. Corn (Zea mays L.) root exudates and their impact on 14C-pyrene mineralization[J]. Soil Biol Biochem, 2001, 33(12):1769-1776. [71] YAN Dazhong, MAO Lingqi, LI Cunzhi, et al. Biodegradation of hexachlorobenzene by a constructed microbial consortium[J]. World J Microbiol Biotechnol, 2015, 31(2):371-377. [72] 章云云, 朱端卫, 王晓, 等.植物根系分泌物的作用及其与药用植物连作障碍的关系[J].湖北农业科学, 2014, 53(6):1241-1245. ZHANG Yunyun, ZHU Duanwei, WANG xiao, et al. Properties of plant root exudates and its obstacles for continuous cropping of medicinal plants[J]. Hubei Agric Sci, 2014, 53(6):1241-1245. [73] 李振侠, 徐继忠, 高仪, 等.苹果砧木SH40和八棱海棠缺铁胁迫下根系有机酸分泌的差异[J].园艺学报, 2007, 34(2):279-282. LI Zhenxia, XU Jizhong, GAO Yi, et al. Difference of organic acid exudation from roots of SH40 and balenghaitang under iron-deficiency stress[J]. Acta Hortic Sin, 2007, 34(2):279-282. [74] 苗欣宇, 周启星.污染土壤植物修复效率影响因素研究进展[J].生态学杂志, 2015, 34(3):870-877. MIAO Xinyu, ZHOU Qixing. Some research progresses in influencing factors for the efficiency of contaminated soil phytoremediation[J]. Chin J Ecol, 2015, 34(3):870-877. [75] 李德华, 向春雷, 姜益泉, 等.低磷胁迫下水稻不同品种根系有机酸分泌的差异[J].中国农学通报, 2005, 21(11):186-189. LI Dehua, XIANG Chunlei, JIANG Yiquan, et al. Difference of organic acid secretion form roots of various rice varieties under the stress of low phosphorus[J]. Chin Agric Sci Bull, 2005, 21(11):186-189. [76] 章爱群, 贺立源, 赵会娥, 等.根分泌物对活化土壤中难溶性磷的作用[J].水土保持学报, 2008, 22(5):102-105. ZHANG Aiqun, HE Liyuan, ZHAO Huie, et al. Effects of root exudates on mobilizing insoluble phosphate in soils[J]. J Soil Water Conserv, 2008, 22(5):102-105. [77] 李廷轩, 马国瑞, 张锡洲.富钾基因型籽粒苋主要根系分泌物及其对土壤矿物态钾的活化作用[J].应用生态学报, 2006, 17(2):368-372. LI Tingxuan, MA Guorui, ZHANG Xizhou. Root exudates of potassium-enrichment genotype grain amaranth and their activation on soil mineral potassium[J]. Chin J Appl Ecol, 2006, 17(2):368-372. [78] 李廷轩, 马国瑞, 张锡洲, 等.籽粒苋不同富钾基因型根系分泌物中有机酸和氨基酸的变化特点[J].植物营养与肥料学报, 2005, 11(5):647-652. LI Tingxuan, MA Guorui, ZHANG Xizhou, et al. Change characteristics of organic acid and amino acid in root exudates in different grain amaranth genotypes[J]. Plant Nutr Fert Sci, 2005, 11(5):647-652. [79] 左元梅, 张福锁.不同禾本科作物与花生混作对花生根系质外体铁的累积和还原力的影响[J].应用生态学报, 2004, 15(2):221-225. ZUO Yuanmei, ZHANG Fusuo. Effects of peanut mixed cropping with different gramineous plants on apoplast iron accumulation and reducing capacity of peanut[J]. Chin J Appl Ecol, 2004, 15(2):221-225. [80] BAETZ U, MARTINOIA E. Root exudates:the hidden part of plant defense[J]. Trends Plant Sci, 2014, 19(2):90-98. [81] 常学秀, 段昌群, 王焕校.根分泌作用与植物对金属毒害的抗性[J].应用生态学报, 2000, 11(2):315-320. CHANG Xuexiu, DUAN Changqun, WANG Huanxiao. Root excretion and plant resistance to metal toxicity[J]. Chin J Appl Ecol, 2000, 11(2):315-320. [82] 贺永华, 沈东升, 朱荫湄.根系分泌物及其根际效应[J].科技通报, 2006, 22(6):761-766. HE Yonghua, SHEN Dongsheng, ZHU Yinmei. Root exudates and their rhizospheric effects[J]. Bull Sci Technol, 2006, 22(6):761-766. [83] 桑伟莲, 孔繁翔.植物修复研究进展[J].环境科学进展, 1999, 7(3):40-44. SANG Weilian, KONG Fanxiang. Progress of study on phytoremediation[J]. Adv Environ Sci, 1999, 7(3):40-44. [84] VYMAZAL J, BŘEZINOVÁT. The use of constructed wetlands for removal of pesticides from agricultural runoff and drainage:a review[J]. Environ Int, 2015, 75:11-20. [85] BAETZ U, MARTINOIA E. Root exudates:the hidden part of plant defense[J]. Trends Plant Sci, 2014, 19(2):90-98. [86] 周紫球, 邱永华, 周建革, 等.毛竹笋对土壤重金属吸收能力初探[J].浙江林业科技, 2013, 33(6):61-63. ZHOU Ziqiu, QIU Yonghua, ZHOU Jiange, et al. Preliminary report on absorbing capacity of soil heavy metal by Phyllostachy pubescens shoot[J]. J Zhejiang For Technol, 2013, 33(6):61-63. [87] GRATANI L, CRESCENTE M F, VARONE L, et al. Growth pattern and photosynthetic activity of different bamboo species growing in the botanical garden of Rome[J]. Flora-Morphol Distr Funct Ecol Plant, 2008, 203(1):77-84. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.2017.06.023







 下载:
下载: