-
磷(P)是植物生长发育不可或缺的必需矿物质营养,不仅作为核酸、磷脂和腺苷三磷酸(ATP)的组成成分参与遗传信息传递与能量代谢[1],还在光合磷酸化、糖类转运及逆境信号传导中发挥关键作用[2]。磷在土壤中具有高流动性和强有机物结合性,但溶解性低,这使得其可利用浓度被限制在约10 μmol·L−1[3]。全球约30%的耕地土壤有效磷浓度低于5 μmol·L−1,中国南方红壤区磷固定率高达70%~90%,严重制约农林生态系统生产力[4]。为适应低磷胁迫,植物进化出由磷酸盐转运蛋白(PHT)介导的复杂调控网络,通过根际酸化、菌根共生及磷转运体激活等多层次机制提高磷获取效率[5]。目前,PHT基因家族在拟南芥Arabidopsis thaliana[6]、水稻Oryza sativa[7]、玉米Zea mays[8]和毛果杨Populus trichocarpa[9]等模式植物中被系统解析。植物PHT家族通常被分为个不同亚家族,分别为PHT1~PHT5[10]。植物PHT1亚家族属于无机磷酸盐/氢离子(Pi/H+)共转运蛋白家族,不仅负责将磷从衰老组织再分配至活跃发育组织,同时维持植物与丛枝菌根(AM)间的磷吸收和共生关系[11]。PHT2、PHT3和PHT4定位于细胞质和质体、线粒体和高尔基膜之间进行能量代谢,PHT5家族在液泡中介导磷的储存和适应功能[12]。PHT1亚家族是植物PHT蛋白家族中受到最广泛关注和深入研究的一类,包含12个跨膜结构域(TM),这些结构域被TM6和TM7间的大亲水环分成2个组[13]。在拟南芥和水稻中分别鉴定出9、13个PHT1基因[6−7]。PHT1通过感知细胞膜内外H+含量梯度差异,参与从土壤到植物细胞的无机磷酸盐获取。YE等[14]研究发现:OsPHT1;4在水稻根表皮细胞中特异性表达,过表达OsPHT1;4能够诱导不同无机磷酸盐水平下植物体内无机磷酸盐含量增加。杨少辉等[15]研究表明:低磷胁迫诱导ThPHT1;8在盐芥Thellungiella salsuginea根部表达,其转基因拟南芥幼苗无机磷酸盐和总磷含量显著提高。
闽楠Phoebe bournei为樟科Lauraceae楠属Phoebe常绿乔木,是中国南方珍贵树种,木材呈金黄色,有金丝,纹理细腻,气味芳香,具有千年不腐特性,且干燥时不易变形,是高档家具和古建筑修复的不可替代材料[16]。天然闽楠林主要分布于福建、江西、湖南、浙江、广西等省份,这些区域土壤pH通常较低(pH为4.5~5.5),活性铝含量高,导致磷元素易被固定形成难溶性磷酸盐[17]。前期调查显示:闽楠人工林土壤有效磷质量分数常低于3 mg·kg−1,仅为杉木Cunninghamia lanceolata林的1/3[18],但闽楠仍能维持较高生长速率,表明其可能已进化出磷高效吸收和利用的策略。然而,目前关于闽楠抗逆机制的研究多集中于干旱响应[19]和高温响应[20],对磷胁迫适应的分子机制,尤其是PHT基因家族的系统研究尚未见报道。
近年来,林木基因组学研究取得突破性进展,闽楠全基因组测序的完成为其抗逆基因挖掘提供了重要契机[21]。本研究基于闽楠染色体级基因组数据,对PHT基因家族进行了全基因组鉴定与系统分析,包括蛋白理化性质、系统发育进化、基因结构、保守基序、染色体定位、启动子顺式元件及种内共线性关系,并结合低磷胁迫下的表达模式筛选耐低磷的关键候选基因,以期为闽楠磷高效利用的遗传改良及樟科树种抗逆育种提供科学依据。
-
从拟南芥信息资源数据库(TAIR)下载拟南芥PHT基因家族蛋白质序列,利用TBtools软件进行Blast序列比对,获取闽楠PHT基因家族候选序列[22]。利用美国国家生物技术信息中心(NCBI)的CD-Search功能和简单模块化结构研究工具(SMART)数据库预测所得候选序列保守结构域,去除无典型保守结构域的序列,最终确定闽楠PHT基因家族成员。利用ExPASy的ProtParam工具进行蛋白质氨基酸数量、分子量、理论等电点等理化性质分析。
-
基于闽楠PTH基因注释(GFF)文件,通过GSDS 2.0在线网站分析闽楠PHT基因结构。根据闽楠PHT基因编码序列(CDS)和基因组序列,利用在线工具MEME Suite,并设置Motifs数量为10,分析闽楠PHT保守基序。
-
根据拟南芥和闽楠PHT蛋白序列,使用MEGA软件,采用邻近法(NJ)并重复1 000次(Bootstrap为1 000),构建系统发育进化树。利用在线工具ITOL对进化树进行分组注释和美化。
-
基于闽楠PHT (PbPHT)基因组文件和基因注释(GFF)文件,采用TBtools软件的Gene Location Visualize from GTF/GFF工具绘制PbPHT基因在染色体上的位置。
-
使用TBtools软件提取PbPHT基因序列转录起始位点上游2 000 bp序列,使用PlantCARE在线网站对PbPHT启动子顺式作用元件进行预测与分析[23]。
-
选取长势一致的2个家系(分别为“靖安”和“宜丰”) 1年生闽楠幼苗进行低磷胁迫处理,对照组和处理组各20株。栽植方式为沙培,对照组(ck)采用全营养液,低磷胁迫组(LP)采用不含磷的营养液(其余营养因子均相同),每3 d浇1次营养液。处理90 d后,分根、茎、叶取样,液氮速冻后,放置−80 ℃超低温冰箱保存。
-
采用RNA植物多糖多酚提取试剂盒(TIANGEN,北京)对闽楠幼苗根(R)、茎(S)、叶(L)分别提取RNA,茎和叶RNA等量混合后用于后续实验。使用Prime Script TMRT reagent Kit(Perfect Real Time)试剂盒(Takara,北京)反转录合成cDNA。利用在线引物设计软件Primer3以PbPHTs基因编码序列(CDS)为模板设计特异性引物,用于实时荧光定量PCR (RT-qPCR)实验。使用CFX96™ Real-Time PCR检测系统(Bio-Rad,美国)。RT-qPCR反应体系配制:SYBR Green 5.0 μL,上下游引物(10 μmol·L−1)各0.2 μL,模板0.8 μL,ddH2O 3.8 μL。反应程序为:95 ℃预变性3 min,95 ℃ 5 s,60 ℃ 30 s,重复40个循环。PbEF1α作为内参基因,按照2−∆∆Ct法计算目的基因相对表达量。利用SPSS软件进行差异显著性t检验分析,利用GraphPad Prism绘图。
-
利用TBtools对闽楠基因组进行Blast得到48个PHT基因家族成员,这些成员都包含7~13个跨膜结构域(TMD),都属于MFS家族。在5个亚家族中,PHT1亚家族包含11个成员,PHT2包含3个成员,PHT3包含24个成员,PHT4包含7个成员,PHT5包含3个成员。
-
PbPHT蛋白分子量为30 459.27 Da (PbPHT3.17)~183 230.14 Da (PbPHT1.10),编码的氨基酸个数在294(PbPHT3.8)~1 616(PbPHT1.10),理论等电点介于5.24~10.42,其中只有PbPHT1.1、PbPHT1.9、PbPHT5.1、PbPHT5.2和PbPHT5.3是酸性蛋白;大多数成员不稳定系数小于40,为稳定蛋白;少数成员总平均亲水性小于0,为亲水性蛋白(表1)。
表 1 闽楠PHT基因家族成员基本信息
Table 1. Basic information of PHT gene family members in P. bournei
基因亚
家族基因
名称氨基酸
个数分子量/
Da理论等
电点不稳定
系数总平均亲水性
(疏水性值)基因亚
家族基因
名称氨基酸
个数分子量/
Da理论等
电点不稳定
系数总平均亲水性
(疏水性值)PbPHT1 PbPHT1.1 507 54 765.73 5.24 39.28 0.545 PbPHT3.11 358 39 645.54 8.75 36.80 −0.091 PbPHT1.2 530 58 479.04 8.93 33.88 0.315 PbPHT3.12 319 35 300.06 9.55 43.06 0.089 PbPHT1.3 537 59 193.72 8.89 35.11 0.237 PbPHT3.13 334 36 558.13 9.22 42.31 0.176 PbPHT1.4 502 55 614.00 8.67 34.11 0.223 PbPHT3.14 307 32 921.16 9.61 26.56 0.187 PbPHT1.5 517 57 636.40 8.23 31.45 0.392 PbPHT3.15 320 35 397.16 9.45 34.67 0.048 PbPHT1.6 518 57 496.88 8.64 40.07 0.298 PbPHT3.16 324 36 565.27 10.02 34.93 −0.167 PbPHT1.7 539 59 846.77 8.71 33.07 0.280 PbPHT3 PbPHT3.17 297 30 459.27 9.30 28.97 0.194 PbPHT1.8 540 58 915.49 8.70 29.74 0.339 PbPHT3.18 371 39 530.93 9.31 38.18 0.175 PbPHT1.9 518 56 223.84 5.63 40.43 0.480 PbPHT3.19 356 38 492.35 9.67 40.40 0.031 PbPHT1.10 1 616 183 230.14 8.19 41.99 −0.205 PbPHT3.20 331 36 539.20 9.44 43.61 −0.034 PbPHT1.11 643 68 331.42 9.65 44.19 0.431 PbPHT3.21 357 38 616.78 9.50 28.79 0.059 PbPHT2 PbPHT2.1 563 58 858.67 9.25 37.54 0.591 PbPHT3.22 309 33 535.18 9.75 28.70 0.127 PbPHT2.2 575 60 303.32 9.33 32.08 0.558 PbPHT3.23 830 91 273.52 8.84 47.18 −0.256 PbPHT2.3 600 66 144.24 8.63 39.25 0.312 PbPHT3.24 512 54 414.49 9.56 45.15 −0.056 PbPHT3.1 852 93 137.34 8.97 32.01 0.025 PbPHT4.1 523 57 210.16 9.62 28.75 0.436 PbPHT3.2 305 32 965.29 9.65 38.93 0.160 PbPHT4.2 518 56 338.01 10.42 44.45 0.404 PbPHT3.3 375 40 068.61 9.23 40.17 0.156 PbPHT4.3 447 48 404.23 9.40 31.46 0.643 PbPHT3.4 377 40 224.75 9.17 40.17 0.151 PbPHT4 PbPHT4.4 558 61 176.23 9.01 47.73 0.303 PbPHT3 PbPHT3.5 509 56 637.27 6.16 32.06 −0.111 PbPHT4.5 543 59 672.97 8.07 95.17 0.301 PbPHT3.6 323 35 219.36 10.01 39.00 −0.048 PbPHT4.6 597 66 446.46 9.31 43.72 0.221 PbPHT3.7 328 35 570.73 8.64 36.53 −0.048 PbPHT4.7 444 48 173.82 9.46 39.81 0.671 PbPHT3.8 294 30 501.51 9.40 32.82 0.243 PbPHT5.1 698 78 009.36 5.90 39.10 0.202 PbPHT3.9 304 32 616.12 9.60 37.30 0.217 PbPHT5 PbPHT5.2 698 78 280.51 5.44 45.68 0.187 PbPHT3.10 394 43 729.81 9.63 43.75 −0.194 PbPHT5.3 697 77 812.15 6.13 40.47 0.185 -
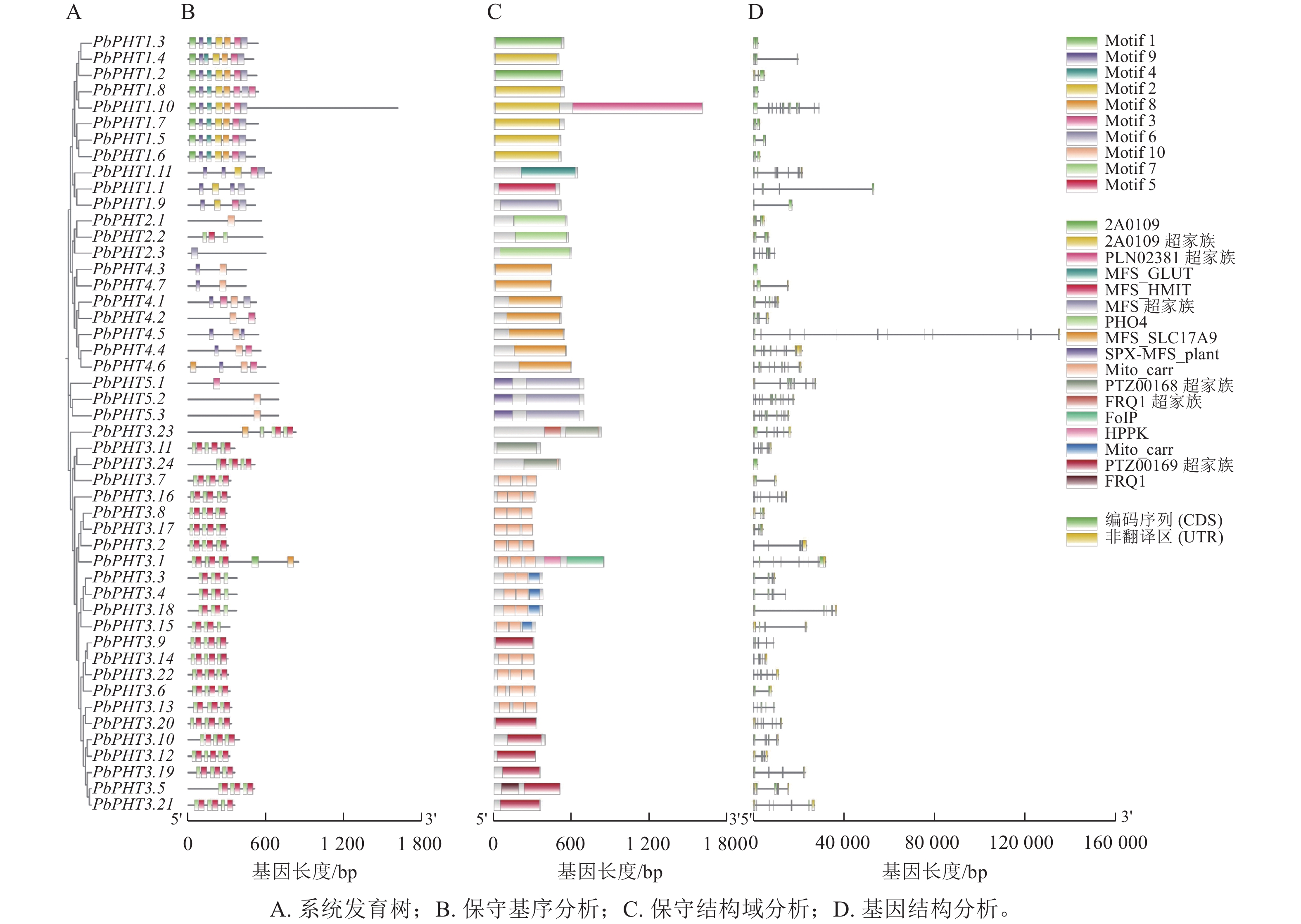
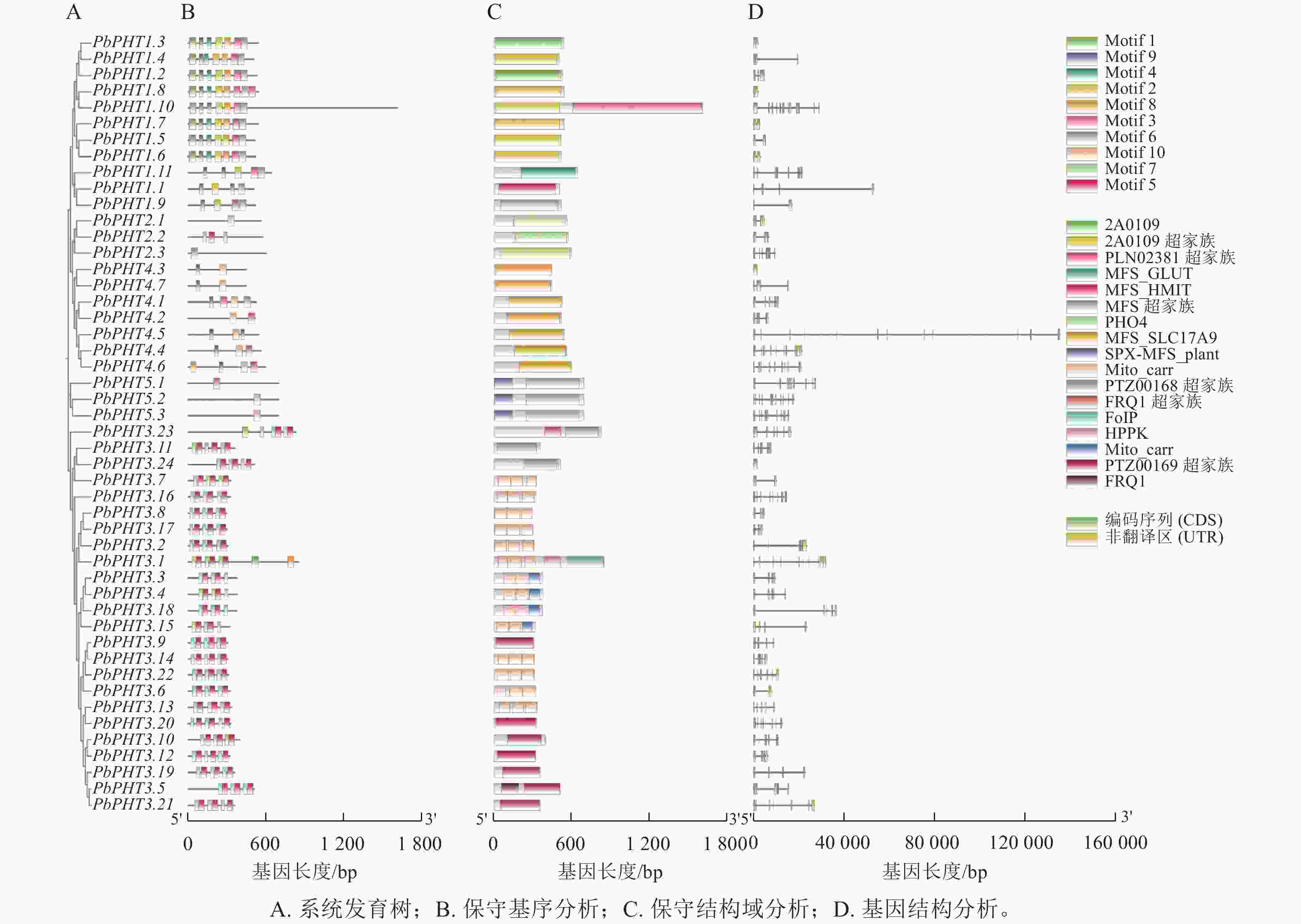
由图1可见:闽楠PHT基因有1~12个外显子。保守基序和结构域分析表明:闽楠PHT成员没有完全统一的基序,但是各亚家族内部表现出较好的一致性。除了PHT1亚家族PbPHT1.3和PbPHT1.8、PHT3亚家族PbPHT3.24、PHT4亚家族PbPHT4.3外,其余基因均具有内含子。例如,PHT1亚家族中8个成员具有Motif 1、Motif 2、Motif 3、Motif 4、Motif 6、Motif 8和Motif 9;PHT3亚家族成员都具有Motif 5和Motif 7;PHT4亚家族中6个成员都具有Motif 9和Motif 10。
-
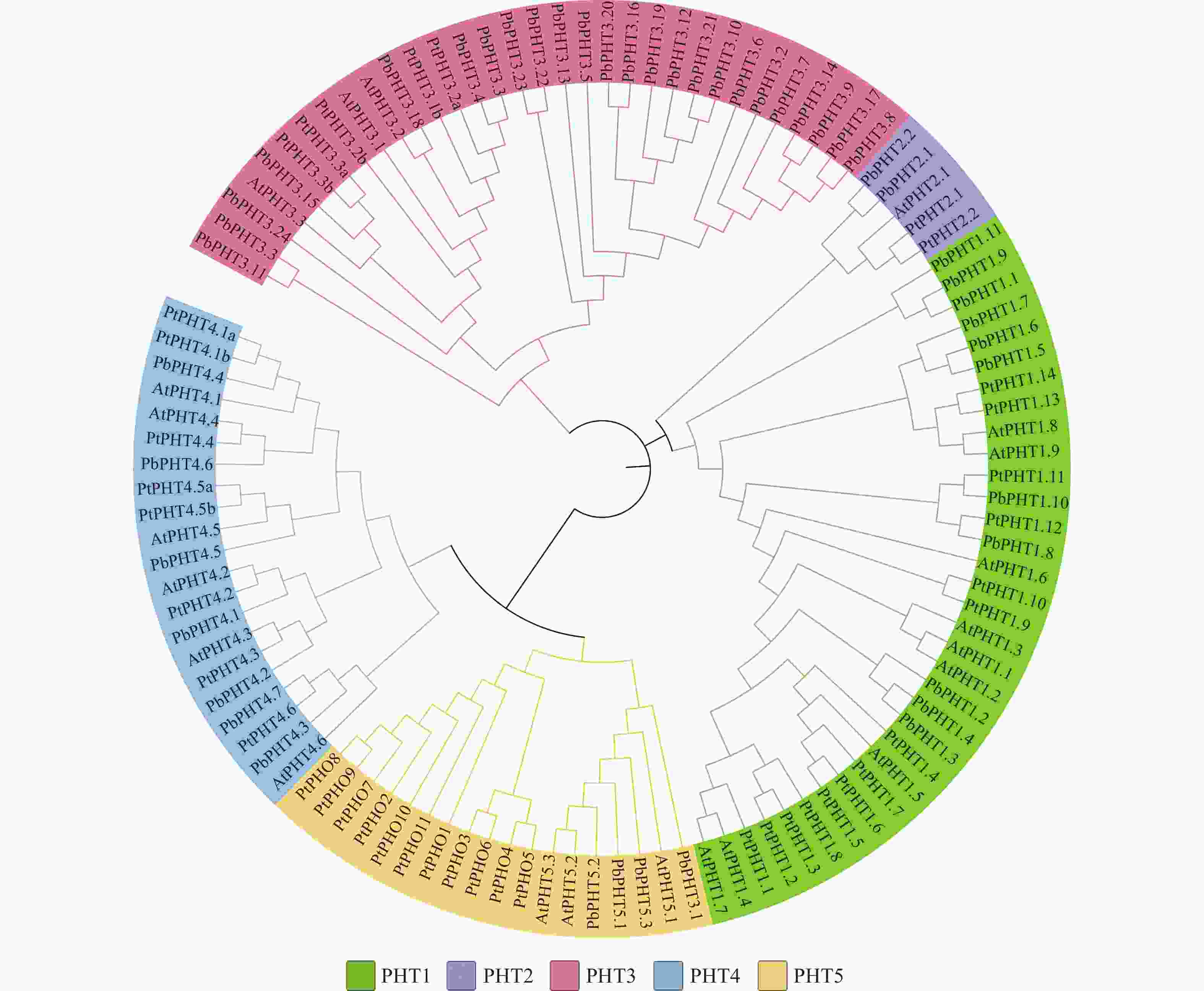
利用拟南芥、毛果杨和闽楠共112条PHT蛋白序列,采用邻近法构建系统进化树。图2表明:112个PHT蛋白质可分为PHT1、PHT2、PHT3、PHT4和PHT5共5个亚家族,PbPHTs蛋白在各亚家族中分布不均匀,在PHT2亚家族仅有2个PbPHTs蛋白,而在PHT3亚家族中,则有24个成员。
-
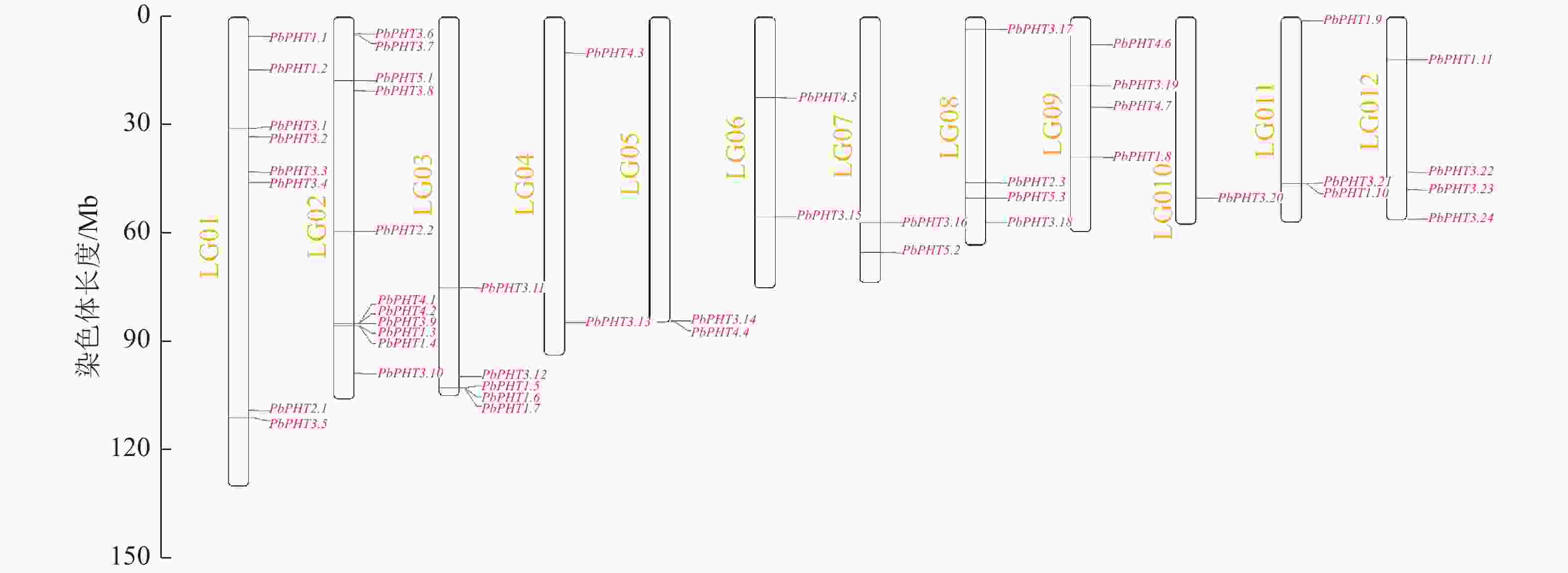
图3表明:闽楠PHT基因不均匀分布在12条染色体上,第4、5、6、7条染色体上各有2个PHT基因,第8、9、12条染色体各有4个PHT基因,第1条染色体有8个PHT基因,第2条染色体有11个PHT基因,第3条染色体有5个PHT基因,第10条染色体有1个PHT基因,第11条染色体有3个PHT基因。
-
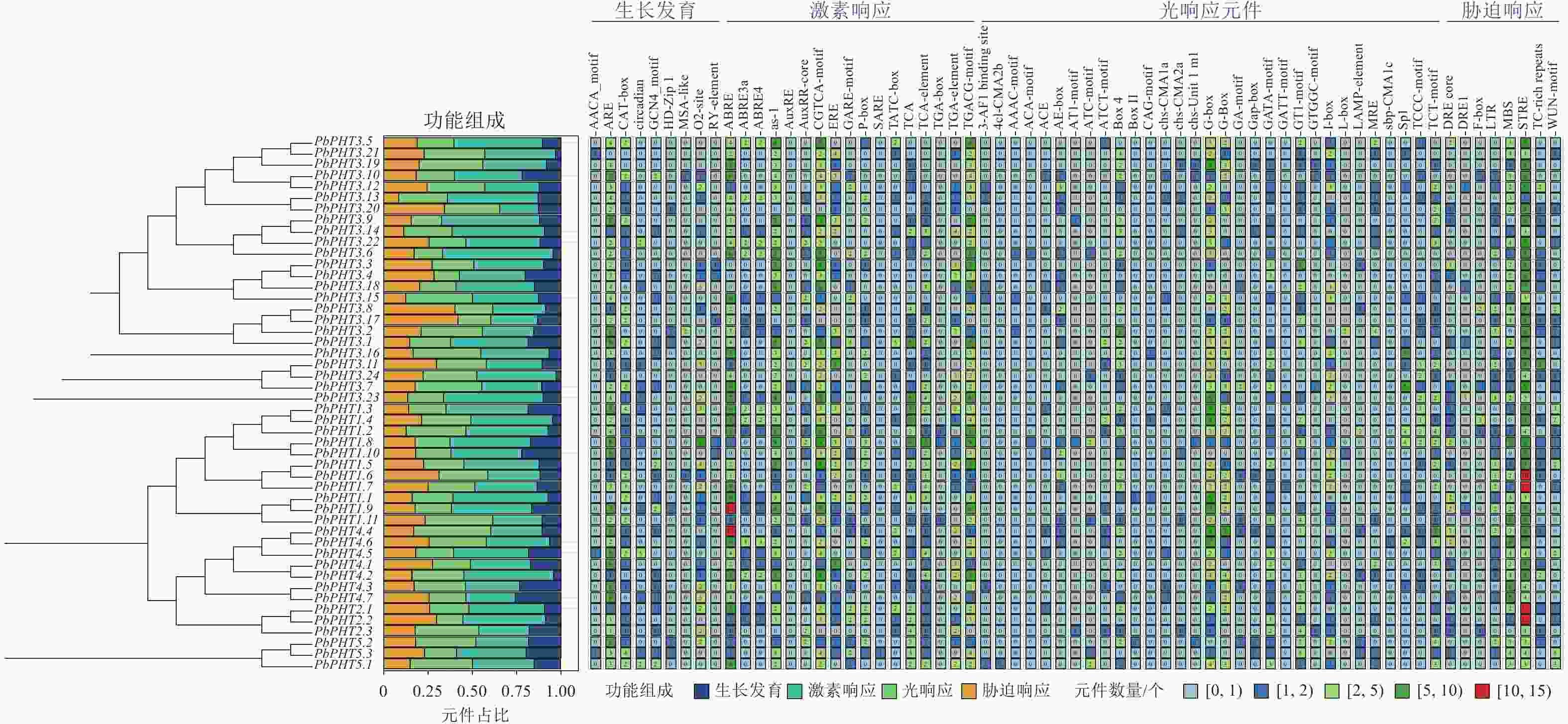
图4显示:不同PHT基因在顺式作用元件的种类和数量上存在明显差异,整体分为生长发育、激素响应、光响应和胁迫响应四大类相关元件。在闽楠PHT基因启动子区域检测到2 677个顺式作用元件,其中激素响应元件数量最多,为1 087个,占比为40.6%,其次为光响应元件703个,胁迫响应元件550个,生长发育相关元件337个。激素响应元件中,茉莉酸甲酯响应元件(TGACG-motif与CGTCA-motif)最多,为304个;ABA响应元件(ABRE、ABRE3a、ABRE4)共248个,其中PbPHT1.9与PbPHT4.4均含有超过10个的ABA响应元件。胁迫响应元件方面,所有PbPHTs基因启动子均检测到3个以上胁迫响应元件(STRE),其中PbPHT1.6、PbPHT1.7、PbPHT2.1和PbPHT1.2的STRE数量均超过10个。
-
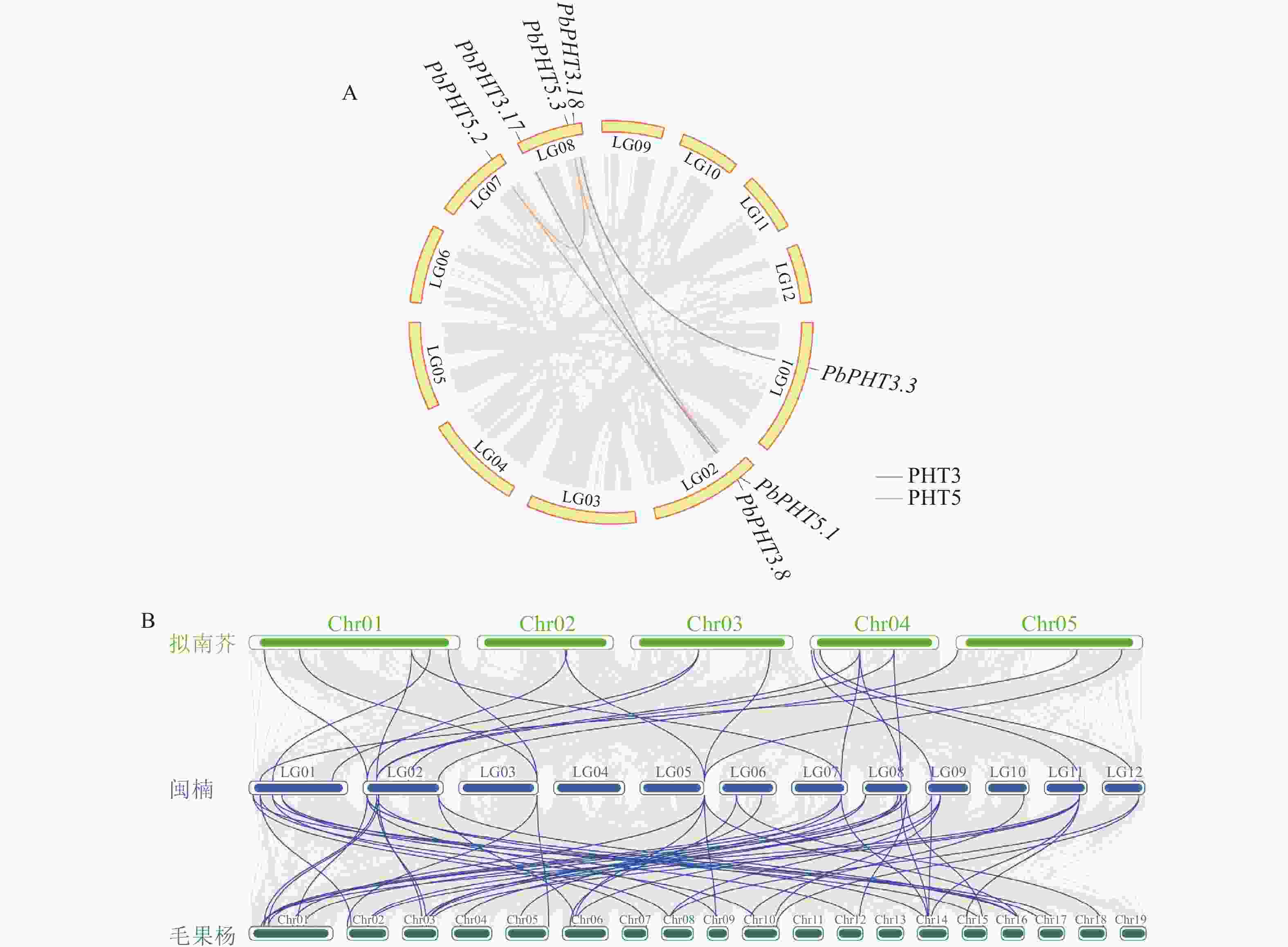
种内共线性分析(图5A)结果表明:在PbPHTs成员中存在5对片段重复基因,其中在PHT3亚家族内发现了2对重复基因对(即PbPHT3.3与PbPHT3.18,PbPHT3.8与PbPHT3.17),而在PHT5亚家族中,PbPHT5.1、PbPHT5.2和PbPHT5.3互为片段重复。此外,还鉴定出4对串联重复基因,分别是PbPHT1.3和PbPHT1.4、PbPHT1.5和PbPHT1.6、PbPHT1.6和PbPHT1.7、PbPHT4.1和PbPHT4.2,这些重复基因主要分布在LG02和LG03染色体上。通过与拟南芥、毛果杨PHT的种间共线性分析结果(图5B)表明:闽楠-拟南芥存在22对共线性基因,闽楠-毛果杨存在52对共线性基因。
-
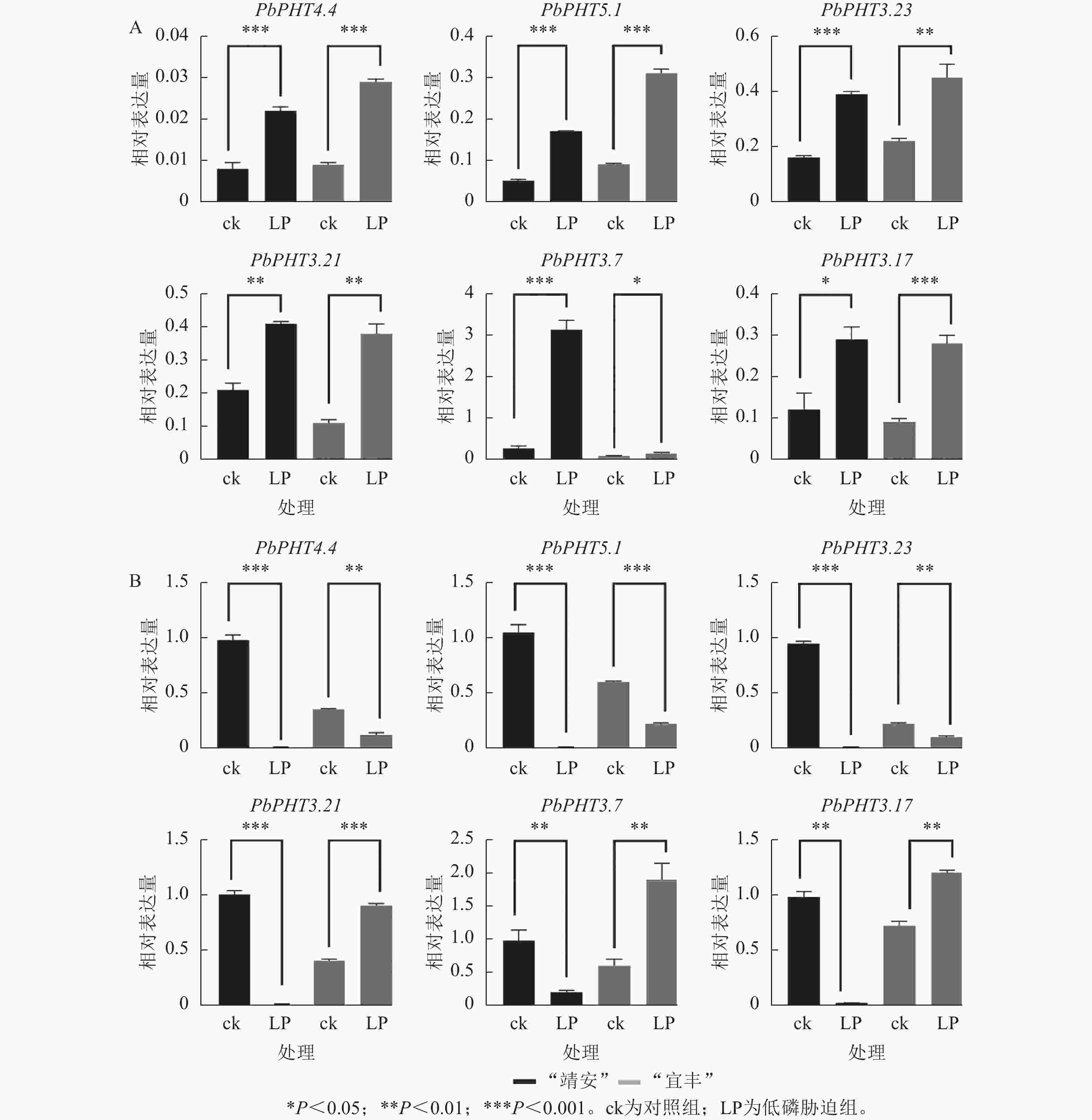
利用RT-qPCR测定了6个PHTs基因在低磷胁迫处理下的表达模式,结果表明PbPHTs在2个不同家系闽楠幼苗根中诱导表达,而在茎叶中呈不同表达模式(图6)。例如,在“靖安”幼苗根中,PbPHT3.7表达水平上调倍数最大,表达量为ck的11倍。在“宜丰”幼苗根中,PbPHT5.1表达水平上调倍数最大,表达量为ck的4倍。在茎叶部,PbPHT4.4、PbPHT5.1、PbPHT3.23在“靖安”和“宜丰”中都下调表达;而PbPHT3.21、PbPHT3.7、PbPHT3.17在“靖安”中下调表达,而在“宜丰”中上调表达。
-
本研究通过全基因组水平鉴定出闽楠48个PHT家族成员,涵盖PHT1~PHT5共5个亚家族,成员数目及分布展现出明显的亚家族特异性[24]。其中,PHT3亚家族拥有24个成员,显著多于其他亚家族,其多拷贝串联重复现象类似于盐芥中PHT1;3的扩增模式[13]。PHT1亚家族中11个成员的数量与典型模式植物相近,为闽楠根系对外源无机磷酸盐高效吸收提供了基础[25]。蛋白理化性质分析显示:除少数成员为酸性或亲水性蛋白外,大多数PHT蛋白具有良好的稳定性和中性至碱性等电点,这与它们需要在不同细胞环境中灵活响应氢离子(H+)梯度相一致;类似研究在毛竹Phyllostachys edulis PHT1家族中也观察到了相同的理化特性分布[26]。基因结构和保守基序分析进一步揭示:亚家族内部尽管存在基序保守性,但不同亚家族间的结构多样性表明:它们在进化过程中经历了功能分化并获得了新功能,这一点亦与毛竹和茶树Camellia sinensis等PHT家族研究结果相符[26−27],也与其他高等木本植物中磷转运蛋白基因家族的进化特点相符,表明闽楠为了适应低磷环境,PHT家族发生了基因扩增和功能分化[28]。
此外,闽楠PHT基因在染色体上的不均匀分布及其顺式作用元件谱的多样性,为深入理解其调控网络提供了重要线索。染色体定位显示:PHT基因集中在第1~3条染色体上,且在LG02、LG03上存在多对串联重复和片段重复基因对,暗示局部基因扩增是家族扩张的重要驱动力。顺式作用元件分析发现:MYCS、P1BS等菌根诱导元件以及ABA、STRE等胁迫响应元件在不同 PHT启动子中高度富集,可能使特定成员在低磷胁迫和菌根共生条件下迅速调节表达[29]。
在低磷胁迫条件下,闽楠不同家系PHT基因的表达具有显著的基因型依赖性,表明其响应磷缺乏的调控网络十分复杂。以“靖安”家系为例,根系中PbPHT3.7表达量较对照上调11.2倍,表明该基因可能通过增强质膜质子泵(H+-ATPase)活性促进根际磷吸收;而“宜丰”家系液泡膜定位的PbPHT5.1表达量上调4.1倍,暗示其通过调控液泡磷库的动态平衡参与磷再利用过程。此外,茎叶组织中PHT基因的表达模式存在显著家系异质性,如PbPHT3.21、PbPHT3.7及PbPHT3.17在“靖安”家系中下调表达,而在“宜丰”家系中上调1.8~2.5倍,表明这些基因可能通过调控韧皮部磷装载效率介导家系特异性的磷分配策略[30]。这与棉花Gossypium hirsutum PHT基因表达的组织特异性和基因型依赖性相吻合[31],进一步印证了PHT家族在植物磷稳态调控中的核心作用。其中“宜丰”家系能更有效维持叶片与根系的无机磷酸盐动态平衡,其根系在胁迫21 d后无机磷酸盐含量显著下降[32]。
-
鉴定了48个闽楠PHT成员,分为PHT1~PHT5共5个亚家族,其中PHT3成员最多(24个),基因扩增与串联重复现象显著。顺式作用元件分析表明:PHT启动子区富含茉莉酸甲酯(304个)和ABA响应元件(248个),暗示其通过激素信号与逆境响应协同调控磷吸收。低磷胁迫下,PHT基因表达呈显著家系依赖性,筛选出PbPHT3.7和PbPHT5.1等关键候选基因,为耐低磷品种选育提供了靶点。
Identification of PHT gene family and expression analysis under low phosphorus stress in Phoebe bournei
-
摘要:
目的 闽楠Phoebe bournei是中国南方重要的珍贵树种,其人工林生产力受低磷胁迫制约。本研究旨在全基因组范围鉴定闽楠PHT基因家族,分析其在低磷胁迫下的表达模式,筛选受低磷胁迫诱导的主要PHT成员,为开发磷高效利用标记基因及选育、创制耐低磷种质提供科学依据。 方法 基于闽楠全基因组数据,利用生物信息学方法鉴定PHT基因家族成员,分析其理化性质、系统发育、染色体定位及顺式作用元件;通过低磷胁迫处理不同家系闽楠幼苗,结合实时定量PCR (RT-qPCR)技术检测PHT表达模式。 结果 从全基因组范围鉴定出48个闽楠PHT基因,不均匀分布于12条染色体(如LG02染色体含11个),分为PHT1~PHT5共5个亚家族,其中PHT3亚家族成员数量最多(24个)。顺式作用元件分析显示:PHT基因启动子区富含激素(40.6%)和胁迫响应元件(20.6%),其中茉莉酸甲酯(304个)和脱落酸响应元件(248个)占比最高。低磷胁迫下,PHT基因呈家系和组织特异性表达,如PbPHT3.7在低磷胁迫的“靖安”家系根系中表达上调11倍,“宜丰”家系中PbPHT5.1上调4倍;茎叶中PbPHT3.21等表达模式在家系间显著分化。 结论 从闽楠基因组鉴定出48个PHT基因,并筛选到低磷胁迫特异诱导表达的候选基因,为闽楠磷高效品种选育提供了关键靶基因,并为樟科Lauraceae植物磷信号网络解析提供了新视角。图6表1参32 Abstract:Objective Phoebe bournei is a valuable tree species in southern regions of China, yet its plantation productivity is often constrained by low-phosphorus stress. This study aims to systematically characterize the P. bournei PHT gene family and elucidate its regulatory mechanisms under low phosphorus stress, providing a molecular basis for genetic improvement of phosphorus efficiency in P. bournei. Method Based on the whole-genome data of P. bournei, bioinformatics methods were employed to identify PHT family members, analyze their physicochemical properties, phylogenetic relationships, chromosomal localization, and cis-acting elements. Low phosphorus stress was applied to seedlings of different families, and reverse transcription real-time quantitative PCR (RT-qPCR) was utilized to detect expression patterns of key genes. Result A total of 48 PbPHT genes were identified, which distributed unevenly on 12 chromosomes, with 11 genes clustered on the LG02 chromosome. It classified into 5 subfamilies (PHT1−PHT5), with PHT3 being the largest subfamily (24 members). Cis-element analysis revealed enrichment of hormone-responsive (40.6%) and stress-responsive elements (20.6%) in promoter regions of PHT genes, predominantly methyl jasmonate- (304) and abscisic acid (ABA)-responsive elements (248). Under low phosphorus stress, PHT gene expression exhibited family- and tissue-specific patterns. In roots, the expression level of PbPHT3.7 in the “Jing’an” family increased 11-fold, and expression level of PbPHT5.1 in the “Yifeng” family increased 4-fold. The expression divergence of PbPHT3.21 in stems and leaves was observed across families. Conclusion The P. bournei PHT family collaboratively regulates low phosphorus stress adaptation through cis-element diversity and family-specific expression patterns. This study identifies key candidate genes for breeding phosphorus-efficient P. bournei cultivars, and also offers new insights into phosphorus signaling networks in Lauraceae plants. [Ch, 6 fig. 1 tab. 32 ref.] -
Key words:
- Phoebe bournei /
- PHT gene family /
- expression patterns /
- low-phosphorus stress
-
表 1 闽楠PHT基因家族成员基本信息
Table 1. Basic information of PHT gene family members in P. bournei
基因亚
家族基因
名称氨基酸
个数分子量/
Da理论等
电点不稳定
系数总平均亲水性
(疏水性值)基因亚
家族基因
名称氨基酸
个数分子量/
Da理论等
电点不稳定
系数总平均亲水性
(疏水性值)PbPHT1 PbPHT1.1 507 54 765.73 5.24 39.28 0.545 PbPHT3.11 358 39 645.54 8.75 36.80 −0.091 PbPHT1.2 530 58 479.04 8.93 33.88 0.315 PbPHT3.12 319 35 300.06 9.55 43.06 0.089 PbPHT1.3 537 59 193.72 8.89 35.11 0.237 PbPHT3.13 334 36 558.13 9.22 42.31 0.176 PbPHT1.4 502 55 614.00 8.67 34.11 0.223 PbPHT3.14 307 32 921.16 9.61 26.56 0.187 PbPHT1.5 517 57 636.40 8.23 31.45 0.392 PbPHT3.15 320 35 397.16 9.45 34.67 0.048 PbPHT1.6 518 57 496.88 8.64 40.07 0.298 PbPHT3.16 324 36 565.27 10.02 34.93 −0.167 PbPHT1.7 539 59 846.77 8.71 33.07 0.280 PbPHT3 PbPHT3.17 297 30 459.27 9.30 28.97 0.194 PbPHT1.8 540 58 915.49 8.70 29.74 0.339 PbPHT3.18 371 39 530.93 9.31 38.18 0.175 PbPHT1.9 518 56 223.84 5.63 40.43 0.480 PbPHT3.19 356 38 492.35 9.67 40.40 0.031 PbPHT1.10 1 616 183 230.14 8.19 41.99 −0.205 PbPHT3.20 331 36 539.20 9.44 43.61 −0.034 PbPHT1.11 643 68 331.42 9.65 44.19 0.431 PbPHT3.21 357 38 616.78 9.50 28.79 0.059 PbPHT2 PbPHT2.1 563 58 858.67 9.25 37.54 0.591 PbPHT3.22 309 33 535.18 9.75 28.70 0.127 PbPHT2.2 575 60 303.32 9.33 32.08 0.558 PbPHT3.23 830 91 273.52 8.84 47.18 −0.256 PbPHT2.3 600 66 144.24 8.63 39.25 0.312 PbPHT3.24 512 54 414.49 9.56 45.15 −0.056 PbPHT3.1 852 93 137.34 8.97 32.01 0.025 PbPHT4.1 523 57 210.16 9.62 28.75 0.436 PbPHT3.2 305 32 965.29 9.65 38.93 0.160 PbPHT4.2 518 56 338.01 10.42 44.45 0.404 PbPHT3.3 375 40 068.61 9.23 40.17 0.156 PbPHT4.3 447 48 404.23 9.40 31.46 0.643 PbPHT3.4 377 40 224.75 9.17 40.17 0.151 PbPHT4 PbPHT4.4 558 61 176.23 9.01 47.73 0.303 PbPHT3 PbPHT3.5 509 56 637.27 6.16 32.06 −0.111 PbPHT4.5 543 59 672.97 8.07 95.17 0.301 PbPHT3.6 323 35 219.36 10.01 39.00 −0.048 PbPHT4.6 597 66 446.46 9.31 43.72 0.221 PbPHT3.7 328 35 570.73 8.64 36.53 −0.048 PbPHT4.7 444 48 173.82 9.46 39.81 0.671 PbPHT3.8 294 30 501.51 9.40 32.82 0.243 PbPHT5.1 698 78 009.36 5.90 39.10 0.202 PbPHT3.9 304 32 616.12 9.60 37.30 0.217 PbPHT5 PbPHT5.2 698 78 280.51 5.44 45.68 0.187 PbPHT3.10 394 43 729.81 9.63 43.75 −0.194 PbPHT5.3 697 77 812.15 6.13 40.47 0.185 -
[1] HU Dandan, CUI Ruifan, WANG Ke, et al. The Myb73-GDPD2-GA2ox1 transcriptional regulatory module confers phosphate deficiency tolerance in soybean[J]. The Plant Cell, 2024, 36(6): 2176−2200. DOI: 10.1093/plcell/koae041. [2] MA Bin, ZHANG You, FAN Yanfei, et al. Genetic improvement of phosphate-limited photosynthesis for high yield in rice[J]. Proceedings of the National Academy of Sciences of the United States of America, 2024, 121(34): e2404199121. DOI: 10.1073/pnas.2404199121. [3] XIANG Chao, REN Jie, ZHAO Xiuqin, et al. Genetic dissection of low phosphorus tolerance related traits using selected introgression lines in rice[J]. Rice Science, 2015, 22(6): 264−274. DOI: 10.1016/j.rsci.2015.05.020. [4] 彭铁双. 磷添加对闽楠人工幼林土壤养分元素及微生物的影响[D]. 长沙: 中南林业科技大学, 2022. PENG Tieshuang. Effects of Phosphorus Addition on Soil Nutrient Elements and Microorganisms in Young Phoebe bournei Plantations[D]. Changsha: Central South University of Forestry & Technology, 2022. DOI:10.27662/d.cnki.gznlc.2022.000410. [5] 王春昱. 马尾松miR156-SPL调控模块在低磷胁迫下的功能研究[D]. 贵阳: 贵州大学, 2023. WANG Chunyu. Functional Study of the miR156-SPL Regulatory Module in Pinus massoniana under Low Phosphorus Stress[D]. Guiyang: Guizhou University, 2023. DOI:10.27047/d.cnki.ggudu.2023.002694. [6] OKUMURA S. Phosphate transporter gene family of Arabidopsis thaliana[J]. DNA Research, 1998, 5(5): 261−269. DOI: 10.1093/dnares/5.5.261. [7] LIU Fang, CHANG Xiaojian, YE Ying, et al. Comprehensive sequence and whole-life-cycle expression profile analysis of the phosphate transporter gene family in rice[J]. Molecular Plant, 2011, 4(6): 1105−1122. DOI: 10.1093/mp/ssr058. [8] WANG Yueli, LI Ronglan, GUO Yuanhao, et al. Genome-wide identification and expression analysis of the phosphate transporter gene family in Zea mays under phosphorus stress[J]. International Journal of Molecular Sciences, 2025, 26(4): 1445. DOI: 10.3390/ijms26041445. [9] ZHANG Chunxia, MENG Sen, LI Mingjun, et al. Genomic identification and expression analysis of the phosphate transporter gene family in poplar[J]. Frontiers in Plant Science, 2016, 7: 1398. DOI: 10.3389/fpls.2016.01398. [10] AHMAD I, RAWOOF A, ISLAM K, et al. Identification and expression analysis of phosphate transporter genes and metabolites in response to phosphate stress in Capsicum annuum[J]. Environmental and Experimental Botany, 2021, 190: 104597. DOI: 10.1016/j.envexpbot.2021.104597. [11] LI Yu, WANG Xue, ZHANG Hao, et al. Molecular identification of the phosphate transporter family 1 (PHT1) genes and their expression profiles in response to phosphorus deprivation and other abiotic stresses in Brassica napus[J]. PLoS One, 2019, 14(7): e0220374. DOI: 10.1371/journal.pone.0220374. [12] MURUGAN N, PALANISAMY V, CHANNAPPA M, et al. Genome-wide in silico identification, structural analysis, promoter analysis, and expression profiling of PHT gene family in sugarcane root under salinity stress[J]. Sustainability, 2022, 14(23): 15893. DOI: 10.3390/su142315893. [13] 邓美菊, 王飞, 毛传澡. 植物磷酸盐转运体及其分子调控机制[J]. 植物生理学报, 2017, 53(3): 377−387. DENG Meiju, WANG Fei, MAO Chuanzao. Plant phosphate transporters and its molecular regulation mechanism[J]. Plant Physiology Journal, 2017, 53(3): 377−387. DOI: 10.13592/j.cnki.ppj.2017.0003. [14] YE Ying, YUAN Jing, CHANG Xiaojian, et al. The phosphate transporter gene OsPht1;4 is involved in phosphate homeostasis in rice[J]. PLoS One, 2015, 10(5): e0126186. DOI: 10.1371/journal.pone.0126186. [15] 杨少辉, 李爽, 寇莹莹, 等. 盐芥ThPHT1;8基因的克隆和功能分析[J]. 天津大学学报, 2018, 51(4): 380−388. YANG Shaohui, LI Shuang, KOU Yingying, et al. Cloning and function analysis of ThPHT1;8 gene in Thellungiella salsuginea[J]. Journal of Tianjin University, 2018, 51(4): 380−388. DOI: 10.11784/tdxbz201704023. [16] WANG Li, WANG Qiguang, FU Ningning, et al. Cyanidin-3-O-glucoside contributes to leaf color change by regulating two bHLH transcription factors in Phoebe bournei[J]. International Journal of Molecular Sciences, 2023, 24(4): 3829. DOI: 10.3390/ijms24043829. [17] 韦如萍, 胡德活, 晏姝, 等. 不同供磷浓度对杉木苗根系和盆栽土壤的影响[J]. 华南农业大学学报, 2016, 37(6): 77−83. WEI Ruping, HU Dehuo, YAN Shu, et al. Effect of phosphorus concentration on Cunninghamia lanceolate seedling roots and potting soil[J]. Journal of South China Agricultural University, 2016, 37(6): 77−83. DOI: 10.7671/j.issn.1001-411X.2016.06.012. [18] 吴文景, 梅辉坚, 许静静, 等. 供磷水平及方式对杉木幼苗根系生长和磷利用效率的影响[J]. 生态学报, 2020, 40(6): 2010−2018. WU Wenjing, MEI Huijian, XU Jingjing, et al. Effects of phosphorus supply levels and methods on root growth and phosphorus use efficiency of Chinese fir seedling[J]. Acta Ecologica Sinica, 2020, 40(6): 2010−2018. DOI: 10.5846/stxb201811152470. [19] YANG Xiaoqing, ZHANG Keai, NVSVROT T, et al. Phosphate (Pi) stress-responsive transcription factors PdeWRKY6 and PdeWRKY65 regulate the expression of PdePHT1;9 to modulate tissue Pi concentration in poplar[J]. The Plant Journal, 2022, 111(6): 1753−1767. DOI: 10.1111/tpj.15922. [20] 余海霞, 汤行昊, 刘南, 等. 控水与补水条件下连续热浪对闽楠光合特性和生长速率的影响[J]. 生态学报, 2023, 43(8): 3224−3235. YU Haixia, TANG Xinghao, LIU Nan, et al. Influences of multiple successive heat waves combined with water control and supplement on photosynthetic characteristics and growth rate of Phoebe bournei seedlings[J]. Acta Ecologica Sinica, 2023, 43(8): 3224−3235. DOI: 10.5846/stxb202201190183. [21] HAN Xiao, ZHANG Junhong, HAN Shuang, et al. The chromosome-scale genome of Phoebe bournei reveals contrasting fates of terpene synthase (TPS)-a and TPS-b subfamilies[J]. Plant Communications, 2022, 3(6): 100410. DOI: 10.1016/j.xplc.2022.100410. [22] CHEN Chengjie, WU Ya, LI Jiawei, et al. TBtools-II: a “one for all, all for one” bioinformatics platform for biological big-data mining[J]. Molecular Plant, 2023, 16(11): 1733−1742. DOI: 10.1016/j.molp.2023.09.010. [23] ROMBAUTS S, DEHAIS P, VAN MONTAGU M, et al. PlantCARE, a plant cis-acting regulatory element database[J]. Nucleic Acids Research, 1999, 27(1): 295−296. DOI: 10.1093/nar/27.1.295. [24] LÜ Sulian, WANG D, JIANG Ping, et al. Variation of PHT families adapts salt cress to phosphate limitation under salinity[J]. Plant, Cell & Environment, 2021, 44(5): 1549-1564. DOI: 10.1111/pce.14027. [25] 刘朝柱, 艾雯妍, 文思颖, 等. 水稻磷转运蛋白Pht1家族研究进展[J]. 植物营养与肥料学报, 2023, 29(9): 1725−1737. LIU Chaozhu, AI Wenyan, WEN Siying, et al. Research progress on phosphate transporter Pht1 family in rice[J]. Plant Nutrition and Fertilizer Science, 2023, 29(9): 1725−1737. DOI: 10.11674/zwyf.2022705. [26] 王绍良, 张雯宇, 高志民, 等. 毛竹磷转运蛋白Ⅰ家族基因鉴定及表达模式[J]. 浙江农林大学学报, 2022, 39(3): 486−494. WANG Shaoliang, ZHANG Wenyu, GAO Zhimin, et al. Identification and expression pattern of phosphorus transporter Ⅰfamily genes of Phyllostachys edulis[J]. Journal of Zhejiang A&F University, 2022, 39(3): 486−494. DOI: 10.11833/j.issn.2095-0756.20210471. [27] 郭丽娜, 郝心愿, 王璐, 等. 茶树CsPHT1;3基因特性及其对硒的响应研究[J]. 茶叶科学, 2023, 43(2): 173−182. GUO Lina, HAO Xinyuan, WANG Lu, et al. Study on the characteristics of CsPHT1;3 and its response to selenium in tea plants[J]. Journal of Tea Science, 2023, 43(2): 173−182. DOI: 10.13305/j.cnki.jts.2023.02.003. [28] 董旭, 王雪, 石磊, 等. 植物磷转运子PHT1家族研究进展[J]. 植物营养与肥料学报, 2017, 23(3): 799−810. DONG Xu, WANG Xue, SHI Lei, et al. Advances in plant PHT1 phosphate transporter family research[J]. Journal of Plant Nutrition and Fertilizer, 2017, 23(3): 799−810. DOI: 10.11674/zwyf.16224. [29] JIA Hongfang, REN Hongyan, GU Mian, et al. The phosphate transporter gene OsPht1;8 is involved in phosphate homeostasis in rice[J]. Plant Physiology, 2011, 156(3): 1164−1175. DOI: 10.1104/pp.111.175240. [30] 周梦岩, 何冬梅, 李亚超, 等. 紫色酸性磷酸酶在植物响应低磷胁迫中的作用研究进展[J]. 分子植物育种, 2021, 19(11): 3763−3770. ZHOU Mengyan, HE Dongmei, LI Yachao, et al. Research progress of the role of purple acid phosphatase in plant response to low phosphorus stress[J]. Molecular Plant Breeding, 2021, 19(11): 3763−3770. DOI: 10.13271/j.mpb.019.003763. [31] 孙淼, 李鹏程, 郑苍松, 等. 低磷胁迫对不同基因型棉花苗期根系形态及生理特性的影响[J]. 棉花学报, 2018, 30(1): 45−52. SUN Miao, LI Pengcheng, ZHENG Cangsong, et al. Effects of low phosphorus stress on root morphology and physiological characteristics of different cotton genotypes at the seedling stage[J]. Cotton Science, 2018, 30(1): 45−52. DOI: 10.11963/1002-7807.smdhl.20180103. [32] 张漪曼, 路龙俊, 张毓婷, 等. 闽楠紫色酸性磷酸酶基因(PAPs)家族分析及3个PAPs在低磷胁迫下的功能[J]. 林业科学, 2025, 61(5): 146−160. ZHANG Yiman, LU Longjun, ZHANG Yuting, et al. Analysis of purple acid phosphatases genes (PAPs) family in Phoebe bournei and the functions of three PAPs under low phosphorus stress[J]. Scientia Silvae Sinicae, 2025, 61(5): 146−160. DOI: 10.11707/j.1001-7488.LYKX20240323. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20250312






 下载:
下载: