-
毛竹Phyllostachys edulis是中国面积最广、经济价值最高的竹种[1],但其主要分布区土壤有效磷含量偏低[2],严重影响毛竹的生长和产量。研究表明:低磷胁迫降低了毛竹叶片叶绿素和金属含量[3],导致磷组分[4]和内源激素含量[5]等也发生变化,进而降低了整体生物量。常用施磷肥来增加土壤磷有效性,但过度施磷会引起水体富营养化、磷矿资源枯竭等问题[6]。因此,为应对缺磷带来的生产危机,研究植物对低磷胁迫的响应机制显得尤为重要[7]。低磷胁迫下,植物根系会分泌化学物质,影响根际土壤养分有效性[8];同时毛竹等植物会调整根冠比[5,9]等生物量分配格局来适应低磷环境。低磷胁迫还会促使植物改变自身对养分的需求,协调植物体内养分平衡[10]。但不同生长时期植物对养分的需求和获取存在差异[11]。快速生长时期,植物对养分需求较大,土壤供应可能不足,会促使植物发挥养分重吸收作用[12]。LU等[13]研究表明:低磷胁迫使紫花苜蓿Medicago sativa的磷素利用效率增强,但其效率随育苗时间延长而降低。张文元[14]研究表明:不同生长阶段毛竹对养分的需求及所处根际土壤化学性质存在差异。低磷胁迫会打破土壤原有的养分平衡,使植物体内养分调控机制发生变化。但施磷肥后不同生长时期土壤养分动态变化及毛竹实生苗适应性响应的研究尚无报道。综上,本研究模拟不同土壤磷环境,旨在探究低磷胁迫对不同生长时期根际土壤养分环境、毛竹幼苗生长和养分生理的影响及其持续效应,为植物对低磷环境的适应机制提供理论基础。
-
试验地设在浙江农林大学果木园大棚。毛竹种子采自广西桂林灵川县,用质量浓度为0.3%高锰酸钾消毒和无菌水冲洗并浸种24 h后催芽。供试土壤挖取于浙江省杭州市临安区青山湖仙人洞毛竹林地1 m以下土层,自然风干过20目筛后,以V(土壤)∶V(珍珠岩)=3∶1混匀成育苗基质。土壤理化性质:有机质5.02 g·kg−1,总氮0.46 g·kg−1,全磷0.24 g·kg−1,全钾13.01 g·kg−1,碱解氮93.63 mg·kg−1,有效磷2.58 mg·kg−1,速效钾54.99 mg·kg−1,pH 4.83。育苗容器采用高14.0 cm、底径11.8 cm、上口径14.0 cm的BN170型PP5塑料育苗软盆,盆底有16个透水孔,且各配套1个塑料托盘。
-
以毛朝明等[2]对松阳县毛竹林土壤养分分级为依据,采用单因素随机区组试验设计,共设4个初始土壤有效磷水平,分别模拟极低磷(2.5 mg·kg−1,P1)、低磷(5.0 mg·kg−1,P2)、中磷(10.0 mg·kg−1,P3)和适磷(20.0 mg·kg−1,P4)土壤环境。每盆装基质1.4 kg,磷肥采用磷酸二氢钾(分析纯),溶解于水后施入基质并均匀搅拌,每盆浇施100 mL,其质量浓度分别为0、153.5、460.6和1 074.8 mg·L−1,折合每盆分别添加磷为0、3.5、10.5和24.5 mg。本底氮肥已足够支撑幼苗生长所需,不再额外施加氮肥。对于低磷土壤,施加分析纯硫酸钾以补齐钾元素,保证单一磷变量。2019年6月14日,每盆播8粒饱满健康的毛竹种子,长出4片真叶后间苗,留2株健壮且长势一致的幼苗,每处理设4个重复,每重复150株苗木,共2 400株。进行常规栽培管理,为减少边缘效应,隔半月随机移动苗木1次,并在培育过程中摒弃异常植株。
-
根据毛竹幼苗苗高增长变化及普遍生长节律[15],于2019年12月中旬(当年生长季末,T1)和2020年6月中旬(翌年快速生长期,T2)进行破坏性取样,分为根、茎、叶3个部分在105 ℃烘箱中杀青30 min后,70 ℃烘至恒量,测定生物量后,粉碎并过100目筛,用于测定养分。测试样品采用H2SO4-H2O2消煮[16],分别采用凯氏定氮法、钼锑抗比色法和火焰光度法测定全氮、全磷、全钾质量分数,并计算毛竹幼苗根冠比、养分积累量、养分分配比例和磷素利用效率[17]。每个指标重复测定4次,每次重复分别随机取6株均匀混合样。
同时将附着在根系上的土壤作为根际土壤。采用pH计电位法测定根际土壤pH,高温外热重铬酸钾-容量法测定有机质质量分数,H2SO4消煮-凯氏定氮法测定全氮质量分数,乙酸铵浸提法测定速效钾质量分数,盐酸-氟化铵-钼锑抗比色法测定有效磷质量分数[16],并计算土壤有效磷变化幅度。有效磷变化幅度=(某时期有效磷质量分数−初始有效磷质量分数)/初始有效磷质量分数×100%。
-
采用Excel 2010和SPSS 19.0统计和分析数据,SigmaPlot 12.5作图。采用单因素方差分析(one-way ANOVA),Duncan法在α=0.05水平上进行多重比较。
-
表1所示:T1时期,与初始有效磷水平相比,P3和P4处理下的根际土壤有效磷质量分数降低,但低磷处理组(P1和P2)处理下反而增加;此时低磷处理组的根际土壤pH分别较P4显著降低了10.60%和8.55% (P<0.05);但根际土壤全氮质量分数随初始有效磷水平降低而增加,其中P1较P4显著提高了19.23% (P<0.05);此时根际土壤有机质和速效钾质量分数在不同土壤有效磷水平间均无显著差异(P>0.05)。T2时期,根际土壤有效磷质量分数与初始设置水平相比均降低,但低磷处理组降幅较P4显著减小(P<0.05);此时根际土壤pH仅在P1下较P4显著降低3.53% (P<0.05);而低磷处理组的根际土壤全氮质量分数分别较P4显著增加了30.76%和11.82% (P<0.05);此时根际土壤速效钾质量分数在不同有效磷水平间仍无显著差异(P>0.05),但低磷处理组的根际土壤有机质质量分数分别较P4均显著增加了10.70% (P<0.05)。
表 1 初始土壤有效磷水平对根际土壤养分环境的影响
Table 1. Effects of initial soil available phosphorus level on soil nutrient environment in rhizosphere
生长时期 初始土壤有效磷水平 有效磷/(mg·kg−1) 有效磷变化幅度/% pH 有机质/(g·kg−1) 全氮/(mg·kg−1) 速效钾/(mg·kg−1) T1 P1 3.05±0.11 d 22.13±4.56 a 4.81±0.07 b 5.53±0.33 a 902.26±37.64 a 65.47±0.89 a P2 6.57±0.04 c 31.47±0.75 a 4.92±0.03 b 5.90±0.31 a 805.16±38.17 ab 65.94±1.63 a P3 8.47±0.21 b −15.30±2.09 b 5.40±0.03 a 5.83±0.42 a 868.47±4.46 ab 64.94±1.13 a P4 14.98±0.87 a −25.10±4.33 b 5.38±0.04 a 5.17±0.07 a 756.77±42.93 b 63.58±0.64 a T2 P1 2.32±0.04 D −7.33±1.76 A 5.19±0.03 B 7.45±0.21 A 1013.74±29.97 A 93.92±3.87 A P2 4.34±0.12 C −13.27±2.48 A 5.42±0.04 A 7.45±0.19 A 866.91±24.09 B 82.20±1.46 A P3 7.53±0.30 B −24.73±2.99 B 5.43±0.01 A 7.21±0.03 AB 836.34±17.01 BC 75.43±2.63 A P4 12.16±0.28 A −39.20±1.39 C 5.38±0.03 A 6.73±0.23 B 775.27±6.81 C 78.91±10.97 A 说明:数据为平均值±标准误。大小写字母分别表示T2和T1时期不同处理间差异显著(P<0.05);有效磷变化幅度中的−表示土壤有效 磷质量分数与初始水平相比降低,否则表示增加 -
表2所示:T1时,低磷处理组(P1和P2)的毛竹幼苗单株生物量分别较P4显著降低了27.09%和15.93% (P<0.05);根冠比较P4分别显著降低22.22%和14.29% (P<0.05);但各土壤有效磷水平下的毛竹幼苗生物量分配率从大到小均依次为根、叶、茎。T2时,低磷处理组的单株生物量较P4分别显著降低了48.96%和43.40% (P<0.05);但根冠比较P4分别显著增加了44.30%和37.97% (P<0.05);此时毛竹幼苗生物量分配率在各土壤有效磷水平下均从大到小依次为根、茎、叶。
表 2 初始土壤有效磷水平对毛竹幼苗生物量及分配的影响
Table 2. Effects of initial soil available phosphorus level on biomass and allocation of Ph. edulis seedlings
生长时期 初始土壤
有效磷水平生物量/(g·株−1) 生物量分配/% 根冠比 根 茎 叶 T1 P1 0.197±0.005 c 49.40±1.19 d 23.35±0.74 a 27.25±0.98 a 0.98±0.05 c P2 0.227±0.003 b 52.00±0.54 c 20.14±0.04 b 27.86±0.58 a 1.08±0.02 c P3 0.264±0.005 a 60.03±0.43 a 17.00±0.42 c 22.97±0.04 b 1.50±0.03 a P4 0.270±0.009 a 55.82±0.65 b 19.50±0.46 b 24.68±0.24 b 1.26±0.03 b T2 P1 0.243±0.020 B 54.56±1.39 A 29.17±2.40 AB 16.27±1.05 B 1.14±0.10 A P2 0.270±0.025 B 52.09±1.33 A 32.06±0.67 A 15.85±1.12 B 1.09±0.06 A P3 0.307±0.012 B 53.34±1.05 A 25.02±0.83 B 21.64±1.31 A 1.14±0.05 A P4 0.477±0.050 A 43.97±1.35 B 32.37±1.43 A 23.66±0.61 A 0.79±0.04 B 说明:数据为平均值±标准误。大小写字母分别表示T2和T1时期不同处理间差异显著(P<0.05) -
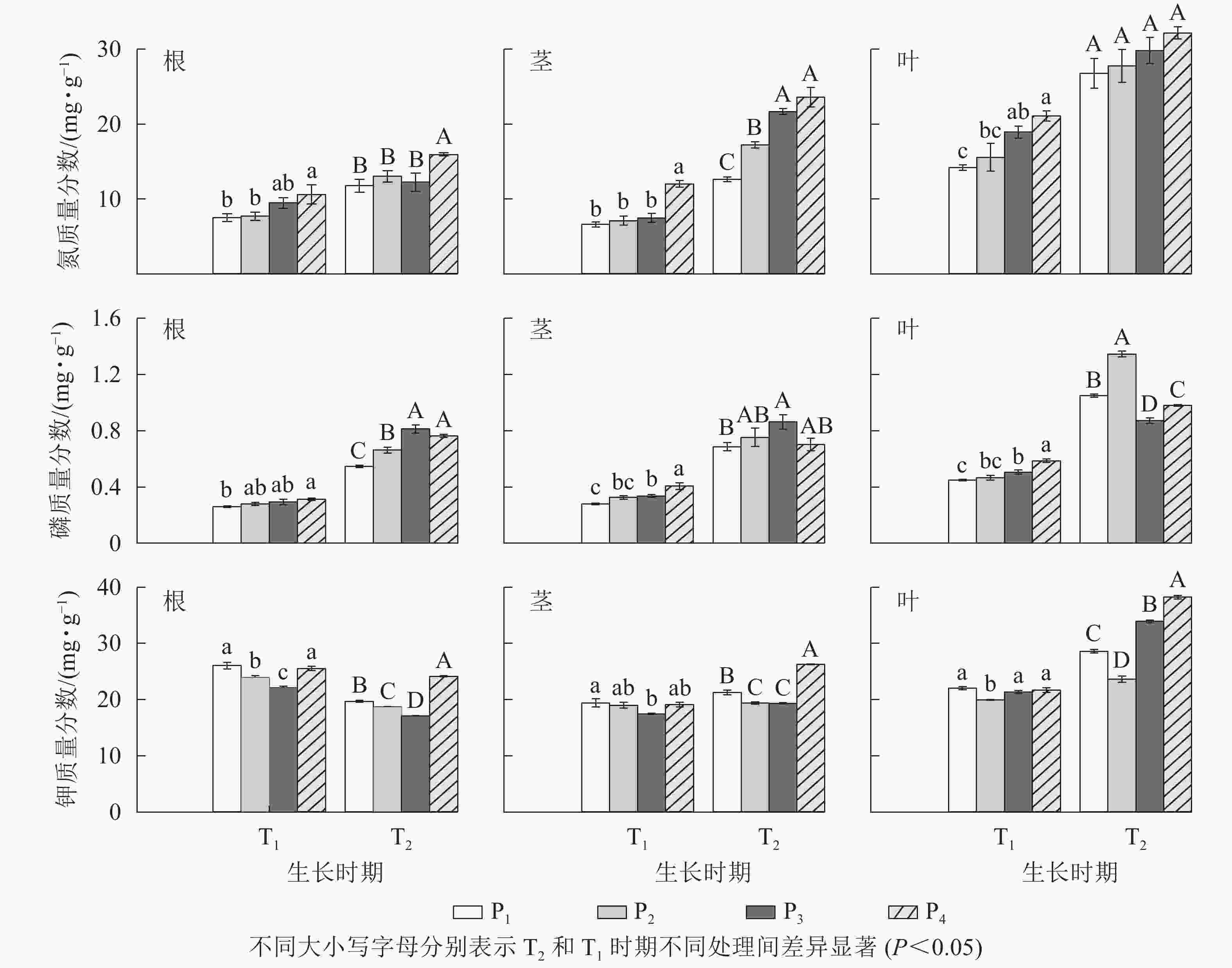
由图1可见:T1时,低磷处理组(P1和P2)较P4均显著降低了毛竹各组织氮质量分数(P<0.05),也显著降低了茎和叶的磷质量分数(P<0.05),但根的磷质量分数仅在P1处理下较P4显著降低了17.01% (P<0.05);此时P1和P4处理的毛竹各组织钾质量分数均无显著差异(P>0.05),但P2处理根和叶的钾质量分数较P4显著降低了6.18%和8.05% (P<0.05)。T2时,毛竹各组织氮质量分数也均随土壤有效磷水平降低而减小,其中低磷处理显著降低了根和茎的氮质量分数(P<0.05),但叶的氮质量分数在不同土壤有效磷水平间无显著差异(P>0.05);此时低磷处理显著降低了根磷质量分数(P<0.05),叶中则显著增加(P<0.05),但茎上无显著差异(P>0.05);而低磷处理组较P4均显著降低了该时期各组织钾质量分数(P<0.05)。
-
由表3显示:无论T1还是T2时期,低磷处理(P1和P2)均显著降低了毛竹幼苗各组织和整株氮、磷、钾积累量(P<0.05)。其中T1时,P1和P2处理的氮积累量较P4分别显著降低了50.28%和38.74% (P<0.05),磷积累量则分别显著降低了42.59%和28.70% (P<0.05),钾积累量则分别显著减小了27.10%和21.55% (P<0.05);T2时,P1和P2处理的氮、磷、钾养分积累量分别依次较P4显著降低了66.86%和57.03%、57.11%和43.16%、60.94%和60.42% (P<0.05)。
表 3 初始土壤有效磷水平对毛竹幼苗养分积累量的影响
Table 3. Effects of initial soil available phosphorus level on nutrient accumulation of Ph. edulis seedlings
生长
时期初始土壤有效磷水平 根养分积累量/(mg·株−1) 茎养分积累量/(mg·株−1) 氮 磷 钾 氮 磷 钾 T1 P1 0.74±0.08 b 0.025±0.001 b 2.53±0.07 b 0.31±0.02 b 0.013±0.001 b 0.89±0.03 b P2 0.91±0.07 b 0.033±0.001 b 2.82±0.06 b 0.33±0.03 b 0.015±0.000 b 0.87±0.01 bc P3 1.50±0.08 a 0.046±0.004 a 3.50±0.09 a 0.34±0.03 b 0.015±0.001 b 0.78±0.01 c P4 1.60±0.18 a 0.047±0.003 a 3.85±0.19 a 0.63±0.01 a 0.021±0.001 a 1.01±0.05 a T2 P1 1.57±0.18 B 0.073±0.009 B 2.62±0.26 B 0.89±0.02 C 0.048±0.002 B 1.49±0.03 B P2 1.81±0.06 B 0.093±0.004 B 2.61±0.18 B 1.50±0.19 B 0.065±0.008 B 1.68±0.17 B P3 2.01±0.23 B 0.133±0.003 A 2.79±0.06 B 1.66±0.05 B 0.066±0.003 B 1.48±0.06 B P4 3.36±0.42 A 0.160±0.016 A 5.08±0.62 A 3.59±0.11 A 0.109±0.015 A 4.03±0.32 A 生长
时期初始土壤有效磷水平 叶养分积累量/(mg·株−1) 整株养分积累量/(mg·株−1) 氮 磷 钾 氮 磷 钾 T1 P1 0.77±0.02 c 0.024±0.001 c 1.18±0.02 b 1.81±0.10 c 0.062±0.001 d 4.60±0.09 c P2 0.99±0.11 bc 0.029±0.001 b 1.26±0.04 b 2.23±0.19 c 0.077±0.001 c 4.95±0.08 c P3 1.16±0.07 b 0.031±0.001 b 1.29±0.04 b 2.99±0.08 b 0.092±0.004 b 5.57±0.13 b P4 1.41±0.02 a 0.039±0.001 a 1.45±0.06 a 3.64±0.20 a 0.108±0.003 a 6.31±0.28 a T2 P1 1.06±0.08 C 0.042±0.006 B 1.14±0.16 C 3.51±0.24 C 0.163±0.016 C 5.25±0.39 B P2 1.24±0.26 BC 0.059±0.010 B 1.03±0.17 C 4.55±0.46 BC 0.216±0.022 BC 5.32±0.51 B P3 2.02±0.31 B 0.058±0.005 B 2.26±0.24 B 5.69±0.57 B 0.257±0.003 B 6.54±0.33 B P4 3.65±0.38 A 0.111±0.014 A 4.33±0.54 A 10.59±0.86 A 0.380±0.045 A 13.44±1.43 A 说明:数据为平均值±标准误。大小写字母分别表示T2和T1时期不同处理间差异显著(P<0.05) 由图2显示:T1时期,氮养分主要分配在根和叶上,分别占40%,且低磷处理组(P1和P2)较P3显著降低了氮在根的分配比例(P<0.05);此时磷养分在各组织分配比例从大到小均依次为根、叶、茎,且低磷处理组也较P3显著降低了磷分配在根的比例(P<0.05);钾养分与磷相似,分配比例从大到小均依次为根、叶、茎,此时低磷处理组较P3和P4均显著降低了其在根的分配比例(P<0.05)。T2时期,氮分配在各组织比例相当,且低磷处理组的氮分配在根的比例较P4均分别显著增加了41.05%和28.85% (P<0.05);钾养分分配比例因土壤有效磷水平不同而异,其中低磷处理组的钾分配比例从大到小依次为根、茎、叶,但中适磷则为根、叶、茎,此时低磷处理组的钾养分分配在根的比例较P4分别显著增加了31.79%和30.86% (P<0.05)。
-
由表4可见:T1时期,低磷处理(P1和P2)显著增加了毛竹茎、叶及整株磷素利用效率,但根的磷素利用效率仅在P1下较P4显著增加了20.31%(P<0.05)。T2时期,低磷处理显著增加了根的磷素利用效率(P<0.05),叶中则显著降低(P<0.05),茎上无显著差异(P>0.05);此时仅P1的整株磷素利用效率较P4显著增加了19.05%,P2与P4间无显著差异(P>0.05)。
表 4 初始土壤有效磷水平对毛竹幼苗磷素利用效率的影响
Table 4. Effects of initial soil available phosphorus level on phosphorus utilization efficiency of Ph. edulis seedlings
生长
时期初始土
壤有效
磷水平磷素利用效率/(g·mg−1) 根 茎 叶 整株 T1 P1 3.85±0.09 a 3.57±0.07 a 2.22±0.03 a 3.16±0.02 a P2 3.58±0.15 ab 3.07±0.11 b 2.15±0.08 ab 2.93±0.07 b P3 3.44±0.21 ab 2.97±0.08 b 1.98±0.06 b 2.86±0.07 b P4 3.20±0.09 b 2.48±0.15 c 1.71±0.03 c 2.50±0.02 c T2 P1 1.83±0.03 a 1.46±0.06 a 0.95±0.01 c 1.50±0.03 a P2 1.51±0.05 b 1.35±0.11 a 0.74±0.01 d 1.25±0.04 b P3 1.23±0.04 c 1.17±0.07 a 1.15±0.02 a 1.19±0.04 b P4 1.31±0.02 c 1.43±0.09 a 1.02±0.01 b 1.26±0.02 b 说明:磷素利用效率=生物量/磷素积累量;数据为平均值±标准误;大小写字母分别表示T2和T1时期不同处理间差异显著(P<0.05) -
根际土壤环境直接影响土壤养分的转化、迁移及被植物吸收的能力[18],根际土壤有效磷作为表征土壤供磷能力的重要指标,是植物吸收磷素的直接形态[19]。本研究中,低磷胁迫显著降低了当年生长季末根际土壤pH,但其有效磷质量分数较初始设置水平增加,这可能是磷素缺乏时,毛竹根系会分泌苹果酸、草酸等有机酸物质进入土壤[20],增强根际酸化能力,并与土壤中磷酸铁、磷酸铝等难溶性磷酸盐作用,释放出磷酸盐,可相对提高磷的有效性;此时根际土壤全氮质量分数随有效磷水平降低而增加,但有机质和速效钾质量分数无显著差异,这表明当年生长季末时,极低磷胁迫会相对更阻碍毛竹幼苗吸收根际土壤氮素,抑制幼苗生长发育。随育苗时间推移,低磷胁迫显著增加了翌年快速生长期的根际土壤有机质质量分数,但有效磷降幅较小,这可能是由于低磷胁迫下的毛竹根系会随着生长分泌更多有机物质,缓解难溶性磷酸盐在土壤中的沉积,维持土壤磷肥力。此时,低磷环境均会显著限制毛竹幼苗吸收土壤氮素。
-
低磷胁迫显著抑制了当年生长季末毛竹幼苗生物量的积累,这可能是由于磷素不足会导致植物体内核酸、核蛋白合成受阻,抑制细胞形成和分裂[21]。植物养分平衡作为生物量积累的基础,其养分浓度和积累量受土壤养分有效性影响[22]。本研究中,养分浓度与积累量随土壤磷水平降低变化规律并不完全一致,主要原因是各组织养分积累量和生物量均随土壤磷水平降低而减小,但两者降幅不完全同步,从而对某些养分浓度造成相对稀释或浓缩[23],这是植物养分协调供应的表现形式之一。养分利用效率反映了植物对养分的利用和适应情况,本研究表明:低磷胁迫显著提高了当年生长季末毛竹整体磷素利用效率,与目前主流观点一致:缺磷素环境下的植物养分利用效率高于富态营养环境[23]。低磷胁迫显著降低了当年生长季末毛竹幼苗根冠比,也相对减少了氮、磷、钾养分在根系的分配比例,这表明生长季末时,低磷胁迫会提高毛竹叶片储存养分的比例,增强光合作用,并尽可能多的制造有机物质,在来年春季新生长时,作为源将养分输送到其他组织促进生长发育。
-
低磷胁迫显著降低毛竹生物量和养分积累量的作用持续到翌年快速生长期,且降幅较当年生长季末更高,这表明了低磷胁迫对毛竹幼苗吸收根际土壤养分的抑制作用随育苗时间延长有所增强,并进一步抑制了生物量的积累。在翌年快速生长期,低磷胁迫显著降低了根的磷质量分数,但叶相反,这可能是毛竹幼苗为应对低磷胁迫采用的“被动”策略,即通过活化细胞壁中所储存的磷素[24],促进磷素内循环,从而提高叶片光合效率[25],以维持正常生理生化活动所需。毛竹整体磷素利用效率至翌年快速生长期时仅在极低磷胁迫下显著增加,这表明毛竹幼苗对低磷胁迫的适应性随育苗时间延长而增强。此外,至翌年快速生长期,低磷胁迫显著提高了毛竹幼苗根冠比和氮、钾养分分配到根系的比例,这可能是由于低磷土壤迫使快速生长期的毛竹幼苗分配更多养分用于支持根系生长,提高根系活力;也可能是当年生长季末储存在叶片中的养分被更多地转运到根系,以维持苗木正常生长发育。
-
低磷胁迫降低了当年生长季末毛竹幼苗根际土壤pH,但维持了根际土壤高氮质量分数,这种作用持续到了翌年快速生长期,此时低磷胁迫还显著增加了根际土壤有机质质量分数。此外,低磷胁迫显著抑制了毛竹生物量和养分的积累,但提高了整株磷素利用效率;低磷抑制作用随育苗时间推移增强,但毛竹幼苗会通过提高根冠比、根系养分分配比例来提高对低磷胁迫的适应性。
Effect of low phosphorus stress on growth and nutrient physiology of Phyllostachys edulis seedlings
-
摘要:
目的 探究低磷胁迫对不同生长时期根际土壤养分环境、毛竹Phyllostachys edulis幼苗生长和养分生理的影响及其持续效应,分析毛竹幼苗对低磷胁迫的适应机制。 方法 通过盆栽播种育苗方式,研究了4种不同土壤有效磷水平:2.5 mg·kg−1(极低磷,P1)、5.0 mg·kg−1(低磷,P2)、10.0 mg·kg−1(中磷,P3)、20.0 mg·kg−1(适磷,P4)对当年生长季末(T1)和翌年快速生长期(T2)根际土壤养分环境、毛竹幼苗生物量及其分配、毛竹幼苗养分吸收利用和分配的影响。 结果 低磷处理组(P1, P2)显著降低T1根际土壤pH (P<0.05),并维持了根际土壤高氮质量分数;这种低磷效应趋势持续至T2,且此时P1和P2的根际土壤有机质质量分数较P4显著增加了10.70% (P<0.05)。低磷处理组均显著降低了2个时期毛竹幼苗生物量及氮、磷、钾养分积累量(P<0.05),且T2时的降幅比T1更高。T1时,低磷处理组显著降低了毛竹幼苗根冠比(P<0.05),也相对降低根系养分的分配比例;但T2时,低磷处理组的根冠比分别较P4显著增加44.30%和37.97% (P<0.05),且显著增加了氮、钾养分在根系的分配比例(P<0.05)。低磷处理组显著增加了T1毛竹幼苗整株磷素利用效率(P<0.05),随育苗时间推移,其利用效率下降,至T2时,仅P1较P4显著增加了19.05% (P<0.05)。 结论 低磷胁迫抑制了毛竹幼苗生长和养分积累,但提高了其整体磷素利用效率;随育苗时间延长至翌年快速生长期时,低磷胁迫对植株的抑制作用增强,但毛竹幼苗通过提高根冠比、根系养分分配比例来提高对低磷胁迫的适应性。图2表4参25 Abstract:Objective To explore the effects of low phosphorus (P) stress on rhizosphere soil nutrient environment, as well as the growth and nutrient physiology of Phyllostachys edulis seedlings at different growth stages and their sustained effects, so as to analyze the adaptation mechanism of Ph. edulis seedlings to low P stress. Method Seeds of Ph. edulis were sown in pots to cultivate young seedlings. Rhizosphere soil nutrient environment, the biomass and its distribution of Ph. edulis seedlings, and the nutrient absorption, utilization and distribution of Ph. edulis seedlings at the end of the current growing season (T1) and the next rapid growing season (T2) were determined under four different soil available phosphorus conditions, 2.5 mg·kg−1 (very low phosphorus, P1), 5.0 mg·kg−1 (low phosphorus, P2), 10.0 mg·kg−1 (medium phosphorus, P3), 20.0 mg·kg−1 (suitable phosphorus, P4). Result Low P treatment group (P1, P2) significantly decreased pH in rhizosphere soil (P<0.05), and maintained the high N content of the rhizosphere soil at T1; The low P effect continued to T2, and the organic matter content of rhizosphere soil of P1 and P2 was significantly increased by 10.70% compared with that of P4 at this season (P<0.05). Low P treatment group significantly reduced the biomass and the accumulation of N, P, K nutrients of Ph. edulis seedlings at both stages (P<0.05), but the decline at T2 was higher than that at T1. At T1, the low P treatment group significantly reduced the root shoot ratio (R/S) and relatively reduced the proportion ratio of nutrients in the root of Ph. edulis seedlings; However, at T2, the R/S of the low P treatment group was significantly increased by 44.30% and 37.97% compared P4 (P<0.05), and the distribution ratio of N and K nutrients in the root was also significantly increased. The low P treatment group significantly increased the phosphorus use efficiency (PUE) of the whole plant of Ph. edulis seedlings (P<0.05), the PUE decreased with the passage of seedlings time, only P1 significanlty increased by 19.05% compared with P4 at T2 (P<0.05). Conclusion Low P stress inhibited the growth and nutrient accumulation of Ph. edulis seedlings, but increased the overall PUE. With the extension of seedling time to the next rapid growing season, the inhibition effect of low P stress on the plant was enhanced, but the adaptability of Ph. edulis seedlings to low P stress was improved by increasing the root-shoot ratio and the proportion of nutrient distribution to root. [Ch, 2 fig. 4 tab. 25 ref.] -
表 1 初始土壤有效磷水平对根际土壤养分环境的影响
Table 1. Effects of initial soil available phosphorus level on soil nutrient environment in rhizosphere
生长时期 初始土壤有效磷水平 有效磷/(mg·kg−1) 有效磷变化幅度/% pH 有机质/(g·kg−1) 全氮/(mg·kg−1) 速效钾/(mg·kg−1) T1 P1 3.05±0.11 d 22.13±4.56 a 4.81±0.07 b 5.53±0.33 a 902.26±37.64 a 65.47±0.89 a P2 6.57±0.04 c 31.47±0.75 a 4.92±0.03 b 5.90±0.31 a 805.16±38.17 ab 65.94±1.63 a P3 8.47±0.21 b −15.30±2.09 b 5.40±0.03 a 5.83±0.42 a 868.47±4.46 ab 64.94±1.13 a P4 14.98±0.87 a −25.10±4.33 b 5.38±0.04 a 5.17±0.07 a 756.77±42.93 b 63.58±0.64 a T2 P1 2.32±0.04 D −7.33±1.76 A 5.19±0.03 B 7.45±0.21 A 1013.74±29.97 A 93.92±3.87 A P2 4.34±0.12 C −13.27±2.48 A 5.42±0.04 A 7.45±0.19 A 866.91±24.09 B 82.20±1.46 A P3 7.53±0.30 B −24.73±2.99 B 5.43±0.01 A 7.21±0.03 AB 836.34±17.01 BC 75.43±2.63 A P4 12.16±0.28 A −39.20±1.39 C 5.38±0.03 A 6.73±0.23 B 775.27±6.81 C 78.91±10.97 A 说明:数据为平均值±标准误。大小写字母分别表示T2和T1时期不同处理间差异显著(P<0.05);有效磷变化幅度中的−表示土壤有效 磷质量分数与初始水平相比降低,否则表示增加 表 2 初始土壤有效磷水平对毛竹幼苗生物量及分配的影响
Table 2. Effects of initial soil available phosphorus level on biomass and allocation of Ph. edulis seedlings
生长时期 初始土壤
有效磷水平生物量/(g·株−1) 生物量分配/% 根冠比 根 茎 叶 T1 P1 0.197±0.005 c 49.40±1.19 d 23.35±0.74 a 27.25±0.98 a 0.98±0.05 c P2 0.227±0.003 b 52.00±0.54 c 20.14±0.04 b 27.86±0.58 a 1.08±0.02 c P3 0.264±0.005 a 60.03±0.43 a 17.00±0.42 c 22.97±0.04 b 1.50±0.03 a P4 0.270±0.009 a 55.82±0.65 b 19.50±0.46 b 24.68±0.24 b 1.26±0.03 b T2 P1 0.243±0.020 B 54.56±1.39 A 29.17±2.40 AB 16.27±1.05 B 1.14±0.10 A P2 0.270±0.025 B 52.09±1.33 A 32.06±0.67 A 15.85±1.12 B 1.09±0.06 A P3 0.307±0.012 B 53.34±1.05 A 25.02±0.83 B 21.64±1.31 A 1.14±0.05 A P4 0.477±0.050 A 43.97±1.35 B 32.37±1.43 A 23.66±0.61 A 0.79±0.04 B 说明:数据为平均值±标准误。大小写字母分别表示T2和T1时期不同处理间差异显著(P<0.05) 表 3 初始土壤有效磷水平对毛竹幼苗养分积累量的影响
Table 3. Effects of initial soil available phosphorus level on nutrient accumulation of Ph. edulis seedlings
生长
时期初始土壤有效磷水平 根养分积累量/(mg·株−1) 茎养分积累量/(mg·株−1) 氮 磷 钾 氮 磷 钾 T1 P1 0.74±0.08 b 0.025±0.001 b 2.53±0.07 b 0.31±0.02 b 0.013±0.001 b 0.89±0.03 b P2 0.91±0.07 b 0.033±0.001 b 2.82±0.06 b 0.33±0.03 b 0.015±0.000 b 0.87±0.01 bc P3 1.50±0.08 a 0.046±0.004 a 3.50±0.09 a 0.34±0.03 b 0.015±0.001 b 0.78±0.01 c P4 1.60±0.18 a 0.047±0.003 a 3.85±0.19 a 0.63±0.01 a 0.021±0.001 a 1.01±0.05 a T2 P1 1.57±0.18 B 0.073±0.009 B 2.62±0.26 B 0.89±0.02 C 0.048±0.002 B 1.49±0.03 B P2 1.81±0.06 B 0.093±0.004 B 2.61±0.18 B 1.50±0.19 B 0.065±0.008 B 1.68±0.17 B P3 2.01±0.23 B 0.133±0.003 A 2.79±0.06 B 1.66±0.05 B 0.066±0.003 B 1.48±0.06 B P4 3.36±0.42 A 0.160±0.016 A 5.08±0.62 A 3.59±0.11 A 0.109±0.015 A 4.03±0.32 A 生长
时期初始土壤有效磷水平 叶养分积累量/(mg·株−1) 整株养分积累量/(mg·株−1) 氮 磷 钾 氮 磷 钾 T1 P1 0.77±0.02 c 0.024±0.001 c 1.18±0.02 b 1.81±0.10 c 0.062±0.001 d 4.60±0.09 c P2 0.99±0.11 bc 0.029±0.001 b 1.26±0.04 b 2.23±0.19 c 0.077±0.001 c 4.95±0.08 c P3 1.16±0.07 b 0.031±0.001 b 1.29±0.04 b 2.99±0.08 b 0.092±0.004 b 5.57±0.13 b P4 1.41±0.02 a 0.039±0.001 a 1.45±0.06 a 3.64±0.20 a 0.108±0.003 a 6.31±0.28 a T2 P1 1.06±0.08 C 0.042±0.006 B 1.14±0.16 C 3.51±0.24 C 0.163±0.016 C 5.25±0.39 B P2 1.24±0.26 BC 0.059±0.010 B 1.03±0.17 C 4.55±0.46 BC 0.216±0.022 BC 5.32±0.51 B P3 2.02±0.31 B 0.058±0.005 B 2.26±0.24 B 5.69±0.57 B 0.257±0.003 B 6.54±0.33 B P4 3.65±0.38 A 0.111±0.014 A 4.33±0.54 A 10.59±0.86 A 0.380±0.045 A 13.44±1.43 A 说明:数据为平均值±标准误。大小写字母分别表示T2和T1时期不同处理间差异显著(P<0.05) 表 4 初始土壤有效磷水平对毛竹幼苗磷素利用效率的影响
Table 4. Effects of initial soil available phosphorus level on phosphorus utilization efficiency of Ph. edulis seedlings
生长
时期初始土
壤有效
磷水平磷素利用效率/(g·mg−1) 根 茎 叶 整株 T1 P1 3.85±0.09 a 3.57±0.07 a 2.22±0.03 a 3.16±0.02 a P2 3.58±0.15 ab 3.07±0.11 b 2.15±0.08 ab 2.93±0.07 b P3 3.44±0.21 ab 2.97±0.08 b 1.98±0.06 b 2.86±0.07 b P4 3.20±0.09 b 2.48±0.15 c 1.71±0.03 c 2.50±0.02 c T2 P1 1.83±0.03 a 1.46±0.06 a 0.95±0.01 c 1.50±0.03 a P2 1.51±0.05 b 1.35±0.11 a 0.74±0.01 d 1.25±0.04 b P3 1.23±0.04 c 1.17±0.07 a 1.15±0.02 a 1.19±0.04 b P4 1.31±0.02 c 1.43±0.09 a 1.02±0.01 b 1.26±0.02 b 说明:磷素利用效率=生物量/磷素积累量;数据为平均值±标准误;大小写字母分别表示T2和T1时期不同处理间差异显著(P<0.05) -
[1] SONG Xinzhang, ZHOU Guomo, JIANG Hong, et al. Carbon sequestration by Chinese bamboo forests and their ecological benefits: assessment of potential, problems, and future challenges [J]. Environ Rev, 2011, 19(1): 418 − 428. [2] 毛朝明, 蒋灵华, 吴恒祝, 等. 松阳县毛竹林土壤养分贫瘠化评价[J]. 浙江林业科技, 2016, 36(1): 59 − 63. MAO Zhaoming, JIANG Linghua, WU Hengzhu, et al. Evaluation of soil nutrient depletion in Phyllostachys heterocycla cv. pubescens stand in Songyang [J]. J Zhejiang For Sci Technol, 2016, 36(1): 59 − 63. [3] 陶晨悦. 氮沉降对不同土壤磷水平下毛竹实生苗生长和养分利用的影响[D]. 杭州: 浙江农林大学, 2019. TAO Chenyue. Effects of Nitrogen Deposition on Growth and Nutrient Utilization of Phyllostachys edulis Seedlings under Different Soil Phosphorus Levels[D]. Hangzhou: Zhejiang A&F University, 2019. [4] 汤祎磊. 模拟氮沉降下毛竹响应不同磷环境的磷素利用机理研究[D]. 杭州: 浙江农林大学, 2020. TANG Yilei. Phosphorus Utilization Mechanism of Phyllostachys edulis in Response to Different Phosphorus Status under Simulated Nitrogen Deposition[D]. Hangzhou: Zhejiang A&F University, 2020. [5] 陈媛文, 高健, 张颖, 等. 水培条件下不同磷水平对毛竹实生苗生长发育的影响[J]. 热带亚热带植物学报, 2013, 21(1): 78 − 84. CHEN Yuanwen, GAO Jian, ZHANG Ying, et al. Effects of different phosphorus concentration on growth and development of Moso bamboo [J]. J Trop Subtrop Bot, 2013, 21(1): 78 − 84. [6] YANG Xiaoyun, FINNEGAN P M. Regulation of phosphate starvation responses in higher plants [J]. Ann Bot, 2010, 105(4): 513 − 526. [7] BAKER A, CEASAR S A, PALMER A J, et al. Replace, reuse, recycle: improving the sustainable use of phosphorus by plants [J]. J Exp Bot, 2015, 66(12): 3523 − 3540. [8] KATO-NOGUCHI H, INO T, SATA N, et al. Isolation and identification of a potent allelopathic substance in rice root exudates [J]. Physiol Plantarum, 2002, 115(3): 401 − 405. [9] 陈可可, 黄莉娟, 王普昶, 等. 2 种雀稗属牧草对低磷胁迫的生长、生理应激响应[J]. 核农学报, 2021, 35(8): 1908 − 1915. CHEN Keke, HUANG Lijuan, WANG Puchang, et al. Growth and physiological responses of two species of paspalum forage to low phosphorus stress [J]. J Nucl Agric Sci, 2021, 35(8): 1908 − 1915. [10] CAKMAK I, YAZICI A, TUTUS Y, et al. Glyphosate reduced seed and leaf concentrations of calcium, manganese, magnesium, and iron in non-glyphosate resistant soybean [J]. Eur J Agron, 2009, 31(3): 114 − 119. [11] LAMBERS H, CHAPIN F S(Ⅲ), PONS T L. Plant Physiological Ecology[M]. New York: Springer-Verlag, 2008. [12] MEDIAVILLA S, GARCIA-IGLESIAS J, GONZALEZ-ZURDO P, et al. Nitrogen resorption efficiency in mature trees and seedlings of four tree species cooccurring in a Mediterranean environment [J]. Plant Soil, 2014, 385(1/2): 205 − 215. [13] LU Jiaoyun, YANG Mei, LIU Mingguo, et al. Leaf stoichiometry and resorption of N and P in lucerne at different growth stages under different water supplies [J]. J Plant Nutr, 2019, 42(5): 501 − 511. [14] 张文元. 毛竹根际土壤肥力质量变化及苗期营养管理研究[D]. 北京: 中国林业科学研究院, 2009. ZHANG Wenyuan. Study on the Variation of Rhizosphere Soil Fertility Quality of Phyllostachys pubescens and Nutrition Management of its Seedlings[D]. Beijing: Chinese Academy of Forestry, 2009. [15] 傅华君, 董晓波, 万雅雯, 等. 南京地区秋季播种一年生毛竹实生苗生长发育规律[J]. 江苏农业科学, 2019, 47(18): 187 − 190. FU Huajun, DONG Xiaobo, WAN Yawen, et al. Growth and development of annual Phyllostachys edulis seedlings sown in autumn in Nanjing area [J]. Jiangsu Agric Sci, 2019, 47(18): 187 − 190. [16] 鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 1999. RU Rukun. Methods of Soil Agricultural Chemical Analysis[M]. Beijing: China Agricultural Science and Technology Press, 1999. [17] CHAPIN F S. The mineral nutrition of wild plants [J]. Ann Rev Ecol Syst, 1980, 11(1): 233 − 260. [18] DENG Q, CHENG X, BOWATTE S, et al. Rhizospheric carbon-nitrogen interactions in a mixed-species pasture after 13 years of elevated CO2 [J]. Agric Ecosyst Environ, 2016, 235: 134 − 141. [19] 贾兴永, 李菊梅. 土壤磷有效性及其与土壤性质关系的研究[J]. 中国土壤与肥料, 2011(6): 76 − 82. JIA Xingyong, LI Jumei. Study on soil phosphorus availability and its relation to the soil properties in 14 soils from different sites in China [J]. Soils Fert Sci China, 2011(6): 76 − 82. [20] MUHAMMAD I I, NOR S, ABDULLAH A, et al. The dynamic responses of oil palm leaf and root metabolome to phosphorus deficiency [J]. Metabolites, 2021, 217(11): 1 − 15. [21] 李梅, 吴江, 吴家胜, 等. 杨桐苗期施磷效应研究[J]. 浙江林学院学报, 2010, 25(2): 64 − 68. LI Mei, WU Jiang, WU Jiasheng, et al. Phosphorus fertilization with Cleyera japonica seedlings [J]. J Zhejiang For Coll, 2010, 25(2): 64 − 68. [22] PAPONOV I A, POSEPANOV O G, LEBEDINSKAI S, et al. Growth and biomass allocation, with varying nitrogen availability, of near-isogenic pea lines with differing foliage structure [J]. Ann Bot, 2000, 85(4): 563 − 569. [23] 于钦民, 徐福利, 王渭玲. 氮磷肥对杉木幼苗生物量及养分分配的影响[J]. 植物营养与肥料学报, 2014, 20(1): 118 − 128. YU Qinmin, XU Fuli, WANG Weiling. Effect of nitrogen and phosphorus fertilization on biomass and nutrient distribution of Cunninghamia lanceolata seedlings [J]. J Plant Nutr Fert, 2014, 20(1): 118 − 128. [24] ZHU Xiaofang, WANG Zhiwei, WAN Jiangxue, et al. Pectin enhances rice (Oryza sativa) root phosphorus remobilization [J]. J Exp Bot, 2015, 66(3): 1017 − 1024. [25] FAROOQ T H, TIGABU M, MA Xiangqing, et al. Nutrient uptake, allocation and biochemical changes in two Chinese fir cuttings under heterogeneous phosphorus supply [J]. iFor-Biogeosci For, 2018, 11(3): 411 − 417. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20210782






 下载:
下载:



