-
苗木质量是影响造林效果的首要因子,选择质量高的苗木不仅能提高造林成活率,而且能达到良好的造林效果[1]。施肥是苗木质量构建中一项十分重要的培育措施[2],有关苗木施肥研究的报道也颇多。蒋云东等[3]对南酸枣Choerospondias axillaris等7种热带阔叶树种的研究表明:复合肥能明显提高各树种苗木的苗高、地径和生物量,其中以施用1.0%复合肥的效果最佳,一般以0.5%~1.0%为宜,尿素对苗木的生长也有促进作用,以0.3%~0.5%为宜。郑辉等[4]研究认为:氮肥、磷施肥用量配比为184 kg·hm-2(氮),120 kg·hm-2(五氧化二磷)时,有利于刺槐Robinia pseudoacacia苗木体内氮素营养物质转化和积累,苗木地径和生物量较好。有关苗木最佳施肥量的研究也时有报道,例如吴俊杰等[5]研究认为:氮肥对白蜡树Fraxinus chinensis的胸径和树高增长贡献最大,其次为磷肥,钾肥最低,白蜡树的最佳经济效益施肥量分别为0.091 kg·株-1(氮),0.023 kg·株-1(五氧化二磷),0.056 kg·株-1(氧化钾)。吴家胜等[6]研究发现,银杏Ginkgo biloba苗木的合理养分元素施用量,氮肥(氮)为2.79~3.47 g·盆-1、磷肥(五氧化二磷)为2.44~2.59 g·盆-1、钾肥(氧化钾)为1.51~1.98 g·盆-1。科学合理的施肥不仅能提高苗木对养分的吸收利用效率,促进苗木高径生长和生物量积累,而且还能避免肥料浪费造成环境污染[7-8]。为此,施肥技术作为培育优质苗木的重要途径也逐渐受到人们的关注和重视。普陀樟Cinnamomum japonicum var. chenii系樟科Lauraceae樟属Cinnamomum常绿乔木,属国家二级重点保护植物,天然分布处往往在临海坡面上,形成了抗风、抗海雾、耐干旱等优良性状,是舟山海岛的主要造林树种。舟山海岛地区土壤贫瘠,尤其困难地所在土壤以粗骨土为主,有机质、养分含量普遍较低,保水保肥性差,造林成活率甚低,生长状况并不理想。普陀樟苗木造林后,本身由于苗体小,竞争力低下,加之造林地的竞争影响和肥力低下等问题广泛存在,在传统施肥技术下的苗木造林效果始终较差。目前,有关普陀樟苗木施肥技术的研究,几乎处于空白,生产中一直沿用施无机肥的施肥方式,并且多数是定植前施基肥,之后很少追肥,至于施肥量、施肥时间及肥料种类也没有统一的标准,传统的养分管理方式不仅没有起到提高苗木质量的作用,反而极大地浪费了肥料。因此,如何科学施肥成为普陀樟苗木培育的研究重点之一。本研究通过设置不同施肥处理,旨在揭示普陀樟苗木生长期养分分配积累状况及吸收利用率,为普陀樟育苗合理施肥技术提供可靠依据,同时也为提高普陀樟苗木的养分库水平作初步的探索。
-
供试苗木为普陀樟1年生苗,平均株高为6.08 cm,地径2.76 mm,生物量1.44 g。试验用土壤为普通圃地土。试验地土壤pH 6.17,有机质为21.23 g·kg-1,碱解氮95.89 mg·kg-1,有效磷44.17 mg·kg-1,速效钾105.50 mg·kg-1。
-
试验于舟山市林业科学研究院试验基地进行,设置3个施肥处理:不施肥(对照)、常规施肥(50 g·m-2)和增量施肥(100 g·m-2),分别用ck,T50和T100表示,完全随机区组设计,3次重复。于2012年5月中旬开始整地,划分小区,各个小区面积为1.0 m×1.0 m,小区四周用预制水泥板隔开,水泥板埋入土壤深度为50 cm,随后将普陀樟苗木定植于小区内,16株·小区-1,株行距为30 cm × 30 cm。试验所用肥料为氮磷钾复合肥[m(氮):m(五氧化二磷):m(氧化钾)=15:15:15],在5月底和7月底分2次施入,并结合施肥进行浅翻、浇水,每次的施肥量各占总用量的50%。各处理具体肥料用量见表 1。
表 1 不同施肥处理肥料用量
Table 1. Fertilizer rate of different treatments
处理 施肥量/(g·m-2) 总养分量/(g·m-2) 5月 7月 总计 氮 五氧化二磷 氧化钾 ck 0 0 0 0 0 0 T50 25 25 50 7.5 7.5 7.5 T100 50 50 100 15.0 15.0 15.0 说明:复合肥m(氮):m(五氧化二磷):m(氧化钾)=15:15:15. -
根据普陀樟苗木生长规律分别在定植后1个月(生长初期)、2个月(速生期)、3个月(速生后期)时测量苗木高度和地径,于6月和9月2次随机挑选4株·小区-1长势均一的苗木进行收获取样,同时采集表层(0~20 cm)土壤样品。植物样品用清水将泥土洗净后,分为根、茎和叶3部分,放置烘箱内于65 ℃烘干至恒量,测定各部分生物量,9月份试验结束时的样品在测定生物量后再进行营养元素的测定。土壤和植物样品的分析参照《土壤农业化学分析方法》[9]。
-
本试验采用以下参数,计算营养元素的吸收利用效率,以根和茎作为养分库[8, 10]。表观吸收率(apparent use efficiency,EAU)=(施肥处理养分增量-对照养分增量)/纯养分量×100%,氮、磷、钾的表观吸收率分别用EAUN,EAUP,EAUK表示;施肥效率(fertilization efficiency,EF)=(施肥结束后的总生物量-施肥前的总生物量)/供养总量;生物量收获指数(biomass harvest index,IBH)=施肥结束后的总生物量/供养总量;养分收获指数,以氮为例,氮收获指数(nitrogen harvest index,INH)=施肥结束后的含氮量/纯氮量×100%,磷、钾收获指数分别用IPH和IKH表示。
所得试验数据采用Excel和SPSS软件进行统计分析。
-
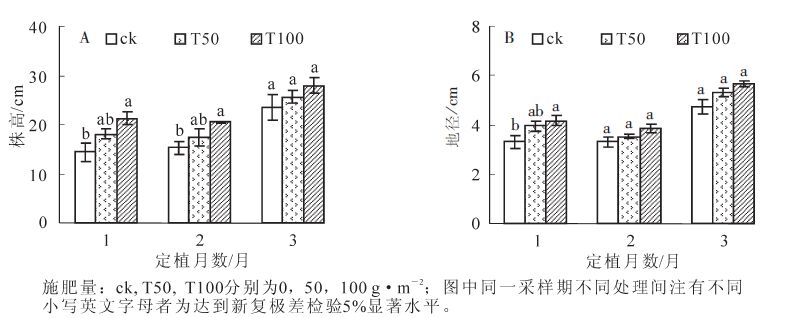
由图 1可知:随着施肥量的增加,普陀樟苗木的株高和地径均增加。可见,增加施肥量促进了普陀樟苗木的高、径生长。从高生长来看(图 1A),T50处理在定植后1,2,3个月分别比对照(ck)增加了25.40%,14.33%和9.48%;T100分别比ck高出48.23%,34.29%和19.39%;T100分别较T50增加了18.20%,17.54%和9.05%。从方差分析的结果来看,T50和ck之间以及T50和T100之间始终没有显著差异。而T100和ck之间,在定植后1个月和2个月,两者差异性达到显著水平(P<0.05),到第3个月时,两者的苗高没有显著差异。从地径变化来看(图 1B),T100处理在定植后1,2,3个月较ck增加,分别达26.06%,16.62%和20.17%;T50增幅分别为19.70%,6.34%和12.95%;T100较T50的增幅分别为5.32%,9.66%和6.39%。方差分析显示,3种处理间在定植后1个月时出现显著差异(P<0.05),之后各处理间差异均不显著。
-
不同施肥处理对普陀樟苗木生物量的影响结果表明(表 2):普陀樟苗木生物量随施肥量的增加而增加。其中,6月T50根、茎、叶和总生物量分别高出对照(ck)36.00%,58.82%,71.77%和61.06%,且两者叶片和总生物量达显著差异(P<0.05);T100各器官和总生物量分别较ck显著增加78.00%,85.29%,79.03%和79.81%(P<0.05);9月T50和T100的叶片和总生物量均显著高出对照(ck)(P<0.05),而根、茎两部分的生物量虽依旧高于ck,但差异并不显著。从T50和T100这2个处理对比来看,6月T100各器官及总生物量始终高于T50,增幅分别达30.88%,16.67%,4.23%和11.64%;而到9月份试验结束时,T100叶片和总生物量分别比T50下降7.56%和1.82%,整个试验过程,T50和T100之间未表现出显著差异。
表 2 不同施肥对普陀樟苗木生物量的影响
Table 2. Effects of different treatments on biomass of Cinnamomum japonicum var. chenii seedlings
处理 植物各器官生物量/g 叶 茎 根 总生物量 6月 9月 6月 9月 6月 9月 6月 9月 ck 1.24±0.06 b 3.60±0.14 b 0.34±0.09 b 1.19±0.20 a 0.50±0.13 b 1.12±0.26 a 2.08±0.28 b 5.91±0.33 b T50 2.13±0.13 a 5.42±0.02 a 0.54±0.02ab 1.78±0.36 a 0.68±0.02ab 1.57±0.25 a 3.35±0.16 a 8.77±0.17 a T100 2.22±0.15 a 5.01±0.26 a 0.63±0.07 a 1.88±0.09 a 0.89±0.01a 1.72±0.07 a 3.74±0.20 a 8.61±0.37 a 说明:表中数据为平均值±标准误) 同一列数后注有不同英文字母者为达到新复极差检验5%(显著水平). -
由表 3可以看出:随着施肥量的增加,苗木各器官养分质量分数及单株养分质量分数均增加。至生长结束时,T100的养分库和全株氮质量分数分别较T50高出3.76%和16.80%;单株含氮量分别高出20.19%和15.09%。T100养分库磷质量分数及单株含磷量分别较T50增幅为11.81%和30.10%;全株分别为14.40%和11.83%。钾质量分数和单株含钾量表现出与氮和磷类似的规律,T100养分库钾质量分数及单株含钾量较T50增加19.40%和40.96%;全株增幅分别为16.29%和13.93%。从养分分配规律来看,各营养元素更多地在叶片中积累,其中氮素表现出叶>根>茎的趋势,而磷素和钾素表现出叶>茎>根的趋势。
从方差分析结果来看,3个处理间的叶片及全株的氮质量分数和单株含量呈显著差异(P<0.05);不同处理间磷质量分数差异性并不显著,但T50和T100叶片及全株磷含量要显著高于ck(P<0.05);T100处理下,叶片、养分库及全株钾质量分数显著高于T50和ck(P<0.05),而T50和T100之间钾含量差异性并不显著。
表 3 不同施肥对普陀樟苗木养分质量分数的影响
Table 3. Effects of different treatments on nutrients contents and concentrations of C. japonicum var. chenii seedlings
指标 处理 叶 茎 根 养分库 全株 ck 14.25±0.33 b 7.16±0.89 a 11.44±0.22 a 9.20 ± 0.43 a 12.27 ± 0.18 b 氮/(mg·g-1) T50 15.74±0.55 b 8.30±1.65 a 12.88 ± 0.84 a 10.37 ± 1.01 a 13.69 ± 0.71 b T100 19.65±1.15 a 8.38±1.05 a 13.44±0.89 a 10.76 ± 0.59 a 15.99 ± 0.88 a 单株含氮量/ ck 51.21±3.32 c 8.43±3.50 a 12.66 ± 3.12 a 21.09 ± 6.66 a 72.30 ± 4.95 c (mg·株-1) T50 85.03 + 2.08 b 14.15 + 2.43 a 20.35 ± 3.88 a 32.35 ± 6.57 a 119.53 ± 2.48 b T100 98.52±3.98 a 16.09±1.07 a 22.97 ± 0.50 a 38.88 ± 0.61 a 137.57 ± 4.52 a ck 2.92±0.41a 3.18±0.99 a 4.24 ± 0.35 a 3.69 ± 0.10 a 3.23 ± 0.23 b 磷/(mg.g-1) T50 3.70±0.15 a 3.78±0.40 a 3.82 ± 0.29 a 3.64 ± 0.61 a 3.68 ± 0.10ab T100 4.29±0.38 a 4.17±0.14 a 3.97 ± 0.51 a 4.07 ± 0.23 a 4.21 ± 0.24 a 单株含磷量/ ck 10.49±2.35 b 3.80±1.50 a 4.79 ± 1.33 a 8.59 ± 2.41 b 19.08 ± 0.91 b (mg·株-1) T50 20.10 + 1.64 a 6.43 + 0.55 a 5.75 ± 0.27 a 11.13 ± 1.48 ab 32.28 ± 1.90 a T100 21.57±1.32 a 7.63±0.36 a 6.90 ± 0.67 a 14.48 ± 1.03 a 36.10 ± 1.46 a ck 4.93±0.18 b 4.50±0.35 a 4.81 ± 0.23 a 4.64 ± 0.13 b 4.81 ± 0.10 b 钾/(mg.g-1) T50 4.95±0.10 b 4.59±0.42 a 5.06 ± 0.71 a 4.69 ± 0.11 b 4.85 ± 0.09 b T100 5.65±0.10 a 5.37±0.43 a 5.90 ± 0.44 a 5.60 ± 0.31 a 5.64 ± 0.17 a ck 17.73±1.52 b 5.31±1.31a 5.31 ± 1.18 b 10.62 ± 2.53 b 28.35 ± 0.96 b 单/(mg·株-1) T50 26.85±1.82 a 8.06±1.46 a 7.66 ± 0.77 ab 14.21 ± 1.49 b 42.57 ± 2.66 a T100 28.38±0.31a 10.10±0.42 a 10.02 ± 0.17 a 20.03 ± 0.25 a 48.50 ± 0.14 a -
表 4中各参数用来表征苗木对养分吸收利用的情况,其中EAU反映了苗木对营养元素的吸收情况,而EF,IBH,INH,IPH及IKH可反映养分元素的利用情况。由表 4可知:养分元素的表观吸收率、施肥效率、收获指数均随着施肥的增加而降低。2种施肥处理下,T100全株氮、磷、钾素的EAU分别较T50下降30.88%,35.47%和29.16%;T100全株的EF比T50下降51.16%。 IBH,INH,IPH和IKH降幅分别达50.91%,42.47%,44.09%和42.99%。比较3种营养元素的表观吸收率和收获指数可以发现,其大小排序为氮>磷>钾。方差分析结果表明:2种施肥处理的养分库仅IBH和IPH出现显著差异(P<0.05);而T100全株各参数均显著高于T50(P<0.05)。
表 4 不同施肥对普陀樟苗木养分吸收及利用的影响
Table 4. Effects of different treatments on nutrient uptake and utilization of Cinnamomum japonicum var. chenii seedlings
器官 处理 EAUN/% EAUP/% EAUK/% EF/(g·g-1) IBH/(g·g-1) INH/% IPH/% IKH/% 养分 T50 3.71 ±0.42a 2.87 ±0.87a 1.26 ±0.04a 2.41 ±0.11a 3.15± 0.11a 6.90 ±1.40a 5.40 ±0.72a 3.67 ±0.39 a 库 T100 1.89 ±0.71a 2.08 ±1.46a 1.21 ±0.32a 1.32 ±0.21a 1.69± 0.21b 4.15 ±0.71a 3.51 ±0.58b 2.58 ±0.33 a 全株 T50 10.07 ±0.53a 6.40 ±1.53a 3.67 ±0.71a 6.90 ±0.35a 8.25± 0.35a 25.50 ±0.91a 15.65 ±0.92a 10.98±0.68a T100 6.96 ±0.39b 4.13 ±0.24b 2.60 ±0.11b 3.37 ±0.15b 4.05± 0.15b 14.67 ±0.91b 8.75 ±0.22b 6.26 ±0.12 b -
从表 5可以看出:试验地土壤总体呈弱酸性,最高pH 6.33,最低为pH 5.62,且随着时间的推移和施肥量的增加,土壤pH值持续下降,T50和T100的降幅分别为4.12%和8.62%。2种施肥处理的土壤有机质、碱解氮、有效磷和速效钾质量分数均高于对照(ck),到9月试验结束时,ck和T100的碱解氮质量分数分别下降13.22%和13.59%,T50增加3.16%; ck和T100的有效磷增幅分别为19.85%和21.25%,T50则下降20.29%;3个处理的速效钾均表现为下降趋势,降幅分别为40.00%,28.02%和12.83%。方差分析结果表明:增加施肥量使各处理间pH值和速效钾质量分数产生显著差异(P<0.05),6月T100碱解氮质量分数要显著高于T50(P<0.05),有效磷显著高于ck(P<0.05),但增加施肥量并未对土壤有机质质量分数产生显著影响。
表 5 不同施肥对土壤养分的影响
Table 5. Effects of different treatments on soil nutrient
月份 处理 pH 有机质/(g·kg-1) 碱解氮/(mg·kg-1) 有效磷/(mg·kg-1) 速效钾/(mg·kg-1) ck 6.33 ± 0.12 a 22.51 ± 6.57 a 106.35 ± 1.87 ab 40.30 ± 3.32 b 106.67 ± 12.94 c 6 T50 6.07 ± 0.01 b 30.65 ± 5.26 a 102.74 ± 0.42 b 58.56 ± 8.73 ab 144.83 ± 5.67 b T100 6.15 ± 0.04 ab 29.35 ± 6.12 a 113.20 ± 3.12 a 60.06 ± 1.19 a 181.83 ± 4.70 a ck 6.27 ± 0.16 a 19.90 ± 8.94 a 92.29 ± 6.97 a 48.30 ± 1.11 a 64.00 ± 8.61 c 9 T50 5.82 ± 0.09 b 24.84 ± 5.49 a 105.99 ± 1.25 a 46.68 ± 12.03 a 104.25 ± 0.43 b T100 5.62 ± 0.26 c 25.40 ± 0.75 a 97.82 ± 1.25 a 72.82 ± 3.03 a 158.50 ± 2.89 a -
普陀樟苗木的高、径生长量随着施肥量的增加而增加。定植后1月至2月,由于施肥的缘故,土壤养分增加,此时苗木正处于速生期,对养分需求较大,因此T50和T100处理下养分供应充足,苗木生长速度加快,3个处理间的株高和地径出现显著差异。到了第3个月,处理间的显著差异消失,这主要是因为此时苗木进入速生后期,生长速度减缓,对养分的需求量也减少。从试验地土壤养分本底值可以看出,有效养分并不低,虽然初期对照(ck)处理下苗木生长较缓慢,但后期生长速度逐渐加快,施肥对株高和地径生长的影响在苗木生长后期并不明显,不同处理间产生的差异随着时间的推移逐渐被土壤本底养分值所掩盖,此外,整个试验过程处于雨水频繁时期,降雨会造成养分大量流失[11]。这点从2个施肥处理的养分吸收利用率上也得到了体现。
试验初(6月),普陀樟苗木各部位的生物量均随着施肥量的增加而增加,而到试验结束时(9月),T100叶片和总生物量分别较T50下降7.56%和1.82%。从分配上看,苗木的生物量主要集中在叶片,以对照(ck)为例,试验结束时(9月),叶片生物量分别为茎和根的3.03倍和3.21倍。通过方差分析也得到相同的结论,T100的根、茎生物量只在6月份时与ck产生显著差异(P<0.05),而T100叶片的生物量始终显著高于ck(P<0.05)。本试验在T100处理下苗木的生物量开始下降,但还未达到显著水平,其原因可能是T100的施肥量(100 g·m-2)已经超出普陀樟的最佳施肥量,苗木受到轻微的毒害作用,从而导致生物量下降[12],这也与李国雷等[13]和魏红旭等[14]的研究结论相一致。因此,普陀樟苗木最适供养量应为50 g·m-2到100 g·m-2。
-
增加施肥量能提高苗木养分库和全株养分质量分数及单株养分含量。有研究认为[15-17],自身载有更高养分含量的苗木在后期造林应用中有更好的生长表现和抵御逆境胁迫的能力。本试验中,在T50和T100处理下,各部位含氮量和含钾量高低排序为叶>根>茎;单株含磷量为叶>茎>根;这表明氮、磷、钾营养元素主要在叶片中积累。苗木在生长后期,养分供应充足,吸收增加,养分库吸收的营养元素转移至叶片中,使得叶营养元素不断积累,但叶片生物量和总生物量开始下降。比较同一部位不同营养元素的积累情况发现,氮、磷、钾元素高低排序为氮>钾>磷,说明苗木对氮素的吸收利用率最高、钾素次之、磷素最低,这主要跟苗木在生长期间对氮素的需求量较大有关,被吸收的氮素进而转化为苗木生物量,因此叶片生物量比茎和根要大[18-20]。因此,在苗木施肥时要注重平衡施肥,磷、钾肥施用要少量多次,提高其利用率,氮肥要适量,避免肥料浪费。
-
养分表观吸收率反映了苗木对营养元素的吸收情况,而施肥效率、收获指数反映的是养分的利用情况。2种不同施肥处理的养分库和全株对氮、磷、钾元素的吸收利用率均不高[8],施肥量更大的T100养分吸收利用率反而小于T50,T100的施肥效率和生物量收获指数仅为T50的48.88%和49.09%,说明过量施肥并不能提高苗木对营养元素的吸收利用,反而会造成大量肥料浪费[20]。比较各养分元素的吸收利用情况发现,3个施肥处理均为氮>磷>钾,这是由于苗木在生长期对氮素的需求量较大,而对磷和钾的需求较小,但从用量上来看,3种营养元素的吸收利用率都偏低,这可能是由于养分元素挥发、淋失,被土壤固定等因素所致[21-22]。
-
随着施肥量的增加和时间的推移,土壤pH值显著下降,呈弱酸性。同一时期不同处理之间土壤有机质相差5~8 g·kg-1,但统计结果显示没有差异,表明土壤有机质存在一定的空间差异。从6月到9月土壤有机质下降3~7 g·kg-1,各处理土壤有机质都略有下降,可能与气温上升、植物生长有关,特别是经过翻耕后移栽的土壤[23-24]。到试验结束时,对照(ck)和T100的碱解氮质量分数分别下降13.22%和13.59%,T100处理土壤中减少的有效氮素并未被植物利用,而是以不同方式损失掉。有研究表明[11],氮素的流失量随施肥量的增加而增加。ck和T100的有效磷质量分数增幅分别为19.85%和21.25%,T50则下降20.29%,这可能是磷素易被土壤当中的铁、铝等元素固定,导致磷素有效性低,适量施肥能促进土壤磷素的释放,增加植物对磷素的吸收,而过量施肥只会导致磷素的大量积累。到9月试验结束时,T50处理土壤氮、磷、钾与试验开始时持平,T100 处理钾积累,ck引起钾亏缺。从移栽成活来看,T50苗木体内养分积累,有利于移栽成活,保持土壤养分平衡;而T100养分浪费。
-
本研究结果显示,增量施肥(T100)处理下普陀樟苗木表现出更大的高径生长量、根茎生物量以及养分质量分数和单株含量,但叶生物量和总生物量开始下降,养分元素吸收及利用率要明显小于T50。T100(100 g·m-2)处理的施肥量已经超出普陀樟苗木的最适供养量,造成肥料极大浪费,并且对苗木产生轻微毒害;而T50处理土壤养分与试验开始时持平,苗木体内养分积累,有利于移栽成活。综合生物量变化和养分吸收利用率分析,普陀樟苗木最适需养量应为50 g·m-2~100 g·m-2,且接近50 g·m-2。本研究设置的施肥梯度较大,未能得出具体的最适供养量,而今后还将进一步细化施肥梯度并结合不同的施肥方式对普陀樟苗木的最佳施肥量进行研究。
Responses of Cinnamomum japonicum var. chenii growth and nutrient uptake to fertilization
-
摘要: 为了解不同施肥水平对普陀樟Cinnamomum japonicum var. chenii苗木生长及养分吸收利用情况的影响,设置了3个水平的田间试验,即不施肥(ck),常规施肥(T50,50 g·m-2)和增量施肥(T100,100 g·m-2),于2012年6月至9月观测苗高和地径,定期采集分析土壤和植物样品。结果表明:普陀樟苗木的苗高、地径、根部和茎部生物量均随施肥量的增加而增加(P<0.05);而叶生物量和总生物量在6月时随施肥量增加而升高(P<0.05),到9月时则呈先升后降的趋势(P<0.05)。苗木体内养分质量分数和单株养分含量随施肥量的增加而增加(P<0.05),不同处理均以叶片养分质量分数最高;养分吸收及利用率随着施肥的增加而降低(P<0.05),T50和T100处理各元素的吸收利用效率均为氮> 磷> 钾。到试验结束时,T50处理土壤养分质量分数与试验开始时持平,T100 处理钾积累,ck引起钾亏缺。从移栽成活来看,T50苗木体内养分积累,有利于移栽成活,保持土壤养分平衡;而T100养分浪费。综合判断,普陀樟苗木最适需养量应为50 g·m-2到100 g·m-2,且较接近50 g·m-2。Abstract: A field experiment was conducted on nursery land of Zhoushan Forestry Academy in 2012 to compare three fertilizer treatments:no fertilizer (ck),a normal rate with 50 g·m-2 of 15-15-15 compound fertilizer (T50), and twice the normal rate(T100),on growth, nutrient uptake and utilization of Cinnamomum japonicum var. chenii seedlings. Results showed that sapling growth of root and stem biomass as well as height and ground diameter significantly increased with increasing rate of fertilizer(P<0.05). Increasing the rate of fertilizer also significantly increased(P<0.05)nutrient concentrations in leaves and nutrient uptake by the plants. By contrast, both nutrient use efficiency and fertilization efficiency decreased significantly (P<0.05) with increasing fertilizer rate,being the same order in T50 and T100:N >P >K. By the end of the experiment,soil available nutrient levels of T50 remained similar to the initial ones;whereas,T100 caused K increased,and ck caused K depleted. For the survival rate, T50 resulted optimal nutrient status in the plants, which was best for transplanting, but T100 induced luxury nutrient supply. Therefore, the optimum fertilizer rate for C. japonicum var. chenii was 50-100 g·m-2.
-
表 1 不同施肥处理肥料用量
Table 1. Fertilizer rate of different treatments
处理 施肥量/(g·m-2) 总养分量/(g·m-2) 5月 7月 总计 氮 五氧化二磷 氧化钾 ck 0 0 0 0 0 0 T50 25 25 50 7.5 7.5 7.5 T100 50 50 100 15.0 15.0 15.0 说明:复合肥m(氮):m(五氧化二磷):m(氧化钾)=15:15:15. 表 2 不同施肥对普陀樟苗木生物量的影响
Table 2. Effects of different treatments on biomass of Cinnamomum japonicum var. chenii seedlings
处理 植物各器官生物量/g 叶 茎 根 总生物量 6月 9月 6月 9月 6月 9月 6月 9月 ck 1.24±0.06 b 3.60±0.14 b 0.34±0.09 b 1.19±0.20 a 0.50±0.13 b 1.12±0.26 a 2.08±0.28 b 5.91±0.33 b T50 2.13±0.13 a 5.42±0.02 a 0.54±0.02ab 1.78±0.36 a 0.68±0.02ab 1.57±0.25 a 3.35±0.16 a 8.77±0.17 a T100 2.22±0.15 a 5.01±0.26 a 0.63±0.07 a 1.88±0.09 a 0.89±0.01a 1.72±0.07 a 3.74±0.20 a 8.61±0.37 a 说明:表中数据为平均值±标准误) 同一列数后注有不同英文字母者为达到新复极差检验5%(显著水平). 表 3 不同施肥对普陀樟苗木养分质量分数的影响
Table 3. Effects of different treatments on nutrients contents and concentrations of C. japonicum var. chenii seedlings
指标 处理 叶 茎 根 养分库 全株 ck 14.25±0.33 b 7.16±0.89 a 11.44±0.22 a 9.20 ± 0.43 a 12.27 ± 0.18 b 氮/(mg·g-1) T50 15.74±0.55 b 8.30±1.65 a 12.88 ± 0.84 a 10.37 ± 1.01 a 13.69 ± 0.71 b T100 19.65±1.15 a 8.38±1.05 a 13.44±0.89 a 10.76 ± 0.59 a 15.99 ± 0.88 a 单株含氮量/ ck 51.21±3.32 c 8.43±3.50 a 12.66 ± 3.12 a 21.09 ± 6.66 a 72.30 ± 4.95 c (mg·株-1) T50 85.03 + 2.08 b 14.15 + 2.43 a 20.35 ± 3.88 a 32.35 ± 6.57 a 119.53 ± 2.48 b T100 98.52±3.98 a 16.09±1.07 a 22.97 ± 0.50 a 38.88 ± 0.61 a 137.57 ± 4.52 a ck 2.92±0.41a 3.18±0.99 a 4.24 ± 0.35 a 3.69 ± 0.10 a 3.23 ± 0.23 b 磷/(mg.g-1) T50 3.70±0.15 a 3.78±0.40 a 3.82 ± 0.29 a 3.64 ± 0.61 a 3.68 ± 0.10ab T100 4.29±0.38 a 4.17±0.14 a 3.97 ± 0.51 a 4.07 ± 0.23 a 4.21 ± 0.24 a 单株含磷量/ ck 10.49±2.35 b 3.80±1.50 a 4.79 ± 1.33 a 8.59 ± 2.41 b 19.08 ± 0.91 b (mg·株-1) T50 20.10 + 1.64 a 6.43 + 0.55 a 5.75 ± 0.27 a 11.13 ± 1.48 ab 32.28 ± 1.90 a T100 21.57±1.32 a 7.63±0.36 a 6.90 ± 0.67 a 14.48 ± 1.03 a 36.10 ± 1.46 a ck 4.93±0.18 b 4.50±0.35 a 4.81 ± 0.23 a 4.64 ± 0.13 b 4.81 ± 0.10 b 钾/(mg.g-1) T50 4.95±0.10 b 4.59±0.42 a 5.06 ± 0.71 a 4.69 ± 0.11 b 4.85 ± 0.09 b T100 5.65±0.10 a 5.37±0.43 a 5.90 ± 0.44 a 5.60 ± 0.31 a 5.64 ± 0.17 a ck 17.73±1.52 b 5.31±1.31a 5.31 ± 1.18 b 10.62 ± 2.53 b 28.35 ± 0.96 b 单/(mg·株-1) T50 26.85±1.82 a 8.06±1.46 a 7.66 ± 0.77 ab 14.21 ± 1.49 b 42.57 ± 2.66 a T100 28.38±0.31a 10.10±0.42 a 10.02 ± 0.17 a 20.03 ± 0.25 a 48.50 ± 0.14 a 表 4 不同施肥对普陀樟苗木养分吸收及利用的影响
Table 4. Effects of different treatments on nutrient uptake and utilization of Cinnamomum japonicum var. chenii seedlings
器官 处理 EAUN/% EAUP/% EAUK/% EF/(g·g-1) IBH/(g·g-1) INH/% IPH/% IKH/% 养分 T50 3.71 ±0.42a 2.87 ±0.87a 1.26 ±0.04a 2.41 ±0.11a 3.15± 0.11a 6.90 ±1.40a 5.40 ±0.72a 3.67 ±0.39 a 库 T100 1.89 ±0.71a 2.08 ±1.46a 1.21 ±0.32a 1.32 ±0.21a 1.69± 0.21b 4.15 ±0.71a 3.51 ±0.58b 2.58 ±0.33 a 全株 T50 10.07 ±0.53a 6.40 ±1.53a 3.67 ±0.71a 6.90 ±0.35a 8.25± 0.35a 25.50 ±0.91a 15.65 ±0.92a 10.98±0.68a T100 6.96 ±0.39b 4.13 ±0.24b 2.60 ±0.11b 3.37 ±0.15b 4.05± 0.15b 14.67 ±0.91b 8.75 ±0.22b 6.26 ±0.12 b 表 5 不同施肥对土壤养分的影响
Table 5. Effects of different treatments on soil nutrient
月份 处理 pH 有机质/(g·kg-1) 碱解氮/(mg·kg-1) 有效磷/(mg·kg-1) 速效钾/(mg·kg-1) ck 6.33 ± 0.12 a 22.51 ± 6.57 a 106.35 ± 1.87 ab 40.30 ± 3.32 b 106.67 ± 12.94 c 6 T50 6.07 ± 0.01 b 30.65 ± 5.26 a 102.74 ± 0.42 b 58.56 ± 8.73 ab 144.83 ± 5.67 b T100 6.15 ± 0.04 ab 29.35 ± 6.12 a 113.20 ± 3.12 a 60.06 ± 1.19 a 181.83 ± 4.70 a ck 6.27 ± 0.16 a 19.90 ± 8.94 a 92.29 ± 6.97 a 48.30 ± 1.11 a 64.00 ± 8.61 c 9 T50 5.82 ± 0.09 b 24.84 ± 5.49 a 105.99 ± 1.25 a 46.68 ± 12.03 a 104.25 ± 0.43 b T100 5.62 ± 0.26 c 25.40 ± 0.75 a 97.82 ± 1.25 a 72.82 ± 3.03 a 158.50 ± 2.89 a -
[1] 孙慧彦,刘勇,马履一,等. 氮磷供给对长白落叶松苗木质量的影响[J]. 内蒙古农业大学学报,2011,32(3):58-62. SUN Huiyan,LIU Yong,MA Lüyi,et al. Effects of supplying of nitrogen and phosphorus to larix olgensis seedling quality[J]. J Inner Mongolia Agric Univ,2011,32(3):58-62. [2] 左海军,马履一,王梓,等. 苗木施肥技术及其发展趋势[J]. 世界林业研究,2010,23(3):39-43. ZUO Haijun,MA Lüyi,WANG Zi,et al. Research on fertilizer application technology for seedlings and its development trends[J]. World For Res,2010,23(3):39-43. [3] 蒋云东,王达明,邱琼,等. 7种热带阔叶树种的苗木施肥试验[J]. 云南林业科技,2003(2):11-16. JIANG Yundong,WANG Daming,QIU Qiong,et al. Fertilization experiment on young plants of seven broad-leaved tree species indigenous to tropical areas[J]. J Yunnan For Sci Technol,2003(2):11-16. [4] 郑辉,刘彦慈,李帅英,等. 氮磷对刺槐生长和蛋白质组分的影响[J]. 河北农业大学学报,2006,29(5):44-46. ZHENG Hui,LIU Yanci,LI Shuaiying,et al. Effects of nitrogen and phosphorus on growth and protein component of Robinia pseudoacacia[J]. J Agric Univ Hebei,2006,29(5):44-46. [5] 吴俊杰,刘方春,马丙尧,等. 滨海盐碱地白蜡的施肥效应[J]. 林业科技开发,2013,27(5):57-60. WU Junjie,LIU Fangchun,MA Bingyao,et al. Growth response of Fraxinus chinensis to fertilizer applications in coastal saline field[J]. China For Sci Technol,2013,27(5):57-60. [6] 吴家胜,张往祥,曹福亮. 氮磷钾对银杏苗生长和生理特性的影响[J]. 南京林业大学学报:自然科学版,2003,27(1):63-66. WU Jiasheng,ZHANG Wangxiang,CAO Fuliang. Effects of different application amount of nitrogen,phosphorus and potassium on growth and physiological properties of ginkgo seedling[J]. J Nanjing For Univ Nat Sci Ed,2003,27(1):63-66. [7] BOIVIN J R,SALIFU K F,TIMMER V R. Late-season fertilization of Picea mariana seedlings:intensive loading and outplanting response on greenhouse bioassays[J]. Ann For Sci,2004,61:737-745. [8] 康瑶瑶,刘勇,马履一,等. 施肥对长白落叶松苗木养分库氮磷吸收及利用的影响[J]. 北京林业大学学报,2011,33(2):31-36. KANG Yaoyao,LIU Yong,MA Lüyi,et al. Effects of fertilization on uptake and availability of N and P nutrient pool of Larix olgensis seedlings[J]. J Beijing For Univ,2011,33(2):31-36. [9] 鲁如坤. 土壤农业化学分析方法[M]. 北京:中国农业科技出版社,2000. [10] 王力朋,李吉跃,王军辉,等. 指数施肥对楸树无性系幼苗生长和氮素吸收利用效率的影响[J]. 北京林业大学学报,2012,34(6):55-62. WANG Lipeng,LI Jiyue,WANG Junhui,et al. Effects of exponential fertilization on seedling growth and nitrogen uptake and utilization efficiency of Catalpa bungei clones[J]. J Beijing For Univ,2012,34(6):55-62. [11] 吴家森,陈闻,姜培坤,等. 不同施肥对雷竹林土壤氮、磷渗漏流失的影响[J]. 水土保持学报,2012,26(2):33-37. WU Jiasen,CHEN Wen,JIANG Peikun,et al. Effects of different fertilization on seepage loses of nitrogen and phosphorus in the soil under Phyllostacys praecox stand[J]. J Soil Water Conserv,2012,26(2):33-37. [12] TIMMER V R. Exponential nutrient loading:a new fertilization technique to improve seedlings performance on competitive sites[J]. 1996,13(1/3):275-295. [13] 李国雷,祝燕,蒋乐,等. 指数施肥对栓皮栎容器苗生长和氮积累的影响[J]. 东北林业大学学报,2012,40(11):6-9. LI Guolei,ZHU Yan,JIANG Le,et al. Effect of exponential fertilization on growth and nitrogen storage of containerized Quercus variabilis seedlings[J]. J Northeast For Univ,2012,40(11):6-9. [14] 魏红旭,徐程扬,马履一,等. 不同指数施肥方法下长白落叶松播种苗的需肥规律[J]. 生态学报,2010,30(3):685-690. WEI Hongxu,XU Chengyang,MA Lüyi,et al. Nutrient uptake of Larix olgensis seedlings in response to different exponential regimes[J]. Acta Ecol Sin,2010,30(3):685-690. [15] CUESTA B,VILLAR-SALVADOR P,PUERTOLAS J,et al. Why do large,nitrogen rich seedlings better resist stressful transplanting conditions? A physiological analysis in two functionally contrasting Mediterranean forest species[J]. For Ecol Manage,2010,260(1):71-78. [16] CUESTA B,VEGA J,VILLAR-SALVADOR P,et al. Root growth dynamics of Aloppo pine(Pinus halepensis Mill.)seedlings in relation to shoot elongation,plant size and tissue nitrogen concentration[J]. Trees,2010,24(5):899-908. [17] KAINER K,DURYEA M. Root wrenching and lifting date of slash pine:effects on morphology,survival,and growth[J]. New For,1990,4(3):207-221. [18] SALIFU K F.TIMMER V R. Nitrogen retranslocation response of young Picea mariana to nitrogen-15 supply[J]. Soil Sci Soc Am J,2003,67(1):309-317. [19] OLIET J A,PLANELLES R,ARTERO F,et al. Field performance of pinus halepensisi planted in Mediterranean arid conditions:relative influence of seedling morphology and mineral nutrition[J]. New For,2009,37(3):313-331. [20] 郝龙飞,王庆成,张彦东,等. 指数施肥对山桃稠李播种苗生物量及养分动态的影响[J]. 林业科学,2012,48(6):33-39. HAO Longfei,WANG Qingcheng,ZHANG Yandong,et al. Effect of exponential fertilization on biomass and nutrient dynamics of Padus maackii seedlings[J]. Sci Silv Sin,2012,48(6):33-39. [21] 陈闻,吴家森,姜培坤,等. 不同施肥对雷竹林土壤肥力及肥料利用率的影响[J]. 土壤学报,2011,48(5):129-136. CHEN Wen,WU Jiasen,JIANG Peikun,et al. Effects of different fertilization on soil fertility quality,fertilizeruse efficiency,and bamboo shoot yields of Phyllostachys praecox stand[J]. Acta Pedol Sin,2011,48(5):129-136. [22] 孙宇,李国雷,刘勇,等. 水施磷肥对长白落叶松苗木生长和磷吸收的影响[J]. 浙江农林大学学报,2011,28(2):219-226. SUN Yu,LI Guolei,LIU Yong,et al. Growth and P-uptake for Larix olgensis seedlings with phosphorus top-dressed using fertigation[J]. J Zhejiang A & F Univ,2011,28(2):219-226. [23] 马嘉伟,黄其颖,程礼泽,等. 菌渣化肥配合施对红壤养分动态变化及水稻生长的影响[J]. 浙江农业学报,2013,25(1):147-151. MA Jiawei,HUANG Qiying,CHENG Lize,et al. Effect of edible fungus residue on dynamic changes of red soil nutrient and rice yield[J]. Acta Agric Zhejiang,2013,25(1):147-151. [24] 温广蝉,叶正钱,王旭东,等. 菌渣还田对稻田土壤养分动态变化的影响[J]. 水土保持学报,2012,26(3):82-86. WEN Guangchan,YE Zhengqian,WANG Xudong,et al. Effect of edible fungus residue on dynamic changes of soil nutrient in paddy field[J]. J Soil Water Conserv,2012,26(3):82-86. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.2014.03.005







 下载:
下载: