-
树冠是林木进行光合作用的物质基础,是制造干物质的载体。树木对太阳辐射和降水的利用受限于树冠的结构和空间分布特征,不同特征的树冠对能量的接受、利用、传输和分配呈现出空间异质性,导致不同冠层叶片的光合作用存在空间差异[1-2]。学者们针对不同冠层光合作用的研究涉及到很多树种,如糖枫Acer saccharum[3],欧洲山杨Populus tremula[4],小叶椴Tilia cordata[4],欧榛Corylus avellana[4],杉木Cunninghamia lanceolata[5],三倍体毛白杨Populus tomentosa[6],樟树Cinnamomum camphora[7],杂种落叶松Larix gmelinii[8],杨树Populus × euramericana[9]等树种。目前,针对用材林人工修枝技术的研究,主要集中在人为设置不同修枝强度进行一些对比试验,很少从不同冠层分枝光合能力差异方面进行研究,难以真正科学指导用材林的人工修枝。因此,本研究以9年生格木Erythrophleum fordii-马尾松Pinus massoniana混交人工林为研究对象,在指定方向分3个冠层测定其叶片的光合作用,评判不同冠层分枝叶片的光合能力,为科学制定格木人工林修枝技术提供理论依据。
-
研究地点位于广西凭祥市中国林业科学研究院热带林业实验中心青山实验场。该地区处于南亚热带季风气候区域内的西南部,与北热带北缘毗邻,属湿润半湿润气候。境内日照充足,雨水充沛,干湿季节明显,光、水、热资源丰富。年均气温为20.5~21.7 ℃,极端高温为40.3 ℃,极端低温为-1.5 ℃;≥10 ℃活动积温为6 000~7 600 ℃。年均降水量为1 200.0~1 500.0 mm,年蒸发量为1 261.0~1 388.0 mm,相对湿度为80%~84%。主要地貌类型以低山丘陵为主,坡度以25°~30°为多。地带性土壤为砖红壤,土层厚度大于1.0 m。
-
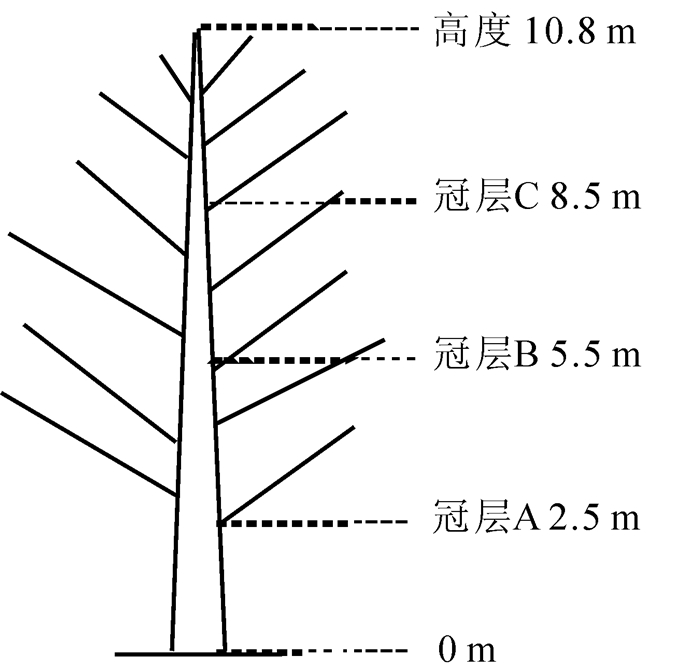
所选试验地为2006年春营造的格木-马尾松混交人工林,造林密度为2 500株·hm-2,混交比例为1:3。设置3个试验样地,在每木检尺的基础上,选出冠形完好的优势木3株·样地-1,根据格木枝条生长特性,将树冠分3层(图 1,从下至上依次为冠层A,冠层B和冠层C),通过人工搭竹架来观测不同冠层叶片的光合指标。
-
于2016年6-7月,在所选3个冠层的指定方位各选取最大枝条上外围的成熟功能叶并标记,用Li-6400XT光合仪(美国Li-Cor公司)观测己标记功能叶的光合参数。
光响应曲线测定:测量时间选择天气晴朗的上午9:30-11:30,为保持其他环境因子稳定且适宜,将叶室温度设为28 ℃,二氧化碳摩尔分数设为(400 ± 10)μmol·mol-1,用Li-6400红蓝光源控制光强,光强依次设为2 000,1 800,1 600,1 400,1 200,1 000,800,600,400,200,100,80,60,40,30,20,10,5,0 μmol·m-2·s-1,并根据该曲线计算出光补偿点、光饱和点及最大净光合速率等重要参数。
二氧化碳响应曲线测定:测量时间仍选择在晴朗天气的上午9: 30-11: 30,使用LED红蓝光源控制光和有效辐射值为光饱和点,设置环境二氧化碳摩尔分数的变化梯度为1 800,1 500,1 200,1 000,800,600,400,200,150,100,50,30,20,0 μmol·mol-1,依次测定不同二氧化碳摩尔分数下的光合速率,绘制二氧化碳响应曲线,并根据曲线计算二氧化碳补偿点、饱和点、羟化效率及最大光合能力等指标。
不同冠层光合参数的日变化:选择晴朗天气8:00-17:00,将Li-6400XT光合仪叶室条件与自然环境保持一致,1 h测定1次3个冠层已标记功能叶的的净光合速率(Pn,μmol·m-2·s-1),蒸腾速率(Tr,mmol·m-2·s-1),胞间二氧化碳摩尔分数(Ci,μmol·mol-1),气孔导度(Gs,mol·m-2·s-1),光合有效辐射(PAR,μmol·m-2·s-1),叶片温度(T,℃)等光合生理指标。
-
用DPS 14.5数据处理软件对格木人工林不同冠层叶片光合特性进行统计分析;利用直角双曲线修正模型分别对其光响应曲线[10-11]和二氧化碳响应曲线[12]进行拟合及参数计算,并用Excel进行分析作图。
-
利用直角双曲线修正模型对格木人工林下、中、上3个冠层叶片的光响应曲线进行拟合,拟合效果较好,确定系数R2值均在0.99以上,其模型参数如表 1所示。由图 2可看出:格木人工林不同冠层叶片净光合速率(Pn)均随着光照强度(PAR)的增强而升高,但其光响应曲线变化趋势的不同阶段各光合参数存在明显差异。
表 1 不同冠层光响应曲线拟合模型参数
Table 1. Model coefficient of light-response curve in different canopy layers
冠层 α β γ Rd/(μmol·m-2·s-1) R2 冠层A 0.033 971 0.000 112 0.005 958 1.145 9 0.995 5 冠层B 0.049 884 0.000 058 0.004 753 0.484 0 0.996 0 冠层C 0.066 298 0.000 066 0.003 333 0.288 9 0.999 5 说明:α,β,γ是3个系数,α是光响应曲线的初始斜率,表示植物在光合作用对光的利用效率,β为修正因子,系数γ=α/Pmax,Rd为暗呼吸速率。 
图 2 格木不同冠层光响应曲线
Figure 2. Light-response curvein different canopy layers of Erythrophleum fordii plantation
从表 2可知:格木人工林中冠层A,冠层B和冠层C叶片的初始斜率(α),最大净光合速率(Pmax)和饱和光强值(Isat)的顺序相同,均为冠层A<冠层B<冠层C,光补偿点(Ic)和暗呼吸速率(Rd)顺序相反,为冠层A>冠层B>冠层C,且3个冠层各参数差异均达到显著或极显著水平。随着格木人工林冠层高度增加叶片光合的初始斜率增大,最大净光合速率增大,而暗呼吸速率却减小,这表明格木叶片对光合物质的积累随着冠层高度增加而增强,对光合产物的消耗在减少。随着格木人工林冠层高度增加,饱和光强增大,而光补偿点却减小,表明随着冠层越高,格木叶片的光合能力越强,光合作用要求的有效辐射强度范围越宽,对较强及弱光的利用效率越高。
表 2 不同冠层光响应曲线各参数统计表
Table 2. Statistical table of model coefficient of light-response curvein different canopy layers
冠层 初始斜率α 最大净光合速率Pmax/
(μmol· m-2·s-1)饱和光强Isat/
(μmol·m-2·s-1)光补偿点Ic/
(μmol·m-2·s-1)暗呼吸速率Rd/
(μmol·m-2·s-1)冠层A 0.033 971 ± 0.013 2 bc 4.468 6 ± 1.12 BCc 1 067.17 ± 9.47 Cc 30.98 ± 6.78 Aa 1.15 ± 0.33 Aa 冠层B 0.049 884 ± 0.019 6 ab 6.242 9 ± 1.86 Bb 1 700.54 ± 7.39 Bb 12.89 ± 5.39 Bb 0.48 ± 0.21 Bb 冠层C 0.066 298 ± 0.021 8 a 14.733 5 ± 3.61 Aa 1 852.14 ± 11.82 Aa 4.42 ± 2.43 Cc 0.29 ± 0.15 BCc -
通过直角双曲线修正模型对格木人工林下、中、上冠层叶片的二氧化碳响应曲线进行拟合,确定系数R2值均在0.99以上,模型参数如表 3所示。格木人工林不同冠层叶片二氧化碳响应曲线与光响应曲线有着相同的变化趋势,随着二氧化碳摩尔分数升高,冠层A,冠层B和冠层C叶片的Pn值不断增高后呈平缓趋势,3个冠层Pn差距增加,趋势线逐渐分离(图 3)。
表 3 不同冠层二氧化碳响应曲线拟合模型参数
Table 3. Model coefficient of CO2 response curvein different canopy layers
冠层 α β γ Rp/(μmol.m-2·s-1) R2 冠层A 0.014 245 0.000 234 38 0.000 12 0.647 6 0.996 2 冠层B 0.023 058 0.000 203 46 0.000 24 1.503 4 0.997 0 冠层C 0.071 167 0.000 099 42 0.002 11 2.141 6 0.992 3 说明α, β, γ是3个系数,α为二氧化碳响应曲线上Cisat=0处的斜率,即为植物的初始羧化效率,β为修正因子,系数γ=α/Amax,Rp为光呼吸速率。 
图 3 格木不同冠层二氧化碳响应曲线
Figure 3. CO2 response curve in different canopy layers of Erythrophleum fordii plantation
从表 3可知:格木人工林3个冠层叶片的二氧化碳响应拟合曲线各参数的均达到显著或极显著水平。冠层A,冠层B和冠层C叶片的初始羟化效率(α)和光合能力(Amax)的顺序相同,均为冠层A<冠层B<冠层C,说明高冠层格木叶片在低二氧化碳浓度条件下,具有更高的光合速率,且潜在的光合能力更强;二氧化碳补偿点(Γ)顺序相反,二氧化碳补偿点低,表明叶片具有净光合速率高、产量高的特点,二氧化碳补偿点经常作为评价植物光合性能的一个可靠指标;光呼吸速率(Rp)大小顺序为冠层A<冠层B<冠层C,光呼吸变化与光合作用保持着一定的平行关系[13],因此,高冠层叶片光合能力较强,光呼吸速率也相应的增高。同时,光呼吸速率和羧化效率共同影响二氧化碳补偿点的变化结果[14]。
-
在格木人工林生长旺盛季节,选择晴朗无云天气测定3个冠层同一天内不同时间的光合参数,并绘制分布图(图 4)。格木人工林3个冠层的PAR,Tr与T的日变化表现出大致相同的规律,为单峰型,分别在12:00,13:00与14:00达到峰值。Pn与Gs日变化曲线呈双峰型,3个冠层Pn峰值出现的时间均不同,分别为冠层A:10:00与15:00,冠层B:11:00与15:00,冠层C:12:00与15:00;冠层A的Gs峰值的时间与冠层B和冠层C不同,冠层A:10:00与15:00,冠层B和冠层C:11:00与16:00。3个冠层Ci的日变化一致,为“U”型曲线,均在13:00出现最低值。3个冠层的各光合参数均随冠层高度增加而增大,Ci与T变化幅度较小。
-
格木不同冠层叶片净光合速率与各光合因子的通径分析结果如表 5所示。冠层A中PAR,T,与Gs对Pn的直接通径系数绝对值较大,其中PAR的直接作用最大。冠层B中Gs与PAR对Pn的直接通径系数绝对值较大,其中Gs的直接作用最大。冠层C中Tr,PAR与Gs对Pn的直接通径系数绝对值较大,其中Tr的直接作用最大。
表 4 不同冠层二氧化碳响应曲线各参数统计表
Table 4. Statistical table of model coefficient of CO2 response curve in different canopy layers
冠层 初始羧化效率α/
(mol·m-2·s-1)光合能力Amax/
(μmol·m-2·s-1)饱和胞间二氧化碳摩尔分数Cisat/(μmol·mol-1) 二氧化碳补偿点Г/
(μmol·mol-1)光呼吸速率Rp/
(μmol·m-2·s-1)冠层A 0.014 2 ± 0.008 5 BCc 11.57 ± 2.67 Cc 1 913.21 ± 11.65 ab 66.21 ± 8.56 Aa 0.65 ± 0.32 Cc 冠层B 0.023 1 ± 0.010 3 Bb 17.04 ± 4.93 ABb 1 988.08 ± 10.85 a 57.16 ± 7.39 ABb 1.50 ± 0.61 ABb 冠层C 0.071 2 ± 0.015 2 Aa 19.74 ± 4.03 Aa 1 758.68 ± 15.67 bc 32.25 ± 9.88 Cc 2.14 ± 1.53 Aa 表 5 不同冠层净光合速率与光合因子的通径分析
Table 5. 5 Path analysis between Pn and physiological factors in different canopy layers
冠层 因子 直接通径系数 间接通径系数 PAR Tr Gs ci T 冠层A PAR 1.171 7 0.080 4 -0.376 3 0.257 0 -0.635 9 Tr 0.111 3 0.846 5 -0.507 7 0.278 5 -0.723 0 Gs 0.864 7 -0.509 9 -0.065 3 -0.170 3 0.257 6 ci -0.346 8 -0.868 3 -0.089 4 0.424 6 0.800 6 T -0.883 3 0.843 4 0.091 1 -0.252 2 0.3143 冠层B PAR 0.471 9 -0.018 3 -0.270 1 -0.187 7 0.021 4 Tr -0.019 1 0.452 5 -0.3143 -0.197 6 0.022 4 Gs 0.879 0 -0.145 0 0.006 8 0.092 6 -0.005 5 ci 0.215 3 -0.411 3 0.017 6 0.378 0 -0.022 5 T 0.023 9 0.422 2 -0.017 9 -0.201 5 -0.202 8 冠层C PAR 0.890 5 -0.860 0 -0.345 5 -0.209 4 0.323 4 Tr -0.896 1 0.854 6 -0.424 7 -0.217 2 0.329 8 Gs 0.830 9 -0.370 3 0.458 0 0.088 0 -0.111 5 ci 0.228 9 -0.8147 0.850 3 0.319 5 -0.344 5 T 0.376 0 0.766 0 -0.786 1 -0.246 3 -0.209 7 -
树冠的组成及树冠生物量的多少直接影响不同高度分枝的叶片对光辐射能的截获[15]。格木人工林不同冠层受到的遮光强度不同,导致3个冠层接受的光辐射存在差异,高冠层各时间段测定的PAR值要高于低冠层的。通径分析表明,光合有效辐射及气孔导度均是影响格木人工林3个冠层的净光合速率的主要因子。
植物光合作用对不同强度的光照具有一定的适应能力,但是光强是影响植物光合作用的重要外界因子[16]。冠层上层到下层光强的衰减会导致不同冠层叶片的光合能力呈现显著差异[17-18]。所处环境光照强度不同,格木不同冠层叶片光合特性表现出了明显的差异。高冠层叶片的光合初始斜率、最大净光合速率均大于低冠层的,而暗呼吸速率相反,这说明格木高冠层叶片光合物质的积累能力较强,对光合产物的消耗也较少;高冠层叶片要求饱和光强较大,而光补偿点却较小,说明高冠层格木叶片对光强适应范围较宽,对光的利用效率较高。3个冠层格木叶片的二氧化碳响应拟合曲线研究结果显示,高冠层叶片的初始羟化效率、光合能力均高于低冠层的,高冠层格木叶片具有更高的光合速率和更强的潜在光合能力。
综合研究结果发现,高冠层分枝叶片的初始羟化效率、光合能力及对光合物质的积累能力均显著高于中冠层与低冠层。这说明下部冠层枝条长期处在较弱光强环境中,处在该冠层分枝叶片的光合能力下降。因此,依据不同冠层分枝叶片的光合特性的差异,可以通过人工修枝措施,修除下冠层光合能力较差的分枝,以优化树冠结构,调节树冠内微环境,提高树木的光合作用能力[8]。此种人工修枝措施一方面能促进格木生长,另一方面又可以优化干形,对格木人工林无节良材的培育具有重要指导意义。
hotosynthetic characteristics in different canopy positions of an Erythrophleum fordii plantation
-
摘要: 评价格木Erythrophleum fordii人工林不同冠层分枝的光合能力,为格木人工林修枝提供光合生理基础。以9年生格木-马尾松Pinus massoniana混交人工林为研究对象,观测格木人工林不同冠层叶片的光响应曲线、二氧化碳响应曲线及光合因子的日变化。结果表明:格木人工林不同冠层叶片的光合初始斜率(α)和最大净光合速率(Pmax)的大小顺序相同,依次为冠层C > 冠层B > 冠层A,而暗呼吸速率(Rd)大小顺序则相反,高冠层叶片的饱和光强(Isat)较大,而光补偿点(Ic)却较低,且3个冠层各参数差异均达到显著或极显著水平;3个冠层叶片的初始羟化效率(α),光合能力(Amax)的顺序相同,均为冠层C > 冠层B > 冠层A,而二氧化碳补偿点(Γ)顺序相反,光呼吸(Rp)变化与光合作用保持着平行关系;3个冠层的光合有效辐射(PAR),蒸腾速率(Tr)与叶片温度(T)的日变化为单峰型,净光合速率(Pn)与气孔导度(Gs)日变化曲线呈双峰型,但峰值出现的时间均不同,3个冠层胞间二氧化碳摩尔分数(Ci)的日变化一致,为“U”型曲线,均在13:00出现最低值;通径分析结果表明:光合有效辐射与气孔导度对3个冠层净光合速率的直接通径系数绝对值均较大,表明光合有效辐射及气孔导度是影响格木人工林3个冠层叶片的净光合速率的主要因子。格木高冠层叶片具有更高的光合速率和更强的潜在光合能力,对光合物质的积累能力较强,消耗光合产物较少。Abstract: To evaluate the photosynthetic characteristics of different canopy positions and to provide a photosynthetic physiological basis for pruning in an Erythrophleum fordii plantation, light intensity, light response curve, CO2 response curve, and the dynamic changes of photosynthetic factors were measured in different canopy positions of an E. fordii × Pinus massoniana plantation. Also, photosynthetic capacity of branches in different canopy positions was analyzed and a path analysis was conducted. Results showed that the different canopy positions significantly affected on initial slope photo inhibition (P < 0.05) and maximum net photosynthetic rate (P < 0.01), and ranked as canopy C > canopy B > canopy A; however, dark respiration rate was opposite. There was significant difference in the saturation light and light compensation point in differentcanopy positions (P < 0.01), the saturation light of higher canopy was greater, but the light compensation point was lower. Initial carboxylation efficiency and photosynthetic capacity higher in the canopy were greater than lower in the canopy with highly significant difference (P < 0.01), and the carbon dioxide compensation point of different positions in the canopy was in the reverse order. The relationship between photorespiration and photosynthesis was parallel. Daytime change of photosynthetic active radiation, transpiration rate, and leaf temperature in the three canopy positions appeared as a single peak and the diurnal variation net photosynthetic rate and stomatal conductance showed a typical curve with a double peak, but the time of the peaks was different. The diurnal change of intercellular CO2 concentration in the three canopies was consistent, as a "U" type curve. The path analysis indicated that photosynthetic available radiation and stomatal conductance were the key factors for the net photosynthetic rate in leaves of the three canopy positions of the E. fordii plantation. The high canopy position's photosynthetic rate, potential photosynthetic capacity, and photosynthetic material accumulating ability were stronger, and less of the photosynthetic product was consumed higher in the canopy than lower in the canopy, which could provide scientific guidance to determine the pruning intensity in E. fordii plantation.
-
表 1 不同冠层光响应曲线拟合模型参数
Table 1. Model coefficient of light-response curve in different canopy layers
冠层 α β γ Rd/(μmol·m-2·s-1) R2 冠层A 0.033 971 0.000 112 0.005 958 1.145 9 0.995 5 冠层B 0.049 884 0.000 058 0.004 753 0.484 0 0.996 0 冠层C 0.066 298 0.000 066 0.003 333 0.288 9 0.999 5 说明:α,β,γ是3个系数,α是光响应曲线的初始斜率,表示植物在光合作用对光的利用效率,β为修正因子,系数γ=α/Pmax,Rd为暗呼吸速率。 表 2 不同冠层光响应曲线各参数统计表
Table 2. Statistical table of model coefficient of light-response curvein different canopy layers
冠层 初始斜率α 最大净光合速率Pmax/
(μmol· m-2·s-1)饱和光强Isat/
(μmol·m-2·s-1)光补偿点Ic/
(μmol·m-2·s-1)暗呼吸速率Rd/
(μmol·m-2·s-1)冠层A 0.033 971 ± 0.013 2 bc 4.468 6 ± 1.12 BCc 1 067.17 ± 9.47 Cc 30.98 ± 6.78 Aa 1.15 ± 0.33 Aa 冠层B 0.049 884 ± 0.019 6 ab 6.242 9 ± 1.86 Bb 1 700.54 ± 7.39 Bb 12.89 ± 5.39 Bb 0.48 ± 0.21 Bb 冠层C 0.066 298 ± 0.021 8 a 14.733 5 ± 3.61 Aa 1 852.14 ± 11.82 Aa 4.42 ± 2.43 Cc 0.29 ± 0.15 BCc 表 3 不同冠层二氧化碳响应曲线拟合模型参数
Table 3. Model coefficient of CO2 response curvein different canopy layers
冠层 α β γ Rp/(μmol.m-2·s-1) R2 冠层A 0.014 245 0.000 234 38 0.000 12 0.647 6 0.996 2 冠层B 0.023 058 0.000 203 46 0.000 24 1.503 4 0.997 0 冠层C 0.071 167 0.000 099 42 0.002 11 2.141 6 0.992 3 说明α, β, γ是3个系数,α为二氧化碳响应曲线上Cisat=0处的斜率,即为植物的初始羧化效率,β为修正因子,系数γ=α/Amax,Rp为光呼吸速率。 表 4 不同冠层二氧化碳响应曲线各参数统计表
Table 4. Statistical table of model coefficient of CO2 response curve in different canopy layers
冠层 初始羧化效率α/
(mol·m-2·s-1)光合能力Amax/
(μmol·m-2·s-1)饱和胞间二氧化碳摩尔分数Cisat/(μmol·mol-1) 二氧化碳补偿点Г/
(μmol·mol-1)光呼吸速率Rp/
(μmol·m-2·s-1)冠层A 0.014 2 ± 0.008 5 BCc 11.57 ± 2.67 Cc 1 913.21 ± 11.65 ab 66.21 ± 8.56 Aa 0.65 ± 0.32 Cc 冠层B 0.023 1 ± 0.010 3 Bb 17.04 ± 4.93 ABb 1 988.08 ± 10.85 a 57.16 ± 7.39 ABb 1.50 ± 0.61 ABb 冠层C 0.071 2 ± 0.015 2 Aa 19.74 ± 4.03 Aa 1 758.68 ± 15.67 bc 32.25 ± 9.88 Cc 2.14 ± 1.53 Aa 表 5 不同冠层净光合速率与光合因子的通径分析
Table 5. 5 Path analysis between Pn and physiological factors in different canopy layers
冠层 因子 直接通径系数 间接通径系数 PAR Tr Gs ci T 冠层A PAR 1.171 7 0.080 4 -0.376 3 0.257 0 -0.635 9 Tr 0.111 3 0.846 5 -0.507 7 0.278 5 -0.723 0 Gs 0.864 7 -0.509 9 -0.065 3 -0.170 3 0.257 6 ci -0.346 8 -0.868 3 -0.089 4 0.424 6 0.800 6 T -0.883 3 0.843 4 0.091 1 -0.252 2 0.3143 冠层B PAR 0.471 9 -0.018 3 -0.270 1 -0.187 7 0.021 4 Tr -0.019 1 0.452 5 -0.3143 -0.197 6 0.022 4 Gs 0.879 0 -0.145 0 0.006 8 0.092 6 -0.005 5 ci 0.215 3 -0.411 3 0.017 6 0.378 0 -0.022 5 T 0.023 9 0.422 2 -0.017 9 -0.201 5 -0.202 8 冠层C PAR 0.890 5 -0.860 0 -0.345 5 -0.209 4 0.323 4 Tr -0.896 1 0.854 6 -0.424 7 -0.217 2 0.329 8 Gs 0.830 9 -0.370 3 0.458 0 0.088 0 -0.111 5 ci 0.228 9 -0.8147 0.850 3 0.319 5 -0.344 5 T 0.376 0 0.766 0 -0.786 1 -0.246 3 -0.209 7 -
[1] VIERLING L A, WESSMAN C A. Photosynthetically active radiation heterogeneity within a monodominant Congolese rain forest canopy [J]. Agric For Meteorol, 2000, 103(3): 265-278. [2] ANTEN N P R. Optimal photosynthetic characteristics of individual plants in vegetation stands and implications for species coexistence [J]. Ann Bot, 2005, 95(3): 495-506. [3] ELLSWORTH D S, REICH P B. Canopy structure and vertical patterns of photosynthesis and related leaf traits in a deciduous forest [J]. Oecologia, 1993, 96(2): 169-178. [4] KULL O, NIINEMETS Ü. Distribution of leaf photosynthetic properties in tree canopies: comparison of species with different shade tolerance [J]. Funct Ecol, 1998, 12(3): 472-479. [5] 张小全, 徐德应, 赵茂盛, 等. CO2增长对杉木中龄林针叶光合生理生态的影响[J].生态学报, 2000, 20(3):390-396. ZHANG Xiaoquan, XU Deying, ZHAO Maosheng, et al. The responses of 17 years old Chinese fir shoots to elevated CO2 [J]. Acta Ecol Sin, 2000, 20(3): 390-396. [6] 富丰珍, 徐程扬, 李广德, 等.冠层部位对三倍体毛白杨光合生理特性的影响[J].中南林业科技大学学报, 2010, 30(3):95-99. FU Fengzhen, XU Chengyang, LI Guangde, et al. Effects of canopy position on photosynthesis physiological characteristics of triploid clones of Populus tomentosa [J]. J Cent South Univ For Technol, 2010, 30(3): 95-99. [7] 黄志宏, 田大伦, 闫文德, 等.城市樟树人工林冠层光合作用的时空特征[J].中南林业科技大学学报, 2011, 31(1):38-46. HUANG Zhihong, TIAN Dalun, YAN Wende, et al. Spatial and temporal characteristics of photosynthesis of urbanplantation Cinnamomum camphora in Central South China [J]. J Cent South Univ For & Technol, 2011, 31(1): 38-46. [8] 张元元. 杂种落叶松人工林冠层光合特征及生长过程机理的研究[D]. 哈尔滨: 东北林业大学, 2012. ZHANG Yuanyuan. Study on Growth Process Mechanism and Photosynthetic Characteristics in Canopy of Hybrid Larch Plantation [D]. Harbin: Northeast Forestry University, 2012. [9] 马永春, 方升佐.欧美杨107不同冠层光合特性的研究[J].南京林业大学学报(自然科学版), 2011, 35(4):39-42. MA Yongchun, FANG Shengzuo. Research on photosynthesis characteristics in different canopy layers of poplar clone 107(Populus × euramericana cv. Neva) [J]. J Nanjing For Univ Nat Sci Ed, 2011, 35(4): 39-42. [10] YE Zipiao, YU Qiang. A coupled model of stomatal conductance and photosynthesis for winter wheat [J]. Photosynthetica, 2008, 46(4): 637-640. [11] 叶子飘.光合作用对光和CO2响应模型的研究进展[J].植物生态学报, 2010, 34(6):727-740. YE Zipiao. A review on modeling of responses of photosynthesis to light and CO2 [J]. Chin J Plant Ecol, 2010, 34(6): 727-740. [12] 叶子飘, 于强.光合作用对胞间和大气CO2响应曲线的比较[J].生态学杂志, 2009, 28(11):2233-2238. YE Zipiao, YU Qiang. A comparison of response curves of winter wheat photosynthesis to flag leaf inte rcellular and air CO2 concentrations. [J]. Chin J Ecol, 2009, 28(11): 2233-2238. [13] 董志新, 韩清芳, 贾志宽, 等.不同苜蓿(Medicago sativa L.)品种光合速率对光和CO2浓度的响应特征[J].生态学报, 2007, 27(6):2272-2278. DONG Zhixin, HAN Qingfang, JIA Zhikuan, et al. Photosynthesis rate in response to light intensity and CO2 concentration in different alfalfa varieties [J]. Acta Ecol Sin, 2007, 27(6): 2272-2278. [14] 蔡时青, 许大全.大豆叶片CO2补偿点和光呼吸的关系[J].植物生理学报, 2000, 26(6): 545-550. CAI Shiqing, XU Daquan. Relationship between the CO2 compensation point and photorespiration in soybean leaves[J]. Acta Phytophysiol Sin, 2001, 26(6): 545-550. [15] MONTEITH J L. 2-does light limit crop production?[G]//JOHWSON C B. Physiological Processes Limiting Plant Productivity. London: Elsevier Ltd, 1981: 23-38. [16] 张其德, 唐崇钦, 林世青, 等.光强度对小麦幼苗光合特性的影响[J].植物学报, 1988, 30(5):508-514. ZHANG Qide, TANG Chongqin, LIN Shiqing, et al. Effects of light intensity on photosynthetic characteristics of wheat seedling [J]. J Integr Plant Biol, 1988, 30(5): 508-514. [17] AMTHOR J S. Scaling CO2-photosynthesis relationships from the leaf to the canopy [J]. Photosynth Res, 1994, 39(3): 321-350. [18] HAN Qingmin, CHIBA Y. Leaf photosynthetic responses and related nitrogen changes associated with crown reclosure after thinning in a young Chamaecyparis obtusa stand [J]. J For Res, 2009, 14(6): 349-357. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.2017.05.014







 下载:
下载: