-
全球陆地生态系统中最大的有机碳库即为土壤碳库,是陆地植被碳库的2~3倍、大气碳库的2倍[1-3]。土壤碳库的变化对大气二氧化碳浓度的影响显著,进而影响气候变化。研究表明:大约50%~90%的土壤有机碳是由周转时间约10 a的活性碳所组成的[4],而植硅体碳是除木炭、有机无机复合体以外稳定的碳,周转速率为200~13 300 a[5]。植硅体碳(PhytOC)是植硅体(phytolith)在沉淀过程中封存于植物细胞的有机碳,在植物死亡、腐烂后被分解释放到土壤中。植硅体及其封存的碳可在土壤或沉积物中长久稳定保存,因此土壤在植硅体碳封存过程中扮演着重要的碳库角色。植硅体是植物在生长过程中吸收土壤溶液中单硅酸[Si(OH)4],沉淀在各器官细胞内的非晶质二氧化硅矿物,具有很强的抗氧化性、抗腐蚀性和抗分解能力,可在土壤中保存千年甚至是万年。土壤本身并不生成植硅体碳,而是植物通过光合作用储存在各器官中。早期的碳循环研究一直没有评估植硅体碳的碳汇潜力。土壤中植硅体碳储量较小,但在全球长期的碳循环研究中其碳汇功能不可忽略。有关土壤植硅体、植硅体碳的研究,已从最初植硅体组成成分[6-7]、碳封存机制[8-9]和土壤植硅体及植硅体碳提取方法的探讨[10],到植硅体和植硅体碳在土壤剖面中的迁移和分布[11-12],再到植硅体碳稳定性,以及近年来关于某种特定植被类型土壤植硅体碳储量的估算等[13-15]。特别是植硅体碳封存方面的研究,已经成为新的研究热点,为人类应对全球气候变暖提供了新对策与碳汇途径。目前,关于土壤植硅体碳研究涉及的领域主要有森林[16-19]、湿地[20-23]、草原[24-26]等生态系统。森林植被类型主要以高富硅的竹亚科Bambusoideae植物为研究对象,且研究集中于热带和南亚热带区域。麻栎Quercus acutissima具有耐干旱、耐贫瘠的特点,是荒山瘠地的先锋树种和水土保持的优良树种,广泛分布于亚热带地区[27]。本研究以北亚热带麻栎林为研究对象,探讨不同林龄(幼龄林、中龄林和成熟林)麻栎林土壤的植硅体碳储量,为中国森林生态系统植硅体碳汇研究提供理论依据。
-
本研究区位于江苏省句容市境内,属北亚热带季风气候区,四季分明,光照充足。年均降水量1 057.0 mm,年际变化较大。研究区地处江淮丘陵地带,地形多为丘陵山地,起伏较平缓。土壤母质为第四纪下蜀组黄土状沉积物,类型以黄棕壤和山地黄棕壤为主,土层厚度一般为40~60 cm,土壤质地为中壤至重壤(Q3x),pH 4.5~5.0。森林植被属中国北亚热带东部区的落叶阔叶混交林。研究地是以麻栎为主的天然次生林,零星散布栓皮栎Q. variabilis、锐齿槲栎Q. aliena var. acuteserrata等;灌木主要有野蔷薇Rosa multiflora、牛鼻栓Fortunearia sinensis、华紫珠Callicarpa cathayana、枸骨Ilex cornuta和白檀Symplocos paniculata等;草本植物主要有爬山虎Parthenocissus tricuspidata、铁线蕨Adiantum capillus-veneris、白茅Imperata cylindrica、麦冬Ophiopogon japonicus和络石Trachelospermum jasminoides等。
-
本研究样地设置在江苏省句容市下蜀林场和句容林场,选取幼龄林(17 a)、中龄林(26 a)和成熟林(65 a)等3种不同林龄的麻栎混交林,于2017年7−8月在每个林地按坡位(坡上、坡中、坡下)选择3个调查样地(20 m×20 m),共9块样地进行调查。对麻栎林样地进行每木检尺,测量记录胸径、树高,确定标准木,并调查地形地貌以及林分特征等指标(表1)。
表 1 样地基本情况
Table 1. Basic characteristics of sampting plots studied
样地 林龄/
a坡度/
(°)坡位 林分密度/
(株·m−2)胸径/
cm树高/
m郁闭度/
%1 17 30 坡下 975 10.2 8.60 48 2 17 34 坡中 700 10.7 8.85 45 3 17 40 坡上 300 14.2 10.31 35 4 26 8 坡下 775 13.4 9.94 80 5 26 8 坡下 825 15.2 10.63 80 6 26 8 坡下 600 14.2 10.31 75 7 65 28 坡下 225 28.6 15.25 55 8 65 31 坡中 325 26.9 14.73 45 9 65 28 坡下 350 25.3 14.20 47 说明:幼龄林坡陡,土壤砾石含量为30%左右,多为禾本 科Gramineae草本植物;中龄林坡缓,土壤砾石含量 为20%左右,土壤紧实,灌草茂盛;成熟林坡陡, 土壤砾石含量为25%左右,草本植物多为络石 本研究在每个样地内沿对角线分别在坡上、坡中、坡下各挖1个60 cm深的土壤剖面,按0~10、10~20、20~40、40~60 cm分层取样,并取原状土和袋装土带回实验室,测定土壤理化性质和植硅体碳。
-
将土壤样品置于通风阴凉处风干,去除根系、砾石,经研磨后过2.000、0.250、0.149 mm直径的筛网,用于分析。土壤基本理化性质测定:土壤容重采用环刀法;pH用电位法测定,土水质量比为1.0∶2.5;土壤砾石含量采用排水法;土壤颗粒组成采用激光粒度分析仪法;有效磷采用盐酸和硫酸溶液浸提法;碱解氮采用碱解扩散法;速效钾采用乙酸铵浸提-火焰光度法;有机碳质量分数采用重铬酸钾氧化-外加热法。麻栎林土壤基本理化性质见表2。
表 2 麻栎林土壤基本理化性质
Table 2. Basic physical and chemical properties of the soil in Q. acutissima forests
林龄 土壤深度/
cm土壤容重/
(g·cm−3)pH 有效磷/
(mg·kg−1)碱解氮/
(mg·kg−1)速效钾/
(mg·kg−1)有机碳/
(g·kg−1)砂粒/
(g·kg−1)粉粒/
(g·kg−1)黏粒/
(g·kg−1)幼龄林 0~10 1.23 4.88 4.78 99.7 149.8 24.37 826 164 10 10~20 1.28 4.72 4.10 72.3 148.2 18.53 572 402 26 20~40 1.30 4.60 2.91 42.0 133.6 14.59 607 353 44 40~60 1.37 4.56 2.33 32.3 113.4 13.61 614 339 57 中龄林 0~10 1.39 4.72 7.58 115.7 218.4 33.54 356 591 54 10~20 1.47 4.67 3.42 70.0 195.3 29.22 258 654 89 20~40 1.51 4.60 1.91 50.3 182.1 22.17 126 765 109 40~60 1.57 4.58 1.65 38.0 162.0 18.08 110 779 121 成熟林 0~10 1.37 4.55 7.51 229.0 226.7 38.77 460 475 66 10~20 1.40 4.51 5.74 135.3 189.4 31.27 370 545 85 20~40 1.46 4.49 3.39 100.3 186.0 26.94 398 467 135 40~60 1.56 4.48 2.33 83.7 165.8 20.58 410 447 155 说明:粒级划分采用国际制土壤粒级划分标准:砂粒(0.020~2.000 mm);粉粒(0.002~0.020 mm);黏粒(<0.002 mm) 有效硅质量分数采用柠檬酸提取-钼蓝比色法;土壤二氧化硅质量分数采用碱溶法-硅钼蓝比色法;植硅体质量分数采用湿式灰化法测定,并用WALKLEY-BLACK[28]方法检验植硅体外缘的有机碳是否完全除去,提取出的植硅体经干燥后称量得到植硅体质量,计算植硅体质量分数;植硅体碳质量分数采用碱溶分光光度法[29]。在测定样品的同时,加入土壤成分分析标准物质(GBW07405),检验其准确性。
-
土壤植硅体质量分数(g·kg−1)=植硅体质量(g)/土壤质量(kg);土壤植硅体碳质量分数(g·kg−1)=植硅体封存有机碳质量(g)/土壤质量(kg);植硅体中有机碳质量分数(g·kg−1)=植硅体封存有机碳质量(g)/植硅体质量(kg)。土壤植硅体碳储量
$({\rm{t}} \cdot {\rm{h}}{{\rm{m}}^{{\text{−2}}}}) = \displaystyle\sum\limits_{i = 1}^{n} {{K_i}} \times {\rho _{\rm{b}}}_i \times {C_i} \times \left( {{\rm{100 {\text{−}} }}{G_i}} \right) \times {\rm{1}}{{\rm{0}}^{{\text{−3}}}}$ ;土壤有机碳储量$({\rm{t}} \cdot {\rm{h}}{{\rm{m}}^{{\text{−2}}}}) = $ $\displaystyle\sum\limits_{i=1}^{n} {{K_i}} \times {{\rm{\rho }}_{\rm{b}}}_i \times {D_i} \times (100{\text{−}}{G_i}) \times {10^{{\text{−3}}}}$ 。其中:Ki为i层土壤深度(cm),ρbi为i层土壤容重(g·cm−3),Ci为i层植硅体碳质量分数(g·kg−1),Di为i层有机碳质量分数(g·kg−1),Gi为直径≥2 mm 的石砾所占的体积百分比(%)。 -
采用SPSS 22.0和Excel 2003进行数据统计分析,平均值计算采用加权平均法。采用最小显著极差(LSR)法对土壤不同土层的二氧化硅、植硅体及植硅体碳等质量分数进行方差分析和显著性检验(显著性水平P<0.05),采用Pearson法对土壤不同土层的二氧化硅、有效硅、植硅体、植硅体碳及有机碳变量间的相关关系进行分析,并用Origin 9.0软件绘图。
-
由图1A可知:麻栎林土壤不同土层有效硅质量分数为45.7~153.3 mg·kg−1,各林龄麻栎林土壤有效硅质量分数随土层深度增加而增大,各分层之间有效硅质量分数差异不显著;不同林龄麻栎林土壤有效硅质量分数差异显著(P<0.05),麻栎林土壤有效硅平均质量分数从大到小依次为幼龄林、成熟林、中龄林。麻栎林土壤不同土层二氧化硅质量分数为181.8~444.1 g·kg−1(图1B),不同林龄之间土壤二氧化硅平均质量分数差异显著(P<0.05);麻栎幼龄林和成熟林土壤二氧化硅质量分数随土层深度增加先增大后减小,中龄林土壤二氧化硅质量分数大致随土层深度增加而减小,各土层之间二氧化硅质量分数差异不显著。
-
麻栎林土壤不同土层植硅体质量分数为7.10~8.23 g·kg−1 (图2A),植硅体碳质量分数为0.09~0.29 g·kg−1 (图2B),幼龄林和成熟林土壤植硅体、植硅体碳质量分数随土层深度增加先增大后减小,而中龄林土壤大致随土层深度增加而减小,各土层之间植硅体、植硅体碳质量分数差异不显著。麻栎林不同土层植硅体、植硅体碳质量分数从大到小大致表现为幼龄林、中龄林、成熟林,不同林龄之间土壤植硅体、植硅体碳平均质量分数差异显著(P<0.05)。
-
由图3A可知:麻栎林土壤不同土层有机碳质量分数为13.60~38.77 g·kg−1,有机碳质量分数随土层深度增加而减小,各土层之间有机碳质量分数差异显著(P<0.05)。不同林龄麻栎林土壤有机碳平均质量分数从大到小依次为成熟林、中龄林、幼龄林,不同林龄之间土壤有机碳质量分数差异显著(P<0.05)。
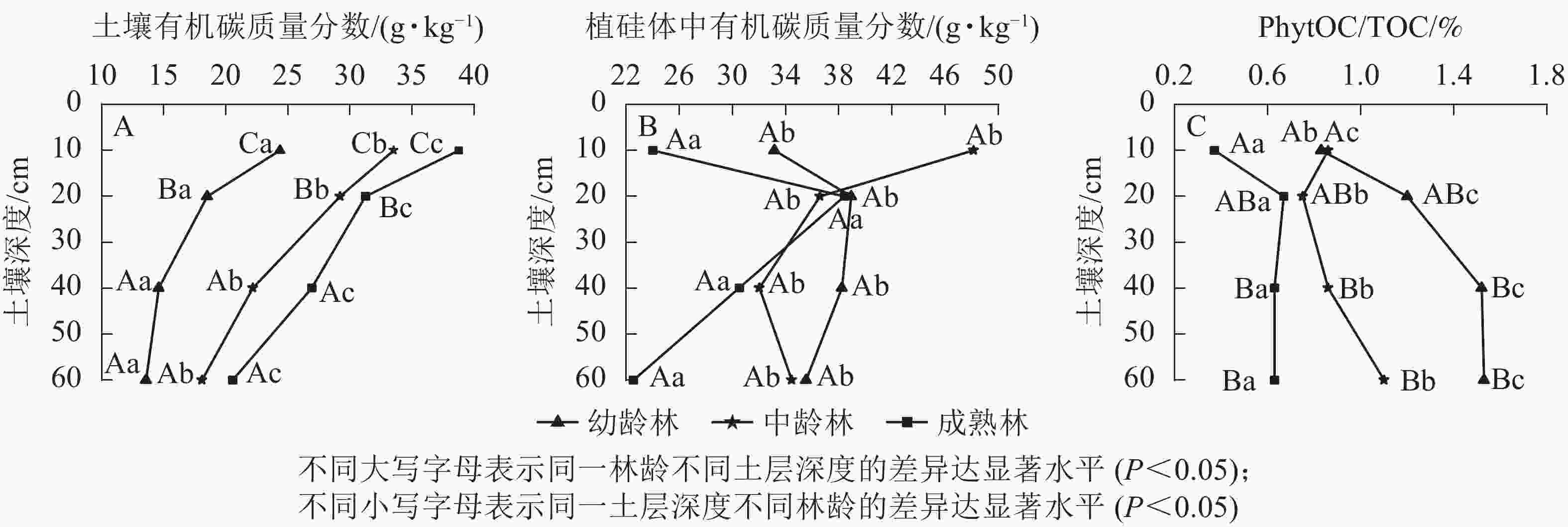
图 3 麻栎林土壤有机碳、植硅体中有机碳质量分数和PhytOC/TOC
Figure 3. Carbon contents, organic carbon contents in phytolith, and PhytOC/TOC in Q. acutissima forests
麻栎林土壤不同土层植硅体中有机碳质量分数为22.57~48.14 g·kg−1 (图3B),与植硅体、植硅体碳质量分数在土壤剖面中的分布规律和差异性一致,即幼龄林和成熟林土壤植硅体中有机碳质量分数随土层深度增加先增大后减小,而中龄林土壤植硅体中有机碳质量分数随土层深度增加而减小,各土层之间植硅体中有机碳质量分数差异不显著,不同林龄之间植硅体中有机碳质量分数差异显著(P<0.05)。土壤植硅体碳与有机碳质量分数比值(PhytOC/TOC)为0.36%~1.49%(图3C),不同土层之间PhytOC/TOC差异不显著,但各林龄之间差异显著(P<0.05)。不同土层植硅体碳中有机碳质量分数从大到小大致表现为幼龄林、中龄林、成熟林。
-
麻栎幼龄林、中龄林、成熟林土壤植硅体碳储量分别为1.16、1.47、1.15 t·hm−2(表3),幼龄林、中龄林、成熟林有机碳储量分别为 94.03、165.28、210.44 t·hm−2,各林龄之间差异不显著。幼龄林、中龄林、成熟林土壤的植硅体碳储量占有机碳储量的比例分别为0.80%~1.50%、0.73%~1.10%、0.36%~0.67%。
表 3 麻栎林土壤植硅体碳储量与有机碳储量
Table 3. PhytOC and organic carbon storages in different soil depths of Q. acutissima forests
林龄 土壤深度/
cm有机碳/
(g·kg−1)植硅体碳/
(g·kg−1)有机碳储量/
(t·hm−2)植硅体碳储量/
(t·hm−2)Phytoc/TOC/% 幼龄林 0~10 24.37 0.198 26.29 0.21 0.80 10~20 18.53 0.223 17.60 0.21 1.19 20~40 14.59 0.214 23.42 0.34 1.45 40~60 13.60 0.203 26.71 0.40 1.50 总计 94.02 1.16 中龄林 0~10 33.54 0.278 37.30 0.31 0.83 10~20 29.22 0.215 34.20 0.25 0.73 20~40 22.17 0.188 50.07 0.43 0.86 40~60 18.08 0.198 43.71 0.48 1.10 总计 165.28 1.47 成熟林 0~10 38.77 0.139 47.78 0.17 0.36 10~20 31.26 0.208 34.53 0.23 0.67 20~40 26.94 0.154 65.18 0.37 0.57 40~60 20.58 0.123 62.95 0.38 0.60 总计 210.44 1.15 -
由表4可知:土壤各层二氧化硅质量分数与植硅体、植硅体碳质量分数之间呈极显著正相关(P<0.01);土壤植硅体碳质量分数与植硅体质量分数之间呈极显著正相关(P<0.01);土壤植硅体碳质量分数与有效硅质量分数之间呈负相关,但未达显著水平(P>0.05);土壤植硅体碳质量分数与有机碳质量分数之间无显著相关关系(P>0.05);植硅体质量分数与有效硅质量分数之间呈显著正相关(P<0.05)。
表 4 麻栎林土壤层5个变量之间的相关性
Table 4. Correlation coefficients between the five variables of Q. acutissima forest soil
变量 二氧化硅 植硅体 植硅体碳 有效硅 有机碳 二氧化硅 1 植硅体 0.534** 1 植硅体碳 0.606** 0.441** 1 有效硅 -0.126 0.372* -0.178 1 有机碳 -0.021 1 说明:*表示P<0.05;**表示P<0.01 -
本研究发现:各林龄麻栎林土壤有效硅质量分数随土层深度增加而增大,与发育于玄武岩[17, 30]、花岗岩[17]的土壤有效硅质量分数的剖面分布规律研究结果一致。本研究麻栎林土壤母岩属于第四纪下蜀组(Q3x)黄土状沉积物,可能是受淋溶等作用有向下迁移的趋势,或是下层母岩风化提高了土壤的有效硅质量分数,而黑钙土、栗钙土和草甸土[30]的有效硅质量分数随土层深度的増加呈现出先减小后增大的趋势。母岩直接影响土壤风化程度和理化性质,并进一步影响土壤有效硅质量分数,因此有效硅质量分数在不同土壤剖面中的分布具有差异性。
FISHKIS等[31]的研究认为:土壤中植硅体碳可向土壤深层迁移,迁移深度可达2.2 m;另有学者认为:植硅体和植硅体碳在土壤剖面表层中容易富集,不易向土壤深层迁移[15, 32]。本研究中麻栎幼龄林和成熟林土壤二氧化硅、植硅体、植硅体碳、植硅体中有机碳质量分数大致随土层深度增加先增大后减小,与中国东部森林[17]的研究结论一致;而中龄林大致随土层深度增加而减小,与东北地区[18]的研究结果一致。究其原因可能是中龄林坡度平缓、容重较大、黏粒含量及含水量较高,因此土壤胶粒等的吸附能力强,且土壤紧实,受淋溶作用影响较小,难以向土壤深层迁移。通常大孔隙越多,优先运移到土壤下层的水量越大[33],幼龄林和成熟林土壤砂粒含量较高、容重较小、孔隙大,有利于植硅体的迁移;幼龄林和成熟林坡度大,水动力条件充足,因而运移速度大,易于向土壤深层迁移。
PhytOC/TOC是衡量土壤植硅体碳稳定性的指标,随着土层深度的增加而增大,且植硅体碳的稳定性也随之增强[16]。本研究与北方阔叶林、针叶林[34]和亚热带森林[35]等土壤的研究均符合这一规律。由于有机碳在土壤中易于分解,且植硅体碳较稳定,有机碳分解速率快于植硅体碳的速率,因而PhytOC/TOC随土层深度的增加而增大。本研究不同土层中土壤有效硅、二氧化硅、植硅体、植硅体碳、植硅体中有机碳质量分数和PhytOC/TOC差异不显著,可能是受动物扰动、淋溶等外在因素导致其在剖面中运移而差异不显著,需进一步深入研究。
-
土壤各层二氧化硅与植硅体、植硅体碳质量分数极显著正相关,与大部分学者的研究结论一致,表明土壤中硅素与植硅体、植硅体碳质量分数密切相关。有学者通过向土壤中施加钢渣粉[36]、岩粉[37]等,提高土壤供应硅素的能力,以及提高植物根系对可溶性硅的吸收,进而增加植物组织中的硅量、植硅体与植硅体碳质量分数。土壤植硅体与植硅体碳质量分数极显著正相关,与张晓东[17]和杨杰[38]的研究结论一致;土壤植硅体与有效硅质量分数呈显著正相关,与中国东部森林玄武岩风化壳土壤的研究结论一致,但与花岗岩风化壳土壤[17]结论相反。本研究麻栎林土壤母岩属于第四纪下蜀组(Q3x)黄土状沉积物,硅的有效性及母岩对植硅体的形成影响显著。本研究认为:土壤植硅体碳与有机碳无显著关系,与杨杰[38]的研究结论不同。这可能是由于林分、林下植被以及土壤、地形等立地条件的不同所致。
-
相关研究表明:毛竹Phyllostachys edulis林[17]、散生竹林[38]、丛生竹林[39]和雷竹Phyllostachys violascens林[40]土层的植硅体碳储量分别为3.91、0.694~5.373、0.485~2.705和8.883 t·hm−2,板栗Castanea mollissima林、杉木Cunninghamia lanceolata林[17]土壤植硅体碳储量分别为2.67、1.18 t·hm−2,本研究麻栎林土壤植硅体碳储量为1.15~1.47 t·hm−2,可知竹类土壤的植硅体碳储量较高。通常植物种间元素含量差异最大的是硅元素,一般认为被子植物高于裸子植物,单子叶植物高于双子叶植物,而单子叶植物中的禾本科、莎草科Cyperaceae植物通常被认为是高富集硅的代表[41]。竹类为超富硅的禾本科植物,因此土壤植硅体碳储量较高。不同森林类型土壤植硅体碳储量受植被类型、林下植物、立地条件和生物量等的影响而具有一定差异,单子叶植物竹子的土壤植硅体碳储量比双子叶植物阔叶林高很多。
-
本研究中麻栎林幼龄林、中龄林与成熟林土壤理化性质及林下植被种类存在较大差异,表现出幼龄林与成熟林土壤的二氧化硅、植硅体、植硅体碳与植硅体中有机碳质量分数随土层深度的增加先增大后减小,有向土壤深层迁移的趋势;而中龄林则随土层深度的增加而减小,在土壤表层富集,表明不同的森林生态系统受多重因素的影响,土壤植硅体碳等在土壤剖面中的分布具有差异性。不同林龄麻栎林土壤植硅体碳储量为1.15~1.47 t·hm−2。这些结论可为中国北亚热带森林生态系统长期稳定的植硅体碳汇功能与植硅体碳循环研究提供参考,对于评价中国森林长期碳汇功能研究具有重要的指导意义。
Soil PhytOC sequestration in Quercus acutissima forest in northern subtropics
-
摘要:
目的 研究北亚热带麻栎Quercus acutissima林土壤植硅体碳(PhytOC)质量分数及剖面分布规律,探讨不同林龄麻栎林土壤植硅体碳储量的差异。 方法 以江苏省句容市不同林龄麻栎林土壤为研究对象,按照0~10、10~20、20~40、40~60 cm分层取土壤样品,测定植硅体和植硅体碳质量分数,并估算麻栎林土壤植硅体碳储量。 结果 土壤有效硅质量分数为45.7~153.3 mg·kg−1,随土层深度增加而增大,各分层之间有效硅质量分数差异不显著,不同林龄麻栎林土壤有效硅质量分数差异显著(P<0.05)。幼龄林和成熟林土壤植硅体、植硅体碳和植硅体中有机碳质量分数均随土层深度增加先增大后减小,而中龄林则随土层深度增加而减小;不同林龄之间土壤植硅体、植硅体碳、植硅体中有机碳质量分数差异显著(P<0.05),而各土层之间差异均不显著。土壤植硅体碳和总有机碳质量分数比值(PhytOC/TOC)为0.36%~1.49%,大致随土层深度的增加而增大;不同土层之间PhytOC/TOC差异不显著,但各林龄之间差异显著(P<0.05)。土壤植硅体与植硅体碳质量分数之间呈极显著正相关关系(P<0.01),植硅体碳与有效硅质量分数之间无相关性;麻栎林土壤植硅体碳储量为1.15~1.47 t·hm−2,幼龄林、中龄林、成熟林土壤的植硅体碳储量占有机碳储量的比例分别为0.80%~1.50%、0.73%~1.10%、0.36%~0.67%,占比较小。 结论 受土壤理化性质、淋溶作用等的影响,植硅体和植硅体碳质量分数在不同林龄麻栎林土壤剖面中的分布具有一定的差异性。植硅体碳储量占有机碳储量的比例较小,但随土层深度的增加而增大,表明植硅体碳较其他形式的碳更加稳定。从时间尺度上来讲,植硅体碳汇是森林长期碳汇的重要组成部分。图3表4参41 Abstract:Objective The purpose is to investigate the content and profile distribution of soil PhytOC in northern subtropical Quercus acutissima forest, and discuss the difference of PhytOC sequestration in Q. acutissima forest at different ages. Method Taking soil samples from Q. acutissima forest of different ages in Jurong City, Jiangsu Province as the research object, the soil samples were collected in layers of 0−10, 10−20, 20−40 and 40−60 cm to determine the content of phytolith, PhytOC, and the PhytOC sequestration in soil of Q. acutissima forest. Result The available silicon content of soil ranged from 45.74 to 153.32 mg·kg−1, which increased with the increase of soil depth. There was no significant difference in the content of soil available silicon among different layers, but there existed significant difference in soil available silicon content among different forest ages (P<0.05). The content of soil phytolith, PhytoOC and organic carbon in phytolith in young forest and mature forest increased first and then decreased with the increase of soil depth, whereas that in half-mature forest decreased with the increase of soil depth. The content of organic carbon in soil phytoliths, PhytoOC and phytoliths was significantly different among different forest ages (P<0.05), but difference was not significant among layers. In addition, the ratio of PhytOC/TOC ranged from 0.36% to 1.49%, which increased with the increase of soil depth. There was no significant difference in the ratio of phytoc/TOC among different soil layers, but there was significant difference among different forest ages (P<0.05). There was an extremely significant positive correlation between soil phytolith content and PhytOC content (P<0.01), but there was no correlation between PhytOC content and available silicon content. The PhytOC sequestrations in the soil of Q. acutissima forest ranged from 1.15 to 1.47 t·hm−2, and the proportions of PhytOC sequestrations to organic carbon storage in young forest, middle-aged forest and mature forest soil accounted for 0.80%−1.50%, 0.73%−1.10% and 0.36%−0.67%, respectively. Conclusion Affected by soil physical and chemical properties, and leaching, etc., the distribution of phytolith and PhytOC in soil profiles of Q. acutissima forest at different ages is different to some extent. The proportion of PhytOC sequestration to organic carbon storage was small, but it increased with the increase of soil depth, indicating that PhytOC is more stable than other forms of carbon. In terms of time scale, PhytOC sink is an important component of long-term carbon sinks in forests. [Ch, 3 fig. 4 tab. 41 ref.] -
Key words:
- forest ecology /
- Quercus acutissima forest /
- soil /
- phytolith /
- PhytOC /
- PhytOC sequestration
-
表 1 样地基本情况
Table 1. Basic characteristics of sampting plots studied
样地 林龄/
a坡度/
(°)坡位 林分密度/
(株·m−2)胸径/
cm树高/
m郁闭度/
%1 17 30 坡下 975 10.2 8.60 48 2 17 34 坡中 700 10.7 8.85 45 3 17 40 坡上 300 14.2 10.31 35 4 26 8 坡下 775 13.4 9.94 80 5 26 8 坡下 825 15.2 10.63 80 6 26 8 坡下 600 14.2 10.31 75 7 65 28 坡下 225 28.6 15.25 55 8 65 31 坡中 325 26.9 14.73 45 9 65 28 坡下 350 25.3 14.20 47 说明:幼龄林坡陡,土壤砾石含量为30%左右,多为禾本 科Gramineae草本植物;中龄林坡缓,土壤砾石含量 为20%左右,土壤紧实,灌草茂盛;成熟林坡陡, 土壤砾石含量为25%左右,草本植物多为络石 表 2 麻栎林土壤基本理化性质
Table 2. Basic physical and chemical properties of the soil in Q. acutissima forests
林龄 土壤深度/
cm土壤容重/
(g·cm−3)pH 有效磷/
(mg·kg−1)碱解氮/
(mg·kg−1)速效钾/
(mg·kg−1)有机碳/
(g·kg−1)砂粒/
(g·kg−1)粉粒/
(g·kg−1)黏粒/
(g·kg−1)幼龄林 0~10 1.23 4.88 4.78 99.7 149.8 24.37 826 164 10 10~20 1.28 4.72 4.10 72.3 148.2 18.53 572 402 26 20~40 1.30 4.60 2.91 42.0 133.6 14.59 607 353 44 40~60 1.37 4.56 2.33 32.3 113.4 13.61 614 339 57 中龄林 0~10 1.39 4.72 7.58 115.7 218.4 33.54 356 591 54 10~20 1.47 4.67 3.42 70.0 195.3 29.22 258 654 89 20~40 1.51 4.60 1.91 50.3 182.1 22.17 126 765 109 40~60 1.57 4.58 1.65 38.0 162.0 18.08 110 779 121 成熟林 0~10 1.37 4.55 7.51 229.0 226.7 38.77 460 475 66 10~20 1.40 4.51 5.74 135.3 189.4 31.27 370 545 85 20~40 1.46 4.49 3.39 100.3 186.0 26.94 398 467 135 40~60 1.56 4.48 2.33 83.7 165.8 20.58 410 447 155 说明:粒级划分采用国际制土壤粒级划分标准:砂粒(0.020~2.000 mm);粉粒(0.002~0.020 mm);黏粒(<0.002 mm) 表 3 麻栎林土壤植硅体碳储量与有机碳储量
Table 3. PhytOC and organic carbon storages in different soil depths of Q. acutissima forests
林龄 土壤深度/
cm有机碳/
(g·kg−1)植硅体碳/
(g·kg−1)有机碳储量/
(t·hm−2)植硅体碳储量/
(t·hm−2)Phytoc/TOC/% 幼龄林 0~10 24.37 0.198 26.29 0.21 0.80 10~20 18.53 0.223 17.60 0.21 1.19 20~40 14.59 0.214 23.42 0.34 1.45 40~60 13.60 0.203 26.71 0.40 1.50 总计 94.02 1.16 中龄林 0~10 33.54 0.278 37.30 0.31 0.83 10~20 29.22 0.215 34.20 0.25 0.73 20~40 22.17 0.188 50.07 0.43 0.86 40~60 18.08 0.198 43.71 0.48 1.10 总计 165.28 1.47 成熟林 0~10 38.77 0.139 47.78 0.17 0.36 10~20 31.26 0.208 34.53 0.23 0.67 20~40 26.94 0.154 65.18 0.37 0.57 40~60 20.58 0.123 62.95 0.38 0.60 总计 210.44 1.15 表 4 麻栎林土壤层5个变量之间的相关性
Table 4. Correlation coefficients between the five variables of Q. acutissima forest soil
变量 二氧化硅 植硅体 植硅体碳 有效硅 有机碳 二氧化硅 1 植硅体 0.534** 1 植硅体碳 0.606** 0.441** 1 有效硅 -0.126 0.372* -0.178 1 有机碳 -0.021 1 说明:*表示P<0.05;**表示P<0.01 -
[1] LAL R. Soil carbon sequestration impacts on global climatic change and food security [J]. Science, 2004, 304(5677): 1623 − 1627. [2] 张梦旭, 刘蔚, 朱猛, 等. 甘肃河西山地土壤有机碳储量及分布特征[J]. 中国沙漠, 2019, 39(4): 64 − 72. ZHANG Mengxu, LIU Wei, ZHU Meng, et al. Soil organic carbon storage and distribution patterns in the mountainous areas of the Hexi Region, Gansu, China [J]. J Desert Res, 2019, 39(4): 64 − 72. [3] 陈仕奇, 吕盛, 高明, 等. 缙云山不同林分下土壤有机碳及矿化特征[J]. 环境科学, 2019, 40(2): 953 − 960. CHEN Shiqi, LÜ Sheng, GAO Ming, et al. Characteristics of soil organic carbon and mineralization with different stands in Jinyun Mountain [J]. Environ Sci, 2019, 40(2): 953 − 960. [4] CHRISTENSEN B T. Matching measurable soil organic matter fractions with conceptual pools in simulation models of carbon turnover: revision of model structure [J]. Eval Soil Org Matter Models, 1996, 38: 143 − 159. [5] 何珊琼, 孟赐福, 黄张婷, 等. 土壤植硅体碳稳定性的研究进展与展望[J]. 浙江农林大学学报, 2016, 33(3): 506 − 515. HE Shanqiong, MENG Cifu, HUANG Zhangting, et al. Research progress and forecast of phytolith-occluded organic carbon stability in soil [J]. J Zhejiang A&F Univ, 2016, 33(3): 506 − 515. [6] 王永吉, 吕厚远. 植物硅酸体的研究及应用简介[J]. 黄渤海海洋, 1989, 7(2): 66 − 68. WANG Yongji, LÜ Houyuan. An introduction of study on plant opal and its uses [J]. J Oceanogr Huanghai Bohai Seas, 1989, 7(2): 66 − 68. [7] HARRISON C C. Evidence for intramineral macromolecules containing protein from plant silicas [J]. Phytochemistry, 1996, 41(1): 37 − 42. [8] EXLEY C. Silicon in life: a bioinorganic solution to biooeganic essentiality [J]. J Inorg Biochem, 1998, 69(3): 139 − 144. [9] CARTER J A. Atmospheric carbon isotope signatures in phytolith-occulated carbon [J]. Quaternary Int, 2009, 193(1/2): 20 − 29. [10] PARR J F. A comparison of heavy liquid floatation and microwave digestion techniques for the extraction of fossil phytoliths from sediments [J]. Rev Palaeobot Palynol, 2002, 120(3/4): 315 − 336. [11] FISHIKIS O, INGWERSEN J, STRECK T. Phytolith transport in sandy sediment: experiments and modeling [J]. Geoderma, 2009, 151(3/4): 168 − 178. [12] 刘利丹, 介冬梅, 刘洪妍, 等. 中国东北自然土壤剖面中植硅体的垂直分布规律[J]. 微体古生物学报, 2019, 36(3): 298 − 308. LIU Lidan, JIE Dongmei, LIU Hongyan, et al. Vertical transport of phytolith in the nature soil profiles, Northen China [J]. Acta Micropalaeontol Sin, 2019, 36(3): 298 − 308. [13] ZHANG Xiaodong, SONG Zhaoliang, KIM M G, et al. The impact of different forest types on phytolith-occluded carbon accumulation in subtropical forest soils [J]. J Soil Sediment, 2016, 16(2): 461 − 466. [14] HUANG Zhangting, LI Yongfu, JIANG Peikun, et al. Long-term intensive management increased carbon occluded in phytolith (PhytOC) in bamboo forest soils [J]. Sci Rep, 2014, 4(1): 3602. [15] 罗东海, 王子芳, 陆畅, 等. 缙云山不同土地利用方式下土壤植硅体碳的含量特征[J]. 环境科学, 2019, 40(9): 4270 − 4277. LUO Donghai, WANG Zifang, LU Chang, et al. Content of soil phytolith-occluded organic carbon in different land use patterns at Jinyun Mountain [J]. Environ Sci, 2019, 40(9): 4270 − 4277. [16] PARR J F, SULLIVAN L A. Soil carbon sequestration in phytoliths [J]. Soil Biol Biochem, 2005, 37(1): 117 − 124. [17] 张晓东. 中国东部森林土壤中植硅体积累和硅形态分布研究[D]. 杭州: 浙江农林大学, 2016. ZHANG Xiaodong. Research on Phytolith Accumulation and Noncrystalline Silicon Distribution of Forest Soils in East China[D]. Hangzhou: Zhejiang A&F University, 2016. [18] 杜方旎, 介冬梅, 刘利丹, 等. 东北地区暗棕壤植硅体垂直迁移特征研究[J]. 土壤通报, 2018, 49(2): 268 − 274. DU Fangni, JIE Dongmei, LIU Lidan, et al. The vertical transportation of phytoliths in dark brown forest soils in northeastern China [J]. Chin J Soil Sci, 2018, 49(2): 268 − 274. [19] 于政公. 基于林龄的寒温带森林土壤植硅体及其封存效应[D]. 呼和浩特: 内蒙古大学, 2019. YU Zhenggong. Forest Soil Phytolith and Its Storages Effcet in Cold Temperate Zone Based on Forest Age[D]. Hohhot: Inner Mongolia University, 2019. [20] CLARKE J. The occurrence and significance of biogenic opal in the regolith [J]. Earth Sci Rev, 2003, 60(3): 175 − 194. [21] BORRELLI N, OSTERRIETH M, ROMANELLI A, et al. Biogenicsilica in wetlands and their relationship with soil and groundwater biogeochemistry in the southeastern of Buenos Aires Province, Argentina [J]. Environ Earth Sci, 2012, 65(2): 469 − 480. [22] 李自民, 宋照亮, 姜培坤. 稻田生态系统中植硅体的产生与积累: 以嘉兴稻田为例[J]. 生态学报, 2013, 33(22): 7197 − 7203. LI Ziming, SONG Zhaoliang, JIANG Peikun. The production and accumulation of phytoliths in rice ecosystems: a case study to Jiaxing Paddy Field [J]. Acta Ecol Sin, 2013, 33(22): 7197 − 7203. [23] LI Zimin, SONG Zhaoliang, LI Beilei. The production and accumulation of phytolith-occluded carbon in Baiyangdian reed wetland of China [J]. Appl Geochem, 2013, 37: 117 − 124. [24] 汝宁. 温带灌丛和沙化草地生态系统硅分布与植硅体碳汇研究[D]. 杭州: 浙江农林大学, 2015. RU Ning. Research on Silicon Distribution and Phytolith Carbon Sequestration in Temperate Shrubland and Desertification of Grassland[D]. Hangzhou: Zhejiang A&F University, 2015. [25] 赵玉营. 草地生态系统植硅体碳汇及其控制机制[D]. 杭州: 浙江农林大学, 2016. ZHAO Yuying. Research on Silicon Distribution and Phytolith Carbon Sequestration of Grassland Ecosystem[D]. Hangzhou: Zhejiang A&F University, 2016. [26] 郭颖. 内蒙古典型草原优势植物植硅体碳积累与环境关系的研究[D]. 呼和浩特: 内蒙古大学, 2019. GUO Ying. Study on the Relationship between the Phytolith-occulded Carbon Accummulation in Dominant Plants and Environmental Factors in the Typical Steppe of Inner Mongolia[D]. Hohhot: Inner Mongolia University, 2019. [27] 张兴旺, 李垚, 方炎明. 麻栎在中国的地理分布及潜在分布区预测[J]. 西北植物学报, 2014, 34(8): 1685 − 1692. ZHANG Xingwang, LI Yao, FANG Yanming. Geographical distribution and prediction of potential ranges of Quercus acutissima in China [J]. Acta Bot Boreali-Occident Sin, 2014, 34(8): 1685 − 1692. [28] WALKLEY A, BLACK I A. An examination of the degtjareff method for determining soil organic matter, and a proposed modification of the chromic acid titration method [J]. Soil Sci, 1934, 37(1): 29 − 38. [29] 杨杰, 李永夫, 黄张婷, 等. 碱溶分光光度法测定植硅体碳含量[J]. 分析化学, 2014, 42(9): 1389 − 1390. YANG Jie, LI Yongfu, HUANG Zhangting, et al. Determination of phytolith-occluded carbon content using alkali dissolution-spectrophotometry [J]. Chin J Anal Chem, 2014, 42(9): 1389 − 1390. [30] 高卓, 介冬梅, 刘利丹, 等. 东北地区土壤有效硅的时空分异及其对芦苇植硅体形成的影响[J]. 第四纪研究, 2015, 35(4): 967 − 976. GAO Zhuo, JIE Dongmei, LIU Lidan, et al. Temporal and spatial variation of available soil silicon and its influence on the formation of phytoliths in Phramites communis in Northeast China [J]. Quaternary Sci, 2015, 35(4): 967 − 976. [31] FISHKIS O, INGWERSEN J, LAMERS M, et al. Phytolith transport in soil: a field study using fluorescent labeling [J]. Geoderma, 2010, 157(1/2): 27 − 36. [32] PIPERNO D R. Phytoliths: a comprehensive guide for archaeologists and paleoecologists [J]. Rowman Altamira, 2006, 60(4): 391. [33] 张小娜, 冯杰. 大孔隙分布对坡地产汇流及溶质运移的影响[J]. 水土保持通报, 2014, 34(6): 22 − 26. ZHANG Xiaona, FENG Jie. Effect of soil macropores distribution on slope runoff yield and solute transport [J]. Bull Soil Water Conserv, 2014, 34(6): 22 − 26. [34] YANG Xiaomin, SONG Zhaoliang, LIU Hongyan, et al. Phytolith accumulation in broadleaf and conifer forests of northern China: implications for phytolith carbon sequestration [J]. Geoderma, 2018, 312: 36 − 44. [35] 林维雷, 应雨骐, 姜培坤, 等. 浙江南部亚热带森林土壤植硅体碳的研究[J]. 土壤学报, 2015, 52(6): 1365 − 1373. LIN Weilei, YING Yuqi, JIANG Peikun, et al. Study on phytolith-occluded organic carbon on soil of subtropical forest of southern Zhejiang [J]. Acta Pedol Sin, 2015, 52(6): 1365 − 1373. [36] 范呈根, 胡丹丹, 吴建富, 等. 施用钢渣粉对水稻生长与产量及重金属含量的影响[J]. 湖南农业大学学报(自然科学版), 2017, 43(2): 125 − 128. FAN Chenggen, HU Dandan, WU Jianfu, et al. Effects of steel slag powder application on rice growth and yield and heavy metals content [J]. J Hunan Agric Univ Nat Sci, 2017, 43(2): 125 − 128. [37] GUO Fengshan, SONG Zhaoliang, SULLIVAN L, et al. Enhancing phytolith carbon sequestration in rice ecosystems through basalt powder amendment [J]. Sci Bull, 2015, 60(6): 1 − 7. [38] 杨杰. 重要散生竹生态系统植硅体碳汇研究[D]. 杭州: 浙江农林大学, 2016. YANG Jie. Phytolith-occluded Carbon Sequestration of Typical Monopodial Bamboo Ecosystems in China[D]. Hangzhou: Zhejiang A&F University, 2016. [39] 项婷婷. 中国重要丛生竹生态系统植硅体碳汇研究[D]. 杭州: 浙江农林大学, 2015. XIANG Tingting. Research of Phytolith-occluded Carbon Sequestration of Important Sympodial Bamboo Ecosystem in China[D]. Hangzhou: Zhejiang A&F University, 2015. [40] 黄张婷. 雷竹生态系统植硅体封存有机碳汇研究[D]. 杭州: 浙江农林大学, 2014. HUNAG Zhangting. Potential of Phytolith-occluded Carbon Sequestration of Phyllostachys praecox Ecosystem[D]. Hangzhou: Zhejiang A&F University, 2014. [41] TRÉGUER P, LEYNAERT A, QUÉGUINER, et al. The silica balance in the world ocean: a reestimate [J]. Science, 1995, 268(5209): 375 − 379. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20200283







 下载:
下载:






