-
长喙毛茛泽泻Ranalisma rostratum 是泽泻科Alismataceae毛茛泽泻属Ranalisma多年生莲座状沼生小草本植物,产于中国的浙江、江西、湖南省以及越南和马来西亚[1]。1930年,在浙江省丽水市南明山首次采到长喙毛茛泽泻标本[2],之后几十年不曾采到,一度被认为灭绝。直到20世纪90年代,研究人员才相继在江西省东乡县和湖南省茶陵县陆续发现野生长喙毛茛泽泻种群[3]。由于人类对其生境的破坏和本身生存、竞争能力较差,湖南茶陵和江西东乡野外长喙毛茛泽泻种群已消失[2]。1999年,国家林业局和农业部正式发布了中华人民共和国《国家重点保护野生植物名录(第1批)》,长喙毛茛泽泻被列为极度濒危的植物,为国家Ⅰ级保护野生植物[4]。2008年,浙江省人文园林有限公司天景水生植物园从杭州植物园交换引入了长喙毛茛泽泻,并进行了大规模的迁地扩繁[5-6]。2015年,浙江省丽水市莲都区林业技术推广站从天景水生植物园引进长喙毛茛泽泻5000株,开始回归原生地试验。目前,在丽水市莲都区布局了3个回归示范点,2019年8月,每个示范点繁育长喙毛茛泽泻小苗不少于5000株,已初步具备了开发利用的物质基础。目前,国内学者围绕长喙毛茛泽泻繁育特性与遗传多样性[7-8]、有性生殖系统[9-13]、生物学特性与生活史[2,14]、种群生态与环境适应性[15-19]等方面开展研究,目的是揭示其濒危机制,为制定保护策略提供依据。但关于长喙毛茛泽泻植株营养成分和毒性试验的研究尚无报道。本研究测定了采自丽水3个示范点的长喙毛茛泽泻植株茎叶和根的主要营养成分,并对茎叶的急性经口毒性进行初步研究,以期为长喙毛茛泽泻的进一步保护利用提供理论依据。
-
本研究所用的长喙毛茛泽泻植株分别来自丽水南明山、莲都区大港头镇和莲都区老竹镇。南明山样地处于丽水市南明山风景名胜区,长喙毛茛泽泻被栽植在一片沼泽地中,沼泽地处于森林边缘,森林整体郁闭度为0.5~0.7;沼泽周围有毛竹Phyllostachys edulis、枫香Liquidambar formosana等乔灌树种;沼泽地水位维持在2~10 cm,伴生植物有蕺菜(鱼腥草)Houttuynia cordata、蕨Pteridium aquilinum var. latiusculum、苎麻Boehmeria nivea、野芋Colocasia antiquorum 等。大港头样地位于丽水市莲都区大港头镇,长喙毛茛泽泻被栽植在水田,伴生植物有丁香蓼Ludwigia prostrata、喜旱莲子草Alternanthera philoxeroides等;水田呈梯田状,有高低落差,水位常年维持在5~15 cm,且有进水出水口,水流较缓;样地周边无乔灌木遮阴。老竹乡样地位于丽水市莲都区老竹乡,长喙毛茛泽泻被栽植在水田里,伴生植物有刺芋(野茨菇)Lasia spinosa、莲Nelumbo nucifera和喜旱莲子草等;水田坡度较为平缓,周围缺乏乔灌木遮阴;8月莲叶已展开,此时郁闭度接近0.9;水田水位及出水情况与大港头样地基本一致。
-
2019年8月26日,每个试验地采集1份样品,每份样品鲜质量为300~1000 g。沥干样品表面水分,用精度为0.01 g的天平称量植株鲜质量,之后摊放在竹篾上曝晒,待连续3 d样品质量下降不超过1%时,认为样品已风干。2020年6月15日,再次采集南明山示范点样品1份,进行相同处理。
-
剪掉风干后的长喙毛茛泽泻样品根系,将茎叶与根系分离,用精度为0.01 g的天平称量茎叶质量和根系质量,计算干鲜比和茎叶与根系生物量比,然后进一步检测风干样品茎叶和根的脂肪、氮、磷、钾和其他金属离子质量分数。每份样品每个指标重复测定3次。
将经营养元素测定后剩余样品的干燥茎叶用于小鼠急性经口毒性试验。称取干燥的茎叶35.00 g,用小型干磨研磨机在常温下(25 ℃)粉碎30 s,待无明显茎叶残渣时停止粉碎,刮取茎叶粉末,过 20目筛,去除未充分粉碎的颗粒,得到绿色均匀粉末状样品。称取上述粉末样品10 g,以质量分数1%羧甲基纤维素钠为溶媒溶解配制成80 mL悬浮样液。每个样品共配制这样的悬浮样液3瓶,每瓶80 mL,4 ℃冰箱冷藏备用。
小鼠急性经口毒性试验委托浙江省医学科学院完成。实验用小鼠Mus musculus由浙江省实验动物中心提供,SPF级,实验动物生产许可证号为SCXK(浙)2019-0002,实验动物使用许可证号为SYXK (浙)2019-0011,实验动物饲料由浙江省实验动物中心提供。实验所用小型干磨研磨机型号为TY-150A,由永康市敬业工贸有限公司生产。实验用天平型号为BS2202S,量程2.0 kg,由赛多利斯(北京)科学仪器有限公司生产。检测环境条件:温度为20~25 ℃,相对湿度为40%~70%。
-
长喙毛茛泽泻样品植株中脂肪、全氮、全磷和6种金属元素质量分数的测定委托浙江方圆检测集团股份有限公司检测,其中脂肪质量分数依据GB 5009.6−2016《食品安全国家标准:食品中脂肪的测定》测定;茎叶和根中全氮质量分数的测定参照HJ 717−2014《土壤质量 全氮的测定 凯氏法》测定,全磷质量分数的测定参照NYT 88−1988《土壤全磷测定法》测定;钾、钙、镁、铁、锰和锌质量分数依据GB 5009.268−2016《食品安全国家标准:食品中多元素的测定》测定。
-
①实验动物:选用健康、成熟,体质量18~22 g(美国癌症研究所分送)小鼠20只,雌雄小鼠各10只。②剂量和给药方法:按限量法设7.5 g·kg−1(体质量)1个剂量组。灌胃前小鼠禁食(禁水)6 h后,用悬浮样液按20 mL·kg−1 灌胃容量对小鼠进行灌胃,共计3次,每次间隔4 h,末次灌胃2 h后小鼠自由进食、饮水。③观察指标:灌胃后,观察小鼠的一般状况、中毒表现和死亡情况,观察期限为14 d,记录小鼠实验期初及期末体质量。
-
由表1可知:长喙毛茛泽泻的干鲜比为0.17~0.19,整个植株,特别是茎叶部分的含水率较高。长喙毛茛泽泻茎叶与根的生物量之比为1.8~2.5,不同取样时间和取样地,茎叶与根的生物量之比相差很大,其中南明山2号样品和大港头镇样品的茎叶与根的生物量之比高于其余2个样地,特别是南明山2号样品。对表1的结果分析发现:未结实的长喙毛茛泽泻植株,其茎叶与根的生物量之比相较已结实的植株要高,茎叶生物量占整个植株的比例大。主要原因在于不同采样时期植株的成熟度和植株长势不一样,南明山2号采集时间为2020年6月中旬,长喙毛茛泽泻还未开花,此时植株生长比较旺盛;而大港头镇、南明山1号和老竹乡样品的采集时间为2019年8月,此时3个样品均已结实,植株长势开始衰败。
表 1 长喙毛茛泽泻3个样地4份样品的干鲜比和生物量
Table 1. Dry-fresh ratio and biomass of 4 batches of R. rostratum from 3 samples places
样品 结实与否 干鲜比 生物量 干质量/g 鲜质量/g 干鲜比 茎叶质量/g 根质量/g 茎叶/根 南明山1号 已结实 144.57 750 0.19 93.33 51.24 1.82 南明山2号 未结实 61.25 370 0.17 43.70 17.55 2.49 大港头镇 已结实 86.56 500 0.17 58.54 28.02 2.09 老竹乡 已结实 165.53 1000 0.17 107.96 57.57 1.88 说明:生物量栏中,茎叶质量和根质量都是指样品的干质量 -
由表2可知:长喙毛茛泽泻植株中脂肪、氮和钾质量分数均为25.00 mg·g−1左右,脂肪质量分数的最大最小值之比小于5,且变异系数为39.86%,说明脂肪在不同样品和植株器官间变异不大。营养元素平均质量分数大于10.00 mg·g−1的有氮和钾,平均质量分数为5.00~10.00 mg·g−1的有铁和钙,平均质量分为1.00~5.00 mg·g−1的有磷和镁,平均质量分数小于1.00 mg·g−1的有锰和锌。锌与大量元素氮和钾的平均质量分数相差了近3个数量级。各营养元素质量分数均值从高到低依次为氮、钾、铁、钙、磷、镁、锰、锌。
表 2 脂肪和各营养元素质量分数范围、均值和变异系数
Table 2. Range, mean values and coefficient variation of fat and nutrient elements
项目 脂肪及各养元素质量分数/(mg·g−1) 变异系数/% 最小值 最大值 最大/最小 平均值 标准差 脂肪 9.00 36.00 4.00 23.13 9.22 39.86 氮 22.40 34.20 1.53 26.50 4.53 17.09 钾 15.90 39.10 2.50 25.08 9.14 36.44 磷 0.50 8.50 17.00 3.87 3.28 84.70 铁 0.17 33.00 194.12 6.49 11.12 171.43 钙 3.30 9.71 2.94 6.21 2.33 37.58 镁 0.00 2.70 900.00 1.07 1.20 111.33 锰 0.38 1.52 4.00 0.68 0.38 56.70 锌 0.03 0.09 2.94 0.06 0.02 36.21 与世界陆生维管植物元素平均质量分数范围相比较[20],丽水3个回归示范点4份长喙毛茛泽泻样品的氮、磷、钾、钙、镁这5种大量必需营养元素质量分数均在正常范围内(表2)。但与陆生高等植物所需元素的适合平均质量分数值相比较[21],该5种元素的质量分数,除镁外,氮、磷、钾和钙均高于已报道的陆生高等植物所需元素的相应组织,这可能与长喙毛茛泽泻为水生草本植物有关。从变异系数来看,8种营养元素从大到小依次为铁、镁、磷、锰、钙、钾、锌、氮,铁质量分数在各样品和组织间变异系数最大,其次是镁和磷,说明铁、镁和磷在各样地和植株器官间质量分数不稳定,受样地环境影响较大。氮质量分数在各样品和植株器官间变异系数最小,说明氮在植株体内相对稳定。从元素质量分数的最大值与最小值之比(以下简称最大最小比)来看,镁的最大,其次是铁,再次是磷,其他元素均小于5.00,最大最小比从大到小的顺序与变异系数的顺序基本一致,进一步说明长喙毛茛泽泻中的镁、铁和磷质量分数不够稳定,而其他元素均较稳定。
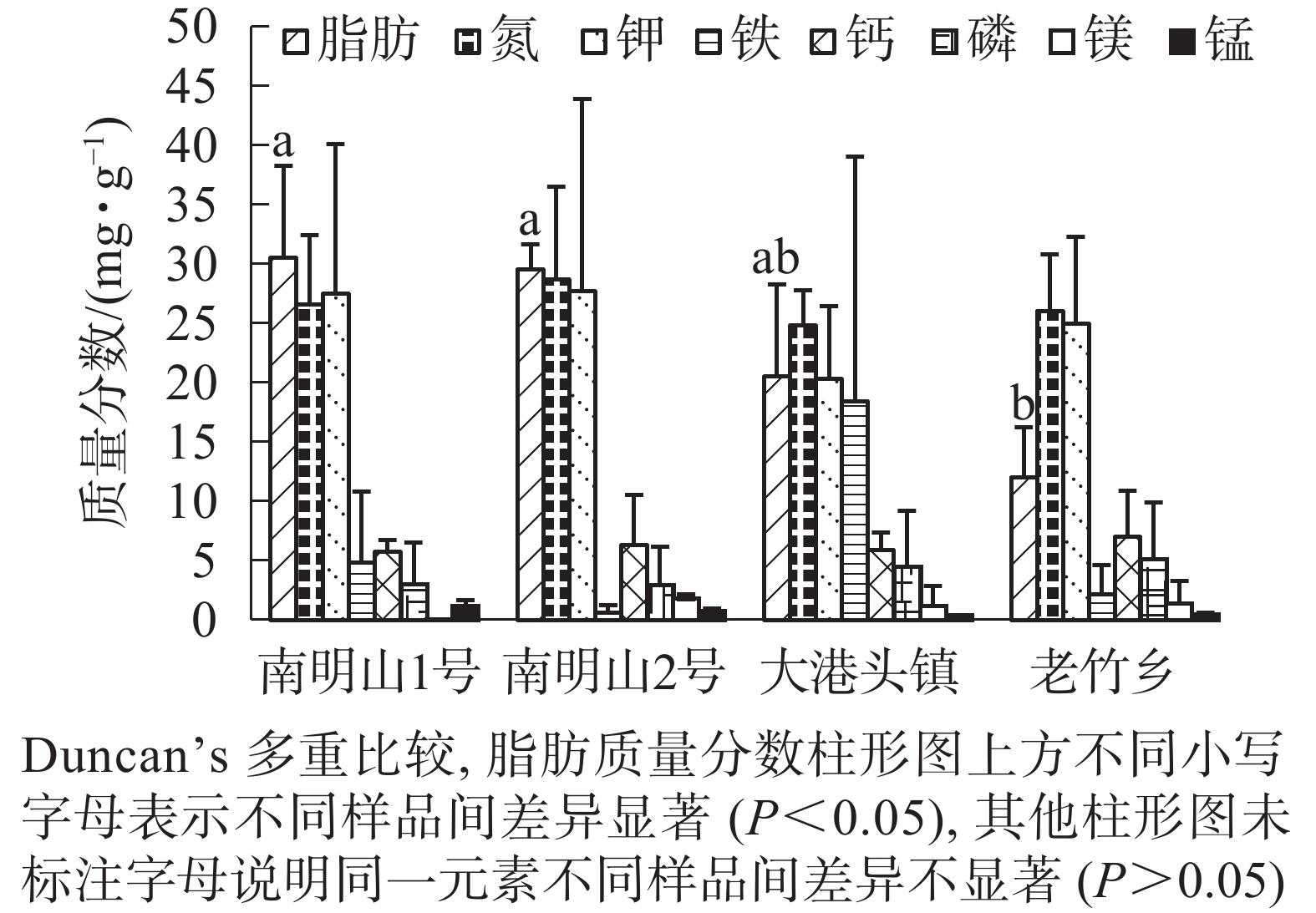
由图1可知:南明山1号样品的脂肪质量分数最高,老竹乡样品中的脂肪质量分数最低,脂肪质量分数在4个样品之间存在显著差异(P<0.05)。7种营养元素在样品内和各样品间的变异系数很大。铁质量分数在大港头镇样品中最高,而在南明山2号样品中的最低,两者均值相差30倍左右,但铁质量分数在4个样品中却无显著差异;镁质量分数均值在南明山1号样品中低于检测限(<0.003 mg·g−1),而在其他各样品中平均质量分数均在1.00 mg·g−1以上;由于锌质量分数极低,锌元素质量分数不纳入样品和器官的比较分析。除了未做分析的锌,7种营养元素在4个样品间均无显著差异。
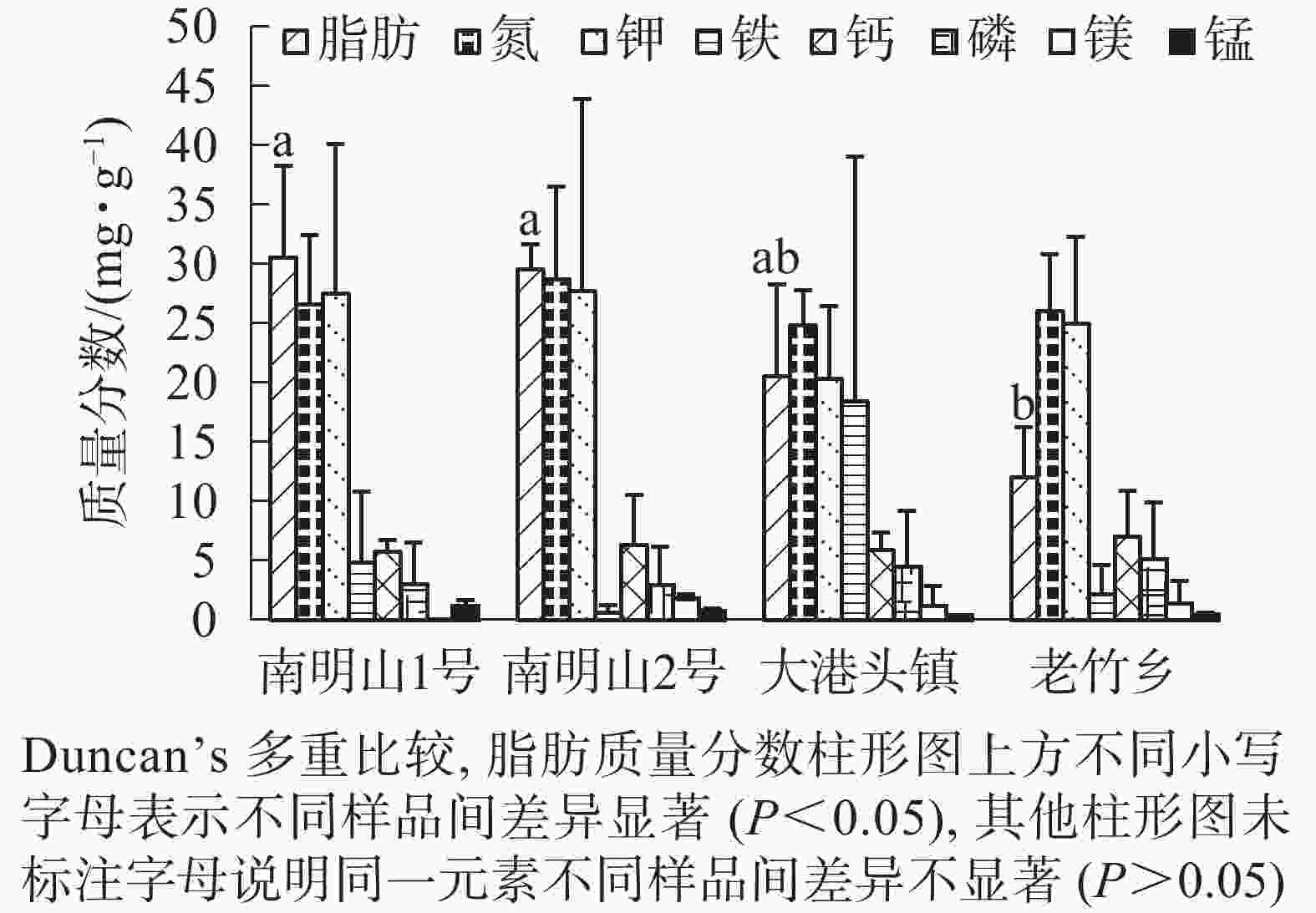
图 1 4个样品茎叶和根的脂肪及营养元素平均质量分数
Figure 1. Average contents of fatty acid and nutrient elements in the stems,leaf and root of the four samples
由表3可见:脂肪质量分数在长喙毛茛泽泻的茎叶和根之间无显著差异,氮、磷、钾和钙在茎叶和根间存在显著差异(P<0.05),说明长喙毛茛泽泻根系对这些元素具有选择吸附性;铁元素在茎叶和根的平均质量分数(分别为1.22和11.75 mg·g−1)虽相差了1个数量级,但茎叶和根间却并无显著差异,原因在于铁质量分数在个别样品(大港镇)的根系中极高,在不同样品的不同组织之间变异极大(变异系数为123.67),导致了方差匀齐度很低。这也说明长喙毛茛泽泻根系对土壤中的铁离子有富集作用。根系中的锰和镁元素在质量分数高于茎叶中的,但在茎叶和根之间差异不显著(P>0.05),表明这2种元素在茎叶和根之间没有明显的分布倾向性。
表 3 长喙毛茛泽泻茎叶与根系的脂肪和营养元素均值及显著性分析
Table 3. Mean value and significance analysis of fat and nutrient elements in stem, leaf and root
测定
指标测定
部位平均值/
(mg·g−1)自由度 组间均
方差F P 脂肪 茎叶 27.00±8.98 1 120.125 1.518 0.264 根 19.25±8.81 氮 茎叶 30.30±3.04 1 115.520 24.754 0.003 根 22.70±0.29 钾 茎叶 32.55±6.50 1 447.005 19.516 0.004 根 17.60±1.87 磷 茎叶 1.00±0.56 1 66.298 43.928 0.001 根 6.75±1.64 铁 茎叶 1.22±1.72 1 221.825 2.067 0.201 根 11.75±14.55 钙 茎叶 8.08±1.67 1 27.975 16.485 0.007 根 4.34±0.78 镁 茎叶 0.37±0.73 1 3.996 3.989 0.093 根 1.78±1.21 锰 茎叶 0.52±0.16 1 0.200 1.447 0.274 根 0.83±0.50 -
由表4可见:脂肪和营养元素质量分数之间的相关系数在较大范围内波动,说明不同元素之间的相互关系较为复杂。分析脂肪和8种营养元素的36 对因子的相关关系可知:7对因子间存在显著相关性,如钾与氮,磷与氮、钾,钙与氮、钾、磷,镁与磷,占总对数的19.44%。其中,氮与钾、钙呈极显著正相关(P<0.01),与磷呈极显著负相关;钾与磷呈极显著负相关(P<0.01),与钙呈显著正相关(P<0.05);磷与钙呈显著负相关(P<0.05),与镁呈显著正相关(P<0.05)。这些结果说明:长喙毛茛泽泻的氮、钾、钙之间存在协同作用,与磷存在拮抗作用;镁与磷存在协同作用。
表 4 长喙毛茛泽泻植株脂肪和8种营养元素间相互关系
Table 4. Correlation between plant fat and 8 nutrient elements
元素 脂肪 氮 钾 磷 铁 钙 镁 锰 锌 脂肪 1 氮 0.527 1 钾 0.522 0.975** 1 磷 −0.695 −0.876** −0.844** 1 铁 −0.399 −0.497 −0.540 0.589 1 钙 0.158 0.850** 0.802* −0.762* −0.343 1 镁 −0.463 −0.402 −0.440 0.717* 0.377 −0.520 1 锰 0.331 −0.348 −0.268 0.168 −0.104 −0.398 −0.243 1 锌 0.065 0.086 −0.107 0.044 0.222 0.024 0.515 −0.264 1 说明:*表示显著相关(双尾t检验,P<0.05); **表示极显著相关(双尾t检验,P<0.01) -
如表5所示:实验期间,小鼠均未出现中毒表现,无死亡。长喙毛茛泽泻叶片对雌雄小鼠经口半致死量(LD50)均大于7.5 g·kg−1(体质量),按急性毒性分级标准判定,属实际无毒级。
表 5 长喙毛茛泽泻茎叶的小鼠急性经口毒性试验结果
Table 5. Acute oral toxicity test in mice of leaf of R. rostratum
性别 小鼠始
质量/g小鼠终
质量/g死亡情况
(死亡数/组鼠数)LD50/
(g·kg−1)雌性 19.9±0.9 28.2±1.7 0/10 >7.5 雄性 19.6±0.6 31.5±1.4 0/10 >7.5 -
长喙毛茛泽泻为水生小草本植物,其叶片为纸质。根据干鲜比结果推测植株自由水含水率在81%以上,显示植株含水率较高。长喙毛茛泽泻植株中脂肪平均质量分数略高于23.13 mg·g−1,且在不同样品间和植株器官间变异不大,进一步的方差分析显示脂肪质量分数在茎叶和根之间差异不显著,但在不同样品间存在显著差异。
长喙毛茛泽泻植株的8种营养元素质量分数显示:5种大量营养元素质量分数均值从高到低依次为氮、钾、钙、磷、镁。从变异系数和各营养元素质量分数的最大值与最小值之比来看,长喙毛茛泽泻中的镁、铁和磷在不同样地和植株器官间不稳定,受样地环境影响较大,而其他元素均较稳定。进一步的方差分析显示:除锌外,其余7种营养元素质量分数在4个样品间均无显著差异,但氮、磷、钾和钙在茎叶和根间差异显著,说明长喙毛茛泽泻根系对这4种元素具有选择吸附性。对长喙毛茛泽泻不同样品和组织中营养元素质量分数的相关分析显示:氮、钾、钙这3种元素两两之间存在显著或极显著正相关,而与磷存在显著或极显著负相关,磷与镁存在显著正相关。
长喙毛茛泽泻茎叶的小鼠经口急性毒性试验表明:雌雄小鼠半致死质量分数均大于7.5 g·kg−1,试验期间各组小鼠均未出现死亡情况。按急性毒性分级标准判定,该样品属实际无毒级。
植物元素特征除与植物本身的遗传学特性有关外,主要受土壤和气候等生境条件的影响,也是植物对所在生境长期适应的结果[22]。罗绪强等[23]对雷公山自然保护区5种常见木本植物叶片的6种大量必需营养元素进行了测定分析。结果表明:6种元素质量分数从高到低依次为氮、钙、钾、硫、镁、磷;惠岑怿等[24]的研究显示:4种旱生针茅属Stipa植物叶片中7种大量元素质量分数均值从高到低依次为碳、氮、钾、硫、镁、磷、钙。这些大量元素质量分数的排序结果与本研究结果有所不同,可能的原因是本研究的研究对象为水生草本植物,而上述2篇文献的研究对象分别为陆生木本植物和旱生草本植物。
对陆地生态系统的高等植物而言,当氮磷比>16时,说明植物生长受到磷的限制,当氮磷比<14时,植物生长受到氮的限制,而当氮磷比为14~16时,氮与磷单独或共同影响植物的生长[25]。长喙毛茛泽泻的氮磷比在4个样品和不同器官间均小于14,说明其生长受到氮的限制。此外,罗绪强等[23]的文献结果显示:氮和磷、氮和钾、磷和钙、钾和钙质量分数之间均具有显著或极显著正相关关系。惠岑怿等[24]的研究结果显示:非金属元素碳、氮、硫、磷 等与金属元素钾之间显著正相关,与其他金属元素显著负相关。本研究结果表明:氮和钾、钾和钙质量分数间存在极显著和显著正相关,但磷与金属元素钾、钙、镁质量分数的相关性与其他文献的结果有明显的不同,说明不同植物体内这些元素之间具有不同的比例组成和协调关系。
石从广等[26]对越南安息香Styrax tonkinesis精炼的种子油开展了大小鼠急性经口毒性试验以及慢性毒性3项试验。结果发现:精炼油对应的小鼠半致死质量分数分别为雌性小鼠17.10 g·kg−1,雄性小鼠10.80 g·kg−1,达到理论无毒的标准;王亚萍等[27]对长兴吊瓜Trichosanthes bracteata籽油的食用安全性进行了评估。结果显示:小鼠经口急性毒性试验的半致死量高达40.00 mL·kg−1以上,表明吊瓜籽油实际无毒。本研究开展小鼠急性经口毒性的材料为茎叶,与上述试验所用的材料为液态油脂有所不同,评判标准不一样,小鼠的半致死质量分数也不同,但结果表明长喙毛茛泽泻的茎叶为实际无毒。
长喙毛茛泽泻是极度濒危植物,野生种质资源极其稀少,导致了对其茎叶的营养元素质量分数和活性化学成分的测定研究难以开展。2015年起,浙江省丽水市相关单位开展了人工栽培的长喙毛茛泽泻回归原生地的项目研究,至2019年已在3个回归示范点培育出了一定数量的苗,可供一个批次的指标测定和毒性试验所需的样品。由于所取的样品数量有限,本研究仅对3个回归示范点4份样品的茎叶和根中的脂肪及8种常见营养元素质量分数进行了定量测定(由于检测手段的限制未测定硫质量分数),这与对中药材泽泻Alisma orientalis的测定偏重于三萜类等活性化学物质的报道[28]有所不同。本研究测定的指标不属于活性物质,而且缺乏大量元素硫的测定结果,同时缺乏近缘物种的各项指标值作为参照,这是本研究的不足之处。下一步的研究应侧重于茎叶活性化学成分的测定,并探讨这些活性化学成分与植株毒理的关联。
Nutritional components of rhizome and leaf of Ranalisma rostratum and its acute oral toxicity
-
摘要:
目的 长喙毛茛泽泻Ranalisma rostratum是极度濒危保护植物,被纳入国家Ⅰ级重点保护植物。近年来,全国先后建立了多个长喙毛茛泽泻繁育基地,其种群数量得到了有效提升。对长喙毛茛泽泻营养成分及急性经口毒性的研究,有利于对其进行更好的保护利用。 方法 选取丽水市3个回归示范点的4批次样品,烘干前后称量样品质量,计算各营养器官的生物量比和干鲜比,测定其茎叶根的主要营养成分和元素(包括脂肪、氮、磷、钾、钙、镁、铁、锰、锌)的质量分数以及茎叶的小鼠Mus musculus急性经口毒性。 结果 ①长喙毛茛泽泻植株的干鲜比为0.17~0.19,整个植株含水率较高。②长喙毛茛泽泻植株中8种元素的平均质量分数从高到低依次为氮、钾、铁、钙、磷、镁、锰、锌,铁质量分数在各样品和组织间变异系数最大,其次是磷和镁。③脂肪质量分数在4个样品之间存在显著差异(P<0.05),除锌外,其余7种元素在4个样品间均无显著差异;脂肪质量分数在长喙毛茛泽泻的茎叶和根之间没有显著差异,而钠、磷、钾、钙质量分数在茎叶和根间差异显著(P<0.05)。④钠、钾、钙这3种元素两两之间存在显著(P<0.05)或极显著(P<0.01)正相关,而与磷存在显著或极显著负相关,磷与镁存在显著正相关。⑤以长喙毛茛泽泻茎叶制取悬浮样品液,喂饲试验显示:对雌雄小鼠经口半致死量均大于7.5 g·kg−1。 结论 长喙毛茛泽泻中的镁、铁和磷质量分数不够稳定,而其他元素均较稳定。钠、磷、钾、钙质量分数在长喙毛茛泽泻的茎叶和根系间的分布有显著差异。小鼠急性经口毒性试验结果显示:其茎叶属实际无毒。图1表5参28 Abstract:Objective Ranalisma rostratum, a critically endangered plant species, is included in the national level Ⅰ key protection plants. Many breeding bases have been established in China in recent years, and the population of R. rostratum has been effectively increased. This study aims to explore the nutritional composition and acute oral toxicity of R. rostratum for its better protection and utilization. Method The 4 batches of samples from 3 regression plots in Lishui City were selected, and weighed before and after drying. The biomass ratio and dry-to-fresh ratio of each vegetative organ were calculated. The main nutrients and elements (including fat, N, P, K, Ca, Mg, Fe, Mn, Zn)in stems, leaves and roots, as well as the acute oral toxicity of stems and leaves in Mus musculus were determined. Result (1) The dry-to-fresh ratio of the plant was 0.17−0.19, indicating that the water content of the whole plant was high. (2) The average contents of 8 nutrient elements from high to low were N, K, Fe, Ca, P, Mg, Mn and Zn. The coefficient of variation of Fe content among samples and tissues was the largest, followed by P and Mg. (3) There was a significant difference in fat content among the 4 samples (P<0.05). There were no significant differences in the other 7 elements except Zn among the 4 samples. There were no significant differences in fat content between stem, leaf and root, but a significant difference in Na, P, K and Ca between the stem, leaf and root (P<0.05). (4) There was a significant (P<0.05) or extremely significant (P<0.01) positive correlation among Na, K and Ca, and the 3 elements had significant or extremely significant negative correlation with P, while P had significant positive correlation with Mg. (5) The stem leaf suspended sample liquid was prepared for the acute oral toxicity test, which showed that the oral LD50 of male and female mice was greater than 7.5 g·kg−1 body weight. Conclusion The mass fraction of Mg, Fe and P in R. rostratum was unstable, while other elements were stable. The distribution of Na, P, K and Ca in the stem, leaf and root of R. rostratum was significantly different. The acute oral toxicity test of stem and leaf in M. musculus showed that it was practically non-toxic. [Ch, 1 fig. 5 tab. 28 ref.] -
Key words:
- botany /
- Ranalisma rostratum /
- nutrient element /
- fat /
- acute oral toxicity test
-
表 1 长喙毛茛泽泻3个样地4份样品的干鲜比和生物量
Table 1. Dry-fresh ratio and biomass of 4 batches of R. rostratum from 3 samples places
样品 结实与否 干鲜比 生物量 干质量/g 鲜质量/g 干鲜比 茎叶质量/g 根质量/g 茎叶/根 南明山1号 已结实 144.57 750 0.19 93.33 51.24 1.82 南明山2号 未结实 61.25 370 0.17 43.70 17.55 2.49 大港头镇 已结实 86.56 500 0.17 58.54 28.02 2.09 老竹乡 已结实 165.53 1000 0.17 107.96 57.57 1.88 说明:生物量栏中,茎叶质量和根质量都是指样品的干质量 表 2 脂肪和各营养元素质量分数范围、均值和变异系数
Table 2. Range, mean values and coefficient variation of fat and nutrient elements
项目 脂肪及各养元素质量分数/(mg·g−1) 变异系数/% 最小值 最大值 最大/最小 平均值 标准差 脂肪 9.00 36.00 4.00 23.13 9.22 39.86 氮 22.40 34.20 1.53 26.50 4.53 17.09 钾 15.90 39.10 2.50 25.08 9.14 36.44 磷 0.50 8.50 17.00 3.87 3.28 84.70 铁 0.17 33.00 194.12 6.49 11.12 171.43 钙 3.30 9.71 2.94 6.21 2.33 37.58 镁 0.00 2.70 900.00 1.07 1.20 111.33 锰 0.38 1.52 4.00 0.68 0.38 56.70 锌 0.03 0.09 2.94 0.06 0.02 36.21 表 3 长喙毛茛泽泻茎叶与根系的脂肪和营养元素均值及显著性分析
Table 3. Mean value and significance analysis of fat and nutrient elements in stem, leaf and root
测定
指标测定
部位平均值/
(mg·g−1)自由度 组间均
方差F P 脂肪 茎叶 27.00±8.98 1 120.125 1.518 0.264 根 19.25±8.81 氮 茎叶 30.30±3.04 1 115.520 24.754 0.003 根 22.70±0.29 钾 茎叶 32.55±6.50 1 447.005 19.516 0.004 根 17.60±1.87 磷 茎叶 1.00±0.56 1 66.298 43.928 0.001 根 6.75±1.64 铁 茎叶 1.22±1.72 1 221.825 2.067 0.201 根 11.75±14.55 钙 茎叶 8.08±1.67 1 27.975 16.485 0.007 根 4.34±0.78 镁 茎叶 0.37±0.73 1 3.996 3.989 0.093 根 1.78±1.21 锰 茎叶 0.52±0.16 1 0.200 1.447 0.274 根 0.83±0.50 表 4 长喙毛茛泽泻植株脂肪和8种营养元素间相互关系
Table 4. Correlation between plant fat and 8 nutrient elements
元素 脂肪 氮 钾 磷 铁 钙 镁 锰 锌 脂肪 1 氮 0.527 1 钾 0.522 0.975** 1 磷 −0.695 −0.876** −0.844** 1 铁 −0.399 −0.497 −0.540 0.589 1 钙 0.158 0.850** 0.802* −0.762* −0.343 1 镁 −0.463 −0.402 −0.440 0.717* 0.377 −0.520 1 锰 0.331 −0.348 −0.268 0.168 −0.104 −0.398 −0.243 1 锌 0.065 0.086 −0.107 0.044 0.222 0.024 0.515 −0.264 1 说明:*表示显著相关(双尾t检验,P<0.05); **表示极显著相关(双尾t检验,P<0.01) 表 5 长喙毛茛泽泻茎叶的小鼠急性经口毒性试验结果
Table 5. Acute oral toxicity test in mice of leaf of R. rostratum
性别 小鼠始
质量/g小鼠终
质量/g死亡情况
(死亡数/组鼠数)LD50/
(g·kg−1)雌性 19.9±0.9 28.2±1.7 0/10 >7.5 雄性 19.6±0.6 31.5±1.4 0/10 >7.5 -
[1] 孙祥钟. 中国植物志: 第8卷[M]. 北京: 科学出版社, 1992: 136. [2] 王建波, 陈家宽, 利容千, 等. 长喙毛茛泽泻的生活史特征及濒危机制[J]. 生物多样性, 1998, 6(3): 167 − 171. WANG Jianbo, CHEN Jiakuan, LI Rongqian, et al. Life history traits and mechanisms of endangerment in Ranalisma rostratum [J]. Chin Biodiersity, 1998, 6(3): 167 − 171. [3] 汪小凡, 陈家宽. 湖南境内珍稀、濒危水生植物产地的考察[J]. 生物多样性, 1994, 2(4): 193 − 198. WANG Xiaofan, CHEN Jiakuan. A survey on the habitats of rare and endangered aquatic plants in Hunan Province [J]. Chin Biodiersity, 1994, 2(4): 193 − 198. [4] 国家林业局, 农业部. 国家重点保护野生植物名录(第1批)[EB/OL]. (1999-09-09)[2021-01-06]. http://www.gov.cn/gongbao/content/2000/content_60072.htm. [5] 赵勋, 周世荣, 苏燕. 长喙毛茛泽泻迁地扩繁技术研究[J]. 湿地科学与管理, 2018, 14(4): 42 − 43. ZHAO Xun, ZHOU Shirong, SU Yan. Ex situ propagation of Ranalisma rostratumt [J]. Wetland Sci Manage, 2018, 14(4): 42 − 43. [6] 苏燕, 赵勋, 沈燕, 等. 长喙毛茛泽泻组培苗移栽试验研究[J]. 湿地科学与管理, 2018, 14(1): 47 − 49. SU Yan, ZHAO Xun, SHEN Yan, et al. Transplanting of tissue cultured plants of Ranalisma rostratum [J]. Wetland Sci Manage, 2018, 14(1): 47 − 49. [7] 周纯, 田惠桥. 濒危植物毛茛泽泻的组织培养[J]. 植物生理学通讯, 1994(4): 277. ZHOU Chun, TIAN Huiqiao. Tissue culture ofRanalisma rostratum [J]. Plant Physiol Commun, 1994(4): 277. [8] 胡小辉, 陈家宽, 王建波. 长喙毛茛泽泻遗传多样性及其与繁育系统的关系[J]. 云南植物研究, 1999, 21(2): 232 − 238. HU Xiaohui, CHEN Jiakuan, WANG Jianbo. Genetic diversity and its relationship with breeding system of Ranalisma rostratum [J]. Acta Bot Yunnan, 1999, 21(2): 232 − 238. [9] 王玉国, 王青峰, 陈家宽, 等. 长喙毛茛泽泻的花器官发生[J]. 云南植物研究, 1998, 20(3): 303 − 308. WANG Yuguo, WANG Qingfeng, CHEN Jiakuan, et al. Floral organogenesis of Ranalisma rostratum (Alismataceae) [J]. Acta Bot Yunnan, 1998, 20(3): 303 − 308. [10] 王建波, 陈家宽, 利容千, 等. 长喙毛茛泽泻的大小孢子发生及雌雄配子体发育[J]. 武汉大学学报(自然科学版), 1994, 40(4): 95 − 101. WANG Jianbo, CHEN Jiakuan, LI Rongqian, et al. Microsporgenesis, megasporogenesis and the development of male and female gametophyte in Ranalisma rostratum Stapf [J]. J Wuhan Univ Nat Sci Ed, 1994, 40(4): 95 − 101. [11] 王建波, 陈家宽, 利容千, 等. 长喙毛茛泽泻双受精过程的细胞学观察[J]. 武汉大学学报(自然科学版), 1995, 41(2): 199 − 202. WANG Jianbo, CHEN Jiakuan, LI Rongqian, et al. Cytological observation on the double fertilization in Ranalisma rostratum [J]. J Wuhan Univ Nat Sci Ed, 1995, 41(2): 199 − 202. [12] 田惠桥, 陈家宽, 郭友好. 濒危植物——长喙毛茛泽泻的受精作用及胚和胚乳的发育[J]. 植物分类学报, 1995, 33(4): 357 − 361. TIAN Huiqiao, CHEN Jiakuan, GUO Youhao. The fertilization and the development of embryo and endosperm in an endangered plant: Ranalisma rostratum Stapf(Alismataceae) [J]. Acta Phytotaxon Sin, 1995, 33(4): 357 − 361. [13] 汪小凡, 陈家宽. 长喙毛茛泽泻(泽泻科)的交配系统研究[J]. 云南植物研究, 1998, 20(3): 315 − 320. WANG Xiaofan, CHEN Jiakuan. Studies on mating system of Ranalisma rostratum(Alismataceae) [J]. Acta Bot Yunnan, 1998, 20(3): 315 − 320. [14] 陈中义, 何国庆, 陈家宽. 濒危植物长喙毛茛泽泻生物学特性观察[J]. 武汉大学学报(自然科学版), 1997, 43(2): 201 − 204. CHEN Zhongyi, HE Guoqing, CHEN Jiakuan. Observation on biological characters of Ranalisma rostratum [J]. J Wuhan Univ Nat Sci Ed, 1997, 43(2): 201 − 204. [15] 陈中义, 陈家宽. 长喙毛茛泽泻的种群分布格局和群落内种间关联[J]. 植物生态学报, 1999, 23(1): 56 − 61. CHEN Zhongyi, CHEN Jiakuan. The spatial pattern of Ranalisma rostratum population and interspecific association in the community [J]. Acta Phytoecol Sin, 1999, 23(1): 56 − 61. [16] 李今, 陈家宽, 周进, 等. 迁地保护中普通野生稻和长喙毛莨泽泻种群动态及评价[J]. 植物生态学报, 1999, 23(3): 275 − 282. LI Jin, CHEN Jiakuan, ZHOU Jin, et al. Dynamics and evaluation ofOryza rufipogon and Ranalisma rostratum population in ex situ conservation of communities [J]. Acta Phytoecol Sin, 1999, 23(3): 275 − 282. [17] 陈家宽, 陈中义. 不同生境内濒危植物长喙毛茛泽泻种群数量动态比较[J]. 植物生态学报, 1999, 23(1): 8 − 13. CHEN Jiakuan, CHEN Zhongyi. Population dynamics ofRanalisma rostratum, an endangered species growing in different habitats [J]. Acta Phytoecol Sin, 1999, 23(1): 8 − 13. [18] 周进, 陈中义, 陈家宽. 普通野生稻-长喙毛茛泽泻-柳叶箬混作种群的竞争效应[J]. 生态学报, 2000, 20(4): 685 − 691. ZHOU Jin, CHEN Zhongyi, CHEN Jiakuan. The effects of competition among the mixed crop populations of Oryza rufipogon, Ranalisma rostrata andIsachne globosa [J]. Acta Ecol Sin, 2000, 20(4): 685 − 691. [19] 朱光冕, 曾柏全, 曾文斌, 等. 弱光下不同水深对长喙毛茛泽泻生长及生理特性的影响[J]. 生态学报, 2019, 39(19): 7295 − 7301. ZHU Guangmian, ZENG Baiquan, ZENG Wenbin, et al. Effects of different water depths on the growth and physiological characteristics of Ranalisma rostratum under low light intensity [J]. Acta Ecol Sin, 2019, 39(19): 7295 − 7301. [20] 鲍恩, 崔仙舟. 元素的环境化学[M]. 北京: 科学出版社, 1986: 71 − 73. [21] TAIZ L, ZEIGER E. 植物生理学[M]. 宋纯鹏, 王学路, 译. 4版. 北京: 科学出版社, 2009: 60 − 127. [22] 蒋裕良. 弄岗喀斯特森林树种元素含量特征及其与生境的联系[D]. 桂林: 广西师范大学, 2016. JIANG Yuliang. Characteristics of Elements Contents in Trees from Nonggang Karst Forest and Their Associations with Habitats[D]. Guilin: Guangxi Normal University, 2016. [23] 罗绪强, 张桂玲, 阮英慧, 等. 雷公山自然保护区常见植物叶片营养元素含量及其化学计量特征[J]. 江苏农业科学, 2019, 47(11): 309 − 312. LUO Xuqiang, ZHANG Guiling, RUAN Yinghui, et al. Nutrirnt contents and stoichiometric characteristics of common plant leaves in the Leigong Mountain Nature Reserve [J]. Jiangsu Agric Sci, 2019, 47(11): 309 − 312. [24] 惠岑怿, 石莎, 冯金朝, 等. 内蒙古地带性针茅植物15种营养元素含量及化学计量特征分析[J]. 云南大学学报(自然科学版), 2019, 41(2): 168 − 177. HUI Chenyi, SHI Sha, FENG Jinchao, et al. Analysis on the content and stoichiometry of 15 nutrient elements of zonal Stipa plants in Inner Mongolia [J]. J Yunnan Univ Nat Sci Ed, 2019, 41(2): 168 − 177. [25] KOERSELMAN W, MEULEMANAM F. The vegetation N∶P ratio: a new tool to detect the nature of nutrient limitation [J]. J Appl Ecol, 1996, 33(6): 1441 − 1450. [26] 石从广, 朱光权, 黄海志, 等. 白花树种子油精炼及其毒理学初步评价[J]. 中国食品学报, 2014, 14(5): 192 − 201. SHI Congguang, ZHU Guangquan, HUANG Haizhi, et al. Refining and toxicology preliminary evaluation ofStyrax tonkinesis seed oil [J]. J Chin Inst Food Sci Technol, 2014, 14(5): 192 − 201. [27] 王亚萍, 杨柳, 朱光权, 等. 长兴吊瓜籽油脂肪酸组成分析和毒理学初步评价[J]. 中国粮油学报, 2018, 33(12): 56 − 62. WANG Yaping, YANG Liu, ZHU Guangquan, et al. Fatty acid composition analysis and toxicology preliminary evaluation of trichosanthes bracteata seed oil [J]. J Chin Cereals Oils Assoc, 2018, 33(12): 56 − 62. [28] 张慧娟, 龚苏晓, 许浚, 等. 泽泻药材的研究进展及其质量标志物的预测分析[J]. 中草药, 2019, 50(19): 4741 − 4751. ZHANG Huijuan, GONG Suxiao, XU Jun, et al. Research progress of Alismatis rhizoma and prediction analysis on its Q-marker [J]. Chin Tradit Herbal Drugs, 2019, 50(19): 4741 − 4751. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20200813






 下载:
下载: