-
浮皮是宽皮柑橘Citrus reticulata果实在成熟后期或采后储藏过程中普遍发生的一种生理性障碍。所谓浮皮,是指白皮层崩溃,包裹果肉的囊瓣膜(囊衣)与果皮分离后浮起,果皮与囊瓣膜之间产生空隙[1],同时果皮增厚,外表面粗糙不平,内表面变得松散[2]。浮皮可提高果实的易剥皮性,便于食用,但同时会导致果实采后营养物质大量减少,风味变淡,严重影响果实的品质和储藏性能。影响浮皮的发生因素诸多,如遗传因素、砧木、环境压力和病害等。目前,关于柑橘果实浮皮的研究集中于生理生化和细胞学形态变化,而在分子方面的研究较少[3]。柑橘果实浮皮是一个复杂的生理过程,浮皮发生机制未有定论,也尚未开发出有效的调控技术[4]。椪柑C. reticulata ‘Ponkan’是典型的易浮皮宽皮柑橘,在完熟和采后储藏过程中浮皮现象尤为严重[5]。
乙烯作为一种气态植物生长调节剂,可促进果实成熟并加速果实衰老,其调控呼吸跃变型果实成熟衰老的机制研究已经非常深入。外源乙烯处理能显著提高网纹甜瓜Cucumis melo var. reticulatus果实细胞壁水解酶的活性,从而加速完熟果实硬度下降[6]。非跃变型果实成熟衰老过程产生的乙烯远低于跃变型果实。乙烯曾被认为在非跃变型果实成熟衰老中发挥的作用非常有限[7]。然而,近年来研究表明:非跃变型果实和跃变型果实成熟衰老的某些分子调控途径非常相似,诸多果实品质变化过程也直接受乙烯调控[8]。柑橘属典型非呼吸跃变型果实,在其成熟衰老整个过程中呼吸速率和乙烯释放率均很低。低水平的内源乙烯参与调控了柑橘果实成熟衰老进程,尤其是柑橘果皮颜色的改变[7]。邓丽莉等[9]研究表明:乙烯在柑橘果实褪绿转色过程中,不同部位果皮着色呈现明显的差异。目前大多相关研究集中在果实果肉部分,而对果皮的研究较少。乙烯与柑橘浮皮有着密切的联系,果实中乙烯增加助长浮皮发生。梁颖[10]研究表明:外源乙烯促进了柑橘果皮1-氨基环丙烷-1-羧酸(ACC)合成酶(ACS)和ACC氧化酶(ACO)及乙烯不敏感转录调节基因EIN3的表达,促进了果实中乙烯释放。刘美迎[11]利用外源乙烯处理葡萄Vitis vinifera果实,促使果皮酚类物质显著提升。综上说明乙烯对非跃变型果实果皮也具有调控作用。
1-甲基环丙烯(1-MCP)是乙烯的竞争性抑制剂,能与乙烯受体不可逆结合,阻断乙烯下游调控作用,具有无毒、低量、高效等优点[12]。目前,1-MCP已在苹果Malus pumila[13]、芒果Mangifera indica[14]等果蔬储藏保鲜中广泛应用。杜欣欣等[15]研究发现:使用300 μL·L−1 1-MCP处理青柠檬Citrus aurantiifolia能有效减缓果皮转黄,抑制可溶性固形物(TSS)含量降低和可滴定酸(TA)含量上升,达到最佳保鲜效果。林旭东等[16]通过微孔膜结合1-MCP处理柑橘,可以较好地保持其外观(果梗鲜绿、稳固)、色泽、硬度及品质指标,维持较低的相对电导率,60 d内可以维持柑橘较好的商品价值。王长锋[17]研究发现:适宜的1-MCP处理可延缓椪柑果皮叶绿素降解,延长果实货架期,提高椪柑果实商品性。
鉴于此,本研究拟通过乙烯和1-MCP处理椪柑果实,研究其对采后果实品质和浮皮特性的影响,分析果实白皮层细胞形态和生理变化,为揭示椪柑果实浮皮的发生机制及储藏中浮皮防治提供理论依据。
-
椪柑属衢州地方品种,于2017年11月26日采自浙江省衢州市柯城区柴家柑橘专业合作社椪柑种植基地。树体在设施环境下栽培,树龄为10 a,平均树高为2.5 m,树体间距为5.0 m。采摘时,在椪柑树体东、南、西、北4个方位的上、中、下部,随机挑选大小、成熟度基本一致,且无机械损伤和病虫害的果实。
-
药品主要有1-MCP (美国罗门哈斯公司,有效成分0.014%)和乙烯气体(杭州悦通气体技术开发有限公司,纯度>99.99%)。
-
在预实验的基础上,确定10.0 μL·L−1乙烯处理4 d,1.0 μL·L−11-MCP处理14 h所得最佳效果。本研究设置3个处理:①对照。将果实置于20 ℃恒温箱储藏。②乙烯处理。将椪柑果实装入密封箱,利用针管加入10.0 μL·L−1乙烯气体后密闭放置4 d。4 d后将椪柑果实装入柑橘保鲜袋,置于20 ℃恒温箱储藏。③1-MCP处理。将1.0 μL·L−11-MCP气体注射入箱内,立即封口密闭,处理14 h。之后装入柑橘保鲜袋,置于20 ℃恒温箱储藏。
每个处理100个果实,3个重复,乙烯和1-MCP处理的储藏期从处理之日算起,分别在处理0、7、14、28、56 d时进行取样。取样时从每个重复中随机挑取10个果实,即每个处理30个果实进行相应指标的测定。
-
将样品洗净擦干,用手术刀切开,放入摄影箱观察果实纵切面。浮皮指数参考文献[2]的方法,通过果实纵切面判断浮皮程度。浮皮程度分为浮皮无(0级),浮皮轻(1级,仅果柄端浮皮),浮皮中等(2级,果柄端与两侧均浮皮),浮皮重(3级,全果浮皮) 4个等级。浮皮指数=Σ(浮皮级果数×代表级值)/(调查总果数×浮皮最重一级的代表值)。果实可溶性固形物使用数显折射仪(日本爱拓PAL-1)测定;抗坏血酸(Vc)采用2, 6-二氯靛酚法[18]测定。质量损失率=(初始质量−当次测量质量)/初始质量×100%;果皮率=果皮质量/果实质量×100%。
-
采用石蜡切片法[19],将预处理后的果皮固定材料取出后洗涤、脱水、透明、透蜡、包埋,使用德国莱卡切片机切成厚度8~10 mm的蜡带,在常温蒸馏水中将蜡带固定于载玻片上,42 ℃烤片机展片,采用番红-固绿双染色法染色,中性树胶封片后观察细胞结构。
选取椪柑不同储藏时间的切片各5张,用OLYMPUS BH-2型显微摄影机进行显微结构观察和摄影。在4倍镜下每张切片选取10个位置进行显微测量和细胞学统计,用Image-ProPlus测定果皮白皮层的细胞直径,统计半径250 μm圆形视野中细胞的数目为细胞密度。
-
纤维素采用蒽酮试剂法测定[20];原果胶采用咔唑比色法测定[20];纤维素酶(Cx)活性以每小时每克鲜质量样品在37 ℃催化羧甲基纤维素水解形成还原糖的微克数表示,单位为μg·h−1·g−1[20];果胶酯酶(PE)活性采用滴定法进行测定,以单位鲜质量样品在30 min内消耗的氢氧化钠(NaOH)量表示果胶酯酶活性,单位为μg·h−1·g−1[21];多聚半乳糖醛酸酶(PG)活性以每小时每克鲜质量样品在37 ℃催化多聚半乳糖醛酸水解生成半乳糖醛酸的微克数表示,单位为μg·h−1·g−1[20];木质素采用木质素试剂盒(D799081-0100)微量法测定,购于上海生工生物工程有限公司。
-
采用SPSS 26.0对各生理指标和酶活进行方差分析,用Origin 2019b作图。
-
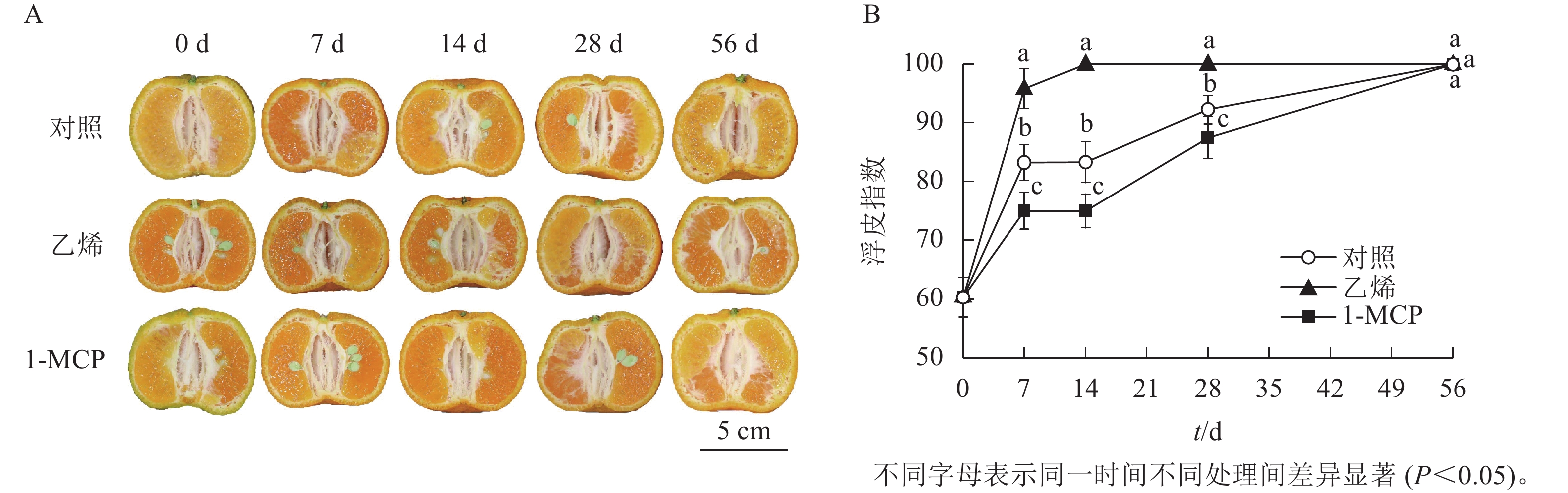
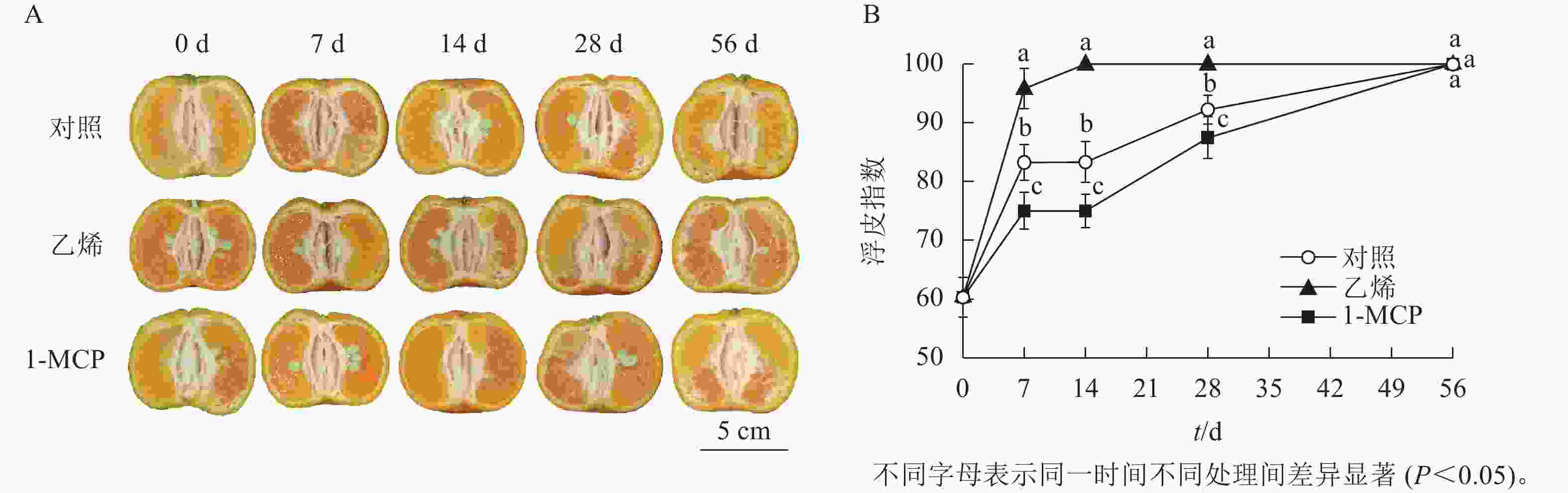
由图1可知:刚采摘的椪柑果实果蒂处海绵层增厚,已出现浮皮现象,浮皮指数达60.30。随着储藏进程,果实浮皮程度加深,皮肉之间间隙增大,中心柱开始空虚,白皮层变薄且呈绒絮松散状,果皮出现不规则隆起。乙烯处理组果实在第14天出现果实皮肉完全分离,浮皮严重,浮皮指数达100.00。1-MCP处理组果实采后浮皮加剧迟缓,与乙烯处理组和对照相比,皮肉间隙更小;第14天浮皮指数为75.00,至第56天时,仍有肉眼可见的白皮层,果皮无明显隆起现象,果皮形态保持完好,组织致密,果实体积增长缓慢。
-
由图2可知:抗坏血酸质量分数在1-MCP和对照处理中呈先下降后上升又下降的趋势,在乙烯处理一直处于下降趋势。1-MCP处理果实的抗坏血酸质量分数峰值出现在第14天,达6.134 mg·kg−1,对照处理的抗坏血酸质量分数峰值出现在第28天,达6.911 mg·kg−1,到第56天时3个处理之间抗坏血酸质量分数差异不显著。3个处理的果实可溶性固形物质量分数呈上升趋势,与对照相比,乙烯处理组上升更为明显,由最初的1.19 mg·g−1升高至1.47 mg·g−1。在整个储藏期内,各处理的果实质量换失率无显著差异,果皮率不断下降,其中乙烯处理的果皮率最高,对照组最低,这可能是由于乙烯处理后果实生理代谢加速,内部物质消耗速率过快导致的。
-
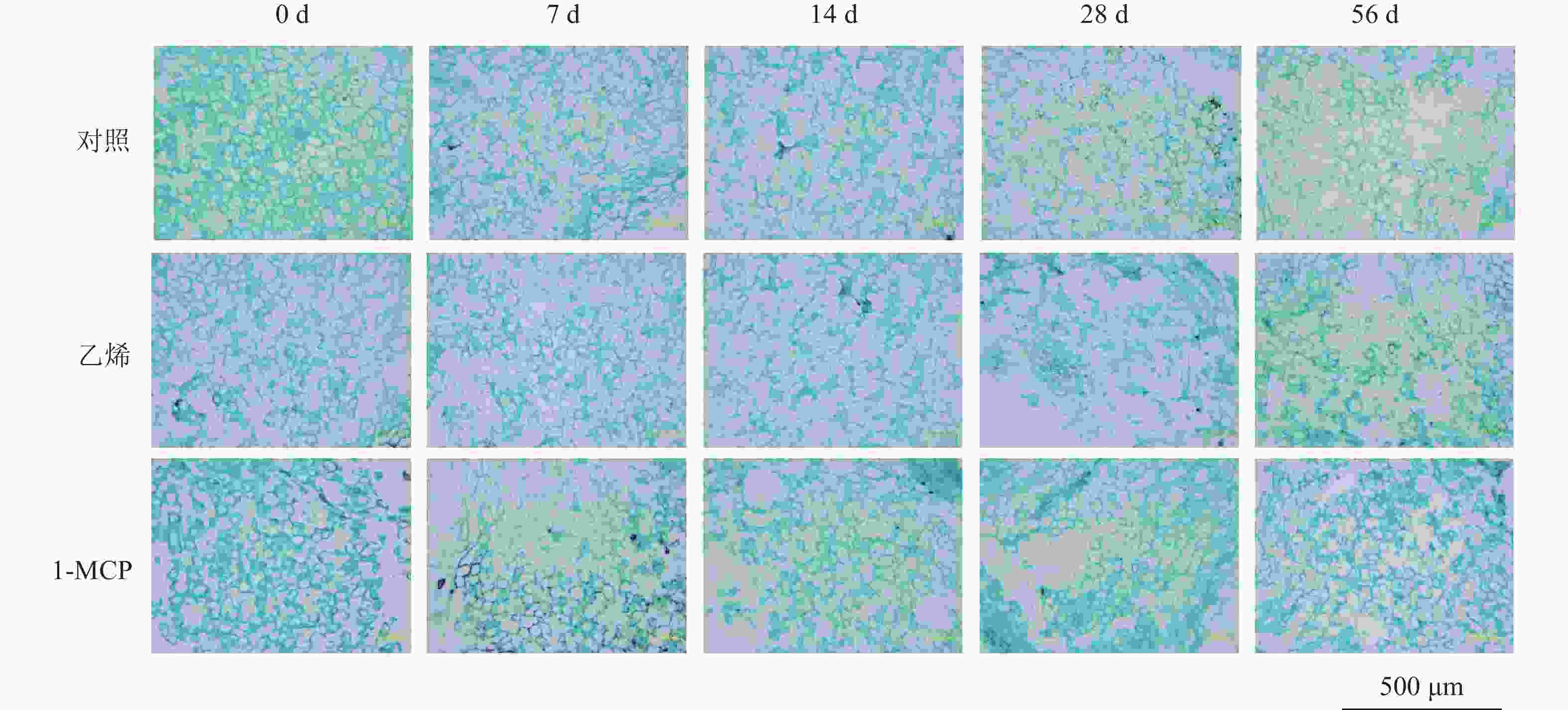
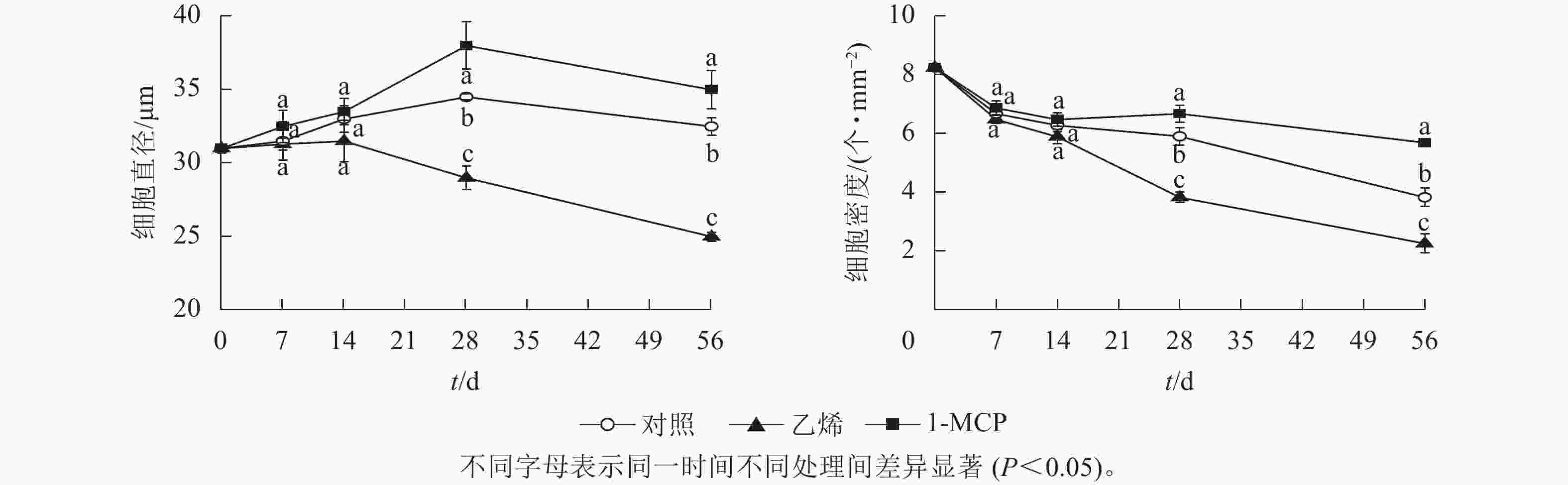
由图3可见:乙烯处理组果皮白皮层细胞在储藏前期快速膨大,第28天时,细胞已经出现裂解、破裂,细胞间隙变大,第56天时,视野内细胞直径较小,且细胞密度低于对照和1-MCP处理。而1-MCP处理后,细胞密度缓慢下降,细胞拉伸、裂解的现象得到缓解,至第56天时,细胞形态完好,细胞密度高于乙烯处理和对照。由图4可知:椪柑果实随着储藏时间的延长,白皮层细胞直径先上升后下降。乙烯处理的白皮层细胞在第28天时出现细胞裂解,白皮层细胞密度和细胞直径下降,白皮层细胞密度从第28天开始显著低于对照和1-MCP处理(P<0.05)。在0~28 d,1-MCP处理的果皮白皮层细胞直径呈上升趋势,而后细胞直径开始下降,第56天时,白皮层细胞直径显著高于乙烯处理(P<0.05)。椪柑果皮白皮层细胞密度在各个处理中都呈下降趋势,在第28天时,由于乙烯处理出现细胞裂解的现象,导致细胞密度开始下降,随着细胞间隙的变大,乙烯处理的果皮白皮层细胞密度下降趋势加快,在第56天时,乙烯处理的果皮白皮层细胞密度显著低于对照和1-MCP处理(P<0.05)。1-MCP处理延缓了果皮白皮层细胞密度的下降。
-
由图5可知:储藏过程中3个处理的纤维素质量分数均呈下降趋势,乙烯处理始终低于对照,1-MCP处理始终高于对照组;第14天时乙烯处理的纤维素质量分数迅速下降并持续显著低于对照和1-MCP处理(P<0.05);第56天时乙烯处理的纤维素质量分数下降为51.3 mg·g−1,1-MCP处理的纤维素质量分数是乙烯处理的1.46倍。

图 5 乙烯和1-MCP处理果实白皮层纤维素质量分数和纤维素酶活性的变化
Figure 5. Changes of cellulose content and cellulase activity of albedo under ethylene and 1-MCP treatment during storage
各处理果皮白皮层纤维素酶活性均呈上升趋势;第14天时乙烯处理的纤维素酶活性迅速上升,第28天酶活性显著高于对照和1-MCP处理,第56天时最高,达125.14 μg·h−1·g−1,是对照的1.98倍;1-MCP处理的纤维素酶活性始终略低于对照,但差异不显著。
-
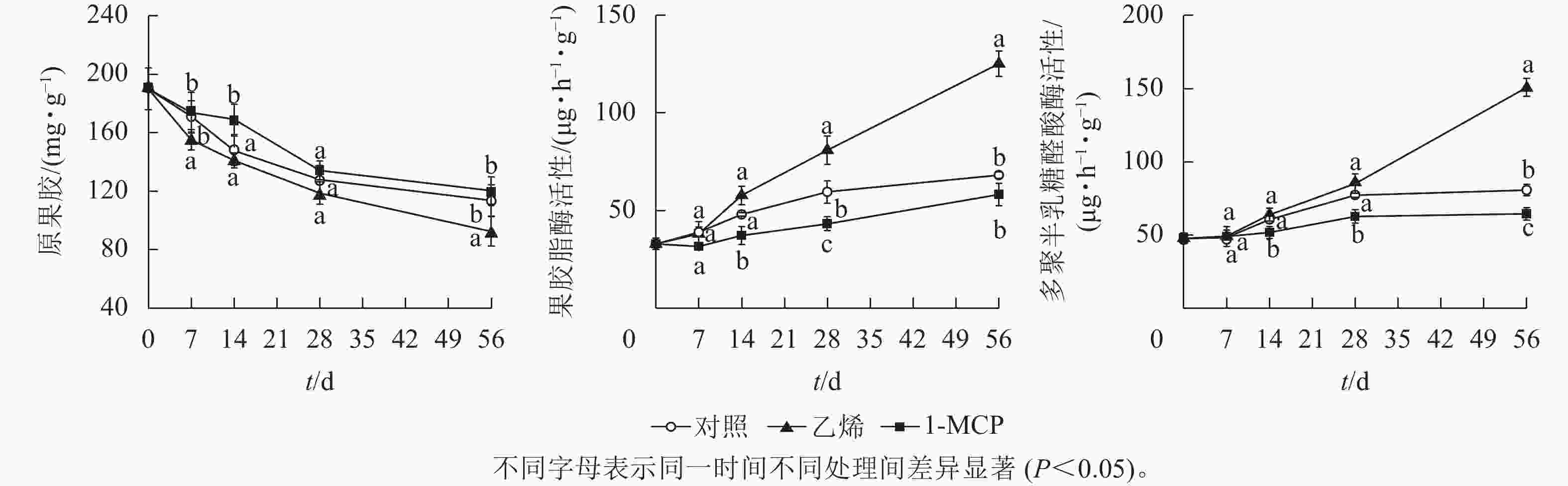
由图6可知:随着储藏期的延长,原果胶质量分数逐渐减少,乙烯处理的原果胶质量分数始终低于对照,1-MCP处理的原果胶质量分数始终高于对照组;第56天时,乙烯处理的原果胶质量分数降至92.82 mg·g−1,与1-MCP处理差异显著(P<0.05)。果皮白皮层果胶酯酶活性总体上呈上升趋势;1-MCP处理的果胶酯酶活性在0~14 d基本不变,第28天时为37.47 μg·h−1·g−1,显著低于对照和乙烯处理(P<0.05);乙烯处理的果胶酯酶活性第56天时为97.95 μg·h−1·g−1,显著高于对照和1-MCP处理(P<0.05)。在整个储藏期内,果皮白皮层多聚半乳糖醛酸酶活性在乙烯处理中上升迅速,而在1-MCP处理中上升缓慢;第56天时乙烯处理的多聚半乳糖醛酸酶活性达150.86 μg·h−1·g−1,是对照的1.87倍,是1-MCP处理的2.33倍,显著高于对照和1-MCP处理(P<0.05),且对照与1-MCP处理也达到显著水平(P<0.05)。
-
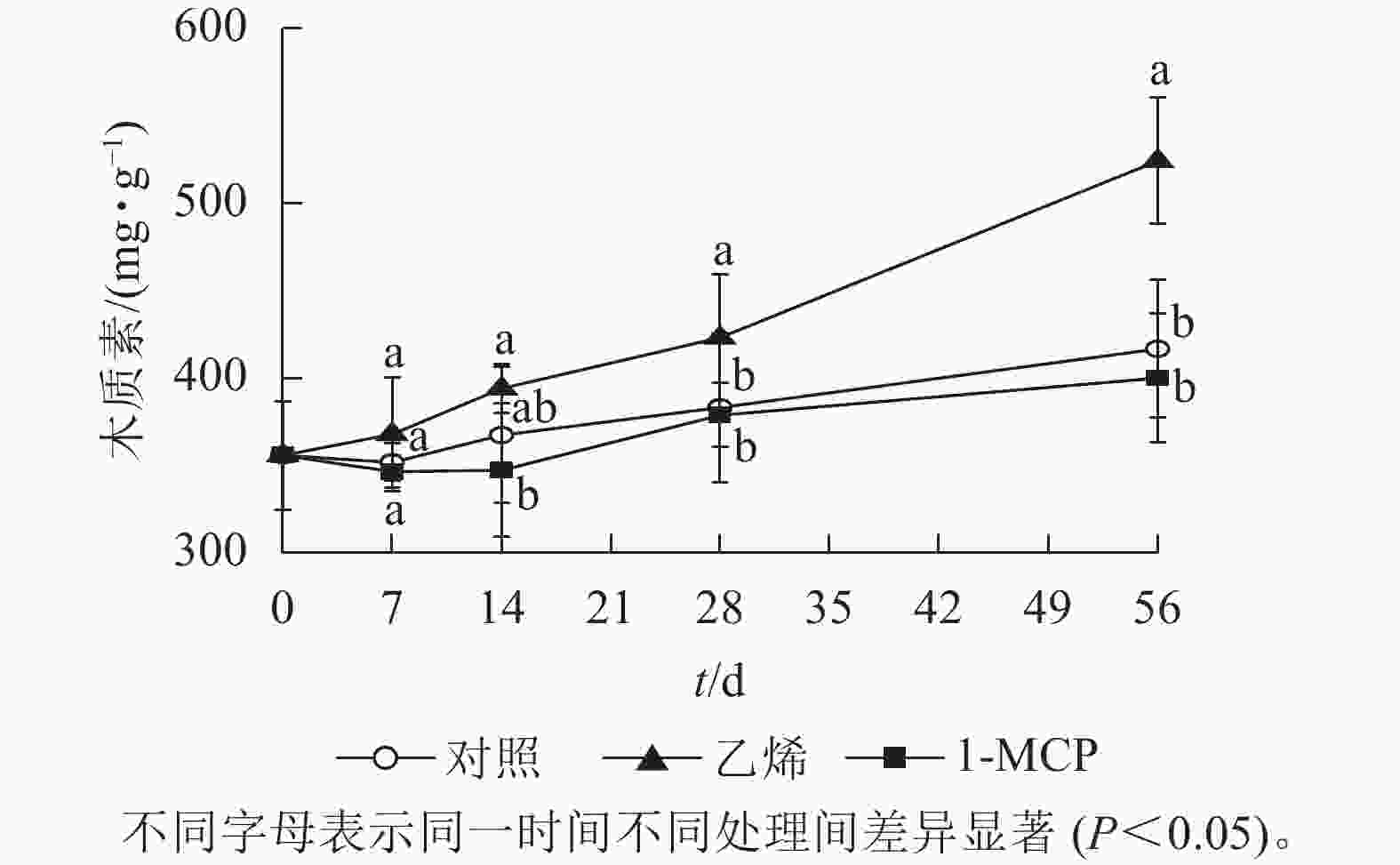
由图7可知:木质素质量分数在3个处理中为上升趋势,其中乙烯处理的上升速度最快,第56天时达523.6 mg·g−1,显著高于对照和1-MCP处理(P<0.05);1-MCP处理与对照的木质素质量分数上升相对较为缓慢,且1-MCP处理略低于对照。
-
柑橘作为一类典型的非呼吸跃变型果实,在正常的采后储藏中,果实品质会逐渐下降。本研究发现:在常温储藏下,乙烯处理后的果实浮皮程度显著大于对照,1-MCP处理的浮皮程度小于对照。
可溶性固形物包括可溶性糖、有机酸、维生素、果胶、单宁等易溶于水的物质,是衡量果实品质的重要指标[22]。到第56天时,各处理果实的可溶性固形物质量分数均显著上升,与对照相比,乙烯处理上升显著。乙烯处理能促进柑橘果肉中淀粉的转化[23],使柑橘果实中的可溶性固形物质量分数升高,果肉变甜,这与秦畅等[24]的研究结果一致。王长锋[17]研究发现:1-MCP处理对可溶性固形物质量分数没有显著影响,这与本研究结果一致。在储藏期间,果实质量换失率均呈上升趋势,且各处理间差异不显著,表明乙烯和1-MCP处理对柑橘果实质量换失率影响较小。此外,乙烯处理后椪柑果皮率高于对照,这可能是由于果肉营养物质向果皮转运引起的[25]。
柑橘浮皮症状主要发生在果皮。IBANEZ等[3]研究发现:柑橘果皮白皮层生理特性活跃,是多数柑橘生理性病害发生的关键部位。浮皮的产生与果皮白皮层细胞结构和形态变化有重要的关系[19, 26]。但浮皮的发生是动态积累的过程,发生的起始时期在外观上未表现出症状,但细胞形态结构已发生变化,这可以通过相关指标来进行判定。本研究通过石蜡切片观察发现:乙烯处理的椪柑果皮细胞密度迅速下降,细胞直径上升趋势明显,白皮层细胞出现破裂、细胞间隙变大,细胞排列松散,单位面积的白皮层细胞密度以及白皮层细胞直径显著降低,浮皮现象加剧。赵迪[26]在温州蜜柑‘宫川’C. unshiu ‘Miyagawa’的浮皮进程中发现:花后110 d,果皮细胞内容物降解,叶绿体及线粒体结构瓦解,叶绿体膨大,基粒片层结构松散、紊乱,果皮细胞表现出一定的衰老特征。花后197 d,‘宫川’果皮整个细胞的原生质体降解呈扁平状,细胞壁与细胞质完全质壁分离。乙烯加速了叶绿体和线粒体的裂解,加快了细胞内容物的降解,使得果皮白皮层细胞出现萎缩、塌陷甚至降解的现象。
果实质地主要取决于纤维素、果胶、木质素等细胞壁物质,它是果实品质的重要指标,又与果实的成熟衰老密切相关。一般果实在成熟衰老过程中,纤维素酶、果胶酯酶和多聚半乳糖醛酸酶等细胞壁降解酶活性增强,果胶、纤维素等细胞壁物质发生降解,从而导致果肉的软化和出汁率的提高[27−28]。木质素作为植物细胞壁的主要组成部分,与纤维素、果胶等物质相互交联,增加了果肉细胞壁机械强度。木质素的积累造成果实口感变差,硬度增加,导致品质下降[29]。朱婉彤等[30]研究表明:乙烯处理后甜瓜Cucumis melo的纤维素、原果胶均低于对照,多聚半乳糖醛酸酶活性、纤维素酶活性在酶活高峰时均高于对照;而1-MCP明显延缓了纤维素及原果胶的下降,降低了纤维素酶、果胶酯酶、多聚半乳糖醛酸酶的活性。谢国芳等[31]研究发现:鲜食菜豆Phaseolus vulgaris经乙烯处理,木质素代谢关键酶活性降解,导致木质化细胞团增加,促进木质纤维化,而1-MCP处理则相反。以上研究结果均与本研究结果相似。在本研究中,随着储藏时间的延长,纤维素酶、果胶酯酶、多聚半乳糖醛酸酶活性上升,促进纤维素和原果胶不断下降。乙烯可加速果实乙烯生物合成及生理作用,加快果实后熟衰老进程。1-MCP则可延缓果实软化,对果胶物质降解起到了减缓作用。果胶物质、纤维素的降解及细胞壁降解酶活性的升高是采后椪柑果实衰老的重要原因。1-MCP可以有效地延缓椪柑果实的衰老。
-
乙烯处理加速了椪柑果实采后生理代谢水平,加重了果实浮皮的发生。1-MCP处理则抑制了储藏期果皮的生理代谢水平,延缓了果皮细胞的衰老,减轻了浮皮障碍的发生。在储藏中若想保持椪柑新鲜,降低浮皮状况,可用1-MCP进行处理。若想使剥皮更加容易,可用乙烯进行处理。
Effects of ethylene and 1-MCP treatment on puffiness and albedo cell wall metabolism of post-harvest Citrus reticulata ‘Ponkan’ fruit
-
摘要:
目的 浮皮是宽皮柑橘Citrus reticulata果实在成熟后期或采后储藏过程中普遍发生的一种生理性障碍。椪柑C. reticulata ‘Ponkan’在采后储藏中极易发生浮皮,严重影响商品价值。通过采后处理,为椪柑果实采后浮皮的防范、储藏保鲜技术提供理论依据。 方法 利用乙烯和1-甲基环丙烯(1-MCP)处理椪柑采后果实,测定椪柑在储藏期间果实主要品质指标及浮皮指数的变化,分析果皮白皮层细胞形态和生理变化特征。 结果 ①乙烯处理促进了储藏期果实可溶性固形物质量分数的提高;加速了果皮白皮层细胞密度、纤维素质量分数、果胶质量分数的下降,促使木质素质量分数及细胞壁降解酶(纤维素酶、果胶酯酶、多聚半乳糖醛酸酶)活性上升。②1-MCP处理减缓了果皮白皮层细胞密度及纤维素质量分数下降;延缓了木质素质量分数及细胞壁降解酶(纤维素酶、果胶酯酶、多聚半乳糖醛酸酶)活性上升;减缓了椪柑果实浮皮指数的上升。 结论 乙烯处理可加速椪柑果实采后生理代谢水平,加重果实浮皮的发生。1-MCP处理可抑制储藏期果皮的生理代谢水平,减轻浮皮障碍的发生。生产中可通过乙烯和1-MCP处理来控制椪柑果实剥皮的难易程度。图7参31 -
关键词:
- 椪柑 /
- 果实采后品质 /
- 浮皮 /
- 乙烯 /
- 1-甲基环丙烯(1-MCP)
Abstract:Objective For the purpose of developing storage and fresh-keep technology, this study is aimed to evaluate different post-harvest methods that target at the prevention of puffiness, a common physiological disorder that occurs in mature or post-harvest storage stages of citrus fruits (Citrus reticulata) which seriously affects its marketability. Method Ethylene and 1-methylcyclopropene (1-MCP) were used to treat the postharvest ‘Ponkan’ fruit, and the main quality indexes and puffing index, as well as the characteristics of albedo cell morphological and physiological changes were studied after treatment. Result (1) Ethylene treatment brought about an increase of soluble solid content during fruit storage, accelerated the decline of cell density, cellulose content, and pectin content of the albedo, while promoting an increase in lignin content and the activity of cell wall-degrading enzymes (cellulases, pectin esterases, and polygalacturonases). (2) 1-MCP treatment slowed down the decrease of albedo cell density and cellulose content, delaying the increase of lignin content and the activity of cell wall degrading enzymes (cellulase, pectin esterase and polygalacturonase), and therefore slowing down the rise of puffiness index. Conclusion Ethylene treatment accelerated the physiological and metabolic level of ‘Ponkan’ fruit during storage and aggravated the occurrence of puffiness whereas 1-MCP treatment inhibited the peel physiological and metabolic level during storage and alleviated the occurrence of puffiness. As a result, the peeling difficulty of the fruit can be controlled by ethylene or 1-MCP treatment during production. [Ch, 7 fig. 31 ref.] -
-
[1] 张世怡, 柯甫志, 赵迪, 等. 柑橘果实浮皮发生机理的研究进展[J]. 园艺学报, 2016, 43(9): 1719 − 1725. ZHANG Shiyi, KE Fuzhi, ZHAO Di, et al. Progress in studies on mechanism of puffing disorder and its regulation in citrus fruits [J]. Acta Horticulturae Sinica, 2016, 43(9): 1719 − 1725. [2] 石学根, 徐建国, 张林, 等. 温州蜜柑完熟果实的浮皮与贮藏性之间的关系[J]. 浙江农业学报, 2008, 20(4): 304 − 307. SHI Xuegeng, XU Jianguo, ZHANG Lin, et al. The relationship between peel puffing and storage of full ripe fruits of satsuma mandarin [J]. Acta Agriculturae Zhejiangensis, 2008, 20(4): 304 − 307. [3] IBANEZ A M, MARTINELLI F, REAGAN R L, et al. Transcriptome and metabolome analysis of citrus fruit to elucidate puffing disorder [J]. Plant Science, 2014, 217: 87 − 98. [4] 张天志. 內源激素变化与宽皮柑橘浮皮关系的研究[D]. 杭州: 浙江农林大学, 2017. ZHANG Tianzhi. Study on the Correlation between Endogenous Horoe and Mandarin Fruits Puffing [D]. Hangzhou: Zhejiang A&F University, 2017. [5] 张林, 柯甫志, 罗文杰, 等. 设施椪柑延后采摘对果实品质的影响[J]. 浙江农业科学, 2013(1): 30 − 32. ZHANG Lin, KE Fuzhi, LUO Wenjie, et al. Effects of delayed picking of ponkan on fruit quality [J]. Journal of Zhejiang Agricultural Sciences, 2013(1): 30 − 32. [6] 吕双双, 李天来, 吴志刚, 等. 外源乙烯对不同成熟度网纹甜瓜果实细胞壁水解酶活性的影响[J]. 西北农业学报, 2009, 18(4): 344 − 350. LÜ Shuangshuang, LI Tianlai, WU Zhigang, et al. Effect of exogenous ethylene on the activity of cell-wall hydrolases of different maturity of muskmelon [J]. Acta Agriculturae Boreali-occidentalis Sinica, 2009, 18(4): 344 − 350. [7] 蒋天梅, 殷学仁, 王平, 等. 乙烯调控非跃变型果实成熟衰老研究进展[J]. 园艺学报, 2011, 38(2): 371 − 378. JIANG Tianmei, YIN Xueren, WANG Ping, et al. Research advance in regulation of ethylene during ripening and senescence of non-climacteric fruit [J]. Acta Horticulturae Sinica, 2011, 38(2): 371 − 378. [8] GIOVANNONI J. Molecular biology of fruit maturation and ripening [J]. Annual Review of Plant Physiology and Plant Molecular Biology, 2001, 52: 725 − 749. [9] 邓丽莉, 袁梓洢, 姚世响, 等. 蜜橘乙烯利处理后果皮不同部位着色差异的研究[J]. 园艺学报, 2019, 46(5): 931 − 938. DENG Lili, YUAN Ziyi, YAO Shixiang, et al. Study on differences of coloration process in different parts of ethephon-degreened mandarin fruit [J]. Acta Horticulturae Sinica, 2019, 46(5): 931 − 938. [10] 梁颖. 变温贮藏和外源乙烯处理对柑橘果实采后品质及乙烯代谢相关基因表达的影响[D]. 武汉: 华中农业大学, 2011. LIANG Ying. Effects of Intermittent Warming and Exogenous Ethylene on the Postharvest Quality and Expression Ofethylene Related Genes in Citrus Fruit [D]. Wuhan: Huazhong Agricultural University, 2011. [11] 刘美迎. 光和外源乙烯调控葡萄果皮酚类物质合成及其机制研究[D]. 杨凌: 西北农林科技大学, 2017. LIU Meiying. Berry Skins Ethylene on Phenolics Synthesis in Grape Regulation of Light and Exogenous [D]. Yangling: Northwest A&F University, 2017. [12] 张二芳, 唐福临, 邵雅馨, 等. 1-MCP及乙烯吸收剂对水蜜桃采后生理及贮藏品质的影响[J]. 食品研究与开发, 2021, 42(23): 20 − 25. ZHANG Erfang, TANG Fulin, SHAO Yaxin, et al. Effect of 1-MCP and ethylene absorbent on the physiology and storage quality of honey peach fruit after harvest [J]. Food Research and Development, 2021, 42(23): 20 − 25. [13] 王志华, 贾朝爽, 包敖民, 等. 1-MCP对龙丰苹果常温贮藏保鲜的效应[J]. 中国果树, 2022(12): 8 − 13. WANG Zhihua, JIA Chaoshuang, BAO Aomin, et al. Effect of 1-MCP on ‘Longfeng’ apple during normal temperature storage [J]. China Fruits, 2022(12): 8 − 13. [14] RARZZAQ K, SINGH Z, KHAN A S, et al. Role of 1-MCP in regulating ‘Kensington Pride’ mango fruit softening and ripening [J]. Plant Growth Reguation, 2016, 78(3): 401 − 411. [15] 杜欣欣, 郭晓萌, 韩冬梅, 等. 基于电子鼻分析1-MCP处理对青柠檬贮藏效果的影响[J]. 保鲜与加工, 2022, 22(1): 16 − 24. DU Xinxin, GUO Xiaomeng, HAN Dongmei, et al. Effect of 1-MCP treatment on green lemon storage based on electronic nose analysis [J]. Storage and Process, 2022, 22(1): 16 − 24. [16] 林旭东, 沈波涛, 朱麟, 等. MAP结合1-MCP处理对“红美人”柑橘冷藏品质的影响[J]. 保鲜与加工, 2020, 20(2): 74 − 78. LIN Xudong, SHEN Botao, ZHU Lin, et al. Effect of different modified atmosphere packagings and 1-MCP treatment on quality of ‘Hongmeiren’ citrus during cold storage [J]. Storage and Process, 2020, 20(2): 74 − 78. [17] 王长锋. 储藏条件对柑橘果实品质的影响[D]. 湘潭: 湘潭大学, 2012. WANG Changfeng. The Effect of Storage Conditions on the Citrus Fruit Quality [D]. Xiangtan: Xiangtan University, 2012. [18] 李合生. 现代植物生理学[M]. 北京: 高等教育出版社, 2002: 194 − 197. LI Hesheng. Modern Plant Physiology [M]. Beijing: Higher Education Press, 2002: 194 − 197. [19] 张世怡. ‘宫川’温州蜜柑浮皮的细胞学和转录组学研究[D]. 杭州: 浙江农林大学, 2018. ZHANG Shiyi. Cytopathology and Transcriptome Analysis of Puffing in Satsuma Mandarin ‘Miyagawa’ [D]. Hangzhou: Zhejiang A&F University, 2018. [20] 曹建康, 姜微波, 赵玉梅. 果蔬采后生理生化实验指导[M]. 北京: 中国轻工业出版社, 2007. CAO Jiankang, JIANG Weibo, ZHAO Yumei. Guidance of Postharvest Physiological and Biochemical Experiments of Fruits and Vegetables[M]. Beijing: China Light Industry Press, 2007. [21] 陈金印. 美味猕猴桃‘金魁’果实后熟软化机理及其调控技术研究[D]. 长沙: 湖南农业大学, 2004. CHEN Jinyin. Study on the Post-ripening Softening Mechanism and its Regulation Technology of Delicious Kiwifruit ‘Jinkui’ Fruit [D]. Changsha: Hunan Agricultural University, 2004. [22] 梁森苗, 王伟, 戚行江, 等. ‘早佳’杨梅的果实品质形成规律[J]. 浙江农林大学学报, 2017, 34(3): 559 − 564. LIANG Senmiao, WANG Wei, QI Xingjiang, et al. Fruit quality of ‘Zaojia’ red bayberry fruits [J]. Journal of Zhejiang A&F University, 2017, 34(3): 559 − 564. [23] 刘光财. 1-MCP和乙烯利对菠萝蜜果实淀粉降解的影响[D]. 湛江: 广东海洋大学, 2020. LIU Guangcai. Effects of 1-MCP and Ethephon on Degradation of Jackfruit Fruit Starch [D]. Zhanjiang: Guangdong Ocean University, 2020. [24] 秦畅, 李丹, 赵韩栋, 等. 外源乙烯处理对黄冠梨果皮褐变和货架期品质的影响[J]. 农业工程学报, 2022, 38(6): 312 − 318. QIN Chang, LI Dan, ZHAO Handong, et al. Effects of exogenous ethylene treatment on the peel browning and shelf life quality of Huangguan pears [J]. Transactions of the Chinese Society of Agricultural Engineering, 2022, 38(6): 312 − 318. [25] 梁芳菲, 王小容, 邓丽莉, 等. 采后柑橘果实糖酸代谢研究进展[J]. 食品与发酵工业, 2018, 44(10): 268 − 274. LIANG Fangfei, WANG Xiaorong, DENG Lili, et al. Research advances in sugar and acid metabolism of postharvest citrus fruit [J]. Food and Fermentation Industries, 2018, 44(10): 268 − 274. [26] 赵迪. 温州蜜柑‘宫川’浮皮性状形成的机理研究[D]. 杭州: 浙江农林大学, 2016. ZHAO Di. Study on the Mechanism of Puffing Formation in Satsuma Mandarin ‘Miyagawa’ [D]. Hangzhou: Zhejiang A&F University, 2016. [27] 郑永华, 李三玉, 席玙芳. 枇杷冷藏过程中果肉木质化与细胞壁物质变化的关系[J]. 植物生理学报, 2000, 26(4): 306 − 310. ZHENG Yonghua, LI Sanyu, XI Yufang. Changes of cell wall substances in relation to flesh woodiness in cold stored loquat fruits [J]. Physiology and Molecular Biology of Plants, 2000, 26(4): 306 − 310. [28] 韩卫娟, 刁松锋, 张悦, 等. 无核君迁子果实发育成熟过程中生理指标变化规律[J]. 浙江农林大学学报, 2022, 39(3): 554 − 561. HAN Weijuan, DIAO Songfeng, ZHANG Yue, et al. Variation patterns of physiological indices of seedless Diospyros lotus during fruit development and ripening [J]. Journal of Zhejiang A&F University, 2022, 39(3): 554 − 561. [29] 薛维文, 周显芳, 张昭其, 等. 果蔬采后木质素积累及其调控对品质的影响研究进展[J]. 园艺学报, 2022, 49(9): 2023 − 2036. XUE Weiwen, ZHOU Xianfang, ZHANG Zhaoqi, et al. Advances in lignin accumulation and lts regulation on the quality of postharvest fruit and vegetables [J]. Acta Horticulturae Sinica, 2022, 49(9): 2023 − 2036. [30] 朱婉彤, 冯作山, 白羽嘉, 等. 乙烯和1-MCP对伯谢克辛甜瓜果实软化及细胞壁降解的影响[J]. 现代食品科技, 2019, 35(12): 94 − 101. ZHU Wantong, FENG Zuoshan, BAI Yujia, et al. Effects of ethylene and 1-MCP treatments on softening and cell wall degradation of bethekxin melon fruit [J]. Modern Food Science and Technology, 2019, 35(12): 94 − 101. [31] 谢国芳, 费颖, 柴裕清, 等. 1-MCP对3种鲜食菜豆采后木质纤维化的影响[J]. 中国食品学报, 2020, 20(4): 206 − 214. XIE Guofang, FEI Ying, CHAI Yuqing, et al. Effect of 1-MCP on lignocellulose of three kinds of fresh common bean in postharvest [J]. Journal of Chinese Institute of Food Science and Technology, 2020, 20(4): 206 − 214. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20230422






 下载:
下载: