-
苹果小吉丁虫Agrilus mali属鞘翅目Coleoptera吉丁虫科Buprestidae,是蔷薇科Rosaceae苹果属Malus果树一种重要蛀干害虫。其幼虫在枝干皮层内蛀食,破坏水分和养分输导组织,导致枝条枯死,危害严重时造成果树整株枯死。2013年,苹果小吉丁虫被列为全国林业危险性有害生物。1999年,苹果小吉丁虫在新疆天山伊犁河谷野果林中被发现暴发成灾[1],伊犁野果林中最主要的建群种为新疆野苹果Malus sieversii,又名塞威氏苹果,为中国珍稀濒危二级重点保护植物[2-4]。近20 a来,因苹果小吉丁虫、苹果腐烂病菌Valsa mali等有害生物危害,导致新疆伊犁河谷野苹果林持续衰退。由于苹果小吉丁虫危害具有隐蔽性,虫态发育不整齐,加之野苹果分布区地形复杂,常规的防治方法很难操作,且效果不佳。苹果小吉丁虫现有监测方法主要是采用设置固定样地,进行人工剥树皮统计虫口密度,费工费时。因此,探索可操作性和效果更佳的防治与监测方法,是当前迫切需要解决的问题。开发植物源性引诱剂,是开展野苹果林苹果小吉丁虫监测与防治的新策略。外界条件作用诱导寄主产生的挥发物,在昆虫化学通信中发挥着重要作用,能影响植食性昆虫寻找和选择寄主、取食、产卵等多种生理过程[5-7]。同时,寄主植物挥发物在植物间接产生防御过程中,可能也充当重要角色[8-9]。已有众多研究报道,由于虫害诱导导致植物挥发性物质发生变化[10-12]。与健康植株相比,被植食性昆虫取食或产卵危害后,植株释放的挥发物在种类和含量上都有很大差异[13-15]。一般植物受害后挥发物的种类会增加,挥发性物质释放量往往高于受害前,因此更容易被植食性昆虫远距离识别[16-17]。榆树Ulmus pumila在受榆紫叶甲Ambrostoma quadriimpressum成虫取食危害后,9 种物质的含量与健康植株相比有显著差异,经触角电位和行为反应测定,其中α-法尼烯、芳樟醇、顺-3-己烯醇、石竹烯对榆紫叶甲雌雄成虫具有引诱活性[18]。受白蜡窄吉丁Agrilus planipennis危害的水曲柳Fraxinus mandshurica释放的挥发物对白蜡窄吉丁雌成虫具有显著引诱作用,雌成虫对芳樟醇的触角电位(electroantennogram, EAG)反应值要大于雄成虫,而雄成虫对己醛、(E)-2-己烯醛、顺-3-己烯醇、3-甲基丁醛肟、2-甲基丁醛肟和乙酸己酯EAG反应值要大于雌成虫[8]。目前,国内外众多研究人员先后研究昆虫与植物之间化学通信关系,解析了昆虫与植物互作机制,研究出害虫监测与防控技术措施。王明等[19]研究发现:机械损伤、茉莉酸甲酯处理及害虫处理等外界因素会导致新疆野苹果树体内挥发性化合物组分,在含量和种类上发生明显改变。在野果林中,苹果小吉丁虫与寄主野苹果化学通信关系研究尚不完善。本研究探讨病虫害危害诱导野苹果产生挥发物对苹果小吉丁虫嗅觉与行为反应的影响,以期筛选出对苹果小吉丁虫具有引诱作用的植物源引诱剂,为苹果小吉丁虫防治与监测工作提供理论支撑。
-
样地位于新疆维吾尔自治区新源县阿勒玛勒乡、巩留县库尔德宁镇野苹果林中。阿勒玛勒乡调查样地海拔1 296.0~1 395.0 m,气候湿润,冬暖夏凉,年平均气温7.7 ℃,1月平均气温−8.1 ℃,7月平均气温20.4 ℃,降水量580 mm,冬季积雪厚度约1.0 m。冬季逆温现象明显。土壤为山地黑棕色野果林土类,具有优越的自然生态条件。植被以野苹果为主,树龄30~55 a,树高6~12 m,胸径17~28 cm,调查样地总面积在6.7 hm2以上。库尔德宁镇调查样地海拔1 237.0~1 380.0 m,全年平均气温7.4 ℃,最高气温37.0~39.0 ℃,极端最低气温−36.0~−38.0 ℃,无霜期150 d左右,年降水量200~780 mm。植被以野苹果为主,树龄25~40 a,树高3~12 m,胸径8~35 cm,调查样地总面积在10 hm2以上。其中健康树选在新源县野果林资源圃,苹果小吉丁虫危害树选在72团8连,苹果腐烂病菌危害树选在新源县野果林资源圃。供试昆虫:从新疆维吾尔自治区新源县、巩留县野苹果林中,采集受苹果小吉丁虫危害野果林枝条带回室内,罩笼自然羽化获得。
-
TA吸附管(珀金埃尔默股份有限公司,美国),玻璃干燥塔,活性炭,烤箱袋(雷诺兹消费品公司,美国),硅胶管。
-
QC-1B气体采样仪(北京市劳动保护研究所),TurboMatrix 650全自动热脱附仪(珀金埃尔默股份有限公司, 美国),7890A Network气相色谱/5975C Network质谱联用仪(安捷伦科技有限公司, 美国),配有NIST 2.0数据处理系统(安捷伦科技有限公司,美国)。触角电位仪(Electroantennogram,EAG)由荷兰Syntech公司生产,主要包括MP-15微动操作台(Syntech公司,荷兰),CS-55刺激控制器(Syntech公司,荷兰),IDAC-4数据采集控制器(Syntech公司,荷兰),配有EAGPro软件,PSM4-150四臂嗅觉仪(南京普森仪器设备有限公司)。
-
液体石蜡(西陇科学股份有限公司),触角电位测试标准品见表1。
表 1 触角电位测定实验所用标准化合物纯度及来源
Table 1. Source and purity of standard chemicals used in EAG testing
标准化合物 质量分数/ % 来源 标准化合物 质量分数/ % 来源 (+)-α-蒎烯 (+)-α-pinene 95 梯希爱 癸醛 decanal 97 阿达玛斯 (−)-α-蒎烯 (−)-α-pinene 98 霍尼韦尔 (+)-柠檬烯 (+)-limonene 99 梯希爱 α-蒎烯 α-pinene 98 奥德里奇 2-甲基丙烯醛 methacrolein 95 阿达玛斯 (+)-β-蒎烯 (+)-β-pinene 95 霍尼韦尔 壬醛 nonanal 95 奥德里奇 丙烯酸丁酯 butyl acrylate 99 奥德里奇 十五烷 pentadecane 99 安谱 乙酸叶醇酯 leaf acetate 97 梯希爱 (−)-β-蒎烯 (−)-β-pinene 99 霍尼韦尔 苯甲醛 benzaldehyde 99 阿达玛斯 顺-3-己烯醇 leaf alcohol 98 奥德里奇 -
动态顶空采样法气路连接方法:首先在采集袋上下斜对角开2个小孔,与硅胶管相连接,并用胶带缠紧。将待测野苹果枝条用采集袋笼罩,釆集袋封口处与待测枝条捆绑处铺垫1层脱脂棉,并用棉线绳捆严实。先利用大气采样仪将袋内存余空气抽干。用硅胶管将玻璃干燥塔(内装活性炭)一端与采集袋下口硅胶管相连,另一端与大气采样仪出气口相连。然后用大气采样仪经玻璃干燥塔将采集袋充气充满。按照吸附管气流箭头方向,使用硅胶管将吸附管与采集袋相连,并与大气采样仪进气口端相连,形成闭合回路。对待测枝条以100 mL·min−1的速率进行抽提采样。采样时间持续30 min。将直径为3~5 cm的枝干,截为30 cm木段,将4根木段放入采集袋内,采用同样的方法搜集枝干挥发物。分别收集健康树、苹果小吉丁虫危害、苹果腐烂病菌危害树枝条和枝干挥发物,以空白作对照,每个处理重复3次[20]。利用气相色谱-质谱联用仪(GC-MS)分析测试吸附管内寄主挥发物成分。
-
全自动热脱附仪(Auto Thermal Desorber, ATD)工作条件:一级热脱附温度260 ℃,冷阱温度为−30 ℃,保持3 min。二级冷阱温度为300 ℃,保持5 min,四通阀温度230 ℃,传输线250 ℃。气谱条件:DB-5ms色谱柱毛细柱 (60 m × 0.25 mm×0.25 μm,安捷伦科技有限公司,美国); 升温程序: 40 ℃ 保持 2 min,以 6 ℃·min−1升至130 ℃,再以 8 ℃·min−1升至280 ℃保持5 min。载气为氦气,流速0.4 mL·min−1。进样器温度250 ℃;分流比为10∶1进样。以色谱峰保留时间定性,以峰面积相对定量计算。质谱条件:电离方式EI,电子能量70 eV,离子源温度250 ℃,传输线温度250 ℃。扫描质荷比范围(m/z) 45~500。
-
将苹果小吉丁虫的头剪下,并将鞭节第9末节顶端用导电胶(Spectra 360, 美国派克实验室公司)固定于“Y”形金属电极测定电极上,头部连接参比电极。电极插入微动操作台探头内并连接Syntech数据采集接口板(Type IDAC-4);同时连接计算机通过EAGPro软件记录测定值。通过分析测定,筛选出13个主要寄主挥发物,选取标样,由液体石蜡溶解稀释为10−1、10−2、10−3、10−4、10−5和10−6 g·g−1 6个质量分数梯度。将一小片滤纸4折成长方形,并放入巴斯德管基部,在滤纸上滴20 μL待测化学标样,并等待其被滤纸完全吸收。以10−3 g·g−1的顺-3-己烯醇作为标准刺激物,液体石蜡的刺激作为对照组对触角进行刺激。每次刺激时,将巴斯德管端部接入由CS-55刺激控制器产生的每次持续1 s的刺激气流气路管,使得刺激气流在混合管中与正常气流混合,作用于触角。每种物质的每轮质量分数梯度EAG刺激试验按以下顺序进行:液体石蜡、标准物的刺激、10−6~10−1 g·g−1的标样、标准物的刺激、液体石蜡。每次刺激之间,触角有1 min的时间间隔来恢复。每种物质的质量分数梯度EAG分别在雌雄成虫触角测试,且至少重复5次。为准确量化EAG反应,每次刺激选取触角产生的第1个反应峰值作为有效值[20]。
-
使用试验中相同的挥发物标样,溶于液体石蜡中,以10−1 g·g−1的质量分数用于测定苹果小吉丁虫对野苹果树的挥发物的行为选择。使用4臂嗅觉仪作为行为测定仪。在每臂的端部各连接1个梨形玻璃瓶陷阱,瓶内随机放入浸润待测标样或液体石蜡的滤纸,其中选择1个梨形玻璃瓶陷阱作为测试处理瓶,其余3个作为对照瓶。梨形瓶另一端连接水过滤的空气、空气流量计与活性炭。4臂中均匀一致地持续通过流速为200 mL·min−1气体。在嗅觉仪中央放入1只饥饿24 h苹果小吉丁虫,稳定后开始计时,每次试验持续观察15 min。当苹果小吉丁虫进入陷阱或走入梨形瓶口的位置则记为有效反应,其余则记为无反应。每次试验完成后,将苹果小吉丁虫从嗅觉仪中移走,将刺激源移走,并将行为仪空吹再进行下1个重复;每个重复测定结束后,用无水乙醇擦拭测试区及梨形瓶,并将擦拭过梨形瓶放入180 ℃烘箱中,15 min干燥清洁。行为学实验在试验室条件下进行:温度为24~26 ℃,相对湿度为40%±10%。每种挥发物标样分别测试雌雄成虫各20只,重复3次,计算反应率、选择反应率和选择系数[21]。反应率=(味源管中虫数+对照管中虫数)/测试总虫数×100%。选择反应率=味源臂试虫数/(味源臂试虫数+对照臂试虫数)×100%。选择系数=(味源管中虫数−对照管中虫数)/(味源管中虫数+对照管中虫数)。其中:选择系数大于0,表示试虫对味源物质有趋性,数值越大,表示趋性越强,最大值为1;选择系数若小于0,则表示试虫对味源有负趋性(即忌避性)。
-
①野苹果挥发物数据处理方法。谱图检索及成分鉴定由ATD-GC/MS操作得到各样品的质谱相对丰度图及总离子流图(total ion current,TIC)。对 TIC 图中各有效峰代表的化学信息,利用专业检索软件TurboMass 5.4.2和标准谱库 NIST05,结合经典气相色谱保留时间数据和相关化学经验,鉴定野苹果枝条和枝干挥发物组分中的化学成分,并用峰面积归一化法计算各化合物在总挥发性组分中的相对百分含量。②触角电位计算方法。每个重复内的EAG反应值计算公式如下:R=(T−C)/(D−C),其中:R为苹果小吉丁虫触角对样品EAG反应相对值,T为单次待测标样所测得的EAG反应值(mV),C为同一待测标样该轮内对照组液体石蜡2次所测得的EAG反应值的平均值(mV),D为同一待测标样该轮内标准物2次所测得的EAG反应值的平均值(mV)[20]。
不同物质、不同质量分数之间的EAG反应值由双因素方差分析(Two-way ANOVA)以及多重比较进行统计计算和对比。
-
收集不同危害条件下野苹果枝条主要挥发物,利用GC-MS分析鉴定,共搜集到挥发性化合物31种,其中从健康植株枝条中搜集到挥发物14种,从苹果小吉丁虫危害枝条中搜集到挥发物24种,从苹果腐烂病菌危害枝条中搜集到挥发物21种。搜集到的31种挥发物可分为8类,包括醇类2种,脂类5种,醛类7种,烷烃类10种,烯烃类1种,酮类2种,萜类3种,其他类1种(表2)。
表 2 不同危害条件下野苹果枝条和枝干主要挥发物成分及相对含量
Table 2. Composition and relative contents of main volatiles released from the branch and limb of the wild apple in different damaged states
类别 化合物名称 CAS号 枝条挥发物相对含量/% 枝干挥发物相对含量/% 健康树 受苹果小吉
丁虫危害受腐烂
病菌危害健康树 受苹果小吉
丁虫危害受腐烂
病菌危害醇类alcohols 顺-3-己烯醇 (Z)-3-hexenol 928-96-1 − 1.82 0.90 2.46 6.70 1.67 丁烯醇 2-buten-1-ol 6117-91-5 1.62 0.61 − − − − 1-戊烯-3-醇 1-penten-3-ol 616-25-1 − − − − 1.00 − 顺-2-己烯-1-醇 (Z)-2-hexenol 928-94-9 − − − 11.86 − 3-辛烯-2-醇 3-octen-2-ol 76649-14-4 − − − − 0.77 2.86 脂类esters 丙酸丁酯 butyl propionate 590-01-2 − 2.18 3.29 − − 1.50 丁酸丁酯 butyl butyrate 109-21-7 − 0.93 2.44 − 2.53 − 丙烯酸丁酯 butyl acrylate 141-32-2 − − 16.36 − − 19.59 梨醇酯 prenyl acetate 1191-16-8 − 0.75 0.75 − 1.65 − 乙酸叶醇酯 leaf acetate 3681-71-8 − 7.00 4.68 − 10.63 − 2-甲基丁酸乙酯 ethyl 2-methylbutyrate 7452-79-1 − − − − 2.97 − 丁酸烯丙酯 allyl butanoate 2051-78-7 − − − − 1.18 0.85 醛类aldehydes 顺-3-己烯醛 (Z)-3-hexenal 6789-80-6 − 3.70 − − − 1.02 己醛 hexanal 66-25-1 − 1.21 1.49 4.60 0.67 13.40 2-甲基丙烯醛 methacrolein 78-85-3 5.21 0.77 − − − − 癸醛 decanal 112-31-2 − 0.90 − − 1.29 − 壬醛 nonanal 124-19-6 − 2.00 − − − − 苯甲醛 benzaldehyde 100-52-7 − 1.30 3.09 − 2.49 1.34 青叶醛 leaf aldehyde 6728-26-3 2.31 − − − − − 丙烯醛 acrolein 107-02-8 − − − 10.16 − 7.12 2-甲基-2-戊烯醛 2-methyl-2-pentenal 623-36-9 − − − − 1.42 − 烷烃类alkanes 2-甲基庚烷 2-methylheptane 592-27-8 − 6.29 0.75 − − − 2,4,4-三甲基-己烷 2,4,4-trimethylhexane 16747-30-1 − 0.68 − − − − 2,4-二甲基庚烷 2,4-dimethylheptane 2213-23-2 − 20.22 − − − − 十五烷 pentadecane 629-62-9 0.52 2.04 6.42 − 1.85 0.72 十七烷 heptadecane 629-78-7 1.64 1.09 2.61 − 3.84 1.71 3,7-二甲基癸烷 3,7-dimethyldecane 17312-54-8 1.25 − 3.42 − − − 二十烷 eicosane 112-95-8 1.51 2.69 4.74 − 2.57 4.92 二十一烷 heneicosane 629-94-7 1.51 0.63 1.34 − − − 二十四烷 tetracosane 646-31-1 1.87 − − − − − 环庚烷 cycloheptane 291-64-5 1.14 − − − − − 烯烃类alkenes 环庚三烯 cyclohetatriene 544-25-2 16.53 6.64 4.67 4.95 1.32 − 酮类ketones 环己酮 cyclohexanone 108-94-1 45.45 2.83 7.39 17.63 − 6.22 苯乙酮 acetophenone 98-86-2 − − 0.94 − − − 2-癸酮 2-decanone 693-54-9 − − − − 0.55 − 萜类terpendoids α-蒎烯 α-pinene 80-56-8 0.86 0.81 0.98 9.85 10.96 3.68 (+)-α蒎烯 (+)-α-pinene 7785-70-8 − − 2.42 − − − (−)-α-蒎烯 (−)-α-pinene 7785-26-4 − − − 1.66 8.96 1.23 (+)-柠檬烯 (+)-limonene 5989-27-5 − 0.76 7.74 1.11 − − 双戊烯 dipentene 138-86-3 − − − − − 1.14 β-蒎烯 β-pinene 127-91-3 − − − 4.92 1.68 1.04 莰烯 camphene 79-92-5 − − − 0.47 2.17 − (+)-香橙烯 (+)-aromandendrene 489-39-4 − − − − 0.85 − 醚类ethers 苯甲醚 anisole 100-66-3 − − − − 3.18 1.56 仲丁醚 isobutyl ether 628-55-7 − − − 1.20 − − 其他 甘菊蓝 azulene 275-51-4 3.43 0.94 2.12 2.68 0.84 2.16 说明:−表示GC-MS没有检测鉴别出该化合物 健康植株枝条特有的挥发物有3种,分别为青叶醛、二十四烷、环庚烷。苹果小吉丁虫危害枝条特有挥发物有5种,分别为顺-3-己烯醛、癸醛、壬醛、2,4,4-三甲基-己烷、2,4-二甲基庚烷。苹果腐烂病菌危害枝条特有挥发物有3种,分别为丙烯酸丁酯、苯乙酮、(+)-α蒎烯。在健康树枝条和受苹果小吉丁虫危害枝条共有,而受苹果腐烂病菌危害枝条中没有采集到的挥发物有2种,分别为丁烯醇、2-甲基丙烯醛。在健康树枝条和受苹果腐烂病菌危害枝条共有,而受苹果小吉丁虫危害枝条没有采集到挥发物有1种,为3,7-二甲基癸烷。在受苹果小吉丁虫和苹果腐烂病菌危害枝条共有,而健康枝条中没有采集到挥发物有9 种,分别为顺-3-己烯醇、丙酸丁酯、梨醇酯、乙酸叶醇酯、丁酸丁酯、己醛、苯甲醛、2-甲基庚烷、(+)-柠檬烯。3种危害条件下野苹果枝条共有挥发物为8种,分别为十五烷、十七烷、二十烷、二十一烷、环庚三烯、环己酮、α-蒎烯、甘菊蓝。
从挥发物相对含量可以看出:3种处理之间挥发物相对含量存在显著差异。与健康植株枝条相比,受苹果小吉丁虫危害枝条释放的挥发物种类增加的为顺-3-己烯醇、丙酸丁酯、丁酸丁酯、梨醇酯、乙酸叶醇酯、顺-3-己烯醛、己醛、癸醛、壬醛、苯甲醛、2-甲基庚烷、2,4,4-三甲基-己烷、2,4-二甲基庚烷、(+)-柠檬烯等14种化合物,十五烷、二十烷相对含量增加,丁烯醇、2-甲基丙烯醛、十七烷、二十一烷、环庚三烯、环己酮、α-蒎烯、甘菊蓝等8种挥发物有所降低,青叶醛、3,7-二甲基癸烷、二十四烷、环庚烷未采集到。受苹果腐烂病菌危害枝条挥发物种类增加的为顺-3-己烯醇、丙酸丁酯、丁酸丁酯、丙烯酸丁酯、梨醇酯、乙酸叶醇酯、己醛、苯甲醛、2-甲基庚烷、苯乙酮、(+)-α蒎烯、(+)-柠檬烯等12种挥发物,十五烷、十七烷、3,7-二甲基癸烷,二十烷、α-蒎烯相对含量增加,二十一烷、环己酮、环庚三烯、甘菊蓝减少,丁烯醇、2-甲基丙烯醛、青叶醛、二十四烷、环庚烷未采集到。总体上,与健康树枝条挥发物种类和相对含量相比较,受苹果小吉丁虫和苹果腐烂病菌危害枝条挥发物种类增加的为顺-3-己烯醇、丙酸丁酯、丁酸丁酯、丙烯酸丁酯、梨醇酯、乙酸叶醇酯、顺-3-己烯醛、己醛、癸醛、壬醛、苯甲醛、2-甲基庚烷、2,4,4-三甲基-己烷、2,4-二甲基庚烷、苯乙酮、(+)-α蒎烯、(+)-柠檬烯等。
-
收集不同危害条件下野苹果枝干主要挥发物,并进行GC-MS分析鉴定。共搜集到挥发性化合物32种,其中从健康植株枝干中搜集到挥发物12种,从苹果小吉丁虫危害枝干中搜集到挥发物25种,从苹果腐烂病菌危害枝干中搜集到挥发物19种。搜集到的32种挥发物可分为9类,包括醇类3种,脂类7种,醛类6种,烷烃类3种,烯烃类1种,酮类2种,萜类7种,醚类2种,其他类1种(表2)。
健康植株枝干特有的挥发物有2种,分别为(+)-柠檬烯、仲丁醚。苹果小吉丁虫危害枝干特有挥发物有10种,分别为1-戊烯-3-醇、顺-2-己烯-1-醇、丁酸丁酯、梨醇酯、乙酸叶醇酯、2-甲基丁酸乙酯、癸醛、2-甲基-2-戊烯醛、2-癸酮、(+)-香橙烯。苹果腐烂病菌危害枝干特有挥发物有4种,分别为丙酸丁酯、丙烯酸丁酯、顺-3-己烯醛、双戊烯。健康树枝干和受苹果小吉丁虫危害枝干共有,而受苹果腐烂病菌危害枝干中没有采集到的挥发物有2种,分别为环庚三烯、莰烯。在健康树枝干和受苹果腐烂病菌危害枝干共有,而受苹果小吉丁虫危害枝干中没有采集到的挥发物有2种,分别为丙烯醛、环己酮。受苹果小吉丁虫危害枝干和受苹果腐烂病菌危害枝干共有,而健康树枝条没有采集到的挥发物有7种,分别为3-辛烯-2-醇、丁酸烯丙酯、苯甲醛、十五烷、十七烷、二十烷、苯甲醚。3种危害条件下野苹果枝干共有挥发物为6种,分别为顺-3-己烯醇、己醛、α-蒎烯、(−)-α-蒎烯、β-蒎烯、甘菊蓝。
3种处理之间野苹果枝干挥发物相对含量存在显著差异。与健康植株枝干释放的挥发物相比,受苹果小吉丁虫危害枝干释放的挥发物种类增加的为1-戊烯-3-醇、顺-2-己烯-1-醇、3-辛烯-2-醇、丁酸丁酯、梨醇酯、2-甲基丁酸乙酯、丁酸烯丙酯、乙酸叶醇酯、癸醛、苯甲醛、2-甲基-2-戊烯醛、十五烷、十七烷、二十烷、2-癸酮、(+)-香橙烯、苯甲醚;顺-3-己烯醇、α-蒎烯、(−)-α-蒎烯、莰烯相对含量增加,己醛、环庚三烯、β-蒎烯、甘菊蓝相对含量有所降低,丙烯醛、环己酮、(+)-柠檬烯、仲丁醚未采集到。受苹果腐烂病菌危害枝干种类增加的为3-辛烯-2-醇、丙酸丁酯、丙烯酸丁酯、丁酸烯丙酯、顺-3-己烯醛、苯甲醛、十五烷、十七烷、二十烷、双戊烯、苯甲醚等11种化合物,己醛相对含量增加,顺-3-己烯醇、丙烯醛、环己酮、α-蒎烯、(−)-α-蒎烯、β-蒎烯、甘菊蓝相对含量降低。总体上,与健康树枝干挥发物种类和相对含量相比较,受苹果小吉丁虫和苹果腐烂病菌危害枝干挥发物种类增加的为1-戊烯-3-醇、顺-2-己烯-1-醇、3-辛烯-2-醇、丙酸丁酯、丁酸丁酯、丙烯酸丁酯、梨醇酯、乙酸叶醇酯、2-甲基丁酸乙酯、丁酸烯丙酯、顺-3-己烯醛、癸醛、苯甲醛、2-甲基-2-戊烯醛、十五烷、十七烷、二十烷、2-癸酮、双戊烯、(+)-香橙烯、苯甲醚等21种。
-
不同危害条件下野苹果枝条与枝干主要挥发物成分种类不同。健康野苹果枝条和健康野苹果枝干共有的挥发物3种,分别为环庚三烯、α-蒎烯、甘菊蓝。苹果小吉丁虫危害野苹果枝条及危害枝干共有挥发物13种,分别顺-3-己烯醇、丁酸丁酯、梨醇酯、乙酸叶醇酯、己醛、癸醛、苯甲醛、十五烷、十七烷、二十烷、环庚三烯、α-蒎烯、甘菊蓝。由表2可以看出:受苹果小吉丁虫危害的枝干挥发物中,顺-3-己烯醇、丁酸丁脂、梨醇酯、乙酸叶醇酯、癸醛、苯甲醛、十七烷、α-蒎烯等相对含量要高于受苹果小吉丁虫危害枝条挥发物相对含量。
苹果腐烂病菌危害的枝条和苹果腐烂病菌危害的枝干共有挥发物为11种,分别为顺-3-己烯醇、丙酸丁酯、丙烯酸丁酯、己醛、苯甲醛、十五烷、十七烷、二十烷、环己酮、α-蒎烯、甘菊蓝。由表2可以看出:苹果腐烂病菌危害的枝条和苹果腐烂病菌危害的枝干共有挥发物相对含量丙酸丁酯、丙烯酸丁酯、己醛、苯甲醛、十五烷、α-蒎烯等6种差异较大外,其他几种挥发物相对含量差别不大。
-
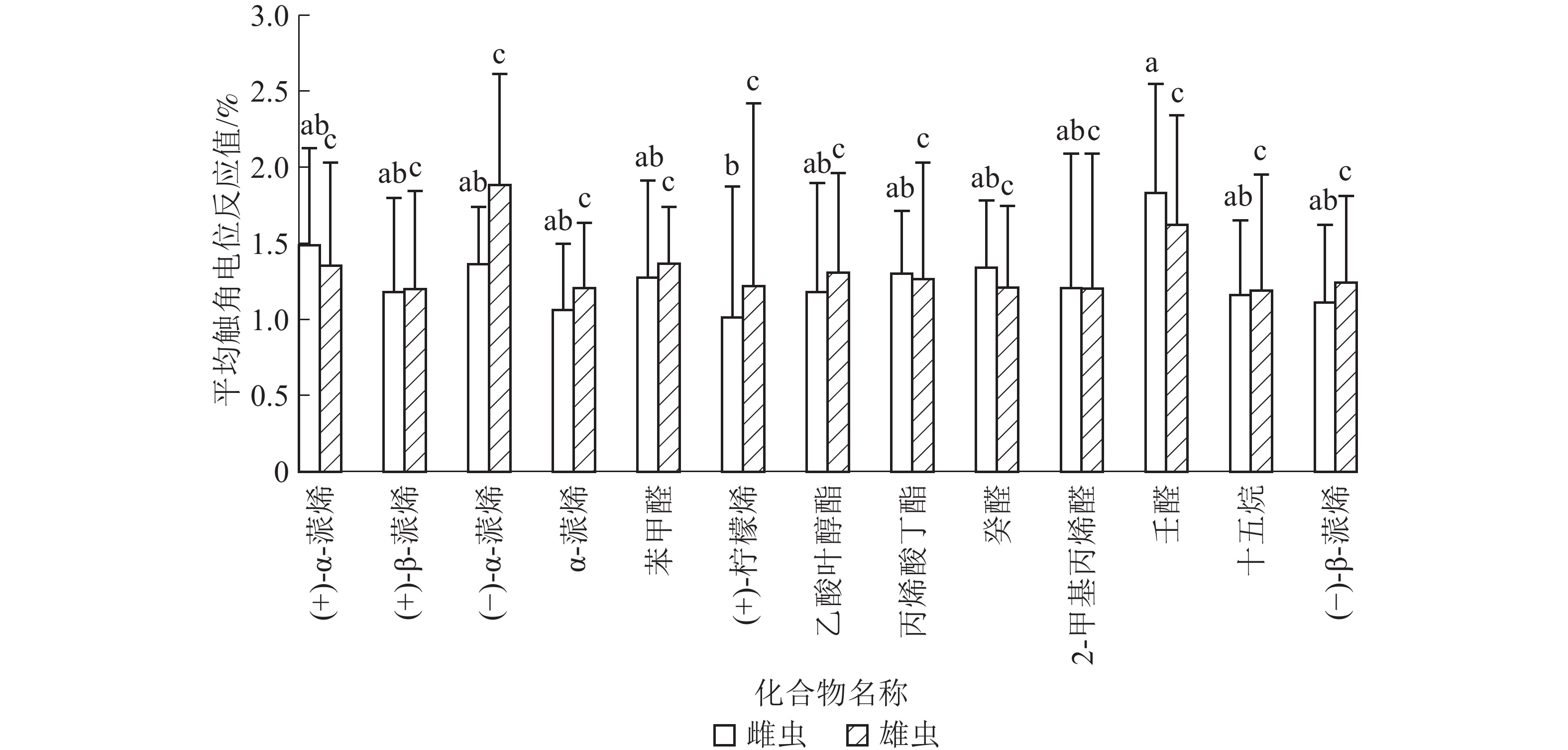
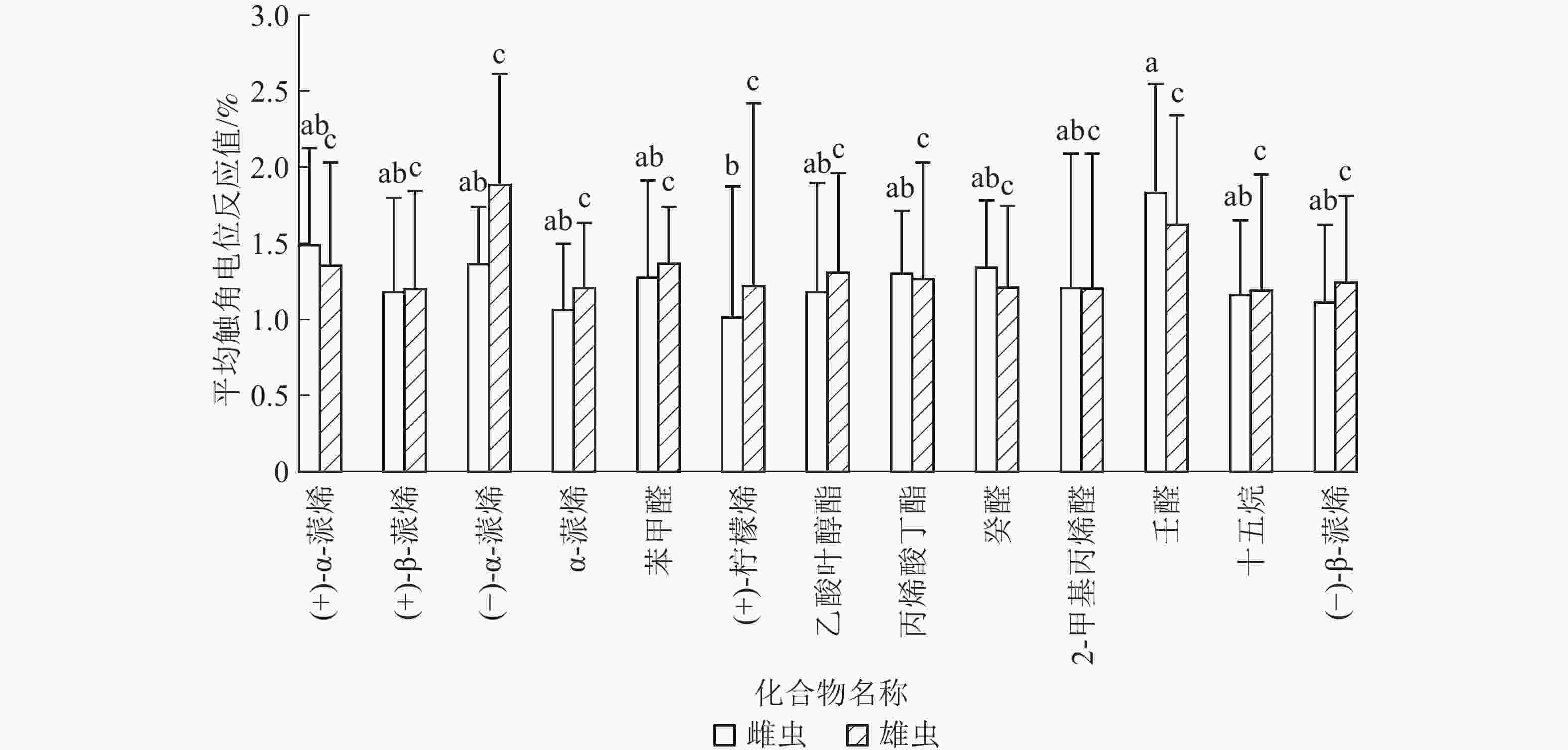
13种寄主挥发物标样在10−1 g·g−1的质量分数下,刺激苹果小吉丁虫雌雄成虫触角,均产生较大的EAG反应值,其中雌虫触角对壬醛产生的EAG反应值最大,且与(+)-柠檬烯差异显著;雄虫触角对(−)-α-蒎烯产生的EAG反应值最大。雌虫触角对壬醛、(+)-α-蒎烯、丙烯酸丁酯、癸醛、2-甲基丙烯醛等5种化合物产生的EAG反应值大于雄虫触角所产生的反应值。雄虫触角对 (−)-α-蒎烯、α-蒎烯、(+)-β-蒎烯、苯甲醛、(+)-柠檬烯、十五烷、乙酸叶醇酯、(−)-β-蒎烯等8种化合物产生的EAG反应值大于雌虫触角所产生的反应值。通过双因素方差分析,雌雄虫对不同化合物标样在在10−1 g·g−1质量分数下产生的EAG反应值,差异不显著(图1)。
-
苹果小吉丁虫雌虫和雄虫对寄主挥发物标样质量分数在10−6~10−1 g·g−1范围内,随着质量分数的升高,雌虫和雄虫触角受刺激,EAG反应值逐渐增大。不同物质在10−1 g·g−1质量分数下刺激苹果小吉丁虫雌虫和雄虫触角均产生最大的EAG反应。在10−1 g·g−1下,壬醛、(+)-α-蒎烯、(−)-α-蒎烯刺激苹果小吉丁虫雌虫触角依次产生较大的EAG;(−)-α-蒎烯、壬醛、苯甲醛刺激苹果小吉丁虫雄虫触角依次产生较大的EAG。在测定的13种植物挥发物标样中,α-蒎烯 、壬醛刺激雄虫触角,随着质量分数升高,EAG反应具有显著差异;其他11种物质刺激雄虫触角,随着质量分数升高,EAG反应差异不显著;(+)-α-蒎烯、(−)-α-蒎烯、壬醛刺激雌虫触角,随着质量分数升高,EAG反应具有显著差异,其他10种物质刺激雌虫触角,随着质量分数升高,EAG反应差异不显著。
对不同物质不同质量分数EAG反应进行双因素方差分析。结果显示:雌虫和雄虫触角对不同种类物质和不同质量分数化合物所产生的EAG反应具有显著差异。13种物质的低质量分数(10−3~10−6 g·g−1)刺激苹果小吉丁虫雌雄成虫触角产生的EAG反应差异不显著(P>0.05),说明苹果小吉丁虫雌雄成虫触角对低质量分数的化学物质反应不够敏感。通过应用LSD多重比较分析,苹果小吉丁虫雌成虫触角对(−)-α-蒎烯、α-蒎烯、苯甲醛、(+)-柠檬烯刺激产生EAG反应与其他9种物质差异显著(P<0.05)。苹果小吉丁虫雄成虫触角对(−)-α-蒎烯刺激产生EAG反应与其他13种物质差异显著(P<0.05),其EAG反应值也相对较大。
-
由表3可以看出:苹果小吉丁虫雌雄成虫对寄主野苹果挥发物标样(-)-α-蒎烯、癸醛、壬醛、α-蒎烯反应率、选择反应率显著高于其他几种,且选择系数均大于0,说明苹果小吉丁虫雌雄成虫对这几种挥发物标样具有一定的趋性。
表 3 苹果小吉丁虫雌雄虫对13种寄主挥发物在10−1 g·g−1下行为反应
Table 3. Behavior orientation responses of male and female A. mali to 13 synthetic monomers at dose 10−1 g·g−1
供试化合物 雄虫 雌虫 反应率/% 选择反应率/% 选择系数 反应率/% 选择反应率/% 选择系数 (+)-α-蒎烯 28.33±4.74 59.05±1.35 0.181±0.027 25.00±7.07 47.62±3.37 −0.048±0.067 (−)-α-蒎烯 50.00±8.16 83.61±3.07 0.672±0.061 51.67±4.71 77.44±3.72 0.549±0.074 α-蒎烯 43.33±4.71 52.50±13.39 0.050±0.268 45.00±4.08 58.98±10.73 0.180±0.215 (+)-β-蒎烯 43.33±10.27 52.69±8.06 0.054±0.161 46.67±14.34 49.43±3.86 −0.011±0.077 丙烯酸丁酯 36.67±2.36 32.14±7.72 −0.357±0.154 38.33±2.36 30.36±5.26 −0.393±0.105 苯甲醛 38.33±6.24 31.02±6.45 −0.380±0.129 43.33±6.24 34.34±7.17 −0.313±0.143 癸醛 45.00±7.07 67.05±5.64 0.341±0.113 43.33±10.27 65.66±1.43 0.313±0.029 (+)-柠檬烯 31.67±2.36 42.06±6.83 −0.159±0.137 30.00±4.08 38.73±3.99 −0.225±0.080 2-甲基丙烯醛 30.00±10.80 28.97±3.41 −0.421±0.068 26.67±8.50 31.75±2.24 −0.365±0.045 壬醛 41.67±6.24 71.31±7.14 0.426±0.143 43.33±9.43 65.56±4.16 0.311±0.083 十五烷 28.33±2.36 41.11±6.85 −0.178±0.137 31.67±6.24 36.94±2.75 −0.261±0.055 乙酸叶醇酯 36.67±4.71 44.44±12.88 −0.111±0.258 43.33±9.43 41.11±6.85 −0.178±0.137 (−)-β-蒎烯 40.00±7.07 56.67±11.09 0.133±0.222 43.33±4.71 52.50±13.39 0.050±0.268 -
植物能够合成并释放多种挥发性有机物(volatile organic compounds,VOCs)。已经有众多研究报道,由于虫害诱导导致植物挥发性物质发生变化[12-14]。植物根、茎、叶、果实、种子均可以合成绿叶挥发物, 但合成部位、组成和含量不仅与植物种类及其生态型有关, 还与组织器官所处发育阶段和生长季节等因素有关。植物除了在正常生理条件下合成绿叶挥发物外,病虫害、有益菌定植、机械损伤、不良环境条件等因素都会影响植物绿叶挥发物的合成与释放[22]。野苹果枝条和枝干均能产生挥发性物质,受苹果小吉丁虫危害的枝条十五烷相对含量增加。有研究显示:十五烷对捕食性天敌拟环纹豹蛛Pardosa pseudoannulata具有引诱效果[23]。因此,十五烷可能在野苹果树间接防御苹果小吉丁虫危害中发挥一定作用。
本研究中,所选取13种寄主挥发物标样在10−1 g·g−1的质量分数下,均能引起雌雄成虫触角产生不同程度触角电位,除(+)-α-蒎烯、丙烯酸丁酯、癸醛、2-甲基丙烯醛等5种化合物引起雌虫触角产生的EAG反应值大于雄虫触角所产生的反应值外,其他8种寄主挥发物标样引起雄虫触角产生的EAG反应值大于雌虫。从整体来看,雄虫对寄主挥发物EAG反应值要大于雌虫,这与崔晓宁[24]测试结果一致。有研究发现:白蜡窄吉丁Agrilus planipennis雄虫触角比雌虫触角更敏感,对顺-3-己烯醇的反应最强,而顺-3-己烯醇对白蜡窄吉丁雌雄虫具有很强的诱集作用[25-26]。伊志豪[27]研究苹果小吉丁虫雌雄成虫触角感器略有差异,这可能是导致雄虫对寄主挥发物EAG反应值要大于雌虫因素之一。
不同危害条件下野苹果枝条与枝干挥发物种类与相对含量会发生变化。通过测定苹果小吉丁虫对寄主13种挥发物触角电位和行为反应,(−)-α-蒎烯、壬醛、癸醛对苹果小吉丁虫成虫具有较好的引诱作用。今后,还可以增加待测化合物种类,以期获得更多对苹果小吉丁虫成虫具有引诱作用化合物,同时在野果林中分别测试(−)-α-蒎烯、壬醛、癸醛3种化合物在不同浓度、不同复配、不同溶剂与助剂条件下,对苹果小吉丁虫成虫引诱效果,最终开发出对苹果小吉丁虫成虫有效的植物源引诱剂。
Electroantennogram and behavioral responses of Agrilus mali to the volatiles from Malus sieversii trees induced by pest and disease
-
摘要:
目的 探索苹果小吉丁虫Agrilus mali对寄主野苹果Malus sieversii 挥发物行为反应。 方法 采用动态顶空套袋吸附法收集不同受害状态下野苹果枝条与枝干挥发物,测定苹果小吉丁虫对寄主挥发物触角电位和行为反应。 结果 共获得9类46种挥发性化合物,包括醇类、脂类、醛类、烷烃类、烯烃类、酮类、萜类、醚类及其他类。与健康枝条释放的挥发物相比,受苹果小吉丁虫危害枝条中二十烷、十五烷相对含量增加,丁烯醇、2-甲基丙烯醛、十七烷、二十一烷、环庚三烯、环己酮、α-蒎烯、甘菊蓝等8种挥发物相对含量有所降低,增加的有化合物种类为顺-3-己烯醇、己醛、癸醛、壬醛、(+)-柠檬烯等14种;受苹果腐烂病菌Valsa mali危害的枝条,十五烷、十七烷、3,7-二甲基癸烷,二十烷、α-蒎烯相对含量增加,二十一烷、环己酮、环庚三烯、甘菊蓝相对含量减少,增加的化合物种类为顺-3-己烯醇、丁酸丁酯、己醛、(+)-α-蒎烯、(+)-柠檬烯等12种。与健康枝干释放挥发物相比,受苹果小吉丁虫危害枝干,顺-3-己烯醇、α-蒎烯、(−)-α-蒎烯、莰烯相对含量增加,己醛、环庚三烯、β-蒎烯、甘菊蓝相对含量有所降低,增加的化合物种类分别为3-辛烯-2-醇、丁酸丁酯、癸醛、十五烷、(+)-香橙烯等17种;受苹果腐烂病菌危害枝干中,己醛相对含量增加,顺-3-己烯醇、丙烯醛、环己酮、α-蒎烯、(−)-α-蒎烯、β-蒎烯、甘菊蓝相对含量降低,增加的化合物种类分别为苯甲醛、十五烷、双戊烯等11种化合物。能引起苹果小吉丁虫雌雄成虫触角产生较强触角电位反应物质包括(−)-α-蒎烯、壬醛、(+)-α-蒎烯、苯甲醛、癸醛、丙烯酸丁酯,行为测定中具有趋向反应的物质有(−)-α-蒎烯、α-蒎烯、(+)-β-蒎烯、β-蒎烯、癸醛、壬醛。 结论 综合触角电位和行为反应测定结果表明:(−)-α-蒎烯、壬醛、癸醛对苹果小吉丁虫成虫具有较好的引诱作用。图1表3参27 Abstract:Objective This study aims to explore the electroantennogram and behavioral responses of Agrilus mali to the volatiles from Malus sieversii trees in different damaged states to provide reference for the research and development of highly effective attractants. Method The volatiles were collected by using dynamic headspace adsorption from branches and limbs of M. sieversii trees. Result There are total of 46 volatile compounds in 9 categories has been obtained, including alcohols, lipids, aldehydes, alkanes, alkenes, ketones, terpenes, ethers and others. Compared with healthy branches, the relative contents of eicosane and pentadecane increased in A. mali damaged branches, while the relative contents of 8 volatiles such as butenol, 2-methylacrolein, heptadecane, heneicosane, cycloheptatriene, cyclohexanone, α-pinene and chamomile decreased. Fourteen compounds were added such as cis-3-hexenol, hexanal, decanal, nonanal, (+)-limonene etc. In Valsa mali damaged branches, pentadecane, heptadecane, 3,7-dimethyldecane, eicosane and α-pinene increased, and heneicosane, cyclohexanone, cycloheptatriene, azulene decreased. Twelve compounds were added such as cis-3-hexenol, butyl butyrate, hexanal, (+)-α-pinene, (+)-limonene, etc. Compared with the volatilides released from healthy limbs, the relative contents of cis-3-hexenol, α-pinene, (−)-α-pinene and camphene were increased in A. mali damaged limbs, and hexanal, cycloheptane, β-pinene, cycloheptatriene, azulene contents decreased. Seventeen compounds were added such as 3-octene-2-alcohol, butyl butyrate, decanal pentadecane, (+)-aromadendrene, etc. In Valsa mali damaged limbs, hexanal increased, and cis-3-hexenol, acrolein, cyclohexanone, α-pinene, (−)-α-pinene, β-pinene and azulene decreased. Eleven compounds were added such as benzaldehyde, pentadecane, dipentene, etc. EAG responses and behaviour of A. mali towards volatiles released by host were tested. The results showed that strong EAG reactants could be produced in the antennae of male and female adults of A. mali, these compounds were (−)-α-pinene, nonanal, (+)-α-pinene, benzaldehyde, decanal, butyl acrylate. A. mali were attracted by (−)-α-pinene, α-pinene, (+)-β-pinene, β-pinene, decanal, nonanal in the behavior bioassay. Conclusion According to the results of EAG responses and behavioral orientation, the (−)-a-pinene, nonanal and decanal had good attraction to the adult of Agrilus mali.[Ch, 1 fig. 3 tab. 27 ref.] -
Key words:
- forest protection /
- Agrilus mali /
- Valsa mali /
- plant volatiles /
- electroantennogram /
- behavioral orientation
-
表 1 触角电位测定实验所用标准化合物纯度及来源
Table 1. Source and purity of standard chemicals used in EAG testing
标准化合物 质量分数/ % 来源 标准化合物 质量分数/ % 来源 (+)-α-蒎烯 (+)-α-pinene 95 梯希爱 癸醛 decanal 97 阿达玛斯 (−)-α-蒎烯 (−)-α-pinene 98 霍尼韦尔 (+)-柠檬烯 (+)-limonene 99 梯希爱 α-蒎烯 α-pinene 98 奥德里奇 2-甲基丙烯醛 methacrolein 95 阿达玛斯 (+)-β-蒎烯 (+)-β-pinene 95 霍尼韦尔 壬醛 nonanal 95 奥德里奇 丙烯酸丁酯 butyl acrylate 99 奥德里奇 十五烷 pentadecane 99 安谱 乙酸叶醇酯 leaf acetate 97 梯希爱 (−)-β-蒎烯 (−)-β-pinene 99 霍尼韦尔 苯甲醛 benzaldehyde 99 阿达玛斯 顺-3-己烯醇 leaf alcohol 98 奥德里奇 表 2 不同危害条件下野苹果枝条和枝干主要挥发物成分及相对含量
Table 2. Composition and relative contents of main volatiles released from the branch and limb of the wild apple in different damaged states
类别 化合物名称 CAS号 枝条挥发物相对含量/% 枝干挥发物相对含量/% 健康树 受苹果小吉
丁虫危害受腐烂
病菌危害健康树 受苹果小吉
丁虫危害受腐烂
病菌危害醇类alcohols 顺-3-己烯醇 (Z)-3-hexenol 928-96-1 − 1.82 0.90 2.46 6.70 1.67 丁烯醇 2-buten-1-ol 6117-91-5 1.62 0.61 − − − − 1-戊烯-3-醇 1-penten-3-ol 616-25-1 − − − − 1.00 − 顺-2-己烯-1-醇 (Z)-2-hexenol 928-94-9 − − − 11.86 − 3-辛烯-2-醇 3-octen-2-ol 76649-14-4 − − − − 0.77 2.86 脂类esters 丙酸丁酯 butyl propionate 590-01-2 − 2.18 3.29 − − 1.50 丁酸丁酯 butyl butyrate 109-21-7 − 0.93 2.44 − 2.53 − 丙烯酸丁酯 butyl acrylate 141-32-2 − − 16.36 − − 19.59 梨醇酯 prenyl acetate 1191-16-8 − 0.75 0.75 − 1.65 − 乙酸叶醇酯 leaf acetate 3681-71-8 − 7.00 4.68 − 10.63 − 2-甲基丁酸乙酯 ethyl 2-methylbutyrate 7452-79-1 − − − − 2.97 − 丁酸烯丙酯 allyl butanoate 2051-78-7 − − − − 1.18 0.85 醛类aldehydes 顺-3-己烯醛 (Z)-3-hexenal 6789-80-6 − 3.70 − − − 1.02 己醛 hexanal 66-25-1 − 1.21 1.49 4.60 0.67 13.40 2-甲基丙烯醛 methacrolein 78-85-3 5.21 0.77 − − − − 癸醛 decanal 112-31-2 − 0.90 − − 1.29 − 壬醛 nonanal 124-19-6 − 2.00 − − − − 苯甲醛 benzaldehyde 100-52-7 − 1.30 3.09 − 2.49 1.34 青叶醛 leaf aldehyde 6728-26-3 2.31 − − − − − 丙烯醛 acrolein 107-02-8 − − − 10.16 − 7.12 2-甲基-2-戊烯醛 2-methyl-2-pentenal 623-36-9 − − − − 1.42 − 烷烃类alkanes 2-甲基庚烷 2-methylheptane 592-27-8 − 6.29 0.75 − − − 2,4,4-三甲基-己烷 2,4,4-trimethylhexane 16747-30-1 − 0.68 − − − − 2,4-二甲基庚烷 2,4-dimethylheptane 2213-23-2 − 20.22 − − − − 十五烷 pentadecane 629-62-9 0.52 2.04 6.42 − 1.85 0.72 十七烷 heptadecane 629-78-7 1.64 1.09 2.61 − 3.84 1.71 3,7-二甲基癸烷 3,7-dimethyldecane 17312-54-8 1.25 − 3.42 − − − 二十烷 eicosane 112-95-8 1.51 2.69 4.74 − 2.57 4.92 二十一烷 heneicosane 629-94-7 1.51 0.63 1.34 − − − 二十四烷 tetracosane 646-31-1 1.87 − − − − − 环庚烷 cycloheptane 291-64-5 1.14 − − − − − 烯烃类alkenes 环庚三烯 cyclohetatriene 544-25-2 16.53 6.64 4.67 4.95 1.32 − 酮类ketones 环己酮 cyclohexanone 108-94-1 45.45 2.83 7.39 17.63 − 6.22 苯乙酮 acetophenone 98-86-2 − − 0.94 − − − 2-癸酮 2-decanone 693-54-9 − − − − 0.55 − 萜类terpendoids α-蒎烯 α-pinene 80-56-8 0.86 0.81 0.98 9.85 10.96 3.68 (+)-α蒎烯 (+)-α-pinene 7785-70-8 − − 2.42 − − − (−)-α-蒎烯 (−)-α-pinene 7785-26-4 − − − 1.66 8.96 1.23 (+)-柠檬烯 (+)-limonene 5989-27-5 − 0.76 7.74 1.11 − − 双戊烯 dipentene 138-86-3 − − − − − 1.14 β-蒎烯 β-pinene 127-91-3 − − − 4.92 1.68 1.04 莰烯 camphene 79-92-5 − − − 0.47 2.17 − (+)-香橙烯 (+)-aromandendrene 489-39-4 − − − − 0.85 − 醚类ethers 苯甲醚 anisole 100-66-3 − − − − 3.18 1.56 仲丁醚 isobutyl ether 628-55-7 − − − 1.20 − − 其他 甘菊蓝 azulene 275-51-4 3.43 0.94 2.12 2.68 0.84 2.16 说明:−表示GC-MS没有检测鉴别出该化合物 表 3 苹果小吉丁虫雌雄虫对13种寄主挥发物在10−1 g·g−1下行为反应
Table 3. Behavior orientation responses of male and female A. mali to 13 synthetic monomers at dose 10−1 g·g−1
供试化合物 雄虫 雌虫 反应率/% 选择反应率/% 选择系数 反应率/% 选择反应率/% 选择系数 (+)-α-蒎烯 28.33±4.74 59.05±1.35 0.181±0.027 25.00±7.07 47.62±3.37 −0.048±0.067 (−)-α-蒎烯 50.00±8.16 83.61±3.07 0.672±0.061 51.67±4.71 77.44±3.72 0.549±0.074 α-蒎烯 43.33±4.71 52.50±13.39 0.050±0.268 45.00±4.08 58.98±10.73 0.180±0.215 (+)-β-蒎烯 43.33±10.27 52.69±8.06 0.054±0.161 46.67±14.34 49.43±3.86 −0.011±0.077 丙烯酸丁酯 36.67±2.36 32.14±7.72 −0.357±0.154 38.33±2.36 30.36±5.26 −0.393±0.105 苯甲醛 38.33±6.24 31.02±6.45 −0.380±0.129 43.33±6.24 34.34±7.17 −0.313±0.143 癸醛 45.00±7.07 67.05±5.64 0.341±0.113 43.33±10.27 65.66±1.43 0.313±0.029 (+)-柠檬烯 31.67±2.36 42.06±6.83 −0.159±0.137 30.00±4.08 38.73±3.99 −0.225±0.080 2-甲基丙烯醛 30.00±10.80 28.97±3.41 −0.421±0.068 26.67±8.50 31.75±2.24 −0.365±0.045 壬醛 41.67±6.24 71.31±7.14 0.426±0.143 43.33±9.43 65.56±4.16 0.311±0.083 十五烷 28.33±2.36 41.11±6.85 −0.178±0.137 31.67±6.24 36.94±2.75 −0.261±0.055 乙酸叶醇酯 36.67±4.71 44.44±12.88 −0.111±0.258 43.33±9.43 41.11±6.85 −0.178±0.137 (−)-β-蒎烯 40.00±7.07 56.67±11.09 0.133±0.222 43.33±4.71 52.50±13.39 0.050±0.268 -
[1] 张汉斐. 伊犁野果林苹果小吉丁虫发生动态及防治[J]. 新疆农业科技, 2000(6): 22 − 22. ZHANG Hanfei. Occurrence and control of Agrilus mali in the wild fruit forest in Yili region [J]. Xinjiang Agric Sci Technol, 2000(6): 22 − 22. [2] 王磊. 新疆野苹果和新疆野杏[J]. 新疆农业科学, 1989(6): 33 − 34. WANG Lei. Malus sieversii and Armeniaca vulgaris [J]. Xinjiang Agric Sci, 1989(6): 33 − 34. [3] 侯博, 许正. 中国伊犁野生果树及近缘种研究[J]. 干旱区研究, 2006, 23(3): 453 − 458. HOU Bo, XU Zheng. Study on wild fruit trees and their kindred species in the Yili Valley China [J]. Arid Zone Res, 2006, 23(3): 453 − 458. [4] 傅立国. 中国植物红皮书[M]. 北京: 科学出版社, 1992. [5] CROOK D J, KHRIMIAN A, FRANCESE J A, et al. Development of a host-based semiochemical lure for trapping emerald ash borer Agrilus planipennis (Coleoptera: Buprestidae) [J]. Environ Entomol, 2008, 37(2): 356 − 365. [6] BEYAERT I, WÄSCHKE N, SCHOLZ A, et al. Relevance of resource-indicating key volatiles and habitat odour for insect orientation [J]. Anim Behav, 2010, 79(5): 1077 − 1086. [7] 孙晓玲, 高宇陈, 陈宗懋. 虫害诱导植物挥发物(HIPVs)对植物性昆虫的行为调控[J]. 应用昆虫学报, 2012, 49(6): 1413 − 1422. SUN Xiaoling, GAO Yu, CHEN Zongmao. Behavior regulation of herbivores by herbivores induced plant volatiles(HIPVs) [J]. Chin J Appl Entomol, 2012, 49(6): 1413 − 1422. [8] RODRIGUEZ-SAONA C, POLAND T M, MILLER J R, et al. Behavioral and electrophysiological responses of the emerald ash borer, Agrilus planipennis, to induced volatiles of Manchurian ash, Fraxinus mandshurica [J]. Chemoecology, 2006, 16(2): 75 − 86. [9] 张苏芳, 孔祥波, 王鸿斌, 等. 植物对昆虫不同防御类型及内在联系[J]. 应用昆虫学报, 2013, 50(35): 1428 − 1437. ZHANG Sufang, KONG Xiangbo, WANG Hongbin, et al. Different strategies of plant resistance to insects and their interaction [J]. Chin J Appl Entomol, 2013, 50(35): 1428 − 1437. [10] ARIMURA G-I, KOST C, BOLAND W. Herbivore-induced, indirect plant defences [J]. Biochim Biophys Acta, 2005, 1734(2): 91 − 111. [11] BALDWIN I T. Methyl jasmonate-induced nicotine production in Nicotiana attenuata: inducing defenses in the field without wounding [J]. Entomol Exp Appl, 1996, 80(1): 213 − 220. [12] KESSLER A, BALDWIN I T. Defensive function of herbivore-induced plant volatile emissions in nature [J]. Science, 2001, 291(5511): 2141 − 2144. [13] VET L E M, DICKE M. Ecology of infochemical use by natural enemies in a tritrophic context [J]. Ann Rev Entomol, 1992, 37(1): 141 − 172. [14] DICKE M. Induced indirect plant defence: communication and exploration in multitrophic context [J]. Mitteilungen der Deutschen Entomologischen Gesellschaft, 1997, 11: 453 − 464. [15] DICKE M, van LOON J J A. Multitrophic effects of herbivoreinduced plant volatiles in an evolutionary context [J]. Entomol Exp Appl, 2000, 97(3): 237 − 249. [16] DICKE M, van BEEK T A, POSTHUMUS M A, et al. Isolation and identification of volatile kairomone that affects acarine predatorprey interactions : involvement of host plant in its production [J]. J Chem Ecol, 1990, 16(2): 381 − 396. [17] TURLINGS T C J, TUMLINSON J H, LEWIS W J. Exploitation of herbivore-induced plant odors by host-seeking parasitic wasps [J]. Science, 1990, 250(4985): 1251 − 1253. [18] 程彬, 付晓霞, 韩启, 等.虫害诱导的家榆挥发物对榆紫叶甲寄主选择行为的影响[J]. 林业科学, 2010, 46(10): 76 − 82. CHENG Bin, FU Xiaoxia, HAN Qi, et al. Effects of herbivore-induced Ulmus pumila volatiles on the host selection process ofAmbrostoma quadriimpressum [J]. Sci Silv Sin, 2010, 46(10): 76 − 82. [19] 王明, 崔晓宁, 孙可可, 等. 诱导条件对新疆野苹果树挥发物释放的影响[J]. 西北农林科技大学学报(自然科学版), 2018, 46(6): 1 − 11. WANG Ming, CUI Xiaoning, SUN Keke, et al. Effects of different inducing conditions on volatiles released form Malus sieversii trees [J]. J Northwest A&F Univ Nat Sci Ed, 2018, 46(6): 1 − 11. [20] 任利利. 松墨天牛和天敌花绒寄甲对几种树木挥发物的电生理及行为反应[D]. 北京: 北京林业大学, 2014. REN Lili. Electrophysiological and Behavioral Responses of Monochamus alternatus and Parasitoid Dastarcus helophoroides to Semiochemicals of Several Tree Species[D]. Beijing: Beijing Forestry University, 2014. [21] 张红兵, 李小鹰, 戴华国, 等. 台湾乳白蚁和黄胸散白蚁对3种饵剂的嗅觉行为反应[J]. 昆虫知识, 2005, 42(3): 289 − 301. ZHANG Hongbing, LI Xiaoying, DAI Huaguo, et al. The olfactory responses of Coptotermes formosanus and Reticulitermes flaviceps to three baited insecticides [J]. Chin Bull Entomol, 2005, 42(3): 289 − 301. [22] 孙海峰, 李震宇, 武滨, 等. 绿叶挥发物产生特征及其生态生理作用研究进展[J]. 植物生态学报, 2013, 37(3): 268 − 275. SUN Haifeng, LI Zhenyu, WU Bin, et al. Review of recent advances on the production and ecophysiological roles of green leaf volatiles [J]. Chin J Plant Ecol, 2013, 37(3): 268 − 275. [23] 汪波, 黄若仪, 谭昭君, 等. 正十五烷对狼蛛嗅觉定位的影响[J]. 江苏农业学报, 2015, 31(3): 538 − 542. WANG Bo, HUANG Ruoyi, TAN Zhaojun, et al. Effect of n-pentadecane on wolf spider’s olfactory orientation [J]. Jiangsu J Agric Sci, 2015, 31(3): 538 − 542. [24] 崔晓宁. 苹果小吉丁虫对寄主植物挥发物的行为反应及嗅觉相关基因功能研究[D]. 杨凌: 西北农林科技大学, 2018. CUI Xiaoning. Behavioral Responses of Agrilus mali to Host-plant Volatiles and Function of Related Olfactory Genes[D]. Yangling : Northwest A&F University, 2018. [25] de GROOT P, GRANT G G, POLAND T M, et al. Electrophysiological response and attraction of Emerald ash Borer to green leaf volatiles (GLVs) emitted by host foliage [J]. J Chem Ecol, 2008, 34(9): 1170 − 1179. [26] GRANT G G, RYALL K L, LYONS D B, et al. Differential response of male and female emerald ash borers(Col., Buprestidae) to (Z)-3-hexenol and manuka oil [J]. J Appl Entomol, 2010, 134(1): 26 − 33. [27] 伊志豪. 苹小吉丁成虫的形态特征及全身感受器的超微结构[D]. 杨凌: 西北农林科技大学, 2016. YI Zhihao. Morphological Characteristics and Ultrastructure of Sensilla for Adults of Agrilus mali Matsumura (Coleoptera: Buprestidae)[D]. Yangling: Northwest A&F University, 2016. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20190738






 下载:
下载: