-
很多植物不仅有很高的观赏价值,而且还通过其叶、枝、干、皮、花、果、芽等释放出多种对人体健康有益的挥发性物质,如α-蒎烯、β-蒎烯、β-月桂烯、莰烯、柠檬烯、1, 8-桉叶油素等挥发油成分具有消炎、降压等疗养活性[1]。植物的挥发油成分可以治疗冠心病、高血压等疾病,且治疗呼吸道系统疾病效果更明显[2],以单萜的治疗效果最明显[3]。因此,研究植物资源的挥发油成分,为开发利用植物挥发油成分的保健应用价值夯实了物质基础,为提高人们体质开辟了新的途径。截至目前已有401种植物的叶、11种植物的花、2种植物的枝、6种植物的果实、2种植物的树皮、43种植物的枝和叶、18种植物的花和叶、12种植物的果和叶、1种植物的花和果实、2种植物的叶和种子、4种植物的根和叶、1种植物的根和枝、6种植物的叶枝花、9种植物的根枝叶、2种植物的叶枝果等都相应被提取了挥发油。同种植物各组织器官用同种方法提取的挥发油成分存在差异,但有共同的组分[4-6],并随树种不同呈现差异性变化。制约植物挥发油成分释放的因素除了植物本身的组织器官类型外,与采集材料提取挥发油成分的季节有关,也与植物的群落结构、种类、株龄、叶龄及植株的发育部位等有关,还与外来生物因素以及温度、光照、水分、土壤、大气成分比例及空气湿度等非生物因素有关[4-10]。在同样的生长条件下,幼树相对大龄树木释放挥发性成分更快[11],但这种差异性多随树龄的增加而逐渐减小[12],也有随树龄的增加而逐渐增加的现象[13]。植物群落结构越丰富,释放萜类化合物的量越多[14]。黄心夜合Michelia martinii隶属木兰科Magnoliaceae含笑属Michelia常绿大乔木,树形呈尖塔状,其嫩枝榄青色,幼叶嫩黄色,春天所发新叶嫩红色,散发扑鼻的香气,花香浓郁,可应用于园林绿化,其干花蕾可入药,是一种具有很大开发价值的园林珍稀树木[15]。徐植灵等[16]通过鉴定黄心夜合干燥花蕾的挥发油,发现黄心夜合干燥花蕾挥发油成分中含有β-榄香烯、β-蒎烯、对-聚伞花素、γ-毕澄茄烯、α-蒎烯、α-衣兰油烯、氧化石竹烯、喇叭醇、莰烯等主要成分。雷凌华等[17-18]发现黄心夜合四季鲜嫩枝挥发油共含77种成分,而四季鲜叶挥发油共含65种成分。这说明黄心夜合各组织的挥发油成分非常丰富,然而有关黄心夜合在同一时期各个组织器官释放挥发油成分及其活性的研究还鲜见报道。本研究以黄心夜合鲜叶、鲜嫩枝、鲜花为材料,以水蒸气蒸馏法萃取其同一时间不同组织的挥发油成分,以气相色谱-质谱联用技术分析其成分,了解黄心夜合3种不同组织的挥发油成分,以期为黄心夜合潜在的园林生态功能、药理功能、养生保健功能的深度开发提供参考。
-
2014年4月在贵阳市王岗村(26°46'41.31"N,106°53'49.67"E)选择15株生长势旺盛、无病虫害、高度6~10 m、胸径20~22 cm的黄心夜合,采集其鲜叶、鲜嫩枝、鲜花。将采集的3类鲜样进行现场清洗、沥干,称量后按1份500 g保存于3~5 ℃冰箱中,1周内将样品处理完毕,以便对比分析黄心夜合同期3种不同组织的挥发油成分。所用有机试剂都为分析纯,水为去离子纯净水。
-
设备包括XPE205分析天平(深圳市时代之峰科技有限公司),ZDHW220V电热套98-1-B(天津市泰斯特仪器有限公司),水蒸汽蒸馏提取器1套。
-
参考文献[18]提取黄心夜合鲜叶挥发油成分,将保存在冰箱中的鲜叶,按1份500 g分别置入5 000 mL的圆底烧瓶,再往瓶中加入3 000~3 500 mL的蒸馏水,浸泡2 h,按常规水蒸气蒸馏法提取,分离收集挥发油,称量,密封保存于-4~0 ℃的冰箱。提取率以鲜质量计。重复5次·样品-1,取平均值。黄心夜合鲜叶挥发油提取率=黄心夜合鲜叶挥发油质量/黄心夜合鲜叶质量×100%。将鲜嫩枝切成6~10 mm长的碎枝粒,处理同鲜叶。将鲜花切成4~8 mm宽的碎条,去嫩枝,长度以鲜花本身宽度为限,处理同鲜叶。
-
黄心夜合挥发性成分的定性定量分析采用气相色谱-质谱联用技术(GC-MS)。气相色谱条件:DB-5MS石英管色谱柱(30 m × 0.25 μm × 0.25 mm),载高纯度氦气;色谱柱升温程序:始温50 ℃,持续4 min,以6 ℃·min-1升至100 ℃,以10 ℃·min-1升至180 ℃,持续5 min,以15 ℃·min-1升到280 ℃,持续15 min;柱前压47 kPa,分流比1: 11.0,流速1.0 mL·min-1;进样口温度250 ℃,进样量1.0 μL。质谱条件:质核比扫描范围45~550 u,全扫描方式;GCMS-QP2010,电子轰击(EI)离子源,电子能量70 eV;检测器电压1.8 kV;离子源温度200 ℃;接口温度220 ℃;四极杆温度150 ℃。实验仪器:QP5050A型气相色谱-质谱联用仪(日本岛津公司),Saturn 2000离子阱质谱仪,CP-3800气相色谱仪(美国Varian公司)。
-
依前述GC-MS条件鉴定分析黄心夜合鲜花、鲜嫩枝、鲜叶挥发油成分,得到鲜花、鲜嫩枝、鲜叶的各峰质谱图和总离子流色谱图。通过对3种组织的质谱图进行NIST标准谱库的检索,自动检索分析各组分的质谱数据,结合谱图人工解析,根据质谱裂解规律对黄心夜合鲜花、鲜嫩枝、鲜叶挥发油成分进行定性分析,经色谱峰面积归一法计算各组分的质量分数。
-
黄心夜合不同组织经水蒸气蒸馏都得到透明的油状液体,并且能明显感受到不同组织提取的油状液体释放香味的差异。鲜嫩枝挥发油释放出的香气清雅,颜色嫩黄清亮;鲜叶挥发油释放的香气幽清,颜色呈嫩桔黄色,晶莹透亮;鲜花挥发油释放的香味浓郁,颜色呈桔黄色,发出浑浊亮光。从表 1可见:黄心夜合鲜花挥发油平均提取率最高,达0.52%,鲜叶挥发油提取率较低,为0.22%,鲜嫩枝挥发油平均提取率最低,仅0.04%。在相同条件下,鲜花释放挥发油的强度和量明显高于鲜叶、鲜嫩枝,而鲜叶释放挥发油的强度和量明显高于鲜嫩枝。
表 1 黄心夜合不同组织的挥发油提取率
Table 1. Rate of extraction of the volatile oils components from fresh different tissues in April of Michelia martinii
样品 样品量/g 提油量/g 提取率/% 鲜叶 500 1.10 0.22 ± 0.02 鲜嫩枝 500 0.20 0.04 ± 0.02 鲜花 500 2.51 0.52 ± 0.02 说明:提取率为平均值±标准差 -
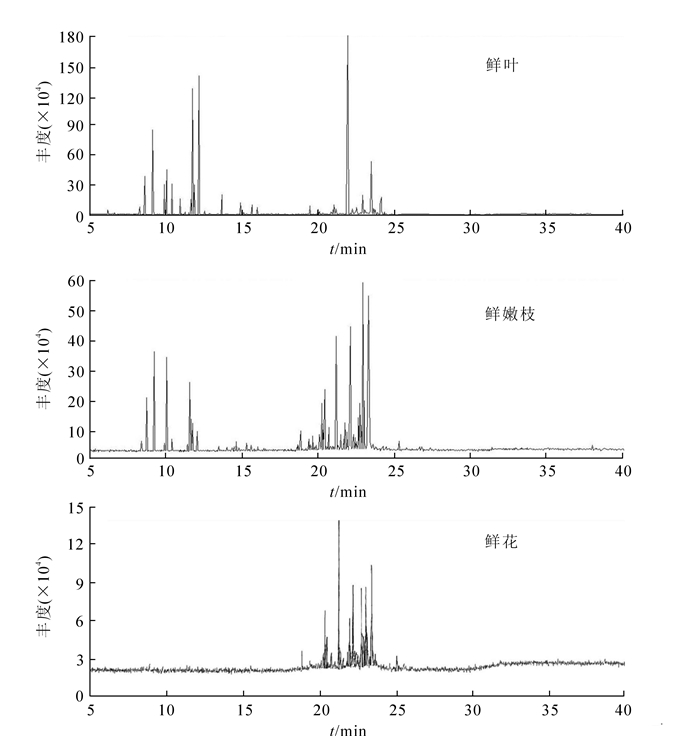
从图 1可以发现:黄心夜合鲜叶、鲜嫩枝和鲜花的挥发油成分有一定差异。鲜嫩枝分离出72个色谱峰,鲜叶分离出85个色谱峰,而鲜花仅分离出28个色谱峰。去掉峰值0.49以下的峰,通过GC-MS分析黄心夜合发现:鲜花中分离鉴定了25个化合物,占总峰面积的99.30%;鲜叶中分离鉴定了21个化合物,占总峰面积的89.34%;鲜嫩枝中分离鉴定了31个化合物,占总峰面积的84.65%。

图 1 黄心夜合不同新鲜组织挥发油成分的总离子流色谱图
Figure 1. Total ions chromatograms of volatile oil components in different fresh tissues of Michelia martinii
从表 2发现:黄心夜合鲜嫩枝挥发油主要包括β-桉叶醇(14.98%)、γ-杜松烯(11.40%)、绿花白千层醇(8.12%)、[1R-(1α, 3α, 4β)]-4-乙烯基-α, α, 4-三甲基-3-(1-异丙烯基)-环己甲醇(5.99%)、莰烯(4.87%)、β-蒎烯(4.57%)等主要成分,释放的成分以萜烯类化合物(45.69%)、醇类化合物(41.98%)为主。鲜花挥发油主要包括桉叶油-4(14)-烯-11-醇(13.59%)、四甲基环癸二烯甲醇(12.79%)、γ-杜松烯(9.56%)、γ-桉叶油醇(8.76%)、表蓝桉醇(8.75%)、氧化石竹烯(5.71%)、十五烷(4.44%)、τ-杜松醇(4.29%)等主要成分,释放的成分以醇类化合物(54.77%)、萜烯类化合物(37.19%)为主。鲜叶挥发油主要包括[1R-(1α, 3α, 4β)]-4-乙烯基-α, α, 4-三甲基-3-(1-异丙烯基)-环己甲醇(17.05%)、β-顺式-罗勒烯(12.00%)、桉叶素(11.41%)、莰烯(7.59%)、β-蒎烯(3.98%)、α-蒎烯(3.39%)等主要成分,释放的成分以萜烯类化合物(42.23%)、醇类化合物(33.2%)为主。
表 2 黄心夜合3种新鲜组织的挥发油成分
Table 2. Volatile oil components of three fresh tissues of Michelia martinii
序号 t/min 化合物名称 化学式 分子质量 相对含量/% 鲜叶 鲜嫩枝 鲜花 1 19.20 2, 4-二异丙烯基-1-甲基环己烷 C15H24 204 0.60 ± 0.15 0.92 ± 0.09 1.63 ± 0.17 2 20.50 γ-依兰油烯 C15H4 204 1.09 ± 0.18 1.63 ± 0.12 0.62 ± 0.16 3 20.64 大根香叶烯 C15H4 204 - 2.59 ± 0.14 1.22 ± 0.19 4 20.73 十五烷 C15H32 212 - - 4.44 ± 0.21 5 20.78 4(14), 11-桉叶二烯 C15H4 204 0.50 ± 0.16 1.28 ± 0.11 1.69 ± 0.18 6 21.39 α-芹子烯 C15H24 204 - - 3.81 ± 0.17 7 21.12 1-(1-Adamantyl)-3-(8-coiumarinyl) guanidine C20H23N3O2 337 - - 0.81 ± 0.08 8 21.15 δ-杜松烯.delta.-Cadinene, (+)- C15H24 204 - - 1.16 ± 0.15 9 21.65 四甲基环癸二烯甲醇 C15H26O 222 - - 12.79 ± 0.07 10 21.78 1-氧化双环外雪松烯 C15H24O 220 - - 2.08 ± 0.22 11 21.95 γ-榄香烯 C15H24 204 0.60 ± 0.19 0.97 ± 0.16 1.31 ± 0.23 12 22.23 匙叶桉油烯 C15H24O 220 - 1.60 ± 0.18 3.57 ± 0.21 13 22.38 氧化石竹烯 C15H24O 220 - 1.20 ± 0.14 5.71 ± 0.19 14 22.60 表蓝按醇 C12H26O 222 - 1.18 ± 0.15 8.75 ± 0.16 15 22.75 1-三异丙基甲硅烷基-苯并环丁烯 C17H28Si 260 - - 0.76 ± 0.17 16 22.81 1-(7a-Methyloctahydro-1H-inden-1-yl) ethanone C12H20O 180 - - 0.90 ± 0.15 17 20.90 3, 4-二甲基-3-环己烯-1-甲醛 C9H14O 138 - - 1.52 ± 0.14 18 23.16 γ-桉叶油醇 C15H26O 222 - 2.35 ± 0.13 8.76 ± 0.14 19 23.29 愈创木醇 C15H26O 222 - 3.22 ± 0.16 3.41 ± 0.18 20 23.37 马兜铃烯 C15H24 204 - 2.09 ± 0.21 2.66 ± 0.22 21 23.46 γ-杜松烯 C15H24 204 - 11.40 ± 0.17 9.56 ± 0.19 22 23.56 δ-杜松醇 C15H26O 222 - 3.24 ± 0.12 3.18 ± 0.14 23 23.78 τ-杜松醇 C15H26O 222 - - 4.29 ± 0.12 24 23.84 桉叶油-4(14)-烯-11-醇 C15H26O 222 - - 13.59 ± 0.15 25 25.52 (+)-喇叭烯 C15H24 204 - - 2.23 ± 0.06 26 8.49 左旋-α-派烯 C10H16 136 - 2.62 ± 0.18 - 27 9.02 莰烯 C10H16 136 7.59 ± 0.19 4.87 ± 0.17 - 28 9.89 β-蒎烯 C10H16 136 3.98 ± 0.23 4.57 ± 0.21 - 29 10.25 β-月桂烯 C10H16 136 2.67 ± 0.21 0.56 ± 0.22 - 30 11.48 香芹烯 C10H16 136 1.54 ± 0.15 3.44 ± 0.19 - 31 11.59 桉叶素 C10H18O 154 11.41 ± 0.12 1.61 ± 0.13 - 32 11.67 β-反式-罗勒烯 C10H16 136 - 1.28 ± 0.18 - 33 11.99 β-顺式-罗勒烯 C10H16 136 12.00 ± 0.13 0.93 ± 0.15 - 34 15.75 α-萜品醇 C10H18O 154 0.63 ± 0.13 - 35 20.73 香树烯 C15H24 204 - 0.96 ± 0.17 - 36 20.87 α-愈创木烯 C15H24 204 - 3.70 ± 0.12 - 37 8.13 三环烯 C10H16 136 0.68 ± 0.19 - - 38 8.48 α-蒎烯 C10H16 136 3.39 ± 0.21 - - 39 9.72 香桧烯 C10H16 136 2.66 ± 0.18 - - 40 10.76 α-水芹烯 C10H16 136 1.40 ± 0.17 - - 41 11.66 右旋-α-派烯 C10H16 136 2.52 ± 0.19 - - 42 13.48 β-芳樟醇 C10H18O 154 1.60 ± 0.15 - - 43 14.69 2-茨酮 C10H16O 152 1.05 ± 0.13 - - 44 15.42 4-萜品醇 C10H18O 154 0.75 ± 0.14 - - 45 20.86 花柏烯 C15H24 204 1.61 ± 0.21 - - 46 22.18 4-氧化-β-紫罗兰酮 C16H26O 234 - 0.70 ± 0.14 - 47 21.15 δ-栀子 C15H24 204 - 1.06 ± 0.15 - 48 21.65 [1R-(1α, 3α,4β)]-4-乙烯基-α, α, 4-三甲基-3-(1-异丙烯基)-环己甲醇 C15H26O 222 17.05 ± 0.13 5.99 ± 0.16 - 49 22.62 绿花白千层醇 C15H26O 222 2.39 ± 0.19 8.12 ± 0.14 - 50 22.95 荜澄茄油烯醇 C15H26O 222 - 0.66 ± 0.13 - 51 23.86 β-桉叶醇 C15H26O 222 - 14.98 ± 0.16 - 52 26.02 2, 3, 3-Trimethyl-2-[(1E)-3-methyl-1, 3-butadienyl]-6-methylen C15H22O 218 - 0.55 ± 0.15 - 说明:“-”表示未检测到。相对含量为均值±标准差 -
从图 1和表 2可发现:峰值在0.5以上的峰中,黄心夜合不同组织挥发油成分丰富度由高到低的顺序为鲜嫩枝、鲜花、鲜叶。鲜花和鲜嫩枝挥发油含2, 4-二异丙烯基-1-甲基环己烷、γ-依兰油烯、大根香叶烯、4(14), 11-桉叶二烯、γ-榄香烯、匙叶桉油烯、氧化石竹烯、表蓝桉醇、γ-桉叶油醇、愈创木醇、马兜铃烯、γ-杜松烯、δ-杜松醇等13种共同成分,共同成分在鲜花挥发油成分中的相对含量达52.07%(其中萜烯类化合物占27.97%,醇类化合物占24.10%),在鲜嫩枝挥发油成分相对含量达33.67%(其中萜烯类化合物占23.68%,醇类化合物占9.99%)。鲜叶和鲜花含γ-榄香烯、4(14), 11-桉叶二烯、γ-依兰油烯、2, 4-二异丙烯基-1-甲基环己烷等4种共同成分,共同成分在鲜花挥发油成分中的相对含量为5.25%(其中萜烯类化合物占3.62%,烷类化合物占1.63%),在鲜叶挥发油成分中的相对含量为2.79%(其中萜烯类化合物占2.19%,烷类化合物占0.60%)。鲜叶和鲜嫩枝挥发油含2, 4-二异丙烯基-1-甲基环己烷、γ-依兰油烯、4(14), 11-桉叶二烯、γ-榄香烯、莰烯、β-蒎烯、β-月桂烯、香芹烯、桉叶素、β-顺式-罗勒烯、[1R-(1α, 3α, 4β)]-4-乙烯基-α, α, 4-三甲基-3-(1-异丙烯基)-环己甲醇、绿花白千层醇等12种共同成分,共同成分在鲜叶挥发油成分中的相对含量为61.42%(其中萜烯类化合物占29.97%,醇类化合物占30.85%,烷类化合物占0.60%),在鲜嫩枝挥发油成分中的相对含量为34.89%(其中萜烯类化合物占18.25%,醇类化合物占15.72%,烷类化合物占0.92%)。3种组织都含2, 4-二异丙烯基-1-甲基环己烷、γ-依兰油烯、4(14), 11-桉叶二烯、γ-榄香烯等4种共同成分,共同成分在鲜花挥发油成分中的相对含量为5.25%(其中萜烯类化合物占3.62%,烷类化合物占1.63%),在鲜叶挥发油成分中的相对含量为2.79%(其中萜烯类化合物占2.19%,烷类化合物占0.60%),在鲜嫩枝挥发油成分中的相对含量为4.80%(其中萜烯类化合物占3.88%,烷类化合物占0.92%)。
-
同质量的黄心夜合鲜花的挥发油提取率较高,高于鲜叶、鲜嫩枝,种类也较丰富,而鲜嫩枝的挥发油提取率最低。在3种组织中,鲜花和鲜嫩枝提取的挥发油成分较丰富,鲜花最丰富。这可能与黄心夜合鲜花的组织结构里分布着有利于释放挥发油的栅栏组织和海绵组织类型有关,而且也与细胞排列方式、以及富含释放挥发油成分的分泌细胞有关,但鲜花组织季节性强,持续时间短,数量有限。鲜嫩枝虽然不受季节限制,一年四季都可采,但鲜嫩枝释放挥发性成分的量相对较少,采集也受限。而鲜叶数量和叶表面积极大,不受季节和数量限制,从组织结构上来看,黄心夜合异面叶叶肉组织分布着有利于释放挥发油的栅栏组织和海绵组织,栅栏组织在上表皮内侧,排列紧密,而海绵组织在下表皮内侧,海绵组织的细胞形状不规则,排列疏松,胞间隙大,释放挥发油成分的分泌细胞多分布在栅栏组织细胞中,也有分布在栅栏与海绵组织细胞之间[19]。所以应重点发挥鲜叶挥发油成分的功能作用。
黄心夜合鲜花挥发油成分富含萜烯类和醇类化合物,萜烯类以单萜烯为主,其中醇类化合物含量高于萜烯类化合物,而萜烯类化合物主要有γ-杜松烯、氧化石竹烯、α-芹子烯、匙叶桉油烯、1-氧化双环外雪松烯、(+)-喇叭烯、马兜铃烯(-)、4(14), 11-桉叶二烯、大根香叶烯等,含量达36.38%,醇类化合物主要有桉叶油-4(14)-烯-11-醇、四甲基环癸二烯甲醇、表蓝桉醇、γ-桉叶油醇、τ-杜松醇、愈创木醇、δ-杜松醇等,含量高达54.77%。黄心夜合鲜花、鲜嫩枝和鲜叶3种组织挥发油成分都含萜烯类化合物,且都以单萜烯为主,同时所含的含氧化合物多以醇类为主。黄心夜合挥发油成分中的α-蒎烯、β-蒎烯、β-月桂烯、β-芳樟醇有明显的降压作用,还具有止咳、祛痰和抑制真菌的作用[20],而芳樟醇、月桂烯不但有助于空气负离子的释放,还能消炎镇痛、保健心血管[19]。这说明黄心夜合3种组织所释放的挥发油成分都具有潜在的保健功能,适于养生。由于春季黄心夜合群落3种组织同时出现,3种组织所释放的成分产生的叠加养生效应可能会更明显。
-
黄心夜合3种新鲜组织中鲜叶、鲜花挥发油提取率较高,鲜花最高,达0.52%,而鲜嫩枝释放挥发油成分丰富度最高,鲜嫩枝和鲜花所释放的挥发油成分相对丰富。黄心夜合鲜花、鲜嫩枝和鲜叶3种新鲜组织在水蒸气蒸馏法提取装置中都释放出2, 4-二异丙烯基-1-甲基环己烷、γ-依兰油烯、4(14), 11-桉叶二烯、γ-榄香烯等4种挥发油成分,这4种萜烯类化合物在鲜叶、鲜嫩枝、鲜花所释放的挥发油成分分别为2.79%、4.80%、5.25%。可以看出,黄心夜合3种新鲜组织所释放的4种萜烯类化合物即共同成分在鲜叶、鲜花、鲜嫩枝中的相对含量较少。但鲜叶和鲜嫩枝所释放的挥发性成分中含共同成分12种,鲜花和鲜嫩枝含共同成分13种,而鲜叶和鲜花仅含4种共同成分。
Volatile components analysis from different fresh tissues of Michelia martinii
-
摘要: 为探讨同一时间内黄心夜合Michelia martinii鲜叶、鲜嫩枝和鲜花的挥发油成分,利用气相色谱-质谱联用技术(GC-MS)对水蒸气蒸馏法提取的黄心夜合鲜叶、鲜嫩枝和鲜花挥发油成分进行了分析。结果表明:去掉峰值0.49以下的峰,从黄心夜合鲜叶、鲜嫩枝、鲜花分别检测出21种、31种和25种成分,3种不同组织样品共有2,4-二异丙烯基-1-甲基环己烷、γ-依兰油烯、4(14),11-桉叶二烯、γ-榄香烯等4种成分,而鲜叶与鲜嫩枝都释放共同的12种挥发性成分,鲜嫩枝与鲜花都释放共同的13种挥发性成分,鲜叶与鲜花都释放共同的4种挥发性成分。黄心夜合鲜叶、鲜嫩枝和鲜花的挥发油成分在提取材料选择、挥发性成分利用与养生保健群落的营建等方面具有一定的应用参考。Abstract: To study volatile components from fresh leaves, fresh twigs, and fresh flowers of Michelia martinii at the same time, volatile oils were extracted by water-steam distillation from the fresh leaves, fresh twigs, and fresh flowers and then detected by gas chromatography-mass spectrometry (GC-MS). Results of GC-MS showed that the volatile oils contents from different organizations of M. martinii at the same time had ingredients of 21 kinds from fresh leaves, of 31 kinds from fresh twigs, and of 25 kinds from fresh flowers (peak values below 0.49 were neglected). Among the three fresh organizations of M. martinii, the common components were four kinds of ingredients, such as.gamma.-Elemene, gamma.-Muurolen, Eudesma-4(14), 11-diene, and Cyclohexane, 2, 4-diisopropenyl-1-methyl-. Four kinds of components were common to fresh leaves and fresh flowers, 13 kinds of components were common to fresh flowers and fresh twigs, and 12 kinds of components were common to fresh leaves and fresh twigs. The volatile oils of flowers were rich in terpenes and alcohols with terpenes dominated by monoterpenes up to 36.38%; content of the alcohol compounds was higher than terpenes with content as high as 54.77%. Terpene compounds had.gamma.-Cadinene, Caryophyllene oxide, .alpha.-Selinene, Spathulen, Diepicedrene-1-oxide, (+) -Ledene, -Aristolene, Eudesma-4(14), 11-diene, and DGermacrene D. While the alcohols had Eudesm-4(14) -en-11-, 2-(4, 8-Dimethyl-3, 7-cyclodecadien-1-yl) -2-p, Epiglobulol, .gamma.-Eudesmol, .tau.-Cadinol, Guaiol, and.delta.-Cadinol. In conclusion M. martinii could provide new application ideas on material selection of extracted essential oils, utilization of volatile components, and landscape community construction for health care.
-
表 1 黄心夜合不同组织的挥发油提取率
Table 1. Rate of extraction of the volatile oils components from fresh different tissues in April of Michelia martinii
样品 样品量/g 提油量/g 提取率/% 鲜叶 500 1.10 0.22 ± 0.02 鲜嫩枝 500 0.20 0.04 ± 0.02 鲜花 500 2.51 0.52 ± 0.02 说明:提取率为平均值±标准差 表 2 黄心夜合3种新鲜组织的挥发油成分
Table 2. Volatile oil components of three fresh tissues of Michelia martinii
序号 t/min 化合物名称 化学式 分子质量 相对含量/% 鲜叶 鲜嫩枝 鲜花 1 19.20 2, 4-二异丙烯基-1-甲基环己烷 C15H24 204 0.60 ± 0.15 0.92 ± 0.09 1.63 ± 0.17 2 20.50 γ-依兰油烯 C15H4 204 1.09 ± 0.18 1.63 ± 0.12 0.62 ± 0.16 3 20.64 大根香叶烯 C15H4 204 - 2.59 ± 0.14 1.22 ± 0.19 4 20.73 十五烷 C15H32 212 - - 4.44 ± 0.21 5 20.78 4(14), 11-桉叶二烯 C15H4 204 0.50 ± 0.16 1.28 ± 0.11 1.69 ± 0.18 6 21.39 α-芹子烯 C15H24 204 - - 3.81 ± 0.17 7 21.12 1-(1-Adamantyl)-3-(8-coiumarinyl) guanidine C20H23N3O2 337 - - 0.81 ± 0.08 8 21.15 δ-杜松烯.delta.-Cadinene, (+)- C15H24 204 - - 1.16 ± 0.15 9 21.65 四甲基环癸二烯甲醇 C15H26O 222 - - 12.79 ± 0.07 10 21.78 1-氧化双环外雪松烯 C15H24O 220 - - 2.08 ± 0.22 11 21.95 γ-榄香烯 C15H24 204 0.60 ± 0.19 0.97 ± 0.16 1.31 ± 0.23 12 22.23 匙叶桉油烯 C15H24O 220 - 1.60 ± 0.18 3.57 ± 0.21 13 22.38 氧化石竹烯 C15H24O 220 - 1.20 ± 0.14 5.71 ± 0.19 14 22.60 表蓝按醇 C12H26O 222 - 1.18 ± 0.15 8.75 ± 0.16 15 22.75 1-三异丙基甲硅烷基-苯并环丁烯 C17H28Si 260 - - 0.76 ± 0.17 16 22.81 1-(7a-Methyloctahydro-1H-inden-1-yl) ethanone C12H20O 180 - - 0.90 ± 0.15 17 20.90 3, 4-二甲基-3-环己烯-1-甲醛 C9H14O 138 - - 1.52 ± 0.14 18 23.16 γ-桉叶油醇 C15H26O 222 - 2.35 ± 0.13 8.76 ± 0.14 19 23.29 愈创木醇 C15H26O 222 - 3.22 ± 0.16 3.41 ± 0.18 20 23.37 马兜铃烯 C15H24 204 - 2.09 ± 0.21 2.66 ± 0.22 21 23.46 γ-杜松烯 C15H24 204 - 11.40 ± 0.17 9.56 ± 0.19 22 23.56 δ-杜松醇 C15H26O 222 - 3.24 ± 0.12 3.18 ± 0.14 23 23.78 τ-杜松醇 C15H26O 222 - - 4.29 ± 0.12 24 23.84 桉叶油-4(14)-烯-11-醇 C15H26O 222 - - 13.59 ± 0.15 25 25.52 (+)-喇叭烯 C15H24 204 - - 2.23 ± 0.06 26 8.49 左旋-α-派烯 C10H16 136 - 2.62 ± 0.18 - 27 9.02 莰烯 C10H16 136 7.59 ± 0.19 4.87 ± 0.17 - 28 9.89 β-蒎烯 C10H16 136 3.98 ± 0.23 4.57 ± 0.21 - 29 10.25 β-月桂烯 C10H16 136 2.67 ± 0.21 0.56 ± 0.22 - 30 11.48 香芹烯 C10H16 136 1.54 ± 0.15 3.44 ± 0.19 - 31 11.59 桉叶素 C10H18O 154 11.41 ± 0.12 1.61 ± 0.13 - 32 11.67 β-反式-罗勒烯 C10H16 136 - 1.28 ± 0.18 - 33 11.99 β-顺式-罗勒烯 C10H16 136 12.00 ± 0.13 0.93 ± 0.15 - 34 15.75 α-萜品醇 C10H18O 154 0.63 ± 0.13 - 35 20.73 香树烯 C15H24 204 - 0.96 ± 0.17 - 36 20.87 α-愈创木烯 C15H24 204 - 3.70 ± 0.12 - 37 8.13 三环烯 C10H16 136 0.68 ± 0.19 - - 38 8.48 α-蒎烯 C10H16 136 3.39 ± 0.21 - - 39 9.72 香桧烯 C10H16 136 2.66 ± 0.18 - - 40 10.76 α-水芹烯 C10H16 136 1.40 ± 0.17 - - 41 11.66 右旋-α-派烯 C10H16 136 2.52 ± 0.19 - - 42 13.48 β-芳樟醇 C10H18O 154 1.60 ± 0.15 - - 43 14.69 2-茨酮 C10H16O 152 1.05 ± 0.13 - - 44 15.42 4-萜品醇 C10H18O 154 0.75 ± 0.14 - - 45 20.86 花柏烯 C15H24 204 1.61 ± 0.21 - - 46 22.18 4-氧化-β-紫罗兰酮 C16H26O 234 - 0.70 ± 0.14 - 47 21.15 δ-栀子 C15H24 204 - 1.06 ± 0.15 - 48 21.65 [1R-(1α, 3α,4β)]-4-乙烯基-α, α, 4-三甲基-3-(1-异丙烯基)-环己甲醇 C15H26O 222 17.05 ± 0.13 5.99 ± 0.16 - 49 22.62 绿花白千层醇 C15H26O 222 2.39 ± 0.19 8.12 ± 0.14 - 50 22.95 荜澄茄油烯醇 C15H26O 222 - 0.66 ± 0.13 - 51 23.86 β-桉叶醇 C15H26O 222 - 14.98 ± 0.16 - 52 26.02 2, 3, 3-Trimethyl-2-[(1E)-3-methyl-1, 3-butadienyl]-6-methylen C15H22O 218 - 0.55 ± 0.15 - 说明:“-”表示未检测到。相对含量为均值±标准差 -
[1] 陈欢, 章家恩.植物精气研究进展[J].生态科学, 2007, 26(3):281-287. CHEN Huan, ZHANG Jiaen. Advances in the study of phytoncidere[J]. Ecol Sci, 2007, 26(3):281-287. [2] 吴楚材, 吴章文, 罗江滨.植物精气研究[M].北京:中国林业出版社, 2006. [3] ATKINSON R. Atmospheric chemistry of VOCs and NOx[J]. Atmos Environ, 2000, 34:2063-2101. [4] LERDAU M, GRAY D. Tansley review:the ecology and evolution of light-dependent and light-independent volatile ogrnaic carbon emission by plants[J]. New Phytol, 2003, 157(2):199-211. [5] ALVARENGA I C A, PACHECO F V, SILVA S T, et al. In vitro culture of Achillea millefolium L. quality and intensity of light on growth and production of volatiles[J]. J Plant Biotechnol, 2015, 122(2):299-308. [6] 姜冬月, 李永红, 沈鑫.芸香叶片和花瓣释放挥发性有机物成分及其变压规律[J].浙江农林大学学报, 2018, 35(3):572-580. JIANG Dongyue, LI Yonghong, SHEN Xin. Components and variation of volatile organic compounds released from leaves and flowers of Ruta graveolens[J]. J Zhejiang A&F Univ, 2018, 35(3):572-580. [7] GUENTHER A B, MONSON R K, FALL R. Isoprene and monoterpene emission rate variability:observations with eucalyptus and emission rate algorithm development[J]. J Geophys Res, 1991, 96(D6):10799-10808. [8] SHAKREY T D, CHEN X, YEH S. Isoprene increase thermotolerance of fosmidomycin-fed leaves[J]. Plant Physiol, 2001, 125(4):2001-2006. [9] SHARKEY T D, LORETO F. Water stress, temperature, and light effects on the capacitt for isoorene emission and photosynthesis of kudzu levaes[J]. Oecologia, 1993, 95(3):328-333. [10] GERSHENZON J. Changes in the level of plant secondary metabolites under water and nutrient stress[J]. Recent Adv Phytochem, 1984, 18:273-320. [11] KIM J C. Factors controlling natural VOC emissions in a southeastern US pine forest[J]. Atmos Environ, 2001, 35(19):3279-3292. [12] JANSON R. Monoterpene emissions from scots pine and norwegian spruce[J]. J Geophys Res, 1993, 98(D2):2839-2850. [13] JOCHUN K, KIJOON K, DEUGSOO K, et al. Seasonal variations of monoterpene emissions from coniferous trees of different ages in Korea[J]. Chemosphere, 2005, 59(11):1685-1696. [14] 马楠. 16种常用园林植物VOCs成分研究及AHP评价[D].杭州: 浙江农林大学, 2012. MA Lan. The Research on 16 Common Landscape Plants VOCs and AHP Evaluation[D]. Hangzhou: Zhejiang A&F University, 2012. [15] 刘玉壶.中国植物志:第30卷第1分册[M].北京:科学出版社, 1996:82-85.. [16] 徐植灵, 潘炯光, 赵中振.辛夷挥发油的研究[J].中国中药杂志, 1989, 14(5):38-40. XU Zhiling, PAN Jiongguang, ZHAO Zhongzhen. Study on the volatile oil of Magnolia liliflora[J]. China J Chin Mater Med, 1989, 14(5):38-40. [17] 雷凌华, 于晓英, 李炎林.不同季节黄心夜合鲜嫩枝的挥发性成分研究[J].湖南农业大学学报(自然科学版), 2016, 42(3):296-300. LEI Linghua, YU Xiaoying, LI Yanlin. Analysis of volatile oil components from fresh twigs of Michelia martini Levl. in four seasons[J]. J Hunan Agric Univ Nat Sci, 2016, 42(3):296-300. [18] 雷凌华, 李胜华, 曾军英, 等.黄心夜合不同季节鲜叶挥发性成分研究[J].植物科学学报, 2017, 35(1):107-114. LEI Linghua, LI Shenghua, ZENG Junying, et al. Study on the volatile components in fresh leaves in four seasons of Michelia martinii Levl.[J]. Plant Sci J, 2017, 35(1):107-114. [19] 雷凌华.黄心夜合精气成分及其释放动态与生物活性研究[D].长沙: 湖南农业大学, 2015: 65-67. LEI Linghua. Study on Chemical Components and their Emission Dynamics Variation and Bioactivities in the Volatile Gas from Michelia martinii[D]. Changsha: Hunan Agricultural University, 2015: 65-67. [20] FUJIMOTO Y, SAKUMA S, KOMATSU S, et al. Inhibition of 15-hydroxyprostahlandin dehydrogenase activity in rabbit gastricantral mucosa by panaxynol isolated from oriental medicines[J]. J Pharm Pharmcol, 1998, 50(9):1075-1078. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.2019.01.024






 下载:
下载: