-
棘托竹荪Dictyophora echinovolvata属担子菌门 Basidiomycotina 腹菌纲 Gasteromycetes 鬼笔科 Phallaceae 竹荪属 Dictyophora 真菌,是中国科学工作者发现并于1988年定名的新种[1]。棘托竹荪是一种名贵的食用菌,香气浓郁,脆嫩爽口,并具有降低血液中脂肪、胆固醇和延缓食品腐败的功能[2]。卢惠妮等[3]研究发现棘托竹荪提取物对5种常见的食源性致病菌均具有明显抑制作用,抑菌率从大到小依次为副溶血弧菌 Vibrio parahaemolyticus,单增李斯特菌 Listeria monocytogenes,大肠埃希菌 Escherichia coli O157:H7,肠炎沙门氏菌 Salmonella enteritidis,金黄色葡萄球菌 Staphylococcus aureus。棘托竹荪提取物同时具有较高的热稳定性和广泛的pH值稳定性;刘文波等[4]利用超声波辅助破碎竹荪干粉,制取水、乙醇和石油醚为提取介质的浸提物以及竹荪挥发油,利用液体培养基连续稀释法对5种供试菌:大肠埃希菌、肠炎沙门菌、副溶血性弧菌、金黄色葡萄球菌和单增李斯特菌等进行抑菌实验,结果所有提取物对供试菌都具有抑菌活性;梁鸣等[5]报道棘托竹荪醇提取物抑菌效果优于水提取物。尽管目前国内外对棘托竹荪的研究已比较广泛,但对乙醇提取工艺的优化研究还比较少,且目前对于竹荪抑菌作用的研究绝大多数还集中在对食品腐败菌的研究,对植物病原菌的抑菌研究尚未见报道。本研究对棘托竹荪抑菌活性物质的乙醇提取工艺进行优化,测定了提取液对常见食品腐败菌与部分植物病原真菌的抑制效果,以期为利用竹荪开发成天然的食品防腐剂和生物农药奠定基础。
HTML
-
棘托竹荪子实体干品购于浙江菇尔康食用菌有限公司,鼓风干燥箱60 ℃烘干至恒量,粉碎物过80目筛,密封避光保存。
-
选用常见食品腐败菌:大肠埃希菌,金黄色葡萄球菌,枯草芽孢杆菌 Bacillus subtilis,蜡状芽孢杆菌 Bacillus cereus 和啤酒酵母 Saccharomyces cerevisiae;部分植物病原真菌:玉米大斑病菌 Exserohilum turcicum,油菜菌核病菌 Sclerotinia sclerotiorum,番茄灰霉病菌 Botrytis cinerea,苹果腐烂病菌 Valsa mali和小麦赤霉病菌 Fusarium graminearum 为供试菌。菌种由生物农药高效制备技术国家地方联合工程实验室与浙江农林大学林业与生物技术学院微生物学实验室提供。
-
马铃薯葡萄糖琼脂(PDA)培养基:马铃薯200.00 g,葡萄糖20.00 g,琼脂20.00 g。马铃薯去皮切成块煮30 min,用纱布过滤取汁,加葡萄糖和琼脂溶化,补水至1 000 mL,pH值自然。Luria-Bertani(LB)培养基:胰化蛋白胨10.00 g,酵母提取物5.00 g,氯化钠 10.00 g,补水至1 000 mL,pH值自然。培养基121 ℃蒸汽灭菌20 min备用。
-
取棘托竹荪粉末10.00 g,分别按照33.3,40.0,50.0,66.7,100.0 g·L-1的料液比加入60.0,70.0,80.0,90.0,1 000.0 g·kg-1的乙醇水溶液,混匀后置于60,65,70,75,80 ℃水浴锅中处理1.5,2.0,2.5,3.0,3.5 h,过滤,所得滤渣再按原条件进行抽提,过滤,弃滤渣,合并2次滤液,过滤除菌浓缩到10.0 mL,置于4 ℃下保存备用。
-
①供试菌株的准备。在无菌室中将供试菌株接入相应斜面培养基上,细菌37 ℃恒温培养18~24 h,植物病原真菌、酵母菌在30 ℃恒温培养44~48 h后备用。②供试菌悬液制备。用接种环挑取少许菌体于装有9.0 mL无菌水的试管内,制成菌悬液。细菌用麦氏比浊法计数,酵母菌用血球计数板计数,调整菌悬液比例为含细胞(或孢子)量109~1010个·L-1。③对食品腐败菌抑菌作用测定。吸取0.2 mL供试细菌悬液涂布于LB平板上,37 ℃培养18~24 h,0.2 mL啤酒酵母涂布于PDA平板上,30 ℃培养48 h,采用祖若夫等[6]的牛津杯法测定抑菌圈,重复3次。④对植物病原真菌的抑制率测定。吸取0.2 mL质量浓度为100.0 g·L-1棘托竹荪提取液涂布于PDA平板上制成含药培养基平板,在对照上则涂布相同体积的溶剂;用打孔器取直径为8 mm的供试菌菌饼,移至含药培养基平板中央,使菌饼培养基面向上;置于26 ℃培养44~48 h,采用欧阳桐娇等[7]的菌丝生长速率法测定菌落直径,重复3次,用公式(1)计算抑菌率。
-
①乙醇体积分数对提取物抑菌能力的影响。准确称取10.00 g竹荪粉末,以50.0 g·L-1的料液比分别加入到体积分数为60%,70%,80%,90%和100%的乙醇水溶液中,于80 ℃水浴2 h后过滤,收集滤渣,用滤渣代替竹荪粉末,用相同的方法再处理1次,合并2次的滤液,过滤并浓缩至10.0 mL。按照方法1.2.2节中③以金黄色葡萄球菌作为指示菌种测定提取液的抑菌圈直径。②料液比对提取物抑菌能力的影响。准确称取10.00 g竹荪粉末,分别以33.3,40.0,50.0,66.7,100.0 g·L-1的料液比加入到体积分数90%乙醇水溶液中,于80 ℃水浴2.0 h后过滤,之后操作同①。③浸提时间对提取物抑菌能力的影响。准确称取10.00 g竹荪粉末,以50.0 g·L-1的料液比加入到体积分数为90%乙醇水溶液中,于80 ℃分别水浴1.5,2.0,2.5,3.0,3.5 h后过滤,之后操作同①。④浸提温度对提取物抑菌能力的影响。准确称取10.00 g竹荪粉末,以50.0 g·L-1的料液比加入到体积分数90%乙醇水溶液中,分别于60,65,70,75和80 ℃水浴2.5 h后过滤,之后操作同①。⑤多因素正交试验。选择乙醇体积分数(A),浸提温度(B),料液比(C),浸提时间(D)4个因素进行4因素3水平正交设计,采用L9(34)正交表进行正交试验以确定最佳工艺参数(表 1)。
水平 A乙醇体积分数/% B料液比/ (g·L-1) C浸提时间/h D浸提温度/℃ 1 80 66.7 2.0 65 2 90 50.0 2.5 70 3 100 40.0 3.0 75 Table 1. Factors and levels of orthogonal experiment
1.1. 材料
1.1.1. 供试材料
1.1.2. 供试菌
1.1.3. 培养基
1.2. 方法
1.2.1. 提取方法
1.2.2. 抑菌试验
1.2.3. 提取工艺优化试验
-
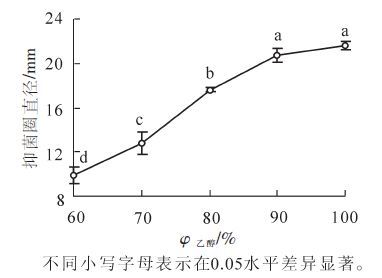
乙醇提取液对金黄色葡萄球菌的抑菌结果见图 1。从图 1可见:随着乙醇体积分数的加大,抑菌效果不断增强,乙醇体积分数从60%~90%时,抑菌圈直径显著增加(P<0.05),而乙醇体积分数为90%~100%时,抑菌圈直径增加不显著,综合考虑工艺成本,确定90%乙醇水溶液为竹荪提取溶剂。乙醇体积分数的差异造成抑菌圈直径的显著差异,可能是因为不同体积分数乙醇提取液的抑菌成分存在差异,乙醇体积分数高更有利于抑菌物质的浸出。
-
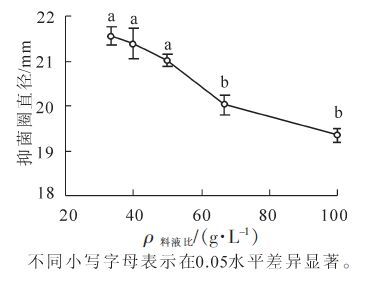
从图 2可以看出:随着料液比的增加,提取液的抑菌效果不断下降,料液比从33.3 g·L-1到40.0 g·L-1和50.0 g·L-1,从66.7 g·L-1到100.0 g·L-1,抑菌圈直径降低均不显著,而料液比从50.0 g·L-1到66.7 g·L-1,抑菌圈直径显著降低(P<0.05),因此确定在料液比为50.0 g·L-1时进行抑菌物质的提取。固液提取中,料液比的大小在较大程度上影响着传质的效率和速度,浓度差是提取过程的一个推动力,保持良好的浓度差可得到较好的提取效果[8]。
-
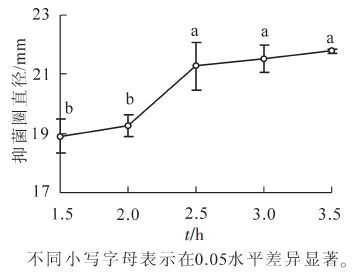
分别浸提1.5,2.0,2.5,3.0与3.5 h后,乙醇提取液对金黄色葡萄球菌的抑菌结果见图 3。由图 3可得:随着浸提时间的增加,提取液的抑菌效果不断上升,提取时间从1.5 h增加到2.0 h,从2.5 h增加到3.0 h和3.5 h,抑菌圈直径增加均不显著,而提取时间从2.0 h增加到2.5 h,抑菌圈直径显著增加(P<0.05)。综合考虑时间成本,确定提取时间为2.5 h。
-
从图 4可见:随着浸提温度的升高,提取液的抑菌效果不断上升,提取温度从60 ℃增加到65 ℃和70 ℃,抑菌圈直径显著增加(P<0.05),而提取温度从70 ℃增加到75 ℃和80 ℃,抑菌圈直径增加均不显著,综合考虑能源成本,确定提取温度为70 ℃。提取温度是影响浸出效果的重要因素,温度高有利于有效成分的溶解和渗透扩散,促进其浸出[9]。
-
以金黄色葡萄球菌为测试菌株,对棘托竹荪子实体的提取工艺进行乙醇体积分数、料液比、浸提时间、浸提温度等4个因素的3个水平进行正交实验测试,结果见表 2。从表 2极差分析结果可知:影响竹荪有效成分提取率的主次因素顺序为A(乙醇体积分数)>D(浸提温度)>B(料液比)>C(浸提时间),A2B3C1D3为提取参数因子的最佳组合,即乙醇体积分数为90%,料液比为40.0 g·L-1,浸提时间为2.0 h,浸提温度75 ℃。
试验号 A乙醇体积分数 B料液比 C浸提时间 D浸提温度 抑菌圈直径/mm 1 1 1 1 1 15.14 2 1 2 2 2 16.23 3 1 3 3 3 18.13 4 2 1 2 3 21.77 5 2 2 3 1 19.66 6 2 3 1 2 21.80 7 3 1 3 2 20.80 8 3 2 1 3 22.00 9 3 3 2 1 20.00 K1 49.50 57.71 58.94 54.80 K2 63.23 57.90 58.00 58.83 K3 62.80 59.94 58.59 61.90 k1 16.50 19.24 19.65 18.27 k2 21.08 19.30 19.33 19.61 k3 20.93 19.98 19.53 20.63 R 4.58 0.74 0.32 2.36 最优水平 A2 B3 C1 D3 Table 2. Design and results of orthogonal experiment
对4个因素进行方差分析,结果见表 3。从表 3可见:A和D因子对提取液抑菌效果有显著性影响(P<0.05),B和C因子对提取液抑菌没有显著性影响。说明乙醇体积分数、浸提温度对竹荪中抑菌物质的提取效果起主要作用。
变异来源 平方和 自由度 均方 F值 显著性 乙醇体积分数 121.86 2 60.93 137.05 ** 料液比 3.06 2 1.53 3.44 浸提时间 0.46 2 0.23 0.51 浸提温度 25.34 2 12.67 28.50 ** e 8.00 18 0.44 总合 158.72 8 说明:F0.05(2,18)=3.55;F0.01(2,18)=6.01。** 表示在0.05水平下差异显著(P<0.05)。 Table 3. VARA analyze of orthogonal experiment
-
按照正交实验优化的提取工艺对棘托竹荪的抑菌物质进行提取,测得的它对食品腐败菌和植物病原真菌的抑菌结果分别见表 4~5。由表 4可见:棘托竹荪乙醇提取液对食品腐败细菌均具有抑制作用,但对啤酒酵母不表现抑制作用。在供试的4种食品腐败细菌中,抑菌效果从高到低依次是金黄色葡萄球菌、枯草芽孢杆菌、蜡状芽孢杆菌和大肠埃希菌。其中提取物对金黄色葡萄球菌的抑菌圈直径显著大于枯草芽孢杆菌与蜡状芽孢杆菌(P<0.05),同时提取物对这3种革兰氏阳性菌(G+)的抑菌圈直径亦显著大于革兰氏阴性菌(G-)大肠埃希菌(P<0.05),可见在当前优化工艺下,棘托竹荪乙醇提取液对革兰氏阳性菌的抑制效果显著大于对革兰氏阴性菌的抑制效果。
供试菌 抑菌直径/mm 大肠埃希菌 22.6±0.51 c 金黄色葡萄球菌 24.08±0.33 a 枯草芽孢杆菌 23.12±0.54 b 蜡状芽孢杆菌 23.02±0.45 b 啤酒酵母 0.00±0.00d Table 4. Antimicrobial activity of the ethanol extract on tested bacteria and Saccharomyces cerevisiae
供试真菌 抑菌率/% 油菜菌核病菌 57.67±0.77 b 苹果腐烂病菌 9.26±0.43 e 玉米大斑病菌 75.01±0.82 a 小麦赤霉病菌 21.34±0.58 d 番茄灰霉病菌 49.65±0.56 c Table 5. Antimicrobial activity of the ethanol extract on phytopathogenic fungi
从表 5可知:棘托竹荪乙醇提取液对供试5种植物病原真菌菌丝生长的抑制效果从高到低依次为玉米大斑病菌、油菜菌核病菌、番茄灰霉病菌、小麦赤霉病菌和苹果腐烂病菌,且五者间的差异均为显著(P<0.05),可见棘托竹荪乙醇提取液对真菌菌丝生长具有广谱的抑制作用,但抑制作用强弱因真菌种类而异。
2.1. 单提取工艺因素试验结果
2.1.1. 乙醇体积分数对提取物抑菌能力的影响
2.1.2. 料液比对提取物抑菌能力的影响
2.1.3. 浸提时间对提取物抑菌能力的影响
2.1.4. 浸提温度对提取物抑菌能力影响
2.2. 多提取因素正交试验结果
2.3. 抑菌效果
-
获得棘托竹荪子实体抑菌物质提取优化工艺为:乙醇体积分数90%,料液比40.0 g·L-1,浸提时间2.0 h,浸提温度75 ℃。极差分析确定影响竹荪有效成分提取率效率的主次因素顺序为A(乙醇体积分数)>D(浸提温度)>B(料液比)>C(浸提时间),A2B3C1D3为提取参数因子的最佳组合,即乙醇体积分数为90%,料液比为40.0 g·L-1,浸提时间为2.0 h,浸提温度75 ℃。方差分析发现乙醇体积分数和浸提温度对竹荪抑菌有效成分提取起关键作用。
本研究结果表明:棘托竹荪乙醇浸提液对食品腐败细菌有明显抑菌效果,但对啤酒酵母不表现抑制作用,该结果与郝景雯等[10-11]和宋飞飞等[12]的研究结论一致。棘托竹荪乙醇浸提液对4种供试细菌的抑菌效果从强到弱依次是金黄色葡萄球菌、枯草芽孢杆菌、蜡状芽孢杆菌和大肠埃希菌,与林陈强[13]报道的结果一致。可见,革兰氏阳性菌相对革兰氏阴性菌对棘托竹荪乙醇提取物质更敏感。革兰氏阳性菌和革兰氏阴性菌细菌对棘托竹荪乙醇提取物的敏感性差异可能与革兰氏阳性菌和革兰氏阴性菌的细胞壁结构与组成的差异有关。棘托竹荪乙醇提取物对革兰氏阳性菌的抑制机理值得进一步探明。
本研究发现:竹荪醇提物对5种植物病原真菌均具有一定抑制作用,其中对植物生产危害性大的玉米大斑病菌、油菜菌核病菌、番茄灰霉病菌等3种植物病原菌抑制效果较好,因此,竹荪具有开发成生物农药的较大潜力。
梁鸣等[5]研究认为:棘托竹荪丙酮提取物的化学成分主要成分为酮、有机酸、倍半萜、酯等,其中酮类物质占主导地位,其对细菌抑菌作用明显,而对霉菌和酵母菌抑菌作用不明显。罗盛莲等[14]研究表明:棘托竹荪乙酸乙酯浸膏水溶液的主要成分是脂肪酸及其酯类、烯烃、邻苯二甲酸酯类、酚类和酮类,其中有机酸和芳香酯类含量较多,对供试的细菌、霉菌和酵母菌均有明显抑菌作用。迄今为止,棘托竹荪乙醇提取物中抑菌活性物质的化学成分尚未明确,值得进一步探讨。
由于竹荪本身是一种名贵食用菌,具有较大的食用与保健功能,其可食部分价格较高,为竹荪开发利用带来了一定的阻力,但是竹荪采收加工时,菌盖和菌托均被弃而不用,而这2部分占总生物量的60%以上[15]。檀东飞等[16]用水蒸汽蒸馏法提取棘托竹荪菌托干品挥发油,表明其挥发油对受试的霉菌、酵母菌、细菌都有强的抑菌作用,若棘托竹荪的菌盖和菌托可提取抑菌活性物质而加以利用,可变废为宝。这些都值得进一步深入研究。










 DownLoad:
DownLoad: