-
近年中国农田土壤镉(Cd)和砷(As)复合污染形势严峻,点位超标率高达19.4%,污染面积约占全国耕地的1/6[1]。由于Cd和As的化学行为对pH和氧化还原电位(Eh)的响应截然相反,传统的单一修复手段难以兼顾。原位钝化是主要修复技术之一,其中生物质炭因多孔及碱性特征广泛用于阳离子重金属(如Cd)修复,但其对阴离子As吸附能力较弱,且易造成二次污染[2]。通过负载铁氧化物制备磁性生物质炭虽可增强对As的专性吸附,但在淹水条件下易诱发水稻Oryza sativa铁毒效应,且灰分增加可能活化孔隙水中的Cd[3−5]。有研究表明:硅(Si)不仅能通过共沉淀和特定吸附协同降低土壤有效态Cd、As,还能缓解铁毒并促进水稻生长[6−8]。因此,对生物质炭进行磁改性并负载Si材料,构建富硅-磁性生物质炭(SBC),有望克服单一材料缺陷,提升Cd-As复合污染修复效能。
外源材料对“重金属-作物”系统的调控不仅依赖于理化钝化,还涉及微生物群落的生态响应。Si、铁(Fe)及生物质炭的添加会改变土壤重金属有效性及作物生理,进而重塑土壤微生物群落结构与功能[9−11]。更为重要的是,这种微生态效应会延伸至地上部。土壤微生物可通过蒸腾流或气流传播至叶际,作物生长及叶片性状的改变也会驱动叶际微生物组的演替[12]。重塑后的叶际微生物组能通过调控植物代谢、促进养分吸收等途径,反过来影响作物的重金属耐受性与生长发育[13−14]。
前期研究已确立了SBC的制备工艺并验证了其对水体Cd-As的吸附性能[15],但SBC在“土壤-水稻”体系中的应用潜力及其微生态机制尚待探究。现有研究多聚焦于根际土壤微生态,缺乏对“修复材料-作物生长-叶际微生物”级联响应的系统解析,特别是叶际微生物组在Cd-As协同阻控中的潜在机制尚不明确。鉴于此,本研究通过水稻盆栽试验,验证SBC对Cd-As复合污染的修复效果,并结合宏基因组技术,深入揭示SBC通过“材料-微生物-基因”多维调控影响叶际微生态、促进水稻生长及阻控重金属积累的机制,为实现重金属污染农田的安全利用提供理论依据。
-
Cd和As复合污染水稻土采自浙江省上虞市某矿区周边农用地(0~20 cm)。将采集土样风干、研磨后,过2 mm筛,室温保存。供试土壤基本理化性质如下:pH为5.72,土壤有机质为19.71 mg·g−1,土壤Cd、As总质量分数分别为0.98和71.72 mg·kg−1,高于GB
15618 —2018环境质量标准(Cd≥0.40 mg kg−1,As≥30.00 mg kg−1),砂粒、粉粒、黏粒质量分数分别占30.77%、58.37%和10.85%。 -
采用共沉淀-限氧热解法合成富硅-磁性生物质炭(SBC),制备工艺详见前期研究[7]。取水稻秸秆浸渍于Fe3+与Fe2+混合溶液,调节pH≥11,混合物静置过滤干燥后,添加质量分数为5%的硅酸钙,700 ℃热解2 h。普通生物质炭(BC)在相同热解条件下制备。BC与SBC的pH分别为7.9和8.3,比表面积分别为58.27和166.64 m2·g−1,孔容分别为0.048 2和0.116 9 cm3·g−1,孔径分别为3.236和2.796 nm,材料表观结构、表面晶体组成、磁滞回线等表征信息详见前期研究[7]。
-
于恒温温室开展水稻(‘甬优8050’‘Yongyou 8050’)盆栽试验。设对照(ck)、质量分数为1%的生物质炭(BC)及质量分数为1%的富硅-磁性生物质炭(SBC)共3个处理(n=4)。每盆装复合污染土4.0 kg,基施尿素0.2 g·kg−1、磷酸二氢钾0.1 g·kg−1。钝化剂混匀后调节含水量至60%田间持水量,平衡15 d后移栽。采用干湿交替水分管理,分蘖期保持3~4 cm水层,生殖生长期行干湿交替(淹水10 d自然落干),收获前10 d断水。分别于分蘖期(45 d)和成熟期(102 d)采集根际土与植株,测定理化及重金属指标,同步采集鲜叶于−80 ℃保存,用于宏基因组测序(编号:时期代码T/M+处理代码)。
-
采集水稻分蘖期与成熟期的根际土,参照ISO 10390测定pH (土水体积比为1.0∶2.5);可溶性有机碳(DOC)经0.01 mol·L−1氯化钙(CaCl2)浸提后用TOC仪检测。有效态Cd、As分别采用0.01 mol·L−1 CaCl2和0.05 mol·L−1磷酸二氢铵(NH4H2PO4)(体积比为1∶25,16 h)浸提,滤液经石墨炉原子吸收分光光度计(AA-
7000 )及双通道原子荧光分光光度计测定。Cd、As标样回收率分别为97%和96%。同步采集水稻植株,用直尺测量株高(茎基部至最高叶尖),并将根、茎叶、籽粒烘干至恒量测定干质量。准确称取0.100 0 g烘干植株样品,加入8 mL浓硝酸和2 mL 过氧化氢(H2O2)微波消解后,测定植株中Cd、As质量分数。采集水稻分蘖期与成熟期新鲜叶片,液氮速冻后于−80 ℃保存。经组织研磨仪(Tissuelyser-48)处理,取0.2 g样品采用MagBeads FastDNA Kit for Soil提取总DNA。DNA经Qubit 4及质量浓度为1%的琼脂糖凝胶电泳检测合格后,构建Illumina TruSeq DNA文库并测序(上海派森诺)。测序数据经fastp质控后,用minimap2去除宿主序列[16],所得高质量序列再用Kaiju进行物种注释[17]。序列经Megahit (v1.1.2)组装后利用Prodigal预测基因[18],通过MMseqs2工具,基于京都基因与基因组百科全书(KEGG)和基因本体论(GO)数据库进行功能注释[19]。 -
数据处理与绘图采用Excel 2021、SPSS 26及Origin 2018。生物信息学分析基于RStudio (v0.99.446)平台完成:利用phyloseq计算α多样性指标;调用vegan包计算Bray-Curtis距离,进行主坐标(PCoA)分析及PERMANOVA (adonis函数)检验;使用corMicro构建共生网络;通过冗余分析(RDA)及置换检验解析环境因子效应。各类图表均由ggplot2绘制,组间差异显著性采用one-way ANOVA (Duncan法)判定。
-
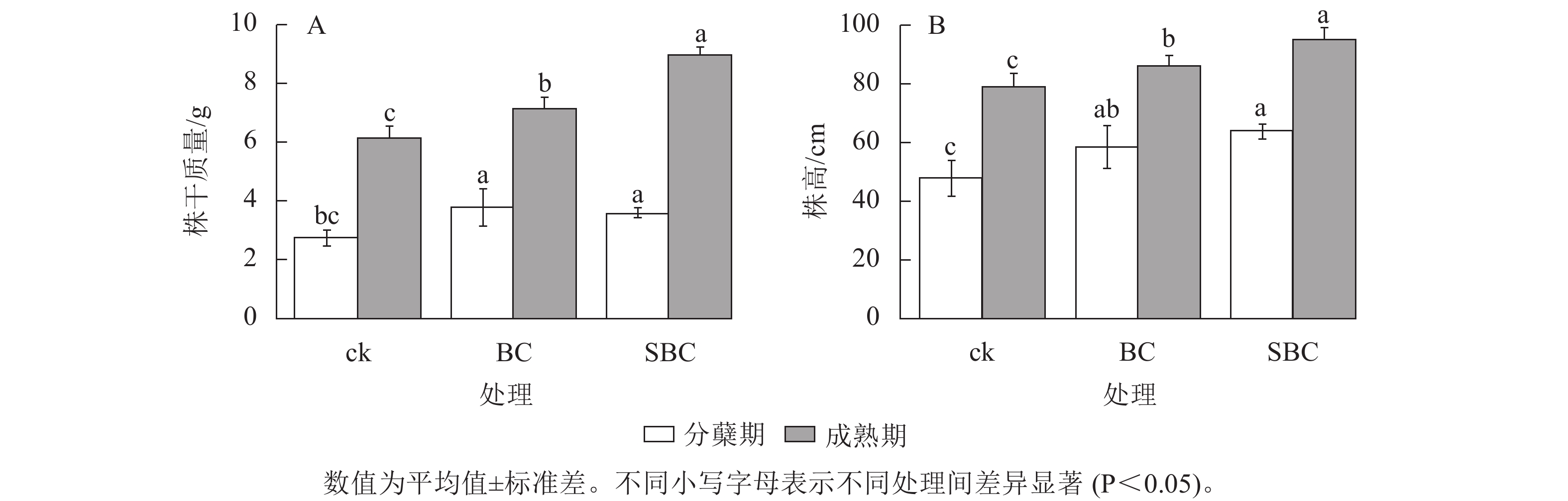
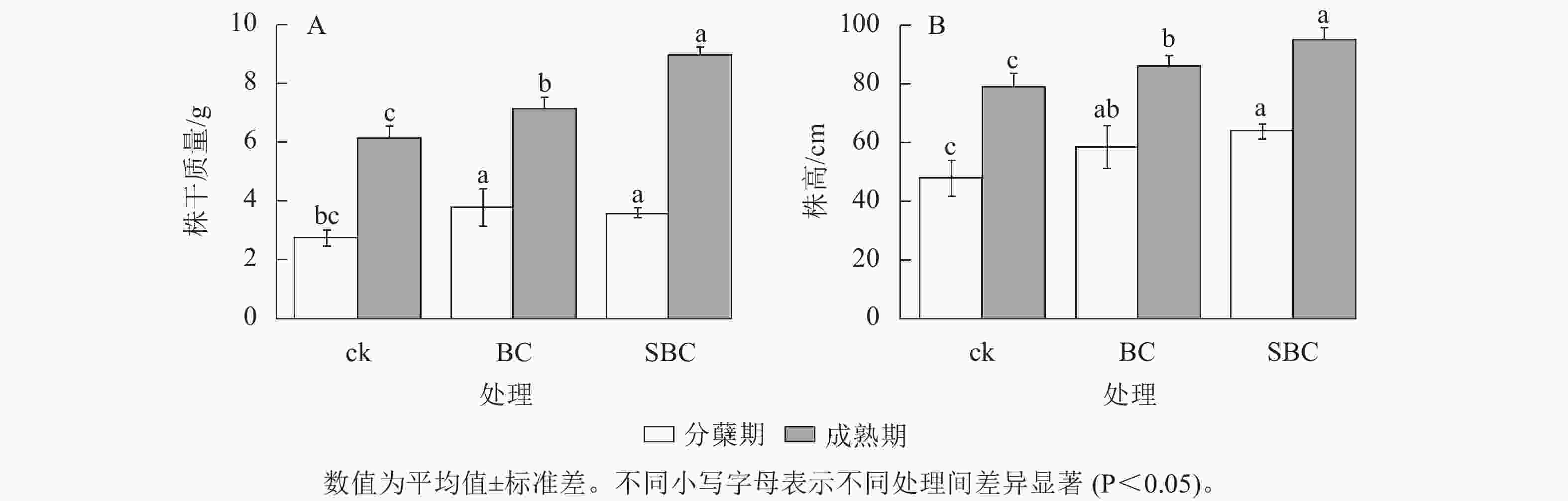
如图1所示:BC、SBC处理显著提升了水稻生物量积累(P<0.05)。水稻株干质量分蘖期较对照分别增加37.3%和26.7%,成熟期增幅达16.6%和46.7%。水稻株高生长响应呈现剂量效应,SBC处理在分蘖期和成熟期分别提高11.9%和25.0%,显著优于BC处理(P<0.05)。
-
与ck相比,各钝化处理均降低了分蘖期叶片Cd总量,且SBC优于BC (表1);SBC处理显著降低了叶片As总量。BC与SBC处理使成熟期叶片Cd总量较ck分别显著降低54.4%和38.4% (P<0.05)。BC处理则使成熟期叶片As总量显著升高81.9%,而SBC处理则使其显著降低38.6% (P<0.05)。
处理 分蘖期Cd/(mg·kg−1) 分蘖期As/(mg·kg−1) 根 茎 叶 根 茎 叶 ck 1.75±0.20 a 0.53±0.08 a 0.25±0.05 a 112.50±10.52 b 8.68±1.18 a 6.40±0.92 b BC 1.48±0.10 b 0.44±0.08 ab 0.14±0.02 b 137.62±22.86 a 9.15±0.71 a 7.99±0.99 a SBC 0.99±0.13 c 0.29±0.01 cd 0.12±0.02 b 50.92±8.55 c 4.17±0.52 c 4.83±1.29 c 处理 成熟期Cd/(mg·kg−1) 成熟期As/(mg·kg−1) 根 茎 叶 籽粒 根 茎 叶 籽粒 ck 1.84±0.50 a 0.44±0.03 a 0.21±0.04 a 0.20±0.03 a 123.36±19.76 a 6.61±1.70 a 4.06±2.30 b 1.76±0.46 b BC 1.61±0.15 a 0.46±0.07 a 0.09±0.03 b 0.15±0.04 b 136.19±8.85 a 8.54±1.35 a 7.39±0.46 a 2.22±0.13 a SBC 1.45±0.48 a 0.25±0.01 b 0.11±0.03 b 0.13±0.04 b 61.70±12.94 c 3.23±0.97 c 2.49±0.46 c 0.78±0.25 c 说明:不同字母表示同一部位不同处理间差异显著 (P<0.05)。 Table 1. Total amount of Cd and As in each part of rice at tillering stage
从表2可见:BC与SBC处理使籽粒Cd质量分数较ck分别显著降低25.4%和51.1% (P<0.05);BC处理使籽粒As质量分数显著升高25.9%,而SBC处理则使其显著降低55.6% (P<0.05)。BC与SBC处理均显著降低分蘖期与成熟期根际及非根际土壤有效态Cd质量分数(P<0.05);BC处理增加了土壤有效态As质量分数,SBC处理则使其显著降低(P<0.05)。这表明SBC通过降低土壤重金属有效性,实现了对水稻籽粒Cd和As累积的同步阻控。
处理 分蘖期根际 分蘖期非根际 pH DOC/
(mg·kg−1)有效态Cd/
(mg·kg−1)有效态As/
(mg·kg−1)pH DOC/
(mg·kg−1)有效态Cd/
(mg·kg−1)有效态As/
(mg·kg−1)ck 5.85±0.08 c 174.41±9.40 c 0.041 9±0.004 5 a 6.54±1.77 b 5.99±0.09 c 148.79±9.54 c 0.060 1±0.004 1 a 7.14±0.74 b BC 6.16±0.07 b 207.78±12.90 b 0.030 8±0.002 7 b 7.36±0.76 a 6.12±0.09 bc 203.70±13.81 b 0.031 5±0.002 4 b 8.34±0.85 a SBC 7.10±0.12 a 259.81±2.70 a 0.019 2±0.001 2 c 4.84±0.55 c 6.33±0.14 ab 251.49±20.10 a 0.026 6±0.004 2 b 5.09±0.51 c 成熟期根际 成熟期非根际 处理 pH DOC/
(mg·kg−1)有效态Cd/
(mg·kg−1)有效态As/
(mg·kg−1)pH DOC/
(mg·kg−1)有效态Cd/
(mg·kg−1)有效态As/
(mg·kg−1)ck 5.80±0.07 c 159.78±16.36 b 0.041 3±0.002 7 a 6.84±0.61 b 5.55±0.31 c 124.93±19.97 b 0.048 4±0.003 8 a 6.70±0.96 b BC 6.34±0.11 b 180.15±23.27 b 0.029 4±0.004 2 b 7.98±1.30 a 6.07±0.16 b 139.98±25.48 b 0.034 7±0.003 1 b 8.34±1.09 a SBC 6.94±0.18 a 277.88±22.88 a 0.012 4±0.001 0 c 4.82±0.24 c 6.41±0.23 a 222.76±21.30 a 0.018 3±0.003 0 c 5.66±0.14 c 说明:不同字母表示不同处理间差异显著 (P<0.05)。 Table 2. Concentrations of soil pH, DOC, bioavailable Cd and As concentrations in paddy soil under different treatments
-
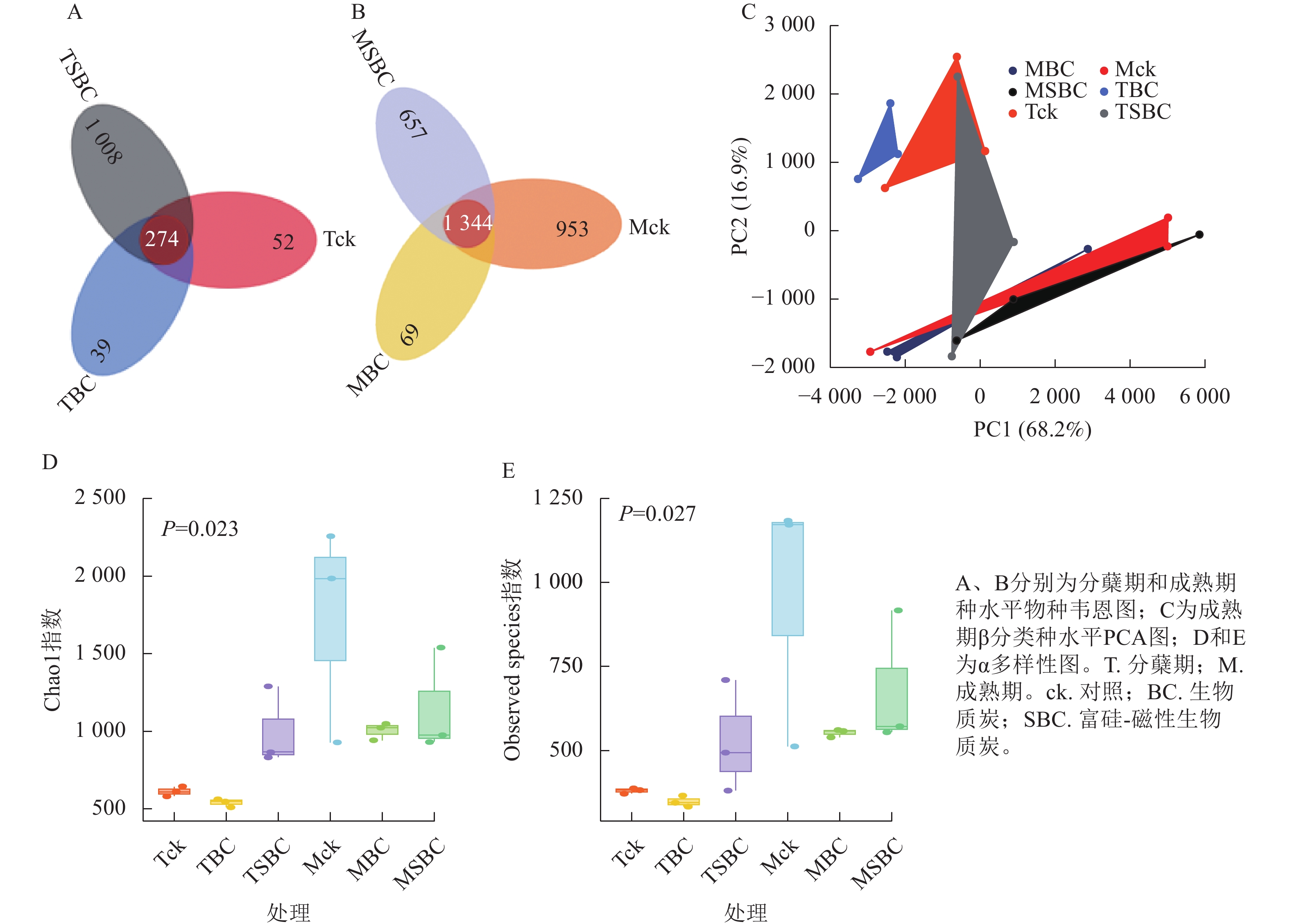
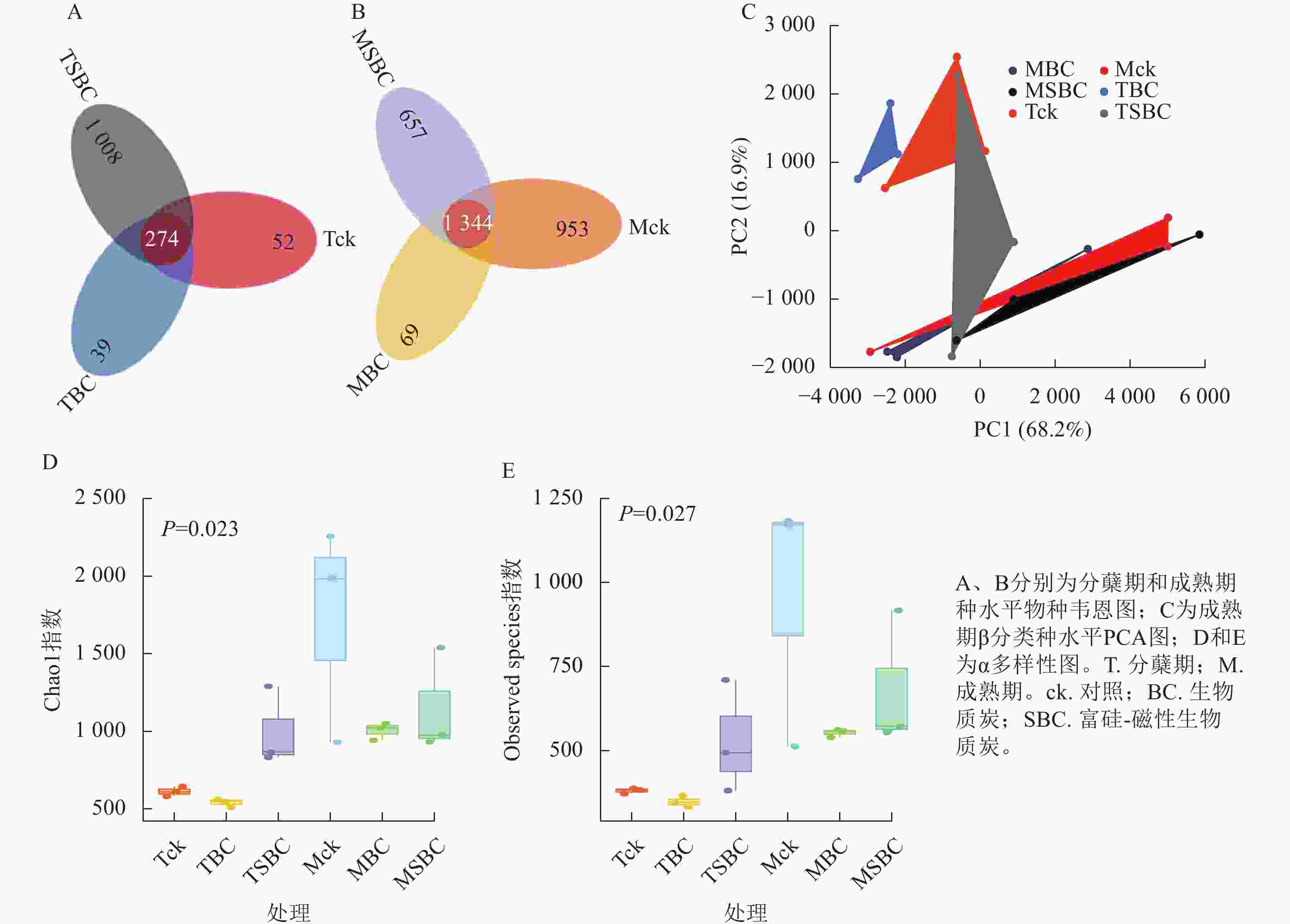
与ck相比,SBC添加提高了水稻分蘖期叶际微生物的数量和多样性,增加了群落中微生物间的相互联系与相互作用,使微生物的群落结构更加丰富和稳定。种水平韦恩图(图2A和图2B)显示:BC处理减少了2个时期微生物种类数,而SBC处理增加分蘖期但减少成熟期种类数。PCA分析(图2C)表明:同一时期ck与BC、SBC处理间群落结构差异明显,且分蘖期与成熟期差异更为突出。α多样性指数(图2D和E)进一步揭示:与ck相比,SBC显著提高了水稻分蘖期α多样性(Chao1和Observed species)指数(P<0.05),而BC与SBC处理均降低了水稻成熟期多样性(P<0.05)。
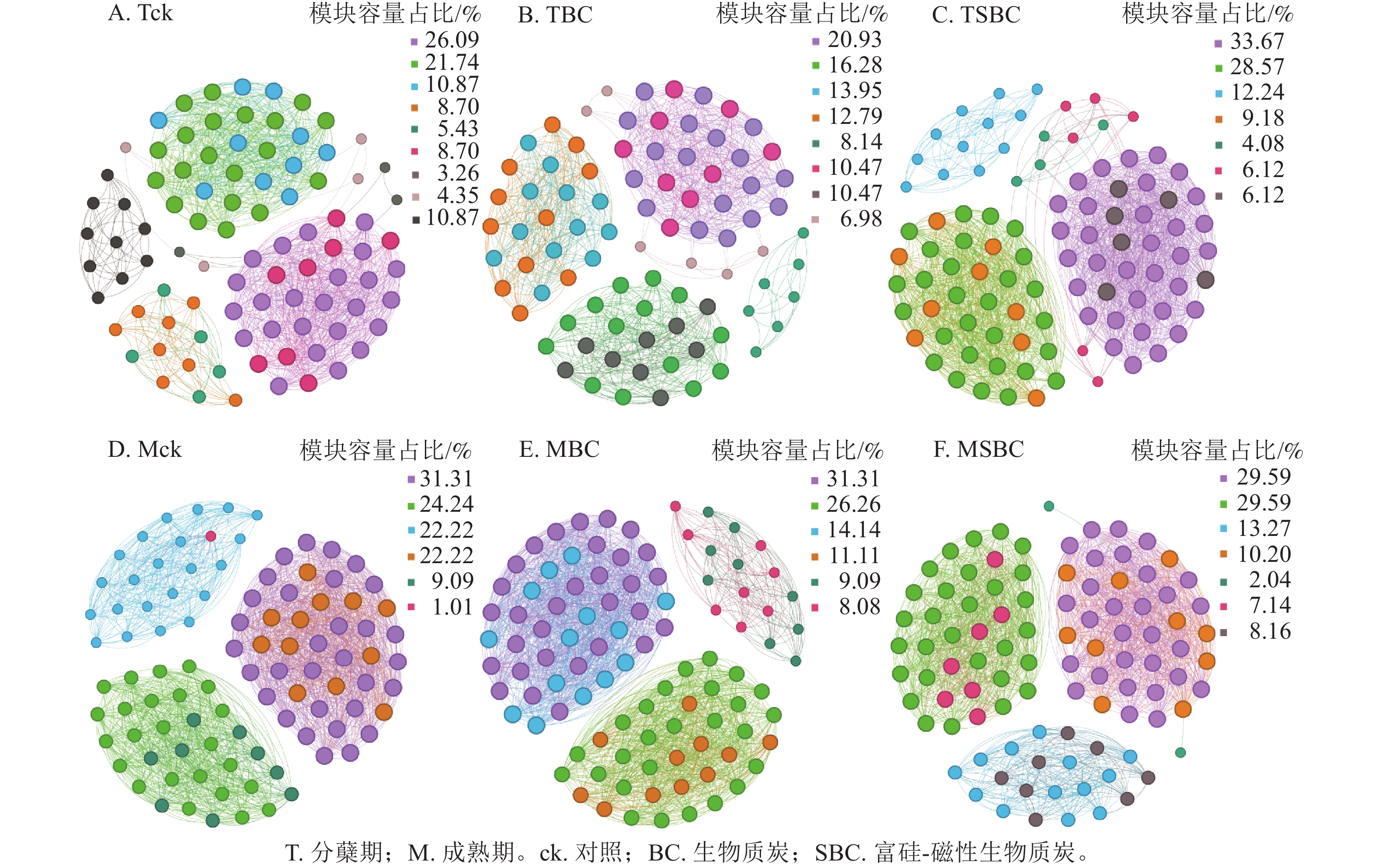
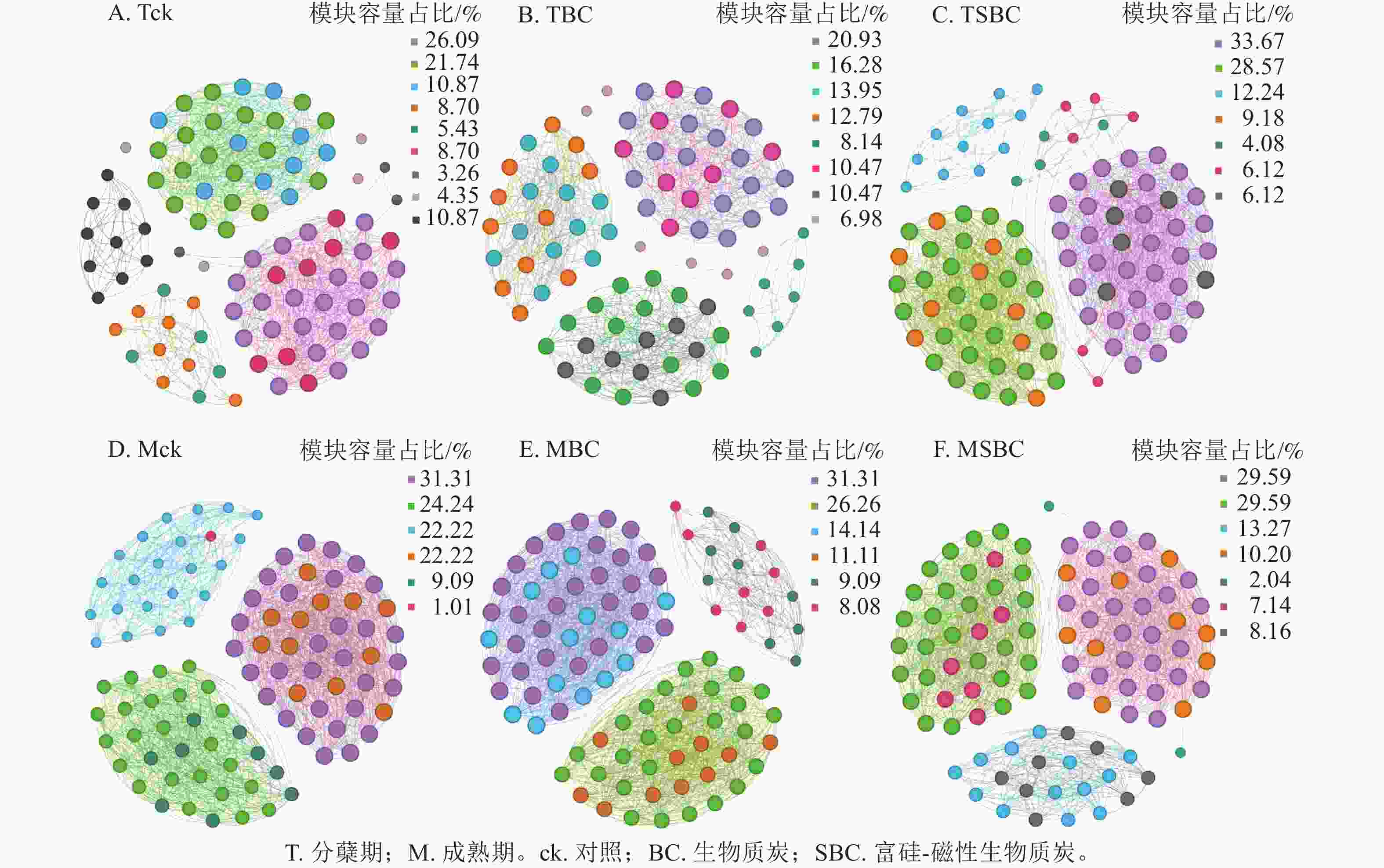
基于Spearman秩相关分析构建的共生网络(图3)显示:不同处理显著重塑了叶际微生物的互作模式(P<0.05)。整体网络呈现聚集性,划分为6~9个主要模块。在分蘖期,材料添加降低了网络模块化程度。ck处理包含9个模块,而BC与SBC处理分别降至8和7个。成熟期SBC处理的模块数增至7个,显著高于BC与ck。拓扑结构分析表明:分蘖期SBC处理组的边数、平均加权度及图密度均高于ck和BC,表明SBC促使叶际微生物群落稳定性增强。
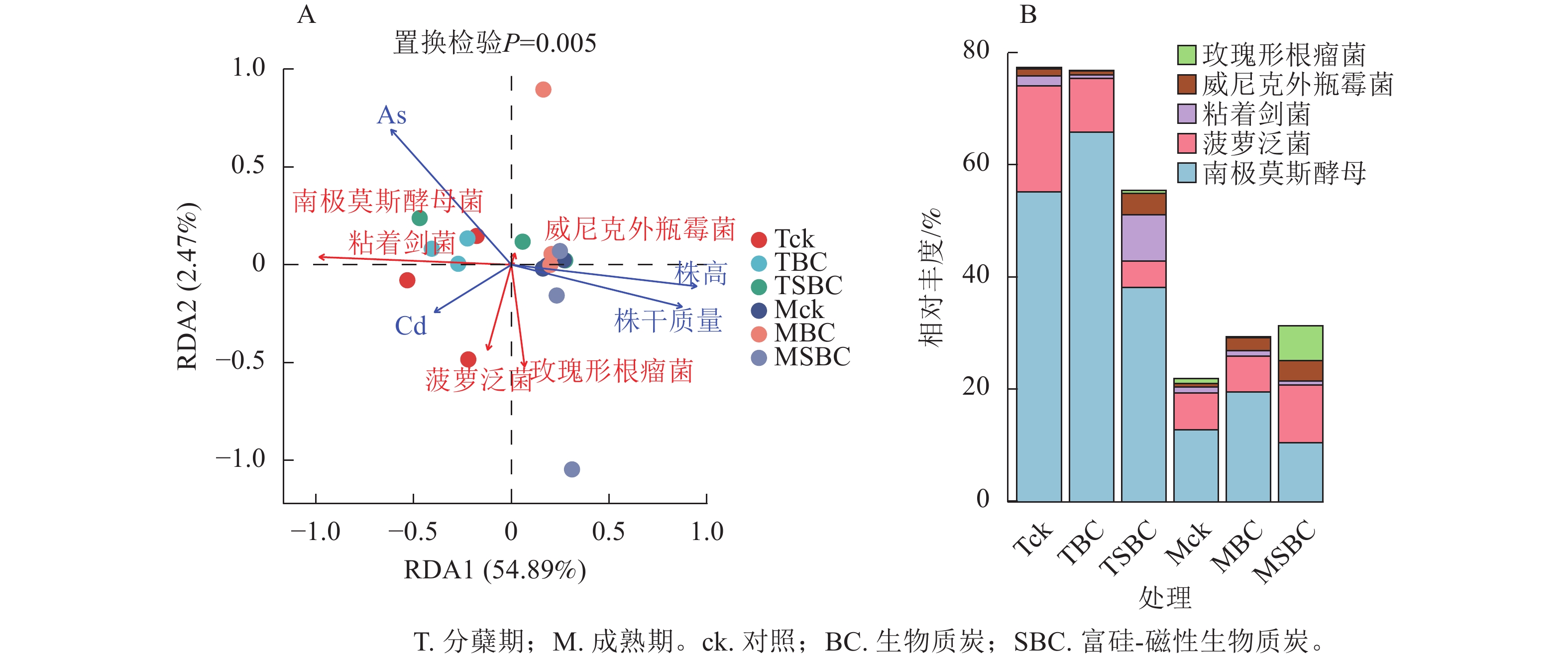
冗余分析(图4A)表明:土壤有效态As、Cd与水稻株干质量及株高呈显著负相关(P<0.01),且As对生长的抑制效应显著强于Cd (P<0.05)。不同处理下土壤有效态Cd与As呈极显著正相关(P<0.001)。在微生物-环境互作层面,5个关键属对重金属表现出物种特异性响应。粘着剑菌Ensifer adhaerens、菠萝泛菌Pantoea ananatis、玫瑰形根瘤菌Rhizobium rosettiformans及南极莫斯酵母Moesziomyces antarcticus与Cd呈正相关,威尼克外瓶霉Hortaea werneckii与Cd呈显著负相关(P<0.01)。南极莫斯酵母、威尼克外瓶霉与As呈正相关,而菠萝泛菌、玫瑰形根瘤菌与As呈显著负相关(P<0.01)。
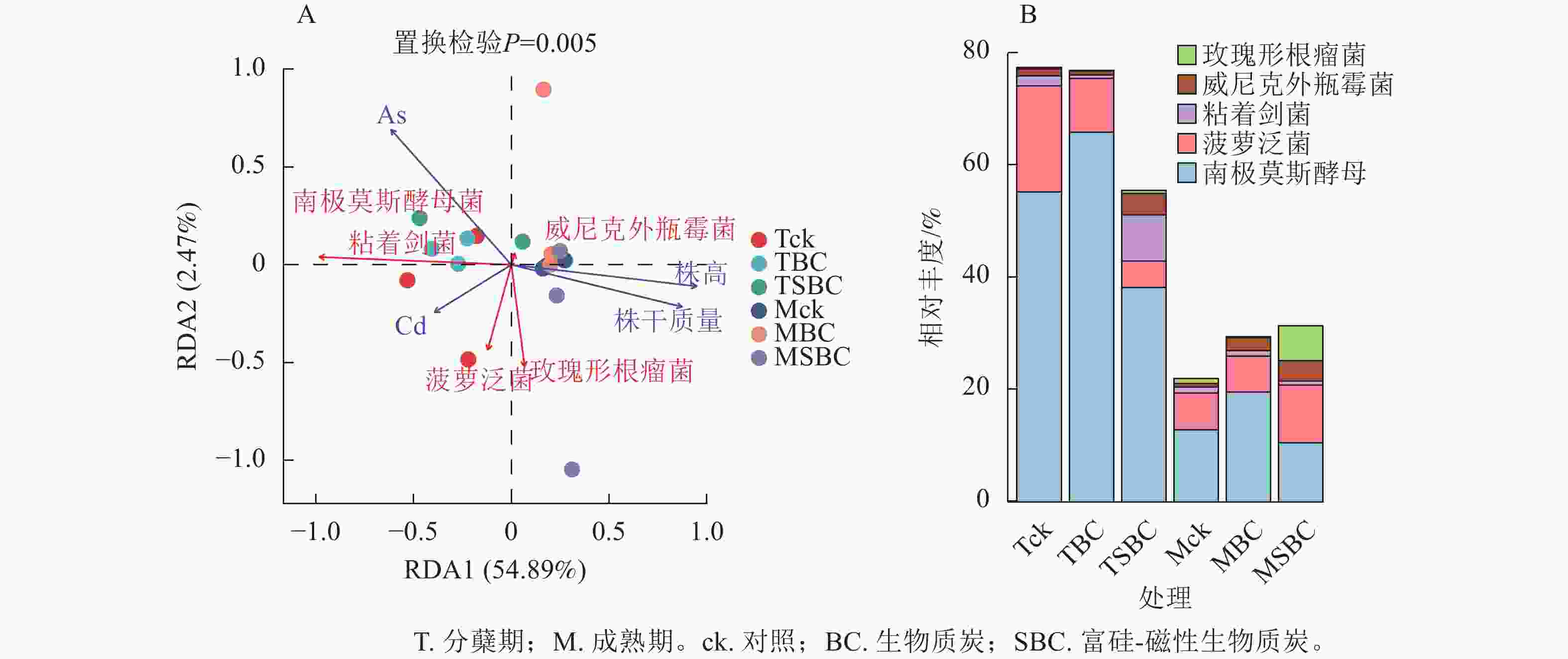
Figure 4. RDA analysis of microbial and environmental factors (A) and the relative abundance of key microorganisms (B)
关键物种丰度分析(图4B)显示:BC与SBC处理在分蘖期引发了截然不同的群落响应。与ck相比,BC显著增加了南极莫斯酵母丰度(19.2%,P<0.05),但降低了菠萝泛菌(49.5%)和粘着剑菌(64.0%)。相反,SBC处理显著富集了促生菌群,使粘着剑菌、玫瑰形根瘤菌和威尼克外瓶霉丰度分别大幅提升379.8%、108.2%和201.4%,同时显著抑制了南极莫斯酵母(30.9%)和菠萝泛菌(75.1%)(P<0.05)。这种特异性响应表明:SBC可能通过筛选特定抗性或代谢功能菌群间接调控重金属行为。
-
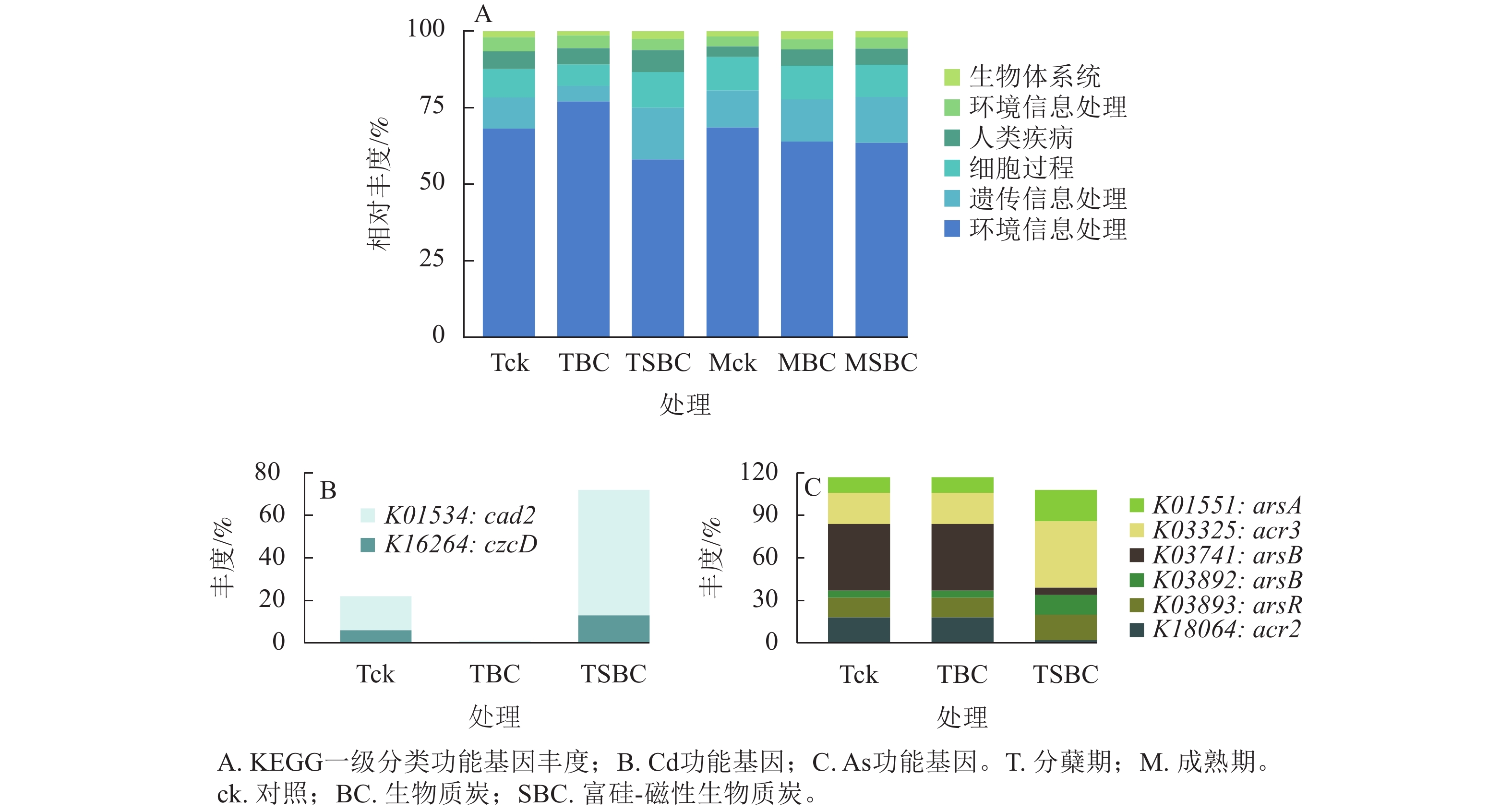
基于KEGG功能注释(图5)可知:不同处理显著改变了水稻叶际微生物的功能谱,尤其是Cd、As代谢通路。一级功能分类显示:群落功能主要富集于新陈代谢、遗传信息处理、细胞过程及环境信息处理。SBC与BC处理在分蘖期引发了截然相反的功能重构。与ck相比,SBC处理显著抑制了新陈代谢功能,但增强了遗传信息处理与细胞过程功能(P<0.05);反之,BC处理则显著上调了新陈代谢功能,而抑制了遗传信息处理与细胞过程功能(P<0.05)。
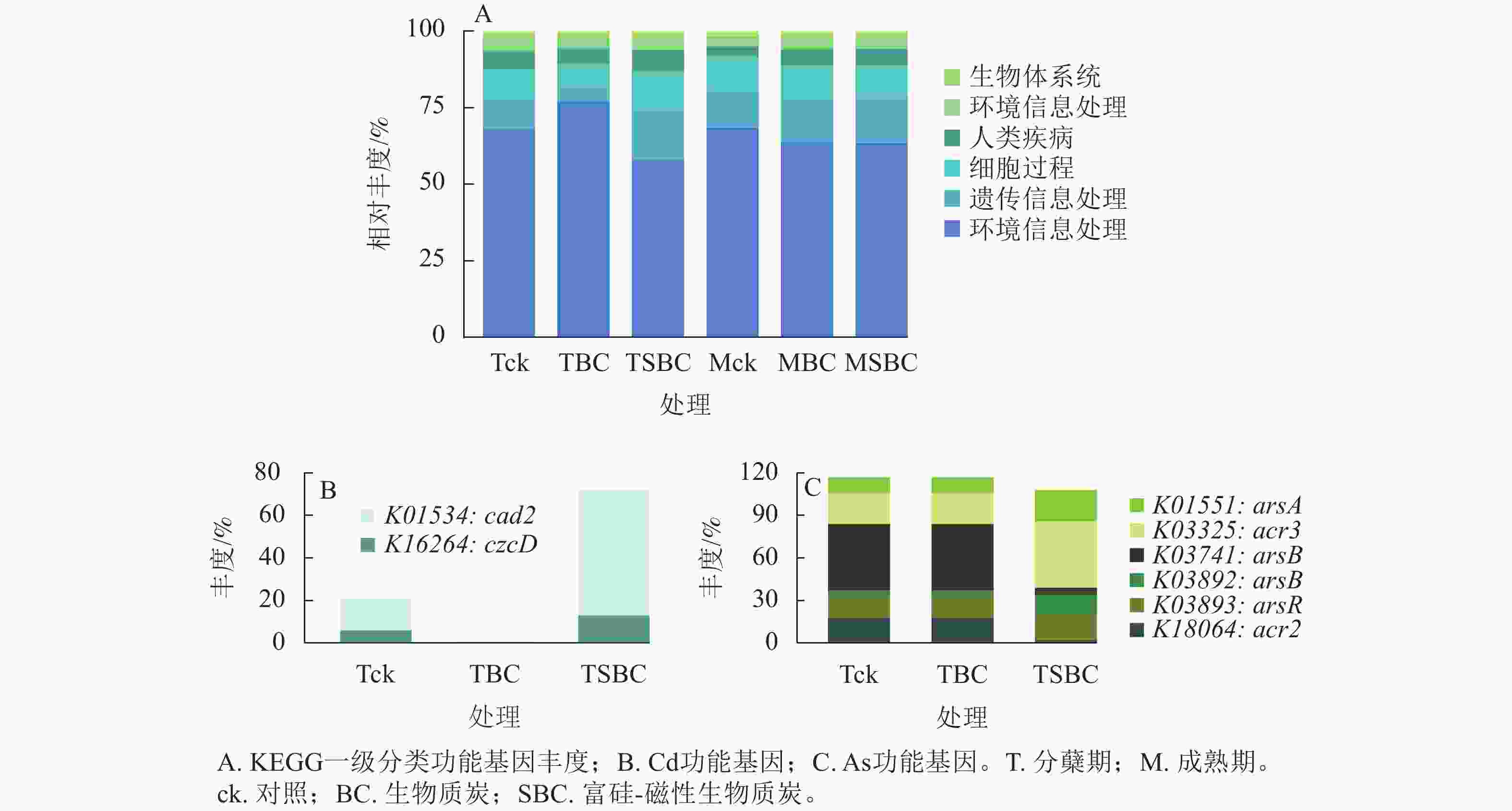
Figure 5. Functional abundance of phyllosphere microbiota in rice at the tillering stage based on KEGG functional annotation
其次,SBC处理诱导了显著的基因表达调控。针对Cd,SBC使外排基因(K16264: czcD 、K01534: cad2)丰度较ck提升227.0% (P<0.05),显著增强了微生物对Cd的胞外排出能力。针对As,SBC表现出促外排与抑转化并重的调控特征。一方面,显著上调As外排相关基因(K03325: acr3、K03741: arsB、K01551: arsA、K03893: arsR),使丰度达94.2% (P<0.05);另一方面,显著下调As还原酶基因(K03741: arsC )丰度89.4% (P<0.05),有效抑制了As(Ⅴ)向高毒形态As(Ⅲ)的转化。此外,抗As蛋白基因(K18064: acr2)丰度亦下调88.9% (P<0.05)。
-
SBC通过改善土壤理化性质与调控微生物群落,促进水稻生长,阻控重金属积累。在促生长方面,SBC利用材料特性与微生物协同作用提升土壤生产力。作为多孔有机载体,SBC增加土壤有机碳,改善土壤通气性与孔隙度,有利于根系扩展及水分渗透[20]。其次,SBC中的Si可提高水稻叶片叶绿素相对含量值(SPAD)和光合作用效率[21],还能增强植株对重金属的抗性并缓解铁毒[22]。此外,SBC可显著提高微杆菌属Microbacterium、粘着剑菌、玫瑰形根瘤菌及藤黄短小杆菌Curtobacterium luteum的丰度,根瘤菌与粘着剑菌通过与根系共生将大气氮转化为氨态氮[23],而微杆菌属等则通过分解有机质活化土壤中的磷、钾[24−25]。这种多途径的养分活化机制共同促进了水稻根系发育与养分吸收。
在降低Cd和As积累方面,SBC表面铁氧化物(Fe3O4)通过配位交换固定As形成Fe-O-As络合物,而硅酸根($\mathrm{SiO}_3^{2-} $)不仅促进As矿化,还能与Cd2+生成稳定的Fe-O-Si-Cd三元复合物[26−27]。其次,SBC的碱性及水解产生的OH−提升了土壤pH,增强了土壤胶体对Cd2+的静电吸附并促使其生成难溶的Cd(OH)2沉淀[28]。相较于普通生物质炭,SBC更能促进Fe、锰(Mn)羟基氧化物的原位生成及DOC的提升,从而提供更多吸附位点并形成Cd-有机络合物[29−30]。最后,SBC释放的Fe3+和$\mathrm{SiO}_3^{2-} $还会竞争植物根系的离子转运通道,从源头上抑制重金属向水稻体内的迁移[31]。
-
SBC的添加显著改善了叶际微生态系统,不仅提高了微生物的多样性和数量,还增强了群落结构的稳定性,进而影响水稻生长及重金属(Cd、As)的积累。鉴于叶际环境相对于土壤环境具有更强的开放性,微生物群落极易受大气、土壤及宿主生长状态的多重影响[32]。本研究结果表明:SBC对叶际微生物的调控效应表现出显著的生育期依赖性。在水稻分蘖期,植株生命活动旺盛,SBC能有效促进作物生长并增大叶片面积,为微生物提供了广阔的生存空间,导致该时期叶际微生物的多样性与数量显著高于成熟期;而随着水稻进入成熟期,叶片衰老限制了微生物的生存与繁殖,导致群落多样性下降。这一动态变化揭示了SBC通过调控宿主生长状态间接驱动了叶际微生物群落的时空演替。
相较于BC,SBC表现出更优异的微生态调控能力。凭借更高的比表面积、更强的吸附能力以及对pH和有机质的显著调节作用,SBC能更有效地优化微生物生存环境[33]。特别是SBC引入的活性硅酸盐和铁氧化物成分,能够调节叶际化学性质,为子囊菌门Ascomycota等特定微生物类群提供适宜的生态位,从而促进其定殖与增殖[34]。这种由材料改性带来的物种多样性提升,显著增加了群落的功能冗余度,即增强了生态系统的“保险效应”,使得不同物种能分担同一生态功能,从而有效缓解单一物种波动对群落整体功能的影响,进一步提升了群落的抗干扰能力与稳定性[35]。
SBC还通过改变环境pH、吸附养分、释放硅元素及发挥直接抗菌作用,重塑了关键微生物的丰度及其生态功能。一方面,SBC的筛选作用抑制了不适应新环境的菌群,如南极莫斯酵母菌和植物病原菌菠萝泛菌因竞争受限或受抑菌作用影响而丰度降低,这虽然可能削弱酵母菌产生的促生激素效应[36],但显著减少了病原菌潜伏,降低植物病害风险[37]。另一方面,环境优化促进了有益功能菌的富集,如粘着剑菌和玫瑰形根瘤菌的丰度显著提高[38],而固氮菌的增加能提升土壤-水稻系统的氮素水平,促进了水稻生长[39];此外,嗜盐真菌的增殖则有助于高盐环境下的有机质分解,可能进一步增强水稻的耐盐性[40]。
-
SBC的添加通过重塑叶际微生物的代谢功能配置与基因表达模式,增强了群落对重金属胁迫的适应能力。在宏观代谢功能层面,SBC改变了微生物群落的资源分配策略。新陈代谢、遗传信息处理及细胞过程是决定微生物适应性的核心要素。在Cd、As胁迫下,微生物通常被迫优先分配资源维持基础新陈代谢以求生存[41]。然而,添加SBC后,叶际微生物的新陈代谢功能丰度显著降低,而遗传信息处理和细胞过程的丰度则相应升高。这种代谢重定向归因于SBC优异的理化性质:其磁性改性与富硅组分在材料表面形成A型与B型三元表面络合物,大幅增强了对Cd和As的吸附效率[6]。这种高效吸附降低了环境毒性,缓解了微生物的代谢压力,使其能将能量用于优化遗传信息传递与细胞生理活动[42]。相比之下,BC吸附能力较弱,导致微生物仍需维持高代谢水平以应对胁迫[43]。这种由材料特性驱动的功能优化提升了群落的功能冗余度,增强了土壤-水稻系统在环境扰动下的稳定性。
在微观功能基因层面,由于SBC对Cd和As的吸附亲和力差异及两者转化机制的不同,微生物展现出差异化的基因调控响应[44]。针对Cd的阻控,SBC主要通过上调外排与转运基因减少积累。SBC处理显著提高了Cd2+跨膜运输的P型ATP酶(K01534: cad2)和Cd外排基因(K16264: czcD)的丰度。这种上调效应源于2个方面协同。首先,SBC促进水稻生长及根系分泌物产生,提高了群落多样性,富集了耐重金属且含高丰度转运蛋白的优势菌群;其次,SBC的高铁含量促进水稻对Fe的吸收,而负责转运Fe的zip蛋白同时负责Cd转运,这一过程间接提升了相关转运蛋白的丰度[45]。这些外排蛋白的高表达加速了Cd从微生物细胞内排出,减少了微生物介导的Cd滞留,进而降低其向水稻组织的迁移。
针对As的阻控,SBC通过调控氧化还原与转运基因降低其生物毒性。SBC使叶际微生物As还原酶基因(K03741: arsC)丰度降低,有效抑制了砷酸盐向高毒性亚砷酸盐的转化。同时,SBC促进了As转运系统的增强,提高了亚砷酸盐转运蛋白基因(K01551: arsA、K03893: arsB)和As酸盐转运蛋白基因(K03325: acr3、K03741: arsB)丰度。这主要得益于SBC分解释放的营养物质促进了代谢活动,及硅元素对特定功能微生物的激活作用[46–47]。此外,SBC使As反应转录抑制因子(K03892: arsR)丰度提升,通过正向调控arsA和arsB的表达进一步增强As的外排。值得注意的是,抗As蛋白基因(K18064: acr2)丰度反而降低,这表明SBC对土壤As的强效吸附钝化显著降低了环境中的有效As含量,从源头上减少了微生物对抗性蛋白的诱导需求。
-
SBC的添加促进了水稻生长并显著降低Cd、As累积,重塑了分蘖期叶际微生物群落,提升了多样性、稳定性与抗逆功能,优化了分蘖期叶际微生物遗传信息处理和细胞过程的功能,提高了微生物和作物整体的环境适应能力,增强了Cd、As外排基因(czcD、cad2、acr3、arsB等)的丰度,增加了微生物体内Cd、As外排,降低了叶际微生物As还原功能基因arsC的丰度,抑制高毒As(Ⅲ)生成,实现“材料-微生物-基因”协同调控,为Cd-As复合污染农田水稻安全生产提供理论依据。
Response of phyllospheric microorganisms to the remediation of cadmium and arsenic co-polluted soil by silicon-magnetic biochar in rice
doi: 10.11833/j.issn.2095-0756.20250276
- Received Date: 2025-05-06
- Accepted Date: 2026-03-05
- Rev Recd Date: 2025-12-30
-
Key words:
- silicon-magnetic biochar /
- Cd-As combined pollution /
- rice /
- phyllospheric microorganisms /
- microbial function /
- metagenome
Abstract:
| Citation: | WANG Jiahao, CHEN Yao, ZHANG Yu, et al. Response of phyllospheric microorganisms to the remediation of cadmium and arsenic co-polluted soil by silicon-magnetic biochar in rice[J]. Journal of Zhejiang A&F University, 2026, 43(X): 1−11 doi: 10.11833/j.issn.2095-0756.20250276 |









 DownLoad:
DownLoad: