-
光强和氮素是陆地多数森林植物进行光合作用的主要限制因子[1]。不同种类的植物对生境光强变化的适应性表现出极大的差异性,喜光植物的光合速率随生境光强增加而大幅增加,阴生植物则受到强烈的光胁迫抑制[2]。一定范围的强光促进植物根系生长、维持水分和营养物质的吸收能力;相反,弱光条件下,植物会提高叶绿素质量分数,增强捕获太阳辐射的能力。植物叶氮含量直接影响光合速率,并最终影响植物光能利用率和生物量的积累。当植物处于一定的氮素供应范围时,增加土壤氮素将提高净光合速率[3],相反土壤施氮超出一定范围后,将会导致植物光合速率下降,生长速率减缓,严重时植物出现枯死现象[4]。
玉铃花Styrax obassia属于安息香科Styracaceae安息香属Styrax的落叶小乔木或灌木,主要分布于华中和华东地区,向东分布至山东半岛,向北分布至辽宁东南部,为安息香科在中国的分布北界[5];在国外分布于日本南部和朝鲜半岛西南部。安息香属在中国有31种植物,仅玉玲花、粉花安息香S. roseus呈现粉红色的花朵[6]。玉铃花树形优雅,枝叶扶疏,穗状花下垂,形如“玉铃”,花期长且香气馥郁,为良好的蜜源植物,也是营造城市园林蝴蝶栖息地的优良树种[7],其花、果实、木材均具有重要的经济价值。
2020年8月作者在清凉峰国家级自然保护区紫茎Stewartia sinensis群落样地调查时仅发现1株玉铃花。该株玉铃花呈单株分布,未见健康的幼苗、幼树。自然条件下玉铃花缺乏幼苗幼树,可能与其种子、幼苗、幼树抗逆性弱有关。种子和幼苗、幼树是植物种群生活史极为脆弱的2个阶段。种子发芽、幼苗阶段对所在生境生活因子的变化幅度最为敏感[8],往往因为关键生态因子的剧烈波动,如光强和气温、以氮素为标志的土壤肥力状况、土壤水分含量不足或过剩等,导致种子发芽、幼苗生长发育受阻乃至出现死亡,最终被环境筛过滤淘汰。可推测:一方面玉铃花自然落种后难以遇到适宜发芽生境,加上种子发芽的内部抑制因素,种子难以发芽;另一方面幼苗对生境环境质量要求较高,表现为群落下层的光强和土壤肥力条件难以满足玉铃花幼苗的生长发育需求,导致玉铃花天然更新在种子发芽和幼苗生长发育2个环节严重受阻。幼苗生长发育过程往往受到2个或更多生态因子的综合影响,在高效培育苗木过程中,需要调控光和氮肥的交互效应,才能实现苗木生长和苗木质量的优化[9]。目前,有关玉铃花的研究多集中于破除种子休眠[10]、遗传多样性的扩增片段长度多态性(AFLP)分析[11]、种苗特性[12]、开花动态与繁育系统[13]等,对其幼苗生态适应性的研究尚未开展。
基于上述分析,根据玉铃花生物学与生态学特性以及野外生长状况,本研究构建遮光与氮素双因素控制试验,模拟不同光强和氮素的生境组合,通过分析比较玉铃花光合生理参数的差异,筛选最有利于玉铃花幼苗光合生理代谢过程的光强+氮素处理组合。
-
试验地位于浙江省杭州市临安区浙江农林大学东湖校区(30°15′20″N,119°43′36″E)。地带性气候属于亚热带湿润季风气候,年均降水量为1 613.9 mm,年均气温为13.0~22.0 ℃,四季分明。地带性植被为亚热带常绿阔叶林。
-
于2021年3月从清凉峰自然保护区的苗圃选取长势良好且高度基本一致的玉铃花幼苗100株,株高为(46.08±3.83) cm、地径为(6.12±0.44) mm,移栽至花盆中(直径20 cm,高15 cm),每盆栽植1株。盆栽土壤的化学性状(平均值±标准误):pH为5.08±0.01,全氮为(1.53±0.01) g·kg−1,碱解氮为(184.92±8.61) mg·kg−1,有效磷为(8.76±0.11) mg·kg−1,速效钾为(275.00±12.19) mg·kg−1,有机质为(31.58±0.10) g·kg−1。
将移栽的玉铃花幼苗置于3层遮阳网下缓苗,正常浇水。30 d后将成活的植株随机分成9组,每组5盆,移至3个不同光强的遮光大棚,分别为轻度遮光(透光率47.30%,L1),中度遮光(透光率20.00%,L2),高度遮光(透光率7.75%,L3)。参考周磊等[14]对细叶桢楠Phoebe hui容器苗的施氮量,每个遮光处理设置1个对照组N0 (不施氮)和2个施氮处理,分别为N1 (施氮0.21 g)、N2 (施氮0.63 g),氮肥为硫酸铵[(NH4)2SO4],每隔15 d喷洒1次,对照组则喷洒等量清水,连续施氮4次。
-
经遮光与施氮处理70 d后,选择6月5—14日晴天9:00—11:00,借助Li-6400便携式光合仪,测定玉铃花幼苗叶片净光合速率(Pn)、蒸腾速率(Tr)、气孔导度(Gs)和胞间二氧化碳摩尔分数(Ci)等。每个处理选择3株幼苗,每株测定3片叶片,每个处理共9个重复。设定光强梯度为2 000、1 500、1 200、1 000、800、600、400、200、100、50、20和0 μmol·m−2·s−1,诱导光强为1 500 μmol·m−2·s−1,诱导时间为30 min。
-
采用乙醇浸提法测定光合色素质量分数[15]。取玉铃花鲜叶去除主脉,剪成约0.20 cm的碎片,取0.20 g放入10 mL体积分数为95%的乙醇离心管,密封至叶组织完全失绿。借助UV-2550型紫外分光光度计,在波长665、649、470 mm进行比色,读取各波长的吸光度,计算光合色素质量分数。具体计算公式如下:CChl a=[13.95×D(665)−6.88×D(649)]×V/(m×1 000);CChl b=[24.96×D(649)−7.32×D(665)]×V/(m×1 000);CCar=[1 000×D(470)×V/(m×1 000)−2.05×CChl a−114.8×CChl b]/245。其中:CChl a、CChl b、CCar分别表示叶绿素a、叶绿素b和类胡萝卜素质量分数(mg·g−1);D(665)、D(649)、D(470)分别表示665、649、470 nm处的吸光度,V为提取液总体积(mL),m为样品鲜质量(g)
-
运用Excel 2010对原始数据进行处理,再借助光合助手(Photosynthesis)软件计算出光饱和点(LSP)、光补偿点(LCP)、表观量子效率(AQY)、暗呼吸速率(Rd)和最大净光合速率(Pmax);利用SPSS 26.0计算光合-光响应特征参数和光合色素质量分数的平均值、标准差,并检验差异显著性;借助 Origin 2019制图。
-
比较图1可知:在L1处理下,当光合有效辐射(PAR)>30 μmol·m−2·s−1时,玉铃花幼苗各施氮处理的Pn从大到小依次为N1、N0、N2,当PAR增加至2 000 μmol·m−2·s−1时,N1处理玉铃花Pn为N2处理的2.88倍。在L2处理下,当PAR由0增加至300 μmol·m−2·s−1时,各施氮处理玉铃花的Pn快速增加,超过300 μmol·m−2·s−1时,玉铃花的Pn从大到小依次为N0、N2、N1, L2+N1处理下玉铃花的Pn相较于L1处理约降低28.80%。在L3处理下,当PAR在50~400 μmol·m−2·s−1变化时,各施氮处理玉铃花的Pn从大到小依次为N0、N2、N1,当PAR>400 μmol·m−2·s−1后,N0和N2处理下玉铃花Pn大致接近,且明显高于N1处理。随遮光程度增加,N2处理对玉铃花Pn的抑制作用逐渐减弱,L3+N2处理玉铃花的Pn比L1处理大约增加304.99%。
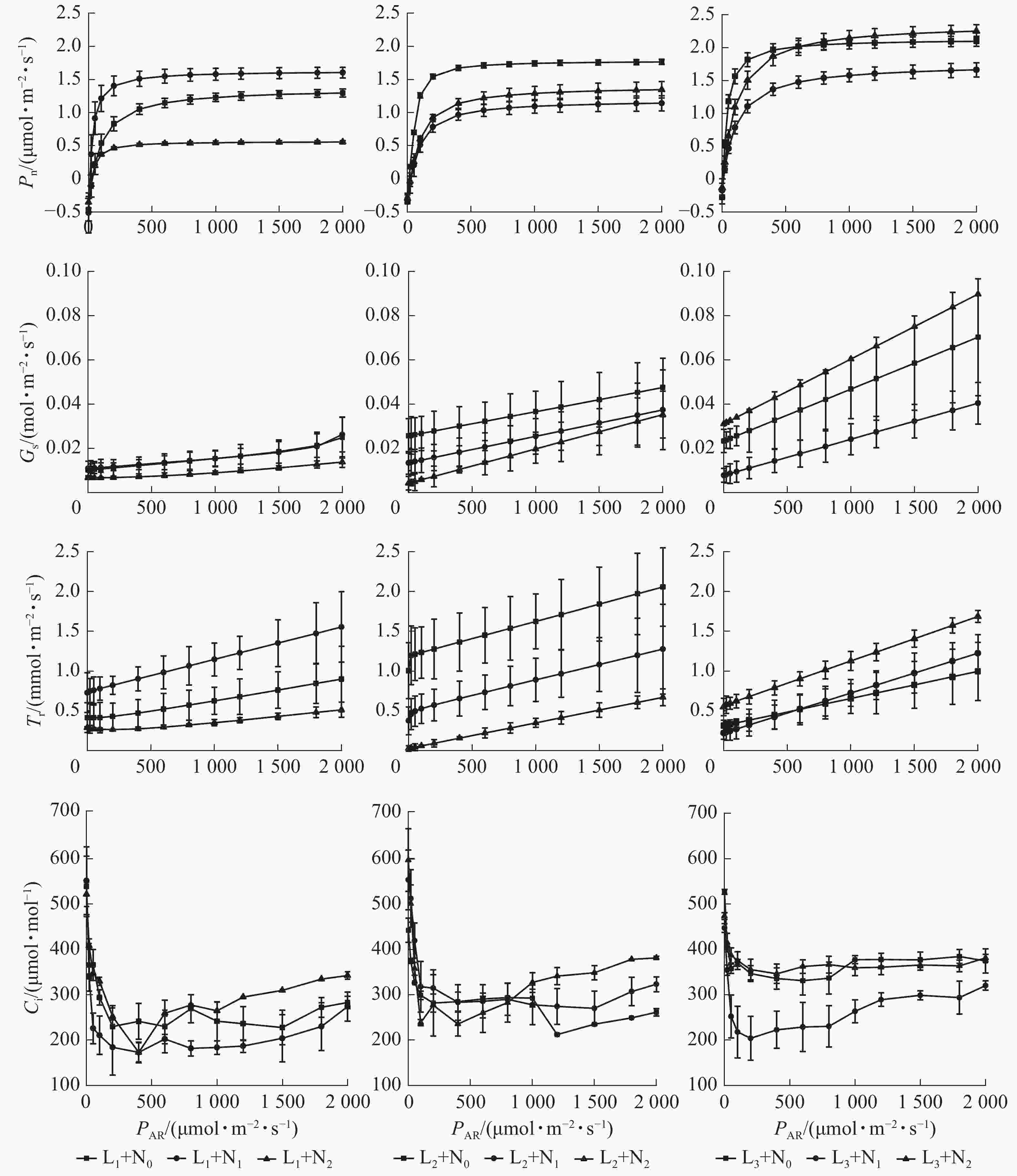
图 1 光强与氮肥施加对玉铃花幼苗光响应的影响
Figure 1. Effects of light intensity and nitrogen application on light response of S. obassia seedlings
在不同遮光+施氮处理下,玉铃花幼苗Gs和Tr均随PAR增大呈增加趋势。L1处理下各施氮处理的玉铃花Gs差异较小。随遮光程度增加,各施氮处理间差异逐渐增大。当PAR为2 000 μmol·m−2·s−1时,L3+N2处理的玉铃花Gs相较于L1+N2处理增加了552.70%,为同一遮光下N1处理的2倍。在L2处理下,各施氮处理玉铃花Tr相差较大,当PAR为2 000 μmol·m−2·s−1时,N2处理下玉铃花Tr相较于N0处理下降了67.40%。在L2+N0处理下玉铃花Tr处于最高水平;在L3+N2处理下玉铃花的Tr明显高于其他2个施氮处理。
在L1、L2和L3处理下,玉铃花的Ci随PAR增加大致呈先下降然后缓慢回升的变化特征。当PAR<400 μmol·m−2·s−1时,N1处理的玉铃花Ci下降幅度最大,随后呈现窄幅波动。
-
光响应特征参数能够反映植物在不同环境因子变化下光合潜能、光能利用能力等特性,进而表征植物的利用弱光、适应强光的能力和光强生态幅的大小范围。分析表1可知:随遮光程度增加,玉铃花幼苗的LCP逐渐降低,各施氮处理在L3处理下比L1分别减小了71.16%、72.70%和75.00%,其中N2的LCP减小幅度最大。不同施氮处理在L1、L2和L3处理下,玉铃花幼苗的LCP分别为24.00~34.67、14.67~16.00和6.00~12.00 μmol·m−2·s−1。不同施氮处理在L1、L2和L3处理下玉铃花幼苗的光饱和点LSP分别为140.00~288.00、164.00~324.00和270.00~481.33 μmol·m−2·s−1。在同一光强条件下,不同施氮处理玉铃花幼苗的AQY从大到小依次为N2、N1、N0;同一施氮水平下,从大到小依次为L3、L2、L1,表明施氮和遮光均能促进AQY的增加。L3+N2处理的Pmax为4.121 μmol·m−2·s−1,相较于L3+N0处理增加了50.78%,显著高于其他处理(P<0.05)。Rd的最小值出现在L3+N2组合处理,说明遮光和施氮能够通过降低呼吸速率来适应弱光环境。
表 1 不同光强与氮肥施加下玉铃花幼苗光合光响应特征参数的变化
Table 1. Changes of photosynthetic light response characteristic parameters of S. obassia seedlings under different light intensity and nitrogen application
处理 LSP/(μmol·m−2·s−1) LCP/(μmol·m−2·s−1) AQY/(mmol−1) Pmax/(μmol·m−2·s−1) Rd/(μmol·m−2·s−1) 光强 氮素 L1 N0 288.00±30.87 b 34.67±5.44 a 0.043±0.301 a 1.649±0.155 de 0.464±0.001 b N1 220.00±28.28 b 29.33±5.76 ab 0.046±0.111 a 1.924±0.225 cde 0.512±0.005 ab N2 140.00±1.89 b 24.00±2.83 ab 0.066±0.080 a 1.247±0.068 e 0.352±0.014 ab L2 N0 164.00±8.49 b 16.00±2.83 ab 0.054±0.305 a 3.246±0.102 b 0.346±0.001 ab N1 226.66±38.84 b 16.00±9.98 ab 0.060±0.056 a 2.276±0.090 cd 0.297±0.009 ab N2 324.00±33.04 ab 14.67±2.18 ab 0.067±0.089 a 2.127±0.217 cde 0.295±0.019 ab L3 N0 270.00±29.70 b 12.00±8.49 ab 0.065±0.080 a 2.733±0.525 bc 0.276±0.002 b N1 306.66±47.19 ab 8.00±3.77 b 0.075±0.110 a 1.943±0.166 cde 0.170±0.011 ab N2 481.33±86.52 a 6.00±1.41 b 0.080±0.421 a 4.121±0.248 a 0.132±0.061 a 说明:数据为平均值±标准误,小写字母表示同一指标在不同处理间差异显著(P<0.05) -
分析表2可知:在L1处理下,各施氮处理的叶绿素a质量分数(CChl a)存在显著差异(P<0.05);随遮光程度的增大,同一遮光处理内的玉铃花叶片CChl a相近,L3处理的不同施氮处理下玉铃花幼苗的CChl a无显著差异(P>0.05)。同一施氮处理不同光强下的玉铃花CChl a存在显著差异(P<0.05)。随遮光程度增加,各组叶绿素b质量分数(CChl b)持续增加,不同施氮组的差异性逐渐减小;L1处理下,施氮显著增加了CChl b (P<0.05),N1、N2处理分别比对照组增加了237.40%和137.80%;L1+N1处理下的CChl a/CChl b为L1+N0的36.00%。L1处理下,不同施氮组的光合色素质量分数均存在显著差异(P<0.05),L2、L3处理下不同施肥处理间差异不显著(P>0.05)。
表 2 光强与氮肥施加对玉铃花幼苗光合色素质量分数的影响
Table 2. Effects of light and nitrogen interaction on photosynthetic pgment contents in seedlings of S. obassia
处理 CChl a/(mg·g−1) CChl b/(mg·g−1) (CChl a+CChl b)/(mg·g−1) CCar/(mg·g−1) CChl a/CChl b 光强 氮素 L1 N0 1.621±0.050 d 0.711±0.024 f 2.332±0.074 f 0.253±0.008 a 2.284±0.019 a N1 1.929±0.033 b 2.399±0.115 d 4.327±0.082 d 0.176±0.017 b 0.822±0.054 c N2 2.080±0.016 a 1.691±0.098 e 3.770±0.085 e 0.257±0.029 a 1.269±0.085 b L2 N0 1.799±0.031 c 2.960±0.126 c 4.760±0.098 c 0.083±0.023 cd 0.619±0.037 d N1 1.640±0.014 d 3.598±0.049 b 5.239±0.038 b 0.123±0.017 bc 0.457±0.010 e N2 1.577±0.020 de 3.806±0.082 b 5.382±0.064 b 0.075±0.018 cd 0.417±0.015 e L3 N0 1.525±0.011 e 4.114±0.024 a 5.638±0.018 c 0.073±0.012 cd 0.371±0.005 e N1 1.530±0.014 e 4.134±0.025 a 5.664±0.016 c 0.070±0.018 cd 0.370±0.005 e N2 1.496±0.020 e 4.136±0.056 a 5.632±0.040 c 0.058±0.024 a 0.362±0.009 e 说明:数据为平均值±标准误,小写字母表示同一指标在不同处理间差异显著(P<0.05) 由表3可知:光强、氮素、光强+氮素对玉铃花幼苗的CChl a、CChl b、CCar、CChl a+CChl b和CChl a/CChl b的影响均达到极显著水平(P<0.01),影响的程度从大到小依次为光强、氮素、光强+氮素。
表 3 光强与氮肥施加对玉铃花幼苗光合色素质量分数影响的方差分析
Table 3. Anova analysis of the effects of light intensity and nitrogen application on photosynthetic pigment content of S. obassia seedlings
变异来源 因变量 平方和 自由度 均方 F P 光强 CChl a 0.722 2 0.361 102.841 0 CChl b 49.298 2 24.649 661.922 0 CCar 0.161 2 0.081 37.618 0 CChl a+CChl b 38.378 2 19.189 727.670 0 CChl a/CChl b 9.629 2 4.814 808.793 0 氮素 CChl a 0.080 2 0.040 11.322 0 CChl b 5.853 2 2.927 78.592 0 CCar 0.008 2 0.004 1.815 0.177 CChl a+CChl b 7.242 2 3.621 137.307 0 CChl a/CChl b 2.666 2 1.333 223.955 0 光强+氮素 CChl a 0.793 4 0.198 56.493 0 CChl b 4.565 4 1.141 30.645 0 CCar 0.032 4 0.008 3.775 0.012 CChl a+CChl b 7.301 4 1.825 69.216 0 CChl a/CChl b 3.859 4 0.965 162.081 0 -
光合作用是植物获取生长所需能量的重要途径,光合能力的大小则反映了植物对某一生境的适应程度。植物光合能力的变化往往受到一系列因素的影响。当Ci下降时,气孔因素是Pn下降的主要原因;相反,当Pn减小未伴随Ci降低,非气孔因素成为光合速率降低的主要原因[16]。本试验中,N2处理下Pn增加的主要原因是气孔因素,随遮光程度的增加,N2处理的玉铃花叶片气体交换能力增强,因而保证了弱光下玉铃花幼苗光合作用所需气体的供给。庞立东等[17]研究发现:施氮能使气孔开放,减少气孔阻力,从而增强蒸腾作用。本研究中,L3处理下施氮增加了气孔开放程度,但Gs的增加并未引起Tr的显著增加,推测可能原因是L3处理下光强较弱,避免了玉铃花幼苗叶片的过度失水。
LSP和LCP可表征植物叶片对强光和弱光的利用能力以及光强生态幅的宽窄幅度。耐荫植物的LSP在50~1000 μmol·m−2·s−1变化或者更低,LCP则小于20 μmol·m−2·s−1[18]。本研究中,玉铃花幼苗的LSP在140.00~481.33 μmol·m−2·s−1变化,LCP在6.00~34.67 μmol·m−2·s−1变化,表明玉铃花幼苗具有较强的耐荫性。
本研究结果显示:随遮光程度增大和施氮量增加,玉铃花幼苗的LCP和Rd逐渐减小,AQY逐渐增大,且相同遮光程度下,施氮处理的LSP、AQY高于不施氮处理,LCP、Rd小于未施氮处理,表明适宜的施氮量有助于玉铃花幼苗更好地适应弱光环境。此变化规律与刘柿良等[19]研究结果相一致。在大棚控制的弱光条件下,玉铃花幼苗通过降低LCP和LSP,增加叶绿素含量等,使光能高效地转化为化学能;同时降低呼吸消耗水平,以维持其基本的代谢平衡,从而保证植物的生长发育[20]。
在本研究中,玉铃花幼苗的Pn在L3+N2处理下达到最大值,为4.121 μmol·m−2·s−1,在L1处理下Pn普遍较小,L0处理下表现最差,出现极严重烧苗、枯死现象;L2处理下,Pn从大到小依次为N0、N1、N2;L3处理下,Pn从大到小依次为为N2、N0、N1。因此,玉铃花幼苗光合能力表现最佳的光强与施氮处理组合为L3+N2,其次为L2+N0。
-
植物光合效率的高低还可通过光合色素的质量分数来表征。本研究中,遮光对玉铃花幼苗光合色素质量分数的影响大于施氮,施氮大于遮光+施氮,且差异均达到极显著水平(P<0.01)。此变化规律与尹子旭等[21]研究结果一致。通常在弱光条件下,植物会通过增加CChl b以提升捕获光能的能力[22],CChl a/CChl b愈低说明植物愈耐荫[23]。一般的阴生植物CChl a/CChl b低于3[24]。本研究中,玉铃花幼苗CChl a/CChl b的远小于3,进一步证实玉铃花苗期具有较强的耐荫性,与其在重度遮光条件下仍表现出较高的光合速率相符合。增加施氮量并不会使叶绿素质量分数持续增加。在本研究中,L1和L2处理下,玉铃花幼苗的光合色素质量分数差异显著(P<0.05),L2与L3差异不显著(P>0.05)。此变化规律与黄玲璞[25]的研究结果一致。
强光条件下植物需要吸收更多的氮肥,光照越强,氮肥对植物生长的促进效果越显著[26]。在本研究中,L1光强下N1处理表现明显优于N2处理,且N2处理叶片出现边缘内卷、变黄。分析原因可能是:N2施氮过多,且L1遮光条件下PAR较高,植物体内水分蒸发较大,推测引起土壤氮素浓度和玉铃花叶氮含量增加,结果超过玉铃花的可耐受限度,出现玉铃花幼苗叶片卷曲、枯死的现象。
-
综上所述,光强和氮素对玉铃花幼苗的光合生理特性有显著影响。玉铃花幼苗表现出较强的耐荫性。在遮光+施氮处理下,玉铃花幼苗通过降低LSP、LCP、Rd、CChl a/CChl b,增加CChl a+CChl b、AQY等,更有效地适应弱光生境,以维持Pn处于较高的水平。本研究中玉铃花幼苗光合生理参数最佳状态的光强、氮素处理组合为L3+N2。
Effects of light intensity and nitrogen application on photosynthetic physiological parameters of Styrax obassia seedlings
-
摘要:
目的 筛选更有利于玉铃花Styrax obassia光合生理参数表达的光强、施氮组合处理,揭示光强、氮素变化与玉铃花幼苗生长的关系。 方法 采用盆栽育苗方法,构建光氮双因素控制试验:4种遮光处理[全光对照(透光率100.00%)、轻度遮光(透光率为47.30%,L1),中度遮光(20.00%,L2)和高度遮光(7.75%,L3)]与3种施氮处理[N2 (施纯氮0.63 g),N1(施纯氮0.21 g)和N0(不施氮)],测定分析玉铃花的光响应进程和光合色素质量分数的变化特征。 结果 ①随遮光程度和施氮量的增加,玉铃花幼苗的净光合速率、表观量子效率和总叶绿素质量分数呈现相应的增加,暗呼吸速率则相对减弱,其光饱和点为140.00~481.33 μmol·m−2·s−1,光补偿点为6.00~34.67 μmol·m−2·s−1、叶绿素a/b<2。②全光及L1+N2处理组合时,玉铃花植株出现枯死现象。③L1处理下,净光合速率的从大到小变化顺序为N1、N0、N2;L3处理下,当光合有效辐射>400.00 μmol·m−2·s−1时,N2处理玉铃花的净光合速率显著高于N0和N1处理(P<0.05);④光强与氮肥施加对玉铃花幼苗光合色素质量分数的影响均达到极显著水平(P<0.01),影响趋势从大到小依次为光照、氮素、光照+氮素。 结论 玉铃花幼苗具有较强的耐荫性,其光合生理参数最佳的光氮处理组合为高度遮光(L3),并施纯氮0.63 g (N2)。图1表3参26 Abstract:Objective This study aims to screen the combination treatment of light intensity and nitrogen application that is more conducive to the expression of photosynthetic physiological parameters, so as to reveal the relationship between the changes of light intensity and nitrogen and the growth of Styrax obassia seedlings. Method Potted seedling cultivation method was adopted to construct the two-factor control test of light and nitrogen. Four shading treatments were prepared: all-light control with 100.00% transmittance, light shading with 47.30% transmittance (L1), moderate shading with 20.00% (L2) and high shading 7.75% (L3). Three nitrogen application treatments were included: N2 (0.63 g pure nitrogen), N1 (0.21 g pure nitrogen) and N0 (no nitrogen application). The light response process and the variation characteristics of photosynthetic pigment content were determined and analyzed. Result (1)With the increase of shading degree and nitrogen application rate, net photosynthetic rate (Pn), apparent quantum efficiency (AQY) and total chlorophyll (Chl) content of S. obassia seedlings increased, while dark respiration rate (Rd) decreased, and light saturation point (LSP) ranged from 140.00 to 481.33 μmol·m−2·s−1. Light compensation point (LCP) varied from 6.00 to 34.67 μmol·m−2·s−1, and the ratio of Chl a to Chl b was less than 2. (2) Under all light and L1 shading+N2 treatment, the plants died. (3) Under L1 shading, the change of Pn ranging from large to small was N1, N0, and N2. Under L3 shading, when photosynthetic effective radiation (PAR)was greater than 400 μmol·m−2·s−1, the Pn of N2 was significantly higher than that of N0 and N1 (P<0.05). (4) Both light intensity and nitrogen application had significant effects on photosynthetic pigment content (P<0.01), and the influence trend in descending order was light, nitrogen, and light+nitrogen. Conclusion The seedlings of S. obassia have strong shade tolerance, and the optimal combination treatment of light and nitrogen is L3+N2. [Ch, 1 fig. 3 tab. 26 ref.] -
表 1 不同光强与氮肥施加下玉铃花幼苗光合光响应特征参数的变化
Table 1. Changes of photosynthetic light response characteristic parameters of S. obassia seedlings under different light intensity and nitrogen application
处理 LSP/(μmol·m−2·s−1) LCP/(μmol·m−2·s−1) AQY/(mmol−1) Pmax/(μmol·m−2·s−1) Rd/(μmol·m−2·s−1) 光强 氮素 L1 N0 288.00±30.87 b 34.67±5.44 a 0.043±0.301 a 1.649±0.155 de 0.464±0.001 b N1 220.00±28.28 b 29.33±5.76 ab 0.046±0.111 a 1.924±0.225 cde 0.512±0.005 ab N2 140.00±1.89 b 24.00±2.83 ab 0.066±0.080 a 1.247±0.068 e 0.352±0.014 ab L2 N0 164.00±8.49 b 16.00±2.83 ab 0.054±0.305 a 3.246±0.102 b 0.346±0.001 ab N1 226.66±38.84 b 16.00±9.98 ab 0.060±0.056 a 2.276±0.090 cd 0.297±0.009 ab N2 324.00±33.04 ab 14.67±2.18 ab 0.067±0.089 a 2.127±0.217 cde 0.295±0.019 ab L3 N0 270.00±29.70 b 12.00±8.49 ab 0.065±0.080 a 2.733±0.525 bc 0.276±0.002 b N1 306.66±47.19 ab 8.00±3.77 b 0.075±0.110 a 1.943±0.166 cde 0.170±0.011 ab N2 481.33±86.52 a 6.00±1.41 b 0.080±0.421 a 4.121±0.248 a 0.132±0.061 a 说明:数据为平均值±标准误,小写字母表示同一指标在不同处理间差异显著(P<0.05) 表 2 光强与氮肥施加对玉铃花幼苗光合色素质量分数的影响
Table 2. Effects of light and nitrogen interaction on photosynthetic pgment contents in seedlings of S. obassia
处理 CChl a/(mg·g−1) CChl b/(mg·g−1) (CChl a+CChl b)/(mg·g−1) CCar/(mg·g−1) CChl a/CChl b 光强 氮素 L1 N0 1.621±0.050 d 0.711±0.024 f 2.332±0.074 f 0.253±0.008 a 2.284±0.019 a N1 1.929±0.033 b 2.399±0.115 d 4.327±0.082 d 0.176±0.017 b 0.822±0.054 c N2 2.080±0.016 a 1.691±0.098 e 3.770±0.085 e 0.257±0.029 a 1.269±0.085 b L2 N0 1.799±0.031 c 2.960±0.126 c 4.760±0.098 c 0.083±0.023 cd 0.619±0.037 d N1 1.640±0.014 d 3.598±0.049 b 5.239±0.038 b 0.123±0.017 bc 0.457±0.010 e N2 1.577±0.020 de 3.806±0.082 b 5.382±0.064 b 0.075±0.018 cd 0.417±0.015 e L3 N0 1.525±0.011 e 4.114±0.024 a 5.638±0.018 c 0.073±0.012 cd 0.371±0.005 e N1 1.530±0.014 e 4.134±0.025 a 5.664±0.016 c 0.070±0.018 cd 0.370±0.005 e N2 1.496±0.020 e 4.136±0.056 a 5.632±0.040 c 0.058±0.024 a 0.362±0.009 e 说明:数据为平均值±标准误,小写字母表示同一指标在不同处理间差异显著(P<0.05) 表 3 光强与氮肥施加对玉铃花幼苗光合色素质量分数影响的方差分析
Table 3. Anova analysis of the effects of light intensity and nitrogen application on photosynthetic pigment content of S. obassia seedlings
变异来源 因变量 平方和 自由度 均方 F P 光强 CChl a 0.722 2 0.361 102.841 0 CChl b 49.298 2 24.649 661.922 0 CCar 0.161 2 0.081 37.618 0 CChl a+CChl b 38.378 2 19.189 727.670 0 CChl a/CChl b 9.629 2 4.814 808.793 0 氮素 CChl a 0.080 2 0.040 11.322 0 CChl b 5.853 2 2.927 78.592 0 CCar 0.008 2 0.004 1.815 0.177 CChl a+CChl b 7.242 2 3.621 137.307 0 CChl a/CChl b 2.666 2 1.333 223.955 0 光强+氮素 CChl a 0.793 4 0.198 56.493 0 CChl b 4.565 4 1.141 30.645 0 CCar 0.032 4 0.008 3.775 0.012 CChl a+CChl b 7.301 4 1.825 69.216 0 CChl a/CChl b 3.859 4 0.965 162.081 0 -
[1] KATAHATA S, NARAMOTO M, KAKUBARI Y, et al. Photosynthetic capacity and nitrogen partitioning in foliage of the evergreen shrub Daphniphyllum humile along a natural light gradient [J]. Tree Physiol, 2007, 27(2): 199 − 208. [2] ZHANG Lingling, WEN Dazhi. Structural and physiological responses of two invasive weeds, Mikania micrantha and Chromolaena odoratato contrasting light and soil water conditions [J]. J Plant Res, 2008, 122(1): 69 − 79. [3] 曾希柏, 侯光炯, 青长乐, 等. 土壤-植物系统中光照与氮素的相互关系研究[J]. 生态学报, 2000, 20(1): 104 − 109. ZENG Xibo, HOU Guangjiong, QING Changle, et al. Interrelation of light and nitrogen in soil-plant system [J]. Acta Ecol Sin, 2000, 20(1): 104 − 109. [4] 陈琳, 曾杰, 徐大平, 等. 氮素营养对西南桦幼苗生长及叶片养分状况的影响[J]. 林业科学, 2010, 46(5): 35 − 40. CHEN Lin, ZENG Jie, XU Daping, et al. Effects of exponential nitrogen loading on growth and foliar nutrient status of Betula alnoides seedlings [J]. Sci Silv Sin, 2010, 46(5): 35 − 40. [5] 陈涛, 陈忠毅. 安息香科植物地理分布研究[J]. 植物研究, 1996, 16(1): 59 − 68. CHEN Tao, CHEN Zhongyi. The geographical distribution of Styracaceae [J]. Bull Bot Res, 1996, 16(1): 59 − 68. [6] 童丽丽, 刘政, 许晓岗, 等. 中国安息香属植物的形态特征及自然地理分布[J]. 金陵科技学院学报, 2019, 35(2): 75 − 80. TONG Lili, LIU Zheng, XU Xiaogang, et al. Morphological characteristics and natural geographical distribution of Styrax speciesin China [J]. J Jinling Inst Technol, 2019, 35(2): 75 − 80. [7] 彭重华, 张程, 巫涛, 等. 湖南安息香科种质资源及其在园林中的应用前景[J]. 广东农业科学, 2011, 38(7): 76 − 79. PENG Zhonghua, ZHANG Cheng, WU Tao, et al. Resources of the Styracaceae in Hunan and their application to landscaping [J]. Guangdong Agric Sci, 2011, 38(7): 76 − 79. [8] MACHADO J L, WALTERS M B, REICH P B. Below-ground resources limit seedling growth in forest understories but do not alter biomass distribution [J]. Ann For Sci, 2003, 60(4): 319 − 330. [9] 王亚江, 葛梦婕, 颜希亭, 等. 光、氮及其互作对超级粳稻产量和物质生产特征的影响[J]. 作物学报, 2014, 40(1): 154 − 165. WANG Yajiang, GE Mengjie, YAN Xiting, et al. Effects of light, nitrogen and their interaction on grain yieldand matter production characteristics of Japonica super rice [J]. Acta Agron Sin, 2014, 40(1): 154 − 165. [10] 褚泽龙. 玉铃花种子休眠与萌发特性研究[D]. 泰安: 山东农业大学, 2015. CHU Zelong. Study on Dormancy and Germination Characteristics of Styrax obassia Sieb. et Zucc. Seeds[D]. Tai’an: Shandong Agricultural University, 2015. [11] 王萱. 玉铃花遗传多样性的AFLP分析[D]. 泰安: 山东农业大学, 2016. WANG Xuan. Genetic Diversity of Styrax obassia Sieb. et Zucc. Based on AFLP Markers[D]. Tai’an: Shandong Agricultural University, 2016. [12] 邢世岩, 董雷雷, 胡爱华, 等. 玉玲花种苗特性研究[J]. 种子, 2008, 27(3): 60 − 62. XIN Shiyan, DONG Leilei, HU Aihua, et al. Study on seeds and seedlings characteristics of Styrax obassia Sieb. et Zucc. [J]. Seed, 2008, 27(3): 60 − 62. [13] 万琦, 赵楠楠, 张明如, 等. 玉铃花开花动态与繁育系统特征[J]. 浙江农林大学学报, 2022, 39(3): 547 − 553. WAN Qi, ZHAO Nanna, ZHANG Mingru, et al. Flowering dynamics and breeding system of Styrax obassia [J]. J Zhejiang A&F Univ, 2022, 39(3): 547 − 553. [14] 周磊, 刘美玲, 李铁华, 等. 施肥对细叶桢楠容器苗生长与光合的影响[J]. 中南林业科技大学学报, 2021, 41(7): 80 − 87. ZHOU Lei, LIU Meiling, LI Tiehua, et al. Effects of fertilization on growth and photosynthetic of Phoebe hui seedlings [J]. J Cent South Univ For Technol, 2021, 41(7): 80 − 87. [15] 张志良, 瞿伟菁, 李小方. 植物生理实验指导[M]. 4版. 北京: 高等教育出版社, 2009. ZHANG Zhiliang, QU Weijing, LI Xiaofang. The Guidance of Plant Physiology Experiments[M]. 4th Ed. Beijing: Higher Education Press, 2009. [16] FARQUHAR G D, SHARKEY T D. Stomatal conductance and photosynthesis [J]. Ann Rev Plant Physiol, 1982, 33(1): 317 − 345. [17] 庞立东, 李卫军, 朱进忠. 追施氮肥对苏丹草光合特性及种子产量的影响[J]. 草业科学, 2014, 31(12): 2286 − 2292. PANG Lidong, LI Weijun, ZHU Jinzhong. Effects of topdressing nitrogen fertilizer on photosynthetic characteristics and seed yields of sudangrass [J]. Pratacultural Sci, 2014, 31(12): 2286 − 2292. [18] 蔡建国, 韦孟琪, 章毅, 等. 遮阴对绣球光合特性和叶绿素荧光参数的影响[J]. 植物生态学报, 2017, 41(5): 570 − 576. CAI Jianguo, WEI Mengqi, ZHANG Yi, et al. Effects of shading on photosynthetic characteristics and chlorophyll fluorescence parameters in leaves of Hydrangea macrophylla [J]. Chin J Plant Ecol, 2017, 41(5): 570 − 576. [19] 刘柿良, 马明东, 潘远智, 等. 不同光强对2种桤木幼苗光合特性和抗氧化系统的影响[J]. 植物生态学报, 2012, 36(10): 1062 − 1074. LIU Shiliang, MA Mingdong, PAN Yuanzhi, et al. Effects of light regimes on photosynthetic characteristics and antioxidant system in seedlings of two alder species [J]. Chin J Plant Ecol, 2012, 36(10): 1062 − 1074. [20] 殷东生, 沈海龙. 森林植物耐荫性及其形态和生理适应性研究进展[J]. 应用生态学报, 2016, 27(8): 2687 − 2698. YIN Dongsheng, SHEN Hailong. Shade tolerance and the adaptability of forest plants in morphology and physiology: a review [J]. Chin J Appl Ecol, 2016, 27(8): 2687 − 2698. [21] 尹子旭, 卢玉生, 张美曼, 等. 光、氮及其互作对设施绿竹叶片碳氮代谢的影响[J]. 生态学杂志, 2020, 39(12): 3979 − 3988. YIN Zixu, LU Yusheng, ZHANG Meiman, et al. Interactive effects of light intensity and nitrogen supply on leaf carbon and nitrogen metabolism of Dendrocalamopsis oldhami [J]. Chin J Ecol, 2020, 39(12): 3979 − 3988. [22] 徐琳煜, 刘守赞, 白岩, 等. 不同光强处理对三叶青光合特性的影响[J]. 浙江农林大学学报, 2018, 35(3): 467 − 475. XU Linyu, LIU Shouzan, BAI Yan, et al. Effects of light intensity treatments on photosynthetic characteristics in Tetrastigma hemsleyanum [J]. J Zhejiang A&F Univ, 2018, 35(3): 467 − 475. [23] 陶巧静, 吴月燕, 付涛, 等. 弱光胁迫对西洋杜鹃生理特性和叶片超微结构的影响[J]. 林业科学, 2015, 51(3): 84 − 92. TAO Qiaojing, WU Yueyan, FU Tao, et al. Effect of low light stress on physiological characteristics and ultrastructure of Rhododendron hybridum leaves [J]. Sci Silv Sin, 2015, 51(3): 84 − 92. [24] 沈娟, 李谦盛, 倪迪安. 2种大吴风草的耐荫特性研究[J]. 植物生理学报, 2014, 50(7): 967 − 972. SHEN Juan, LI Qiansheng, NI Di’an. Study on the shade tolerance characters of two Farfugium japonicum plants [J]. Plant Physiol J, 2014, 50(7): 967 − 972. [25] 黄玲璞. 光氮互作对格木幼苗生长、生理特性的影响研究[D]. 南宁: 广西大学, 2018. HUANG Lingpu. A Research on Interaction of Light and Nitrigen on Erythrophleum fordii Oliv. Seedlings[D]. Nanning: Guangxi University, 2008. [26] 粟春青, 亢亚超, 韦艺, 等. 光氮互作对闽楠幼苗生长发育的影响[J]. 广西林业科学, 2019, 48(2): 207 − 212. SU Chunqing, KANG Yachao, WEI Yi, et al. Effects of photon-nitrogen interaction on growth of Phoebe bournei seedlings [J]. Guangxi For Sci, 2019, 48(2): 207 − 212. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20210605






 下载:
下载:


