-
小麦孢囊线虫Heterodera avenae是一种在世界范围内分布广泛的植物寄生线虫,严重威胁小麦Triticum aestivum产量[1]。小麦孢囊线虫侵染小麦后,会阻碍植株根系对水分和养分的吸收,致使叶片黄化、植株矮小、枯萎甚至死亡[2]。小麦孢囊线虫病害可导致全球小麦减产20%~30%,发病严重的地区甚至减产达70%,每年造成全球经济损失约1 730亿美元[3]。大多数小麦品种对小麦孢囊线虫都不具有抗性,农户往往会采用更方便快捷的化学防治法,如喷洒百威颗粒剂、苯线磷颗粒剂等农药来杀死线虫[4−5]。化学药物防治虽然见效快,但容易导致线虫病害反复暴发,而且频繁使用还会带来环境污染等生态安全隐患[6−7]。而生物防治具有绿色环保、生态友好等特点,但生防菌剂资源匮乏,推广应用受限[8−9]。化肥和农药的大量使用导致了土壤生物多样性的减少,并加剧了小麦孢囊线虫的侵染[10]。因此,如何在减少化肥、农药投入的同时,减少小麦孢囊线虫发生,稳定提高小麦产量,是发展绿色农业亟须解决的难题。
磷是植物必需营养元素之一,磷肥有助于增强植物对土传病害的抗性[11−12]。最新研究揭示了磷肥对植物寄生线虫的作用规律:随着过磷酸钙施用量的增加,土壤中植物寄生线虫的相对丰度受到高磷浓度的抑制[13];单施钙镁磷酸酯、钙磷酸酯和钾磷酸酯对番茄Solanum lycopersicum根结线虫Meloidogyne病的防控率分别为98%、66%和47%,而磷酸一钙和磷酸二铵抑制率分别为30.2%和44.8%[14−15];施用磷酸一铵能有效降低土壤孢囊的数量,而过磷酸钙和磷酸二铵能抑制孢囊线虫的孵化[16−17]。然而,磷肥防控植物寄生线虫发生的作用机制尚不清楚。
根系分泌物作为植物与环境之间物质和信息交流的关键媒介,含有的杀线活性物质可通过抑制植物寄生线虫的侵染和繁殖来增强植物的抗病性[18]。例如,非寄主植物万寿菊Tagetes erecta的根系分泌物可以通过影响线虫对寄主植物的定位来抑制线虫侵染[19],大豆Glycine max抗线品种的根系分泌物可以显著降低病土中大豆孢囊线虫的孵化率[20]。目前,关于根系分泌物的研究大多集中于对线虫趋避方面的影响,少量研究分泌物中杀线活性物质成分的鉴定,如有机酸类、黄酮类和萜类化合物等[21−22]。施肥会影响植物根系分泌物的组成,磷肥诱导的小麦根系分泌物组成与孢囊线虫发生的协同作用机制仍有待探索。基于此,本研究通过盆栽试验,设置不同供磷水平处理,探究小麦孢囊线虫的发生规律、小麦根系分泌物组成特征及其与孢囊线虫的相互关系,初步揭示磷肥调控小麦孢囊线虫发生机制,为构建兼顾减肥与减药的植物寄生线虫绿色防控技术体系奠定理论基础。
-
本研究在温室中进行,供试土壤取自河南的砂壤。土壤基本理化性质为全氮1.05 g·kg−1,全磷1.26 g·kg−1,全钾6.6 g·kg−1,pH 7.48,每盆用土1 kg。共设置4个不同磷水平处理P1、P2、P3和P4,分别表示每盆施过磷酸钙0、0.50、1.00、1.50 g (即0、72、144、216 kg·hm−2 P2O5)。所有处理保持氮和钾供给一致,即每盆施用尿素 0.56 g(即234 kg·hm−2N)、KCl0.18 g(即99 kg·hm−2K2O)。每盆种3株小麦,1盆为1个重复,每个处理8盆。在16 ℃温室生长7 d后开始接种线虫。每盆接种新孵化的小麦孢囊线虫500头,隔1 d再接种500头,共接种1 000头线虫。然后置于22 ℃温室中生长,变温培养有利于线虫发育形成孢囊。接种线虫6周后收样。
-
小麦孢囊线虫孢囊取自河南省开封市的小麦田,采用土壤悬液过筛法收集土壤中的孢囊。把经4 ℃低温滞育4个月的孢囊放置于孵化筛上,再把孵化筛放置在装有无菌水的培养皿中,水面没过孵化筛底部,置于16 ℃培养箱孵化5 d,将培养皿中的水收集于烧杯,并加水稀释至线虫浓度为100头·mL−1,以待接种使用。
-
取整盆鲜土样品,置于容器中,加入适量清水,充分搅拌1 min,以释放土壤中的孢囊。静置沉淀30 s,随后将悬液依次通过20目筛和80目筛过滤。沉淀下来的泥土加水再重复过滤1次。将最终保留在80目筛上的残渣用少量清水冲洗,将收集到筛上的残渣,转移至体视镜下观察并记录孢囊数量。
-
将整株小麦挖出用自来水反复冲洗根系,以去除表面的土壤和杂质。随后用无菌水对根系进行3次冲洗至无菌水不再浑浊,以确保彻底清洁。将植株根系浸泡在100 mL无菌水中,并用黑色塑料袋对根系做遮光处理,22 ℃光照培养6 h,中途3 h将收集液轻轻摇匀。收集完成后,将植株取出,收集液经过0.22 μm无菌滤膜(Millipore)过滤,以去除微生物及颗粒杂质,置于−20 ℃冰箱冷冻,再将冷冻的收集液放置于冷冻干燥机中冻干,收集冻干后残留的粉末并于−80 ℃保存备用。
-
分别对小麦植株地上部、地下部称量,记录鲜质量。将地上部放入纸信封中,105 ℃杀青30 min,65 ℃恒温烘干至恒量,测量干质量。采用H2SO4-H2O2联合消煮,钼锑抗比色法测定小麦地上部磷浓度。采用水土质量比2.5∶1.0浸提,电位法测定pH。采用0.5 mol·L−1NaHCO3浸提,钼锑抗比色法测定土壤有效磷(Olsen-P)。采用液相色谱-质谱联用仪(LC-MS)测定根系分泌物:取50 mg根系分泌物冻干样本于1.5 mL离心管中,加入400 μL提取液[V(乙腈)∶V(甲醇)=1∶1],涡旋混匀30 s后,低温超声提取30 min (5 ℃,40 kHz),将样品静置于−20 ℃冰箱30 min,然后于4 ℃,13 000 g离心机离心15 min,移取上清液并用氮气吹干,后加入120 µL复溶液(V(乙腈)∶V(水)=1∶1)复溶,低温超声萃取5 min(5 ℃,40 kHz),再次置于4 ℃,13 000 g离心机离心5 min, 移取上清液至带内插管的进样小瓶中上机分析。
-
将LC-MS原始数据导入代谢组学处理软件Progenesis QI(Waters Corporation,美国)进行基线过滤、峰识别、积分、保留时间校正、峰对齐,最终得到保留时间、质荷比和峰强度的数据矩阵,数据矩阵用80%规则来去除缺失值,即保留至少一组样品中非零值80%以上的变量,再进行填补空缺值(原始矩阵中最小值填补空缺值),为减小样品制备及仪器不稳定带来的误差,用总和归一化法对样本质谱峰的响应强度进行归一化,得到归一化后的数据矩阵。同时删除质量控制(QC)样本相对标准偏差(RSD)>30%的变量,并进行对数化(lg)处理,得到最终用于后续分析的数据矩阵。同时将LC-MS质谱信息与代谢公共数据库京都基因和基因组数据库(KEGG,https://www.kegg.jp/)数据库进行匹配,得到代谢物信息。
采用SPSS 21.0软件对土壤孢囊、土壤pH、Olsen-P、小麦生物量、地上部含磷量进行单因素方差分析(ANOVA)。基于Tukey检验显著差异(P<0.5)。根系分泌物预处理后的数据上传美吉生物云平台上(https://cloud.majorbio.com)进行数据分析。R软件包ropls (Version1.6.2)进行主成分分析(PCA),并使用7次循环交互验证来评估模型的稳定性。通过维恩(Venn)图、相关性热图和火山图分析等分析,研究不同处理根系分泌物组成差异,并筛选变化倍数大于1倍,P<0.05的差异显著代谢物。采用KEGG化合物分类数据库对鉴定的差异代谢物进行通路分类。利用iPath3.0 (http://pathways.embl.de)对差异根系分泌物参与的代谢途径进行可视化分析,查看整个生物系统的代谢通路信息。
-
不同供磷水平处理对土壤孢囊的抑制效果存在显著差异(表1)。施磷处理的土壤孢囊数均显著低于未施磷处理(P<0.05),且P3处理显著低于其他处理(P<0.05),为19个,较P1、P2和P4处理分别降低55.49%、28.70%和44.20%。不同供磷水平处理的土壤pH之间无显著差异,而各处理土壤Olsen-P质量分数存在显著差异。施磷处理土壤的Olsen-P质量分数显著高于未施磷P1处理,且土壤Olsen-P质量分数随着施磷水平的增加而增加,其中P4处理土壤Olsen-P质量分数显著高于其他处理(P<0.05),为156.5 mg·kg−1;P2最低,为120.0 mg·kg−1,但也较P1处理显著提高53%。与P1处理相比,施磷的3个处理的小麦地上部鲜质量显著增加(P<0.05)。且P4处理的小麦地上部鲜质量显著大于其他处理(P<0.05),P3和P2处理间差异不显著,但分别较P1处理显著提高了17.6%和12.3%(P<0.05)。而不同处理间小麦地下部鲜质量无显著差异。此外,不同处理间小麦地上部含磷量也因供磷水平不同而改变,其中P4处理显著高于其他处理(P<0.05),P3处理次之,显著高于P1和P2(P<0.05),P4和P3较P1处理分别提高17.5%和9.0%,而P2与P1处理间无差异。
表 1 不同供磷水平处理小麦孢囊线虫病害和小麦生长状况
Table 1. Occurrence of cereal cyst nematode and wheat growth under different P treatments
处理 土壤孢囊数量/(个·盆−1) pH 土壤Olsen-P/(mg·kg−1) 地上部鲜质量/(g·株−1) 地下部鲜质量/(g·株−1) 地上部磷(g·kg−1) P1 43±3 a 7.64±0.03 a 68.25±5.93 d 1.87±0.09 c 1.21±0.05 a 3.54±0.04 c P2 27±1 c 7.64±0.05 a 120.00±0.60 c 2.10±0.02 b 1.13±0.02 a 3.56±0.04 c P3 19±1 d 7.69±0.02 a 133.90±4.10 b 2.20±0.02 b 1.10±0.01 a 3.86±0.06 b P4 35±2 b 7.67±0.03 a 156.50±2.40 a 2.41±0.01 a 1.03±0.02 a 4.16±0.12 a -
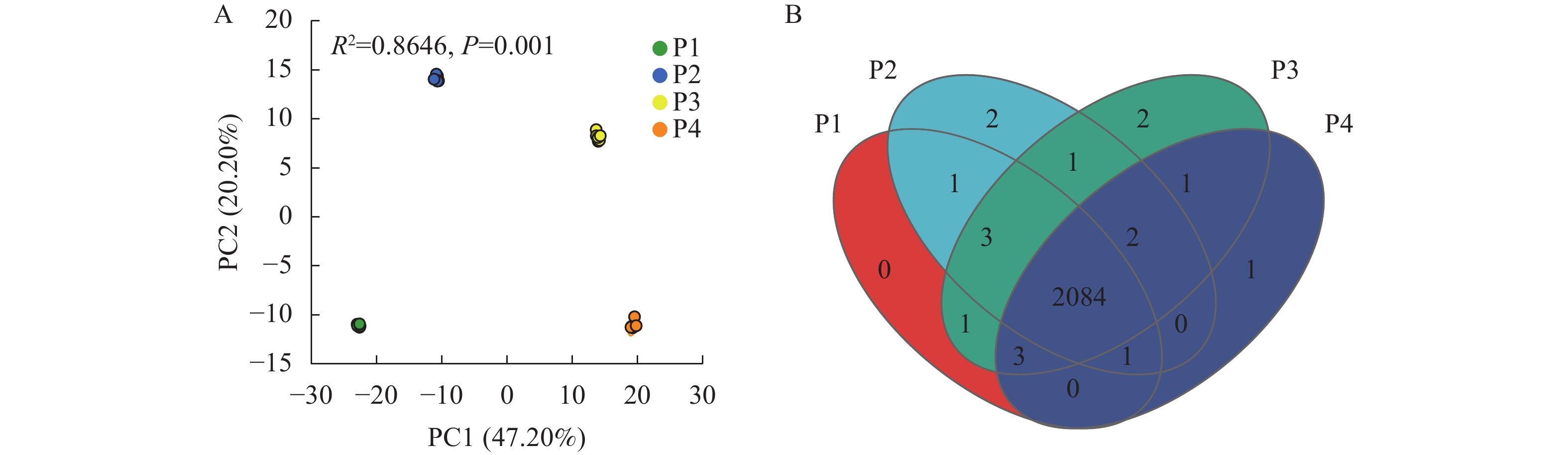
通过主成分分析(PCA)研究不同供磷水平处理间小麦根系分泌物差异,结果如图1A所示。PCA图的总解释度为67.40%,且差异极显著(P<0.001)。其中,4个处理完全分开,说明不同供磷水平处理的小麦根系分泌物存在显著差异。
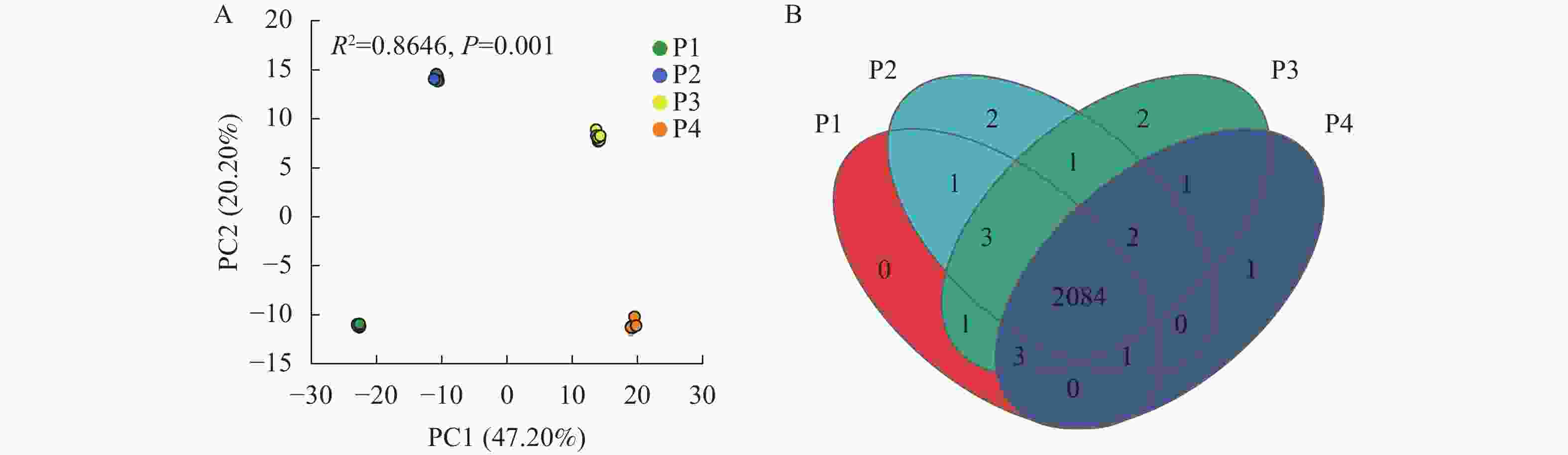
图 1 不同供磷水平处理小麦根系分泌物的主成分(PCA)分析(A)和维恩图分析(B)
Figure 1. Principal component analysis (PCA) (A) and Venn diagram (B) of wheat root exudates under different P treatments
通过维恩(Venn)图分析不同供磷水平小麦根系分泌物的数量差异,结果如图1B所示。4个处理总共测得2 102种分泌物。其中,P1处理无独有分泌物;P2处理独有分泌物2种,分别是洋川芎内酯(senkyunolide)和吲哚菲苏啶(indolophenanthridine);P3处理独有分泌物2种,分别是甲氧苄氨嘧啶(trimethoprim)和(2S)-2,3-二羟丙基(7Z, 10Z, 13Z, 16Z, 19Z)-docosa-7,10,13,16,19-五烯酸酯[(2S)-2,3-dihydroxypropyl (7Z, 10Z, 13Z, 16Z, 19Z)-docosa-7,10,13,16,19-pentaenoate];P4处理独有分泌物1种,为脱氧胆酸盐(deoxycholate),4个处理共同拥有分泌物为2 084种。
-
通过热图分析不同供磷水平的小麦根系分泌物组成特征,结果如图2所示。P1处理有17种物质富集,如13-羟基过氧化亚麻酸、9,10-环氧-18-羟基十八烷酸、13(S)-氢过氧化亚油酸等。相对于P1处理,P2处理有23种物质富集,如油酸酰胺、法尼基丙酮、香叶基香茅醇等,P3处理有8种物质富集,如(+)-麦角酸、地衣淀粉、噻吗洛尔等。P4处理有8种物质富集,如依折麦布葡萄糖醛酸苷、岩藻黄醇、麦芽四糖等。反映了不同供磷水平处理根系分泌物存在组成差异。
-
通过差异分泌物火山图研究P1和P3处理间小麦根系分泌物差异,结果如图3所示。相较于P1,P3显著上调了434种根系分泌物(P<0.05),显著下调了248种根系分泌物(P<0.05)。总计682种差异分泌物。
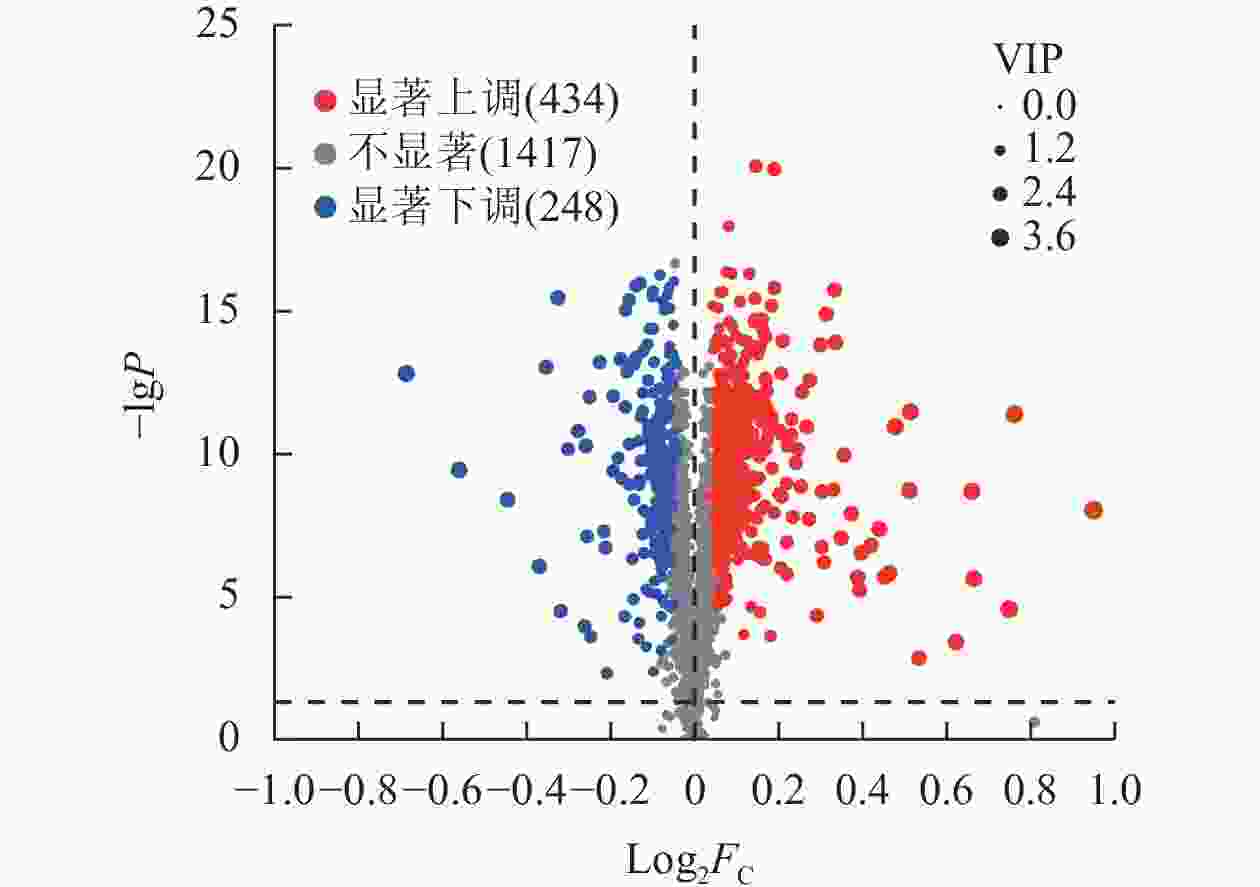
图 3 P3与P1处理小麦根系差异分泌物火山图
Figure 3. Volcano plot of differential rhizosphere exudates of wheat between P3 and P1 treatments
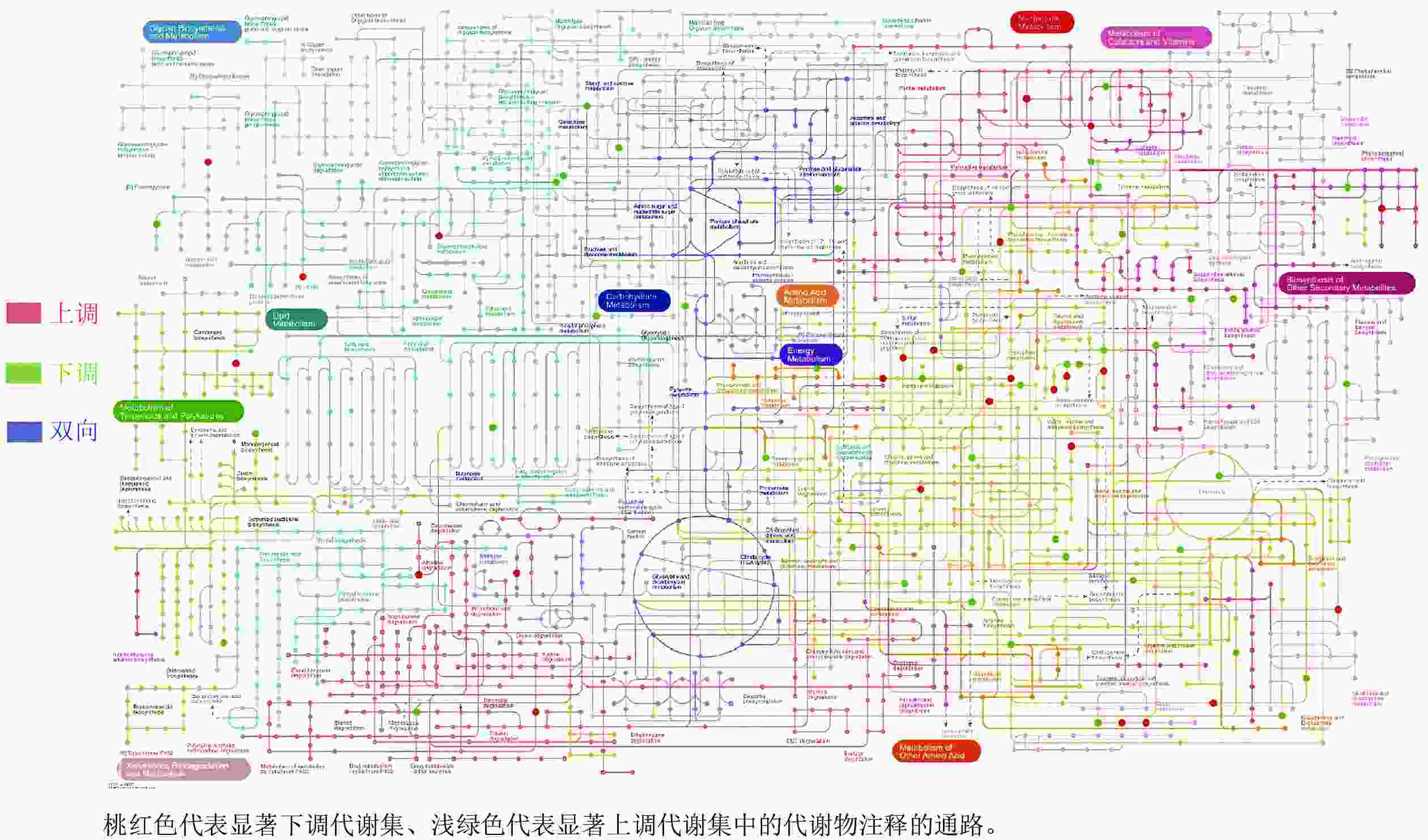
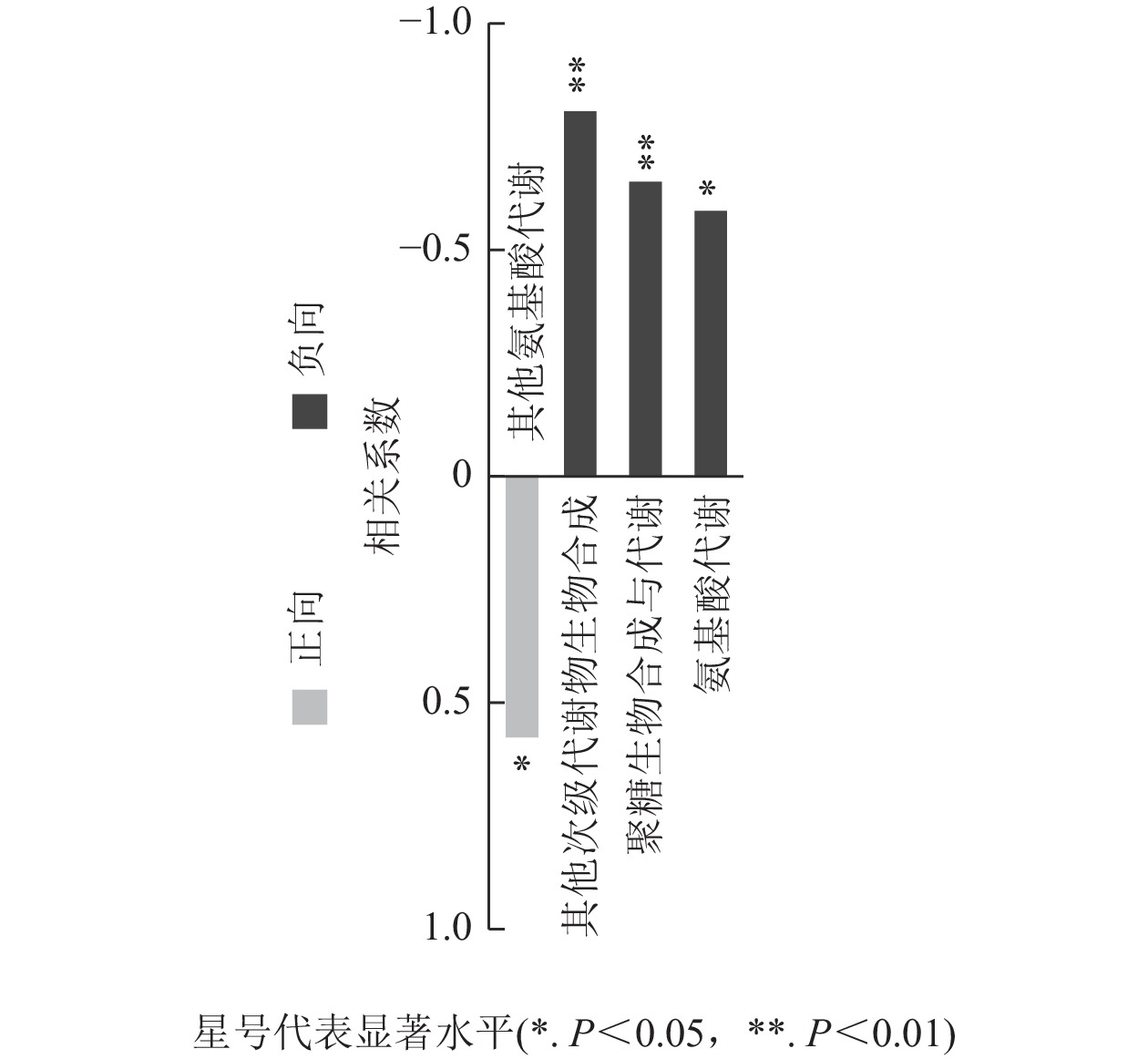
对前面分析得到的P3显著上调的434种与显著下调的248种根系分泌物做iPath分析,其代谢途径结果如图4所示。682种分泌物参与的通路包括聚糖生物合成与代谢、核苷酸代谢、辅因子与维生素代谢、脂质代谢、碳水化合物代谢、氨基酸代谢、其他次生代谢产物的生物合成、能量代谢、萜类化合物和聚酮类化合物的代谢、异种生物降解与代谢、其他氨基酸的代谢。其中,P3处理显著上调分泌物参与的通路多集中在聚糖生物合成与代谢、氨基酸代谢和其他次生代谢产物的生物合成,而显著下调分泌物参与的通路则主要聚集在其他氨基酸代谢,且显著上调和显著下调的两类差异分泌物间没有共同通路。进一步关联分析差异代谢通路与土壤孢囊的相关性,发现P3处理显著上调的3个代谢通路均与孢囊病情指数显著负相关(P<0.05)(图5)。
-
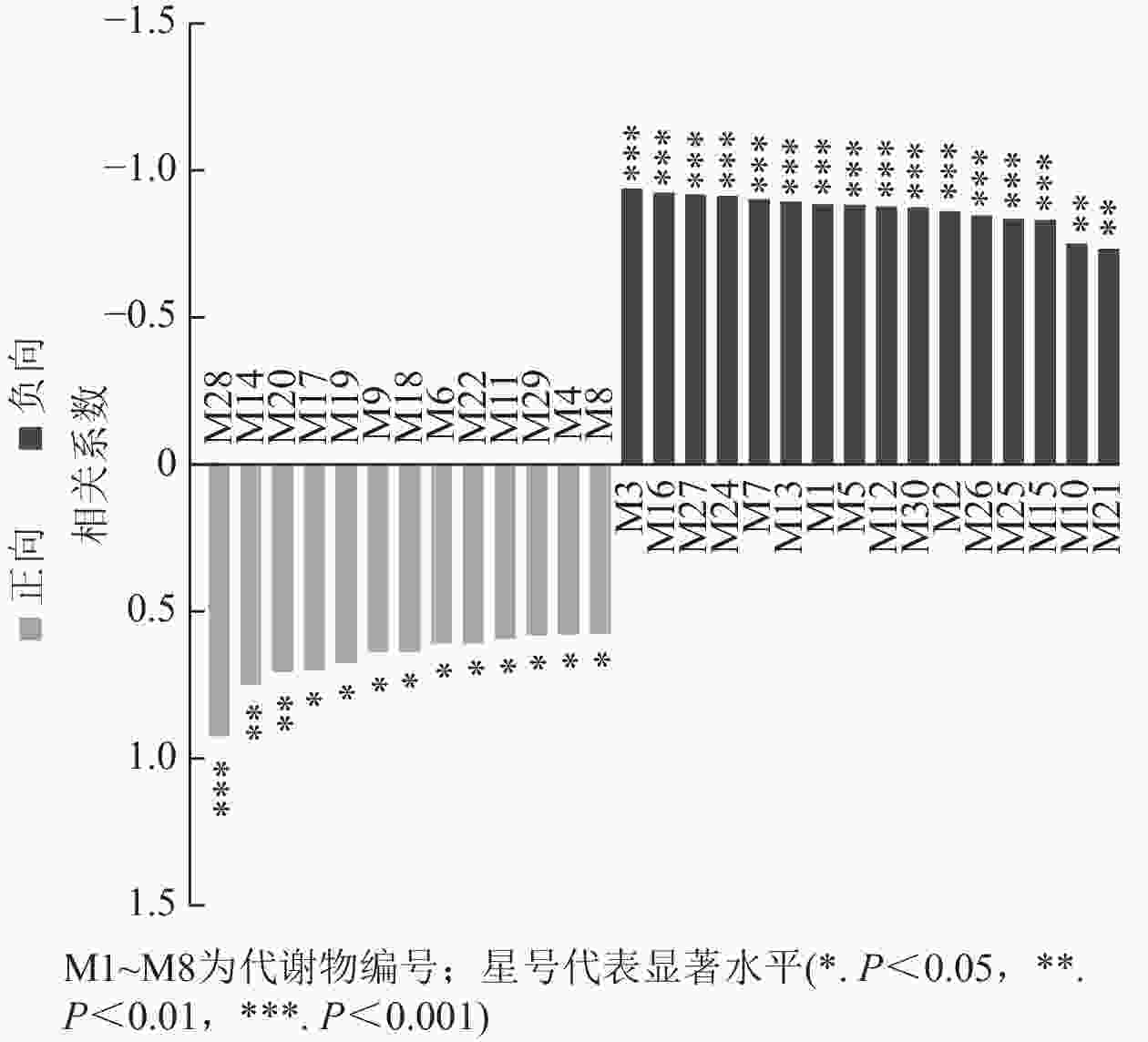
通过单因子相关性分析小麦差异根系分泌物与土壤孢囊的相关性,结果如图6所示。其中与土壤孢囊呈显著负相关的差异根系分泌物16种,分别是胞苷一磷酸-N-三甲基-2-氨基乙基膦酸酯、DHMBOA葡萄糖苷、甜菜碱、焦谷氨酸、1-3-(4,5-二氢呋喃酮)-5-(羟甲基)-吡咯-2-羧醛、正亮氨酸、L-谷氨酸、吲哚丙烯酸、4-氧代-2-铃兰氨酸、哌啶、10,20-二羟基二十烷酸、雌三醇-16-葡萄糖醛酸苷、17β-雌二醇-3-磺酸、酪胺、肉桂酸和2-羟基肉桂酸等(表2)。这16种差异根系分泌物的一级分类水平包括有机氧化物、有机酸及其衍生物、有机杂环化合物、脂质和类脂分子、苯环化合物及苯丙烷类和聚酮类等6大类物质。其二级分类水平包括有机氧化物、羧酸及其衍生物、吲哚及其衍生物、内酰胺、哌啶类、脂肪酰类、类固醇及其衍生物、苯及其衍生物和肉桂酸及其衍生物等9类物质。这些差异根分泌物可能与磷肥调控小麦抵抗孢囊线虫侵染有关。
表 2 与小麦孢囊线虫病害显著负相关的差异根系分泌物
Table 2. Metabolites that are significantly negatively correlated with cyst
编号 代谢物 分类 与土壤孢囊的相关性 一级分类 二级分类 P r M1 胞苷一磷酸-N-三甲基-2-氨基乙基磷酸酯CMP-N-trimethyl-2-
aminoethylphosphonate有机氧化物 有机氧化物 <0.01 −0.748 7 M2 DHMBOA葡萄糖苷DHMBOA hexose <0.001 −0.915 2 M3 甜菜碱betaine 有机酸及其衍生物 羧酸及其衍生物 <0.001 −0.890 5 M4 焦谷氨酸pyroglutamic acid <0.001 −0.843 1 M5 1-3-(4,5-二氢呋喃酮)-5-(羟甲基)-吡咯-2-羧醛1-3-(4,5-
dihydrofuranone)-5-(hydroxymethyl)-pyrrole-2-carboxyaldehyde<0.001 −0.871 3 M6 正亮氨酸norleucine <0.001 −0.881 9 M7 L-谷氨酸L-glutamic acid <0.001 −0.920 7 M8 吲哚丙烯酸indoleacrylic acid 有机杂环化合物 吲哚及其衍生物 <0.001 −0.934 8 M10 4-氧代-2-铃兰氨酸4-oxo-2-azetidinecarboxylic acid 内酰胺 <0.001 −0.910 1 M11 哌啶piperidine 哌啶类 <0.001 −0.874 8 M13 10,20-二羟基二十烷酸10,20-dihydroxyeicosanoic acid 脂质和类脂分子 脂肪酰类 <0.01 −0.730 2 M17 雌三醇-16 -葡萄糖醛酸苷estriol-16-glucuronide 类固醇及其衍生物 <0.001 −0.831 9 M18 17 β -雌二醇- 3 -磺酸17beta-estradiol 3-sulfate <0.001 −0.829 0 M21 酪胺tyramine 苯环化合物 苯及其衍生物 <0.001 −0.899 5 M25 肉桂酸cinnamic acid 苯丙素类和聚酮类 肉桂酸及其衍生物 <0.001 −0.858 7 M26 2-羟基肉桂酸2-hydroxycinnamic acid <0.001 −0.879 9 -
磷肥不仅可以促进植物获取更多的磷,还可以提高植物对土传病害的抗性,包括植物寄生线虫病[12]。李亮亮等[13]研究发现伴随着磷肥的施用,土壤有效磷含量增加,显著改变土壤线虫群落组成,尤其抑制植物寄生线虫群落的相对丰度。ZHANG等[23]在大豆田中观察到大豆孢囊线虫Heterodera glycines发生程度与土壤有效磷含量显著负相关。类似的,QIU等[10]发现小麦田施用有机肥显著促进土壤有效磷含量增加,与小麦孢囊线虫病的危害程度也呈显著负相关关系,显示土壤磷可能是抑制小麦孢囊线虫发生的关键地力因子。本研究中,施用过磷酸钙可有效降低盆栽小麦土壤中的孢囊数量,其抑制效果随施磷量的增加呈先降低后上升的趋势。由此推测,虽然磷肥对于小麦孢囊线虫病有抑制作用,但其抑制效果会随施磷量的改变而不同,且过量施磷可能加重线虫病害暴发。
磷元素在植物抵抗土传病害中扮演着重要的角色,它除了是一种植物必需营养元素,还是植物体内多种酶促反应和免疫系统的信号转导的重要组分[24]。有研究表明:当植物体内磷营养不足时植物抗逆性降低,更易受到病原物和线虫的侵害[25]。而且,植物受到土传病害的侵染时,往往需要更多的磷营养,以促进植物细胞内合成多种抗病物质和激活防御酶[26]。磷酸盐作为诱导小麦防卫基因表达和产生抗病性的激发子,能有效激活防御反应,如胼胝质沉积、细胞壁增厚、气孔关闭、细胞程序性死亡等,从而保护小麦减少线虫侵染[27]。此外,根系作为土传病害最直接的入侵部位,其形态、数量与磷元素息息相关。植株在缺磷土壤中主根生长受到抑制,侧根数量增加,形成更多的根系接触面来增加土壤磷的获取,同时也为土传病害入侵增加了更多位点和机会[28]。正是因其能以直接和间接的方式作用于多种病原物,磷酸盐被美国环境保护署列为生物杀虫剂[29]。本研究发现:过量施用磷肥,小麦地上部磷含量虽然一直增加,但是小麦孢囊线虫病害却并没有减轻,反而比的发病程度更高,推测体内磷营养可能在一定范围内对植物抵抗病虫害具有促进作用,超过临界值反而不利于植物抗逆性。
当植物遭遇生物或非生物逆境胁迫时,会调整其根系分泌物的物质组成以抵御逆境造成的伤害[30]。不同供磷水平下小麦受到孢囊线虫侵染时,也会改变根系分泌物组成。有机氧化物是根系分泌物的重要组成部分,本研究发现的胞苷-磷酸-N-三甲基-2-氨基乙基膦酸酯作为乙基磷酸酯的一种,不仅可以供给植物生长所需的磷,还可以控制由卵菌引起的植物病害[31]。而DHMBOA葡萄糖苷(即HDMBOA-Glc)作为玉米Zea mays等禾本科Poaceae植物中重要的苯并噁嗪类次生代谢产物,不仅有助于提高作物抗性,减少了化学农药使用,且对作物的生长与健康起到了积极的促进作用[32]。当玉米受到镰刀菌Fusarium graminearum感染时,HDMBOA葡萄糖苷的积累有助于提高植物的抗病性[33]。此外,本研究发现的关键根系分泌物如甜菜碱、吲哚丙烯酸和肉桂酸等在植物寄生线虫防治中均表现出有效杀线活性[34-36]。例如HANSEN等[34]研究发现,甜菜碱通过激活秀丽隐杆线虫Caenorhabditis elegans的DEG-3/DES-2受体,可导致线虫神经系统功能紊乱,引发过度的肌肉收缩,最终导致线虫死亡。而CHEN等[35]指出吲哚丙烯酸通过抑制根结线虫的V型ATP酶(V-ATPase)活性,破坏线虫细胞内pH平衡,从而抑制其生长和繁殖。JAVIER等[36]研究发现,肉桂酸通过与组蛋白去乙酰化酶(HDAC)的相互作用,抑制根结线虫生长。
除了直接抑制植物寄生线虫,根系分泌物还可能通过诱导根际微生物的方式间接抑制线虫病害[37]。本研究发现的关键根系分泌物中的有机酸和脂类物质,不仅可以作为营养源,促进微生物的生长和繁殖,还能特异性地富集有益微生物[38]。尤其有机酸类物质是芽孢杆菌Bacillus和假单胞菌Pseudomonas等微生物的引诱剂[39−40]。而芽孢杆菌和假单胞菌可通过合成抗生素、表面活性剂等生防因子显著减少小麦孢囊线虫在内的多种植物病害发生[41−43]。
-
本研究发现,当施用量在0~144 kg·hm−2P2O5范围内,磷肥对小麦孢囊线虫的抑制效果逐渐增强。施磷量为144 kg·hm−2P2O5时,显著改善小麦地上部含磷量,且土壤孢囊数最低,比不施磷肥显著降低55%。而随着施磷量继续增加,土壤孢囊数也显著增加,过量施磷可能会加重小麦孢囊线虫病害。与对照相比,最优施磷量处理的小麦根系分泌物有682种差异物质,其中显著上调434种,显著下调248种。其中,显著上调物质参与的通路多集中在聚糖生物合成与代谢、氨基酸代谢和其他次生代谢产物的生物合成,而显著下调物质参与的通路则主要聚集在氨基酸代谢,且两类差异物质不存在共同通路。进一步相关性分析发现,最优施磷量处理富集的根系分泌物中与土壤孢囊数显著负相关的有16种,涵盖有机氧化物、有机酸、有机杂环化合物、脂质、苯环化合物和聚酮类等6类物质,且有报道指出胞苷一磷酸-N-三甲基-2-氨基乙基膦酸酯、DHMBOA葡萄糖苷、甜菜碱、吲哚丙烯酸和肉桂酸等物质对植物病害具有抑制效果。由此推测,这些差异根系分泌物可能是磷肥抑制小麦孢囊线虫发生的关键因子,但是这些物质对孢囊线虫的杀线活性还有待进一步探究。
Phosphorus regulated secretion of wheat roots and its impact on occurrence of cereal cyst nematodes
-
摘要:
目的 小麦孢囊线虫Heterodera avenae病是一种分布广危害大的小麦Triticum aestivum土传病害,对粮食安全造成了严重威胁。施用磷肥可以有效减少小麦田土壤孢囊数量,本研究目的是揭示根系分泌物在磷肥调控小麦孢囊线虫发生过程中的作用。 方法 利用小麦盆栽试验设置不同供磷水平(P1,0 kg·hm−2 P2O5;P2,72 k·hm−2 P2O5;P3,144 kg·hm−2 P2O5;P4,216 kg·hm−2 P2O5),分析不同处理下小麦孢囊线虫发生规律,通过液相色谱-质谱联用仪代谢组测定根系分泌物组成差异。 结果 P3处理显著改善小麦地上部磷质量分数,且土壤孢囊数最低,比P1处理显著降低55%。随着供磷水平增加,P4处理的土壤孢囊数却显著高于P3处理,表明过量施磷可能会加重小麦孢囊线虫病害。主成分分析表明:P3处理的小麦根系分泌物组成显著区别于P1处理。相较于P1处理,P3处理共有682种差异根系分泌物,其中显著富集434种,显著降低248种。这些差异根分泌物参与聚糖生物合成与代谢、氨基酸代谢和其他次生代谢产物的生物合成。与土壤孢囊做相关性分析发现:P3处理有16种显著负相关物质,包括有机氧化物、有机酸、有机杂环化合物、脂质、苯环化合物和聚酮类等6类,部分物质对植物病害具有抑制效果。 结论 控制磷肥施用量可能通过刺激根系分泌具有抗病性的物质,以抵御小麦孢囊线虫侵染。这些发现初步揭示了磷肥抑制小麦孢囊线虫发生的调控机制,为减肥、减药的植物寄生线虫绿色防控技术体系提供理论依据。图6表2参43 Abstract:Objective Cereal cyst nematode (CCN) is a widespread and severe soil-borne disease in wheat, seriously threat to the food security in China. The application of phosphate fertilizer can effectively reduce the number of cysts in wheat field. Aim to reveal the role of root exudates in the regulation of CCN occurrence by phosphate fertilizer. Method A wheat pot experiment was conducted with applying different phosphorus levels (P1: 0 kg·hm−2 P2O5; P2: 72 kg·hm−2 P2O5; P3: 144 kg·hm−2 P2O5; P4: 216 kg·hm−2 P2O5). By analyzing the occurrence of CCN, as well as the composition differences of wheat root exudates which were determined by LC-MS metabolomics under different treatments. Result Under P3 treatment, the phosphorus concentration in shoot was significantly improved, and the number of cysts was the lowest, which was 55% lower than that of P1. As increased phosphorus supplying, the number of cysts under P4 treatment was significantly higher than that of P3, suggesting that excessive application of phosphorus might aggravate CCN diseases. The PCA analysis indicated that the composition of root exudates under P3 treatment was significantly different from that of P1. Compared with P1 treatment, there were 682 dissimilar root exudates under P3 treatment, among which 434 were significantly enriched and 248 were significantly reduced. These significant different root exudates are involved in glycan biosynthesis and metabolism, amino acid metabolism, and the biosynthesis of other secondary metabolites. Correlation analysis with cysts revealed that there were 16 significantly negatively correlated root exudates under P3 treatment, including organic oxides, organic acids, organic heterocyclic compounds, lipids, benzene ring compounds, and polyketides, and it has been reported that some of these substances have inhibitory effects on plant diseases. Conclusion Resistance of CCN can be enhanced by optimizing phosphate fertilizer application, which stimulates the root secretion of disease-suppressive compounds. These findings initially reveal the regulatory mechanism of phosphate fertilizer in inhibiting the occurrence of CCN, providing a theoretical basis for the green control technology system of plant parasitic nematodes through reduction of fertilizers and pesticides. [Ch, 6 fig. 2 tab. 43 ref.] -
Key words:
- Heterodera avenae /
- phosphorus application rate /
- metabolome /
- phosphate fertilizer
-
表 1 不同供磷水平处理小麦孢囊线虫病害和小麦生长状况
Table 1. Occurrence of cereal cyst nematode and wheat growth under different P treatments
处理 土壤孢囊数量/(个·盆−1) pH 土壤Olsen-P/(mg·kg−1) 地上部鲜质量/(g·株−1) 地下部鲜质量/(g·株−1) 地上部磷(g·kg−1) P1 43±3 a 7.64±0.03 a 68.25±5.93 d 1.87±0.09 c 1.21±0.05 a 3.54±0.04 c P2 27±1 c 7.64±0.05 a 120.00±0.60 c 2.10±0.02 b 1.13±0.02 a 3.56±0.04 c P3 19±1 d 7.69±0.02 a 133.90±4.10 b 2.20±0.02 b 1.10±0.01 a 3.86±0.06 b P4 35±2 b 7.67±0.03 a 156.50±2.40 a 2.41±0.01 a 1.03±0.02 a 4.16±0.12 a 表 2 与小麦孢囊线虫病害显著负相关的差异根系分泌物
Table 2. Metabolites that are significantly negatively correlated with cyst
编号 代谢物 分类 与土壤孢囊的相关性 一级分类 二级分类 P r M1 胞苷一磷酸-N-三甲基-2-氨基乙基磷酸酯CMP-N-trimethyl-2-
aminoethylphosphonate有机氧化物 有机氧化物 <0.01 −0.748 7 M2 DHMBOA葡萄糖苷DHMBOA hexose <0.001 −0.915 2 M3 甜菜碱betaine 有机酸及其衍生物 羧酸及其衍生物 <0.001 −0.890 5 M4 焦谷氨酸pyroglutamic acid <0.001 −0.843 1 M5 1-3-(4,5-二氢呋喃酮)-5-(羟甲基)-吡咯-2-羧醛1-3-(4,5-
dihydrofuranone)-5-(hydroxymethyl)-pyrrole-2-carboxyaldehyde<0.001 −0.871 3 M6 正亮氨酸norleucine <0.001 −0.881 9 M7 L-谷氨酸L-glutamic acid <0.001 −0.920 7 M8 吲哚丙烯酸indoleacrylic acid 有机杂环化合物 吲哚及其衍生物 <0.001 −0.934 8 M10 4-氧代-2-铃兰氨酸4-oxo-2-azetidinecarboxylic acid 内酰胺 <0.001 −0.910 1 M11 哌啶piperidine 哌啶类 <0.001 −0.874 8 M13 10,20-二羟基二十烷酸10,20-dihydroxyeicosanoic acid 脂质和类脂分子 脂肪酰类 <0.01 −0.730 2 M17 雌三醇-16 -葡萄糖醛酸苷estriol-16-glucuronide 类固醇及其衍生物 <0.001 −0.831 9 M18 17 β -雌二醇- 3 -磺酸17beta-estradiol 3-sulfate <0.001 −0.829 0 M21 酪胺tyramine 苯环化合物 苯及其衍生物 <0.001 −0.899 5 M25 肉桂酸cinnamic acid 苯丙素类和聚酮类 肉桂酸及其衍生物 <0.001 −0.858 7 M26 2-羟基肉桂酸2-hydroxycinnamic acid <0.001 −0.879 9 -
[1] JAIN A, LI Tongda, HUSTON D C, et al. Insights from draft genomes of Heterodera species isolated from field soil samples[J]. BMC Genomics, 2025, 26(1): 158. DOI: 10.1186/s12864-025-11351-0. [2] XU Zhipeng, LI Huixia, LIU Yonggang, et al. First report of cyst nematode (Heterodera elachista) on Zea mays in Gansu Province, China[J]. Plant Disease, 2021, 105(2): 511. DOI: 10.1094/pdis-01-20-0037-pdn. [3] ELLING A A. Major emerging problems with minor Meloidogyne species[J]. Phytopathology, 2013, 103(11): 1092−1102. DOI: 10.1094/PHYTO-01-13-0019-RVW. [4] ZHANG Dianli, WANG Hongyan, JI Xiaoxue, et al. Effect of abamectin on the cereal cyst nematode (CCN, Heterodera avenae) and wheat yield[J]. Plant Disease, 2017, 101(6): 973−976. DOI: 10.1094/PDIS-10-16-1441-RE. [5] ZHANG Jie, FU Bo, LIN Qitong, et al. Colonization of Beauveria bassiana 08F04 in root-zone soil and its biocontrol of cereal cyst nematode (Heterodera filipjevi)[J]. PLoS One, 2020, 15(5): e0232770. DOI: 10.1371/journal.pone.0232770. [6] WANG Jia, ZENG Guangzhi, HUANG Xiaobing, et al. 1, 4-naphthoquinone triggers nematode lethality by inducing oxidative stress and activating insulin/IGF signaling pathway in Caenorhabditis elegans[J]. Molecules, 2017, 22(5): 798. DOI: 10.3390/molecules22050798. [7] PUNDIR S, SINGH R, SINGH V K, et al. Mapping of QTLs and meta-QTLs for Heterodera avenae Woll. resistance in common wheat (Triticum aestivum L. )[J]. BMC Plant Biology, 2023, 23(1): 529. DOI: 10.1186/s12870-023-04526-y. [8] 张晓, 王东, 辛正. 生物防治技术在卫生害虫防制中的研究和应用进展[J]. 中国媒介生物学及控制杂志, 2021, 32(3): 378−384 ZHANG Xiao, WANG Dong, XIN Zheng. Research and application progress in biological control technology for hygiene pest control[J]. Chinese Journal of Vector Biology and Control, 2021, 32(3): 378−384. DOI: 10.11853/j.issn.1003.8280.2021.03.024. [9] ABD-ELGAWAD M M M, ASKARY T H. Factors affecting success of biological agents used in controlling the plant-parasitic nematodes[J]. Egyptian Journal of Biological Pest Control, 2020, 30(1): 17. DOI: 10.1186/s41938-020-00215-2. [10] QIU Wei, SU Huiqing, YAN Lingyun, et al. Organic fertilization assembles fungal communities of wheat rhizosphere soil and suppresses the population growth of Heterodera avenae in the field[J]. Frontiers in Plant Science, 2020, 11: 1225. DOI: 10.3389/fpls.2020.01225. [11] SHEN Jianbo, YUAN Lixing, ZHANG Junling, et al. Phosphorus dynamics: from soil to plant[J]. Plant Physiology, 2011, 156(3): 997−1005. DOI: 10.1104/pp.111.175232. [12] CAO Yifan, SHEN Zongzhuan, ZHANG Na, et al. Phosphorus availability influences disease-suppressive soil microbiome through plant-microbe interactions[J]. Microbiome, 2024, 12(1): 185. DOI: 10.1186/s40168-024-01906-w. [13] LI Liangliang, LUO Zhuzhu, LI Lingling, et al. Long-term phosphorus fertilization reveals the phosphorus limitation shaping the soil micro-food web stability in the Loess Plateau[J]. Frontiers in Microbiology, 2024, 14: 1256269. DOI: 10.3389/fmicb.2023.1256269. [14] SIDDIQUI Z A, IQBAL A, MAHMOOD I. Effects of Pseudomonas fluorescens and fertilizers on the reproduction of Meloidogyne incognita and growth of tomato[J]. Applied Soil Ecology, 2001, 16(2): 179−185. DOI: 10.1016/S0929-1393(00)00083-4. [15] HABASH S, AL-BANNA L. Phosphonate fertilizers suppressed root knot nematodes Meloidogyne javanica and M. incognita[J]. Journal of Nematology, 2011, 43(2): 95−100. [16] AL-HAZMI A S, DAWABAH A A M. Effect of urea and certain NPK fertilizers on the cereal cyst nematode (Heterodera avenae) on wheat[J]. Saudi Journal of Biological Sciences, 2014, 21(2): 191−196. DOI: 10.1016/j.sjbs.2013.10.002. [17] YADAV S, KANWAR R S. Effect of some fertilizers on hatching of cereal cysts nematode, Heterodera avenae[J]. Saudi Journal of Biological Sciences, 2021, 28(8): 4442−4445. DOI: 10.1016/j.sjbs.2021.04.039. [18] ZAMBELLI A, NOCITO F F, ARANITI F, et al. Unveiling the multifaceted roles of root exudates: chemical interactions, allelopathy, and agricultural applications[J]. Agronomy, 2025, 15(4): 845. DOI: 10.3390/agronomy15040845. [19] 杨帆. 伴生植物根系分泌物对根结线虫及番茄抗性的影响[D]. 哈尔滨: 东北农业大学, 2020 YANG Fan. Effects of Root Exudates from Companion Cropping Plants on Root knot Nematode and Resistance of Tomato[D]. Harbin: Northeast Agricultural University, 2020. DOI:10.27010/d.cnki.gdbnu.2020.000247. [20] 司兆胜. 土壤环境对大豆胞囊线虫繁殖影响及大豆抗性机制研究[D]. 哈尔滨: 东北农业大学, 2004 SI Zhaosheng. The Effect of Enviroment Situation on Soybean Cyst Nematode Hatch and the Mechanism of Soybean Resisting Soybean Cyst Nematode[D]. Harbin: Northeast Agricultural University, 2004. [21] ABDEL-RAHMAN A A, KESBA H H, AL-SAYED A A. Activity and reproductive capability of Meloidogyne incognita and sunflower growth response as influenced by root exudates of some medicinal plants[J]. Biocatalysis and Agricultural Biotechnology, 2019, 22: 101418. DOI: 10.1016/j.bcab.2019.101418. [22] LI Tao, WANG Hongyun, XIA Xiubo, et al. Inhibitory effects of components from root exudates of Welsh onion against root knot nematodes[J]. PLoS One, 2018, 13(7): e0201471. DOI: 10.1371/journal.pone.0201471. [23] ZHANG Huiying, TIAN Mengyang, JIANG Meiguang, et al. Effects of nitrogen and phosphorus additions on soil nematode community of soybean farmland[J]. Soil Ecology Letters, 2023, 6(2): 230200. DOI: 10.1007/s42832-023-0200-8. [24] MARSCHNER H. Mineral Nutrition of Higher Plants[M]. 2nd ed. London: Academic Press, 1995. [25] CHIOU T J, LIN Shui. Signaling network in sensing phosphate availability in plants[J]. Annual Review of Plant Biology, 2011, 62: 185−206. DOI: 10.1146/annurev-arplant-042110-103849. [26] 徐龙超, 依艳丽, 周晓阳. 钙、磷平衡对番茄光合作用特性及防御酶活性的影响[J]. 北方园艺, 2013(9): 190−193. XU Longchao, YI Yanli, ZHOU Xiaoyang. Effects of calcium and phosphorus interaction on photosynthesis and defense enzyme activity of tomato[J]. Northern Horticulture, 2013(9): 190−193. [27] 万宣伍, 田卉, 张伟, 等. 植物诱导抗性的机理及应用[J]. 植物医学, 2022, 1(1): 18−25. WAN Xuanwu, TIAN Hui, ZHANG Wei, et al. Mechanism and application of induced resistance in plant[J]. Plant Health and Medicine, 2022, 1(1): 18−25. DOI: 10.13718/j.cnki.zwyx.2022.01.003. [28] SVISTOONOFF S, CREFF A, REYMOND M, et al. Root tip contact with low-phosphate media reprograms plant root architecture[J]. Nature Genetics, 2007, 39(6): 792−796. DOI: 10.1038/ng2041. [29] SHARMA S, SUNDARESHA S, TIWARI R K, et al. Effect of phosphorous acid on late blight disease mitigation and minimization of fungicide doses under field conditions[J]. Journal of Plant Pathology, 2023, 105(3): 825−836. DOI: 10.1007/s42161-023-01376-3. [30] CHAI Y N, SCHACHTMAN D P. Root exudates impact plant performance under abiotic stress[J]. Trends in Plant Science, 2022, 27(1): 80−91. DOI: 10.1016/j.tplants.2021.08.003. [31] MANGHI M C, MASIOL M, CALZAVARA R, et al. The use of phosphonates in agriculture. chemical, biological properties and legislative issues[J]. Chemosphere, 2021, 283: 131187. DOI: 10.1016/j.chemosphere.2021.131187. [32] TZIN V, HOJO Y, STRICKLER S R, et al. Rapid defense responses in maize leaves induced by Spodoptera exigua caterpillar feeding[J]. Journal of Experimental Botany, 2017, 68(16): 4709−4723. DOI: 10.1093/jxb/erx274. [33] POLONI A, SCHIRAWSKI J. Red card for pathogens: phytoalexins in sorghum and maize[J]. Molecules, 2014, 19(7): 9114−9133. DOI: 10.3390/molecules19079114. [34] HANSEN T V A, SAGER H, TOUTAIN C E, et al. The Caenorhabditis elegans DEG-3/DES-2 channel is a betaine-gated receptor insensitive to monepantel[J]. Molecules, 2022, 27(1): 312. DOI: 10.3390/molecules27010312. [35] CHEN Min, HUANG Ying, MA Li, et al. Cis-3-indoleacrylic acid: a nematicidal compound from Streptomyces youssoufiensis YMF3.862 as V-ATPase inhibitor on Meloidogyne incognita[J]. Journal of Agricultural and Food Chemistry, 2024, 72(44): 24347-24358. [36] VANEGAS J A G, PACULE H B, CAPITÃO R M, et al. Methyl esters of (E)-cinnamic acid: activity against the plant-parasitic nematode Meloidogyne incognita and in silico interaction with histone deacetylase[J]. Journal of Agricultural and Food Chemistry, 2022, 70(22): 6624−6633. DOI: 10.1021/acs.jafc.1c08142. [37] CHEN Lin, LIU Yunpeng, CHEN Lin, et al. The function of root exudates in the root colonization by beneficial soil rhizobacteria[J]. Biology, 2024, 13(2): 95. DOI: 10.3390/biology13020095. [38] PARASAR B J, SHARMA I, AGARWALA N. Root exudation drives abiotic stress tolerance in plants by recruiting beneficial microbes[J]. Applied Soil Ecology, 2024, 198: 105351. DOI: 10.1016/j.apsoil.2024.105351. [39] SHARMA M, SALEH D, CHARRON J B, et al. A crosstalk between Brachypodium root exudates, organic acids, and Bacillus velezensis B26, a growth promoting bacterium[J]. Frontiers in Microbiology, 2020, 11: 575578. DOI: 10.3389/fmicb.2020.575578. [40] WEN Tao, ZHAO Mengli, YUAN Jun, et al. Root exudates mediate plant defense against foliar pathogens by recruiting beneficial microbes[J]. Soil Ecology Letters, 2021, 3(1): 42−51. DOI: 10.1007/s42832-020-0057-z. [41] LIANG Y, HUANG Y, LIU C, et al. Functions and interaction of plant lipid signalling under abiotic stresses[J]. Plant Biology, 2023, 25(3): 361−378. DOI: 10.1111/plb.13507. [42] KUŹNIAK E, GAJEWSKA E, KUŹNIAK E, et al. Lipids and lipid-mediated signaling in plant–pathogen interactions[J]. International Journal of Molecular Sciences, 2024, 25(13): 7255. DOI: 10.3390/ijms25137255. [43] BALLEUX G, HÖFTE M, ARGUELLES-ARIAS A, et al. Bacillus lipopeptides as key players in rhizosphere chemical ecology[J]. Trends in Microbiology, 2025, 33(1): 80−95. DOI:10.1016/j.tim.2024.08.001. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20250364






 下载:
下载: