-
类胡萝卜素是广泛分布于自然界的一类色素,迄今已发现了近800种[1],主要存在于植物的叶、花、果实和根等器官中,在吸引昆虫、鸟类传播花粉和种子中发挥作用[2]。类胡萝卜素可作为多种生物活性物质的前体,经过氧合酶或非酶裂解作用可以形成阿朴类胡萝卜素[3],后者及其衍生物可生成β-紫罗兰酮(β-ionone)等香气物质及脱落酸(abscisic acid,ABA)等植物生长调节剂[4]。作为类胡萝卜素裂解氧合酶(carotenoid cleavage oxygenases,CCO)中的重要成员,类胡萝卜素裂解双加氧酶1(carotenoid cleavage dixoygenase 1,CCD1)在不同的植物中所裂解的底物、作用位点不尽相同。研究发现[5],CCD1在C9~C10(C9′~C10′)位时剪切番茄红素、胡萝卜素、玉米黄质或脱辅基类胡萝卜素等,形成β-紫罗兰酮,β-环柠檬醛(β-cyclocitral),香叶基丙酮(geranylacetone)和假紫罗兰酮(pseudoionone)等芳香类物质;在番茄红素C5~C6(C5′~C6′)位裂解时则形成6-甲基-5-庚烯-2-酮[6],认为CCD1对基于类胡萝卜素代谢途径的香气物质合成发挥着重要作用。桂花Osmanthus fragrans在中国栽培历史悠久,集绿化、美化和香化为一体,花香和花色是其重要观赏性状。类胡萝卜素裂解双加氧酶1(OfCCD1)[7]降解桂花中的着色物质——α-胡萝卜素和β-胡萝卜素[8],合成主要香气物质α-紫罗酮和β-紫罗酮[9]。基因启动子控制着基因在特定的组织[10]、特定的发育阶段[11]以及一定的环境条件下表达[12];分离相关基因启动子,分析其序列及其作用元件,并研究其功能,可明确该基因的调控因子及其作用机制。本研究利用染色体步移技术克隆了OfCCD1启动子,通过启动子序列分析、载体构建和瞬时表达分析,初步明确了其功能,为揭示OfCCD1基因调控花色花香代谢机制奠定基础。
HTML
-
供试材料为6~8年生地栽丹桂品种‘堰虹桂’‘Yanhong Gui’,栽植于浙江农林大学桂花资源圃。
-
Taq聚合酶、限制酶(DraⅠ,EcoRⅤ,PvuⅡ,StuⅠ),质粒载体PMD18-T,大肠埃希菌Escherichia coli DH5α,胶回收试剂盒,DNA片段纯化试剂盒和无缝连接试剂盒均购自Takara公司(大连)。
-
参照十六烷基三甲基溴化铵法(CTAB)提取‘堰虹桂’基因组DNA[13]。
-
根据‘堰虹桂’转录组数据库中的CCD1序列(GenBank登录号MG138152)[14]和BALDERMANN等发表的OfCCD1(GenBank登录号AB526197.1)序列[9],用Primer Primer 5.0设计下游特异性引物1(GSP1),特异性引物2(GSP2)和特异性引物4(GSP4);利用上述2段序列的重复序列设计特异性引物3(GSP3);利用接头引物1(AP1)与GSP1,接头引物2(AP2)与GSP2经2轮聚合酶链式反应(PCR)获得的启动子片段设计特异性引物5(GSP5)。利用pBI121质粒上的β-葡萄糖苷酸酶(β-Glucosidase,GUS)基因序列设计上游引物GUS-F和下游引物GUS-R。引物及接头均由上海生工合成(表 1)。
引物名 称序列(5'→3') GSP1 CTTCACAAACAGCCATTCCAACCAGTCTAT GSP2 TCGGGCTTTACTGCCACCACACCATTTTC GSP3 GAGGAGGAGTCTCATCAACTGGAGCAAAAT GSP4 GCATCATTTTCACAAACAGCCATTCCAAC GSP5 AGCCTCAAGTTTTGTCCTATTGCCAC AP1 GTAATACGACTCACTATAGGGC AP2 ACTATAGGGCACGCGTGGT GWA GTAATACGACTCACTATAGGGCACGCGTGGTCGACGGCCCGGGCTGGT CCD1P-L-F TGATTACGCCAAGCTAAAGGAAGAGTATTCACTTTTGGC CCD1P-L-R CCGGGGATCCTCTAGCTGTTGATCCTAATTGAACTCTCAC CCD1P-S-F TGATTACGCCAAGCTGAAGCACATGTCTCCCA CCD1P-S-R CCGGGGATCCTCTAGCTCTTGGTTCTGAATTGA GUS-F TGATTACGCCAAGCTGATCAGTTCGCCGATGCAG GUS-R CCGGGGATCCTCTAGAAGTGCGCTTGCTG Table 1. Primer sequences used in the cloning of OfCCD1 promoters
-
① DNA文库的构建。分别用Dra Ⅰ,EcoR Ⅴ,Pvu Ⅱ,Stu Ⅰ 4种限制性内切酶对提取到的DNA进行酶切。酶切体系为基因组DNA 25.0 μL(100 mg·L-1),限制内切酶8.0 μL,10×限制酶buffer 10.0 μL,灭菌水57.0 μL,总体积100.0 μL,37 ℃过夜。取5.0 μl酶切产物用质量分数0.6%琼脂糖进行检测。按照DNA纯化试剂盒的说明书对酶切产物进行纯化后加接头。分别取4组酶切纯化的DNA各4.8 μL,染色体步移接头GWA 1.9 μL,10×连接缓冲液0.8 μL,T4 DNA连接酶0.5 μL,16.0 ℃过夜;70.0 ℃水浴5 min,加入32.0 μL去离子水。②聚合酶链式反应(PCR)扩增。取AP1,引物GSP1/GSP3,模板各1.0 μL,预混合Taq酶10.0 μL,去离子水补至20.0 μL进行第1轮PCR。扩增程序为94.0 ℃ 5 min;94.0 ℃ 25 s,72.0 ℃ 3 min,7循环;94.0 ℃ 25 s,65.0 ℃ 3 min,32循环;67.0 ℃ 7 min。取第1轮产物1.0 μL并稀释50倍作为第2轮PCR的模板。第2轮PCR体系为:AP2,GSP2/GSP4/GSP5,模板各1.0 μL,预混合Taq酶10.0 μL,去离子水补至20.0 μL。扩增程序为94.0 ℃ 5 min;94.0 ℃ 25 s,72.0 ℃ 3 min,5循环;94.0 ℃ 25 s,65.0 ℃ 3 min,20循环;67.0 ℃ 7 min。取GUS-F,GUS-R和pBI121质粒各1.0 μL,预混合Taq酶10.0 μL,去离子水补至20.0 μL进行GUS序列扩增。扩增程序为95.0 ℃ 5 min;95.0 ℃ 30 s,69.8 ℃ 30 s,72.0 ℃ 1 min,35循环;72.0 ℃ 10 min;4.0 ℃ 10 min。质量分数为1.2%的琼脂糖凝胶电泳检测。
-
切胶回收按照MiniBEST Agarose Gel DNA Extraction Kit Ver.4.0(TaKaRa,大连)的说明书进行。载体连接按照PMD18-T载体说明书(Takara,大连)进行,连接后的重组质粒导人大肠埃希菌DH5α感受态细胞中,在50 mg·L-1氨苄青霉素的固体LB培养基上进行蓝白斑筛选,挑取白色单菌落菌液PCR检测后将阳性克隆送公司测序。序列初步分析采用DNAMAN软件进行。启动子序列作用元件分析采用在线网站PlantCARE(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/)进行。
-
根据获得的OfCCD1的启动子序列,利用Takara(http://www.clontech.com)无缝连接引物设计软件设计3对无缝连接引物CCD1P-S-F和CCD1P-S-R,CCD1P-L-F和CCD1P-L-R,GUS-F和GUS-R。具体操作步骤按照Takara无缝连接试剂盒的说明书进行。将重组好的表达载体利用冻融法转入农杆菌Agrobacterium tumefaciens GV3101感受态。随后将烟草Nicotiana tabacum叶片剪切成0.5 cm × 0.5 cm的叶块,在农杆菌菌液吸光度D(600)为0.6的侵染液中浸染10 min;无菌滤纸吸干叶片表面的菌液,将侵染的外植体移至于无菌水浸润的滤纸上培养24 h并进行GUS染色,37 ℃下保温16~24 h。V(乙酸):V(乙醇)=3:1的混合液脱色后取出,对染色结果进行拍照。
1.1. 植物材料
1.2. 主要试剂
1.3. 方法
1.3.1. DNA提取
1.3.2. 引物设计与合成
1.3.3. DNA文库的构建、扩增
1.3.4. PCR产物回收、连接、转化鉴定及序列测定与分析
1.3.5. 表达载体的构建及瞬时表达分析
-
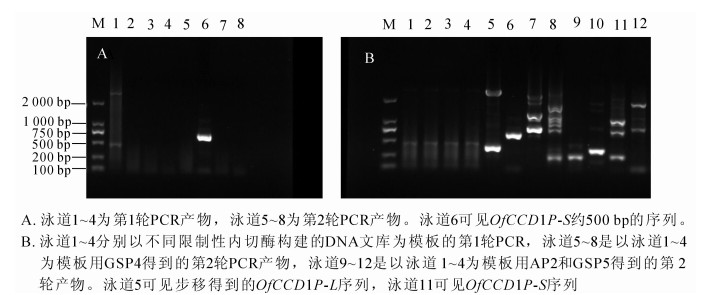
以‘堰虹桂’DNA为模板,分别利用引物GSP1和GSP2,接头引物AP1和AP2进行2轮PCR,在EcoR文库扩增得到条带;经比对和拼接得到长度为511 bp的序列(图 1A)。利用引物GSP3和GSP4,接头引物AP1和AP2经过2轮PCR,在DraⅠ文库中得到约2 000 bp的条带(图 1B)。测序后,经比对和拼接得到长度为2 747 bp的条带,命名为OfCCD1P-L(图 2)。利用GSP3和GSP5经过2轮PCR后在Pvu Ⅱ文库中得到750 bp左右的条带(图 1B),经过拼接比对得到OfCCD1上游981 bp的启动子序列,命名为OfCCD1P-S(图 3)。
-
利用PlantCARE网站对启动子序列进行序列分析发现,OfCCD1P-L有TATA-box和CAAT-box等基本作用元件,同时有7个响应元件,响应茉莉酸甲酯、赤霉素、水杨酸、乙烯的元件,以及热激元件,鸟类成髓细胞性白血病病毒癌基因同源物(MYB)结合位点,并有4个响应脱落酸(ABA)的核心序列ACGT(表 2)。OfCCD1P-S中含有TATA-box和CAAT-box等基本作用元件,同时有3个光响应元件,1个热激响应元件以及1个ABA响应元件(表 3),并有4个ABA响应元件(ABRE)核心序列ACGT。
顺式作用元件名称 位置 序列(5′→3′) 功能 G-Box -326, -664, -2 584 CACGTA 光响应元件 GA-motif -257, -2 738 AAAGATGA 光响应元件的一部分 ATCT-motif -2 564 AATCTAATCT 参与光响应的部分保守DNA序列 Box I -429, -l 649 TTTCAAA 光响应元件 AE-box -737 AGAAACAT 光响应元件的一部分 Box 4 -733 ATTAAT 参与光响应的部分保守DNA序列 GAG-motif -300 AGAGATG 光响应元件的一部分 CAAT-box -ll5, -569 CAAT 一般元件 CAT-box -l 839 GCCACT 与分生组织相关的顺式元件 CGTCA-motif -2 580 CGTCA 茉莉酸甲酯响应元件 TGACG-motif -486 TGACG 茉莉酸甲酯响应元件 HSE -2 066 AAAAAATTTC 热激响应元件 LTR -l 4ll CCGAAA 低温响应元件 MBS -96l, -l 256 TAACTG MYB结合位点 P-box -2 002 CCTTTTG 赤霉素响应元件 Skn-l_motif -968, -l 3l0, -l 544, -2 33l GTCAT 胚乳中表达的必备元件 TATA-box -268, -356, -879, -894, -909 TATA 一般元件 TC-rich repeats -l l49, -2 5l9 ATTTTCATCA 参与防御和胁迫的元件 TCA-element -42l, -l 340 TCAGAAGAGGA 水杨酸响应元件 GCN4_motif -402 TGTGTCA 胚乳中表达的必备元件 ERE -428 ATTTCAAA 乙烯响应元件 GCN4_motif -402 TGTGTCA 胚乳中表达的必备元件 Table 2. Cis-acting elements in OfCCD1P-L
顺式作用元件名称 位置 序列(5'→3') 功能 3-AF1 binding site -911 AAGAGATATTT 光响应元件 GATA-motif -102 AAGATAAGATT 光响应元件的一部分 ACE -316 ACGTGGA 光响应元件 AAGAA-motif -443 GAAAGAA ABRE -324 ACGT 脱落酸响应元件 CAAT-box -12, -267, -530, -547, -566, -659, -723 CAAT(T) 一般元件 HSE -901 AAAAAATTTC 热激响应元件 Skn-1_motif -278, -503 GTCAT 在胚乳中表达所必须的元件 TATA-box -54, -158, -472, -623 TAATA/TATA 基本元件 TC-rich repeats -673 ATTTTCTTCA 参与防御和胁迫的元件 Table 3. Cis-acting elements in OfCCD1P-S
-
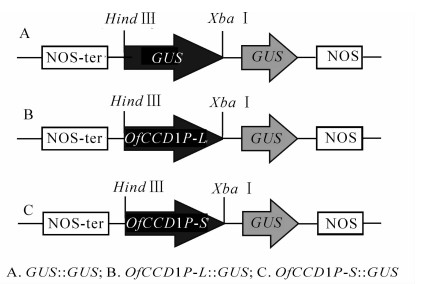
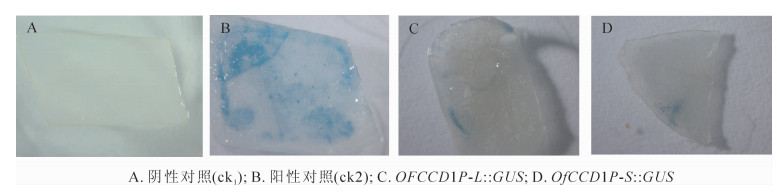
将克隆得到的启动子和GUS片段分别与pBI121质粒进行重组(图 4),以含GUS::GUS表达载体的菌株为阴性对照(ck1),以含pBI 121载体菌株为阳性对照(ck2),对构建的OfCCD1P-L::GUS和OfCCD1P-S::GUS表达载体进行瞬时表达分析(图 5)。从图 5可以看出,阴性对照没有着色,阳性对照着色范围和程度最好,OfCCD1P-L::GUS表达载体和OfCCD1P-S::GUS表达载体均有着色,但着色都比阳性对照要弱。
2.1. 启动子克隆
2.2. 启动子序列分析
2.3. 植物表达载体构建与瞬时表达分析
-
桂花OfCCD1基因有2个拷贝[14]。在启动子克隆过程中,第1次步移并未得到足够长的序列。目前,已报道的OfCCD1序列有2个:ZHANG等[14]发现的CCD1序列(GenBank登录号MG138152)和BALDERMANN发表的OfCCD1序列(GenBank登录号AB526197.1)[9]。本研究利用上述2个序列的重复序列设计了引物GSP3,并在GSP3 5′上游设计了GSP4,利用已获得的部分OfCCD1启动子序列设计了引物GSP5,分别步移从而获得了OfCCD1P-S和OfCCD1P-L的启动子序列。其中OfCCD1P-L长度为2 747 bp,OfCCD1P-S长度为981 bp。原因是OfCCD1启动子区域的2个拷贝所含酶切位点不同,构建文库时OfCCD1P-L启动子区域被内切酶截断的区域短,步移得到的启动子就较长;而OfCCD1P-S启动子区域大部分被截断,所得的启动子序列就较短。类似地,已报道的CCD家族其他成员的启动子长度也有差异,如拟南芥Arabidopsis thaliana的AtCCD7[10]和AtNCED2[15],花生Arachis hypogaea的AhNCED1[16]启动子都有2 000 bp左右,而菊花Chrysanthemum morifolium的CmCCD4a-5[17]和桂花的OfCCD4[18]启动子则分别为1 094 bp和1 337 bp。上述文献中进行启动子克隆所用方法不尽相同,这也是造成获得启动子长度不一的因素。
本研究所获得的2个OfCCD1启动子所含元件种类是具有一致性的,都含有光响应元件、热激响应元件和ABA响应元件,其中较多的是光响应元件。在桂花中,OfCCD1的表达受光照影响[9],证实了OfCCD1启动子中的光响应元件的存在。同一个亚家族的其他成员,如CCD4[19]和CCD2[20]的启动子中也发现了光响应元件。这表明光响应元件在CCD家族的启动子中可能是普遍存在的。不过功能上可能有差异,因为在藏红花Crocus sativus中,CsCCD2的表达是受光抑制的[20]。
此外,克隆得到的2个启动子中含有4个ACGT序列[21]。ACGT是启动子中一个重要的顺式作用元件,该序列可以响应水杨酸(salicylic acid,SA),紫外线,ABA和茉莉酸(jasmonic acid,JA)[22]的处理。有研究表明:响应ABA至少需要2个ACGT序列,且2个ACGT之间的碱基数不同,响应的激素种类也不同。MEHROTRA等[23]的研究发现:当2个ACGT序列之间的距离是5 bp时,这段序列响应SA的处理;当距离是25 bp时,该序列响应ABA处理。在碱蓬Suaeda salsa[24]和大豆Glycine max[25]中ABA处理会使CCD1的表达量升高,因此,桂花中OfCCD1的表达极有可能响应ABA的诱导,具体的响应机制还需要进一步研究。














 DownLoad:
DownLoad: