-
花椒Zanthoxylum bungeanum为芸香科Rutaceae花椒属Zanthoxylum落叶灌木,俗称红花椒,是一种兼具生态、经济和社会效益的优良经济树种[1]。目前,在中国花椒栽培已覆盖20多个省份,形成了以花椒、竹叶花椒Z. armatum和青花椒Z. schinifolium为主的不同栽培区域[2]。花椒多栽植于北方或南方高海拔冷凉地区,是栽培面积最大的种类[3],其干果皮可作为中药、香料和调味原料等,已被广泛应用于食品、医药、农药、化工、保健和美容等多个领域[4−6],具有极高的综合开发利用潜力。然而,花椒落花落果现象严重,落花率和落果率分别达72.7%和59.1%,整个花序坐果率仅为11.2%[7],严重制约花椒的丰产与稳产。花果脱落是受树体营养、激素平衡及环境因子共同调控的复杂生理过程[8−9]。花芽分化作为花器官形态建成与发育的关键起始阶段,其进程与质量直接决定花器发育水平及后期坐果潜能,是影响花果发育与脱落的重要内在基础[10]。云南昭通是典型的南方高海拔冷凉花椒产区,其花果发育问题与全国花椒类似,但因缺乏对当地花椒花芽分化规律的基础研究,生产中难以通过营养调控等措施有效解决落花落果问题。因此,研究花椒花芽分化过程中形态结构与内源激素变化规律,可为制定针对性保花保果措施,提高坐果率和产量提供科学依据。
形态解剖学观察是研究植物花芽分化最直观的方法而被普遍采用。常剑文等[11]采用徒手切片法阐述花椒花芽分化的过程,将其划分为未分化期、分化始期、花序轴分化期、花蕾分化期、萼片分化期和雌蕊分化期6个时期,并指出在河北省涉县城关镇,花芽分化始于当年6月初,翌年3月底结束。胡梅等[12]的研究结果指出:四川省三台县芦溪镇竹叶花椒花芽分化包括7个时期,从当年7月底延续至翌年3月中旬完成1个周期的花芽分化;桂薇竹[13]基于贵州省贞丰县金井村异常的雌雄花芽分化研究指出:顶坛花椒Z. armatum ‘Dingtan’花芽分化包括7个时期。不同产地、不同种类和具有特异性的花椒,其花芽形态分化进程和阶段都呈现极大的差异,甚至出现罕见的雄蕊分化现象,因此有必要针对不同种或品种及同一种或品种的不同栽培区域开展花芽分化研究,为其丰产栽培提供理论支撑。目前,花椒花芽分化的研究多集中于北方暖温带及南方亚热带地区[11−13],未见关于冷凉地区花椒花芽分化的相关研究。基于已有研究资料,有必要对冷凉山区栽培的花椒花芽分化相关阶段的形态及结构等开展研究,为提高产量和质量的栽培措施研发提供理论依据。
花芽分化是植物从营养生长向生殖生长过渡的关键阶段[14],受植物遗传特性、植物体营养物质和环境条件等共同影响,其中内源激素是影响花芽分化的关键因子之一。多种内源激素相互作用协同调控花芽按照一定程序完成分化[15−17]。常见的花芽分化内源激素包括脱落酸(abscisic acid, ABA)、赤霉素(gibberellin a3, GA3)、生长素(indole-3-acetic acid, IAA)和玉米核苷素(zeatin riboside, ZR)等[18]。有研究指出:低水平的GA3、IAA和高水平的ABA以及ABA/GA3促进汉源葡萄青椒Z. armatum ‘Hanyuan Putao Qingjiao’花芽分化[19−20];周朝彬等[21]的研究结果表明:高浓度的ABA、IAA和GA3促进顶坛花椒花芽分化;桂薇竹[13]指出:低水平的GA3促进顶坛花椒花器官的分化和发育。目前,有关花椒内源激素动态特征变化的研究亦不多,且主要集中于竹叶花椒的研究,针对冷凉地区花椒花芽分化过程中内源激素的变化规律及调控机制的研究不足。本研究以典型冷凉地区云南昭通产区的花椒为研究对象,在观察其花芽分化进程和形态变化的基础上,结合石蜡切片法观察花芽结构变化,同时测定花芽内源激素质量分数,分析其变化特征与规律,旨在解析冷凉山区栽培的花椒花芽分化过程中形态与结构及内源激素的动态变化,为研究有效调控养分和激素的培育措施,提高花椒坐果率和产量提供基础理论支撑。
-
研究地位于云南省昭通市鲁甸县龙树镇花椒基地(27°21' N,103°27' E),海拔为2 184 m,年平均气温为10.9 ℃,年平均降水量为1 047.0 mm,1月和7月(最低和最高)平均气温分别为5.0和16.0 ℃,无霜期为200.0 d,年日照时数为1 702.0 h,属暖温带低纬度山地季风气候[22]。黄壤土。经测定土壤pH为4.73,土壤有机质为46.2 g·kg−1;全氮、全磷和全钾分别2.09、1.56和6.29 g·kg−1,碱解氮、有效磷和速效钾分别为211.0、69.9和208.0 mg·kg−1。研究地属花椒适宜生长区域。
-
试验材料采集于统一规范管理的花椒种植园。该椒园于2020年采用‘小龙袍’‘Xiaolongpao’穗条嫁接于2年生实生‘大红袍’‘Dahongpao’砧木建成,株行距3 m×4 m。田间管理措施一致,全年未发生显著病虫害危害。选择椒园内无病虫害、生长势基本一致的10株作为采样植株,采集其样品并测定相关指标。所选植株平均地径、株高和冠幅分别为6.16 cm,2.97 m和14.56 m2。
-
参照常剑文等[11]的研究确定采样时间和方法,于2024年5月23日至2025年3月31日共采样32次。其中,5月23日至10月31日隔7~10 d采样1次;11月1日至翌年2月1日隔30 d采样1次;翌年2月1日至3月31日隔10 d采样1次。在树冠中部外围东、南、西、北4个方向各采集1枝春梢,从每枝梢基部往上第6~10节处各取1~2个芽作为测定样品。每次采集的样品混合后均分为3份,其中一份用于形态观察,保鲜保存;一份置于福尔马林-丙酸-乙醇(formalin-propionic acid-alcohol, FPA)固定液[甲醛∶丙酸∶体积分数为70%乙醇为1∶1∶18 (体积比)]中保存于4 ℃低温冰箱,用于芽结构观察;另一份用锡箔纸包裹放入液氮中速冻,随后转存于−80 ℃冰箱,用于内源激素质量分数测定。
-
通过直观及体视显微镜观察保鲜保存的花芽样品的形态特征,并拍照记录芽的形态,测定其横径和纵径。芽的结构采用常规石蜡切片法[23]观测,每个时期分别采集10~20个花芽制作有效石蜡切片10张,共计320张。采用光学显微镜观察花芽结构并拍照记录。
-
采用智绪等[24]超高效液相色谱串联质谱法(UPLC-MS/MS)测定和计算不同发育时期花芽的GA3、IAA、ZR和ABA质量分数,并计算其比值。每个样品3次重复。
-
试验数据采用SPSS 26软件进行方差分析(ANOVA),处理间存在显著或极显著差异的指标,采用邓肯氏(Duncan’s)[25]法进行多重比较。数据分析采用Excel 2021软件,图片选用Photoshop CS3软件处理。
-
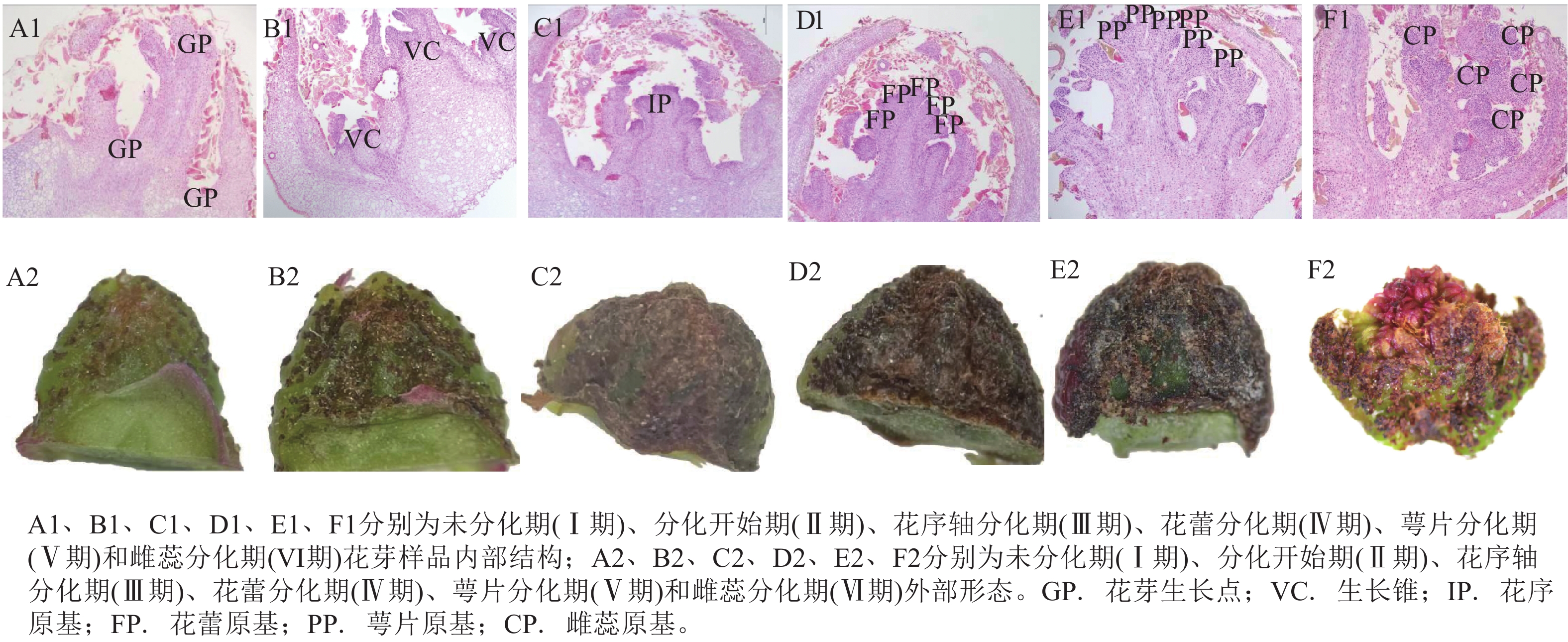
由图1可见:花椒花芽在分化期间呈现一系列具有典型特征的结构与形态变化,可将其划分为6个阶段,即未分化期(Ⅰ期)、分化开始期(Ⅱ期)、花序轴分化期(Ⅲ期)、花蕾分化期(Ⅳ期)、萼片分化期(Ⅴ期)和雌蕊分化期(Ⅵ期)。
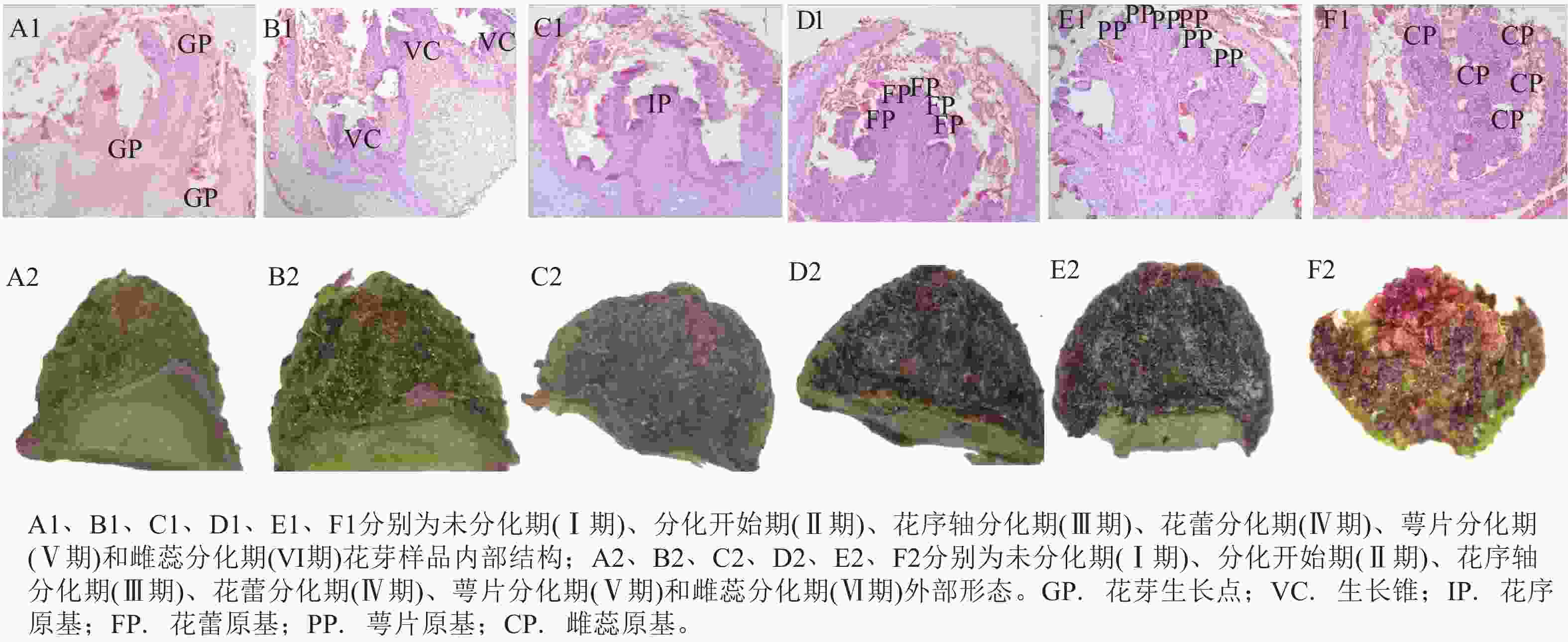
Figure 1. Internal and external morphology of flower buds during different stages of differentiation
各时期解剖结构与形态呈现相对应的特点,可通过形态观测判断其结构发育的阶段。① Ⅰ期(图1A1)。此阶段,花芽生长点(GP)处的原分生组织细胞体积较小,性状相似且排列紧密整齐。外部形态呈现芽体较小,生长点扁而宽,与叶芽无明显区别的特点(图1A2)。② Ⅱ期(图1B1)。主生长锥(VC)逐渐变宽、膨大并向上突起,且沿纵向伸长呈“八”字形,主生长锥两侧的附生长锥也同步隆起呈椭圆状,标志着花序总轴分化启动。外部形态的芽体略微膨大、黑色斑点增多,包裹更加紧密,与未分化期相比形态差异明显(图1B2)。③ Ⅲ期(图1C1)。花序原基(IP)上陆续分化出多个圆形或近圆形的小凸起,并逐渐伸长、增多,此为花序二级轴和三级轴,随后凸起逐渐伸长呈椭圆状。外部芽体明显增大且更加饱满,表面布满被毛,颜色加深(图1C2)。④ Ⅳ期(图1D1)。花序原始体继续伸长,分轴增多,在分轴顶端出现略呈弧面的小凸起,即随着花序延伸生长,花蕾原基(FP)逐渐彼此分离,顶端形态由圆扁状过渡到扁平状,形成伞房状花序的顶端花原基。外部芽体整体继续膨大伸长,外部被一层柔软的胶质绒毛覆盖,芽尖略带红色(图1D2)。⑤ Ⅴ期(图1E1)。花蕾原基进一步发育呈半圆形,在其外侧出现小凸起,逐渐伸长并向内弯曲生长,即为萼片原基(PP)。形态方面,芽体继续膨大,整体呈棕褐色,被两侧叶原基紧密包裹(图1E2)。⑥ Ⅵ期(图1F1)。随着分化继续进行,前期内卷的萼片原基逐渐张开,其内部的花蕾原基进一步隆起呈半球形,此为雌蕊原基(CP),该原基顶端变得圆润饱满,细胞排列更为紧密。外部芽体逐渐膨大,整体呈饱满的圆球形或近球形,芽体表面附着的胶状物逐渐干燥脱落,芽顶端可隐约观察到内部的雌蕊原基(图1F2)。
-
根据采样时间对应的花芽解剖结构观察(表1),可明确花椒花芽分化进程的时间。①Ⅰ期。自开花结束(4月底)至5月下旬上半期。5月23日100%的腋芽尚未开始形态分化(表1),是花芽未分化的证据。Ⅰ期大约持续20 d,说明花椒花芽处于未分化的时间较短。②Ⅱ期。始于5月下旬的下半期,为花芽分化临界期,持续至6月中旬。5月31日Ⅱ期花芽比例为40%,至6月13日Ⅱ期的花芽比例降至20%,同时Ⅲ期花芽比例明显增加,并出现Ⅳ期花芽(表1),表明Ⅱ期花芽分化将结束。6月6日,同时观测到Ⅰ~Ⅲ期花芽,说明花芽分化过程是渐进的。Ⅱ期花芽分化进程较快。③Ⅲ期。该期持续时间较长,自6月初至7月中旬,约40 d。6月6日Ⅲ期花芽比例占10%,标志花序轴分化期正式开始,至6月20日达到最高值70%,随后其比例逐渐降低,至7月14日降至10%(表1)。与Ⅱ期花芽类似,7月4—14日,同时观察到的Ⅲ、Ⅳ和Ⅴ期花芽并存(表1),进一步证实花芽分化是一个渐进、连续的过程,且各分化阶段之间存在明显重叠。④Ⅳ期。6月中旬至8月上旬,是花蕾分化期,延续约60 d。6月13日Ⅳ期花芽比例占20%,峰值出现在7月4日,8月12日降至10%(表1),说明该分化期时间跨度最长且主要集中6月下旬至7月上旬。在此期间,存在Ⅱ期或Ⅲ期花芽重叠的现象。7月4—14日,Ⅲ~Ⅴ期花芽同时存在(表1)。⑤Ⅴ期。7月初至8月中旬,持续约50 d,分化时间跨度仅次于Ⅳ期。7月4日Ⅴ期花芽比例占10%,8月19日全部分化完成,此后至翌年2月21日,为下一时期,Ⅴ期花芽比例逐渐下降,至3月12日降至10%,说明花椒花芽分化跨年度完成。与Ⅲ和Ⅳ期相一致,该期内Ⅲ~Ⅴ期的花芽同时出现。⑥Ⅵ期。翌年2月下旬至3月下旬,花芽分化再次启动,进入雌蕊分化期,其延续约30 d。3月21日,显微结构显示子房体已十分清晰,所有花芽全部雌蕊分化。3月31日,子房体顶端已分化柱头原始体,芽体萌动,花蕾显现,标志着整个花芽分化过程全面完成。
采样日期 各分化阶段花芽比例/% 采样日期 各分化阶段花芽比例/% Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ Ⅵ Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ Ⅵ 05-23 100 - - - - - 09-20 - - - - 100 - 05-31 60 40 - - - - 09-30 - - - - 100 - 06-06 20 70 10 - - - 10-08 - - - - 100 - 06-13 - 20 60 20 - - 10-15 - - - - 100 - 06-20 - - 70 30 - - 10-22 - - - - 100 - 06-26 - - 40 60 - - 10-31 - - - - 100 - 07-04 - - 20 70 10 - 11-21 - - - - 100 - 07-14 - - 10 60 30 - 12-21 - - - - 100 - 07-22 - - - 40 60 - 01-21 - - - - 100 - 07-29 - - - 30 70 - 02-01 - - - - 100 - 08-05 - - - 20 80 - 02-11 - - - - 100 - 08-12 - - - 10 90 - 02-21 - - - - 40 60 08-19 - - - - 100 - 03-02 - - - - 20 80 08-26 - - - - 100 - 03-12 - - - - 10 90 09-02 - - - - 100 - 03-21 - - - - - 100 09-10 - - - - 100 - 03-31 - - - - - 100 说明:-表示无此项。 Table 1. Flower bud ratio at each stage of flower bud differentiation
-
在花芽分化的不同阶段,腋芽的形态与大小呈现极显著的阶段性变化。Ⅰ~Ⅵ期,腋芽横径、纵径和纵径/横径分别为1.15~4.05 mm、0.85~3.75 mm和0.73~0.92。其中,横径不同分化时期间两两具有极显著的差异(P<0.01),纵径除Ⅲ期和Ⅳ期之间外,两两分化期间亦呈极显著的差异(P<0.01),纵径/横径则仅Ⅰ期的极显著地低于Ⅲ~Ⅵ期的(P<0.01,表2)。腋芽的形态变化与其尺寸生长相一致。在Ⅰ期,腋芽呈扁平状,未出现分化特征;Ⅱ~Ⅴ期,从腋芽开始伸长,略微膨大,随分化期延长极显著膨大,纵径与横径同步增加;在Ⅵ期,横径和纵径达到最大值,芽体趋于圆形,形态分化最为明显,标志着花蕾结构已全面构成。基于腋芽形态和纵横径尺寸变化与花芽分化的同步变化规律,可通过腋芽形态和尺寸判断花芽的分化期。
花芽分化期 横径/mm 纵径/mm 横径/纵径 花芽分化期 横径/mm 纵径/mm 横径/纵径 Ⅰ 1.15±0.05 Df 0.85±0.06 Df 0.73±0.02 Bc Ⅳ 2.06±0.05 Cc 1.74±0.07 Cc 0.85±0.04 Aab Ⅱ 1.35±0.05 De 1.11±0.05 De 0.82±0.03 ABb Ⅴ 3.49±0.07 Bb 2.98±0.09 Bb 0.85±0.02 Aab Ⅲ 1.81±0.13 Cd 1.51±0.06 Cd 0.85±0.06 Aab Ⅵ 4.05±0.05 Aa 3.75±0.06 Aa 0.92±0.01 Aa 说明:同列数据后不同大写字母表示不同时期间差异极显著(P<0.01),不同小写字母表示不同时期间差异显著(P<0.05)。 Table 2. Morphological characteristics of Z. bungeanum flower buds at different developmental stages
-
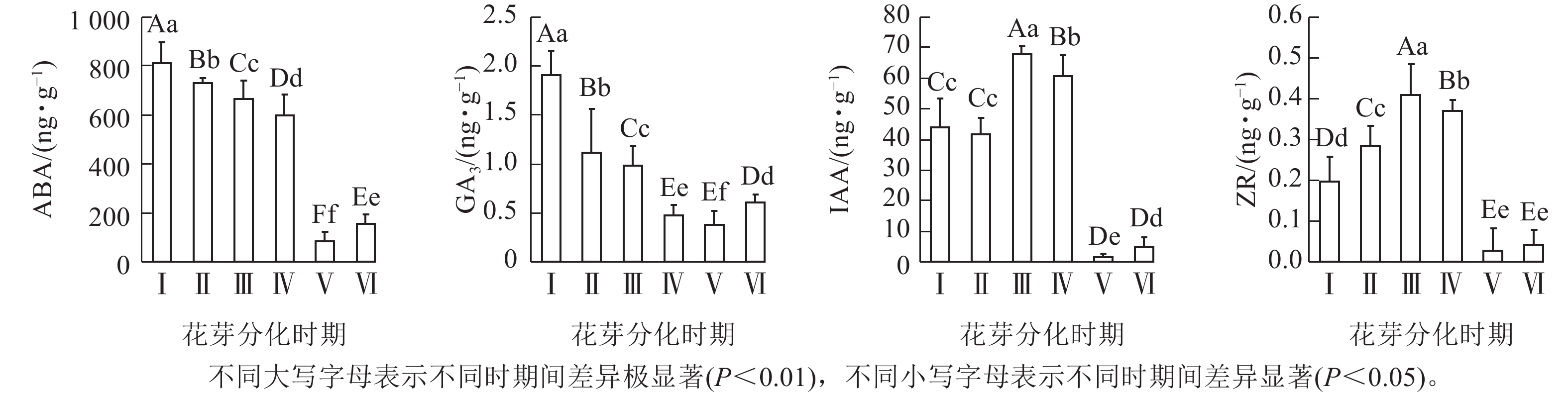
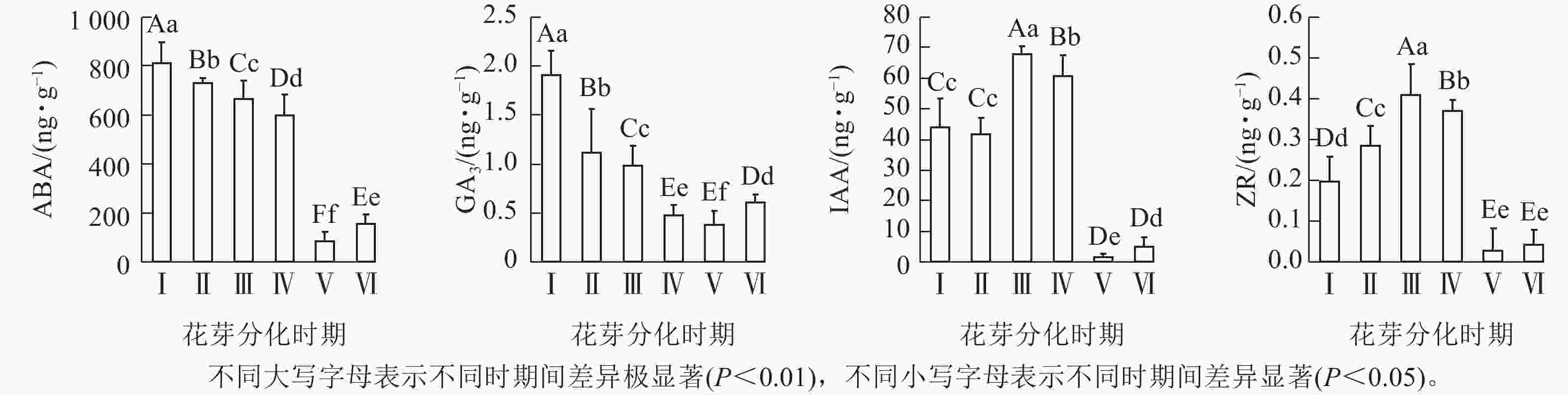
由图2可知:花椒花芽分化过程中ABA、GA3、IAA和ZR质量分数分别为84.61~810.73、0.37~1.91、1.41~67.73和0.03~0.41 ng·g−1。分化期内,4种内源激素质量分数均存在极显著差异(P<0.01),其中,Ⅰ期的ABA和GA3质量分数极显著高于Ⅴ期的,且除Ⅳ~Ⅴ期外,随花芽分化的进展,其余各时期呈现持续极显著降低,至Ⅵ期极显著地回升高于Ⅴ期的。这说明较高水平的ABA和GA3可能抑制花椒花芽分化启动,反之,低水平ABA和GA3有利于诱导花芽分化进行,促进形态结构的建成。与ABA和GA3变化不同,IAA和ZR质量分数均在Ⅲ期达到峰值,且极显著高于其余各个时期(P<0.01),至Ⅴ和Ⅵ期降至最低,且极显著低于其余各时期(P<0.01),表明高水平的IAA和ZR促进花芽分化的进行。在整个花芽分化过程中,Ⅴ期的内源激素质量分数均极显著低于Ⅰ~Ⅳ期(P<0.01),与Ⅵ期无显著差异,说明Ⅴ期时花椒分化形态结构基本建成,对内源激素需求相应较低,也间接说明Ⅰ~Ⅳ期可能是花芽分化的关键时期。因此,在花椒分化关键时期内,可通过外源喷施调节剂调控内源激素,抑制或促进花芽分化进程,从而调节花椒开花结实,实现花椒的优质丰产。
-
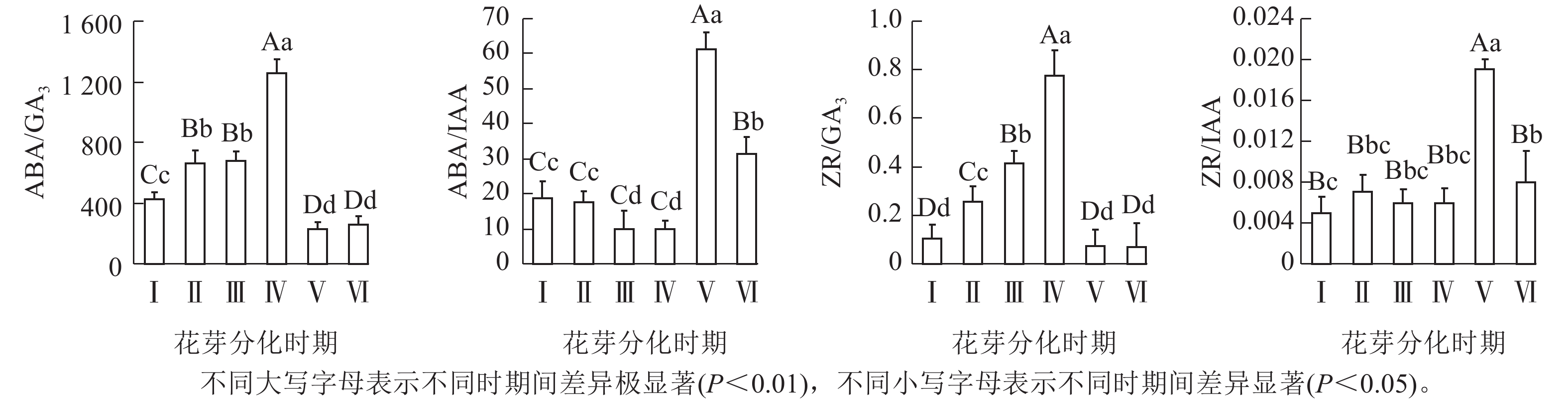
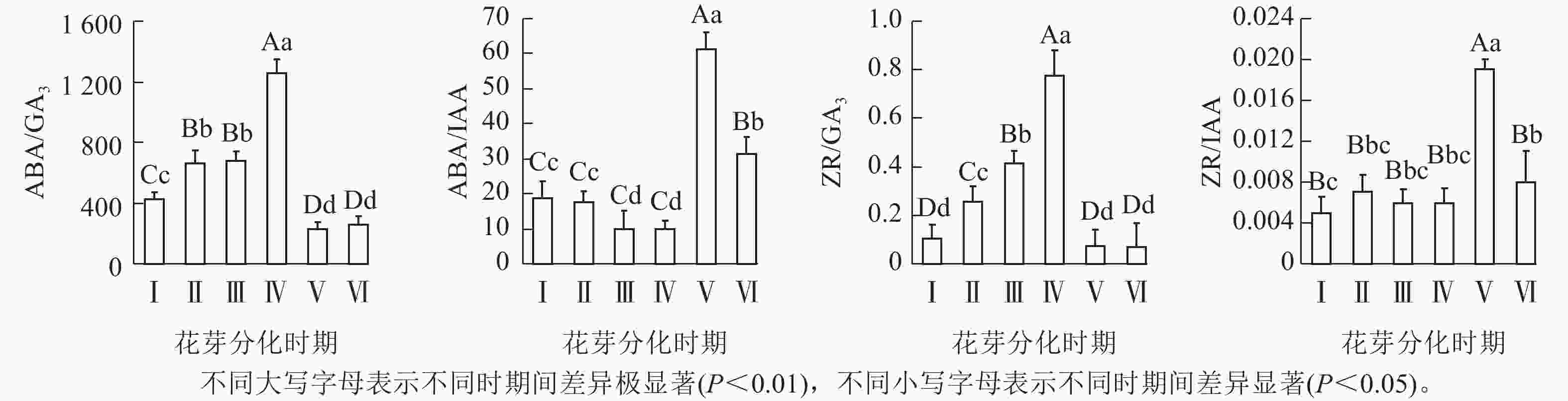
图3显示:花椒花芽形态构建过程中,不同分化时期的ABA/GA3、ABA/IAA、ZR/GA3和ZR/IAA比值分别为226.134~
1258.782 、9.809~61.088、0.069~0.777和0.005~0.019。综合地,ABA/GA3比值呈现先上升后下降的趋势,其中,从Ⅰ~Ⅳ期,ABA/GA3比值逐渐升高,Ⅳ期时达到最高,极显著高于Ⅰ、Ⅱ、Ⅲ和Ⅴ、Ⅵ期的(P<0.01),Ⅴ期时降至最低。ABA/IAA则随着花芽分化进行,Ⅰ~Ⅳ期整体呈下降趋势但差异不显著,Ⅴ期时上升并达到峰值,且极显著高于其余分化期的(P<0.01)。ZR/GA3的变化趋势与ABA/GA3比值基本一致,即Ⅲ期时达到最高且极显著高于各个分化时期的(P<0.01)。Ⅴ期的ZR/IAA极显著高于其余各期(P< 0.01),Ⅰ~Ⅳ和Ⅵ期无显著的差异。总体上,较高比值的ABA/GA3、ZR/GA3、ABA/IAA和ZR/IAA促进花芽分化;分化期内,Ⅴ期的内源激素比值变化极显著低于或高于Ⅰ~Ⅳ期的(P<0.01),说明分化启动后,ABA/IAA和ZR/IAA通过降低比值、ABA/GA3与ZR/GA3通过累积的方式促进花芽分化进行。翌年花芽分化再次启动后,ABA/GA3与ZR/GA3与上一期无显著变化,但ABA/IAA和ZR/IAA极显著低于Ⅴ期,说明较低比值的ABA/GA3与ZR/GA3有益于后期花器官结构的建成,而较高比值的ABA/GA3与ZR/GA3则可能推动前期形态与结构的同步进行。 -
花芽分化是植物从营养生长向生殖生长转变的重要环节,花芽分化的优劣直接影响果实的产量和品质[26],因此,对特定物种及其生态条件下花芽分化形态与结构特征的认知,是精准制定培育措施的科学保障。本研究将昭通冷凉山区‘小龙袍’花椒花芽分化进程分为6个时期,与常剑文等[11]对花椒花芽分化阶段的划分类似,但与竹叶花椒的研究结果有差异[11, 13]。本研究中未出现子房与花柱及雄蕊分化现象,是否与种内较为相似,种间差异较大有关,有待更多研究加以实证。多数学者认为:植物花芽分化结束后,雌蕊、雄蕊内部结构形态进一步发育成熟,属于植物花芽分化结束后的性细胞成熟阶段,并不属于花芽分化[27],即花芽分化进程的阶段划分没有统一标准,是根据植物分化过程的特征划分花芽分化的不同时期。花椒的无融合生殖特性使其花芽分化进程表现出与其他植物不同的特点:花芽分化以雌蕊发育为核心,雄蕊分化过程简化或缺失。FEI等[28]研究发现:花椒属孢子体无融合生殖,其胚珠中的珠心细胞可直接发育为不定胚,无需经过受精过程,这一生殖特性决定了花椒花芽分化过程中雌蕊发育的主导地位,而雄蕊则逐渐退化缺失。本研究中花芽分化进展不同阶段划分与已有研究的基本一致,且未发现雄蕊原基的分化,这与花椒普遍存在的无融合生殖特性相符。
与某些植物[29]短期内完成花芽分化进程不同,花椒花芽分化跨年度且延续时间极长。本研究采样地位于高海拔冷凉地区的云南昭通,花椒花芽分化始于5月下旬的下半期,翌年3月下旬完成花芽分化,跨越2个年度历时约10个月,与北方暖温带地区花椒花芽分化进程基本一致[11],但分化始期及翌年再次分化时间略早于北方。这是否与昭通气候相对较温暖有关,需进一步研究。此外,本研究结果基于春梢花芽的观测,夏梢、秋梢的花芽分化进程是否与春梢类似,也有待进一步研究。
-
植物激素是调控植物花芽分化的重要物质,ABA在花芽分化中的作用一直存在争议。普遍认为高水平ABA促进休眠,低水平ABA有利于花芽的后续分化[30]。本研究呈现高质量分数ABA抑制花椒花芽分化启动,低质量分数则促进花芽分化的趋势,这与山茶花Camellia和木棉Bombax ceiba相比差异较大[31−32],可能是物种不同导致的。GA3与花和果实发育有关[33]。有研究认为:GA3在植物的花芽分化进程中表现为高水平抑制、低水平促进的作用[34]。本研究中GA3质量分数变化趋势与ABA一致,亦与前人研究结果相一致,是否其对花芽分化具有共同的作用,有待更多物种的研究加以总结。IAA具有促进植物器官建成的功能[35]。本研究中花芽分化启动后Ⅱ~Ⅳ期IAA质量分数总体呈上升趋势,至Ⅴ期降至最低。高水平的IAA可能有利于花椒花芽分化,进而影响开花和结果,这与顶坛花椒的研究结果[21]相一致。ZR具有促进花芽分化的作用。对小叶丁香Syringa microphylla、木棉和马铃薯Solanum tuberosum的研究[15, 30, 36]发现:高水平的ZR有利于花芽分化。本研究中,花芽分化启动后,ZR质量分数变化趋势与IAA基本一致,是否ZR对植物花芽分化的影响具有共性亦需进一步研究。
大量研究表明:ABA/GA3、ABA/IAA、ZR/GA3和ZR/IAA体现了植物内源激素之间的动态变化关系[37−38]。番石榴Eugenia uniflora和罗汉果Siraitia grosvenorii的ABA/GA3、ABA/IAA、ZR/GA3和ZR/IAA升高诱导花芽分化,促进其芽体由营养生长向生殖生长转变[37−38],与本研究结果相一致。花芽分化未启动前,ABA/GA3和ABA/IAA保持较高水平,可能与花芽营养生长对其需求较高有关,对苹果Malus domestica[37]花芽分化研究得到类似的结果。本研究中花椒花芽分化启动后,Ⅱ~Ⅳ期ABA/GA3和ZR/GA3逐渐升高并呈现极显著的差异,ABA/IAA和ZR/IAA变化较为平缓略有降低但无显著的差异,可能是ABA、GA3和ZR三者之间的平衡扮演重要的调控角色。这一结果与对葡萄Vitis vinifera [20]和罗汉果[38]的研究结果相一致。尚需更多的研究揭示其成因。
-
昭通冷凉山区‘小龙袍’花椒花芽分化时间较长,可划分为具有明显区别的6个时期,即未分化期(Ⅰ期)、分化开始期(Ⅱ期)、花序轴分化期(Ⅲ期)、花蕾分化期(Ⅳ期)、萼片分化期(Ⅴ期)和雌蕊分化期(Ⅵ期)。同一时期的解剖结构与形态密切相关,不同时期呈现重叠现象。高水平ABA和GA3抑制花椒花芽分化的启动,低水平ABA和GA3及高水平的IAA和ZR有利于花椒花芽分化的启动和结构建成,以降低ABA/IAA、升高ABA/GA3与ZR/GA3方式促进花芽分化进程。生产实践中,调整性的冠幅重度修剪尽可能在花芽未分化期开展,以免严重影响开花结实和产量。在花椒花芽分化的关键时期,可通过相关培育措施(如施肥、修剪和喷施外源激素等)调控内源激素和养分,促进花芽分化,保障养分供给,实现优质丰产。
Flower bud differentiation process of Zanthoxylum bungeanum and changes in endogenous hormones
doi: 10.11833/j.issn.2095-0756.20260129
- Received Date: 2026-01-13
- Accepted Date: 2026-04-13
- Rev Recd Date: 2026-04-03
-
Key words:
- Zanthoxylum bungeanum /
- flower bud differentiation /
- morphological structure /
- endogenous hormone
Abstract:
| Citation: | LI Zhengyin, LI Lianfang, FAN Huaigang, et al. Flower bud differentiation process of Zanthoxylum bungeanum and changes in endogenous hormones[J]. Journal of Zhejiang A&F University, 2026, 43(X): 1−10 doi: 10.11833/j.issn.2095-0756.20260129 |









 DownLoad:
DownLoad: