-
黄脊竹蝗Ceracris kiangsu隶属于直翅目Orthoptera丝竹蝗科Oedipodidae竹蝗属Ceracris[1],其若虫、成虫分散或群聚取食竹叶,是取食量很大的一种森林昆虫[2],分布于湖南、四川、江西、云南、广西、浙江、广东等10个省份[3]。黄脊竹蝗的发生具有周期性,并且严重影响竹材的材质和使用价值,给林业生产带来极大的损失[4]。一直以来,人们对黄脊竹蝗的研究主要以防治为主,对其人工饲养也是为了观察其生活习性以便进行更有效的防治。蝗虫体内蛋白质和脂肪含量很高,氨基酸和维生素的种类也很多[5],含有大量人体所必需的微量元素,也可以作为饲料喂养各种畜禽[6],因此,对黄脊竹蝗这一昆虫资源的食饲用价值进行探索与开发有很大的意义。目前,国内已经有许多学者探究了不同饲料对资源昆虫的取食和生长等方面的影响。陈申芝[7]测定了东亚飞蝗Locusta migratoria manilensis对莴苣Lactuca sativa、胡萝卜Daucus carota、麦麸Triticum aestivum、黑麦草Lolium perenne、玉米Zea mays等5种不同植物叶片的取食量以及东亚飞蝗取食这5种食料后的体质量变化。封洪强等[8]探究了金色狗尾巴草Setaria glauca、狗尾草Setaria viridis、鸭跖草Commelina communis、水稻Oryza sativa等对中华稻蝗Oxya chinensis生存及生长发育的影响。张守科等[9]通过黄脊竹蝗的取食偏好试验,测定了其对竹类7个属9个种的取食差异。而关于不同食料对黄脊竹蝗的取食和生长的影响探究较少。本研究从食料和饲用昆虫的角度对黄脊竹蝗进行人工饲养,对比研究了毛竹Phyllostachys edulis、玉米以及芒草Miscanthus sinensis 等3种不同寄主植物对黄脊竹蝗的取食偏好、体质量、体长、产卵情况以及存活率的影响,初步筛选出利于黄脊竹蝗生长发育以及繁殖的寄主植物,为深入探索规模化饲养的关键技术提供理论和实践依据。
-
黄脊竹蝗卵块采自湖南省益阳市桃江县。将卵块放置于50 cm×50 cm×50 cm养虫笼中孵化,选择阳光充足的室外作为孵化环境,同时做好防暴雨和暴晒措施,待若虫孵化后供试。
-
3种寄主植物分别为玉米、毛竹和芒草。玉米在浙江农林大学森林保护研究所试验林地种植,不施农药,定期施肥除草,待幼苗长至1 m高后采集叶片供试。芒草和毛竹叶采自浙江农林大学校外东湖村,选取长势良好的幼嫩叶片以供黄脊竹蝗取食。以上寄主植物在试验前均用清水浸泡洗净。黄脊竹蝗卵块孵化出若虫后将这3种寄主植物插入锥形瓶中,用水培法维持叶片新鲜,供黄脊竹蝗取食。
-
在长60 cm×宽30 cm×高180 cm的养虫笼内饲养200头黄脊竹蝗若虫,试验前期同时投喂3种植物叶片(玉米、芒草、毛竹),并让其自由选择取食的植物。每天8:30、11:30和17:30观察并记录其发育进度,适时补充3种植物叶片。根据其发育进度选取龄期一致的60头竹蝗若虫分别进行1~5龄期的取食试验,每次取食试验准备3个长50 cm×宽50 cm×高50 cm的养虫笼,每笼供试黄脊竹蝗20头,雌雄比例、龄期、体长一致,同时放入毛竹、玉米和芒草3种寄主植物叶片各25 g。供取食的叶片取至植物尖端幼嫩部位,用水培法保鲜。每次试验前进行14 h的饥饿处理,取食时长控制为24 h。每次取食结束后用网格纸测量被取食叶片的缺刻面积。
-
准备9个长50 cm×宽50 cm×高50 cm的养虫笼,各笼饲养20头2龄竹蝗,测量每笼黄脊竹蝗的起始体质量和单头蝗虫的体长,保持每笼黄脊竹蝗雌雄比例一致。笼中放入少量新鲜的水,每笼每次放置一种寄主植物叶片25 g。供取食的叶片取至植物尖端幼嫩部位,用水培法保鲜。隔2 d更换1次食物和水,每次试验结束后清理1次养虫笼。20 d后测量每笼黄脊竹蝗的最终体质量和单头的体长。试验结束,计算不同寄主植物饲养下黄脊竹蝗体质量和体长的增长量。每种寄主植物3个重复。
-
在上述方法中饲养的虫源羽化后,从3种不同寄主植物饲喂的养虫笼中各抓取同日龄、健康无损伤成虫5对(雌雄配对,标记好不同寄主植物饲养),分别放入9个50 cm×宽50 cm×高50 cm养虫笼中,并准备同等质地的砂土供其产卵。砂土土层厚度8 cm,含水量15%,粒度40目。每天更换新鲜的寄主植物叶片,观察并记录其产卵前期及产卵量,直至成虫死亡。
-
观察上述方法中饲养的黄脊竹蝗,记录养虫笼中黄脊竹蝗从2~5龄期的存活数量和死亡数量。
-
数据处理和分析均使用Excel 2007和SPSS 16.0处理,显著性采用Duncan新复极差法进行多重比较。文中数据均为平均值±标准差。
-
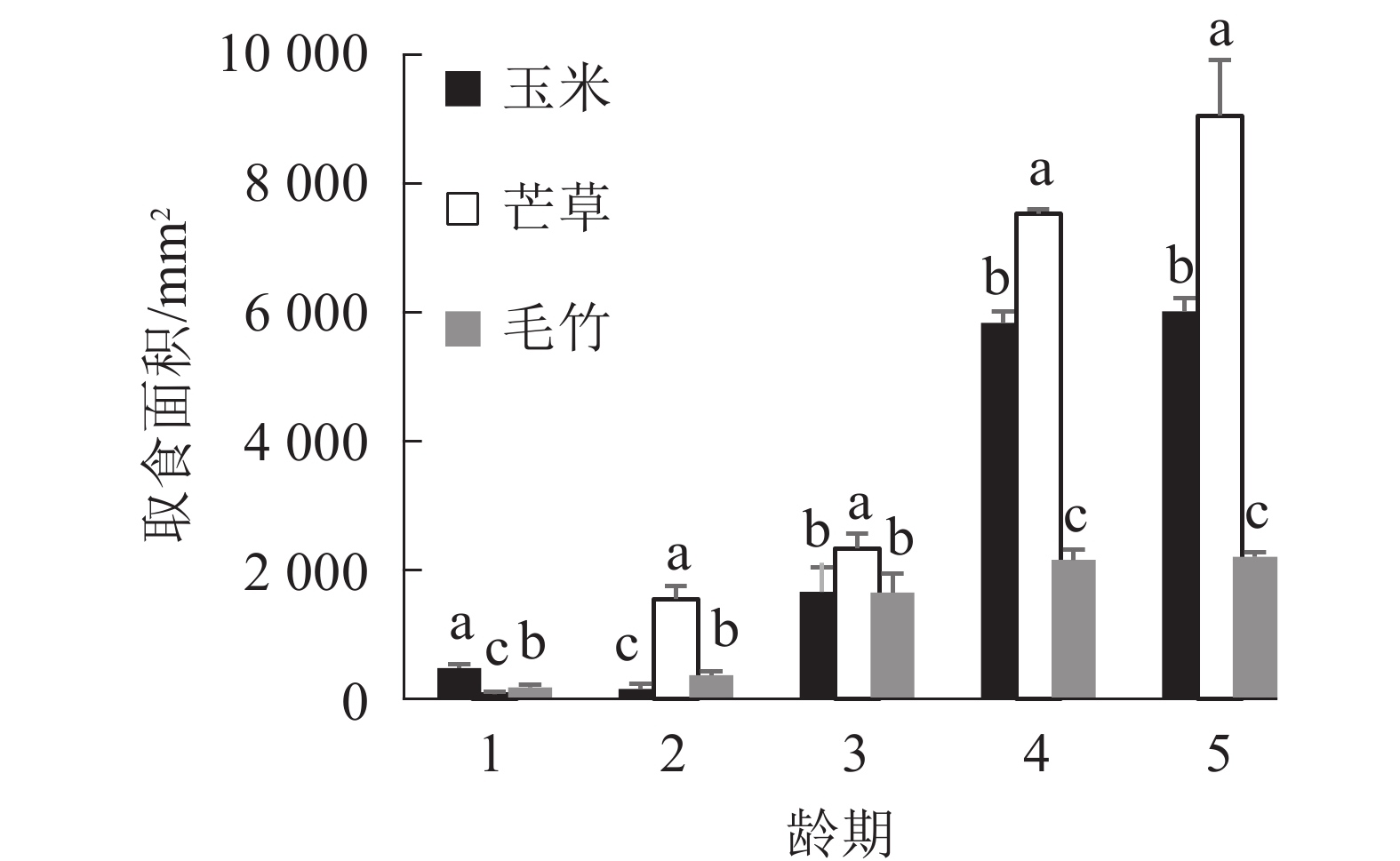
图1显示:1龄黄脊竹蝗若虫对3种不同寄主植物叶片的取食面积之间差异显著(P<0.05),对玉米叶的取食面积最大,平均为474.67 mm2;对毛竹取食面积次之,平均为179.33 mm2;对芒草取食面积最小,平均为76.00 mm2。黄脊竹蝗1龄若虫对玉米叶的取食量明显高于另外2种寄主植物,同时毛竹叶和芒草叶的取食量之间差异显著(P<0.05)。
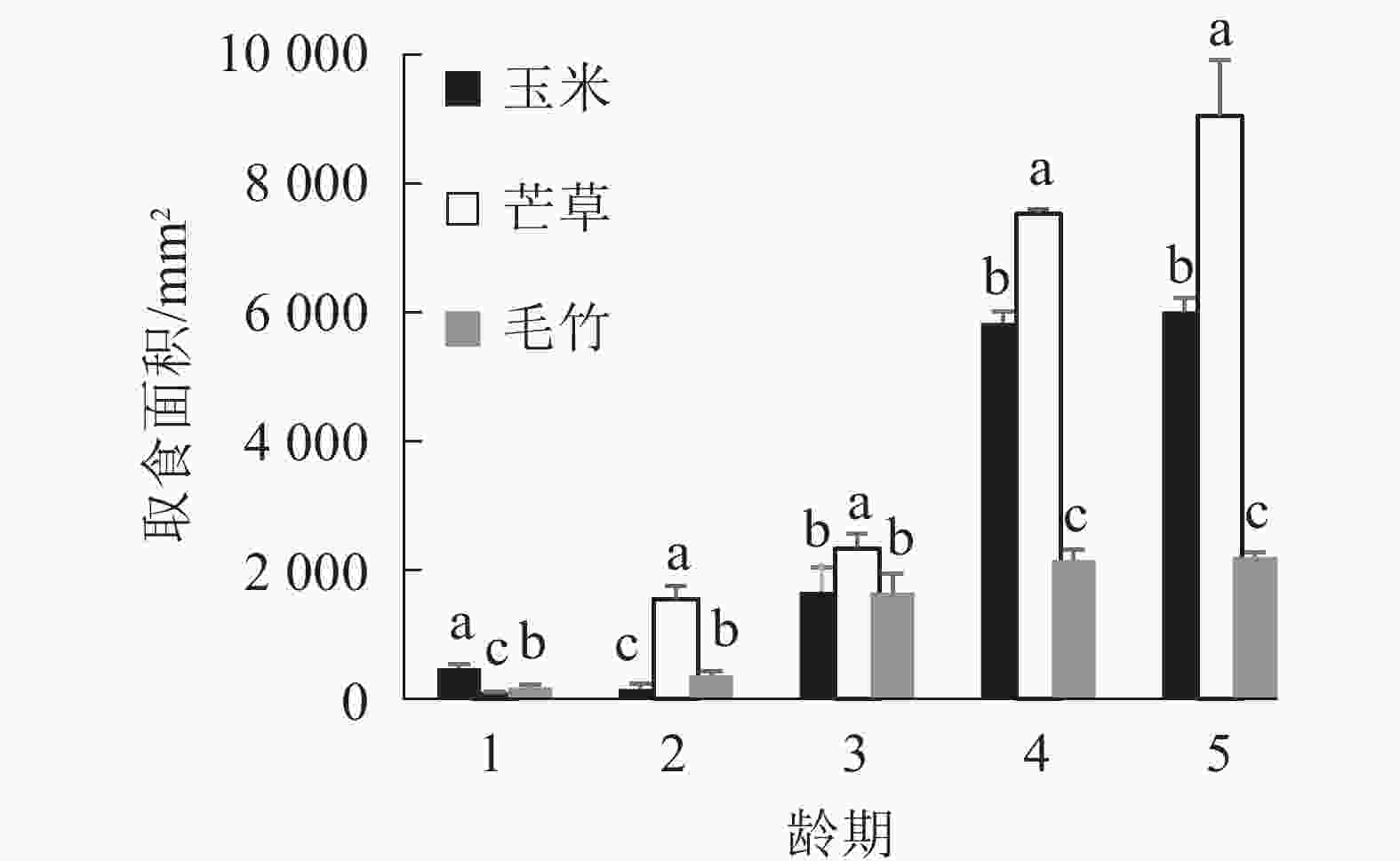
图 1 1~5龄期黄脊竹蝗若虫取食不同寄主植物叶面积比较
Figure 1. Comparison of the feeding area of different host plants by the 1st to the 5th instar C. kiangsu
2龄黄脊竹蝗若虫对3种不同寄主植物叶片的取食面积之间差异显著(P<0.05),2龄若虫取食偏好从大到小依次为芒草、毛竹、玉米,与1龄若虫相比发生了显著变化,由1龄若虫最喜欢取食的玉米变为2龄若虫最喜欢的芒草。对芒草叶取食面积最大,平均为1 556 mm2;毛竹取食面积次之,平均为372 mm2;玉米叶取食面积最小,平均为157 mm2。
3龄若虫取食面积从大到小依次为芒草、玉米、毛竹,其中芒草叶取食面积最大,平均为2 343 mm2,而玉米叶和毛竹叶取食面积平均分别为1 659和1 649 mm2,两者差异不显著(P>0.05)(图1)。4龄和5龄若虫取食面积从大到小依次为芒草、玉米、毛竹,其中芒草叶取食面积仍然最大,但是玉米叶取食面积显著高于毛竹叶(P<0.05)。综上所述,2~5龄黄脊竹蝗若虫都是最喜欢取食芒草叶,另外,2~5龄期黄脊竹蝗若虫取食玉米叶的面积逐渐上升,在2龄若虫期玉米叶取食量显著低于毛竹叶(P<0.05),但是在4龄和5龄若虫期玉米叶取食量则显著高于毛竹叶(P<0.05)。
-
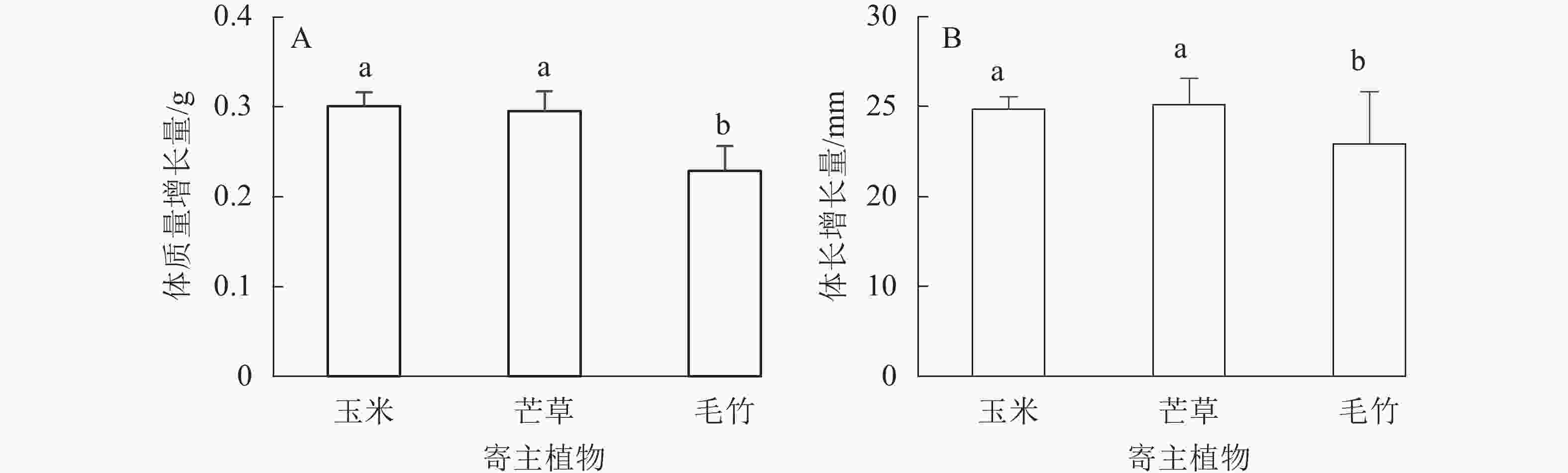
不同寄主植物饲养后,平均每头黄脊竹蝗体质量增长量从大到小依次为玉米(0.301 g±0.015 g)、芒草(0.295 g±0.022 g)、毛竹(0.229 g±0.027 g),其中玉米叶与芒草叶饲养对黄脊竹蝗体质量增长差异不显著(P>0.05),这2种寄主植物对黄脊竹蝗体质量增长量都显著高于毛竹叶(P<0.05)(图2A)。在3种单一植物饲养下,玉米和芒草对黄脊竹蝗的平均每头体长增长量差异不显著(P>0.05),而这2种寄主植物对黄脊竹蝗体长增长量显著高于毛竹叶(P<0.05)(图2B),从大到小依次为芒草(25.120 mm±0.682 mm)、玉米(24.860 mm±1.436 mm)、毛竹(22.910 mm±2.914 mm)。
-
玉米饲养的黄脊竹蝗羽化后第38天开始产卵,毛竹饲养的黄脊竹蝗第39天开始产卵,芒草饲养的黄脊竹蝗羽化后第44天开始产卵。玉米、毛竹和芒草饲养的黄脊竹蝗种群平均产卵前期分别为41.2 d±3.7 d、41.7 d±2.2 d、55.4 d±6.9 d,其中芒草饲养的种群产卵前期显著大于其他2种植物饲养的种群(P<0.05)(表1)。
表 1 黄脊竹蝗取食不同寄主植物的产卵前期
Table 1. Effect of feeding different host plants on the pre-oviposition periods of C. kiangsu
寄主植物 最短产卵
前期/d最长产卵
前期/d平均产卵
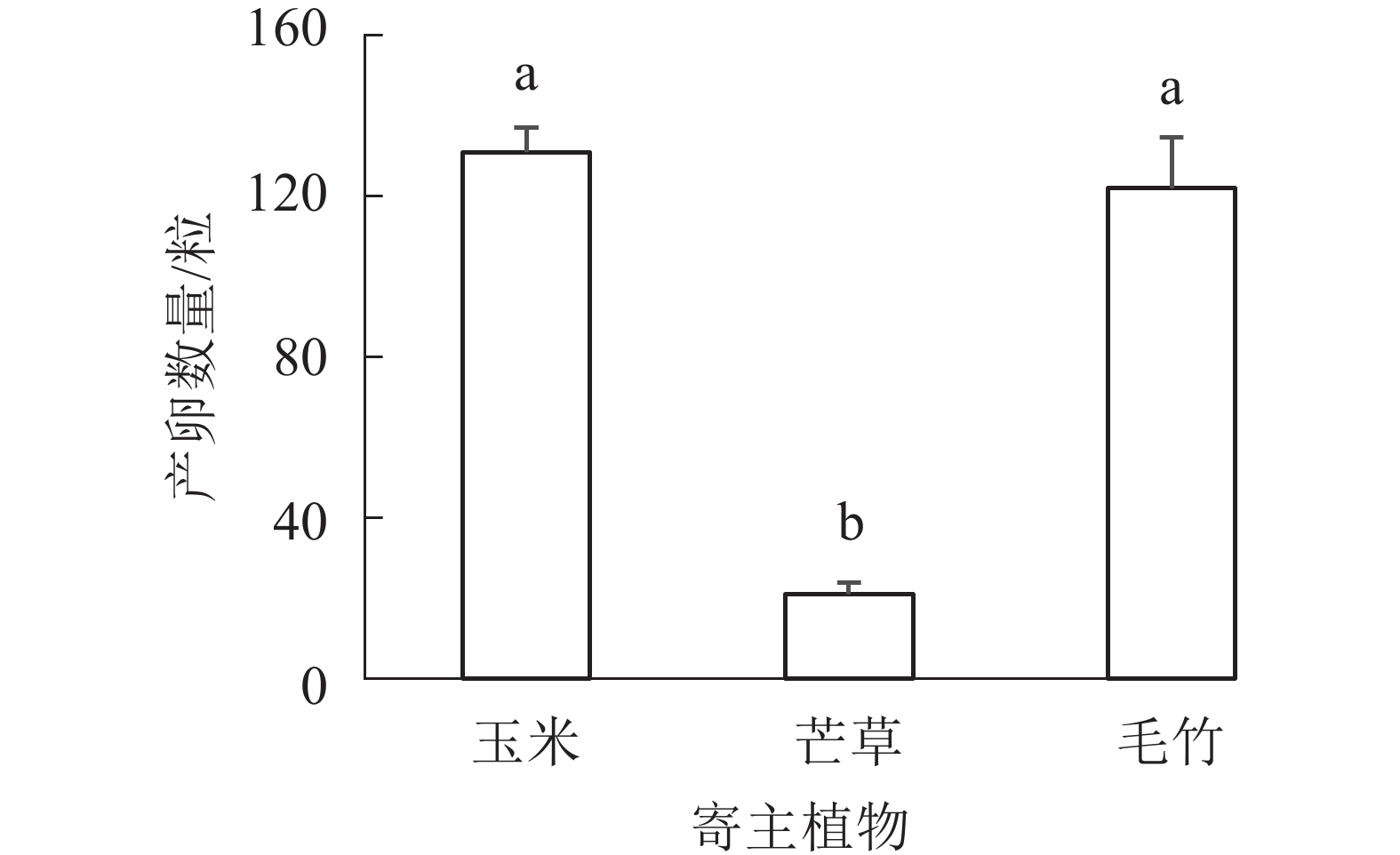
前期/dn 玉米 38 48 41.2±3.7 b 5 毛竹 39 45 41.7±2.2 b 5 芒草 44 61 55.4±6.9 a 5 说明:不同字母表示不同寄主植物间产卵前期差异显著 (P<0.05),n表示样本量(黄脊竹蝗雌雄对数) 由图3可以看出:黄脊竹蝗取食不同寄主植物后每雌虫产卵量差异显著(P<0.05),其中取食玉米和毛竹后,产卵数量相对较多,平均每笼收集到卵粒分别为131粒(玉米饲喂)和122粒(毛竹饲喂),而取食芒草收集到的卵粒最少,为21粒。玉米和毛竹饲养种群之间的产卵量差异不显著(P>0.05),前两者产卵量都显著高于芒草(P<0.05)。
-
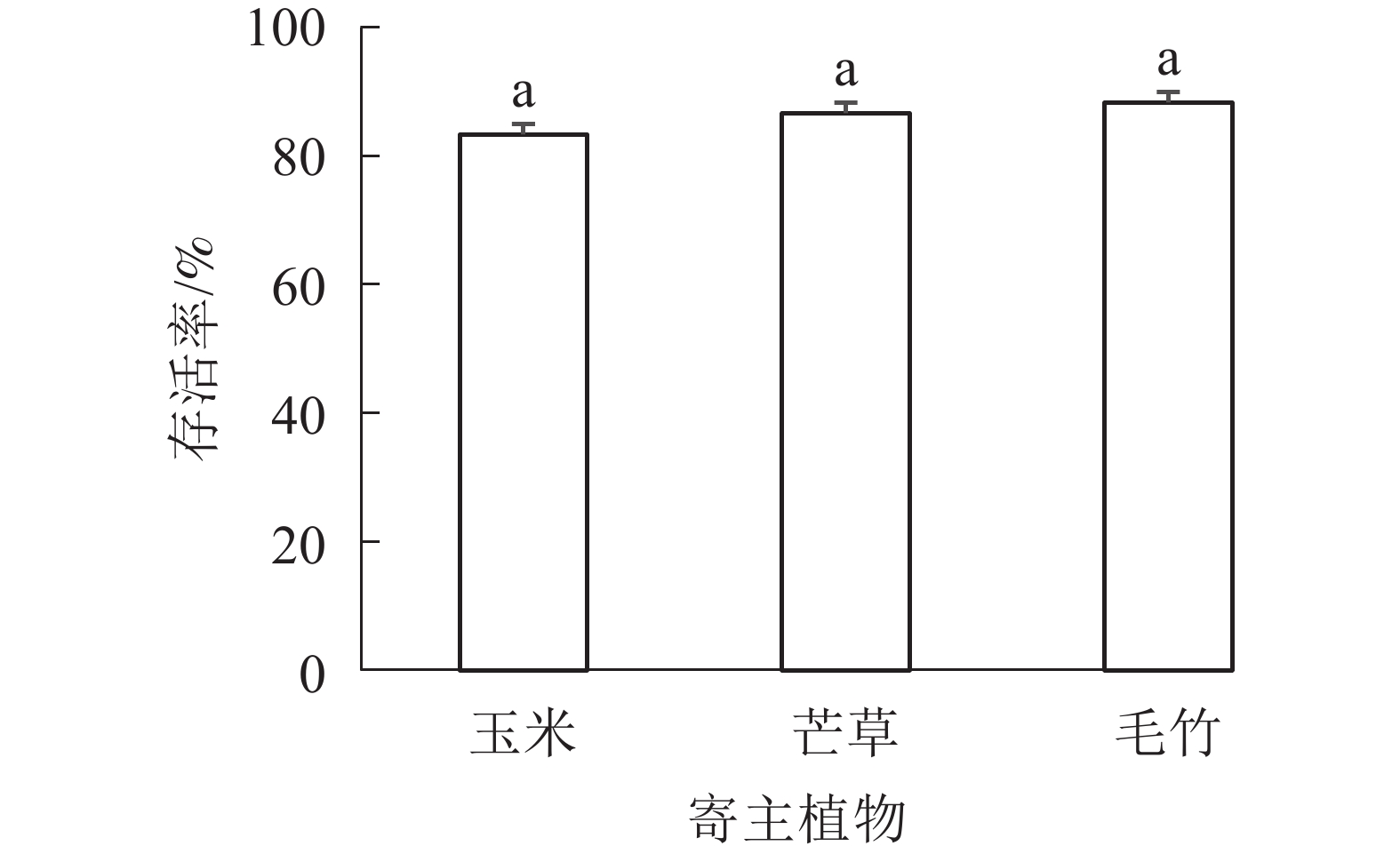
图4表明:单一寄主植物饲养蝗虫的存活率由高到低依次为毛竹(88.33%)、芒草 (86.67%)、玉米 (88.33%),但是3种寄主植物之间存活率差异不显著(P>0.05)。
-
在种间竞争、食物资源丰度及植物防御等压力条件下,植食性昆虫往往会产生不同的寄主选择机制[10-11]。尹姣等[12]、李超等[13]研究也显示:当几种不同的寄主植物同时存在时,昆虫取食行为具有一定的选择性。本研究表明:黄脊竹蝗1龄若虫的平均取食面积从大到小依次为玉米、毛竹、芒草,而2~5龄若虫对芒草的取食面积都显著大于其他2种寄主植物(P<0.05)。黄脊竹蝗在不同龄期的取食偏好性不同,有可能是种间竞争及食物资源丰度等压力条件的影响,也可能是由于昆虫在生长过程中,取食器与消化系统发育状况不同,导致对食物的偏好随之发生改变[14]。
不同寄主植物由于所含次生物质以及营养成分不同,对多食性昆虫的选择行为和生长发育及繁殖均有不同程度的影响[15]。昆虫若虫期的食物营养对其生长发育及繁殖有很大影响,即使在相同的环境条件下,食物的营养不同,昆虫若虫期的生长发育及成虫期的繁殖也会表现出一定的差异性,致使昆虫种群的增长受到影响[16-17]。本研究也显示:供试寄主植物的不同对黄脊竹蝗的生长发育和繁殖力产生的影响存在差异。如芒草与玉米饲喂的黄脊竹蝗平均体质量和体长增长量差异不显著(P>0.05),但与毛竹饲喂的黄脊竹蝗体质量和体长增长量差异显著(P<0.05);在不同寄主植物饲养下,成虫产卵前期存在明显差异(P<0.05),芒草饲养的种群产卵前期显著大于其他2种植物饲养的种群(P<0.05);此外,黄脊竹蝗取食不同寄主植物后每雌虫产卵量同样差异显著(P<0.05)。说明芒草饲喂有利于黄脊竹蝗体质量和体长的增长,却使黄脊竹蝗产卵前期延长,并且产卵量极少,造成此现象的原因可能是芒草叶中含有某种抑制黄脊竹蝗生殖系统发育的物质或芒草叶的营养成分不能满足其发育及生殖的需求。而玉米叶和毛竹叶可能含有的营养物质对黄脊竹蝗生殖系统发育有促进作用,使其产卵数量多,产卵前期相对较短。
综上所述,在3种寄主植物资源丰富、外部环境条件也相同的情况下,黄脊竹蝗取食玉米后的体质量增长量略高于芒草饲养的种群,显著高于毛竹饲养种群,且其产卵量显著高于芒草饲养种群。可以初步推测:玉米是相对适宜黄脊竹蝗的取食和生长发育及产卵需求的寄主植物。另外,从寄主植物获取的难易程度来考虑,玉米可以大量种植,且种植成本低,生长周期较短,种植技术成熟,成活率高,而芒草为户外野生禾本科Gramineae植物,不易大批量获取。可见,相对于其他2种寄主植物,玉米是相对适合黄脊竹蝗人工饲养的食物来源。
Effects of three different host plants on the feeding preference and developmental status of Ceracris kiangsu
-
摘要:
目的 研究黄脊竹蝗Ceracris kiangsu在3种不同寄主植物上的取食偏好和发育状况,有助于了解它们与寄主植物的关系。 方法 采用网格坐标纸计算面积法,测定不同龄期黄脊竹蝗对玉米Zea mays、芒草Miscanthus sinensis和毛竹Phyllostachys edulis 等3种寄主植物的取食选择性,并观察3种不同寄主植物对黄脊竹蝗体质量、体长、产卵前期、产卵量和存活率的影响。 结果 不同龄期黄脊竹蝗对寄主植物取食偏好性发生了改变,其中1龄若虫的平均取食面积从大到小依次为玉米(474.67 mm2±66.03 mm2)、毛竹(179.33 mm2±41.38 mm2)、芒草(76.00 mm2±42.11 mm2),而2~5龄若虫对芒草的取食面积都显著大于其他2种寄主植物(P<0.05)。不同寄主植物饲喂后,黄脊竹蝗平均体质量增长量从大到小依次为玉米(0.301 g±0.015 g)、芒草(0.295 g±0.022 g)、毛竹(0.229 g±0.027 g);黄脊竹蝗平均体长增长量从大到小依次为芒草(25.120 mm±0.682 mm)、玉米(24.860 mm±1.436 mm)、毛竹(22.910 mm±2.914 mm)。在不同寄主植物饲养下,成虫产卵前期存在显著差异(P<0.05),平均产卵前期从大到小依次为芒草(55.4 d±6.9 d)、毛竹(41.7 d±2.2 d)、玉米(41.2 d±3.7 d),其中芒草饲养的种群产卵前期显著大于其他2种植物饲养的种群;黄脊竹蝗取食不同寄主植物后雌虫产卵量差异显著(P<0.05),从大到小依次为毛竹(122.00粒±6.08粒)、玉米(121.00粒±12.70粒)、芒草(21.00粒±2.89粒);单一寄主植物饲养黄脊竹蝗的存活率影响差异不显著(P>0.05),存活率由高到低依次为毛竹(88.33%±1.70%)、芒草(86.67%±1.66%)、玉米(83.33%±1.60%)。 结论 从寄主植物获取的难易程度以及对黄脊竹蝗体质量、体长增长量和繁殖能力来考虑,玉米叶可以大量种植,芒草为户外野生禾本科Gramineae植物,不易大批量获取。相对来说,玉米叶是最适合黄脊竹蝗人工饲养的食物来源。图4表1参17 Abstract:Objective To further the relationship of Ceracris kiangsu with their host plants, an investigation was conducted of its feeding preferences and developmental status when living on three different host plants. Method The grid area calculation method was employed to determine the feeding selectivity of bamboo locust of different ages and observation was made of the effects of three different host plants on the body weight, body length, pre-laying period, spawning volume and survival rate of C. kiangsu. Result The feeding preference of host plants of C. kiangsu changes as its age accumulates; the average feeding area of first-instar nymphs was Zea mays (474.67 mm2±66.03 mm2)>Phyllostachys edulis (179.33 mm2±41.38 mm2)>Miscanthus sinensis (76.00 mm2±42.11 mm2) while the feeding area of the nymphs from the second to the fifth instar on M. sinensis was significantly larger than that on the other two host plants(P<0.05). The weight growth of different host plants was Z. mays (0.301 g±0.015 g)>M. sinensis (0.295 g±0.022 g)>Ph. edulis(0.229 g±0.027 g) whereas the length growth of different host plants was M. sinensis (25.120 mm±0.682 mm)>Z. mays (24.860 mm±1.436 mm)>Ph. edulis (22.910 mm±2.914 mm). When breeding on different host plants, C. kiangsu demonstrates significant differences in the pre-spawing period of the adults(P<0.05) and the average pre-spawning period of the three populations was M. sinensis (55.4 d± 6.9 d)>Ph. edulis (41.7 d±2.2 d)>Z. mays (41.2 d±3.7 d), and the pre-spawning period of the population feeding on M. sinensis was significantly longer than that of those feeding on the other two plants(P<0.05). The population of spawn per female was significantly different after feeding on different host plants, and the result was Ph. edulis (122.00 seeds±6.08 seeds)>Z. mays (121.00 seeds±12.70 seeds)>M. sinensis (21.00 seeds±2.89 seeds), yet there was no significant difference in the survival rate of C. kiangsu feeding on different host plants(P>0.05) with the survival rates as follows: Ph. edulis(88.33%±1.70%)>M. sinensis (86.67%±1.66%)>Z. mays (83.33%±1.60%). Conclusion With the difficulty of obtaining the host plants and the weight growth, body length calculation and reproductive capacity of C. kiangsu taken into consideration, corn leaves, compared with other two host plants which are not easy to obtain in large quantities, can be planted in large quantities, thus making the most suitable food source for artificial breeding of C. kiangsu. [Ch, 4 fig. 1 tab. 17 ref.] -
表 1 黄脊竹蝗取食不同寄主植物的产卵前期
Table 1. Effect of feeding different host plants on the pre-oviposition periods of C. kiangsu
寄主植物 最短产卵
前期/d最长产卵
前期/d平均产卵
前期/dn 玉米 38 48 41.2±3.7 b 5 毛竹 39 45 41.7±2.2 b 5 芒草 44 61 55.4±6.9 a 5 说明:不同字母表示不同寄主植物间产卵前期差异显著 (P<0.05),n表示样本量(黄脊竹蝗雌雄对数) -
[1] 张威, 张守科, 舒金平, 等. 环境温湿度对黄脊竹蝗趋尿行为的影响[J]. 浙江农林大学学报, 2017, 34(4): 704 − 710. ZHANG Wei, ZHANG Shouke, SHU Jinping, et al. Ambient temperature and humidity along with urine-pudding for Ceracris kiangsu, the yellow-spined bamboo locust [J]. J Zhejiang A&F Univ, 2017, 34(4): 704 − 710. [2] 徐天森, 王浩杰. 中国竹子主要害虫[M]. 北京: 中国林业出版社, 2004: 45 − 51. [3] 陈良昌, 黄向东, 廖运先, 等. 黄脊竹蝗生活习性观察和防治试验[J]. 湖南林业科技, 2013, 40(6): 37 − 40. CHEN Liangchang, HUANG Xiangdong, LIAO Yunxian, et al. Life habit and control of Ceracris kiangsu Tsai [J]. J Hunan For Sci Technol, 2013, 40(6): 37 − 40. [4] 程佳, 潘涌智, 舒金平. 黄脊竹蝗研究现状及进展[J]. 山东林业科技, 2010, 40(2): 116 − 119. CHENG Jia, PAN Yongzhi, SHU Jinping. The research and development of the Ceracris kiangsu Tsai [J]. J Shandong For Sci Technol, 2010, 40(2): 116 − 119. [5] 孙涛, 刘志云, 秦丽萍. 祁连山区几种草地蝗虫蛋白质营养评价[J]. 应用昆虫学报, 2011, 48(4): 902 − 908. SUN Tao, LIU Zhiyun, QIN Liping. Protein nutrition evaluation of rangeland grasshoppers in the Qilian Mountain [J]. Chin J Appl Entomol, 2011, 48(4): 902 − 908. [6] 徐燕. 亚洲飞蝗食药用价值的初步研究[D]. 长春: 东北师范大学, 2013. XU Yan. Preliminary Studies on the Dietary and Medicinal Values of Locusta migratoria[D]. Changchun: Northeast Normal University, 2013. [7] 陈申芝. 不同饲料对东亚飞蝗生长发育的影响及东亚飞蝗肠道细菌的初步鉴定[D]. 泰安: 山东农业大学, 2008. CHEN Shenzhi. Effect to Growth and Development of Locusta migratoria manilensis (Meyen) Reared on Different Kinds of Diets and Preliminary Identification of Intestinal Bacterium of Locusta migratoria manilensis (Meyen)[D]. Tai’an: Shandong Agricultural University, 2008. [8] 封洪强, 丁秀云, 王小奇, 等. 中华稻蝗人工饲养技术初探[J]. 沈阳农业大学学报, 2001, 32(5): 349 − 352. FENG Hongqiang, DING Xiuyun, WANG Xiaoqi, et al. Preliminary studies on artificial rearing technique of Chinese rice Grasshopper Oxya chinensis (Thunberg) [J]. J Shenyang Agric Univ, 2001, 32(5): 349 − 352. [9] 张守科, 张威, 舒金平, 等. 黄脊竹蝗取食偏好与竹叶品质的关系[J]. 生态学杂志, 2017, 36(8): 2266 − 2273. ZHANG Shouke, ZHANG Wei, SHU Jinping, et al. Relationship between the feeding preference of yellow-spined bamboo locust, Ceracris kiangsu and bamboo leaf quality [J]. Chin J Ecol, 2017, 36(8): 2266 − 2273. [10] 钦俊德, 王琛柱. 论昆虫与植物的相互作用和进化的关系[J]. 昆虫学报, 2001, 44(3): 360 − 365. QIN Junde, WANG Chenzhu. The relation of interaction between insects and plants to evolution [J]. Acta Entomol Sin, 2001, 44(3): 360 − 365. [11] RAZMJOU J, NASERI B, HEMATI S A. Comparative performance of the cotton bollworm, Helicoverpa armigera (Hübner) (Lepidoptera: Noctuidae) on various host plants [J]. J Pest Sci, 2014, 87(1): 29 − 37. [12] 尹姣. 草地螟的寄主植物选择对其种群增长的影响[D]. 北京: 中国农业科学院, 2001. YIN Jiao. The Population Growth of Meadow Moth, Loxostege sticticalis, as Affected by Host Plant Preference[D]. Beijing: Chinese Academy of Agricultural Sciences, 2001. [13] 李超, 程登发, 郭文超, 等. 不同寄主植物对马铃薯甲虫的引诱作用[J]. 生态学报, 2013, 33(8): 2410 − 2415. LI Chao, CHENG Dengfa, GUO Wenchao, et al. Attraction effect of different host-plant to Colorado potato beetle Leptinotarsa decemlineata [J]. Acta Ecol Sin, 2013, 33(8): 2410 − 2415. [14] 陈申芝, 卿玉弢, 朱晓英, 等. 普通齿蛉幼虫的消化系统结构和取食分析[J]. 应用昆虫学报, 2011, 48(4): 1033 − 1037. CHEN Shenzhi, QING Yutao, ZHU Xiaoying, et al. The structure of alimentary system and feeding analysis of the larva of Neoneuromus ignobilis [J]. Chin J Appl Entomol, 2011, 48(4): 1033 − 1037. [15] BERNYS E A. Relationship between deterrence and toxicity of plant secondary compounds for the alfalfa weevil Hypera brunneipennis [J]. J Chem Ecol, 1991, 17(12): 2519 − 2526. [16] 阮永明, 吴坤君. 不同食料植物对棉铃虫生长发育和繁殖的影响[J]. 昆虫学报, 2001, 44(2): 205 − 212. RUAN Yongming, WU Kunjun. Performances of the cotton bolloworm, Helicoverpa armigera on different food plants [J]. Acta Ecol Sin, 2001, 44(2): 205 − 212. [17] 武海卫, 康智, 信善林, 等. 不同食料植物对美国白蛾生长发育和繁殖的影响[J]. 应用昆虫学报, 2012, 49(4): 963 − 968. WU Haiwei, KANG Zhi, XIN Shanlin, et al. Effects of different food plants on the growth, development and reproduction of fall webworm, Hyphantria cunea, larvae [J]. Chin J Appl Entomol, 2012, 49(4): 963 − 968. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20190723






 下载:
下载: