-
桂花Osmanthus fragrans是中国十大传统名花之一,因独特芳香和优美树型而广受喜爱,在园林绿化和食品添加等领域中应用广泛[1−3]。近年来,在桂花成花[4]、花开放[5]、花香释放[6]、花色呈现[7]等方面分子机制研究已取得了一定进展,但未见稳定的组织原位杂交技术体系的成熟应用。原位杂交技术对于准确解析基因的空间表达位置及其在发育过程中的功能具有重要作用。
原位杂交(in situ hybridization,ISH)技术通过标记的探针与靶序列之间的特异性核酸杂交配对,实现对组织中目标核酸精确定位,从而在细胞甚至亚细胞水平下揭示基因的时空表达特征。原位杂交具有定位精度高、空间分辨率强等优点,已广泛应用于植物营养器官[8−9]和生殖器官的发育[10−11]、自交不亲和性[12]、胚胎发生[13]及种子和果实发育[14−15]等研究领域,在基因功能解析中发挥着重要的作用,至今仍是基因表达定位分析的理想技术手段之一[16−18]。目前,原位杂交技术已在多种植物中成功应用,如欧洲葡萄Vitis vinifera[19]、番茄Solanum lycopersicum[20]、毛果杨Populus trichocarpa[21]、黄瓜Cucumis sativus[22]等。为明确不同桂花品种花芽发育过程中的表达特征,本研究对原位杂交流程进行了系统优化,以建立适用于桂花组织稳定检测方法,并以OfPIF4、OfPIF5、OfUFO、OfYAB2和OfAUX5基因为例,对优化后的技术体系在不同桂花品种中进行验证,以评估其可靠性和适用性,为后续开展桂花特异性表达基因的空间定位及功能研究提供技术支撑。
-
选用桂花品种‘堰虹桂’‘Yanhonggui'和‘四季桂’‘Sijigui’不同发育时期的花芽和叶芽,栽培于浙江农林大学平山基地种质资源圃。所使用的全部仪器设备用过氧化氢进行酶灭活处理,离心管和枪头等耗材均需无核糖核酸酶(RNase)和脱氧核糖核酸酶(DNase)污染,避免RNA降解。实验用水为经焦碳酸二乙酯(DEPC)处理并高温高压灭菌的无RNase水。
-
①设计探针。为保证检测基因的特异性,选取mRNA的特异性区域,长度为200~500 bp。在正向引物5'端添加SP6的核心序列(GATTTAGGTGACACTATAGaatGCT),在反向引物的5'端添加T7的核心序列(tgTAATACGACTCACTATAGGG)。分别以‘堰虹桂’和‘四季桂’花芽的cDNA为模板,利用PCR仪进行扩增,表1为扩增所用序列。②体外转录。取2 μg DNA 加入200 μL PCR管中,然后依次加入10×转录缓冲液(transcriptionbuffer),10×NTPlabeling Mix,RNase抑制剂(RNase inhibitor),RNA聚合酶(RNApolymerase)和适量的无RNase水,使得总体积为20 μL,吸打混匀后放于PCR仪中37 ℃ 2 h进行转录。③探针纯化 取20 μL的反转录产物,PCR管中加入75 μL双蒸水(ddH2O),100 g·L−1tRNA(1 μL),RNase-free DNase(1 μL)放于PCR仪中37 ℃温浴10 mim。加入等体积 4 mol·L−1醋酸铵(97 μL),2倍体积乙醇(194 μL),于−20 ℃冰箱放置30 min,4 ℃ 14 000 r·min−1离心5 min,倒掉上清液,加入600 μL 70%(体积分数)乙醇清洗。4 ℃离心后留沉淀吹干。④水解、中和。在沉淀中加入100 μL的无RNase水和100 μL 2×碳酸盐缓冲液,置于60 ℃金属浴中进行水解反应。加入10 μL 10%(体积分数)冰醋酸,0.1 倍体积的3 mol·L−1 醋酸钠(pH 5.2),2倍体积的无水乙醇于−20 ℃放置至少3 h或者过夜。4 ℃ 14 000 r·min−1,离心5 min,倒掉上清液,加入600 μL 70%(体积分数)乙醇清洗2次,4 ℃离心后留沉淀风干。最后在沉淀中加入20 μL的无RNase水混匀后测浓度,然后再加入20 μL甲酰胺于−20 ℃冰箱保存。
表 1 扩增引物序列
Table 1. Amplification primer sequence
基因 正向引物序列 (5’→3’) 反向引物序列(3’→5’) OfIAA14 ATGGAAGTTGGCCAGAA AATGCGGCCTTCTCAG OfPIF4 CTCCTTCTCCTCTCCGACA AGCATCAGAACTCGGGAC OfPIF5 CCAATTCCTGGTTGGAGTATTGAG TTGATCCTGTCCCTCCGTT OfUFO AGTTCAAGAAAGTCATCGGAA TCTCCCCTACAAAATGTCGAA OfYAB2
OfAUX5CAATCGTGCAAATAAGACACT
ATGGAATCCTCGGACAAGGTTTTCACACTTTACTCCGACCAG
TGCCCAATAATCCATAGAA -
①取材与固定。取不同时期的花芽样品,置于预冷的福尔马林-乙酸-乙醇(FAA)固定液中。为筛选固定液充分渗入样品组织的最佳条件,设置2种真空抽气时间处理,分别为抽真空30 min(1次)和30 min(2次),真空压强为0.08 MPa。抽真空结束缓慢放气后,更换新鲜FAA 固定液,并置于4 ℃摇床上振荡固定过夜。②脱水。将固定后的样品按乙醇梯度进行脱水处理,每个梯度处理90 min。脱水梯度(体积分数)依次为:50%、70%、85%、95%、100%;随后更换新鲜100%乙醇,并于4 ℃条件下置于摇床中振荡脱水过夜。③透明。在室温条件下将样品置于摇床中处理,依次更换新鲜100%乙醇2 h,随后转入乙醇与二甲苯体积比为1∶1 的混合液中处理1 h,再置于100%二甲苯中透明处理3 次(每次 1 h)。透明结束后,更换新鲜100%二甲苯,并加入约1/4 体积的固体石蜡,在室温条件下静置渗蜡过夜。④浸蜡。将样品在60 ℃烘箱中渗蜡过夜。随后连续处理4~7 d更换新鲜纯液体石蜡,每日更换2 次(早晚各1次),以保证石蜡充分渗入组织。⑤包埋与切片。将熔融的液体石蜡倒入包埋模具内,待石蜡完全凝固后,将石蜡块置于4 ℃冰箱中保存备用。用切片机(Leica)切取厚度为10 μm,同时需在显微镜(ZEISS)下观察组织结构完整性。切片置于无RNase水中展平后贴附于载玻片上,吸去多余水分,并于42 ℃烤片机中烘烤过夜备用。
-
①脱蜡复水。将玻片依次置于二甲苯中脱蜡2 次(每次 10 min),随后经乙醇梯度(体积分数)复水处理:100%乙醇1 min,95%乙醇30 s,85%乙醇30 s,70%乙醇30 s,50%乙醇30 s,30%乙醇30 s,随后置于质量分数为0.85% 氯化钠溶液中2 min,最后转入磷酸盐缓冲溶液(PBS)中平衡2 min。②蛋白酶K溶液消化。将玻片置于37 ℃条件下用蛋白酶K溶液处理,以消化组织内部蛋白质并提高探针对细胞RNA的可及性。为优化消化条件,分别设置10、15、20、25和30 min不同消化时间梯度。消化结束后,立即用体积分数为0.2%的甘氨酸PBS溶液处理2 min以中和蛋白酶活性并终止反应,随后用PBS清洗2 min。③交联。体积分数为4%的甲醛PBS溶液,10 min,在摇床上进行。随后PBS清洗,2 min。④乙酸酐封闭。置于乙酸酐溶液(pH 8),在摇床上振荡10 min,随后用PBS清洗2 min。⑤脱水。玻片依次置于质量分数为0.85%的氯化钠溶液中处理2 min,随后经乙醇梯度(体积分数)再次脱水:30%、50%、70%、85%、95%,各处理30 s;随后置于100%乙醇中处理2 次(每次1 min)。脱水完成后,待乙醇完全挥发后即可进行后续杂交实验。⑥预杂交。设置预杂交与不预杂交处理进行对比,每张玻片用量为150 μL的杂交液(无探针)。将杂交液涂布于玻片上,密封在保湿盒中,放入烘箱孵育1.5 h。⑦杂交。将探针稀释后,于80 ℃金属浴中变性2 min。每张载玻片加入约150 μL含探针的杂交液,探针与杂交液体积比为1∶4。将混合后的探针杂交液均匀滴加于载玻片上,分别在50和55 ℃条件下进行杂交,杂交时间分别设置为15和20 h。
-
①洗涤去杂交液。取出杂交后的玻片。在55 ℃的0.2×SSC溶液中洗去残留杂交液:0.2×SSC,2 次,每次1 h;37 ℃ 1×NTE,2 次,每次5 min。②RNase处理。置于37 ℃含20 μg·mL−1 RNase A的NTE中处理30 min,以去除非特异性RNA。随后再次置于37 ℃ 1×NTE洗涤2 次,每次5 min。随后在55 ℃ 0.2×SSC中洗涤1 h。③封闭与抗体孵育。在TBS中平衡玻片5 min,随后在罗氏封闭液中于摇床上封闭45 min,再于TBST溶液中摇床处理45 min。将含1∶1 250稀释抗体的TBST 溶液涂于玻片上,在避光、湿润条件下室温孵育2 h。随后用TBST洗涤玻片4 次,每次15 min。④显色。玻片平衡于Buffer C缓冲液中5 min,随后用NBT/BCIP显色液覆盖组织,避光显色1~3 d。
-
当显色达到预期效果后,进行乙醇梯度(体积分数)脱水以去除浮色:10%乙醇10 s,30%乙醇10 s,50%乙醇10 s,70%乙醇5 s,80%乙醇5 s,95%乙醇5 s,100%乙醇5 s,最后置于二甲苯中2 min。脱水后用中性树脂封片以终止显色反应,切片在显微镜(Olympus)下观察并拍照记录。
-
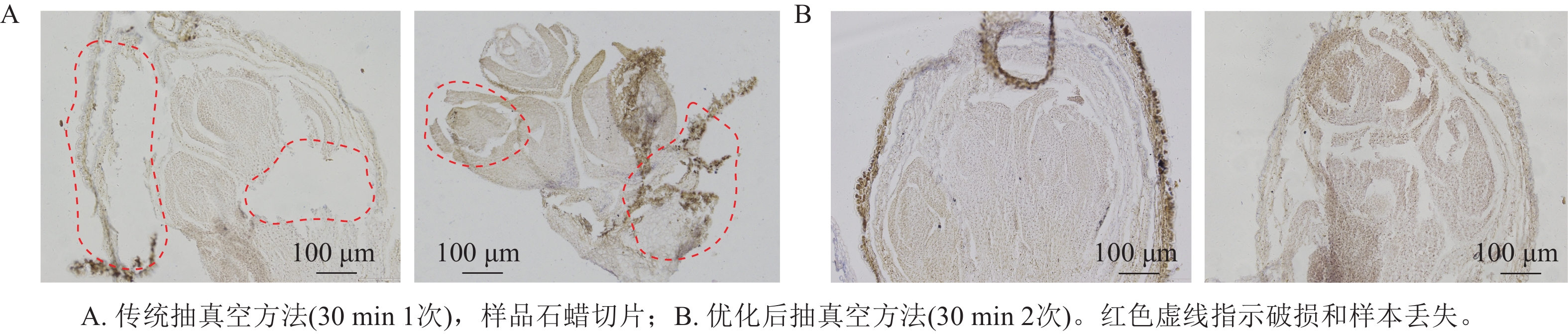
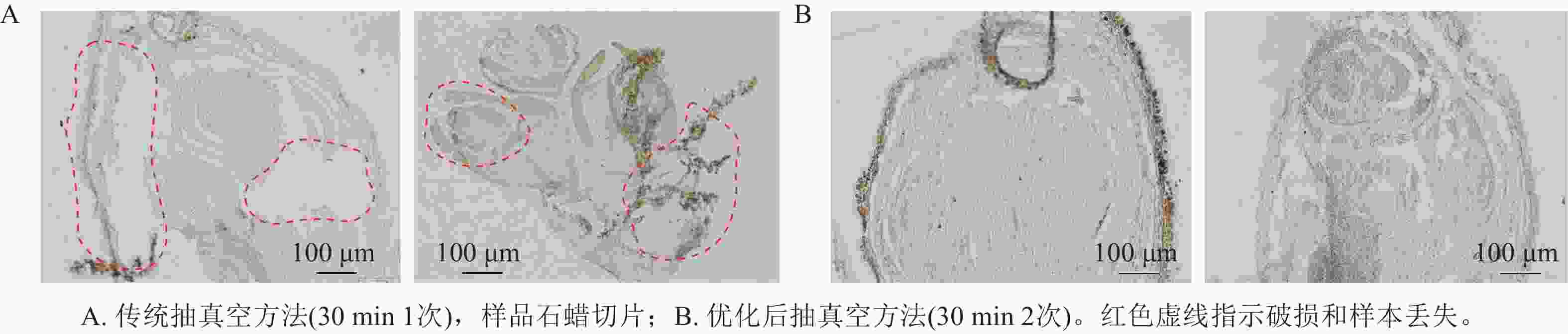
采用2种抽真空时间进行优化,结果表明:采用单次抽真空处理的样品,由于固定液未能充分渗透至组织内部,导致后续浸蜡不完全,切片过程中样品出现明显断裂和破损,切片质量较差(图1A)。相比之下,2次抽真空处理的样品,固定液能够充分渗透至组织内部,浸蜡过程更加充分,切片时组织结构完整,内部结构清晰可见,样品整体完整性明显提高(图1B),从而有效提升了制片质量和效率。
-
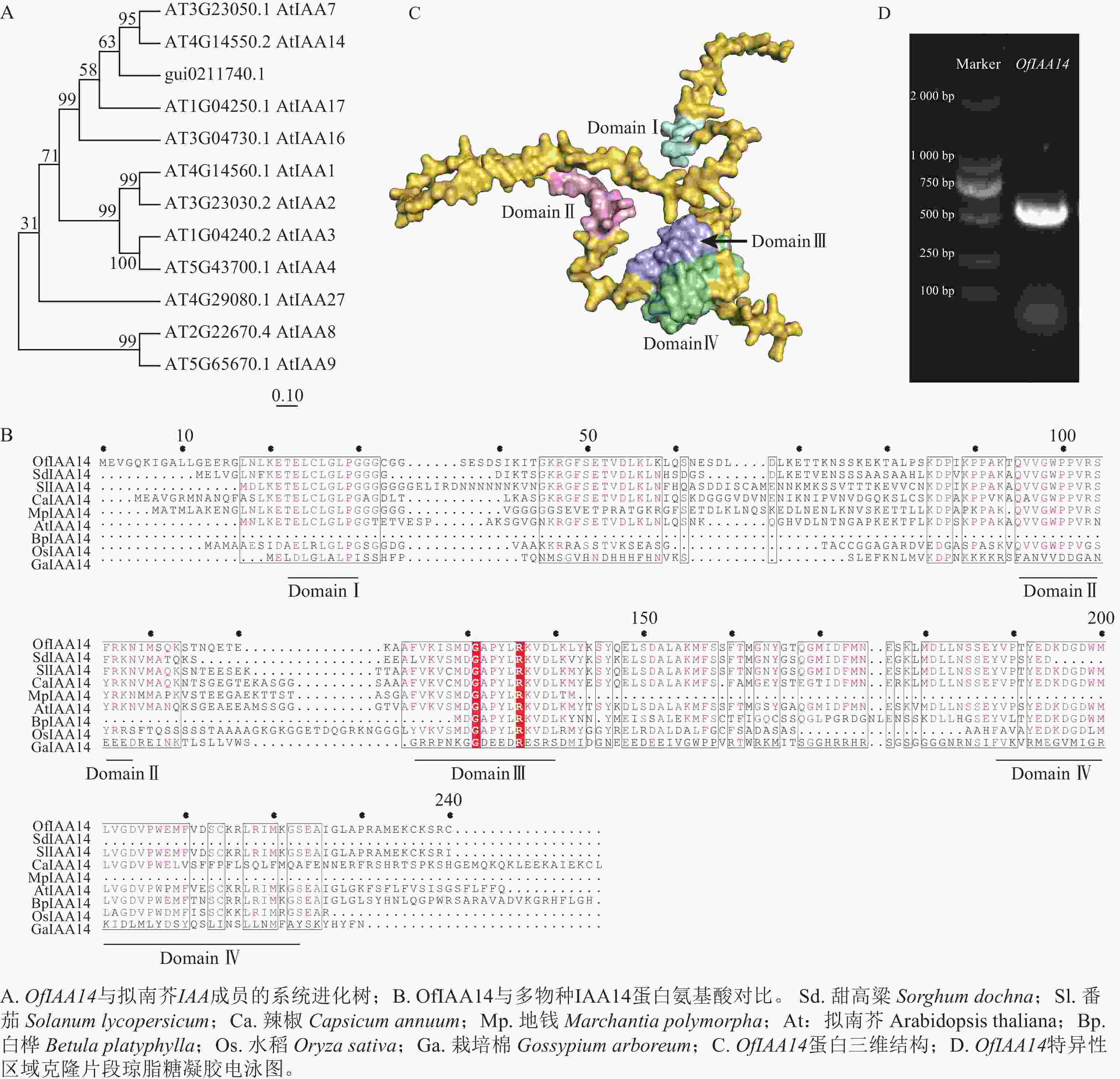
在转录组数据中筛选获得候选基因,利用美国国家生物技术信息中心(NCBI )数据库进行蛋白序列比对及系统进化分析。结果表明:该基因与拟南芥同源基因AtIAA14 聚为一支,具有较高的序列保守性,表示该基因在功能上可能具有一定的保守性,因此命名为OfIAA14(图2A)。进一步对多个物种IAA14 蛋白的氨基酸序列进行比对分析,结果显示:OfIAA14 蛋白包含典型的保守结构域Domain Ⅰ、Domain Ⅱ、Domain Ⅲ 和Domain Ⅳ(图2B)。同时,利用AlphaFold 对OfIAA14 蛋白的三维结构进行预测,并通过PyMOL 对其结构域进行可视化标注(图2C)。最后制备OfIAA14 的原位杂交探针,采用PCR 进行扩增和克隆,获得长度约为500 bp 的特异性片段(图2D)。
-
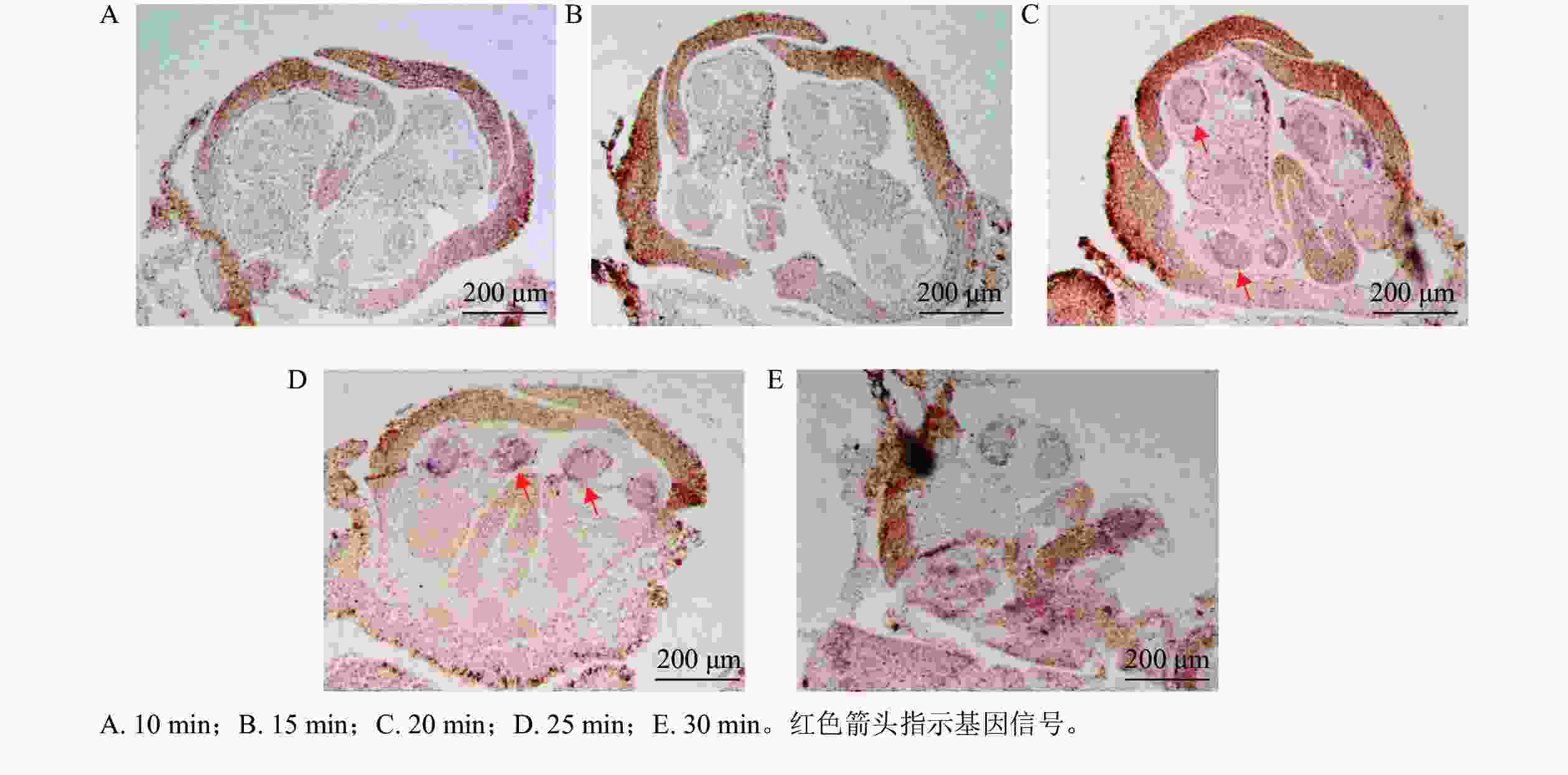
以OfIAA14为对象基因,进行花芽切片蛋白酶K消化效果比较。结果显示:消化10 min 的花芽切片组织结构完整,但是没有信号显示(图3A);消化15 min 的切片组织和10 min相似,并且没有观察到明显信号(图3B);消化20 min 的切片显示组织结构良好,组织内部结构清晰可见,可见明显信号(图3C);消化25 min 的切片与20 min相似,结构完整可见明显信号(图3D);消化30 min 的切片表面出现明显空白斑块(图3E),提示组织过度消化,结构组织受到破坏,即桂花花芽原位杂交的最佳蛋白酶 K消化时间为20~25 min。
-
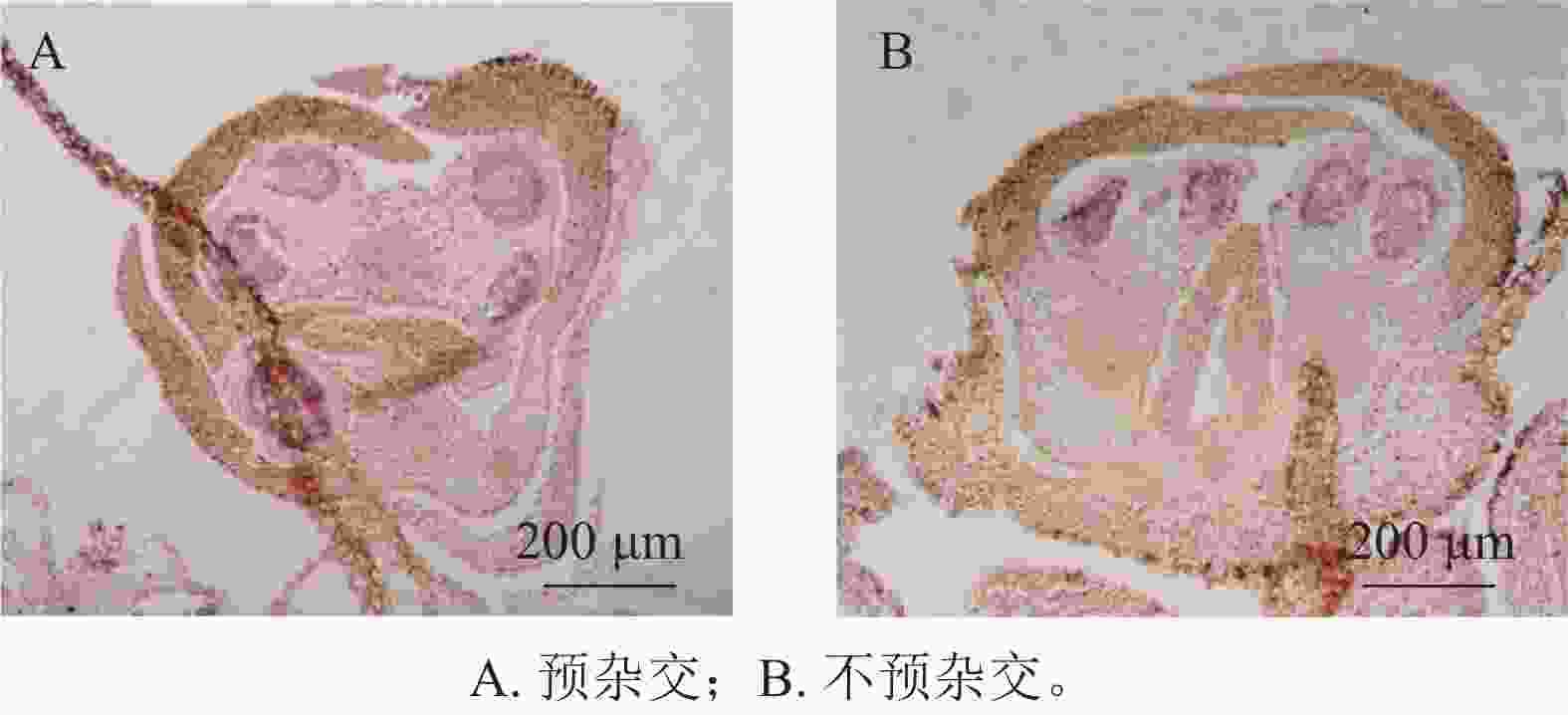
在蛋白酶K消化20 min的条件下,设置了预杂交和不预杂交2种处理进行对比实验。结果表明:在桂花组织中,是否进行预杂交对杂交信号强度和背景水平影响不明显(图4A、4B)。因此,在桂花原位杂交体系中可省略预杂交步骤,从而简化实验流程并减少杂交液的使用。
-
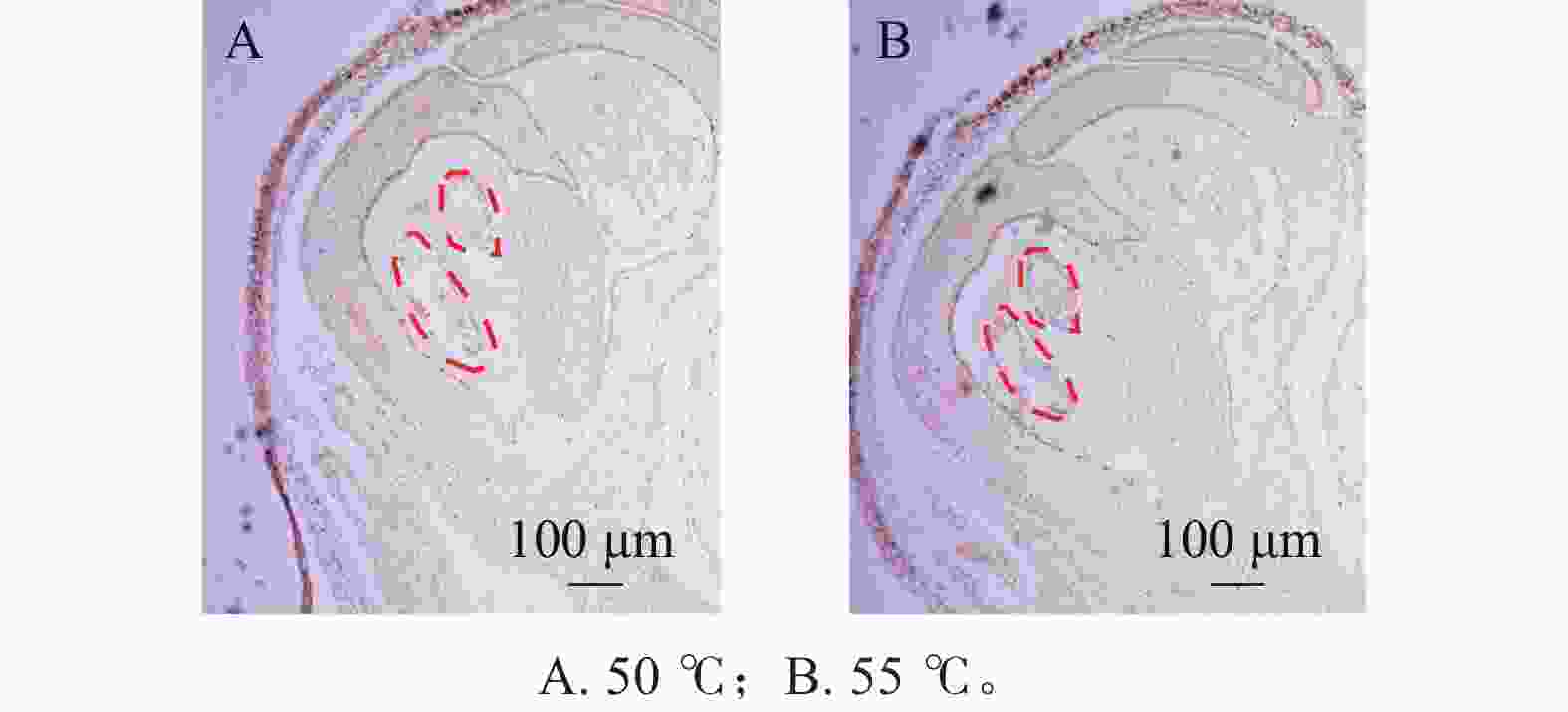
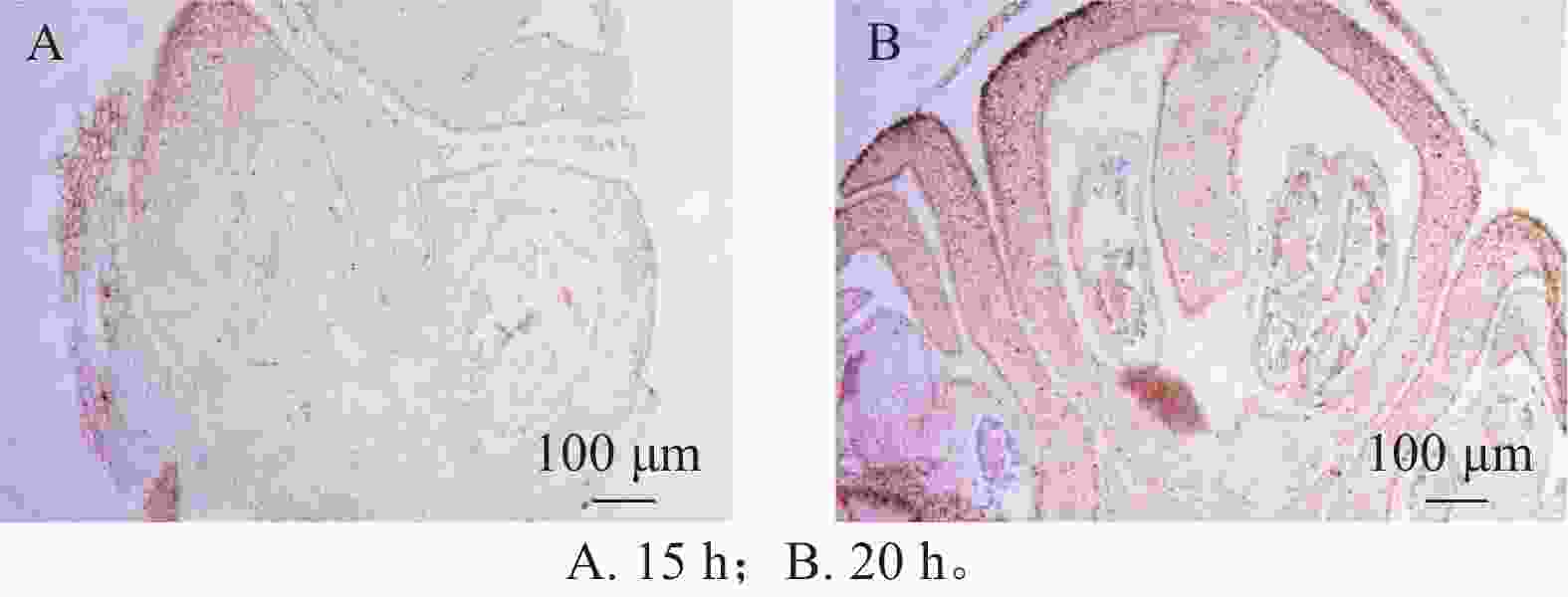
在蛋白酶K处理20 min的基础上,分别设置2种杂交温度(50和55 ℃)及2种杂交时间(15和20 h)进行比较。结果表明:在50 ℃条件下,杂交信号相对较弱,但背景干扰较低(图5A);而在55 ℃条件下,杂交信号明显增强,但背景干扰亦有所增加(图5B)。杂交时间比较结果显示,与15 h相比,20 h处理获得的杂交信号显著增强(图6A、6B),而15 h条件下信号相对较弱。综合考虑信号强度、背景干扰及实验稳定性,在保证背景可控的前提下,确定50 ℃、20 h为桂花原位杂交的适宜温度和时间。
-
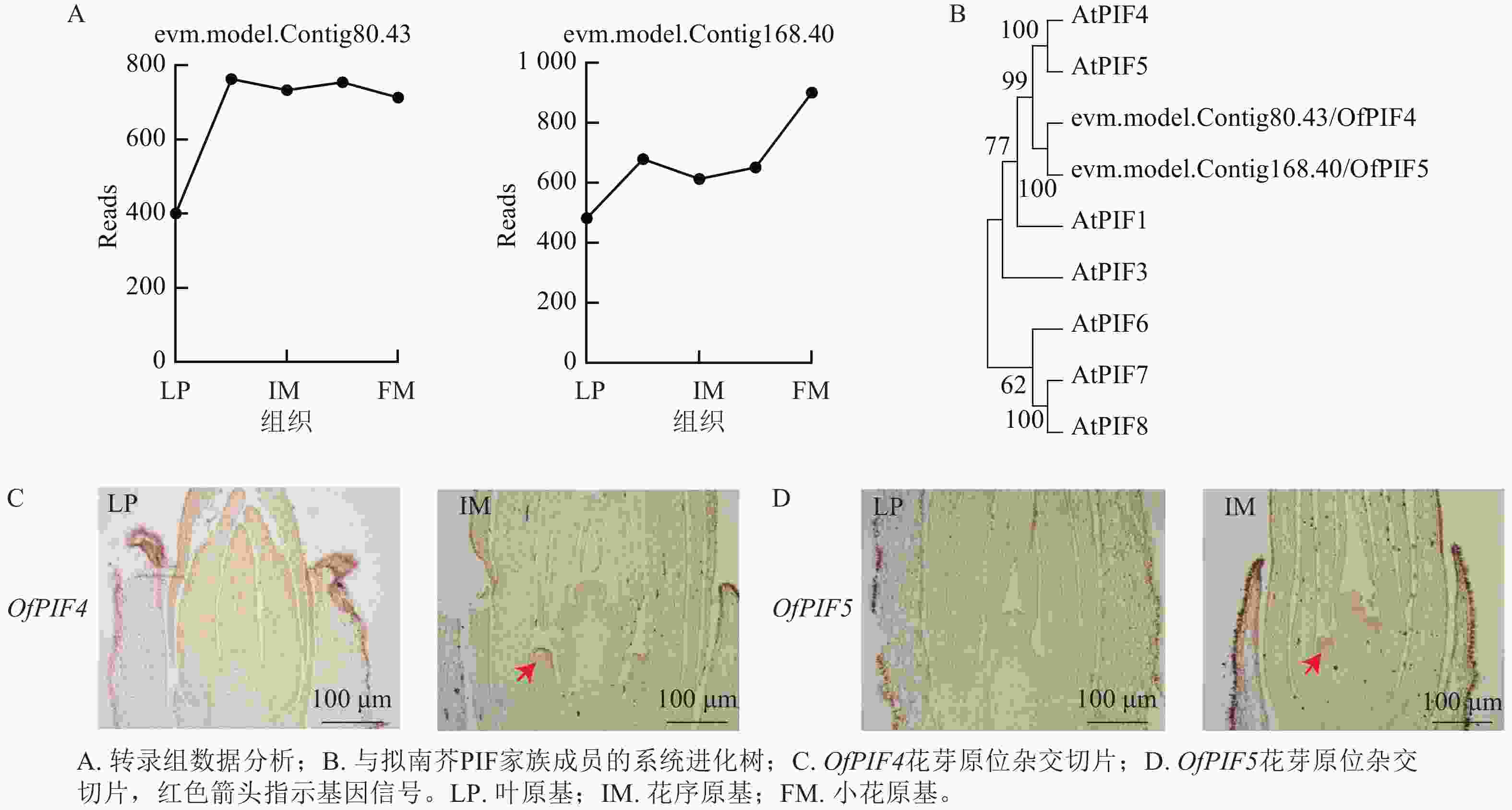
为验证优化的原位杂交在不同组织和发育阶段的准确性,从转录组差异表达基因中筛选候选基因evm.model.Contig80.43-gene、evm.model.Contig168.40-gene,对叶原基(LP)、花序原基(IM)以及小花原基(FM)的基因Reads数进行分析,发现在花序原基时期,2个基因的Reads数明显上升(图7A)。通过系统进化树,最终命名为OfPIF4、OfPIF5(图7B)。利用优化的原位杂交在‘四季桂’花芽不同发育时期对OfPIF4、OfPIF5进行时空特异性检测,结果显示,OfPIF4和OfPIF5的基因信号在花芽分化期后的花序原基中就可以明显检测到,与转录组数据一致(图7C、7D),同时更进一步明确该基因在组织上的时空表达。
-
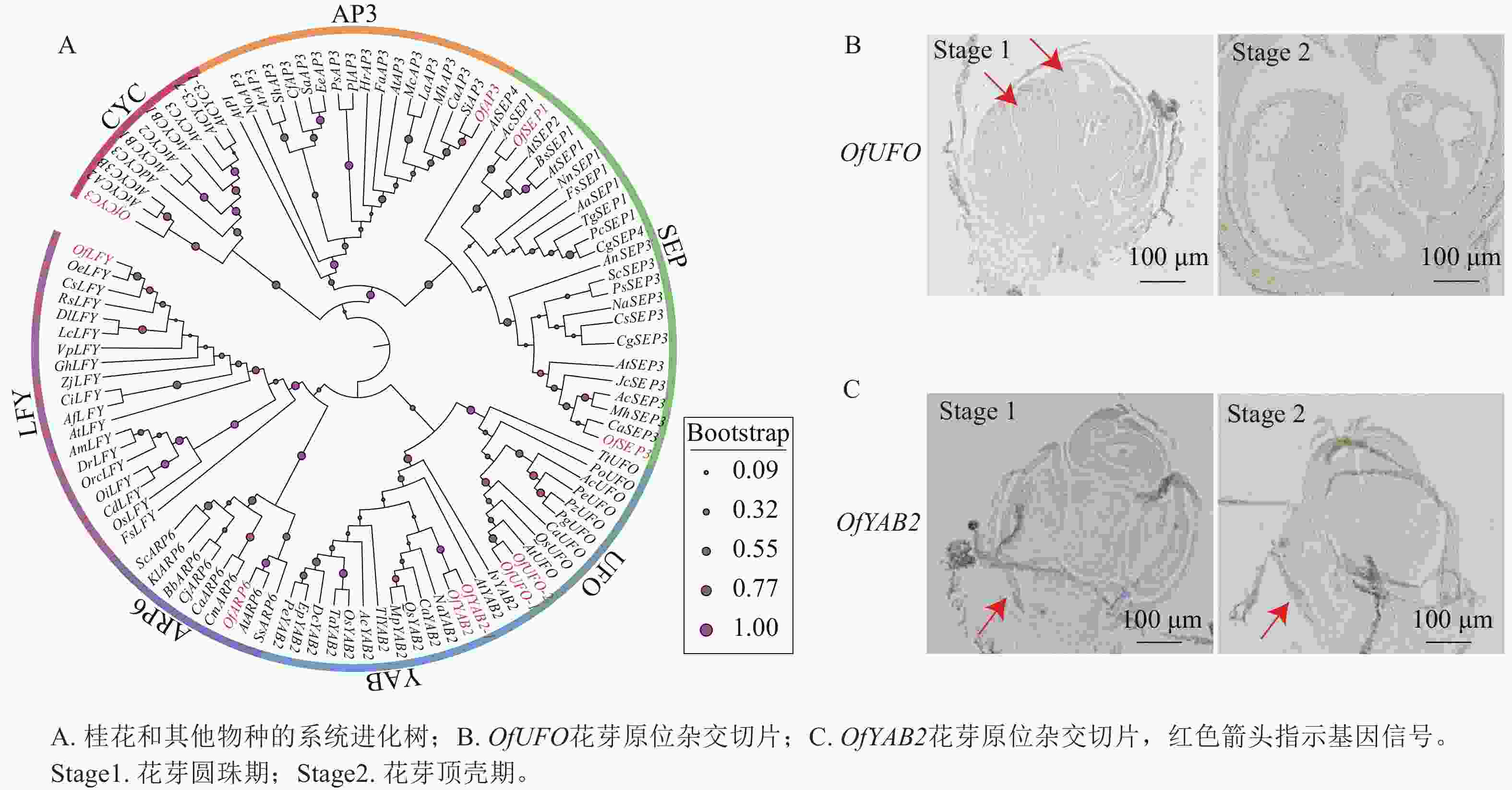
基于转录组数据筛选获得多个与花器官发育相关的候选基因(图8A),并选取OfUFO和OfYAB2作为代表基因进行表达验证。选取桂花品种‘堰虹桂’花芽发育Stage 1和 Stage 2时期的样品[5],采用优化的原位杂交检测OfUFO 和OfYAB2在不同花器官中的表达分布特征。结果显示:OfUFO的杂交信号主要分布于Stage 1花粉粒中(图8B),而OfYAB2的信号主要定位于Stage 1和Stage 2苞片组织(图8C),提示两者可能分别参与花粉发育和苞片形成过程。
-
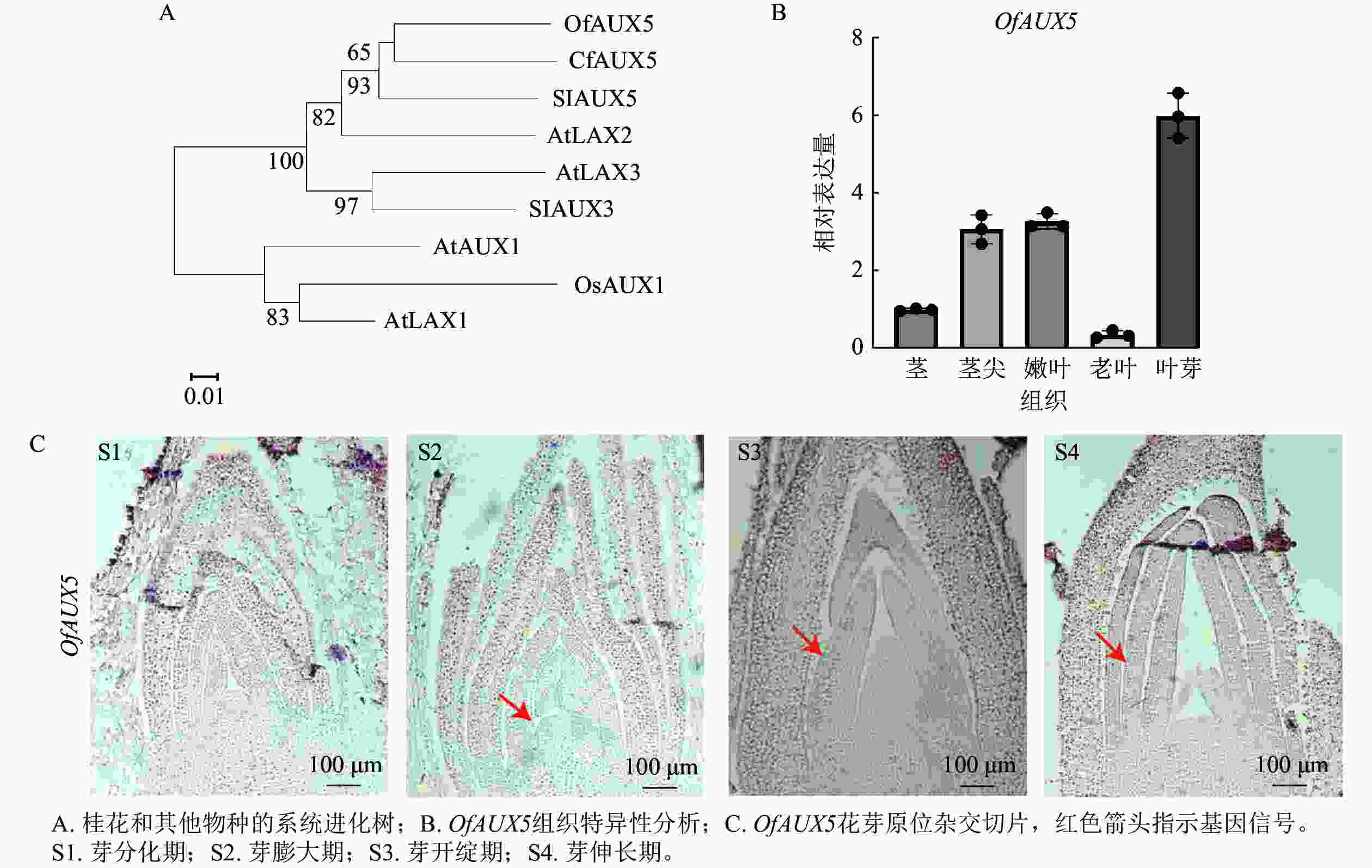
选取‘堰虹桂’叶芽发育阶段S1~S4时期的样品,选择叶芽发育相关的OfAUX5基因进行验证。通过构建系统进化树,表明OfAUX5与大花四照花Cornus florida中的CfAUX5蛋白具有65%的同源性,两者在结构和功能上具有相似的功能(图9A)。组织特异性分析表明OfAUX5基因在叶芽组织中高表达(图9B)。原位杂交试验进一步证实OfAUX5的杂交信号主要定位于生长点和幼叶处,且在幼叶处杂交信号最强(图9C)。推测该基因在‘堰虹桂’叶芽发育阶段中发挥功能。通过以上结果表明,优化的原位杂交方法适用于不同桂花品种、组织及发育阶段的mRNA定位表达研究。
-
RNA原位杂交技术已被广泛用于不同植物的基因表达情况,但在桂花中鲜有报道,本研究的目的是优化适用于不同桂花品种、组织及发育阶段的原位杂交技术流程。若想通过杂交信号判断基因表达定位,保持组织结构的完整性至关重要。在切片前需要对其抽真空时间进行选择,以避免样品的完整性受到影响。因此在本研究中选择抽真空2次,每次30 min进行,切片效果良好且具有较好的组织完整性。
在杂交前需用蛋白酶K处理组织切片,以提高探针在组织中的渗透能力并增强其与靶RNA 的结合效率。然而,蛋白酶K消化时间过长可能破坏组织结构并加剧非特异性结合[23]。消化时间过短则会限制探针渗透,降低杂交信号强度[24]。本研究结果表明,当消化时间为20~25 min时,组织结构基本完整,且可获得清晰稳定的杂交信号。
预杂交通常被认为是原位杂交过程中的关键步骤,其主要作用是封闭样本中的非特异性结合位点,从而降低背景信号并提高杂交信号的特异性和稳定性。但本研究预杂交与不预杂交处理对桂花组织中杂交信号的强度和完整性影响不显著,说明在本体系中可省略预杂交步骤,不仅简化了实验流程,同时降低了试剂消耗和操作时间。
杂交温度和时间对探针与靶序列的特异性结合和检测灵敏度具有重要影响。较高的杂交温度虽然有助于提高结合特异性,但可能对组织结构稳定性产生不利影响[25]。因此,本研究结果表明,在50 ℃条件下可获得清晰稳定的杂交信号,且背景干扰相对较低;结合杂交时间对比结果,20 h处理的信号强度明显优于15 h。综合考虑信号质量与实验稳定性,确定50 ℃、20 h为桂花原位杂交的适宜条件。
为验证该优化体系的可靠性和适用性,进一步在不同桂花品种、组织及发育阶段中对多个基因进行检测。结果显示,OfPIF4和OfPIF5主要在花序原基中表达,而OfUFO和OfYAB2主要在花粉和苞片中表达,OfAUX5主要在幼叶中表达。上述表达模式与已知功能特征相一致,进一步证明了所建立原位杂交方法具有良好的可靠性和普适性。
-
本研究建立了一套高效、稳定且可操作性强的桂花组织原位杂交技术体系,为桂花基因时空表达模式解析及功能研究提供了可靠的技术支撑,且该优化体系可在不同桂花品种、组织及发育阶段中获得清晰且具有良好特异性的杂交信号,显示出较高的稳定性和适用性,并有助于进一步明确目标基因在特定组织和发育阶段中的生物学功能。
Construction of the in situ hybridization system for Osmanthus fragrans and its universality in different tissues
-
摘要:
目的 原位杂交技术广泛应用于基因时空表达模式及功能研究。本研究以桂花不同品种不同组织不同发育阶段为材料,建立高效且稳定的桂花原位杂交体系,为桂花功能基因时空表达定位提供技术方法。 方法 以桂花生长素响应因子OfIAA14为检测基因,在常规原位杂交流程基础上,对样品抽真空时间、蛋白酶K消化时间、是否进行预杂交、杂交温度和杂交时间等关键参数进行比较,同时在不同品种、不同组织及其不同发育阶段等方面进行相关基因功能验证。 结果 在抽真空30 min、0.08 MPa(2次)、蛋白酶K 消化20~25 min、无需预杂交、杂交温度50 ℃、杂交时间20 h的条件下,可获得最佳杂交信号。进一步选用OfPIF4、OfPIF5、OfUFO、OfYAB2和OfAUX5等基因,对原位杂交优化体系在桂花不同品种、不同组织及不同发育阶段中的适用性进行验证,均获得良好的组织结构保持和清晰稳定的信号表达,表明该方法具有较好的可靠性和一定的普适性。 结论 本研究建立了一套适用于桂花组织的原位杂交优化技术体系,可为深入解析桂花开花发育相关基因的时空表达特征及分子调控机制提供可靠的技术支撑。图9表1参25 Abstract:Objective In situ hybridization(ISH)technology is widely used for studying the spatiotemporal expression patterns and functions in different tissues. This study utilizes materials from different cultivars, tissues, and developmental stages of Osmanthus fragrans to establish an efficient and stable in situ hybridization system for this flower species, providing a technical method for the spatiotemporal expression localization of functional genes in O. fragrans. Method Using the auxin response factor OfIAA14 as the detection gene, based on the conventional ISH process, key parameters such as sample vacuumization time, protease K digestion time, whether to perform pre-hybridization, and hybridization temperature and time were systematically optimized and compared. Meanwhile, the functional verification of related genes was conducted across different varieties, tissues, and developmental stages. Result The results showed that the optimal hybridization signal could be obtained under the conditions of vacuumization for 30 min at 0.08 MPa (2 times), proteinase K digestion for 20−25 min, no pre-hybridization, hybridization temperature at 50 ℃, and hybridization time of 20 h. Furthermore, genes such as OfPIF4, OfPIF5, OfUFO , OfYAB2 and OfAUX5 were selected to verifty the applicability of the optimized system in different O. fragrans cultivars, tissues and developmental stages. Good tissue structure preservation and clear and stable signal expression were obtained, indicating that the method has good reliability and certain universality. Conclusion This study established an optimized ISH technology system suitable for O. fragrans tissues, providing reliable technical support for in-depth analysis of the spatiotemporal expression characteristics and molecular regulation mechanisms of genes related to flower development in O. fragrans. [Ch, 9 fig. 1 tab. 25 ref.] -
Key words:
- Osmanthus fragrans /
- in situ hybridization /
- condition optimization /
- gene expression
-
表 1 扩增引物序列
Table 1. Amplification primer sequence
基因 正向引物序列 (5’→3’) 反向引物序列(3’→5’) OfIAA14 ATGGAAGTTGGCCAGAA AATGCGGCCTTCTCAG OfPIF4 CTCCTTCTCCTCTCCGACA AGCATCAGAACTCGGGAC OfPIF5 CCAATTCCTGGTTGGAGTATTGAG TTGATCCTGTCCCTCCGTT OfUFO AGTTCAAGAAAGTCATCGGAA TCTCCCCTACAAAATGTCGAA OfYAB2
OfAUX5CAATCGTGCAAATAAGACACT
ATGGAATCCTCGGACAAGGTTTTCACACTTTACTCCGACCAG
TGCCCAATAATCCATAGAA -
[1] 向其柏, 刘玉莲. 中国桂花品种图志[M]. 杭州: 浙江科学技术出版社, 2008. XIANG Qibai, LIU Yulian. An Illustrated Monograph of the Sweet Osmanthus Cultivars in China[M]. Hangzhou: Zhejiang Science & Technology Press, 2008. [2] 彭琳, 王艺光, 董彬, 等. 桂花OfLCYB提高转基因烟草类胡萝卜素含量和低温胁迫的抗性[J]. 农业生物技术学报, 2025, 33(1): 1−14. PENG Lin, WANG Yiguang, DONG Bin, et al. Osmanthus fragrans OfLCYB increased carotenoid content and resistance to low temperature stress in transgenic tobacco(Nicotiana tabacum)[J]. Journal of Agricultural Biotechnology, 2025, 33(1): 1−14. DOI: 10.3969/j.issn.1674-7968.2025.01.001. [3] 郭罕年, 熊欣, 胡飞杨, 等. 桂花OfSAUR21基因的克隆及功能验证[J]. 浙江农林大学学报, 2025, 42(5): 1059−1067. GUO Hannian, XIONG Xin, HU Feiyang, et al. Cloning and functional verification of OfSAUR21 gene in Osmanthus fragrans[J]. Journal of Zhejiang A&F University, 2025, 42(5): 1059−1067. DOI: 10.11833/j.issn.2095-0756.20250446. [4] YE Yong, LU Xinke, KONG En, et al. OfWRKY17-OfC3H49 module responding to high ambient temperature delays flowering via inhibiting OfSOC1B expression in Osmanthus fragrans[J]. Horticulture Research, 2025, 12(1): uhae273. DOI: 10.1093/hr/uhae273. [5] ZHONG Shiwei, ZHU Huijun, LI Wenle, et al. DNA methylome analysis reveals novel insights into active hypomethylated regulatory mechanisms of temperature-dependent flower opening in Osmanthus fragrans[J]. Horticulture Research, 2024, 11(3): uhae010. DOI: 10.1093/hr/uhae010. [6] LAN Yangang, HUANG Xue, LI Ziyi, et al. The OfJAZ3-OfMYB21 complex mediates jasmonic acid signaling pathway to regulate linalool biosynthesis in Osmanthus fragrans[J]. Horticulture Research, 2026, 13(3): uhaf321. DOI: 10.1093/hr/uhaf321. [7] TANG Meng, SONG Tao, LAM L P Y, et al. Integrated multi-omics reveals flower color regulatory networks in Osmanthus fragrans[J]. Molecular Horticulture, 2026, 6: 1. DOI: 10.1186/s43897-025-00158-y. [8] MARTINEAU B, TAYLOR W C. Cell-specific photosynthetic gene expression in maize determined using cell separation techniques and hybridization in situ[J]. Plant Physiology, 1986, 82(2): 613−618. DOI: 10.1104/pp.82.2.613. [9] YOKOYAMA R, TAKAHASHI T, KATO A, et al. The ArabidopsisERECTAgene is expressed in the shoot apical meristem and organ primordia[J]. The Plant Journal, 1998, 15(3): 301−310. DOI: 10.1046/j.1365-313x.1998.00203.x. [10] ELLIOTT R C, BETZNER A S, HUTTNER E, et al. AINTEGUMENTA an APETALA2-like gene of Arabidopsis with pleiotropic roles in ovule development and floral organ growth[J]. The Plant Cell, 1996, 8(2): 155−168. DOI: 10.1105/tpc.8.2.155. [11] SAMACH A, KOHALMI S E, MOTTE P, et al. Divergence of function and regulation of class B floral organ identity genes[J]. The Plant Cell, 1997, 9(4): 559−570. DOI: 10.1105/tpc.9.4.559. [12] CORNISH E C, PETTITT J M, BONIG I, et al. Developmentally controlled expression of a gene associated with self-incompatibility in Nicotiana alata[J]. Nature, 1987, 326(6108): 99−102. DOI: 10.1038/326099a0. [13] CHENG Jinchen, SEELEY K A, GOUPIL P, et al. Expression of DC8 is associated with, but not dependent on embryogenesis[J]. Plant Molecular Biology, 1996, 31(1): 127−141. DOI: 10.1007/bf00020612. [14] DOMÍNGUEZ F, CEJUDO F J. Germination-related genes encoding proteolytic enzymes are expressed in the nucellus of developing wheat grains[J]. The Plant Journal, 1998, 15(4): 569−574. DOI: 10.1046/j.1365-313x.1998.00233.x. [15] WEBER H, BORISJUK L, HEIM U, et al. A role for sugar transporters during seed development: molecular characterization of a hexose and a sucrose carrier in fava bean seeds[J]. The Plant Cell, 1997, 9(6): 895−908. DOI: 10.1105/tpc.9.6.895. [16] SMITH A G, HINCHEE M, HORSCH R. Cell and tissue specific expression localized byin situ RNA hybridization in floral tissues[J]. Plant Molecular Biology Reporter, 1987, 5(1): 237−241. DOI: 10.1007/bf02669718. [17] MEYEROWITZ E M. In situ hybridization to RNA in plant tissue[J]. Plant Molecular Biology Reporter, 1987, 5(1): 242−250. DOI: 10.1007/bf02669719. [18] NADEAU J A, ZHANG X S, LI J, et al. Ovule development: identification of stage-specific and tissue-specific cDNAs[J]. The Plant Cell, 1996, 8(2): 213−239. DOI: 10.1105/tpc.8.2.213. [19] YAO Jin, LI Xingmei, WU Na, et al. Improvement of RNA in situ hybridisation for grapevine fruits and ovules[J]. International Journal of Molecular Sciences, 2023, 24(1): 800. DOI: 10.3390/ijms24010800. [20] KIM M, PHAM T, HAMIDI A, et al. Reduced leaf complexity in tomato wiry mutants suggests a role for PHANandKNOX genes in generating compound leaves[J]. Development, 2003, 130(18): 4405−4415. DOI: 10.1242/dev.00655. [21] SUN Yi, JIANG Jianing, ZHANG Qiongyue, et al. The vascular-cambium-specific transcription factor PtrSCZ1 and its homologue regulate cambium activity and affect xylem development in Populus trichocarpa[J]. Frontiers in Plant Science, 2025, 16: 1546660. DOI: 10.3389/fpls.2025.1546660. [22] SUN Jinjing, LI Feng, WANG Donghui, et al. CsAP3: a cucumber homolog to Arabidopsis APETALA3 with novel characteristics[J]. Frontiers in Plant Science, 2016, 7: 1181. DOI: 10.3389/fpls.2016.01181. [23] KITAZAWA S, KITAZAWA R, MAEDA S. In situ hybridization with polymerase chain reaction-derived single-stranded DNA probe and S1 nuclease[J]. Histochemistry and Cell Biology, 1999, 111(1): 7−12. DOI: 10.1007/s004180050327. [24] FOUQUET R, LÉON C, OLLAT N, et al. Identification of grapevine aquaporins and expression analysis in developing berries[J]. Plant Cell Reports, 2008, 27(9): 1541−1550. DOI: 10.1007/s00299-008-0566-1. [25] HOLLAND M S, MACKENZIE C D, BULL R W, et al. A comparative study of histological conditions suitable for both immunofluorescence and in situ hybridization in the detection of Herpesvirus and its antigens in chicken tissues[J]. Journal of Histochemistry & Cytochemistry, 1996, 44(3): 259−265. DOI: 10.1177/44.3.8648086. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20260156






 下载:
下载: