-
桉树为桃金娘科Myrtaceae桉属Eucalyptus的总称[1−2],是目前世界上种植数量最多的阔叶树种之一[3]。桉树生长速度快、轮伐周期短、适应能力强、木材产量高,与杨树Populus和松树Pinus并称世界上三大速生树种[4−5]。其中,尾叶桉Eucalyptus uropylla和巨桉E. grandis的杂交种尾巨桉E. uropylla×E. grandis DH32-29杂种优势明显,其干形通直、适应性广、出材率高、材质优良、耐寒性好,是中国南方地区林业生产中的主栽品种[6]。
植物遗传转化是分子育种的关键步骤[7−8],不仅可用于鉴定基因功能,还可以用于改良植物品种的短板性状,尤其适用于育种世代周期较长的树种,实现其目标性状的遗传改良[9]。预培养时间是遗传转化研究中讨论较多的影响因素之一。有研究表明:处于分裂期或代谢活跃期的“感受态细胞”更容易被根癌农杆菌Agrobacterium tumefaciens感染而转化。预培养有利于外植体在切口处形成微愈伤,改变其生理生化状态,促进受体细胞分裂,提高细胞代谢活性,易于整合外源DNA,提高转化率[10]。预培养时间过短,细胞未进入最佳分化阶段;预培养时间过长,外植体伤口会产生保护层,阻碍农杆菌与分裂细胞的接触,因此,适宜的预培养时间可显著提高农杆菌转化效率[11]。一般1~4 d的预培养时间较为适宜[12]。此外预培养时间的长短与物种和外植体类型有关,石榴Punica granatum嫩茎为受体材料时,遗传转化过程中预培养3 d的转化率最高[11]。香蕉Musa nana最佳的预培养时间为1 d,转化效率最高达6.87%[13]。
外植体不同发育阶段对转化效率有很大影响,当外植体培养到细胞发育的适宜状态时,可提高遗传转化的效率[14]。最新研究发现:杨树和烟草Nicotiana tabacum的DNA合成期(S期)是进行遗传转化的最佳细胞周期处理时间点[15]。因此,本研究以尾巨桉DH32-29叶片为材料,EHA105为转化农杆菌,通过观察细胞周期S期细胞数量,确认预培养时间,从而建立高效、稳定的农杆菌介导的植物转化体系。
-
以尾巨桉无性系DH32-29为外植体进行遗传转化研究,并在含有木本植物培养基(WPM)的预培养液体培养基(2.46 g·L−1WPM + 30.00 g·L−1蔗糖 + 1.00 g·L−1水解酪蛋白)上培养。组培苗由中国林业科学研究院热带林业研究所林木生物育种课题组繁殖保存。
-
将继代20~25 d的尾巨桉DH32-29组培苗的3~5片叶片切去叶尖后,置于WPM液体培养基中培养0、1、2、3、4、5、6、7 d。培养条件:培养温度为(25±2) ℃,光照强度为2 000 lx,光周期为16 h光照/8 h黑暗,每个预培养时间点使用至少3个独立培养批次的外植体,每批次含60片叶片。
-
将体外培养的桉树叶片置于体视显微镜(Olympus)下观察,记录不同预培养时间处理的体外培养材料切口处发育状态。
-
本研究使用流式细胞仪(BD FACSCalibur)检测细胞周期。将3~5片桉树叶片切碎后,放入300.0 μL裂解液,置于10 cm的培养皿中,再加入1.2 mL的碘化丙啶(PI)混合染液,通过30 μm尼龙网过滤至检测管中,避光孵育10 min,每个处理采集2个样品。峰图由Cyflow®倍性分析仪进行分析,并使用modfitLT软件鉴别峰图中DNA合成前期(G1期)、DNA合成期(S期)和DNA合成后期/有丝分裂期(G2/M期)所占比例。
-
EdU是胸腺嘧啶核苷类似物。在细胞增殖过程中,EdU会被摄取到细胞核中,与DNA合成过程中的DNA结合,形成EdU-DNA复合物。这个复合物可以被抗EdU抗体识别并结合,从而形成EdU-DNA-抗体复合物。通过检测这个复合物的信号强度,可以确定细胞增殖的速率和细胞周期。EdU染色可以准确定位细胞周期S期的细胞,使其发出绿色荧光。
将桉树叶片在分化培养基上培养1、2、3、4、5、6和7 d,然后置于含10 mmol·L−1 EdU的分化培养基上培养24 h,孵育结束后,用磷酸盐缓冲液(PBS)清洗材料3次(此时将切口处朝下)。然后用质量浓度为4.0%的多聚甲醛固定,避光处理30 min后用PBS洗涤3次。然后用体积分数为0.5%Triton X-100处理15 min促渗。根据YF 488 Click-iT EdU成像试剂盒(百瑞极)处理样品。最后在激光共聚焦显微镜(徕卡仪器有限公司)拍照观察,设置波长为495~515 nm检测GFP信号,650 nm检测叶绿体发出的荧光。
-
RT-qPCR是通过荧光染料或荧光标记的特异性探针,对PCR产物进行标记跟踪,实时在线监控反应过程,结合相应的软件可以对产物进行分析,计算待测样品模板的初始浓度。为了验证上述实验,在细胞周期S期,选择不同分化培养时间7个关键基因的表达水平进行RT-qPCR检测。
使用植物总RNA提取试剂盒(Aidlab),从植物组织中提取总RNA。使用cDNA合成试剂盒(Takara)合成cDNA。RT-qPCR分析采用罗氏LightCycler 96仪器进行。对每个样品进行3次生物重复。Primer 5设计基因特异性引物(表1)。采用2−ΔΔCt方法计算基因相对表达水平[16]。
表 1 特异性引物
Table 1. Specific primer
引物 碱基序列(5'→3') EgrCDKD3-F GCTCGGTGAGGGTACGTATG EgrCDKD3-R GCAGGTTCCCTTTGTGAGGA EgrCYCD3;3-F CCTCCGCGAGATAAAGGACC EgrCYCD3;3-R ACGGCCAACATAGCAGTCAA EgrCYCD1;1-F TGCGATGGGCTAAGCAAAGA EgrCYCD1;1-R ACGATGGCGATAACGAGGAC EgrCYCH1;1-F CGGATTTCCAGAGCTCGACG EgrCYCH1;1-R TGGACGGGAATGCTTGTCAT EgrCDKB1;2-F CTATTCGATCGGCGTGGACA EgrCDKB1;2-R GGTAACTCCTGGCCATTGCT EgrCYCD6;1-F GCTCGGTGAGGGTACGTATG EgrCYCD6;1-R GCAGGTTCCCTTTGTGAGGA EgrCYCA3;4-F TGCTCAAGAAGGTCACAAGACTA EgrCYCA3;4-R GTGAGTTCTTGGTTGCGTGAT -
GUS基因是目前常用的一种报告基因,其产物β-葡萄糖苷酸酶是一种水解酶,能催化许多β-葡萄糖苷酯类物质的水解,它可以将5-溴-4-氯-3-吲哚-β-葡萄糖苷酸酯分解为蓝色的物质[17]。将含有GUS基因的pBI121载体转入尾巨桉离体叶片中。将叶片放入1.5 mL离心管中,加入GUS染色液,用锡纸包好离心管,真空抽滤30 min,37 ℃孵育16 h。用体积分数为70%的乙醇浸泡样本3 h,直至阴性对照呈白色,将样本保存于乙醇中,用体视显微镜观察并拍照。同时统计GUS染色率,处理叶片蓝色覆盖面积≥50%视为转化成功。GUS染色率=染色叶片个数/总外植体个数×100%。
-
采用Excel 2021进行数据处理,SPSS 24.0[18−19]进行数据分析,GraphPad Prism 5进行图表绘制。使用SPSS 24.0进行单因素方差分析(one-way ANOVA),使用Duncan极差法进行多重比较分析。
-
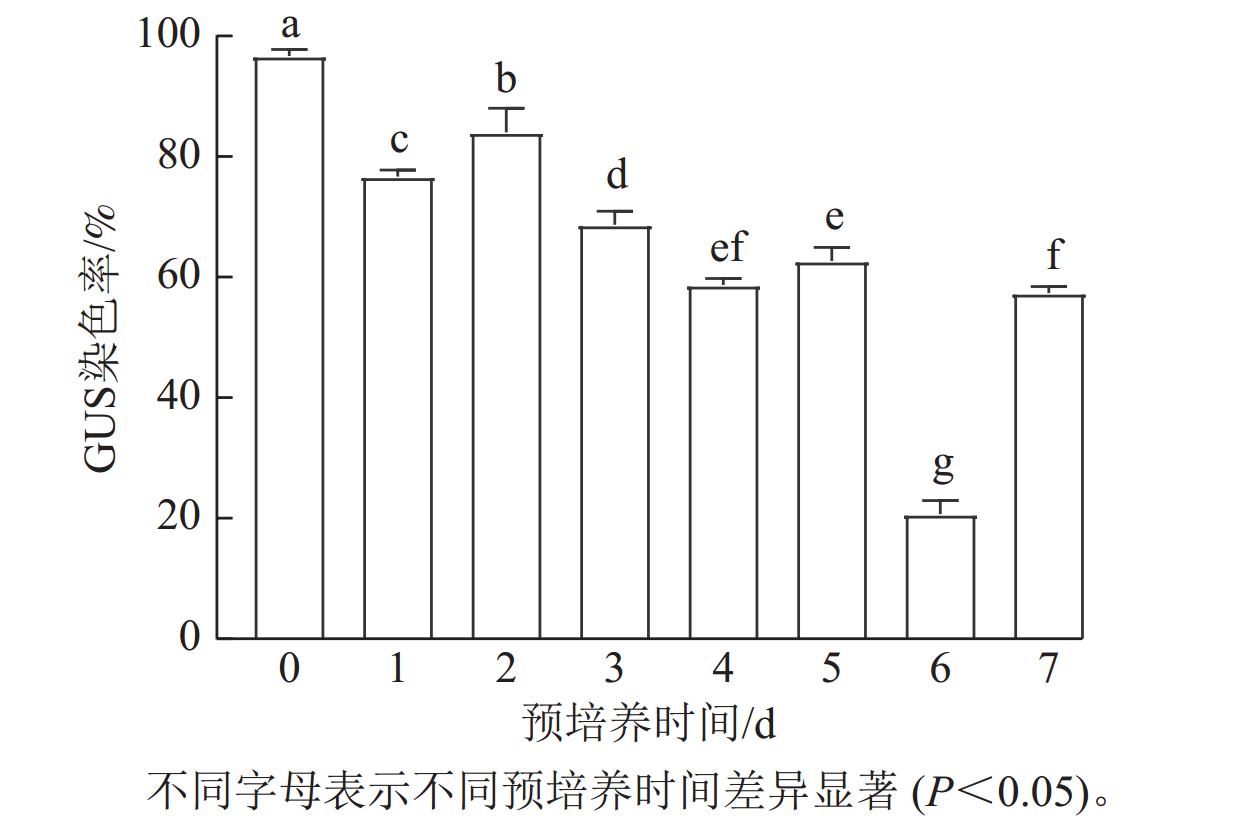
经过不同预培养时间的叶片伤口处能够明显看到蓝色,主要为切口处(图1)。预培养0 d时,转化效率最高,GUS染色率为97.33%;预培养2 d时,转化效率次之,染色率为84.31%;预培养6 d时,转化效率最低,GUS染色率为20.62%。预培养1和3 d的染色率均在80%以上(图2)。GUS染色结果说明:预培养0~3 d的染色率较高。
-
预培养0 d时G2/M期细胞比例最高,1~7 d时S期细胞占比均高于0 d,且在整个预培养时间中,S期细胞在预培养5 d时比例最高,为26.88%,而在预培养5 d时,G2/M期细胞占比为56.12%,G1期细胞为17.00%。预培养3 d时,S期细胞占比为23.54%,仅次于处理5 d。表明尾巨桉DH32-29叶片离体预培养3~5 d为最佳遗传转化时间(图3)。
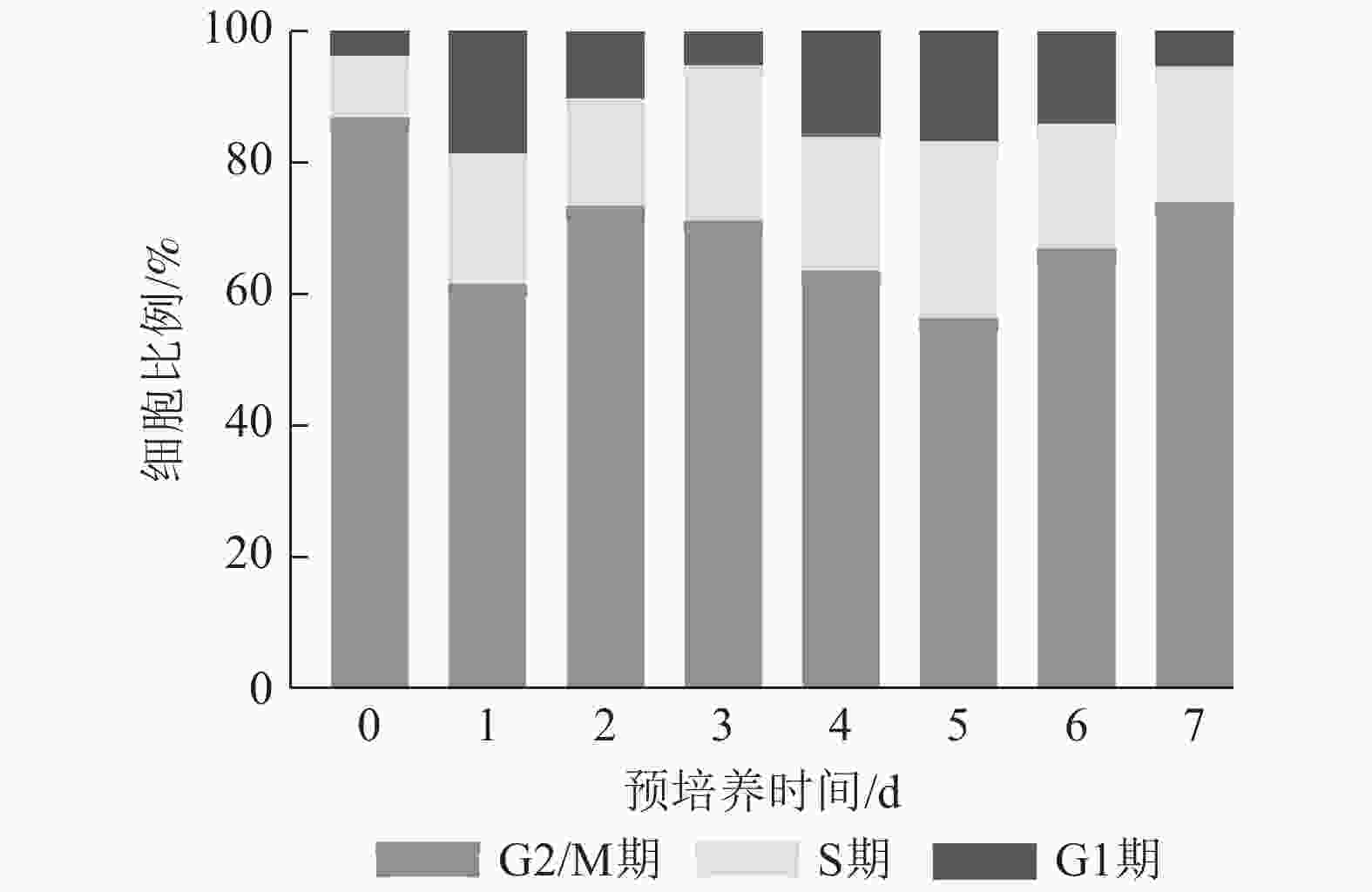
图 3 尾巨桉DH32-29叶片不同离体培养时间下的细胞周期鉴定
Figure 3. Identification of cell cycle in leaves of E. urophylla × E. grandis DH32-29 under different in vitro culture time
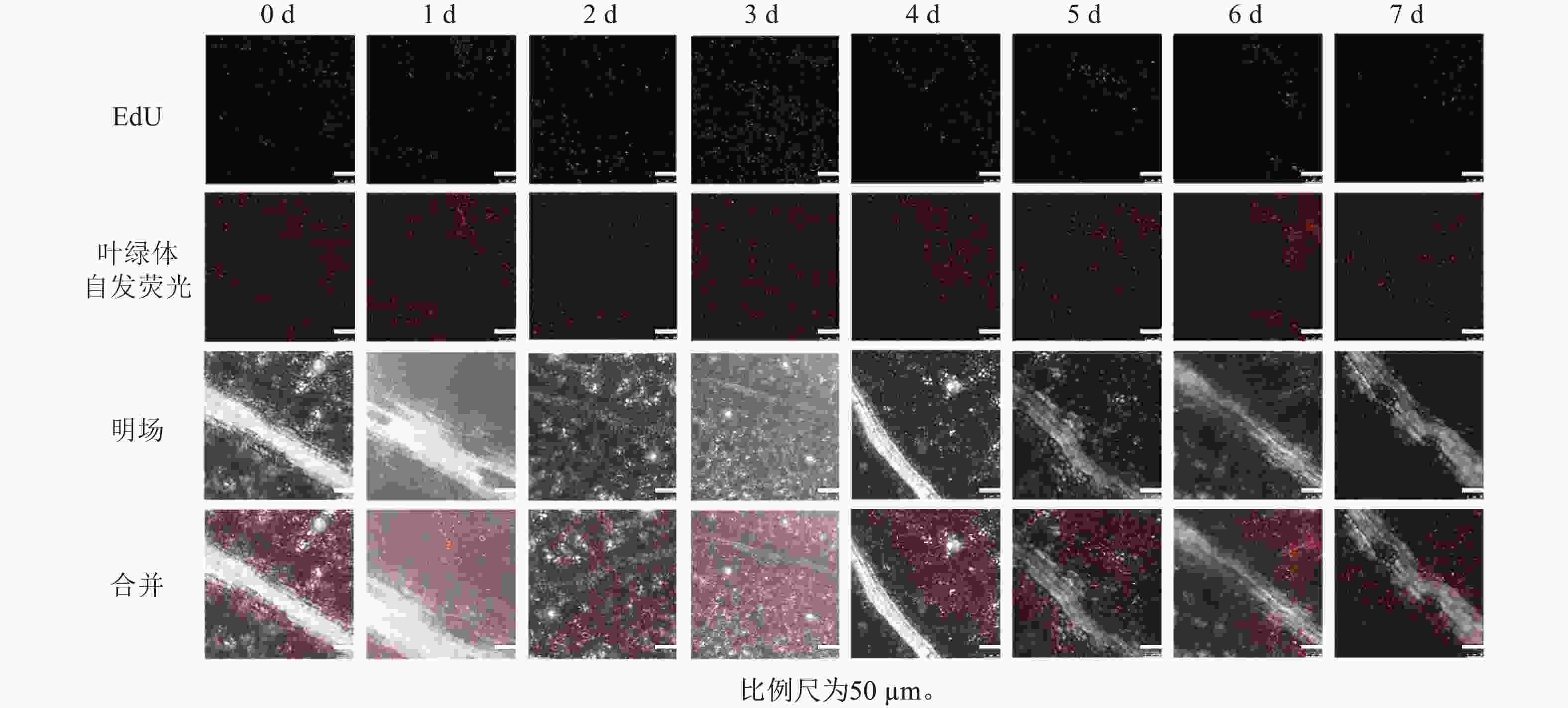
本研究采用EdU染色对不同离体培养的桉树叶片进行染色,观察它们的荧光信号分布(图4)。预培养0~1 d出现少量绿色荧光,2~3 d绿色荧光最多,4 d后荧光数量逐渐减少,但4 d荧光信号仍较强,而且荧光主要分布于叶脉两侧靠近切口处,7 d 绿色荧光最少,部分叶片无绿色荧光,这说明细胞周期S期的细胞数量在离体后先升高后降低,且2~3 d时S期细胞数量较高。说明尾巨桉DH32-29叶片离体培养2~3 d,其转化效率可能最佳。
-
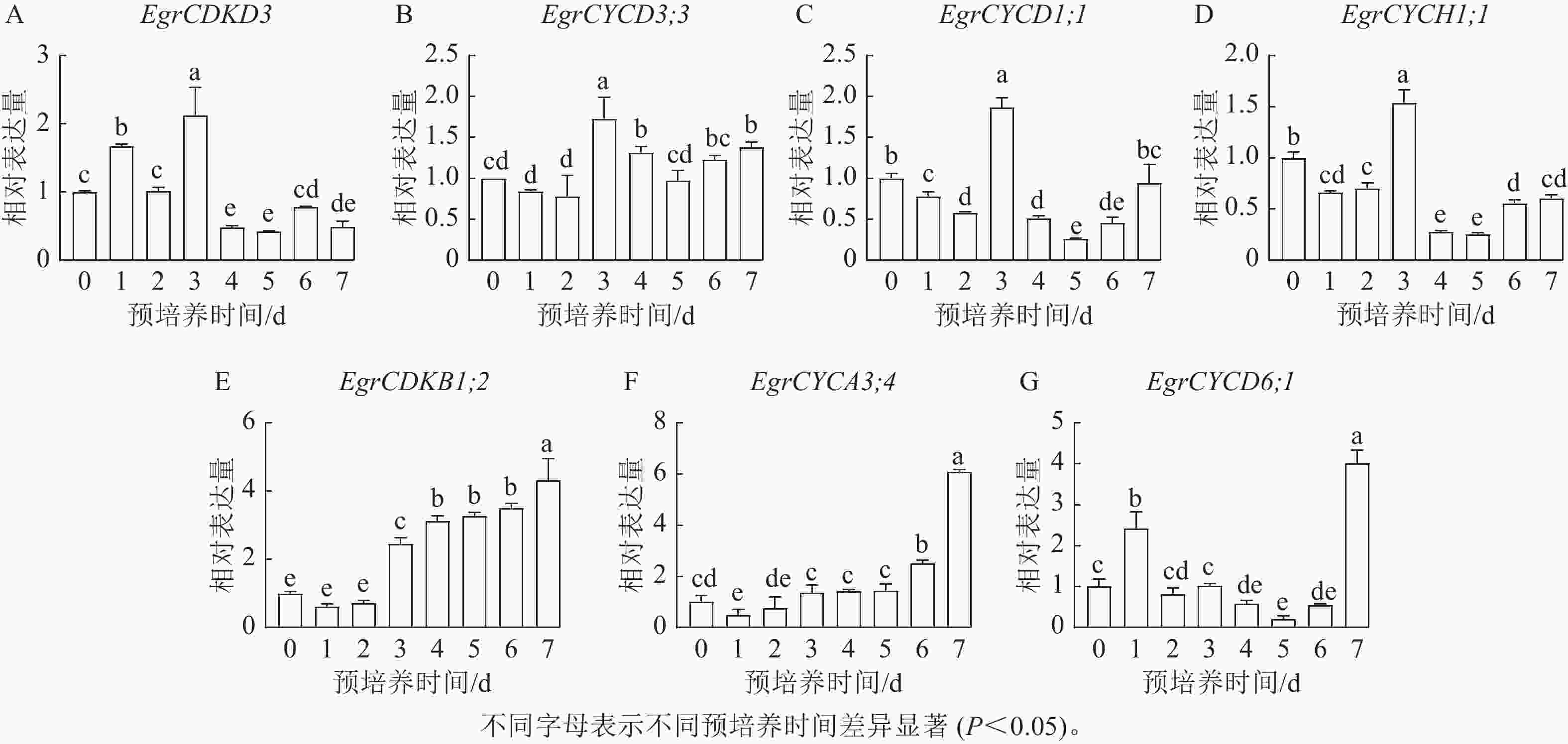
图5表明:细胞周期EgrCDKD3离体培养1 d时表达量升高,显著高于0 d (P< 0.05),2 d后迅速升高,但4 d后表达量降低。细胞周期EgrCYCD3;3和EgrCYCD1;1在0~2 d表达量逐渐递减,但在3 d时表达量显著升高后迅速下降(P<0.05),2 d时表达量升高,3 d时表达量最大,4 d时表达量迅速下降,之后表达量逐渐升高。S期关键基因EgrCDKD3、EgrCYCD3;3、EgrCYCD1;1和EgrCYCH1;1均在3 d时,表达量达到峰值,这与EdU染色结果一致。但EgrCDKB1;2、EgrCYCA3;4和EgrCYCD6;1在G2/M期发挥作用,在预培养7 d时,在桉树叶片中达到最高值。综上所述,尾巨桉DH32-29叶片离体预培养3~4 d为最佳遗传转化时间。
-
图6表明:随着预培养时间的延长,叶片逐渐卷曲,离体培养0~2 d的桉树叶片切口处湿润,切口处为绿色,整个叶片平整无皱缩;培养3 d后,叶片切口处开始变得干燥,且小部分切口转为红色;培养4 d后,尾巨桉叶片开始卷曲,且切口处干燥和起皱明显;5 d观察到少量愈伤组织形成;6~7 d愈伤组织大量出现。切口处干燥皱缩,几乎整个切口变为红色。因此,可推断当叶片切口开始干燥且变红时,是进行遗传转化的最佳处理时间。
-
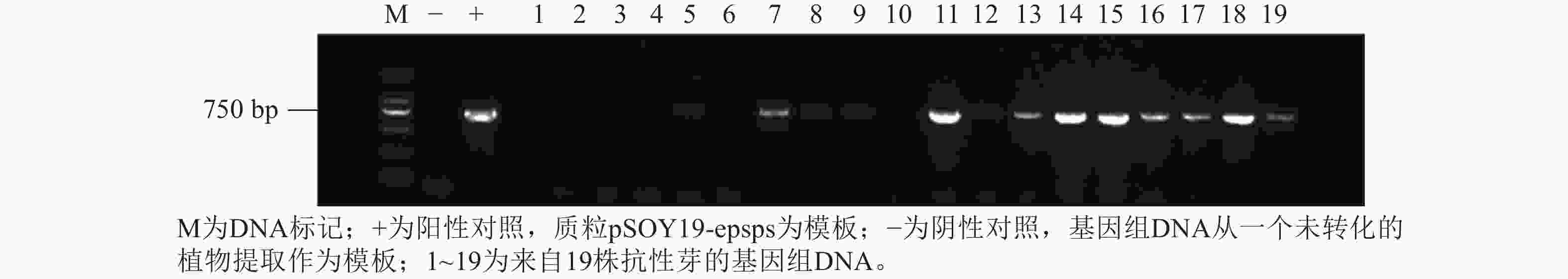
为了确定稳定的转化效率,通过农杆菌介导法将抗草甘膦基因G10-EPSPS转入尾巨桉DH32-29叶片中(图7),将含有G10-EPSPS基因的根癌农杆菌EHA105菌液(600 nm波长下的吸光度约0.4,农杆菌浓度为0.4),在4 ℃条件下以4 000 r·min−1离心10 min,弃上清后加入等体积重悬液重新悬浮菌体。将叶片置于重悬菌液中振荡侵染30 min,取出后用无菌滤纸吸干表面菌液,随后转移至共培养基中进行共培养。分别提取野生型植株和抗性植株的DNA,并用特异性引物对G10-EPSPS进行PCR扩增。结果表明:G10-EPSPS基因成功转入到桉树中,最高转化效率达4.67%。
-
本研究确定预培养3 d时S期细胞最多,最高转化效率为4.67%,是前期报道的尾巨桉DH32-29[20]转化效率的6倍。
农杆菌转化法因具有遗传稳定性高、嵌合体少等优势,在桉树研究中得到了广泛应用,但在桉树转基因过程中存在的转化效率低、稳定性差等问题,极大地制约了桉树转基因育种工作的开展。高效的遗传转化体系建立是桉树转基因育种的基础,因此进一步提高遗传转化效率变得尤其重要[21]。活跃分裂的细胞即细胞分裂的S期最容易通过农杆菌进行遗传转化[22],在此期间细胞对农杆菌转化十分敏感,预培养处理有助于植物获得更高的转化效率[10]。在进行遗传转化时,预培养可以促进植物细胞的分裂,使代谢活跃,让细胞更容易融合外源DNA,进而提高转化效率,不同的预培养时间对外植体的转化效率有着一定的影响[23]。
本研究发现:外植体叶片出现逐渐卷曲,切口处从绿色湿润转变完红色干燥,后期有透明愈伤组织形成,与杨树和烟草中的报道相似[14]。流式细胞仪检测结果显示:S期细胞在处理5 d时比例最高,为26.88%,而此时,G2/M期细胞占比为56.12%,G1期细胞为17.00%,处理3 d的S期细胞次之。EdU染色和荧光定量结果显示:预培养3 d的S期细胞较多,且大多集中于叶脉切口附近。这与流式细胞仪的结果有所不同,可能与外植体状态有关。
预培养时间与物种以及外植体类型有关,不同植物种类、同一物种内的不同基因型、同一物种的不同外植体以及外植体的不同发育阶段对转化效率影响很大,培养外植体可以提高遗传转化率达到合适的细胞发育状态。杜仲Eucommia ulmoides在预培养5 d时,GUS瞬时转化效率最高[23],杜鹃Rhododendron simsii预培养0 d最为合适[24],番茄Solanum lycopersicum预培养3 d时遗传转化效率最高,而在之前的研究中,番茄大多预培养2 d,但转化效率未高于预培养0 d[25−26]。在本研究中,尾巨桉DH32-29预培养3 d时遗传转化效率最高。不同物种的研究结果不同,这可能是外植体发育状态不一致导致的,但稳定遗传转化效率的预培养处理时间为1~3 d,这与外植体最佳培养时间为1~4 d的结论相符合[27]。对大麦Hordeum vulgare进行遗传转化时,培养1 d的转化率高于未培养的,1 d后转化率急剧下降[28]。在杨树中,以叶片作为外植体进行转化时,其预培养3 d的遗传转化效率最高,而以茎段为外植体进行遗传转化时,预培养4 d的遗传转化效率最高[21]。在以烟草叶片为外植体进行遗传转化时,预培养5 d的遗传转化效率最高[21]。在流式细胞仪检测结果中,预培养5 d比3 d的S期细胞占比稍高,这可能是由于植物材料的影响。此外,流式细胞仪检测时,细胞孵育时间的长短均会在一定程度上影响研究结果。
本研究在构建的尾巨桉DH32-29遗传转化体系[20]基础上进一步优化,但影响遗传转化效率的多种因素仍未被研究,通过探索更多的影响因素有望获得更高效与稳定的转化体系。后期需进一步优化尾巨桉DH32-29的遗传转化方式,从而加快尾巨桉DH32-29转基因良种的培育过程。
-
本研究优化了尾巨桉DH32-29的转化体系,通过GUS染色确定预培养0~3 d时的转化效率相对较高,流式细胞仪、EdU染色以及RT-qPCR确定预培养3 d为最佳处理时间。利用优化后的体系,将G10-EPSPS基因成功转入桉树中,使遗传转化效率由不足1.00%提高至4.67%。
Effect of preculture on genetic transformation efficiency of Eucalyptus urophylla × E. grandis DH32-29
-
摘要:
目的 为获得稳定、高效的遗传转化效率,得到大量转基因株系和创制优良品种,研究不同预培养时间对尾巨桉Eucalyptus urophylla × E. grandis DH32-29遗传转化的影响。 方法 尝试精细化调整不同预培养时间,通过5-乙炔基-2'-脱氧尿苷(EdU)染色和流式细胞仪检测DNA合成期(S期)细胞周期的细胞数量,采用实时荧光定量PCR (RT-qPCR)检测S期相关基因EgrCDKD3、EgrCYCD3;3、EgrCYCD1;1和EgrCYCH1;1的表达量,确定尾巨桉DH32-29稳定遗传转化的最佳处理时间。 结果 外植体叶片不同的预培养时间影响了尾巨桉DH32-29叶片的瞬时转化效率和稳定转化效率。预培养3 d时,外植体S期细胞数量占比最高,S期关键基因EgrCDKD3、EgrCYCD3;3、EgrCYCD1;1和EgrCYCH1;1表达量达到峰值,表明预培养3 d时,外植体适宜进行农杆菌Agrobacterium tumefaciens的浸染。稳定转化表明:预培养3 d能够大幅度提高农杆菌介导的桉树遗传转化效率,将最初转化效率从0.77%提高至4.67%。 结论 预培养对于农杆菌介导的桉树遗传转化效率至关重要,经过3 d预培养可有效提高桉树的遗传转化效率。图7表1参28 Abstract:Objective To obtain a stable and efficient genetic transformation rate, generate a large number of transgenic lines, and create improved varieties, the effects of different preculture treatment durations on genetic transformation of Eucalyptus urophylla × E. grandis DH32-29 were studied. Method This study aimed to fine-tune different preculture durations to determine the optimal timing for stable genetic transformation of E. urophylla × E. grandis DH32-29, 5-ethynyl-2'-deoxyuridine (EdU) staining and flow cytometry were used to quantify the proportion of cells in the DNA synthesis (S) phase of the cell cycle, and RT-qPCR was used to measure the expression levels of S phase-related genes EgrCDKD3, EgrCYCD3;3, EgrCYCD1;1, and EgrCYCH1;1. Result The duration of preculture of leaf explants significantly affected both the transient and stable transformation efficiency of E. urophylla × E. grandis DH32-29. After 3 days of preculture, the proportion of explant cells in the S phase was the highest, and the expression levels of key S-phase genes EgrCDKD3, EgrCYCD3;3, EgrCYCD1;1, and EgrCYCH1;1 peaked, indicating that explants precultured for 3 days are optimal for Agrobacterium tumefaciens infection. Further stable transformation assays demonstrated that a 3-day preculture substantially improved the efficiency of Agrobacterium-mediated genetic transformation in eucalyptus, increasing the transformation efficiency from 0.77% to 4.67%. Conclusion Preculture is crucial for the efficiency of Agrobacterium-mediated genetic transformation in eucalyptus. A 3-day preculture period can effectively enhance the genetic transformation efficiency of eucalyptus. [Ch, 7 fig. 1 tab. 28 ref.] -
Key words:
- Eucalyptus urophylla × E. grandis /
- transformation efficiency /
- flow cytometry /
- EdU staining /
- cell cycle /
- preculture
-
表 1 特异性引物
Table 1. Specific primer
引物 碱基序列(5'→3') EgrCDKD3-F GCTCGGTGAGGGTACGTATG EgrCDKD3-R GCAGGTTCCCTTTGTGAGGA EgrCYCD3;3-F CCTCCGCGAGATAAAGGACC EgrCYCD3;3-R ACGGCCAACATAGCAGTCAA EgrCYCD1;1-F TGCGATGGGCTAAGCAAAGA EgrCYCD1;1-R ACGATGGCGATAACGAGGAC EgrCYCH1;1-F CGGATTTCCAGAGCTCGACG EgrCYCH1;1-R TGGACGGGAATGCTTGTCAT EgrCDKB1;2-F CTATTCGATCGGCGTGGACA EgrCDKB1;2-R GGTAACTCCTGGCCATTGCT EgrCYCD6;1-F GCTCGGTGAGGGTACGTATG EgrCYCD6;1-R GCAGGTTCCCTTTGTGAGGA EgrCYCA3;4-F TGCTCAAGAAGGTCACAAGACTA EgrCYCA3;4-R GTGAGTTCTTGGTTGCGTGAT -
[1] 王豁然. 桉树生物学概论[M]. 北京: 科学出版社, 2010. WANG Huoran. A Chinese Appreciation of Eucalypts[M]. Beijing: Science Press, 2010. [2] 黄六贴. 桉树主要病虫害及防治措施[J]. 现代农业科技, 2022(6): 80−81. HUANG Liutie. Main diseases and insect pests of Eucalyptus and their control measures[J]. Modern Agricultural Science and Technology, 2022(6): 80−81. DOI: 10.3969/j.issn.1007-5739.2022.06.025. [3] DAI Ying, HU Guojian, DUPAS A, et al. Implementing the CRISPR/Cas9 technology in Eucalyptus hairy roots using wood-related genes[J]. International Journal of Molecular Sciences, 2020, 21(10): 3408. DOI: 10.3390/ijms21103408. [4] FEUILLET C, LAUVERGEAT V, DESWARTE C, et al. Tissue- and cell-specific expression of a cinnamyl alcohol dehydrogenase promoter in transgenic poplar plants[J]. Plant Molecular Biology, 1995, 27(4): 651−667. DOI: 10.1007/bf00020220. [5] 陈健波, 项东云, 张建明, 等. 广西耐寒桉树育种研究现状与对策[J]. 广西林业科学, 2003, 32(1): 7−11. CHEN Jianbo, XIANG Dongyun, ZHANG Jianming, et al. The present status of studies on cold tolerant Eucalyptus selection in Guangxi, China[J]. Guangxi Forestry Science, 2003, 32(1): 7−11. DOI: 10.19692/j.cnki.gfs.2003.01.002. [6] 袁滔. 广西尾巨桉DH系列无性系育苗技术[J]. 南方农业, 2023, 17(15): 266−269. YUAN Tao. DH series clone seedling breeding technology of Eucalyptus urophglla × E. grandis in Guangxi Province[J]. South China Agriculture, 2023, 17(15): 266−269. DOI: 10.19415/j.cnki.1673-890x.2023.15.064. [7] ALIU E, LEE K, WANG Kan. CRISPR RNA-guided integrase enables high-efficiency targeted genome engineering in Agrobacterium tumefaciens[J]. Plant Biotechnology Journal, 2022, 20(10): 1916−1927. DOI: 10.1111/pbi.13872. [8] 徐成成, 刘锦, 吴恩, 等. 基于组织培养的木本植物器官发生型再生研究进展[J/OL]. 浙江农林大学学报, 2025-11-26. https://link.cnki.net/urlid/33.1370.S.20251126.1125.002. XU Chengcheng, LIU Jin, WU En, et al. Advances in organogenesis regeneration of woody plants based on tissue culture[J/OL]. Journal of Zhejiang A&F University, 2025-11-26. https://link.cnki.net/urlid/33.1370.S.20251126.1125.002. [9] WANG Haihai, WANG Cuiting, LIU Hua, et al. An efficient Agrobacterium-mediated transformation and regeneration system for leaf explants of two elite aspen hybrid clones Populus alba × P. berolinensis and Populus davidiana × P. bolleana[J]. Plant Cell Reports, 2011, 30(11): 2037−2044. DOI: 10.1007/s00299-011-1111-1. [10] 唐靖雯, 王宁, 伍程程, 等. 白花玉石籽石榴遗传转化体系的建立[J]. 果树学报, 2024, 41(12): 2621−2633. TANG Jingwen, WANG Ning, WU Chengcheng, et al. Establishment of genetic transformation system for Baihuayushizi pomegranate[J]. Journal of Fruit Science, 2024, 41(12): 2621−2633. DOI: 10.13925/j.cnki.gsxb.20240326. [11] JACQ B, LESOBRE O, SANGWAN R, et al. Factors influencing T-DNA transfer in Agrobacterium-mediated transformation of sugarbeet[J]. Plant Cell Reports, 1993, 12(11): 621−624. DOI: 10.1007/bf00232811. [12] WEN Shuangshuang, GE Xiaolan, WANG Rui, et al. An efficient Agrobacterium-mediated transformation method for hybrid poplar 84K (Populus alba × P. glandulosa) using calli as explants[J]. International Journal of Molecular Sciences, 2022, 23(4): 2216. DOI: 10.3390/ijms23042216. [13] 甘珊珊, 王静毅, 程运江, 等. 香蕉遗传转化体系优化[J]. 热带农业科学, 2024, 44(10): 17−24. GAN Shanshan, WANG Jingyi, CHENG Yunjiang, et al. Optimization of the banana genetic transformation system[J]. Chinese Journal of Tropical Agriculture, 2024, 44(10): 17−24. [14] HAN Xue, MA Shurong, KONG Xianghui, et al. Efficient Agrobacterium-mediated transformation of hybrid poplar Populus davidiana Dode × Populus bollena Lauche[J]. International Journal of Molecular Sciences, 2013, 14(2): 2515−2528. DOI: 10.3390/ijms14022515. [15] XIA Yufei, CAO Yuan, REN Yongyu, et al. Effect of a suitable treatment period on the genetic transformation efficiency of the plant leaf disc method[J]. Plant Methods, 2023, 19: 15. DOI: 10.1186/s13007-023-00994-3. [16] LIVAK K J, SCHMITTGEN T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2–ΔΔCt method[J]. Methods, 2001, 25(4): 402−408. DOI: 10.1006/meth.2001.1262. [17] DEININGER P. Gus protocols: using the gus gene as a reporter of gene expression[J]. Analytical Biochemistry, 1992, 207(2): 356. DOI: 10.1016/0003-2697(92)90027-5. [18] 薛薇. 基于SPSS的数据分析[M]. 北京: 中国人民大学出版社, 2006. XUE Wei. Data Analysis based on SPSS[M]. Beijing: China Renmin University Press, 2006. [19] CAVANAGH B L, WALKER T, NORAZIT A, et al. Thymidine analogues for tracking DNA synthesis[J]. Molecules, 2011, 16(9): 7980−7993. DOI: 10.3390/molecules16097980. [20] WANG Xiaoping, CHEN Shanshan, ZHANG Haonan, et al. Agrobacterium-mediated genetic transformation of the most widely cultivated superior clone Eucalyptus urophylla × Eucalyptus grandis DH32-29 in southern China[J]. Frontiers in Plant Science, 2022, 13: 1011245. DOI: 10.3389/fpls.2022.1011245. [21] 陈珊珊. 尾巨桉DH32-29不定芽再生机制及遗传转化体系优化的研究[D]. 哈尔滨: 东北林业大学, 2023. CHEN Shanshan. Study on the Mechanism of in vitro Shoot Regeneration and Optimization of Genetic Transformation System in Eucalyptus grandis × E. urophylla[D]. Harbin: Northeast Forestry University, 2023. DOI: 10.27009/d.cnki.gdblu.2023.001039. [22] 陈梅, 陈露倩, 陈思, 等. 农杆菌介导的黄瓜遗传转化体系优化研究[J]. 四川农业大学学报, 2024, 42(3): 540−545, 571. CHEN Mei, CHEN Luqian, CHEN Si, et al. Optimization of the genetic transformation system of cucumber mediated by Agrobacterium tumefaciens[J]. Journal of Sichuan Agricultural University, 2024, 42(3): 540−545, 571. DOI: 10.16036/j.issn.1000-2650.202310365. [23] 刘闵豪, 徐郡儡, 叶靖, 等. 农杆菌介导的杜仲叶片愈伤组织遗传转化体系[J]. 林业科学, 2020, 56(2): 79−88. LIU Minhao, XU Junlei, YE Jing, et al. Agrobacterium tumefaciens-mediated transformation of leaf callus in Eucommia ulmoides[J]. Scientia Silvae Sinicae, 2020, 56(2): 79−88. DOI: 10.11707/j.1001-7488.20200209. [24] LONG Fenfang, ZUO Weiwei, LI Huie, et al. Genetic transformation of Rhododendron delavayi for anthocyanin synthesis using Agrobacterium-mediated transformation[J]. Plant Cell, Tissue and Organ Culture (PCTOC), 2024, 157(2): 47. DOI: 10.1007/s11240-024-02775-9. [25] 邱实, 张文举, 许馥慧, 等. Micro-Tom番茄转基因植株再生体系的优化[J]. 上海大学学报(自然科学版), 2018, 24(2): 322−330. QIU Shi, ZHANG Wenju, XU Fuhui, et al. System optimization for tomato Micro-Tom transgenic regeneration[J]. Journal of Shanghai University (Natural Science Edition), 2018, 24(2): 322−330. DOI: 10.12066/j.issn.1007-2861.1773. [26] 张杨, 诸燕, 韩之刚, 等. 过表达紫花苜蓿ChOMT基因创制高异黄酮营养强化番茄[J]. 浙江农林大学学报, 2026, 43(2): 303−309. ZHANG Yang, ZHU Yan, HAN Zhigang, et al. Overexpression of Medicago sativa ChOMT gene in constructing homoisoflavone-enriched tomatoes[J]. Journal of Zhejiang A&F University, 2026, 43(2): 303−309. DOI: 10.11833/j.issn.2095-0756.20250186. [27] HUSAINI A M. Pre- and post-agroinfection strategies for efficient leaf disk transformation and regeneration of transgenic strawberry plants[J]. Plant Cell Reports, 2010, 29(1): 97−110. DOI: 10.1007/s00299-009-0801-4. [28] ISMAGUL A, MAZONKA I, CALLEGARI C, et al. Agrobacterium-mediated transformation of barley (Hordeum vulgare L.)[M]//FLEURY D, WHITFORD R. Crop Breeding. Methods in Molecular Biology, vol 1145. New York: Humana Press, 2014: 203−211. DOI:10.1007/978-1-4939-0446-4_16. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20250347







 下载:
下载: