-
君迁子Diospyros lotus果实又名黑枣、软枣,为柿科Ebenaceae柿属Diospyros落叶乔木,分为有核和无核2个大类[1-2]。无核君迁子果实可食率高,硬熟期果皮呈浅黄色,软熟期果皮呈黄褐色,后呈黑色,主要分布在河南、河北、山东、陕西、山西等中西部地区,具有肉厚味甜、风味独特、质地细嫩、果汁少、口感好、耐储藏运输等优良特性[2-3],鲜果富含维生素C、维生素A、碘、果胶、膳食纤维等[4]。黑枣具有止渴,去烦热,令人润泽等功效,为“五黑固肾粥”的主要配方之一[5-6]。因此,无核君迁子为药食同源果品,除鲜食外,可加工成枣面、黑枣酒、黑枣醋等,开发价值高,市场潜力巨大。
果实质地、糖含量、糖酸比和黄酮、酚类、单宁等活性物质,是果实内在品质的重要组成部分,对果实的鲜食和加工品质均有重要影响[7-9]。其中,质地变软是果实发育成熟最明显的标志,是果实采收和品质评价的重要指标[10]。无核君迁子果实因其独特的风味和食疗保健价值而深受消费者喜爱,但目前关于无核君迁子的研究主要集中在栽培技术、粗加工技术等方面[11-13],关于发育成熟软化过程中生理指标变化规律的研究尚未见报道。
本研究以不同时期无核君迁子果实为研究对象,测定其单宁、黄酮、总酚、花青素、糖、果胶组分以及果胶降解酶活性,从果实发育、成熟、软化全过程对果实内在品质变化进行了系统研究,并对其相关性进行分析,以期为无核君迁子果实的深入开发利用提供参考。
-
试验材料为中国林业科学研究院经济林研究所选育的‘无核1号’ ‘Wuhe 1’果实,试验基地位于河南省新乡市原阳县原武镇靳屋村(34°55′30″~34°56′45″N,113°46′24″~113°47′59″E)。选择树势健壮、无病虫害的无性系单株10株,从花后约5周至花后27周的6个时期,即2020年6月15日(幼果期)、7月15日(膨大期)、8月15日(青果期)、9月15日(转色期)、10月15日(初熟期)和11月15日(软熟期),在树冠中部外围,按东、南、西、北4个方向采样,每个方向采集果实5个,混合均匀后低温冷藏带回实验室,冰水冲洗后用纱布吸干表面水分,切碎经液氮速冻于−80 ℃超低温冰箱中保存,用于相关指标测定。
-
可溶性单宁和不溶性单宁测定采用Folin-Ciocalteu法,参考余轩[14]的方法,以单宁酸为标准品,测定725 nm处的吸光度。
-
总酚测定采用Folin-Ciocalteu法[15],以没食子酸为标准品,测定760 nm处的吸光度;黄酮测定采用三氯化铝(醋酸-醋酸钠)显色法测定[15],以芦丁为标准品,测定400 nm处的吸光度;花青素测定采用曹建康等[16]的方法,以530 nm处的吸光度D(530)和600 nm处的吸光度D(600)的差值D花青素表示花青素含量。
-
淀粉采用蒽酮比色法测定[16],以葡萄糖为标准品,测定620 nm处的吸光度。糖组分的提取方法参照杜改改等[17]的方法并稍作改进。精密称取试验材料中无核君迁子果肉1.000 g,5 mL蒸馏水沸水提取30 min,冰水中冷却后10 000 g离心20 min,收集上清液。在滤渣中再次准确加入5 mL蒸馏水,重复提取1次,合并2次上清液,0.45 μm微孔滤膜过滤后上机测定。糖组分检测参照GB 5009.8—2016《食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖的测定》,色谱柱为CNW Athena NH2-RP(4.6 mm×250.0 mm,5 µm),柱温为40 ℃,流动相为体积分数75%的乙腈水溶液,流速为1.0 mL·min−1,检测器为Waters 2414示差折光检测器,根据峰面积和标准曲线计算果糖、葡萄糖、蔗糖的质量分数。可滴定酸采用酸碱滴定法[16]测定。糖酸比由可溶性糖质量分数与可滴定酸质量分数的比值计算。
-
参考齐秀东等[10]的方法,进行水溶性果胶、离子结合果胶、共价结合果胶的提取,以半乳糖醛酸为标准,用咔唑比色法测定各果胶组分。
多聚半乳糖醛酸酶的提取和测定参考REN等[18]的方法并加以改进,多聚半乳糖醛酸酶活性以每小时每克样品在37 ℃催化半乳糖醛酸水解生成半乳糖醛酸的质量表示,单位为mg·g−1·h−1;果胶裂解酶的提取和测定参考ZHI等[19]的方法并加以改进,果胶裂解酶活性定义为每克组织每分钟分解果胶产生1 nmol不饱和半乳糖醛酸所需的酶量为1个酶活力单位,单位为16.67 nkat·g−1·min−1。
-
利用Excel软件计算各指标的平均值、标准差、线性回归方程等;利用SPSS 20.0进行方差分析、Duncan多重比较(显著性水平为0.05)、Pearson相关性分析,利用Excel和GraphPad Prism 6作图。
-
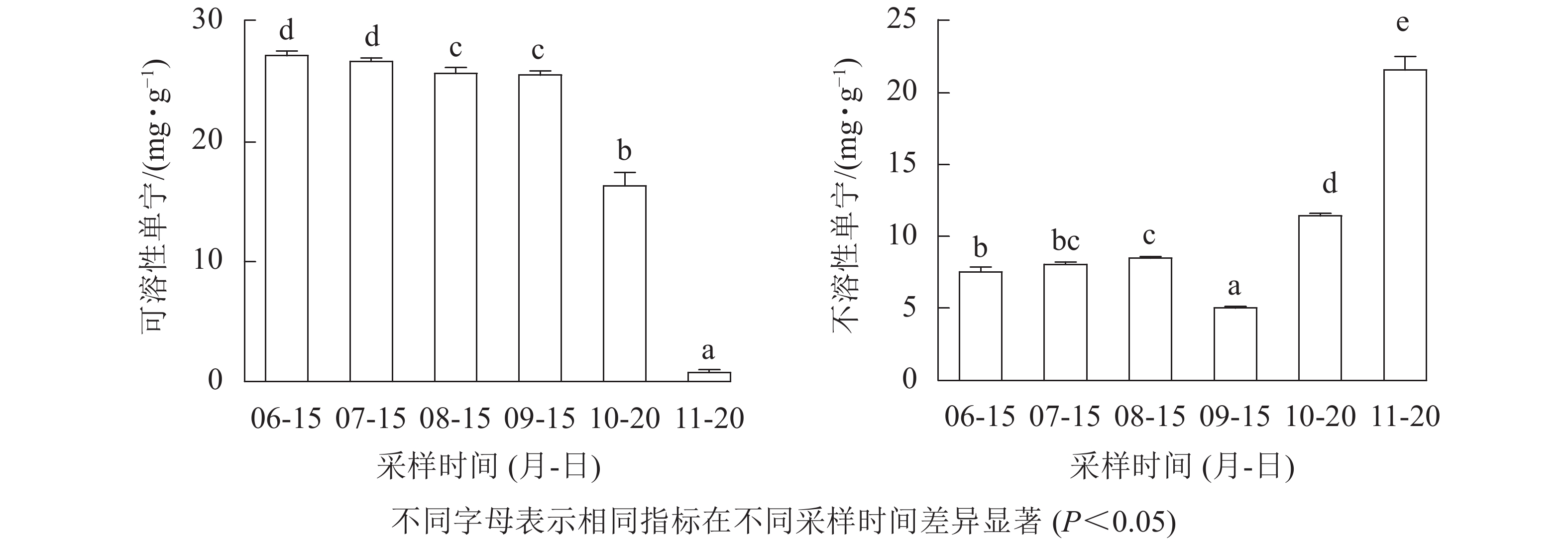
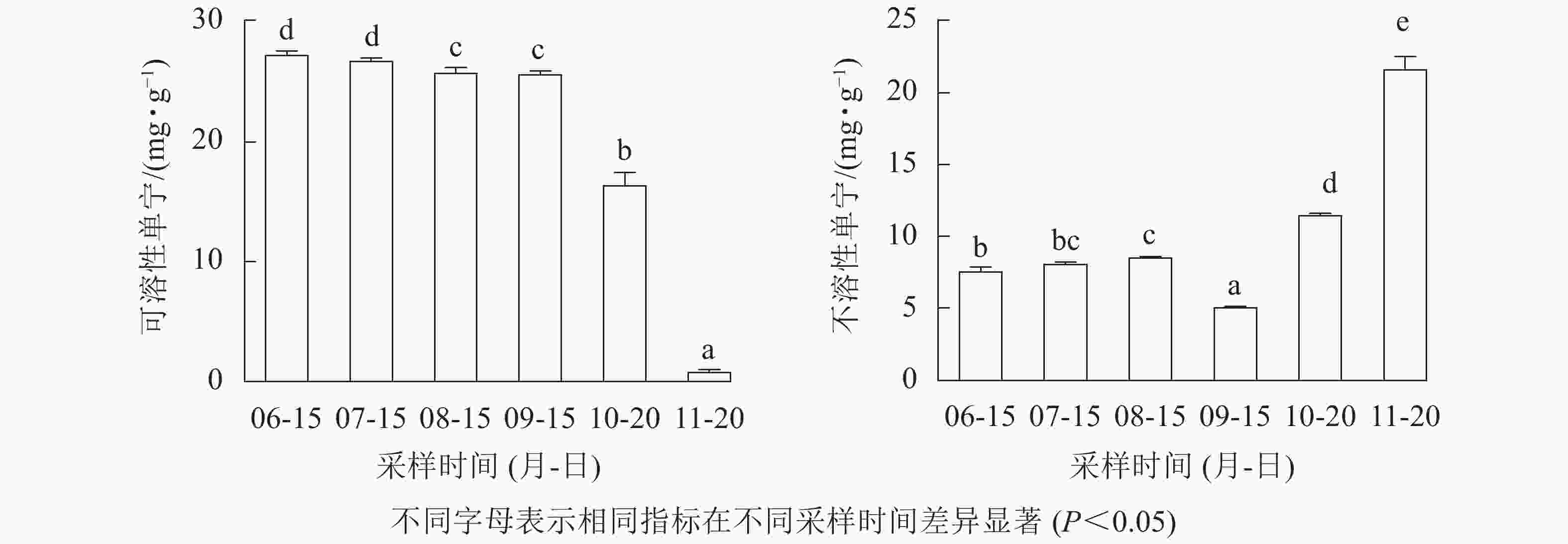
如图1所示:无核君迁子果实发育成熟过程中可溶性单宁质量分数随着果实的发育成熟不断降低,果实软熟期降至(0.75±0.23) mg·g−1,低于可食用阈值(2.00 mg·g−1)[20],口尝无涩味;不溶性单宁质量分数随着果实成熟过程逐渐上升,软熟期上升至(21.63±0.94) mg·g−1,这可能与果实脱涩过程中可溶性单宁向不溶性单宁的转化有关[21]。
-
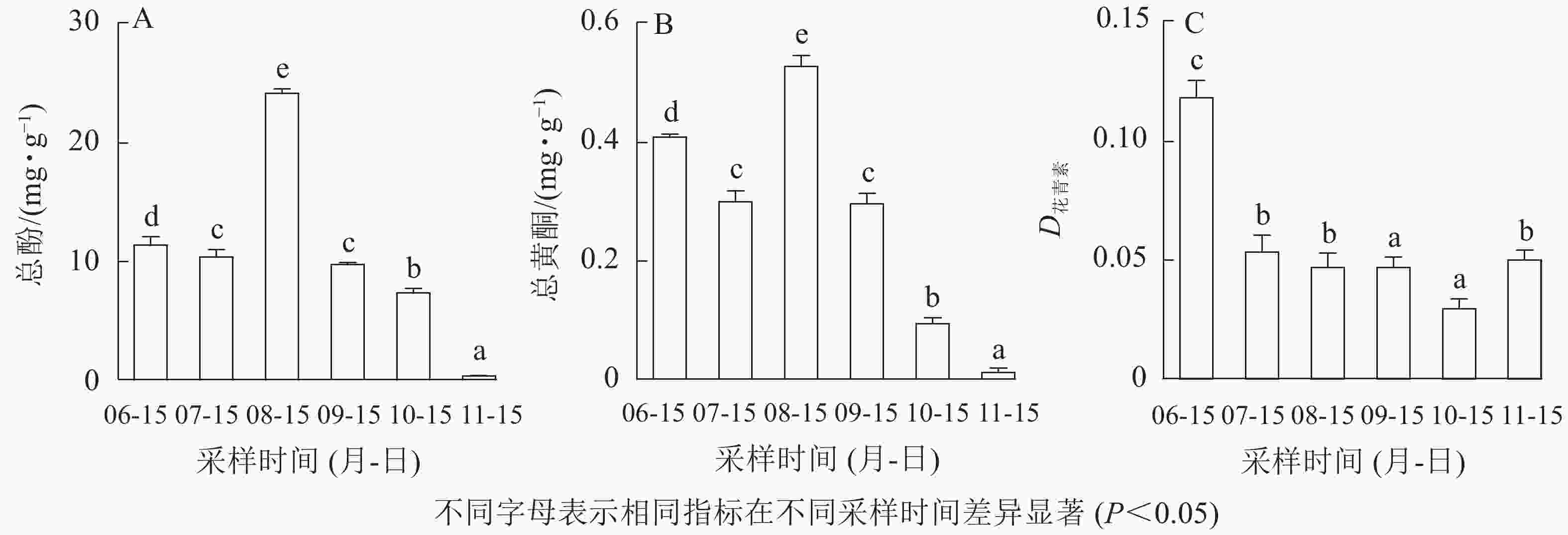
如图2A和图2B所示:无核君迁子果实在幼果期和膨大期,果实中黄酮和酚类物质质量分数较低,8月中旬青果期最高,后随着果实的成熟软化逐渐降低。花青素如图2C所示:幼果期最高,初熟期最低,其他时期花青素无显著性差异。
-
由表1可知:无核君迁子果实发育成熟过程中淀粉逐渐积累,呈显著上升趋势(P<0.05),果实软熟期淀粉质量分数高达 (56.70±3.60) mg·g−1。无核君迁子果实中果糖和葡萄糖质量分数呈相似的增加趋势,在6—7月,葡萄糖质量分数高于果糖,8月后果糖质量分数高于葡萄糖。根据甜度值计算方法,定义蔗糖甜度为100,则果糖为175,葡萄糖为75[22]。由此可知,8月后由于果糖质量分数增加且超过葡萄糖,无核君迁子果实甜度呈增加的趋势。蔗糖在7月中旬后的样品中未检出,无核君迁子果实可溶性糖以葡萄糖和果糖为主,因此其糖积累类型为己糖积累型。无核君迁子可滴定酸呈先升后降的变化趋势,在7月中旬达到峰值后随着果实成熟度的增加而下降,导致酸味显著降低。糖酸比呈逐渐上升的变化趋势,糖酸比越高果实甜度越大,说明果实甜味随着发育成熟逐渐增加。
表 1 淀粉、可溶性糖、可滴定酸和糖酸比在果实发育成熟过程中的变化
Table 1. Changes of soluble starch, soluble sugar, titratable acid and sugar-acid ratio during fruit development and ripening
采样时间(月-日) 淀粉/(mg·g−1) 果糖/(mg·g−1) 葡萄糖/(mg·g−1) 蔗糖/(mg·g−1) 可滴定酸/(mg·g−1) 糖酸比 06-15 9.48±0.79 a 9.85±0.34 a 17.25±0.40 a 8.09±0.17 5.05±0.05 e 6.96±0.16 a 07-15 12.27±0.91 ab 11.58±0.53 a 17.68±0.10 a 16.01±0.14 6.05±0.37 d 7.49±0.36 a 08-15 13.74±0.31 b 37.59±0.45 b 33.58±0.56 b − 4.43±0.23 c 16.08±0.80 b 09-15 20.77±1.45 c 60.34±2.41 c 46.63±2.07 c − 4.13±0.17 bc 25.97±1.73 c 10-15 24.90±0.20 d 95.30±2.62 d 78.42±2.53 d − 3.85±0.18 ab 45.22±3.23 d 11-15 56.70±3.60 e 151.85±5.61 e 132.88±4.65 e − 3.54±0.16 a 80.43±3.64 e 说明:同列不同的字母表示差异显著(P<0.05)。−表示未检出 -
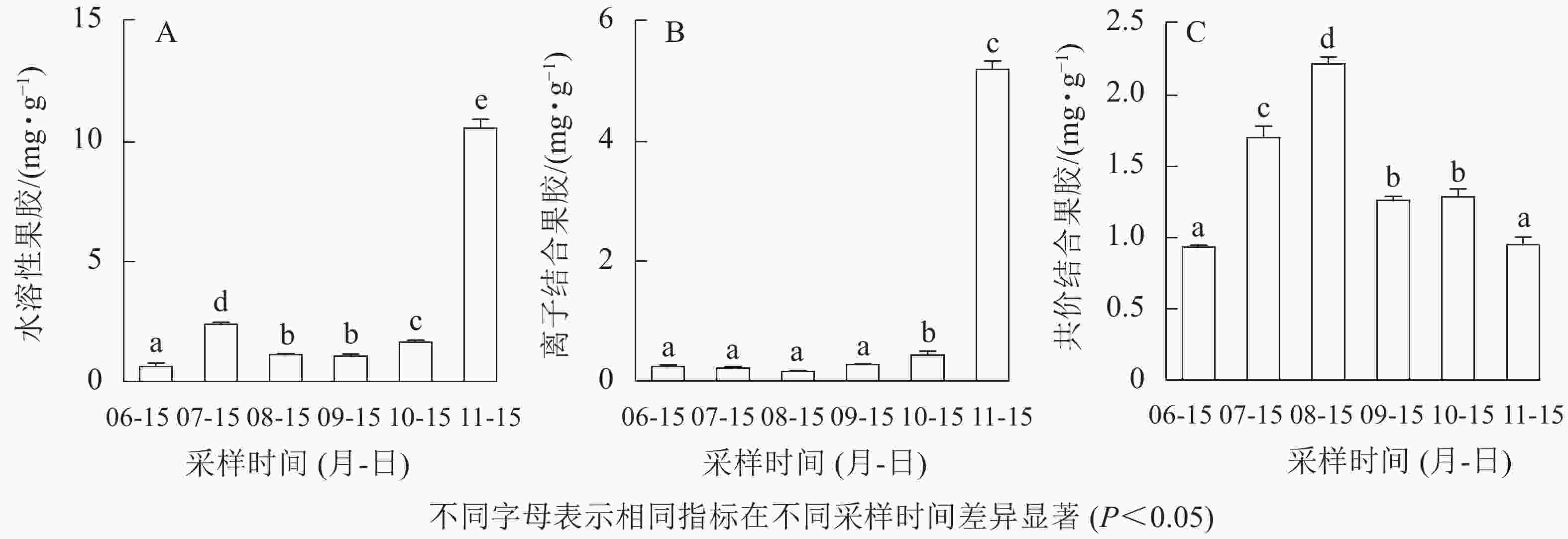
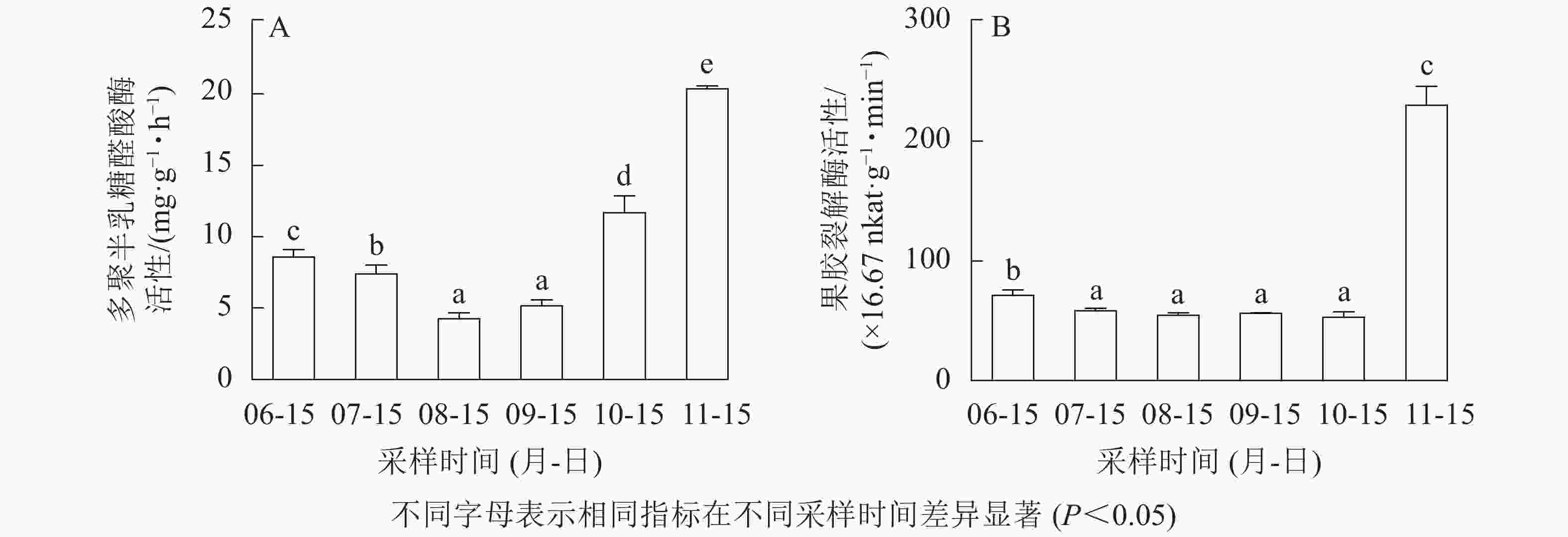
无核君迁子果实发育成熟过程中水溶性果胶和离子结合果胶质量分数呈上升的变化趋势(图3A和图3B),均在果实软熟期质量分数最高,分别为(10.59±0.39)、(5.21±0.13) mg·g−1。由图3C可知:共价结合果胶质量分数呈先上升后下降的变化趋势,果实软熟期则显著下降(P<0.05)。如图4所示:无核君迁子果实发育成熟期间多聚半乳糖醛酸酶活性在6—8月逐渐下降,8月后活性逐渐上升,在果实软熟期活性最高,为(20.39±0.18) mg·g−1·h−1;果胶裂解酶活性在果实软熟期显著升高(P<0.05),为(230.48±15.59)×16.67 nkat·g−1·min−1。
-
相关性分析(表2)表明:无核君迁子果实发育成熟过程中,可溶性单宁与总酚、黄酮和可滴定酸呈极显著正相关(P<0.01),与不溶性单宁、淀粉、果糖、葡萄糖、糖酸比、水溶性果胶、离子结合果胶以及多聚半乳糖醛酸酶、果胶裂解酶活性呈极显著负相关(P<0.01),说明无核君迁子可溶性单宁在果实发育成熟过程中逐渐转化为不溶性单宁,其转化过程可能与糖组分和细胞壁组分的变化有关。总酚、黄酮与不溶性单宁、淀粉、果糖、葡萄糖、糖酸比、水溶性果胶、离子结合果胶以及多聚半乳糖醛酸酶、果胶裂解酶活性呈极显著负相关(P<0.01),与可溶性单宁、共价结合果胶呈极显著正相关(P<0.01);花青素与果糖呈显著负相关(P<0.05);淀粉、果糖、葡萄糖均与糖酸比、水溶性果胶、离子结合果胶及多聚半乳糖醛酸酶、果胶裂解酶活性呈极显著正相关(P<0.01),与可滴定酸呈极显著负相关(P<0.01),说明无核君迁子果实发育成熟过程中,在果胶降解酶的参与下,细胞壁果胶组分降解,进而导致果实软化、可溶性糖升高以及活性成分变化;随着果实的发育成熟,可溶性糖上升,可滴定酸下降,从而引起果实糖酸比逐渐上升,果实甜度增加。果实水溶性果胶与离子结合果胶呈极显著正相关(P<0.01),水溶性果胶和离子结合果胶均与多聚半乳糖醛酸酶、果胶裂解酶活性呈极显著正相关(P<0.01);共价结合果胶与多聚半乳糖醛酸酶、果胶裂解酶活性呈显著负相关(P<0.05);多聚半乳糖醛酸酶和果胶裂解酶活性呈极显著正相关(P<0.01),说明多聚半乳糖醛酸酶和果胶裂解酶参与了无核君迁子果实的软化过程,这与果胶降解、细胞壁结构解体有关。
表 2 无核君迁子果实发育成熟过程中各指标的Pearson相关性分析
Table 2. Pearson correlation coefficients analysis of seedless D. lotus fruit
指标 可溶性单宁 不溶性单宁 总酚 黄酮 花青素 淀粉 果糖 葡萄糖 可溶性单宁 1 不溶性单宁 −0.963** 1 总酚 0.706** −0.615** 1 黄酮 0.837** −0.735** 0.908** 1 花青素 0.325 −0.215 0.065 0.406 1 淀粉 −0.973** 0.911** −0.709** −0.808** −0.348 1 果糖 −0.946** 0.841** −0.651** −0.834** −0.500* 0.951** 1 葡萄糖 −0.975** 0.893** −0.679** −0.843** −0.439 0.972** 0.994** 1 可滴定酸 0.666** −0.527* 0.310 0.504* 0.384 −0.678** −0.826** −0.784** 糖酸比 −0.973** 0.892** −0.692** −0.848** −0.431 0.971** 0.991** 0.998** 水溶性果胶 −0.922** 0.941** −0.668** −0.708** −0.201 0.938** 0.803** 0.855** 离子结合果胶 −0.936** 0.942** −0.669** −0.696** −0.133 0.953** 0.831** 0.880** 共价结合果胶 0.453 −0.364 0.819** 0.605** −0.393 −0.453 −0.404 −0.432 多聚半乳糖醛酸酶 −0.941** 0.944** −0.807** −0.846** −0.098 0.891** 0.824** 0.877** 果胶裂解酶 −0.893** 0.920** −0.647** −0.636** −0.030 0.911** 0.765** 0.822** 指标 可滴定酸 糖酸比 水溶性果胶 离子结合果胶 共价结合果胶 多聚半乳糖
醛酸酶果胶裂解酶 可滴定酸 1 糖酸比 −0.784** 1 水溶性果胶 −0.437 0.859** 1 离子结合果胶 −0.524* 0.881** 0.986** 1 共价结合果胶 0.309 −0.443 −0.382 −0.459 1 多聚半乳糖醛酸酶 −0.492* 0.882** 0.896** 0.906** −0.611** 1 果胶裂解酶 −0.463 0.823** 0.969** 0.991** −0.480* 0.888** 1 说明:*表示P<0.05;**表示P<0.01 -
果实是植物储藏淀粉的重要器官之一。本研究表明:淀粉在无核君迁子果实生长发育期间逐渐积累,果实成熟后淀粉质量分数高达(56.70±3.60) mg·g−1。田娟等[23]对22份不同地区火棘Pyracantha果实淀粉质量分数的研究表明:仅有2份资源淀粉的质量分数高于(56.70±3.60) mg·g−1。由此可知:成熟的无核君迁子果实中淀粉质量分数较高,具有潜在的开发利用价值。可溶性糖是水果中的重要营养成分,其种类和构成比例在很大程度上影响果品的甜度和口感[24]。本研究表明:无核君迁子果实中以葡萄糖和果糖为主,糖积累类型为己糖积累型;葡萄糖在果实发育早期高于果糖,后期低于果糖,由于果糖甜度高于葡萄糖,这是果实成熟过程中甜度逐渐增加的主要原因。
多酚和黄酮是植物中广泛存在的次生代谢产物,具有抗氧化、抗衰老、提高免疫力等保健作用。无核君迁子果实总酚和黄酮质量分数在8月中旬最高,此时是提取多酚、黄酮类物质的最佳采收时期。花青素是一类生物活性极强的可溶性黄酮类物质,除具有防治心血管疾病、抗高血压、降血脂、降血糖、抗癌等活性[25-26]外,也是决定果实色泽的主要色素。本研究表明:无核君迁子花青素在果实发育初期最高,随后下降,果实软熟期略有回升,但决定无核君迁子发育过程中颜色变化的花青素种类和质量分数有待深入研究。
根据柿Diospyros kaki单宁在醇中溶解性的不同,分为可溶性单宁和不溶性单宁2类,柿果实涩味主要是由可溶性单宁引起的[27]。本研究表明:无核君迁子果实发育成熟过程中可溶性单宁不断下降,软熟期降至可食用阈值以下,同时也伴随着不溶性单宁逐渐上升的过程。有关涩柿脱涩单宁聚合的研究可归结为缩合学说和凝胶学说[28],胶凝学说认为可溶性单宁在脱涩过程中与果肉中的果胶、多糖发生胶凝反应,形成凝胶,涩味消失。本研究表明:可溶性单宁与不溶性单宁、淀粉、果糖、葡萄糖、水溶性果胶、离子结合果胶以及多聚半乳糖醛酸酶、果胶裂解酶活性呈极显著负相关(P<0.01),这说明无核君迁子果实脱涩过程不仅存在单宁缩合效应,还存在单宁缩合与凝胶综合作用。
果胶主要起着粘连细胞的作用,与果实质地密切相关[10]。研究表明:果胶在果实成熟之前呈不溶状态,随着果实成熟软化逐步降解,使果胶的平均分子质量和果胶多糖交联能力下降,细胞结构随之受损,导致果实软化[24]。而这些过程往往伴随着果胶降解酶,如多聚半乳糖醛酸酶和果胶裂解酶等的参与,它们通过降解果胶多糖组分,使细胞间连接减少,细胞离散而参与果实质地软化,且在果实软化的不同阶段起不同的作用[10]。本研究发现:水溶性果胶和离子结合果胶质量分数呈上升的变化趋势,共价结合果胶质量分数呈先上升后下降的变化趋势。齐秀东等[10]对秋子梨‘京白梨’ Pyrus ussuriensis ‘Jingbaili’发育软化与果胶的关系研究表明:水溶性果胶和离子结合果胶逐渐增加,而共价结合果胶先升后降;罗自生[29]对柿果实软化过程中细胞壁组分的研究表明:水溶性果胶质量分数逐渐增加。这些均与本研究结果一致。相关性分析表明:无核君迁子果实水溶性果胶、离子结合果胶与多聚半乳糖醛酸酶、果胶裂解酶活性呈极显著正相关(P<0.01),共价结合果胶与多聚半乳糖醛酸酶、果胶裂解酶活性呈显著负相关(P<0.05);淀粉、果糖、葡萄糖与水溶性果胶、离子结合果胶及多聚半乳糖醛酸酶、果胶裂解酶活性呈极显著正相关(P<0.01),说明多聚半乳糖醛酸酶、果胶裂解酶参与了细胞壁果胶组分降解,导致无核君迁子果实的软化和可溶性糖的升高。
无核君迁子与柿树嫁接成活率高,是中国北方的主要砧木树种,目前对君迁子的研究主要集中在嫁接适宜性及成活率方面,而忽略了其作为果树的经济价值,本研究对其果实资源的开发利用具有参考价值。
Variation patterns of physiological indices of seedless Diospyros lotus during fruit development and ripening
-
摘要:
目的 探讨无核君迁子Diospyros lotus果实发育成熟过程中生理指标的变化规律,为无核君迁子果实资源的进一步开发利用提供参考。 方法 以不同时期无核君迁子果实为材料,测定单宁、总酚、黄酮、花青素、糖和果胶组分以及果胶降解酶活性的变化规律,并分析其相关性。 结果 无核君迁子果实发育成熟过程中,可溶性单宁和花青素不断降低,不溶性单宁、淀粉、果糖、葡萄糖、糖酸比、水溶性果胶、离子结合果胶逐渐上升,总酚、黄酮、可滴定酸和共价结合果胶先升后降;多聚半乳糖醛酸酶和果胶裂解酶活性在果实软熟期显著上升(P<0.05)。相关性分析表明:水溶性果胶、离子结合果胶与多聚半乳糖醛酸酶、果胶裂解酶活性呈极显著正相关(P<0.01),共价结合果胶与多聚半乳糖醛酸酶、果胶裂解酶活性呈显著负相关(P<0.05),淀粉、果糖、葡萄糖与水溶性果胶、离子结合果胶及多聚半乳糖醛酸酶、果胶裂解酶活性呈极显著正相关(P<0.01)。 结论 无核君迁子果实发育成熟过程中,可溶性单宁逐渐下降至可食用阈值以下,多聚半乳糖醛酸酶和果胶裂解酶参与催化细胞壁果胶组分降解,进而引起无核君迁子果实果胶组分变化、可溶性糖升高以及活性成分变化。图4表2参29 Abstract:Objective This study, with an investigation of the variation patterns of physiological indices of seedless Diospyros lotus during fruit development and ripening, is aimed to provide a theoretical basis for the further utilization of such resources. Method With fruits of seedless D. lotus of different stages collected, a survey was conducted of the variation patterns of tannin, total polyphenols and flavonoids, anthocyanins, sugar and pectin composition, as well as the activity of pectin degrading enzyme before an analysis was conducted of the correlation. Result During the fruit development and ripening there was a constant decrease in the contents of soluble tannin and anthocyanin and a gradual increase in the contents of insoluble tannin, starch, fructose, glucose, sugar-acid ratio, water soluble pectin and ironic soluble pectin whereas there was first an increase and then a decrease in the contents of total polyphenols, flavonoids, titratable acids and covalent soluble pectin content. There was a significant increase in the activities of polygalacturonase and pectate lyase at the later stage of fruit ripening (P< 0.05). There was a significant positive correlation between the contents of water soluble pectin and ironic soluble pectin and the activities of polygalacturonase and pectate lyase (P<0.01), a significant negative correlation between the contents of covalent soluble pectin and the activities of polygalacturonase and pectate lyase (P< 0.05) and a significant positive correlation between the contents of starch, fructose and glucose and the contents of water soluble pectin, ironic soluble pectin as well as the activities of polygalacturonase and pectate lyase (P< 0.01). Conclusion During the development and ripening of seedless D. lotus, the content of soluble tannin gradually decreased to below the edibility threshold while polygalacturonase and pectate lyase enzymes were involved in the catalytic degradation of pectin components in the cell wall, which led to the change of pectin components, the increase of soluble sugar content and the change of active components in the fruit. [Ch, 4 fig. 2 tab. 29 ref.] -
表 1 淀粉、可溶性糖、可滴定酸和糖酸比在果实发育成熟过程中的变化
Table 1. Changes of soluble starch, soluble sugar, titratable acid and sugar-acid ratio during fruit development and ripening
采样时间(月-日) 淀粉/(mg·g−1) 果糖/(mg·g−1) 葡萄糖/(mg·g−1) 蔗糖/(mg·g−1) 可滴定酸/(mg·g−1) 糖酸比 06-15 9.48±0.79 a 9.85±0.34 a 17.25±0.40 a 8.09±0.17 5.05±0.05 e 6.96±0.16 a 07-15 12.27±0.91 ab 11.58±0.53 a 17.68±0.10 a 16.01±0.14 6.05±0.37 d 7.49±0.36 a 08-15 13.74±0.31 b 37.59±0.45 b 33.58±0.56 b − 4.43±0.23 c 16.08±0.80 b 09-15 20.77±1.45 c 60.34±2.41 c 46.63±2.07 c − 4.13±0.17 bc 25.97±1.73 c 10-15 24.90±0.20 d 95.30±2.62 d 78.42±2.53 d − 3.85±0.18 ab 45.22±3.23 d 11-15 56.70±3.60 e 151.85±5.61 e 132.88±4.65 e − 3.54±0.16 a 80.43±3.64 e 说明:同列不同的字母表示差异显著(P<0.05)。−表示未检出 表 2 无核君迁子果实发育成熟过程中各指标的Pearson相关性分析
Table 2. Pearson correlation coefficients analysis of seedless D. lotus fruit
指标 可溶性单宁 不溶性单宁 总酚 黄酮 花青素 淀粉 果糖 葡萄糖 可溶性单宁 1 不溶性单宁 −0.963** 1 总酚 0.706** −0.615** 1 黄酮 0.837** −0.735** 0.908** 1 花青素 0.325 −0.215 0.065 0.406 1 淀粉 −0.973** 0.911** −0.709** −0.808** −0.348 1 果糖 −0.946** 0.841** −0.651** −0.834** −0.500* 0.951** 1 葡萄糖 −0.975** 0.893** −0.679** −0.843** −0.439 0.972** 0.994** 1 可滴定酸 0.666** −0.527* 0.310 0.504* 0.384 −0.678** −0.826** −0.784** 糖酸比 −0.973** 0.892** −0.692** −0.848** −0.431 0.971** 0.991** 0.998** 水溶性果胶 −0.922** 0.941** −0.668** −0.708** −0.201 0.938** 0.803** 0.855** 离子结合果胶 −0.936** 0.942** −0.669** −0.696** −0.133 0.953** 0.831** 0.880** 共价结合果胶 0.453 −0.364 0.819** 0.605** −0.393 −0.453 −0.404 −0.432 多聚半乳糖醛酸酶 −0.941** 0.944** −0.807** −0.846** −0.098 0.891** 0.824** 0.877** 果胶裂解酶 −0.893** 0.920** −0.647** −0.636** −0.030 0.911** 0.765** 0.822** 指标 可滴定酸 糖酸比 水溶性果胶 离子结合果胶 共价结合果胶 多聚半乳糖
醛酸酶果胶裂解酶 可滴定酸 1 糖酸比 −0.784** 1 水溶性果胶 −0.437 0.859** 1 离子结合果胶 −0.524* 0.881** 0.986** 1 共价结合果胶 0.309 −0.443 −0.382 −0.459 1 多聚半乳糖醛酸酶 −0.492* 0.882** 0.896** 0.906** −0.611** 1 果胶裂解酶 −0.463 0.823** 0.969** 0.991** −0.480* 0.888** 1 说明:*表示P<0.05;**表示P<0.01 -
[1] YAMAGISHI M, MATSUMOTO S, NAKATSUKA A, et al. Identification of persimmon (Diospyros kaki) cultivars and phenetic relationships between Diospyros species by more effective RAPD analysis [J]. Sci Hortic, 2005, 105(2): 283 − 290. [2] MAO Weitao, YAO Guoxin, WANG Shangde, et al. Chromosome-level genomes of seeded and seedless date plum based on third-generation DNA sequencing and Hi-C analysis[J/OL]. For Res, 2021, 1: 9[2021-05-01]. doi: 10.48130/FR-2021-0009. [3] 唐霞, 梁爽, 张华, 等. 发酵型黑枣酒加工工艺的研究[J]. 食品工业, 2015, 36(9): 1 − 5. TANG Xia, LIANG Shuang, ZHANG Hua, et al. Study on processing technology of fermentation dateplum persimmon wine [J]. Food Ind, 2015, 36(9): 1 − 5. [4] 畅凌冰, 王治军, 梁臣, 等. 黑枣的价值及繁育[J]. 绿色科技, 2012(10): 68 − 69. CHANG Lingbing, WANG Zhijun, LIANG Chen, et al. Study of values and breeding of dateplum persimmon [J]. J Green Sci Technol, 2012(10): 68 − 69. [5] 滕宁宁, 王明, 吴一飞, 等. 君迁子药学研究概况[J]. 辽宁中医药大学学报, 2010, 12(9): 81 − 82. TENG Ningning, WANG Ming, WU Yifei, et al. Overview of pharmacological research of Diospyros lotus L. [J]. J Liaoning Univ Tradit Chin Med, 2010, 12(9): 81 − 82. [6] 乔小全, 任广跃, 乔梦, 等. 干燥方式对黑枣粉品质特性的影响[J]. 食品与机械, 2018, 34(8): 189 − 194, 220. QIAO Xiaoquan, REN Guangyue, QIAO Meng, et al. Effects of different drying methods on the powder quality characteristic in dateplum persimmon [J]. Food Mach, 2018, 34(8): 189 − 194, 220. [7] TIEMAN D, ZHU Guangtao, RESENDE M, et al. A chemical genetic roadmap to improved tomato flavor [J]. Science, 2017, 355: 391 − 394. [8] 程焕. 杨梅风味特征组分鉴定及变化规律的研究[D]. 杭州: 浙江大学, 2017. CHENG Huan. Study on the Flavor Characteristics and Changes of Chinese bayberry (Myrica rubra)[D]. Hangzhou: Zhejiang University, 2017. [9] 关军锋. 果实品质生理[M]. 北京: 科学出版社, 2008: 1 − 18. GUAN Junfeng. Physiology of Fruit Quality[M]. Beijing: Science Press, 2008: 1 − 18. [10] 齐秀东, 魏建梅, 高海生, 等. 梨果实发育软化与果胶多糖降解特性的关系[J]. 中国农业科学, 2015, 48(15): 3027 − 3037. QI Xiudong, WEI Jianmei, GAO Haisheng, et al. Pectin polysaccharide degradation in relation to the texture softening in pear fruit [J]. Sci Agric Sin, 2015, 48(15): 3027 − 3037. [11] 周淑荣, 郭文场, 刘佳贺. 黑枣的栽培管理[J]. 特种经济动植物, 2018, 21(11): 48 − 49. ZHOU Shurong, GUO Wenchang, LIU Jiahe. Cultivation and management of dateplum persimmon [J]. Spec Econ Anim Plant, 2018, 21(11): 48 − 49. [12] 刘春晖, 谢春阳. 响应面法对黑枣真空冷冻干燥时间工艺的优化[J]. 食品工业, 2015, 36(3): 199 − 202. LIU Chunhui, XIE Chunyang. Optimization of process dateplum persimmon vacuum freeze drying time of response surface method [J]. Food Ind, 2015, 36(3): 199 − 202. [13] 昝立峰, 杨香瑜, 张策, 等. 响应面优化涉县无核黑枣果酒发酵工艺[J]. 食品研究与开发, 2019, 40(8): 139 − 144. ZAN Lifeng, YANG Xiangyu, ZHANG Ce, et al. Optimization of fermentation of dateplum fruit wine by response surface methodology [J]. Food Res Dev, 2019, 40(8): 139 − 144. [14] 余轩. ‘磨盘柿’果实乙醇和冻融脱涩技术的研究[D]. 武汉: 华中农业大学, 2010. YU Xuan. Ethanol and Frozen-Thawing Treatments for ‘Damopan’ Persimmon Astringency Removal[D]. Wuhan: Huazhong Agricultural University, 2010. [15] 韩卫娟, 李加茹, 李华威, 等. 不同(品)种柿叶总酚与总黄酮含量年动态变化研究[J]. 中国农业大学学报, 2016, 21(2): 31 − 40. HAN Weijuan, LI Jiaru, LI Huawei, et al. Annual variation of total polyphenol and flavonoid contents in leaves of different species (varieties) of Diospyros [J]. J China Agric Univ, 2016, 21(2): 31 − 40. [16] 曹建康, 姜微波, 赵玉梅. 果蔬采后生理生化实验指导[M]. 北京: 中国轻工业出版社, 2007: 8 − 54. CAO Jiankang, JIANG Weibo, ZHAO Yumei. Postharvest Physiological and Biochemical Experimental Guidance for Fruits and Vegetables [M]. Beijing: China Light Industry Press, 2007: 8 − 54. [17] 杜改改, 李泰山, 刁松锋, 等. 6个杏李品种果实甜酸风味品质分析[J]. 果树学报, 2017, 34(1): 41 − 49. DU Gaigai, LI Taishan, DIAO Songfeng, et al. Analysis of sweet and sour flavor in six Prunus domestica×armeniaca cultivars and evaluation of their flavor quality [J]. J Fruit Sci, 2017, 34(1): 41 − 49. [18] REN Yuanyuan, SUN Pengeng, WANG Xuanxuan, et al. Degradation of cell wall polysaccharides and change of related enzyme activities with fruit softening in Annona squamosa during storage[J/OL]. Postharvest Biol Technol, 2020, 166: 111203[2021-05-20]. doi: 10.1016/j.postharvbio.2020.111203. [19] ZHI Huanuan, LIU Qiqi, XU Juan, et al. Ultrasound enhances calcium absorption of jujube fruit by regulating the cellular calcium distribution and metabolism of cell wall polysaccharides [J]. J Sci Food Agric, 2017, 97(15): 5202 − 5210. [20] 孙鹏, 李加茹, 韩卫娟, 等. 涩柿资源果实CO2脱涩难易及其与表型、内含物相关性[J]. 中国农业大学学报, 2016, 21(6): 28 − 40. SUN Peng, LI Jiaru, HAN Weijuan, et al. CO2 de-actringence status among astringent persimmon resources and its correlation with fruit morphological characteristics and content of active ingredients [J]. J China Agric Univ, 2016, 21(6): 28 − 40. [21] BUBBA M D, GIORDANI E, PIPPUCCI L, et al. Changes in tannins, ascorbic acid and sugar content in astringent persimmons during on-tree growth and ripening and in response to different postharvest treatments [J]. J Food Compos Anal, 2009, 22: 668 − 677. [22] 赵剑波, 吴本宏, 姜全, 等. 桃种质资源糖酸品质研究进展[J]. 北方园艺, 2008(4): 107 − 109. ZHAO Jianbo, WU Benhong, JIANG Quan, et al. Advances on quality of sugars and acids in peach germplasm rresources [J]. North Hortic, 2008(4): 107 − 109. [23] 田娟, 王磊, 陈庆富. 不同地区火棘果实中淀粉含量的研究[J]. 河南农业科学, 2011, 40(11): 109 − 112. TIAN Juan, WANG Lei, CHEN Qingfu. The variation of starch content in Pyracantha fruit of different regions [J]. J Henan Agric Sci, 2011, 40(11): 109 − 112. [24] 叶玉平. 细胞壁多糖降解引起采后菠萝果实成熟软化机理的初步研究[D]. 湛江: 广东海洋大学, 2014. YE Yuping. Preliminary Study on the Mechanism of Ripening and Softening of Postharvest Pineapple Fruit by Induced Degradation of Cell Wall Polysaccharides [D]. Zhanjiang: Guangdong Ocean University, 2014. [25] 王华, 李茂福, 杨媛, 等. 果实花青素生物合成分子机制研究进展[J]. 植物生理学报, 2015, 51(1): 29 − 43. WANG Hua, LI Maofu, YANG Yuan, et al. Recent advances on the molecular mechanisms of anthocyanin synthesis in fruits [J]. Plant Physiol J, 2015, 51(1): 29 − 43. [26] 张慧文, 张玉, 马超美. 原花青素的研究进展[J]. 食品科学, 2015, 36(5): 296 − 304. ZHANG Huiwen, ZHANG Yu, MA Chaomei. Progress in procyanidins research [J]. Food Sci, 2015, 36(5): 296 − 304. [27] 王玥. 柿果胶与单宁互作及其对柿果涩味的影响[D]. 武汉: 华中农业大学, 2019. WANG Yue. The Interaction between Persimmon Pectin and Persimmon Tannin and Its Effect on the Astringency of Persimmon[D]. Wuhan: Huazhong Agricultural University, 2019. [28] 张宝善, 伍晓红, 陈锦屏. 柿单宁研究进展[J]. 陕西师范大学学报(自然科学版), 2008, 36(1): 99 − 105. ZHANG Baoshan, WU Xiaohong, CHEN Jinping. Research progress in procyanidins [J]. J Shaanxi Norm Univ Nat Sci Ed, 2008, 36(1): 99 − 105. [29] 罗自生. GA3对柿果实成熟软化及细胞壁组分代谢的影响[J]. 浙江大学学报(农业与生命科学版), 2006, 32(4): 415 − 419. LUO Zisheng. Effect of GA3 on ripening and cell wall component metabolism of persimmon fruit [J]. J Zhejiang Univ Agric Life Sci, 2006, 32(4): 415 − 419. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20210421






 下载:
下载: