-
防风Saposhnikovia divaricata为伞形科Apiaceae多年生草本植物,以未抽薹的干燥根入药。其味辛、甘,性温,归膀胱、肝、脾经,具有祛风解表、胜湿止痛、止痉之效,常用于治疗发烧、头痛、过敏性鼻炎、风湿性关节炎、免疫系统疾病等[1−4]。目前已从防风中分离出 100 多种化合物,其中色原酮、香豆素类化合物是其发挥药效的主要物质基础[5]。防风主要分布于内蒙古、辽宁、吉林、黑龙江、河北、河南、山东、甘肃等地区[6]。受生长环境、采收时间、种质资源等[7−8]因素的影响,不同产地的防风药效成分及其临床药效差异较大。
中药具有多成分、多靶点作用的特点,检测单一成分难以全面反映药材内在质量,因此多指标、多成分的质量控制已成为发展趋势。《中国药典》2020年版一部“防风”药材项下,将升麻素苷和5-O-甲基维斯阿米醇苷作为评价防风药材质量的中药指标成分,规定两者占比不得低于0.24%。但升麻素、亥茅酚苷、补骨脂素、花椒毒素、佛手柑内酯、欧前胡素等色原酮和香豆素化合物均为表征不同产地、不同年限、不同商品规格的防风药材质量的特征成分,也都具有一定的抗菌、解热抗炎的功效[9−13]。因此,仅以升麻素苷和5-O-甲基维斯阿米醇苷作为防风药材的质量标志物(Q-Marker),无法全面评价防风的内在质量,为此,亟需建立完整的防风质量评价体系。
近年来,与炎症相关的疾病发病率逐年递增,寻找一种安全有效的抗炎药物成为研究的热点[14−15]。临床及实验证实很多中药具有很好的抗炎作用,且毒副作用小[16−17]。防风药材质量的差异可能会导致活性成分的差异进而呈现不同的临床疗效。目前关于不同产地防风药材抗炎活性的研究较少,且抗炎活性成分尚未明确,不利于其进一步开发利用。本研究通过建立防风药材多指标成分的高效液相色谱(HPLC)测定方法,结合建立脂多糖诱导的RAW 264.7小鼠巨噬细胞炎症模型,通过化学成分和药效指标相关联,筛选出与抗炎作用相关的药效成分群,探讨防风抗炎作用的药效基础,为完善防风药材质量标准提供依据。
-
2022年9—10月,分别在内蒙古自治区、吉林省、河北省、新疆维吾尔自治区等采集17批防风样品(表1),经吉林农业大学中药材学院韩忠明教授鉴定为伞形科植物防风的干燥根。将防风根洗净泥沙,置于恒温干燥箱中60 ℃烘干至恒质量,粉碎后过60目筛,备用。
表 1 17批防风药材样品信息
Table 1. Sample information of 17 batches of Saposhnikoviae radix
样品序号 产地 生长年限 /a 样品序号 产地 生长年限 /a S1 内蒙古自治区赤峰市松山区南地村 1 S10 吉林省白城市永茂林场 2 S2 内蒙古自治区赤峰市松山区柳条沟村 1 S11 吉林省白城市枫林湾中药材种植基地 2 S3 内蒙古自治区赤峰市松山区西道村 1 S12 河北省承德市隆化县兴隆庄村 1 S4 内蒙古自治区通辽市科尔沁区庆和林场 1 S13 河北省承德市丰宁满族自治县胡麻营村 1 S5 内蒙古自治区赤峰市林西县 2 S14 河北省承德市围场县天桥村 1 S6 吉林省长春市吉林农业大学药园 1 S15 新疆省维吾尔自治区阿勒泰哈巴河实验站 1 S7 吉林省白山市江源区平川村 1 S16 新疆省维吾尔自治区阿勒泰哈巴河实验站 1 S8 吉林省白山市江源区平川村 2 S17 新疆省维吾尔自治区阿勒泰哈巴河实验站 2 S9 吉林省白城市青山林场 2 升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、补骨脂素、花椒毒素、佛手柑内酯、欧前胡素对照品(批号分别为111522-202214、111523-202212、111710-200602、111714-200501、110739-202319、112077-202101、112078-202101、110826-202219),均购自中国食品药品检定研究院;5-O-甲基维斯阿米醇、亥茅酚对照品(批号分别为B23192、B23109),均购自源叶生物科技有限公司。
-
称取防风粉末0.2 g于锥形瓶中,加6 mL甲醇溶液,超声提取1 h,放冷,用甲醇补足质量,摇匀,过0.22 μm滤膜,即得供试品溶液。配置1 mL甲醇溶液含升麻素苷0.110 μg、5-O-甲基维斯阿米醇苷0.170 μg、升麻素0.018 μg、亥茅酚苷0.014 μg、5-O-甲基维斯阿米醇0.002 μg、补骨脂素0.002 μg、花椒毒素0.003 μg、亥茅酚0.002 μg、佛手柑内酯0.001 μg、欧前胡素0.004 μg的混合溶液为对照。
取5 g防风粉末,按液料比为1∶30 (质量体积比)加入甲醇溶液,超声提取1 h,旋蒸浓缩至10 mL,冷冻干燥,得不同批次的提取物冻干粉。取冻干粉 10 mg,溶于4 mL RAW 264.7培养基中,制成质量浓度为 2.5 g·L−1的母液,于4 ℃避光保存。
-
色谱条件:色谱柱 Supfex AQ-C18(4.6 mm×250.0 mm,5 μm),流动相为水(A)-乙腈(B)梯度洗脱(0~8 min,20.0%~40.5%B;8~20 min,40.5%~55.0%B;20.0~25.0 min,55%B,25.0~35.0 min,55.0%~65.0%B,35.0~40.0 min,65.0%~80.0%B),流速1 mL·min−1,柱温25 ℃,波长254 nm,进样量 15 μL。
-
吸取混合对照品溶液1、5、10、15、20 μL,注入液相色谱仪进行测定,以进量(x,μg)为横坐标,峰面积(y)为纵坐标进行线性回归,计算线性回归方程和相关系数。
-
分别取混合对照品溶液、样品溶液、空白溶剂(体积分数为100%的甲醇),根据“1.3” 色谱条件分别进样15 μL,比较色谱图。
-
精密吸取同一混合对照品溶液15 μL,根据“1.3”色谱条件测定升麻素苷等10种物质的峰面积(RSD)。重复6次。
-
精密吸取同一供试品溶液15 μL,分别于0、2、4、8、12、24 h进样,按照“1.3”色谱条件测定10种物质的RSD值。重复6次。
-
分别精密称取同一批供试品6份,根据“1.2”方法制备供试品溶液,按照“1.3”色谱条件测定10种物质的RSD值。重复6次。
-
取对数生长期细胞,2.5×104个·孔−1细胞接种于96孔板,设置仅含完全培养基的空白对照组和用完全培养基稀释成质量浓度为100、200、400、600、800 mg·L−1 的防风醇提物组,药物干预24 h后,采用CCK-8法检测不同质量浓度防风醇提物对RAW 264.7细胞活性的影响,细胞存活率=(加药组吸光度−空白组吸光度)/(正常组吸光度−空白组吸光度)×100%。结果显示:当防风醇提物质量浓度低于200 mg·L−1时对RAW 264.7细胞活性无影响。将细胞以2.5×104个·孔−1接种于96孔板中,培养24 h后,弃上清液,根据CCK-8细胞活力检测结果,设置正常对照组、模型对照组(LPS质量浓度为5 mg·L−1)和防风醇提物组(防风醇提物200 mg·L−1与 LPS 5 mg·L−1)共同干预细胞。药物干预细胞24 h后,取细胞上清按试剂盒说明书检测一氧化氮(NO)、白细胞介素6 (IL-6)和白细胞介素1β (IL-1β)含量。
-
根据17批防风样品中10种化学成分的质量分数,用Metaboanalyst 5.0进行系统聚类;将10种化学成分的质量分数标准化处理后进行主成分分析,得相关系数的特征值和方差贡献率;将10种化学成分与NO、IL-6和IL-1β的表达量进行相关性分析;采用均值化法对数据进行无量纲化处理,以NO、IL-6和IL-1β水平为参考序列,以化学成分质量分数为比较序列,求参考序列与比较序列的灰色关联系数[18]。采用SPSS 21.0进行显著性检验(α=0.05)、主成分分析以及相关性分析,采用Excel 22.0进行灰色关联度分析,采用Metaboanalyst 5.0进行聚类分析绘图,Origin 2022软件进行柱形图绘制。
-
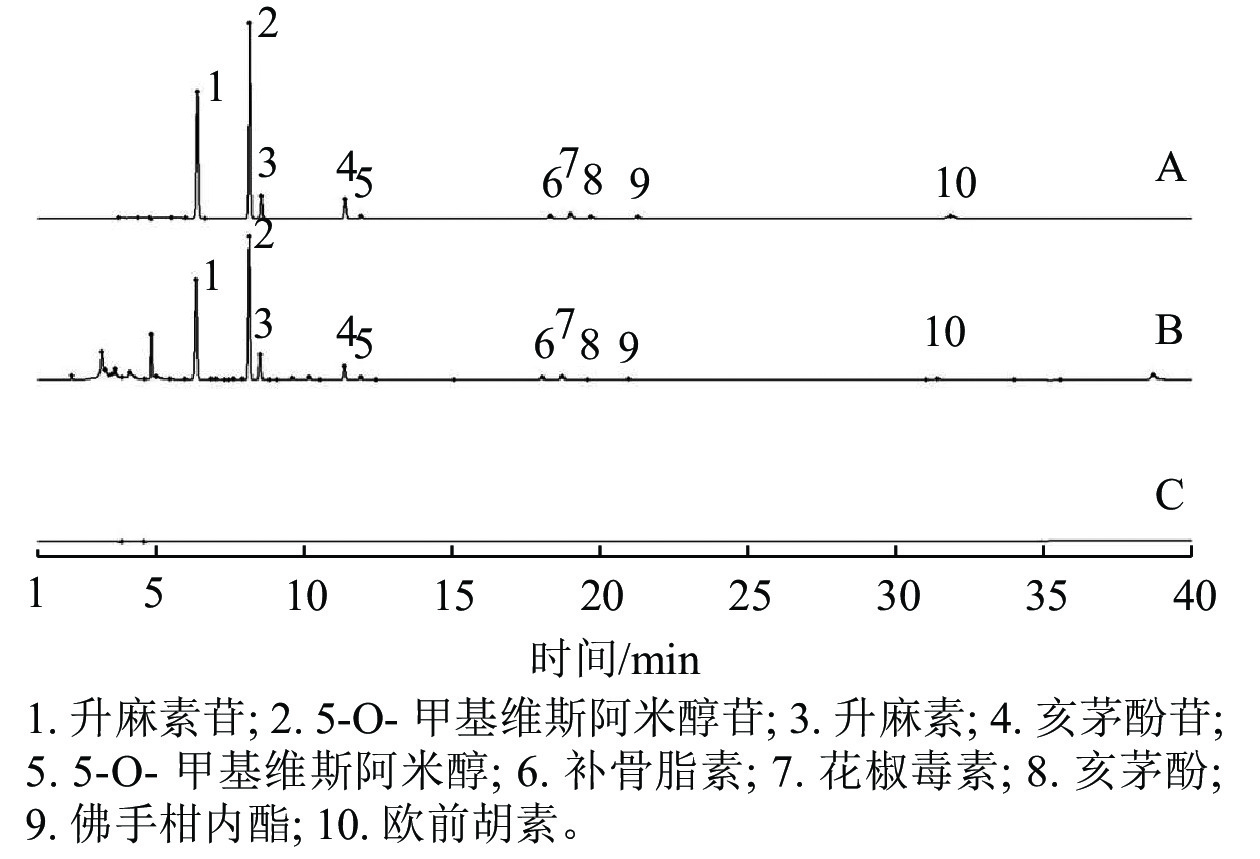
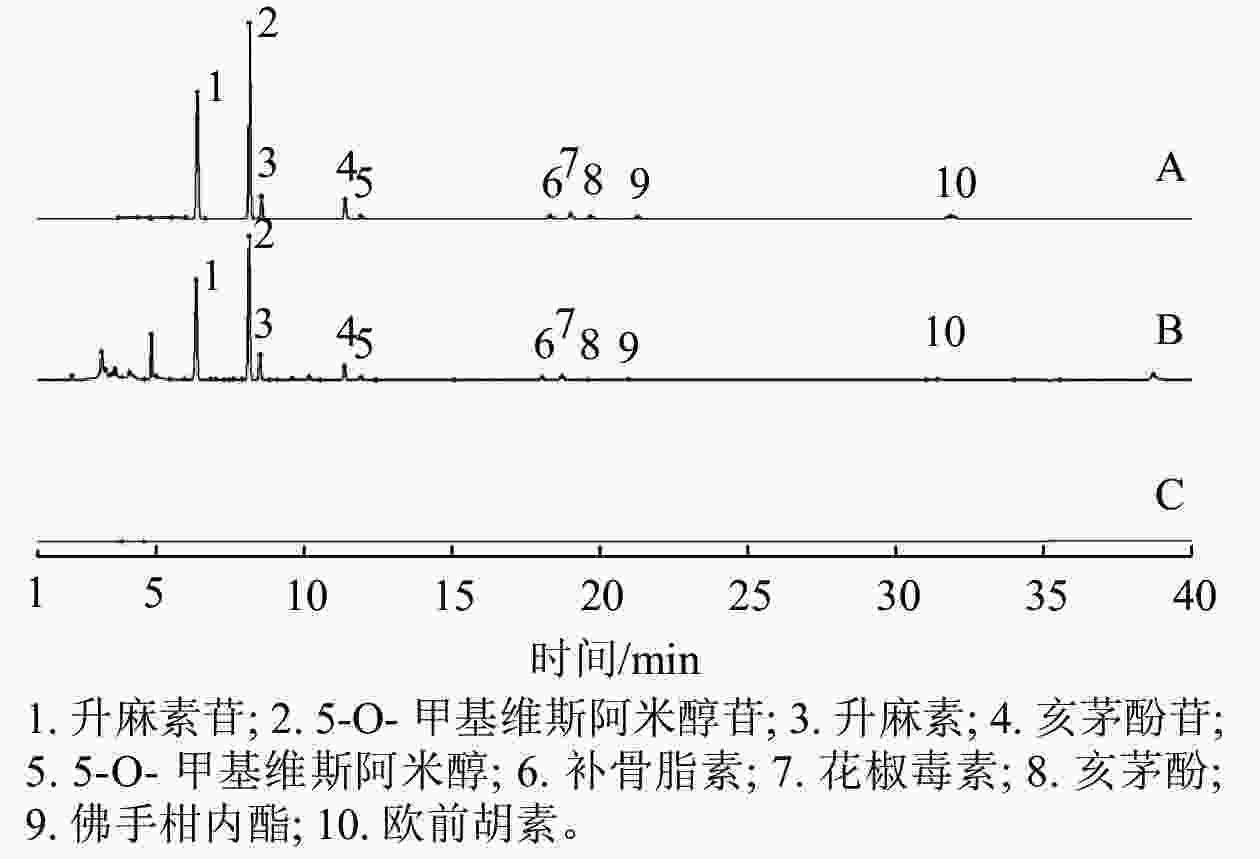
表2显示:升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇、补骨脂素、花椒毒素、亥茅酚、佛手柑内酯、欧前胡素等10种化学成分的线性关系良好,决定系数(R2)均大于0.999 0。专属性试验结果(图1)可见:空白溶剂对样品的检测无干扰。精密度试验测得升麻素苷等10种化学成分的RSD分别为0.61%、0.54%、0.53%、0.62%、0.50%、0.69%、0.69%、2.10%、0.63%和1.16%,表明该方法精密度良好。稳定性试验测得10种化学成分的RSD分别为1.15%、0.80%、0.75%、0.98%、1.32%、0.77%、0.84%、4.16%、1.68%和1.29%,表明该方法稳定性良好。重复性试验测得10种化学成分的RSD分别为4.58%、1.62%、1.62%、1.71%、1.24%、3.10%、1.69%、4.76%、1.50%和1.88%,表明该方法重复性良好。
表 2 防风10种化学成分线性关系考察结果
Table 2. Results of linear relationship between ten components of Saposhnikoviae radix
成分 回归方程 R2 线性范围/μg 升麻素苷 y=2250.7x+24.200 0.999 6 0.110~1.130 5-O-甲基维
斯阿米醇苷y=1947.2x+79.014 0.999 1 0.170~3.000 升麻素 y=2401.8x+5.534 0.999 6 0.018~0.350 亥茅酚苷 y=2693.3x+0.829 0.999 9 0.014~0.280 5-O-甲基维
斯阿米醇y=2915.1x−0.029 0.999 9 0.002~0.040 补骨脂素 y=3480.5x+0.555 0.999 9 0.002~0.040 花椒毒素 y=4947.8x+0.905 0.999 9 0.003~0.060 亥茅酚 y=3119.3x−2.227 0.999 2 0.002~0.040 佛手柑内酯 y=4601.6x+0.230 0.999 9 0.001~0.020 欧前胡素 y=4115.7x+0.172 0.999 8 0.004~0.080 说明: x指进量(mg); y指峰面积。 -
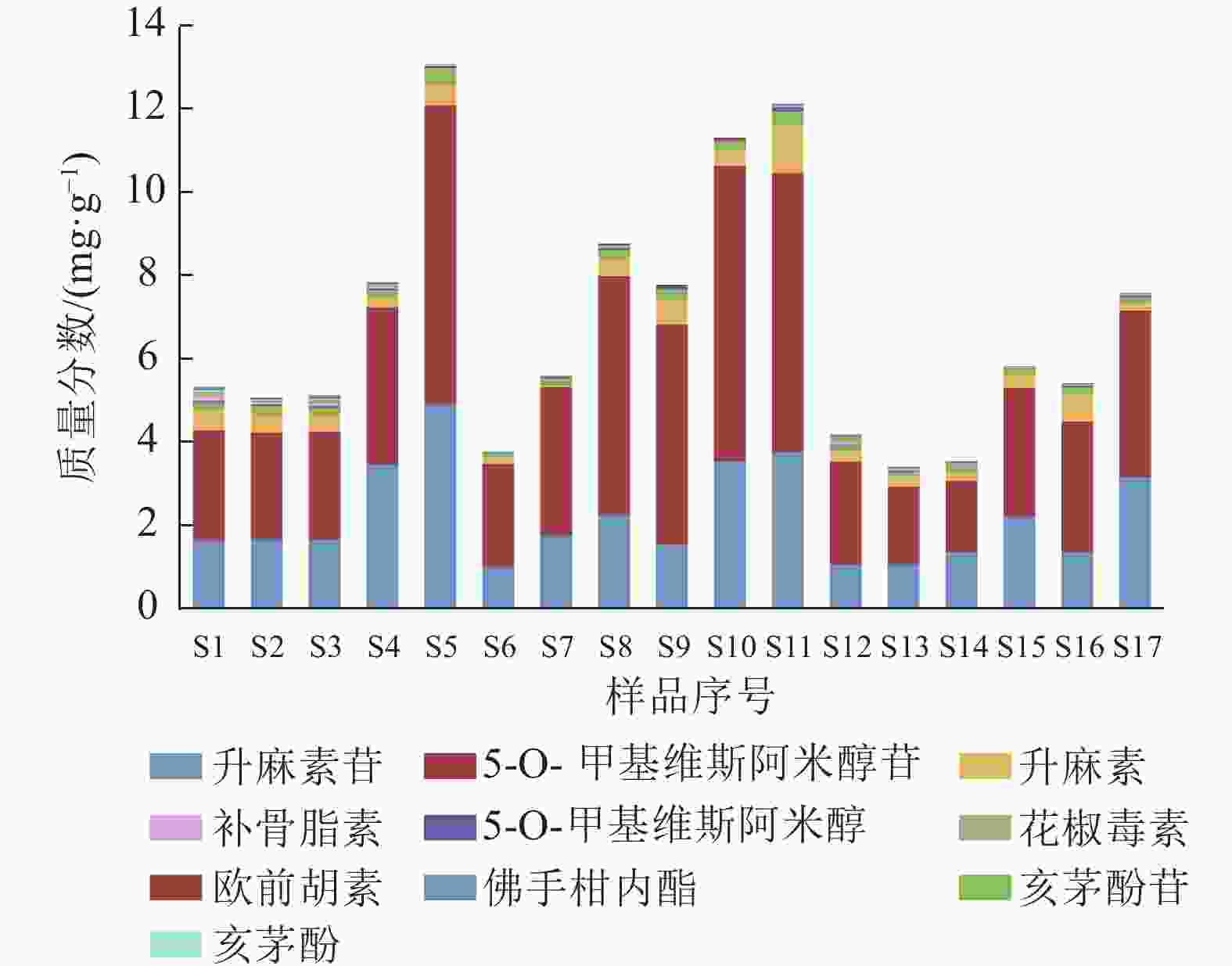
由图2可见:17批防风样品升麻素和5-O-甲基维斯阿米醇苷质量分数总和为 2.93~12.09 mg·g−1 ,均符合《中国药典》(2020年版)防风项下规定升麻素苷、5-O-甲基维斯阿米醇苷2种成分质量分数总和不少于0.24%的规定。其中产自内蒙古自治区赤峰市林西的S5 10种化学成分质量分数最高,为13.06 mg·g−1;河北省承德县胡麻营的S13 10种化学成分质量分数最低,为3.41 mg·g−1,两者相差3.83倍。防风中10种化学成分质量分数差异较大,质量分数从高到低分别为5-O-甲基维斯阿米醇苷、升麻素苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇、花椒毒素、欧前胡素、佛手柑内酯、补骨脂素、亥茅酚。
-
由图3可见:17批防风样本聚为4类,产自内蒙古的S5和吉林的S8~S11聚为第一大类,表现为富含升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇和欧前胡素;产自内蒙古的S1~S4聚为第二大类,表现为富含补骨脂素、花椒毒素、亥茅酚、佛手柑内酯;产自河北的S12~S14聚为第三大类,补骨脂素、花椒毒素、佛手柑内酯质量分数相对较高;产自吉林的S6~S7和新疆的S15~S17聚为第四大类,10种化学成分质量分数相对较低。整体来看,防风药材样本具有一定的区域特征,但同一产地不同批次的药材之间存在差异性,这可能是因为生长年限、土壤、降水量等因子影响了防风次生代谢产物的积累。
-
由表3可见:以主特征值>1为提取标准,提取3个主成分,分别代表了变量总方差的44.033%、28.648%、10.611%,累计贡献率达83.292%,大于80.00%。这表明这3个主成分是影响防风质量评价的主要因子,可全面反映防风药材的综合质量特征。以提取的主成分的因子得分乘以相应主成分特征值的算术平方根计算综合得分,对17批防风样品进行综合评价,结果见表4。来自内蒙古的S5和吉林的S8~S11综合得分在1以上,质量相对较好;来自内蒙古的S1和河北的S12综合得分较低,质量相对较差。
表 3 特征值及累计方差贡献率
Table 3. Eigenvalue and cumulative variance contribution rates
主成分 特征值 方差/% 累积贡献率/% 1 4.403 44.033 44.033 2 2.865 28.648 72.681 3 1.061 10.611 83.292 表 4 17批防风药材样品综合得分值
Table 4. Comprehensive score value of 17 batches of Saposhnikoviae radix
样品 综合得分 样品 综合得分 S1 −2.05 S10 2.41 S2 −0.51 S11 4.39 S3 −1.91 S12 −2.52 S4 0.16 S13 −1.92 S5 3.77 S14 −1.72 S6 −1.91 S15 −0.71 S7 −0.74 S16 −0.03 S8 1.56 S17 −0.16 S9 1.88 -
由表5可见:与正常对照组比较,模型对照组NO、IL-6和IL-1β质量浓度显著升高(P<0.01),说明RAW 264.7炎性模型造模成功;与模型对照组比较,各受试药物组可不同程度地降低NO、IL-6和IL-1β水平,说明防风醇提物质量浓度为200 mg·L−1时具有一定的抗炎效果。其中防风样品S8~S11、S17对细胞中炎症因子NO表达量具有较强的抑制作用,S7、S9~S11、S17对细胞中炎症因子IL-6表达量具有较强的抑制作用,S5、S8~S11对炎症因子IL-1β表达量具有较强的抑制作用。可能因为防风样品S5、S8~S11中富含升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇和欧前胡素,且综合质量较高,样品S7、S17中具有其他低成分高活性的物质,因此抗炎活性较强。
表 5 17批防风样品的抗炎活性
Table 5. Anti-inflammatory capacity of 17 batches of Saposhnikoviae radix
组别 NO/(μmol·L−1) IL-6 /(μg·L−1) IL-1β/(ng·L−1) 组别 NO/(μmol·L−1) IL-6 /(μg·L−1) IL-1β/(ng·L−1) 正常对照 2.57±0.32 2.00±0.55 63.53±2.60 S9 20.02±0.94** 28.50±1.68** 138.09±17.62** 模型对照 37.57±3.39## 57.88±1.35## 227.92±26.06## S10 19.02±0.71** 24.45±2.29** 125.46±6.26** S1 29.60±1.30** 40.97±2.22 207.76±5.80* S11 10.02±2.36** 24.21±2.36** 127.43±7.70** S2 20.77±0.82** 42.07±1.89** 181.86±2.09** S12 24.85±3.54** 45.73±1.28** 140.71±14.37** S3 35.10±0.35 45.40±2.56** 178.25±1.62** S13 35.35±0.47 35.54±1.41** 180.71±10.66** S4 23.43±0.12** 38.02±1.82** 138.25±20.17** S14 26.77±1.77** 45.83±7.21** 167.92±8.35** S5 26.35±2.36** 36.59±3.03** 112.35±3.48** S15 25.60±0.82** 57.50±1.75 159.07±28.28** S6 36.93±0.82 40.26±0.27** 214.32±5.80 S16 25.52±2.83** 36.11±0.34** 176.94±6.72** S7 24.35±4.71** 29.59±1.21** 173.33±9.51** S17 20.43±2.71** 34.88±3.17** 147.60±5.10** S8 18.02±1.41** 35.59±0.54** 135.46±7.42** 说明:防风醇提物剂量均为200 mg·L−1。与正常对照组比较,*P<0.05,**P<0.01;与模型组比较,##P<0.01。 -
将10个化学成分与NO、IL-6和IL-1β的表达量进行相关性分析(表6)表明:升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷和5-O-甲基维斯阿米醇与NO表达量呈显著或极显著负相关,5-O-甲基维斯阿米醇苷、5-O-甲基维斯阿米醇、欧前胡素与IL-6表达量呈显著或极显著负相关,升麻素苷、5-O-甲基维斯阿米醇苷、亥茅酚苷与IL-1β表达量呈显著或极显著负相关,表明升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇、欧前胡素与抗炎活性呈正相关,是防风发挥抗炎作用的主要活性成分。
表 6 化学成分变量组与药效变量组的相关系数
Table 6. Canonical correlation analysis of components and pharmacodynamics indexes
成分 药效指标 NO 1L-6 IL-1β 升麻素苷 −0.512* −0.392 −0.736** 5-O-甲基维斯阿米醇苷 −0.658** −0.703** −0.787** 升麻素 −0.543* −0.442 −0.315 亥茅酚苷 −0.534* −0.456 −0.690** 5-O-甲基维斯阿米醇 −0.599* −0.540* −0.391 补骨脂素 0.268 0.319 0.424 花椒毒素 0.322 0.424 0.329 亥茅酚 0.212 0.219 0.346 佛手柑内酯 0.349 0.380 0.307 欧前胡素 −0.474 −0.535* −0.386 说明:*表示显著相关(P<0.05);**表示极显著相关(P<0.01)。 -
由表7可见:与NO表达量有较大关联性的成分贡献从大到小依次为亥茅酚苷、5-O-甲基维斯阿米醇、5-O-甲基维斯阿米醇苷、升麻素苷、升麻素、花椒毒素、佛手柑内酯、欧前胡素、补骨脂素、亥茅酚;与IL-6表达量有较大关联性的成分贡献从大到小依次为亥茅酚苷、5-O-甲基维斯阿米醇、5-O-甲基维斯阿米醇苷、升麻素苷、升麻素、花椒毒素、欧前胡素、佛手柑内酯、补骨脂素、亥茅酚;与IL-1β表达量有较大关联性的成分贡献从大到小依次为亥茅酚苷、5-O-甲基维斯阿米醇、升麻素、5-O-甲基维斯阿米醇苷、升麻素苷、花椒毒素、欧前胡素、佛手柑内酯、补骨脂素、亥茅酚。各化学成分与各药效指标的关联度均大于0.6,说明防风体外抗炎作用是多组分协同作用的结果。其中升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇与NO、IL-6、IL-1β表达量的关联系数排名靠前且均大于0.8,说明这5种化学成分对防风发挥抗炎活性的贡献较大。
表 7 防风药材化学成分质量分数和抗炎指标的灰色关联度
Table 7. Grey correlation between chemical composition contents and anti-inflammatory index
成分 NO IL-6 IL-1β 灰色关联度 排名 灰色关联度 排名 灰色关联度 排名 升麻素苷 0.801 4 0.813 4 0.801 5 5-O-甲基维斯阿米醇苷 0.806 3 0.818 3 0.806 4 升麻素 0.800 5 0.809 5 0.819 3 亥茅酚苷 0.849 1 0.862 1 0.859 1 5-O-甲基维斯阿米醇 0.842 2 0.853 2 0.840 2 补骨脂素 0.737 9 0.762 9 0.732 9 花椒毒素 0.781 6 0.793 6 0.778 6 亥茅酚 0.700 10 0.703 10 0.675 10 佛手柑内酯 0.758 7 0.769 8 0.757 8 欧前胡素 0.753 8 0.775 7 0.769 7 -
目前,关于防风的药材质量标准研究大多为单一种类成分的测定,且研究成分数量较少[19−21]。本研究采用HPLC-DAD法同时测定防风中6种色原酮和4种香豆素成分的质量分数。在供试品溶液制备过程中,本研究考察了超声和加热回流2种常用的提取方式,以及不同提取溶剂、料液比、超声时间对防风中10种化学成分提取率的影响,结果显示:提取溶剂体积分数为100%甲醇、液料比为1∶30(质量体积比)、超声提取60 min时防风中化学成分提取率最高。在《中国药典》(2020版)和文献[22−23]的洗脱方法基础上进行优化,发现当柱温为25 ℃,流速为1 mL·min−1时基线平稳,峰形良好,各成分分离度高。该方法专属性强,准确度和分离度良好,能较全面有效地评价防风质量,为其质量控制提供参考依据。
高质量道地药材不仅主要成分含量较高,而且高活性成分含量也较高[24]。由于不同产地生态环境因素的差异,导致药用植物生理生化反应及体内代谢不同。体内次生代谢产物的形成和积累发生变化,使得药材质量发生变化[25],但植物次生代谢产物的形成和积累不仅与生长环境有关,也与其生长年限有关[26]。本研究聚类分析结果也显示:17批防风药材呈现一定的区域性特征,并且同一产地不同生长年限的药材之间也存在差异性,内蒙古、吉林产地2年生防风药材中升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇质量分数和10种化学成分总质量分数明显高于其1年生防风药材,说明防风药材质量不仅具有一定地域性,同时其药材有效成分含量的高低也受到种植年限的影响。17批防风药材中以吉林、内蒙古产区的2年生防风药材综合得分较高,综合质量较优,与河北产地的药材质量存在较大的差异。该结果与防风的道地药材主要分布于内蒙古扎鲁特旗以北和吉林西部的结论相符合[27]。
本研究通过体外细胞试验表明:不同产地的防风醇提物均能不同程度地降低NO、IL-6和IL-1β的表达量。通过双变量相关性分析和灰色关联度分析发现:升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇能显著降低 LPS 诱导的RAW 264.7炎症细胞上清液中NO、IL-6、IL-1β的表达,且与这3个细胞炎症指标的关联系数较大。有研究表明:升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇通过抑制 NF-κB 和MAPKs信号通路减轻LPS诱导的RAW 264.7细胞炎症反应[28−30]。推测以上5个成分可能是防风抗炎活性的关键物质基础。
-
本研究建立了防风药材多指标质量分数的测定方法,并筛选出升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇为防风药理作用的关键活性成分。不同产地和不同生长年限防风药材的化学成分质量分数、抗炎活性之间存在差异,17批药材中以内蒙古和吉林的2年生防风药材综合质量较优,因此入药时,要充分考虑防风的产地和生长年限,才能保证临床疗效的稳定性。
Comprehensive quality evaluation of Saposhnikoviae radix based on multi-component contents determination
-
摘要:
目的 建立防风Saposhnikovia divaricata药材多指标成分同时定量分析的测定方法,并以多指标成分为评价指标,结合不同成分对防风药材抗炎活性的贡献,分析不同产地的防风药材质量,为防风药材质量的综合评价提供科学依据。 方法 采用高效液相色谱(HPLC)建立防风6种色原酮和4种香豆素成分同时定量的测定方法,采用聚类分析和主成分分析对防风药材质量进行综合评价;采用脂多糖诱导的RAW 264.7小鼠巨噬细胞炎症模型,分析防风10种化学成分与抗炎活性的相关关系。 结果 防风10种化学成分在各自范围内线性关系、准确度和分离度均良好。聚类分析和主成分分析把17批样品分为4类,其中以内蒙古S5和吉林S8~S11产地的2年生防风的综合质量相对较好;17批防风醇提物能不同程度地抑制脂多糖诱导的RAW264.7细胞分泌一氧化氮(NO)、白细胞介素6 (IL-6)、白细胞介素1β (IL-1β);其中升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇、欧前胡素与抗炎活性呈正相关;灰色关联度分析表明:防风抗炎活性是多种成分协同作用的结果,升麻素苷、5-O-甲基维斯阿米醇苷、升麻素、亥茅酚苷、5-O-甲基维斯阿米醇与3个细胞炎症指标(NO、IL-6和IL-1β)的关联度均大于0.8,是发挥抗炎作用的主要物质基础。 结论 本研究建立的防风多指标成分测定方法良好,可用于防风色原酮和香豆素成分的同时测定,结合抗炎活性与灰色关联度分析法建立了基于生物活性的防风药材质量综合评价模式,为建立防风药材质量综合评价的标准提供了新的方法和科学依据。 图3表7 参30 Abstract:Objective To establish a method for quantitative analysis of multi-index components in Saposhnikoviae radix (Saposhnikovia divaricata), and for comprehensive quality evaluation of the medicinal materials from different areas, using the contents of multiple-index components as evaluation indexes, and the contribution of different components to the anti-inflammatory activity. Method The concentrations of 6 chromones and 4 coumarins from Saposhnikoviae radix were quantified by high-performance liquid chromatography (HPLC). The quality was comprehensively evaluated using cluster analysis and principal component analysis. The correlations between 10 chemical components and their anti-inflammatory activities were analyzed in a lipopolysaccharide-induced macrophage inflammation model in RAW 264.7 mice. Result The 10 kinds of chemical components had good linear relationship, accuracy, and separation in their respective ranges, respectively. 17 batches of samples were grouped into 4 categories by cluster analysis and principal component analysis. The quality of 2-year-old S. divaricata grown in Inner Mongolia (S5) and Jilin (S8 to S11) were relatively better. 17 batches of S. divaricata alcohol extracts differentially inhibited NO, IL-6, and IL-1β secreted by lipopolysaccharide-induced RAW 264.7 cells. Prim-O-glucosylcimifugin, 5-O-methylvisammioside, cimifugin, sec-O-glucosylhamaudol, 5-O-methylvisamminol, and imperatorin were positively correlated with anti-inflammation. The anti-inflammatory effect of S. divaricata is the result of the combined action of several components, and the correlation degrees among prim-O-glucosylcimifugin, 5-O-methylvisammioside, cimifugin, sec-O-glucosylhamaudol, and 5-O-methylvisamminol with three cellular indicators of inflammation (NO, IL-6, and IL-1 β) were over 0.8, which were the main material basis for the anti-inflammatory activity, according to the gray correlation analysis. Conclusion A comprehensive evaluation model of the quality of S. divaricata based on biological activity and combining the anti-inflammatory activity and gray correlation analysis was established, which provided a new method and scientific basis for the establishment of quality standards for a comprehensive evaluation of the quality of S. divaricata. [Ch, 3 fig. 7 tab. 30 ref.] -
Key words:
- Saposhnikovia divaricata /
- chromone /
- coumarin /
- anti-inflammatory /
- correlation analysis
-
表 1 17批防风药材样品信息
Table 1. Sample information of 17 batches of Saposhnikoviae radix
样品序号 产地 生长年限 /a 样品序号 产地 生长年限 /a S1 内蒙古自治区赤峰市松山区南地村 1 S10 吉林省白城市永茂林场 2 S2 内蒙古自治区赤峰市松山区柳条沟村 1 S11 吉林省白城市枫林湾中药材种植基地 2 S3 内蒙古自治区赤峰市松山区西道村 1 S12 河北省承德市隆化县兴隆庄村 1 S4 内蒙古自治区通辽市科尔沁区庆和林场 1 S13 河北省承德市丰宁满族自治县胡麻营村 1 S5 内蒙古自治区赤峰市林西县 2 S14 河北省承德市围场县天桥村 1 S6 吉林省长春市吉林农业大学药园 1 S15 新疆省维吾尔自治区阿勒泰哈巴河实验站 1 S7 吉林省白山市江源区平川村 1 S16 新疆省维吾尔自治区阿勒泰哈巴河实验站 1 S8 吉林省白山市江源区平川村 2 S17 新疆省维吾尔自治区阿勒泰哈巴河实验站 2 S9 吉林省白城市青山林场 2 表 2 防风10种化学成分线性关系考察结果
Table 2. Results of linear relationship between ten components of Saposhnikoviae radix
成分 回归方程 R2 线性范围/μg 升麻素苷 y=2250.7x+24.200 0.999 6 0.110~1.130 5-O-甲基维
斯阿米醇苷y=1947.2x+79.014 0.999 1 0.170~3.000 升麻素 y=2401.8x+5.534 0.999 6 0.018~0.350 亥茅酚苷 y=2693.3x+0.829 0.999 9 0.014~0.280 5-O-甲基维
斯阿米醇y=2915.1x−0.029 0.999 9 0.002~0.040 补骨脂素 y=3480.5x+0.555 0.999 9 0.002~0.040 花椒毒素 y=4947.8x+0.905 0.999 9 0.003~0.060 亥茅酚 y=3119.3x−2.227 0.999 2 0.002~0.040 佛手柑内酯 y=4601.6x+0.230 0.999 9 0.001~0.020 欧前胡素 y=4115.7x+0.172 0.999 8 0.004~0.080 说明: x指进量(mg); y指峰面积。 表 3 特征值及累计方差贡献率
Table 3. Eigenvalue and cumulative variance contribution rates
主成分 特征值 方差/% 累积贡献率/% 1 4.403 44.033 44.033 2 2.865 28.648 72.681 3 1.061 10.611 83.292 表 4 17批防风药材样品综合得分值
Table 4. Comprehensive score value of 17 batches of Saposhnikoviae radix
样品 综合得分 样品 综合得分 S1 −2.05 S10 2.41 S2 −0.51 S11 4.39 S3 −1.91 S12 −2.52 S4 0.16 S13 −1.92 S5 3.77 S14 −1.72 S6 −1.91 S15 −0.71 S7 −0.74 S16 −0.03 S8 1.56 S17 −0.16 S9 1.88 表 5 17批防风样品的抗炎活性
Table 5. Anti-inflammatory capacity of 17 batches of Saposhnikoviae radix
组别 NO/(μmol·L−1) IL-6 /(μg·L−1) IL-1β/(ng·L−1) 组别 NO/(μmol·L−1) IL-6 /(μg·L−1) IL-1β/(ng·L−1) 正常对照 2.57±0.32 2.00±0.55 63.53±2.60 S9 20.02±0.94** 28.50±1.68** 138.09±17.62** 模型对照 37.57±3.39## 57.88±1.35## 227.92±26.06## S10 19.02±0.71** 24.45±2.29** 125.46±6.26** S1 29.60±1.30** 40.97±2.22 207.76±5.80* S11 10.02±2.36** 24.21±2.36** 127.43±7.70** S2 20.77±0.82** 42.07±1.89** 181.86±2.09** S12 24.85±3.54** 45.73±1.28** 140.71±14.37** S3 35.10±0.35 45.40±2.56** 178.25±1.62** S13 35.35±0.47 35.54±1.41** 180.71±10.66** S4 23.43±0.12** 38.02±1.82** 138.25±20.17** S14 26.77±1.77** 45.83±7.21** 167.92±8.35** S5 26.35±2.36** 36.59±3.03** 112.35±3.48** S15 25.60±0.82** 57.50±1.75 159.07±28.28** S6 36.93±0.82 40.26±0.27** 214.32±5.80 S16 25.52±2.83** 36.11±0.34** 176.94±6.72** S7 24.35±4.71** 29.59±1.21** 173.33±9.51** S17 20.43±2.71** 34.88±3.17** 147.60±5.10** S8 18.02±1.41** 35.59±0.54** 135.46±7.42** 说明:防风醇提物剂量均为200 mg·L−1。与正常对照组比较,*P<0.05,**P<0.01;与模型组比较,##P<0.01。 表 6 化学成分变量组与药效变量组的相关系数
Table 6. Canonical correlation analysis of components and pharmacodynamics indexes
成分 药效指标 NO 1L-6 IL-1β 升麻素苷 −0.512* −0.392 −0.736** 5-O-甲基维斯阿米醇苷 −0.658** −0.703** −0.787** 升麻素 −0.543* −0.442 −0.315 亥茅酚苷 −0.534* −0.456 −0.690** 5-O-甲基维斯阿米醇 −0.599* −0.540* −0.391 补骨脂素 0.268 0.319 0.424 花椒毒素 0.322 0.424 0.329 亥茅酚 0.212 0.219 0.346 佛手柑内酯 0.349 0.380 0.307 欧前胡素 −0.474 −0.535* −0.386 说明:*表示显著相关(P<0.05);**表示极显著相关(P<0.01)。 表 7 防风药材化学成分质量分数和抗炎指标的灰色关联度
Table 7. Grey correlation between chemical composition contents and anti-inflammatory index
成分 NO IL-6 IL-1β 灰色关联度 排名 灰色关联度 排名 灰色关联度 排名 升麻素苷 0.801 4 0.813 4 0.801 5 5-O-甲基维斯阿米醇苷 0.806 3 0.818 3 0.806 4 升麻素 0.800 5 0.809 5 0.819 3 亥茅酚苷 0.849 1 0.862 1 0.859 1 5-O-甲基维斯阿米醇 0.842 2 0.853 2 0.840 2 补骨脂素 0.737 9 0.762 9 0.732 9 花椒毒素 0.781 6 0.793 6 0.778 6 亥茅酚 0.700 10 0.703 10 0.675 10 佛手柑内酯 0.758 7 0.769 8 0.757 8 欧前胡素 0.753 8 0.775 7 0.769 7 -
[1] CHEN Yanchun, CHEN Zhiling, WANG Gan, et al. The effects of Saposhnikovia divaricata aqueous extracts on the inflammation and intestinal microflora in allergic rhinitis mice[J/OL]. Evidence-based Complementary and Alternative Medicine, 2022: 1052359[2023-11-10]. doi: 10.1155/2022/1052359. [2] URBAGAROVA B M, SHULTS E E, TARASKIN V V, et al. Chromones and coumarins from Saposhnikovia divaricata (Turcz. ) Schischk. growing in Buryatia and Mongolia and their cytotoxicity[J/OL]. Journal of Ethnopharmacology, 2020, 261: 112517[2023-11-10]. doi: 10.1016/j.jep.2019.112517. [3] SUN Yan, JIANG Peng, JIANG Yikai, et al. New chromones from the roots of Saposhnikovia divaricata (Turcz. ) Schischk. with anti-inflammatory activity[J/OL]. Bioorganic Chemistry, 2023, 134: 106447[2023-11-10]. doi: 10.1016/j.bioorg.2023.106447. [4] MATUSIEWICZ M, BACZEK K B, KOSIERADZKA I, et al. Effect of juice and extracts from Saposhnikovia divaricata root on the colon cancer cells caco-2 [J]. International Journal of Molecular Sciences, 2019, 20(18): 4526 − 4549. [5] YANG Min, WANG Congcong, WANG Wenle, et al. Saposhnikovia divaricata-an ethnopharmacological, phytochemical and pharmacological review [J]. Chinese Journal of Integrative Medicine, 2020, 26(11): 873 − 880. [6] KREINER J, PANG E, LENON G B, et al. Saposhnikoviaa divaricata: a phytochemical, pharmacological, and pharmacokinetic review [J]. Chinese Journal of Natural Medicines, 2017, 15(4): 255 − 264. [7] 郝佳, 刘宇航, 殷洁, 等. 不同磷浓度对土壤理化性质及防风生长和药材品质的影响[J]. 华南农业大学学报, 2022, 43(3): 59 − 67. HAO Jia, LIU Yuhang, YIN Jie, et al. Effects of different phosphorus concentrations on soil physicochemical property, growth and medicinal materials quality of Saposhnikovia divaricata [J]. Journal of South China Agricultural University, 2022, 43(3): 59 − 67. [8] 郭旭, 田新, 郝佳, 等. 不同产地防风色原酮含量与土壤因子的关系[J]. 华南农业大学学报, 2020, 41(4): 30 − 37. GUO Xu, TIAN Xin, HAO Jia, et al. Relationships between Saposhnikovia divaricata chromone content and soil factors in different regions[J]. Journal of South China Agricultural University, 2020, 41(4): 30 − 37. [9] LI Yazhen, CHEN Jiahong, TSAI Chengfang, et al. Anti-inflammatory property of imperatorin on alveolar macrophages and inflammatory lung injury [J]. Journal of Natural Products, 2019, 82(4): 1002 − 1008. [10] ERDENEBILEG S, SON Y J, KIM M, et al. Saposhnikovia divaricata root and its major components ameliorate inflammation and altered gut microbial diversity and compositions in DSS-induced colitis[J/OL]. Integrative Medicine Research, 2023, 12(4): 100998[2023-11-10]. doi: 10.1016/j.imr.2023.100998. [11] WEI Jianxu, ZHANG Xiaomeng, LI Yuan, et al. Novel application of bergapten and quercetin with anti-bacterial, osteogenesis-potentiating, and anti-inflammation tri-effects [J]. Acta Biochimica et Biophysica Sinica, 2021, 53(6): 683 − 696. [12] DUAN Juan, HU Xuantao, LI Tao, et al. Cimifugin suppresses NF-kappaB signaling to prevent osteoclastogenesis and periprosthetic osteolysis[J/OL]. Frontiers in Pharmacology, 2021, 12: 724256[2023-11-10]. doi: 10.3389/fphar.2021.724256. [13] ZHU Chan, YANG Yang, SONG Yizhi, et al. Mechanisms involved in the antinociceptive and anti-inflammatory effects of xanthotoxin [J]. The European Journal of Neuroscience, 2023, 58(7): 3605 − 3617. [14] LIN Yimu, XIAO Shuyi, YAO Wei, et al. Molecular photoacoustic imaging for early diagnosis and treatment monitoring of rheumatoid arthritis in a mouse model [J]. American Journal of Translational Research, 2021, 13(8): 8873 − 8884. [15] JIN Shangyi, LI Mengtao, FANG Yongfei, et al. Chinese registry of rheumatoid arthritis (CREDIT): Ⅱ. prevalence and risk factors of major comorbidities in Chinese patients with rheumatoid arthritis [J]. Arthritis Research &Therapy, 2017, 19(1): 251 − 259. [16] KONG Chaojun, JIA Longfei, JIA Jianping. γ-mangostin attenuates amyloid-β42-induced neuroinflammation and oxidative stress in microglia-like BV2 cells via the mitogen-activated protein kinases signaling pathway[J/OL]. European Journal of Pharmacology, 2022, 917: 174744[2023-11-10]. doi: 10.1016/j.ejphar.2022.174744. [17] LEE Y T, YUNUS MHM, UGUSMAN A, et al. Natural compounds affecting inflammatory pathways of osteoarthritis[J/OL]. Antioxidants , 2022, 11(9) [2023-11-10]. doi: 10.3390/antiox11091722. [18] 何江, 尚芳红, 李隆云, 等. 佛手指纹图谱的建立及抗氧化谱效关系研究[J]. 中草药, 2023, 54(23): 7841 − 7852. HE Jiang, SHANG Fanghong, LI Longyun, et al. Establishment of fingerprints and spectrum-effect relationship of antioxidant activity of Citri sarcodactylis fructus [J]. Chinese Traditional and Herbal Drugs, 2023, 54(23): 7841 − 7852. [19] 杨琳琳, 李千, 王璇, 等. 生长方式及年限对防风品质影响研究[J]. 中国中药杂志, 2023, 48(15): 4106 − 4114. YANG Linlin, LI Qian, WANG Xuan, et al. Effects of growth patterns and years on quality of Saposhnikoviae radix samples [J]. China Journal of Chinese Materia Medica, 2023, 48(15): 4106 − 4114. [20] 张金华, 林天凤, 张榆, 等. 防风色原酮类对照提取物含量标定及其在防风药材质量控制中的应用[J]. 中国中药杂志, 2021, 46(21): 5658 − 5664. ZHANG Jinhua, LIN Tianfeng, ZHANG Yu, et al. Calibration on chromone reference extract and application on quality control of Saposhnikoviae radix [J]. China Journal of Chinese Materia Medica, 2021, 46(21): 5658 − 5664. [21] 王浩, 郭凌阁, 尚兴朴, 等. 基于防风外观性状和内在指标性成分划分防风药材商品规格等级研究[J]. 中草药, 2020, 51(20): 5320 − 5327. WANG Hao, GUO Lingge, SHANG Xingpu, et al. Based on appearance and index components to study on standards of commodity classes of Saposhnikovia radix [J]. Chinese Traditional and Herbal Drugs, 2020, 51(20): 5320 − 5327. [22] BATSUKH Z, TOUME K, JAVZAN B, et al. Metabolomic profiling of Saposhnikoviae radix from Mongolia by LC-IT-TOF-MS/MS and multivariate statistical analysis [J]. Journal of Natural Medicines, 2020, 74(1): 170 − 188. [23] WANG Simao, QIAN Yuexin, SUN Mengxiao, et al. Holistic quality evaluation of Saposhnikoviae radix (Saposhnikovia divaricata) by reversed-phase ultra-high performance liquid chromatography and hydrophilic interaction chromatography coupled with ion mobility quadrupole time- of -flight mass spectrometry-based untargeted metabolomics [J]. Arablan Journal of Chemistry, 2020, 13(12): 8835 − 8847. [24] 孟祥才, 邓代千, 杜虹韦, 等. 高品质道地药材的科学内涵[J]. 中草药, 2023, 54(3): 939 − 947. MENG Xiangcai, DENG Daiqian, DU Hongwei, et al. Scientific connotation of high-quality genuine medicinal materials [J]. Chinese Traditional and Herbal Drugs, 2023, 54(3): 939 − 947. [25] CHEN Bingrui, ZOU Hui, ZHANG Boyang, et al. Distribution pattern and change prediction of Saposhnikovia divaricata suitable area in china under climate change[J/OL]. Ecological Indicators, 2022, 143[2023-11-10]. doi: 10.1016/j.ecolind.2022.109311. [26] YIP Kaman, XU Jun, ZHOU Shanshan, et al. Characterization of chemical component variations in different growth years and tissues of morindae officinalis radix by integrating metabolomics and glycomics [J]. Journal of Agricultural and Food Chemistry, 2019, 67(26): 7304 − 7314. [27] 郭梅, 安琪, 申亚君, 等. 基于多指标一测多评结合信息熵-响应面法的防风药材质量评价研究[J]. 中国中药杂志, 2021, 46(10): 2537 − 2546. GUO Mei, AN Qi, SHEN Yajun, et al. Quality evaluation of Saposhnikoviae radix based on QAMS combined with information entropy-response surface method [J]. China Journal of Chinese Materia Medica, 2021, 46(10): 2537 − 2546. [28] LIU Guiming, XIE Jing, SHI Yurui, et al. Sec-O-glucosylhamaudol suppressed inflammatory reaction induced by LPS in RAW 264.7 cells through inhibition of NF-kappaB and MAPKs signaling[J/OL]. Bioscience Reports, 2020, 40(2): BSR20194230[2023-11-10]. doi: 10.1042/BSR20194230. [29] LIU Aimin, ZHAO Wei, ZHANG Buxin, et al. Cimifugin ameliorates imiquimod-induced psoriasis by inhibiting oxidative stress and inflammation via NF-kappaB/MAPK pathway[J/OL]. Bioscience Reports, 2020, 40(6): BSR20200471[2023-11-10]. doi: 10.1042/BSR20200471. [30] KONG Xiangying, LIU Chunfang, ZHANG Cun, et al. The suppressive effects of Saposhnikovia divaricata chromone extract on rheumatoid arthritis via inhibition of nuclear factor-kappaB and mitogen activated proteinkinases activation on collagen-induced arthritis model [J]. Journal of Ethnopharmacology, 2013, 148(3): 842 − 850. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20230567






 下载:
下载: