-
维生素B6(VB6)是一类吡啶化合物的总称,包括吡哆醛(PL),吡哆醇(PN),吡哆胺(PM),磷酸吡哆醛(PLP),磷酸吡哆醇(PNP),磷酸吡哆胺(PMP)等,其中PLP是其主要活性形式,作为辅酶参与生物体内100多种生化反应,包括氨基酸代谢、抗生素合成、免疫调节等生理反应及氧化胁迫等抗逆反应[1]。细胞内VB6各组分的平衡是机体进行正常代谢的前提,因而VB6对植物的生长发育至关重要。研究[2]发现,自然界中VB6有从头合成(de novo synthetic pathway)和补救合成(salvage pathway)2种方式,补救合成途径使VB6异养型生物能够利用外源摄入的PN,PM和PL来合成机体代谢所需要的活化型PLP并维持细胞各型VB6浓度相对稳定。从头合成已被广泛研究,而补救合成途径的研究却相对缺乏。其中,吡哆醛还原酶(PLR)是VB6补救合成途径中的作用酶,最初在酵母中被发现,属于醛酮还原酶(aldo-keto reductase),在还原型烟酰胺腺嘌呤二核苷酸磷酸(NADPH)存在的条件下催化PL转换成PN[3-4],从而可维持细胞内VB6动态平衡,对于生物体进行正常的生理活动具有重要意义。植物性食物中VB6主要以PN或其糖基化形态存在,并推测植物中可能有高效的PN生成机制[5]。迄今为止,植物中只有拟南芥Arabidopsis thaliana的AtPLR1基因得到分离鉴定,对酵母突变体进行互补实验表明AtPLR1像酵母PLR一样,可催化PL形成PN[6]。T-DNA插入的Atplr1突变体根系生长较野生型明显缓慢,氯化钠、甘露醇胁迫下Atplr1的生长受到抑制[6],推测PLR可能与植物抵抗盐害和渗透压胁迫有关。烟草Nicotiana tabacum是一种重要的模式植物及经济作物,对其PLR进行克隆和功能分析,有助于进一步明确植物体内VB6的补救合成途径,同时为烟草良种选育提供理论储备。本研究以AtPLR1为模板,经过对美国生物技术信息中心(NCBI)公共数据库(http://www.ncbi.nlm.nih.gov/)中的序列进行比对和拼接并结合cDNA末端快速扩增技术-聚合酶链式反应(RACE-PCR)得到了烟草NtPLR1基因的全长序列。以此为基础,分析了其生物功能和表达特性,结果NtPLR1可催化PL形成PN。NtPLR1在叶片中表达最高,与紫外线、氧化及氯化钠胁迫和外源PL处理有应答反应。
HTML
-
烟草‘云烟85’Nicotiana tabacum‘Yunyan 85’种子和pET32a原核表达载体为实验室保存。pEASY-Blunt载体、菌株BL21(DE3)Rosetta和大肠埃希菌Escherichia coli DH5α购自TransGen公司。
-
紫外线处理:在无菌操作台上用紫外线照射生长至旺长期的烟草,照射时间分别为2 h,4 h和8 h,取茎尖以下的第3片叶,液氮冷冻,备用。
盐处理:用100.0 mmol·L-1的氯化钠溶液浇灌旺长期烟草,处理1 d,4 d和7 d后取样,取茎尖以下第2片叶。液氮冷冻,备用。
氧化处理:浇灌亚硫酸氢钠-亚硫酸钠(NaHSO3-Na2SO3)混合物(10.0 mmol·L-1,以亚硫酸钠浓度计),处理1 d,4 d和7 d后取样,取茎尖以下第2片叶,液氮冷冻,备用。
PL处理:将旺长期烟草根部洗净,置于添加100.0 mg·L-1 PL的水培液中,用锡纸将烟草根部及水培液遮住,茎叶接受正常光照。分别于培养的第2天、第4天和第8天采集茎尖以下第2片叶,液氮冷冻,备用。
以上均设置重复3个·处理-1。
-
根据RNAiso Plus RNA提取试剂盒使用说明书(Takara),进行总RNA提取。提取的RNA用质量分数为1.0%琼脂糖凝胶电泳进行纯度与完整性检测。参照PrimeScript RT reagent Kit with gDNA Eraser反转录试剂盒(Takara)对质量合格的RNA进行反转录,置于-20 ℃备用。
-
以拟南芥吡哆醛PLR的氨基酸序列(NP_200170.2)为模板,在烟草表达序列标签(EST)数据库里同源检索,根据得到的EST序列,设计引物3RACE-1,3RACE-2,3RACE-3(表 1)进行巢式PCR扩增目的基因3′端序列。扩增产物经切胶回收,连接pEASY-Blunt载体后,转化至大肠埃希菌DH5α感受态细胞,筛选阳性克隆子进行测序。3′端序列扩增产物测序结果验证后,使用DNAMAN软件将它与EST起始序列结合得到全长cDNA序列。随后设计全长克隆引物NtPLR-F1和NtPLR-R1(表 1),扩增NtPLR1序列。PCR反应程序为95 ℃预变性3.0 min;94 ℃变性30 s,60 ℃退火30 s,72 ℃延伸1.5 min,共28个循环;72 ℃延伸10.0 min。获得的NtPLR1序列在NCBI(http://www.ncbi.nlm.nih.gov/)数据库BLAST中进行序列比对。用ProtParam软件(http://web.expasy.org/protparam/)在线分析该蛋白的分子量和等电点;采用DNAMAN 7.0软件对基因编码的氨基酸序列进行比对分析。
用途 引物名称 引物序列(5'→3') 3'-RACE 3RACE-1 TGCAAATTATGCACCTCTGCAGGAACG 3RACE-2 TGCAGTTGGGGTGAGCAACTATGGACC 3RACE-3 TGCGCTCAGCCCAGGTACAATTTTCAT 目的片段扩增NtPLR1 NtPLR-F1 ATGGCTCTCTCACTCCCAGCTTCAAAATC NtPLR-R1 CTTTGTCTGAAATACGTTTTGGATC 原核表达 NtPLR-F2 GGATCCATGGCTCTCTCACTCCCAGCTTCAAAATC NtPLR-R2 GTCGACCTTTGTCTGAAATACGTTTTGGATC qRT-PCR NtPLR-F3 TGGCAAAAGGTAAAGATGGG NtPLR-R3 GTTGATGCCATTCTCCACCG 说明:下划线分别表示BamH1和Sal1。 Table 1. Primers used in NtPLR1 gene cloning and expression analysis
-
根据NtPLR1基因的cDNA序列,设计特异性定量引物(表 1),以18 S rRNA为内参基因,以根、茎、叶及紫外线、氧化、氯化钠处理下不同时间点取样叶片的cDNA为模板,进行荧光实时定量PCR(qRT-PCR)分析。qRT-PCR反应程序为95 ℃ 3.0 min,95 ℃ 10 s,55 ℃ 40 s,35个循环;溶解曲线:从65 ℃按0.5 ℃/循环增加到95 ℃。以2-ΔΔCt法计算相对表达量。
-
VB6检测参照张剑韵等[7-9]的方法,加以改进。VB6色谱分析所用色谱柱为H&E公司的XP ODS-A 5 μm 120 A(250.0 mm × 4.6 mm)。高效液相色谱仪为Waters 600,配备2475荧光检测仪。流动相A(分析用):体积分数为1%乙腈(CH3CN)-25.0 mmol·L-1磷酸二氢钾(KH2PO4)-25.0 mmol·L-1高氯酸钠(NaClO4),pH 2.5;流速为0.5 mL·min-1。进样量均为5.0 μL,荧光检测波长为395 nm,调整激发波长为290 nm。
-
原核表达载体构建:根据载体pET32a多克隆位点信息,设计带有酶切位点(BamH1和Sal1)的原核表达引物(表 1),以云烟85 cDNA为模板扩增NtPLR1基因的cDNA片段。经琼脂糖凝胶电泳分离,回收目的条带后,连接pEASY-Blunt载体,转化至大肠埃希菌DH5α感受态细胞。挑取经PCR和测序验证的阳性菌落,扩大培养,使用质粒小抽试剂盒(TransGen2)提取质粒,即得到pEASY-NtPLR1载体。用限制性内切酶BamH1和Sal1双酶切pEASY-NtPLR1和pET32a质粒后进行T4连接,即得到pET32a-NtPLR1重组质粒。测序正确后,提取目的质粒并转化至BL21(DE3)Rosetta菌株,即得到融合表达菌。
蛋白诱导表达:37 ℃培养融合表达菌至D(600)约为0.60,加入终浓度为1.0 mmol·L-1的异丙基硫代半乳糖苷(IPTG),并在18 ℃/37 ℃ 200 r·min-1诱导24 h。以含pET32a空质粒的BL21(DE3)Rosetta为对照。离心收获菌体,8 000 r·min-1离心10.0 min,弃上清,用PBS重悬。重复1次后进行超声波破碎。分别取上清和沉淀,加入上样缓冲液,沸水浴5.0 min,冷却至室温后,取20.0 μL进行SDS-PAGE(5%浓缩胶,10%分离胶)电泳检测。电泳后,经考马斯亮蓝染色、拍照,分析蛋白表达结果。
1.1. 实验材料
1.2. 处理方法
1.3. 总核糖核酸(RNA)提取及互补脱氧核糖核酸(cDNA)的合成
1.4. 基因克隆及生物信息学分析
1.5. NtPLR1表达特性分析
1.6. VB6标准试剂的配制及VB6的色谱分析条件
1.7. 基因原核表达载体的构建及蛋白诱导表达
-
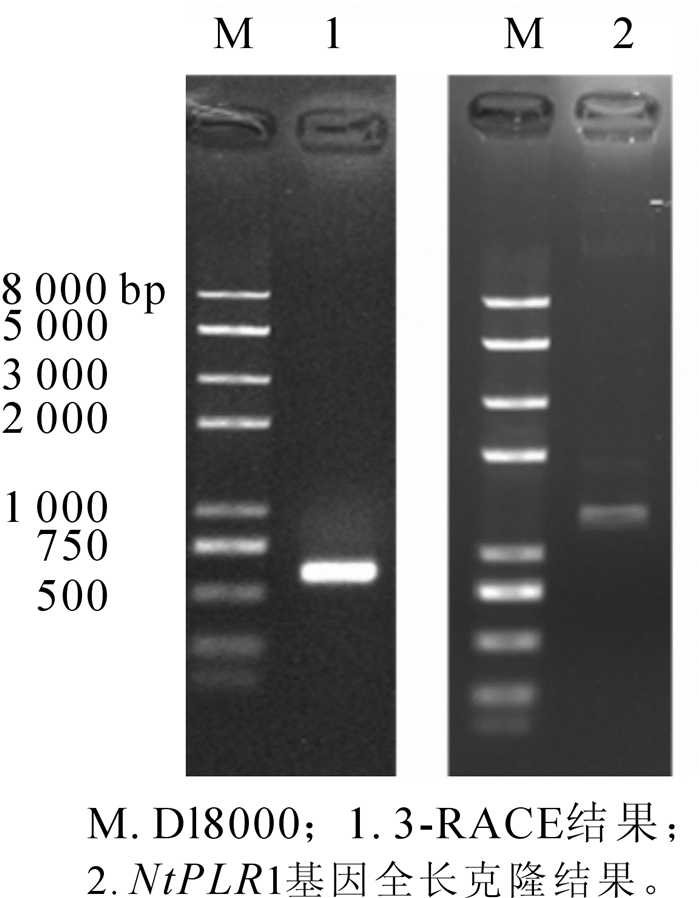
以拟南芥吡哆醛PLR的氨基酸序列(NP_200170.2)为模板,在烟草EST数据库里同源检索到一条同源性(79%)序列(GenBank: HS082453.1)。以此EST序列为起点,进行延伸检索后得到4条候选EST序列,登录号分别为GenBank:FS425789,GenBank:FS385536.1,GenBank:FS432618,GenBank:FS431044.1。使用DNAMAN比对5条EST序列,发现它们来源于同一基因,拼接后得到1条长800 bp的起始序列。根据该序列设计3轮3′-RACE引物(表 1),进行巢式PCR扩增得到大小约为700 bp单一明亮条带(图 1中泳道1)。将该条带测序后和起始序列拼接得到全长cDNA序列。随后设计全长克隆引物(表 1),PCR扩增得到大小约1 500 bp的序列(图 1中泳道2)。测序正确后,将此全长序列命名为NtPLR1,其cDNA长度为1 370 bp,开放阅读框1 110 bp,5′非编码区(UTR)长55 bp,3′UTR长205 bp。编码369个氨基酸,起始密码子为ATG,终止密码子为TGA(图 2),具有Aldo-keto还原酶家族保守底物结合位点[6](图 2中下划线强调部分)。在线预测其编码蛋白的分子量为41 070.5 Da,理论等电点为9.42。氨基酸多序列比对结果显示,NtPLR1与AtPLR相似性为75%(图 3),与栗酒裂殖酵母Schizosaccharomyces pombe[10],酿酒酵母Saccharomyces cerevisiae[11]PLR的氨基酸相似性分别为24%和26%。
-
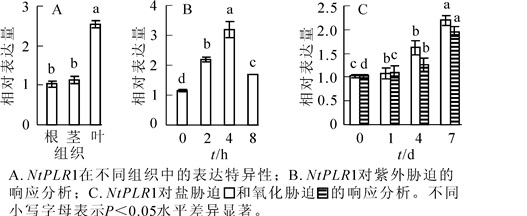
分别提取烟草根、茎、叶的总RNA,D(260)/D(280)为1.9~2.0,表明RNA纯度较好,可进行后续实验。如图 4A所示:NtPLR1在根、茎和叶均有表达,在叶中表达最高,根、茎表达水平较低。对不同逆境胁迫下NtPLR1的表达分析发现:紫外线胁迫下,随时间延长,NtPLR1基因在烟草叶片中的表达量表现出先升高后下降的趋势,并在紫外线处理4 h时达到最大值(图 4B)。氧化及氯化钠(100.0 mmol·L-1)浇灌处理时,随胁迫时间的增加,NtPLR1基因在烟草叶片中的表达持续升高,7 d时表达最高(图 4C)。在以上逆境胁迫下,NtPLR1表达呈现不同程度的上调,这表明NtPLR1与紫外线、氧化、氯化钠胁迫有应答反应。
-
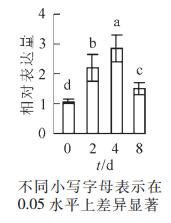
烟草水培液添加外源PL后,分别于培养的第2天、第4天、第8天取样,分析NtPLR1基因的表达水平和PL,PN含量。定量PCR分析结果表明:NtPLR1表达随处理时间延长呈现先上升后下降的趋势,在第4天表达量达到最高,第2天、第4天、第8天的NtPLR1表达量分别是对照的2.20,2.85和1.50倍(图 5)。
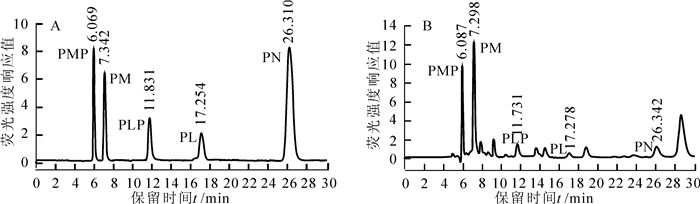
VB6标准品高效液相色谱法(HPLC)检测结果如图 6A,峰型和区分度良好。对未处理的烟草叶片提取液分析发现,在PMP,PM,PLP,PL及PN的洗脱位置上均出现了相应的洗脱峰(图 6B),说明检测方法可行。据此,对PL处理组烟草叶片进行HPLC分析,结果表明:随时间延长,处理组烟草叶片中PL含量逐渐降低,PN含量增幅明显(图 7),同时,PMP,PM含量有小幅增长,表明烟草吸收外源PL后,主要将PL转化为PN。PL处理后NtPLR1的表达受到诱导,而在8 d时表达下降,结合PN,PMP和PM含量的逐渐增多可知,NtPLR1在烟草中催化PL形成PN。VB6各组分在烟草中动态转化,且各组分间存在反馈调节。
-
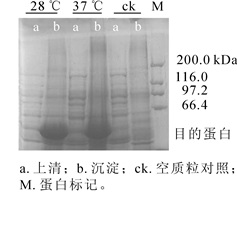
将重组质粒pET32a-NtPLR1转入BL21(DE3)Rosetta,分别在28 ℃和37 ℃条件下经异丙基硫代半乳糖苷(IPTG)诱导后,超声波破碎菌体,离心分离上清和沉淀。将上清和沉淀分别进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)检测,结果显示:上清中无目的条带,而沉淀中在约53 kDa处出现明显蛋白条带,因pET32a的组氨酸标签(his-tag)约为12 kDa,故蛋白条带的大小与预期相符。仅沉淀中出现目的条带,表明NtPLR1在大肠埃希菌中以包涵体形式存在(图 8)。
2.1. NtPLR1克隆及氨基酸序列分析
2.2. NtPLR1表达特性分析
2.3. PL对NtPLR1表达的诱导效果及对PN生成量的影响
2.4. NtPLR1原核载体构建及重组蛋白诱导表达
-
VB6在自然界中广泛地存在,主要以辅酶的形式参与生物体内多种物质代谢反应,是生物机体内很多重要酶系的辅酶[12]。植物体内,VB6参与淀粉、亚油酸等物质的合成[13],对于生长素、叶绿素以及乙烯的合成是不可或缺的[14-15]。近年来的研究还发现,VB6具有抗氧化作用,可猝灭超氧阴离子自由基及单线态氧[16];除此之外,在低温、渗透压、盐害、紫外及病菌等逆境中,VB6可以提高植株的抵抗力,发挥一定的抗逆作用[13, 17-20]。
VB6从头合成途径和补救合成途径普遍存在于植物和微生物中[21-24]。植物和微生物是VB6自养生物,动物自身无法从头合成VB6,只能从食物中获得VB6前体物质,通过补救合成途径满足机体对VB6的需求。VB6补救途径由多种酶参与,PLR是其中一种VB6补救合成酶,对于细胞进行正常生理活动具有重要意义。在研究拟南芥Atplr1时发现,Atplr1的VB6总水平下降,其中PL,PLP,PM和PMP水平显著下降,而PN和PNP无显著变化,推测在拟南芥内可能存在PLR的同工酶[6]。而HUANG等[25]的研究认为:烟草叶际PL—PN的转换可能受叶际微生物的影响较大。VB6对植物的生长发育、逆境适应及人和动物的营养具有重要意义,其从头合成途径已有较多的研究,而补救途径还有许多不明之处,有待深入研究。本研究从烟草中克隆得到烟草NtPLR1,并设置了不同的逆境胁迫条件对NtPLR1进行探究,结果表明:NtPLR1在叶中表达最高且受紫外线,氧化和氯化钠胁迫的诱导,推测NtPLR1参与烟草植株对紫外线、氧化和氯化钠胁迫的抗逆反应。外源添加PL后,NtPLR1表达量与对照相比显著上调,表明PL对NtPLR1有显著的诱导作用。此外,外源PL处理的前4 d NtPLR1的表达呈上升趋势,而在培养的第8天时NtPLR1的表达降低,相应的PL持续降低,而PN,PM和PMP等都有不同程度的升高,表明VB6各组分在烟草叶片中可相互转化并存在反馈调节。目前,本实验室正在进行NtPLR1重组蛋白的优化表达及体外酶活测定,以期为进一步探明烟草PLR基因功能及VB6补救合成过程奠定基础。

















 DownLoad:
DownLoad: