-
油桐Vernicia fordii隶属大戟科Euphorbiaceae油桐属Vernicia,是中国亚热带地区重要的经济树种和四大木本油料树种之一,已有上千年的栽培历史[1]。油桐产品桐油作为优质的干性油,具有致密度高、干燥快、绝缘、耐酸碱等优良特性,在电子工业、高级印刷油墨、生物柴油、环保油漆及其他化工行业得到广泛应用[2]。油桐为多年生落叶乔木,叶片阔卵形,掌状网脉,叶柄圆形,叶柄顶部与叶片基部连接处具有2个凸起的馒头形紫褐色无柄腺体[3]。
植物与食草动物间的互作会相互影响物种的进化轨迹,也使植物界出现了许多物理和化学防御措施[4−5]。在某些植物谱系中演化出了间接防御策略,即通过招募蚂蚁当保镖来防御草食动物[6]。与帮助授粉的花蜜腺不同,参与防御的蜜腺通常生长在叶片上,被称为花外蜜腺(extrafloral nectary),或称叶腺[7]。花外蜜腺的形状有无定形、凸起、扁平、凹陷、洞形5种类型,主要分布在叶片、叶柄、托叶、茎、花萼外侧等营养器官上,如在乌桕Triadica sebifera上为绕叶缘一周,在榕树Ficus microcarpa上分布在叶背面基部,在白楸Mallotus paniculatus上分布在正面叶脉,在蓖麻Ricinus communis上则分布在叶柄与叶片连接处等[8]。利用腺体分泌蜜露吸引蚂蚁来抵御食草节肢动物啃食叶片是非常有效的防御机制[9]。蜜露的主要成分为氨基酸、糖分、酯类以及其他有机化合物等,是各种昆虫的食物来源之一[10]。蜜露能够在幼嫩器官的花外蜜腺上被发现,而成熟以后的叶片上本就不明显的无定形的和很小的扁平蜜腺更加不易发现,结构明显的蜜腺虽然清晰可辨但是已经丧失了分泌蜜露的功能[11]。
植物腺体的发生受到特定部位细胞中转录因子的调控,蜜腺细胞的定向增殖与分化,最终形成具有分泌腔和导管结构的复杂组织系统。MAXIMO等[12]首次系统描述了无患子科Sapindaceae植物花外蜜腺的结构特征、形态多样性和蜜露成分组成。蜜腺结构由多层分泌型表皮细胞构成,下方为转移细胞层,并通过独立的维管束系统实现代谢物运输[13]。大戟科鹦鹉桐Joannesia princeps的叶柄顶端腺体分泌的蜜露表现为持续性大量外泌特征,蜜露在角质下腔积累导致角质层膨胀破裂后完成释放[14]。棉花Gossypium色素腺体分泌的棉酚具有抗病虫害功能。GoPGF是调控棉花腺体形成的主效转录因子,激活GhANT-GoPGF调控通路,介导腺体细胞中棉酚的合成[15]。WANG等[16]揭示了柑橘Citrus reticulata油腺形成的分子调控网络,DRNL-LMI1级联反应激活MYC5,促进油腺的发育和精油的生物合成。
现有研究对高等植物腺体的结构和发育过程已取得一定进展,但对油桐腺体形成发育的分子机制研究鲜有报道,其调控机制尚不清晰。本研究通过对油桐主根、根尖、当年生枝、腺体、叶芽、幼嫩叶片、成熟叶片、雄花苞、雌花苞及种仁发育初期、中期、后期等12个部位或发育阶段进行转录组测序(RNA-seq),采用加权基因共表达网络分析(WGCNA)构建基因共表达网络,挖掘与腺体相关的特异性模块;结合模块内枢纽基因表达特征、基因互作网络及蛋白互作网络分析,参考基因本体论数据库(GO)与京都基因与基因组百科全书(KEGG)富集分析结果,筛选可能参与腺体发育的基因;利用实时荧光定量逆转录聚合酶链式反应(RT-qPCR)对候选基因进行表达验证,初步解析油桐腺体形成的分子机理。
-
转录组测序材料为7年生油桐‘浙江座桐’V. fordii ‘Zhejiang Zuotong’,种植于中国林业科学研究院亚热带林业研究所后山(30°03′N,119°57′E)。于2023年4—12月,采集主根、根尖、当年生枝条、腺体、叶芽、幼嫩叶片、成熟叶片、雄花苞、雌花苞及种仁发育初期、中期和后期等12个部位或发育阶段样品,每个部位或发育阶段设2个生物学重复,共计24个样本(表1)。取样后立即置于液氮,并于−80 ℃超低温冰箱保存备用。RT-qPCR实验材料于2025年6月12日采集,为油桐的根、茎、叶、叶柄、腺体和果实等6种组织,采后立即放入液氮速冻并储存于−80 ℃备用。腺体形态结构观察材料同期取自不同生长状态的油桐叶片,并使用尼康D610相机拍照记录。
表 1 油桐样本信息
Table 1. Sample information of V. fordii
组织部位 样本编号 采样时间 组织部位 样本编号 采样时间 主根 AR_a、AR_b 2023-12-02 成熟叶片 ML_a、ML_b 2023-06-16 根尖 AP_a、AP_b 2023-12-02 雌花苞 FB_a、FB_b 2023-04-15 当年生枝条 S_a、S_b 2023-06-16 雄花苞 MB_a、MB_b 2023-04-15 腺体 G_a、G_b 2023-06-16 种仁发育初期 K1_a、K1_b 2023-07-01 叶芽 LB_a、LB_b 2023-06-16 种仁发育中期 K2_a、K2_b 2023-08-08 幼嫩叶片 YL_a、YL_b 2023-06-16 种仁发育后期 K3_a、K3_b 2023-08-22 说明:a、b表示2个重复。 -
植物样品总RNA使用HiPure HP Plant RNA Mini Kit试剂盒(R4165,美吉)提取。Nanodrop 2000 (Thermo Scientific)对所提RNA的浓度和纯度进行检测,Agilent 2100 Bioanalyzer (Agilent Technologies)测定RNA完整值(RNA integrity number, RIN)。符合D(260)/D(280)比值为1.9~2.1,D(260)/D(230)比值≥2.0,且RIN≥7.5的RNA样品用于后续建库和测序。
-
转录组测序工作委托上海美吉生物科技有限公司完成。质检合格的样品mRNA在Illumina HiSeq X Ten平台进行转录组测序,测序读长为双端150 bp (PE150)。对获得的原始测序数据进行质控,选择fastp软件[17]对原始数据进行过滤,用Trimmatic去除接头和低质量碱基片段[18],HISAT构建参考基因组索引[19],并将转录组数据比对到参考基因组[20](https://ngdc.cncb.ac.cn/gsa/browse/CRA001732),通过Subread比对到各转录本的读序进行计数[21],根据转录本与基因的对应关系将读序数标准化为每百万转录本数(transcripts per million,VTPM)的读序对。最后通过Blast对Unigene进行功能数据库(NR,Swissprot,Pfam,KOG,KEGG,GO等)注释,从而得到功能注释信息。原始转录组数据已上传到国家生物信息中心——中国国家基因库(China National GeneBank, CNCB)数据库(https://ngdc.cncb.ac.cn/bioproject/browse/PRJCA042784),项目编号为PRJCA042784。
-
根据各样本所有基因的表达值,使用Spearman方法计算组内及组间样本的相关系数,绘制成热图,可直观显示组间样本差异及组内样本重复情况。通过主成分分析(principal component analysis,PCA)将样本中上万维度的信息变换为数个维度的综合指标,根据各样本在第1主成分(PC1)和第2主成分(PC2) 2个综合指标中的数值大小,绘制二维散点。样本相关性热图和PCA图使用在线ChiPlot网站(https://www.chiplot.online/)进行绘制[22]。
-
利用Tbtools v2.210[23]中的插件WGCNAshiny[24]构建加权基因共表达网络。为提高分析准确性,首先对平均表达量较低的基因进行过滤(VTPM<5)[25],以去除噪音基因并保留潜在的组织特异性表达基因。通过评估不同软阈值(power)下网络的尺度独立性和平均连通性,确定合适的软阈值以满足无尺度网络特征。随后基于拓扑重叠矩阵(topological overlap matrix, TOM)对基因进行分层聚类,并采用动态树切分法划分共表达模块,同时绘制基因系统聚类树。相关参数设置为:power=8,minModuleSize=30,mergeCutHeight=0.25。
将油桐不同组织部位作为表型性状,并以数值型分类变量形式构建表型矩阵。计算模块特征向量(module eigengene,ME)与表型之间的相关性。相关系数绝对值接近1且P<0.05的模块被定义为关键模块。灰色(grey)模块包含未被聚类的基因,视为无效模块。
-
模块成员关系(module membership, MM)表示基因与ME的相关性,基因显著性(gene significance, GS)反映基因表达水平与目标性状的关联程度。在模块内同时满足|GS|>0.6且|MM|>0.8的基因被定义为枢纽基因(hub genes)。利用eggnog-mapper (http://eggnog-mapper.embl.de/)对枢纽基因序列进行功能注释,并通过TBtools对其进行GO功能注释与KEGG通路富集分析及可视化。基于STRING数据库(http://string-db.org/)[26]构建枢纽基因蛋白互作网络(protein-protein interaction, PPI)。在模块内以权重值(weight)>0.4为阈值,利用Cytoscape v3.10.4[27]构建基因互作网络,并借助MCODE插件[28]进行聚类分析,以识别网络中高度相互关联的节点群集。最后,综合基因功能富集分析、PPI网络和基因互作网络聚类结果,筛选模块中的候选基因,使用TBtools绘制基因表达热图。
-
利用Primer3Plus网站(http://www.primer3plus.com/)设计引物(表2),提交浙江有康生物科技有限公司进行引物合成。提取总RNA后,使用PrimeScript FAST RT Reagent Kit with gDNA Eraser 反转录试剂盒(RR092A,TaKaRa)合成cDNA。使用TB Green Premix Ex Taq Ⅱ FAST qPCR实时定量试剂盒(CN830A,TaKaRa),Quantstudio 5实时荧光定量PCR仪(赛默飞)完成分析。对cDNA进行稀释作为模板,以油桐EF1α (elongation factor 1-alpha) 基因为内参[29],设置20 μL定量体系,扩增程序为95 ℃预变性30 s;95 ℃变性5 s,56 ℃退火30 s,40个循环。每个样品设3个重复,用2-ΔΔCT法计算相对表达量。采用GraphPad Prism 10软件进行差异显著性分析与线性回归拟合,并作图。
表 2 RT-qPCR引物序列
Table 2. Primers used for RT-qPCR
基因 ID 基因名称 正向引物(5′→3′) 反向引物(5′→3′) Vf01g02365 LSH4 ACTACCGCTATCTCAATGGG AGAGAAAGTGGTGGCCTATG Vf04g00587 RAD4 GAAATTACTCTCCTTGGACTCC CACGACCAGACTCAATATGC Vf07g00391 HDG5 TGCAAGTGGTTCTCTTCACC ATTGCCCAGGTTCCTTCTTC Vf04g00884 GHI AATCTTCCTTGTGCCGCTAG CGCATCTGTCCAAGCATTTC Vf10g01491 LOB TCAAAGGCTCCAGAAGGAAC TTGGCGATGATGATGAGGAG Vf10g01688 SWEET10 TTGCACCTCTTGGCATTGTG GGAACAGCAACGAAAAGGTC EF1α GCCTGGTATGGTTGTGACCT GGATCATCCTTGGAGTTGGA -
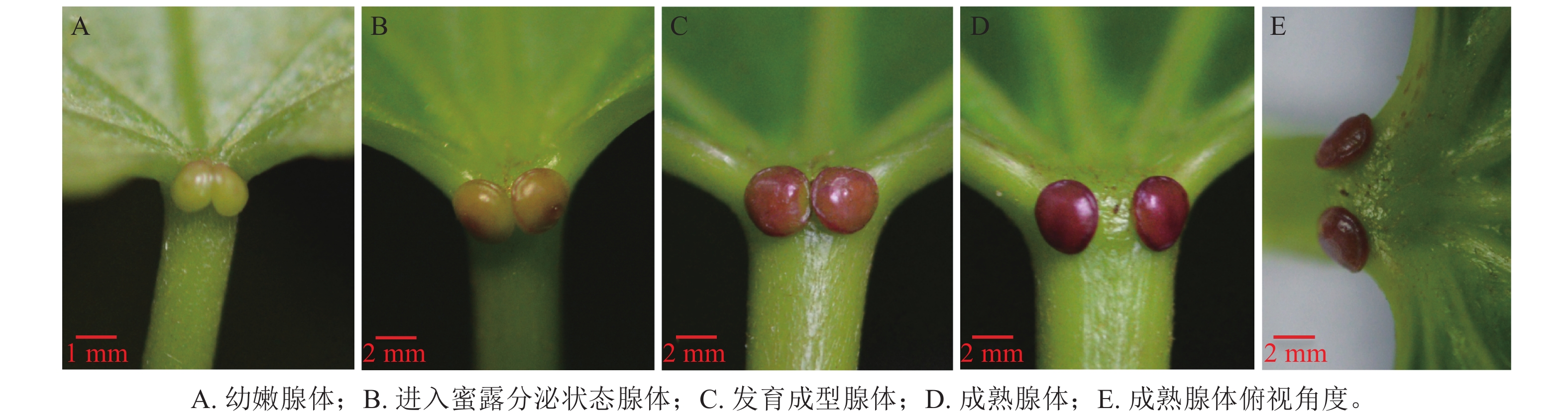
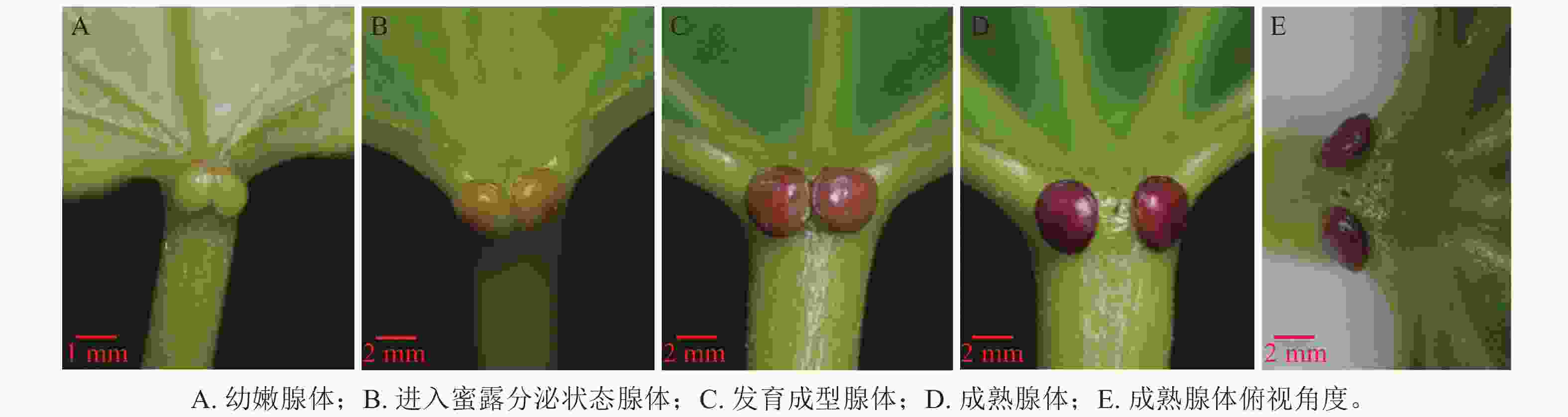
油桐花外蜜腺的形态结构特征如图1所示,可见位于叶柄顶部与叶片基部连接处的腺体区域表皮细胞明显不同于周围组织,形成独立功能单元。根据腺体形态特征及变化过程,初步划分为4个状态:幼嫩腺体、进入蜜露分泌的腺体、发育成型腺体、成熟腺体。幼嫩状态的腺体(图1A),叶柄基部对称出现2个椭圆形突起,体积较小,颜色呈淡绿色,分泌功能尚未发育完全;进入蜜露分泌状态腺体(图1B)形态逐渐饱满,表面呈褐绿色,分泌功能成熟,开始分泌蜜露;发育成型的腺体(图1C)呈现2个红色圆形突起,体积达到最大值,形态饱满;成熟状态的腺体(图1D)呈深红色,分泌功能减弱。从俯视角度观察(图1E),2个腺体间距扩大,分离明显,对称分布在叶柄两侧,随后可能进入生理功能衰退状态。
-
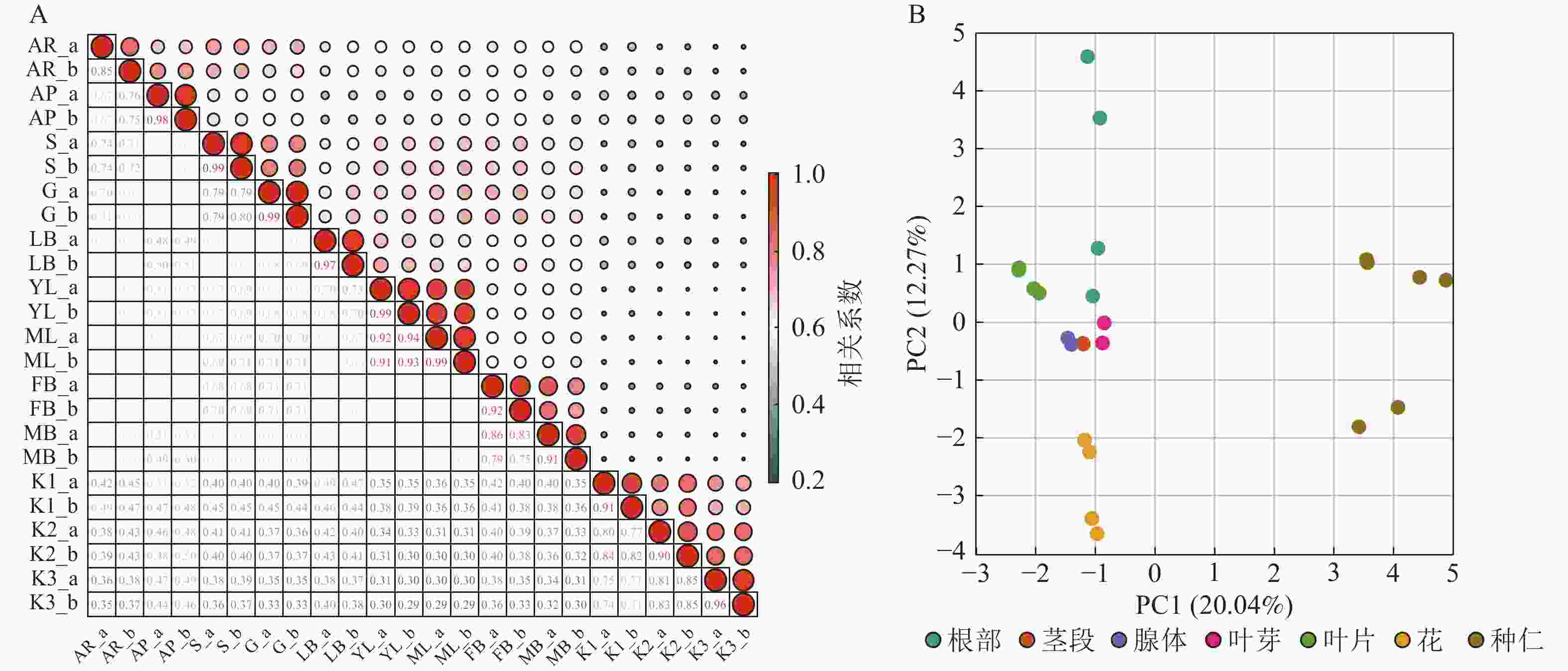
基于油桐不同部位与发育阶段组合的12个转录组样本中全部基因的VTPM值,计算样本间的表达相关系数。同一样本2个生物学重复的基因表达水平相关系数(r)为0.85~0.99(图2A),表明重复样本间相关性较好,可用于后续的WGCNA分析。PCA分析(图2B)显示:PC1(20.04%)和PC2(12.27%)共同解释了32.31%的基因表达变异,揭示了样本间的显著差异。种仁和根分别独立分布在右方和左上方,与其他部位距离最大;花位于左下方形成独特聚类;茎、腺体、叶芽、叶片则聚集于中间偏左区域,彼此距离较近,基因表达模式相似性较高,在PCA图上的广泛分布及显著距离,表明基因表达模式存在组织特化功能及生理代谢差异。此结果为后续挖掘腺体组织特异性基因及分子调控机制提供了重要依据。
-
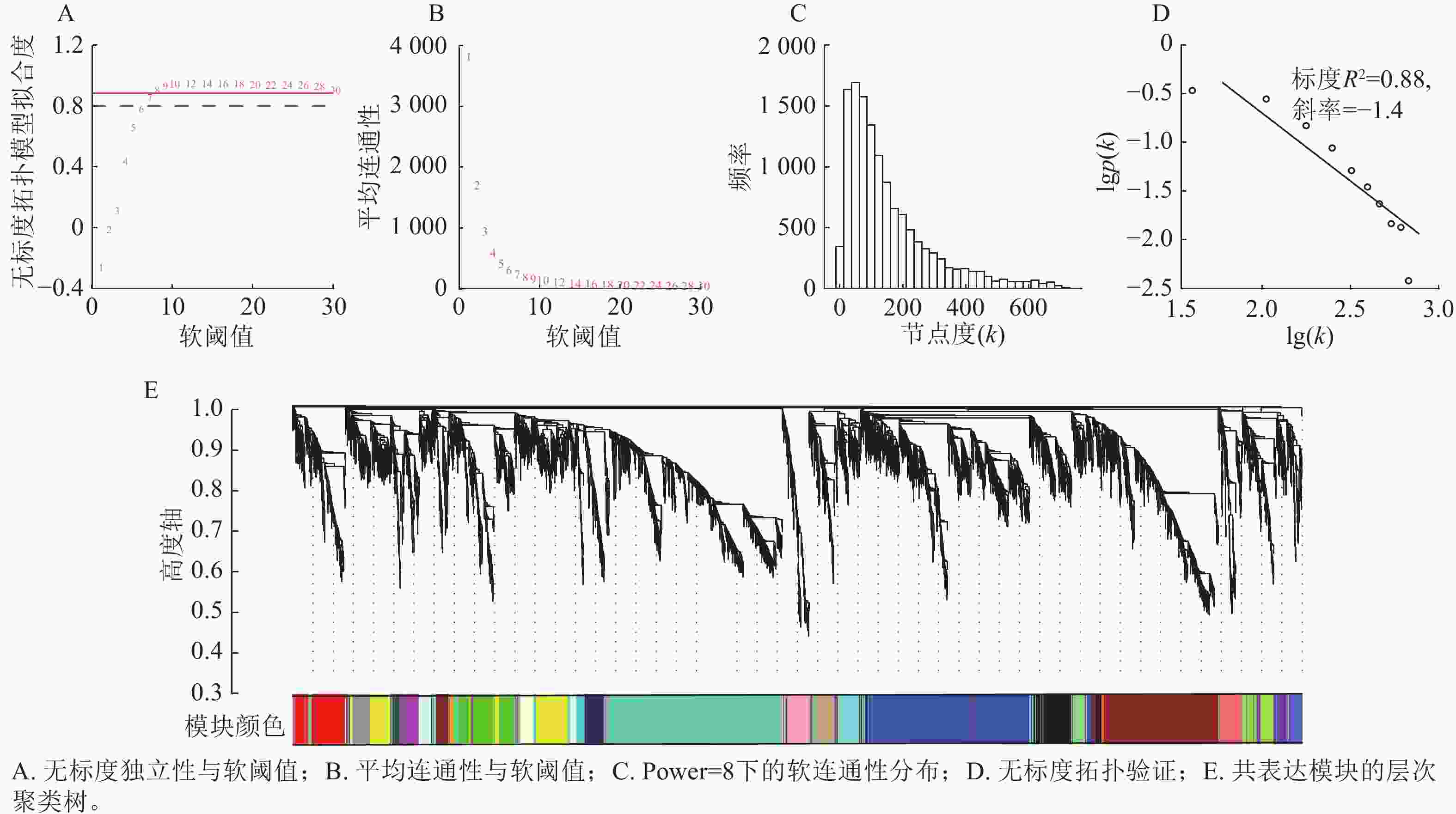
首先过滤去除平均表达值偏低(VTPM<5)的基因,最终选取12 943个基因作为输入集,进行WGCNA分析。由图3可知:当power=8时,无标度拓扑模型拟合度(R2)超过0.80 (图3A),平均连通性显著降低并趋于平缓(图3B);节点连接度的频率分布呈现“低连接度节点占多数,高连接度节点占少数”的无标度网络特征(图3C),且无尺度拓扑检验的标度(R2)为0.88(图3D)。综合表明:power=8适用于构建符合无尺度特性的基因共表达网络。以所有基因间的相异系数为基本元素构建分层聚类树,采用动态树切分法对基因进行模块划分,再通过计算各个模块的模块特征向量,对模块划分进行优化合并,最终得到27个基因共表达模块(图3E)。
-
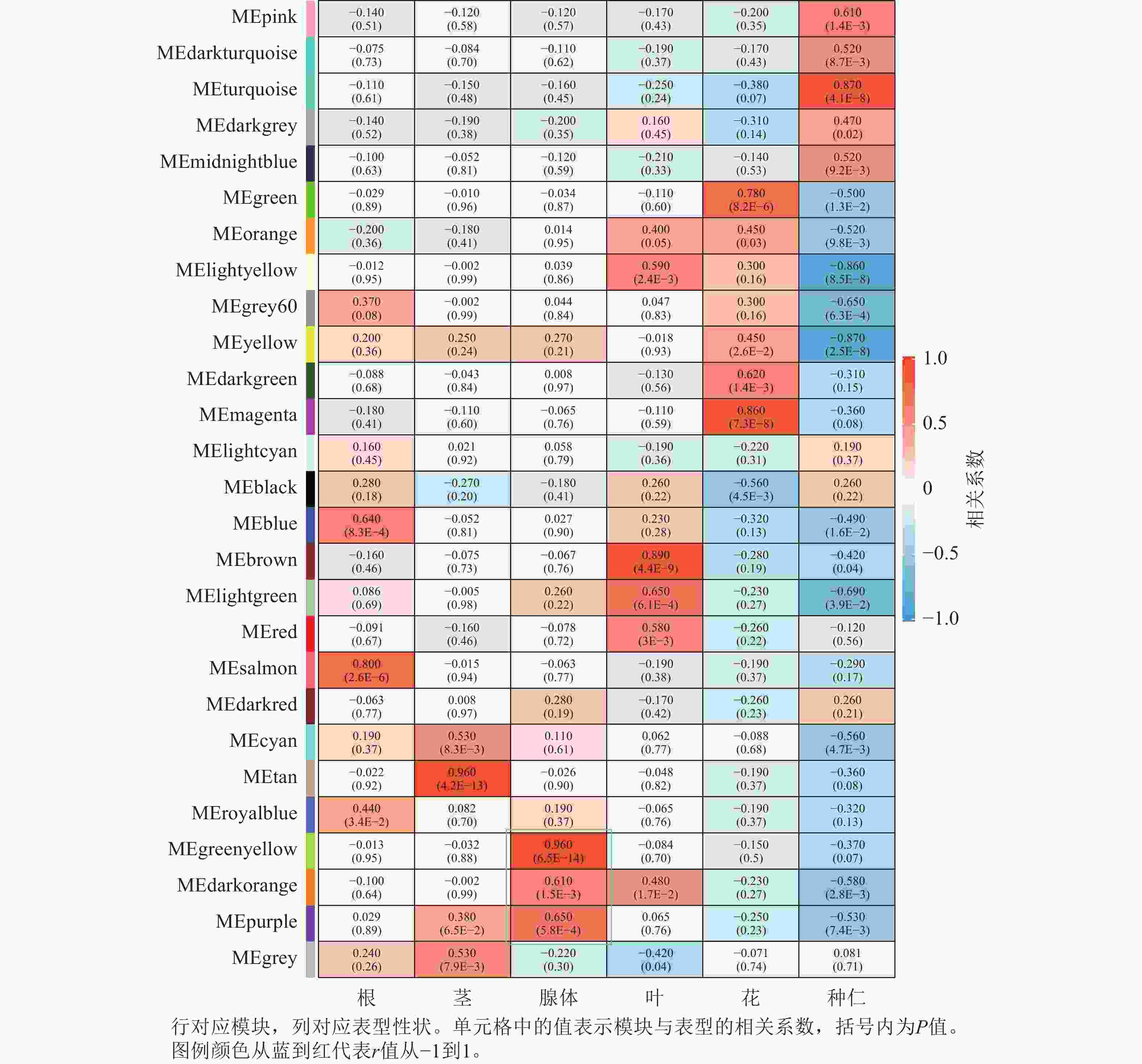
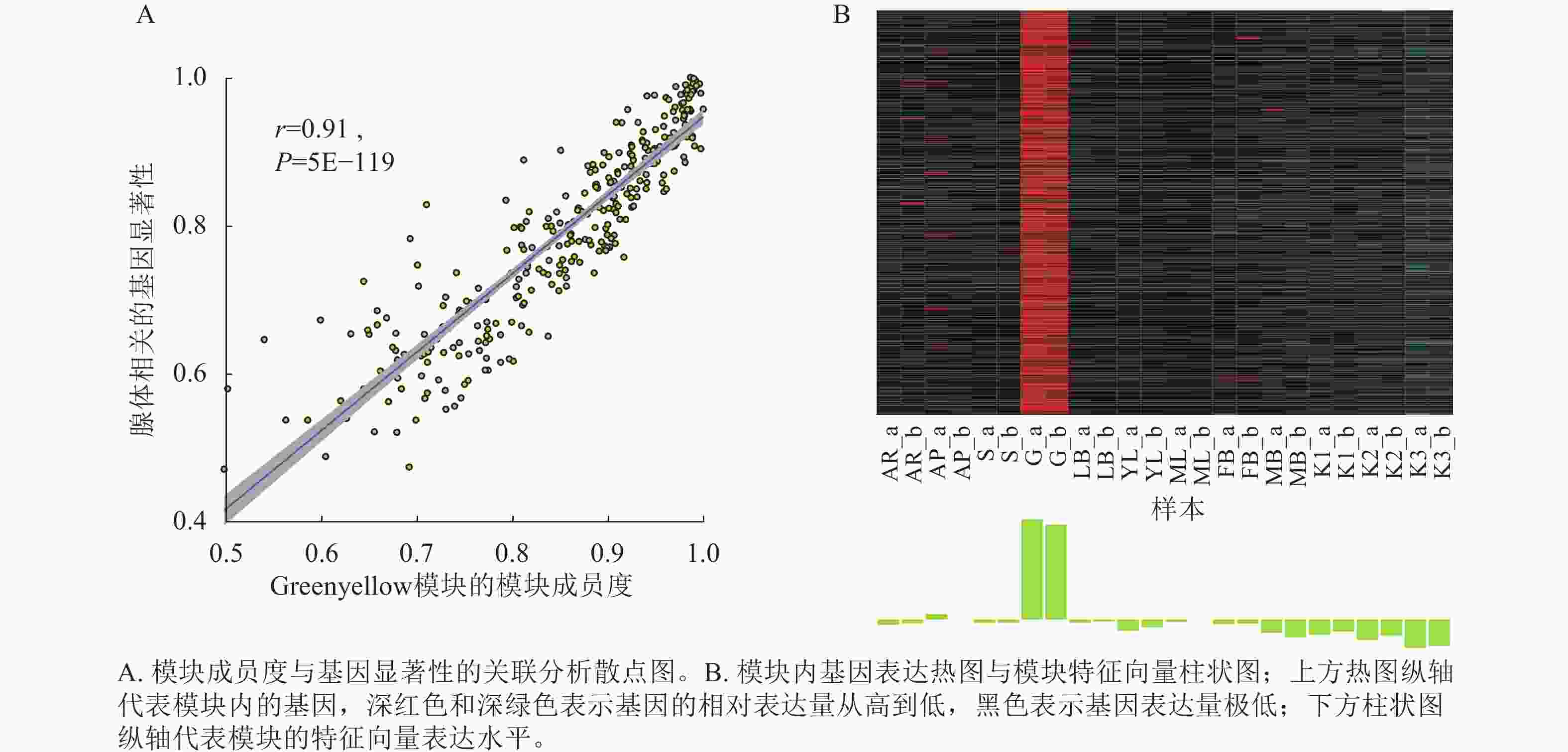
将基因不同共表达模块与油桐不同组织部位样本表型进行相关性分析(图4),将相关系数(r)>0.60的模块定义为关键模块,鉴定到greenyellow、darkorange和purple等3个与油桐腺体发育显著相关的模块。其中,油桐腺体与greenyellow模块(r=0.96,P=6.5E−14)呈极显著正相关,作为组织特异性模块进行后续分析。将greenyellow模块与其包含的308个基因进行相关性分析,计算所得相关系数,输出为散点图(图5A)。散点呈显著正相关分布,越位于右上角的基因,说明模块内基因的共表达程度越高,对性状的影响越强,可能是模块中驱动性状关联的枢纽基因,为后续腺体形成发育相关基因的筛选提供了可靠依据。图5B所示为greenyellow模块所有基因表达量热图与模块特征向量柱状图,上方热图以标准化后的颜色深浅梯度,直观呈现了模块内所有基因在样本中的表达丰度差异;下方柱状图是模块内所有基因表达模式的综合体现,其波动趋势与热图中基因整体表达模式高度契合,说明模块内基因表达的强协同性,也验证了模块特征向量的代表性,为后续模块功能解析奠定基础。
-
greenyellow模块本身包含非常多的基因,其中满足|GS|>0.6且|MM|>0.8的枢纽基因有154个。GO富集分析结果显示:greenyellow模块的枢纽基因主要涉及生长、细胞生长、蛋白质修饰过程、分解代谢、对光刺激的响应、对内源刺激的响应、对生物刺激的响应、胚后发育、解剖结构发育、生殖过程、多细胞生物发育和细胞分化等生物过程;转录调节因子活性和DNA结合转录因子活性等分子功能;膜和质膜等细胞组分(图6A)。KEGG富集分析表明:模块内枢纽基因显著富集于转运蛋白、泛素系统、信号转导及环境信息处理等相关通路(图6B)。
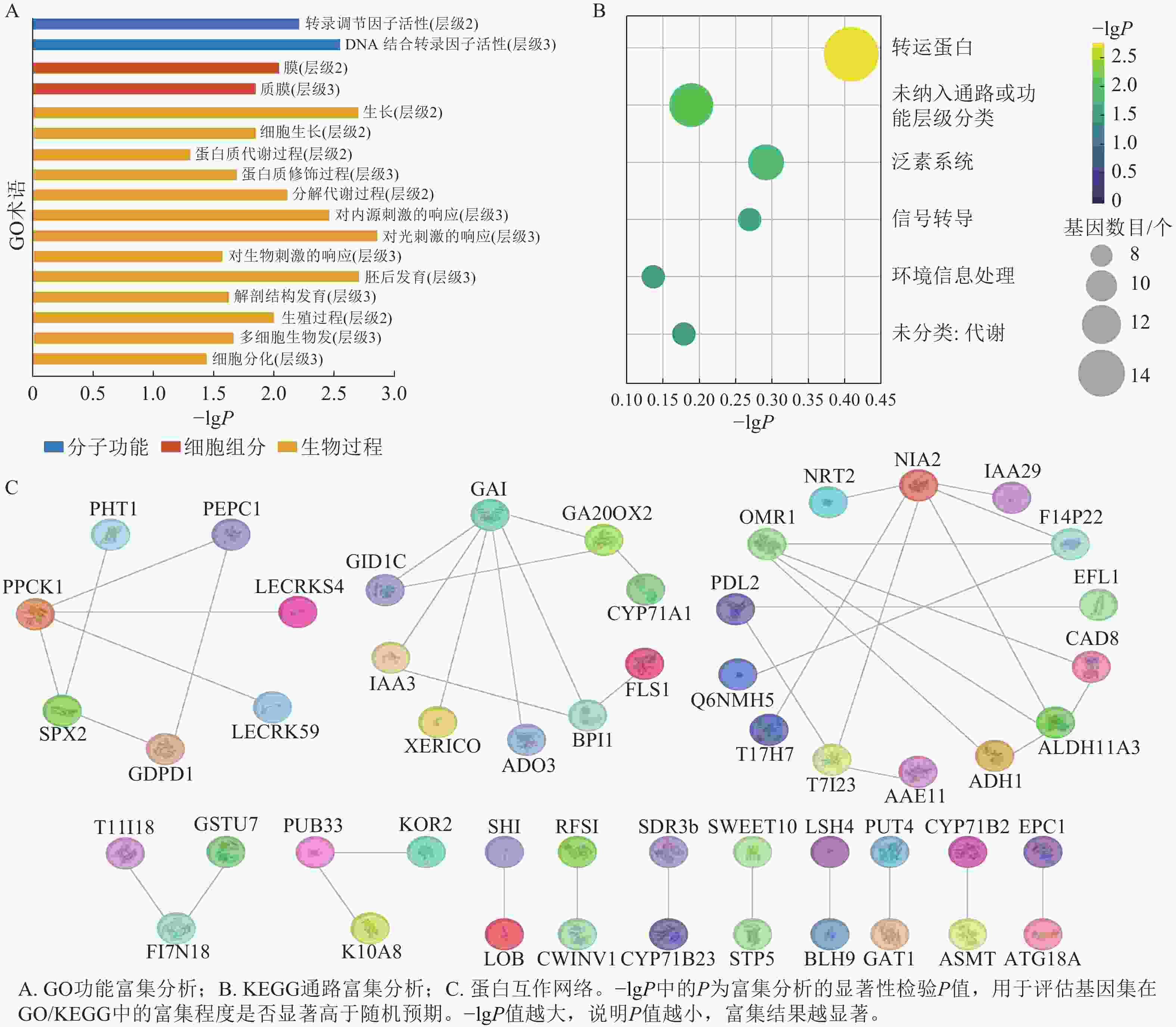
图 6 greenyellow模块枢纽基因的功能富集与蛋白互作网络
Figure 6. Functional enrichment analysis and protein-protein interaction network of hub genes in the greenyellow module
PPI网络(图6C)展示了枢纽基因编码蛋白的互作模式与功能聚类特征,其中包含PCK1、PEPC1等蛋白互作集群涉及磷转运、碳代谢相关功能;以GAI、IAA3为核心的互作集群富集了赤霉素合成、激素信号传导类蛋白;包含NIA2、OMR1等蛋白的互作集群涉及氮代谢与物质跨膜转运相关功能。此外,网络中还存在涉及转录调控、次生代谢等功能的小型互作集群(LOB、SWEET10等蛋白聚集区域)。不同功能类别的蛋白通过直接或间接的互作关系构建成关联网络,提示这些蛋白可能通过协同作用,共同参与油桐腺体发育过程中的激素调控、物质代谢、信号转导等生理进程。
根据greenyellow模块内基因的weight值与基因间的连通性构建基因互作网络,通过MCODE识别出24个高度关联的基因聚类(图7A),并绘制其表达热图(图7B)。从网络结构可见:SWEET10、ZAT10、CWINV1、LOB、CHI、SRS1、HDG5等基因对应的节点尺寸显著大于其他节点,可能在网络的调控过程中承担关键作用;不同功能基因通过广泛互作形成复杂调控网络,为解析油桐腺体发育的分子调控机制提供了基因互作层面的依据。最后,通过整合RNA-Seq基因表达数据、基因功能注释、PPI网络、基因互作网络聚类分析结果,并参考GO和KEGG富集分析,从greenyellow模块中最终筛选出6个候选基因,其对应的核苷酸序列(nucleotide,Nt)功能注释信息详见表3。
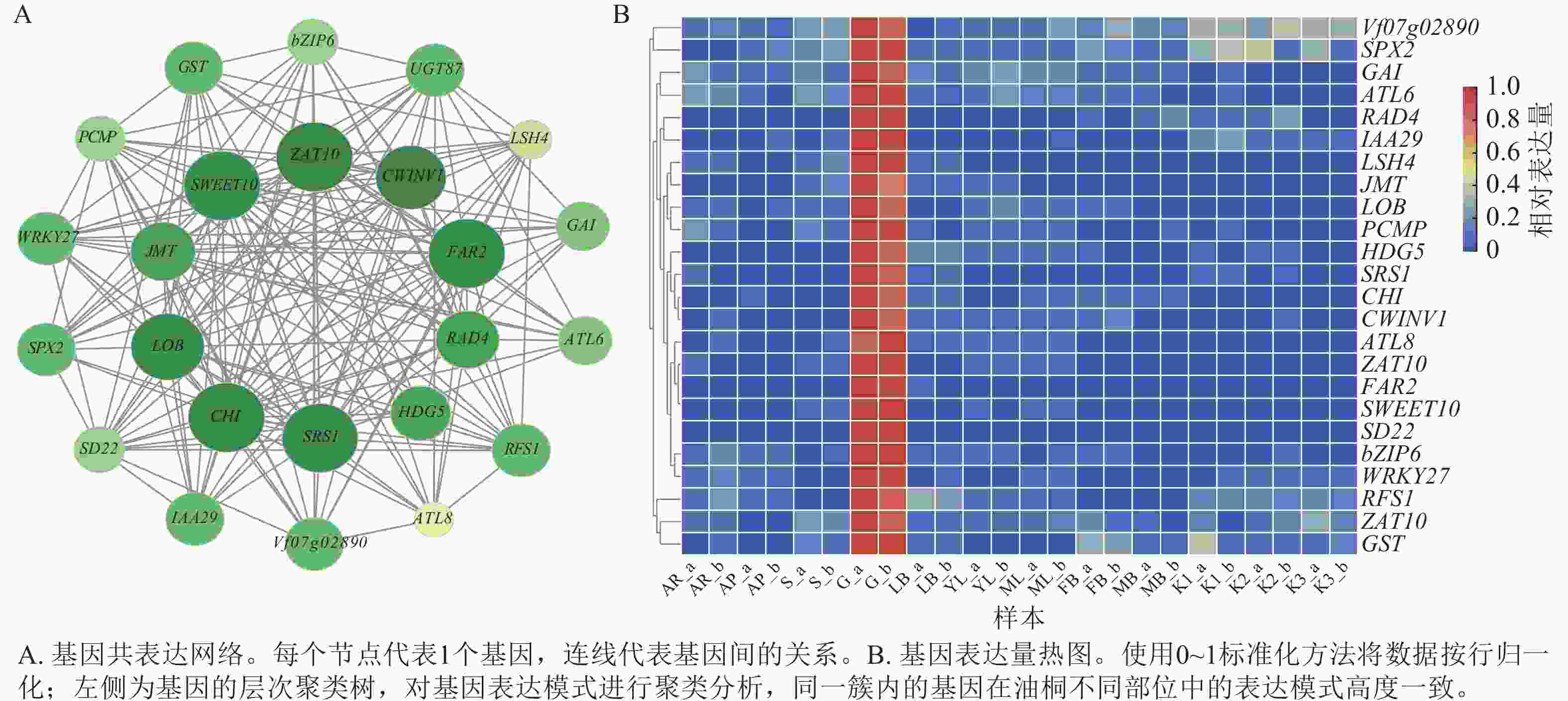
图 7 greenyellow模块候选基因表达分析
Figure 7. Functional enrichment and candidate gene expression in the greenyellow module
表 3 核心候选基因功能注释信息
Table 3. Functional term information of key candidate genes
基因ID 基因名称 功能注释 功能描述 Vf01g02365 LSH4 Light-dependent short hypocotyls 4 (Arabidopsis thaliana) LSH4参与光信号响应过程,并在植物器官发育中发挥重要作用[30]。 Vf04g00587 RAD4 RADIALIS-like 4 isoform X4 (Populus alba) RAD4属于MYB转录因子家族,功能涉及分生组织维持、器官形态建成及泛素化调控等过程[31]。 Vf04g00884 CHI Chitinase (Ricinus Communis) CHI作为分泌蜜露的PR-3类防御蛋白,可降解真菌细胞壁结构成分几丁质[32]。 Vf07g00391 HDG5 Homeobox-leucine zipper protein (Cannabis sativa) HDG5通过转录调控参与器官发育及胁迫适应[33]。 Vf10g01491 LOB LATERAL ORGAN BOUNDARIES (Jatropha curcas) LOB是调控侧生器官边界形成的核心转录因子,通过限制边界区细胞增殖维持器官分离[34]。 Vf10g01688 SWEET10 Bidirectional sugar transporter SWEET10 (Populus alba) SWEET10是糖转运蛋白,功能涉及源–库运输、介导赤霉素转运及生物和非生物胁迫反应等[35−36]。 -
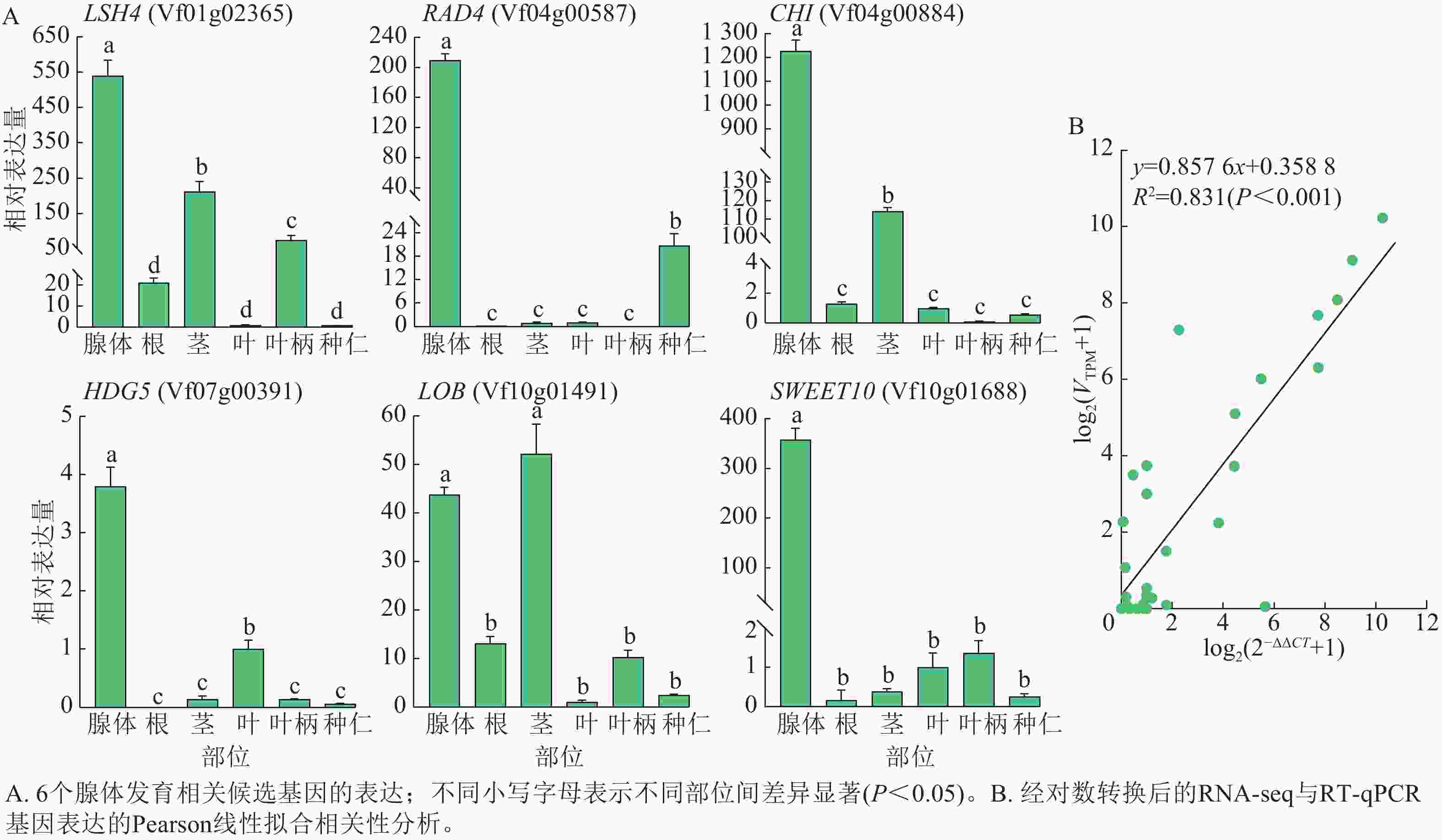
从以上结果中,选择可能与油桐腺体形成发育相关的6个核心候选基因LSH4、RAD4、GHI、HDG5、LOB和SWEET10,在油桐腺体、根、茎、叶、叶柄、种仁等6个组织中进行RT-qPCR验证(图8A)。其中,RAD4、HDG5、SWEET10均在腺体中呈现高表达特征,在叶片、种仁中的表达水平显著低于腺体,在根、茎段、叶柄等组织中仅呈低水平表达;LSH4、GHI在腺体中表达最高,茎段次之,其他组织表达极低;LOB在茎段中表达量略高于腺体。推测RAD4、GHI和SWEET10可能在腺体形成发育过程中发挥着重要的调控作用。此外,图8B的线性拟合相关性分析显示:经对数转换后的RT-qPCR相对表达量与RNA-seq表达量呈显著相关(R2=0.831,P<0.001),表明RNA-Seq数据具有较高的准确性。
-
植物腺体种类丰富、结构多样,具有重要的生态功能和分类学价值。蜜腺是植物体上一种常见的分泌蜜露的外分泌结构,是植物在长期演化过程中,适应获取异源基因、保证繁衍和进化而形成的一种特殊腺体[37]。花蜜腺是被子植物吸引昆虫访花的重要媒介物,而花外蜜腺同样能吸引传粉昆虫访花[38]。接骨草Sambucus javanica两性花无蜜腺结构,其花外蜜腺在花盛开时十分活跃,呈鲜艳的橘黄色并分泌大量蜜露,弥补了这一缺陷,吸引了大量传粉昆虫[39]。植物还可通过花外蜜腺提供的蜜露来吸引蚂蚁、蜘蛛、寄生蜂等,保护植物免受草食者或真菌的危害[40]。有研究表明:蚂蚁的存在能降低植物叶片受到的侵害和花器官被损害的程度[41]。在大戟属Euphorbia植物的分类中,植物的习性、营养器官的形态、体内所含乳汁的颜色以及花序、果实和种子的特征等均可为划分类群提供依据,但其腺体所具有的分类学意义尤其特别[42]。油桐叶柄与叶片连接处为2个扁平的无柄腺体,其同属的千年桐Vernicia montana不仅叶柄顶端有2个杯状腺体,在叶片深裂处也可观察到微小的杯状腺体[3],两者腺体着生位置、形状、数量及颜色所存在的差异可作为分类的重要依据之一。
WGCNA是一种系统分析多个样本间基因表达模式的方法。近年来,WGCNA被广泛用于植物器官形态建成以及发育调控中关键通路、基因的发掘。本研究通过对不同组织部位的转录组数据进行WGCNA分析,获得了与腺体发育显著相关的组织特异性表达模块。GO/KEGG富集分析表明:模块内枢纽基因涉及生长、细胞分化、解剖结构发育、蛋白质代谢、生物胁迫响应等生物过程,富集于转运蛋白、泛素系统、信号转导及环境信息处理等相关通路。有研究表明:RAD-like基因对于兰科Orchidaceae植物花两侧对称的正常发育是必需的,通过与CYC2等基因协同作用,调控器官在空间上的不对称分化与边界建立[43]。值得注意的是,油桐腺体在叶柄两侧呈现稳定的对称分布特征,这在形态学上与花两侧对称具有一定相似性。RAD4在油桐腺体中的显著组织特异性表达,推测RAD4基因可能在油桐腺体对称分布及形成发育过程发挥潜在的调控作用。对蓖麻花外蜜腺的蛋白质组分析发现:其分泌蜜露中含有复杂的蛋白混合物,包括防御相关几丁质酶和β-1,3-葡聚糖酶,以及多种水解酶[32]。由GHI编码的几丁质酶属于PR-3类防御蛋白,能够降解真菌细胞壁的结构成分几丁质,从而破坏其结构抑制真菌生长,可与β-1,3-葡聚糖酶、抗菌肽等一起形成多层防御体系,防止蜜露被微生物快速消耗或污染。毛果杨Populus trichocarpa的花是风媒花,缺少功能花内蜜腺,具有花外蜜腺,存在SWEET10同源基因,且毛果杨花外蜜腺富含己糖[44]。蜜露的合成与分泌过程高度依赖SWEET蛋白家族介导的糖分跨膜运输[36],以及蛋白质修饰、萜类合成等次生代谢通路的协同作用,共同维持腺体的功能完整性。RT-qPCR验证结果显示:RAD4、GHI、SWEET10等基因在油桐腺体中呈显著高表达。这一结果也证明,通过WGCNA方法鉴定的油桐腺体相关组织特异性模块及核心基因具有一定的准确性和可参考性,为后续深入解析腺体形成发育机理奠定了坚实基础。
-
基于油桐不同组织部位与发育阶段组合的RNA-Seq数据进行WGCNA分析,鉴定到1个与腺体相关组织特异性模块(greenyellow模块)。通过对模块内枢纽基因进行GO/KEGG富集分析、蛋白互作网络构建和基因互作网络聚类分析,筛选获得6个候选基因;经RT-qPCR表达验证,进一步鉴定出RAD4、GHI、SWEET10等与腺体形成及发育密切相关的核心基因。
Analysis of tissue-specific expressed genes in gland of Vernicia fordii
-
摘要:
目的 挖掘油桐Vernicia fordii腺体发育相关的组织特异性模块并筛选核心基因,为后续深入解析腺体发生机制奠定基础,并为植物分泌组织(如分泌腔、腺毛)的发育机制研究提供理论依据。 方法 基于油桐12个组织部位与发育阶段组合样本的转录组测序(RNA-seq)数据,结合加权基因共表达网络分析(WGCNA),鉴定腺体相关组织特异性模块;通过模块内枢纽基因的功能富集分析、蛋白互作网络构建和基因互作网络聚类分析,筛选核心基因;利用实时荧光定量逆转录PCR (RT-qPCR)验证基因在油桐不同部位中的表达模式。 结果 WGCNA分析将过滤后的12 943个基因划分为27个共表达模块,获得与腺体高度相关的greenyellow模块。参考基因本体论数据库(GO)与京都基因与基因组百科全书(KEGG)富集分析表明:模块内枢纽基因涉及生长、解剖结构发育、细胞分化、蛋白质代谢、光信号感知反应、生物胁迫响应等生物过程,富集于转运蛋白、泛素系统、信号转导及环境信息处理等相关通路。根据模块内基因的互作网络以及基因功能注释,筛选得到LSH4、RAD4、GHI、HDG5、LOB、SWEET10等基因可能在腺体发育中起关键调控作用。RT-qPCR验证结果显示:候选基因在油桐不同部位中的表达呈现显著的组织特异性,其表达趋势与RNA-seq数据高度吻合。 结论 鉴定到1个与腺体相关组织特异性模块,筛选到RAD4、GHI、SWEET10等与腺体形成发育密切相关的核心基因。图8表3参44 -
关键词:
- 油桐 /
- 腺体 /
- 转录组测序 /
- 加权基因共表达网络分析
Abstract:Objective The objective is to identify tissue-specific modules related to gland development in Vernicia fordii and to screen core regulatory genes, so as to lay a foundation for further in-depth analysis of gland ontogenesis and provide theoretical support for the study of the developmental mechanisms of plant secretory tissues such as secretory cavities and glandular trichomes. Method Based on transcriptome sequencing (RNA-seq) data of 12 tissue parts and developmental stage combination samples of V. fordii, combined with weighted gene co-expression network analysis (WGCNA), the tissue-specific modules related to glands were identified. Core genes were screened through functional enrichment analysis of hub genes within the module, protein-protein interaction (PPI) network construction, and gene interaction network clustering analysis. Quantitative reverse transcription PCR (RT-qPCR) was subsequently applied to verify the expression patterns of candidate genes in different parts of the tree. Result WGCNA clustered the 12 943 filtered genes into 27 co-expression modules, and identified the greenyellow module that was highly related to the gland development. Gene Ontology (GO) and Kyoto Encyclopedia of Genes and Genomes (KEGG) enrichment analysis revealed that hub genes within this module were mainly involved in biological processes such as growth, anatomical structure development, cell differentiation, protein metabolism, light signal perception response, and biotic stress response, and were enriched in related pathways such as transporters, the ubiquitin system, signal transduction, and environmental information processing. Based on the interaction network of genes within the module and gene functional annotations, several genes such as LSH4, RAD4, HDG5, GHI, LOB, and SWEET10 were identified as potential key regulators in gland development. RT-qPCR verification results showed that the expression of each candidate gene in different parts of V. fordii exhibited significant tissue specificity, and its expression trend was highly consistent with the RNA-Seq data. Conclusion One tissue-specific module related to gland is identified, and core genes (RAD4, GHI, SWEET10), which are closely related to gland formation and development, are screened. [Ch, 8 fig. 3 tab. 44 ref.] -
表 1 油桐样本信息
Table 1. Sample information of V. fordii
组织部位 样本编号 采样时间 组织部位 样本编号 采样时间 主根 AR_a、AR_b 2023-12-02 成熟叶片 ML_a、ML_b 2023-06-16 根尖 AP_a、AP_b 2023-12-02 雌花苞 FB_a、FB_b 2023-04-15 当年生枝条 S_a、S_b 2023-06-16 雄花苞 MB_a、MB_b 2023-04-15 腺体 G_a、G_b 2023-06-16 种仁发育初期 K1_a、K1_b 2023-07-01 叶芽 LB_a、LB_b 2023-06-16 种仁发育中期 K2_a、K2_b 2023-08-08 幼嫩叶片 YL_a、YL_b 2023-06-16 种仁发育后期 K3_a、K3_b 2023-08-22 说明:a、b表示2个重复。 表 2 RT-qPCR引物序列
Table 2. Primers used for RT-qPCR
基因 ID 基因名称 正向引物(5′→3′) 反向引物(5′→3′) Vf01g02365 LSH4 ACTACCGCTATCTCAATGGG AGAGAAAGTGGTGGCCTATG Vf04g00587 RAD4 GAAATTACTCTCCTTGGACTCC CACGACCAGACTCAATATGC Vf07g00391 HDG5 TGCAAGTGGTTCTCTTCACC ATTGCCCAGGTTCCTTCTTC Vf04g00884 GHI AATCTTCCTTGTGCCGCTAG CGCATCTGTCCAAGCATTTC Vf10g01491 LOB TCAAAGGCTCCAGAAGGAAC TTGGCGATGATGATGAGGAG Vf10g01688 SWEET10 TTGCACCTCTTGGCATTGTG GGAACAGCAACGAAAAGGTC EF1α GCCTGGTATGGTTGTGACCT GGATCATCCTTGGAGTTGGA 表 3 核心候选基因功能注释信息
Table 3. Functional term information of key candidate genes
基因ID 基因名称 功能注释 功能描述 Vf01g02365 LSH4 Light-dependent short hypocotyls 4 (Arabidopsis thaliana) LSH4参与光信号响应过程,并在植物器官发育中发挥重要作用[30]。 Vf04g00587 RAD4 RADIALIS-like 4 isoform X4 (Populus alba) RAD4属于MYB转录因子家族,功能涉及分生组织维持、器官形态建成及泛素化调控等过程[31]。 Vf04g00884 CHI Chitinase (Ricinus Communis) CHI作为分泌蜜露的PR-3类防御蛋白,可降解真菌细胞壁结构成分几丁质[32]。 Vf07g00391 HDG5 Homeobox-leucine zipper protein (Cannabis sativa) HDG5通过转录调控参与器官发育及胁迫适应[33]。 Vf10g01491 LOB LATERAL ORGAN BOUNDARIES (Jatropha curcas) LOB是调控侧生器官边界形成的核心转录因子,通过限制边界区细胞增殖维持器官分离[34]。 Vf10g01688 SWEET10 Bidirectional sugar transporter SWEET10 (Populus alba) SWEET10是糖转运蛋白,功能涉及源–库运输、介导赤霉素转运及生物和非生物胁迫反应等[35−36]。 -
[1] 史良. 发展油桐生产[J]. 浙江农业科学, 1962(1): 42−44. SHI Liang. Developing tung tree (Vernicia fordii) production[J]. Journal of Zhejiang Agricultural Sciences, 1962(1): 42−44. [2] 陈益存. 加强科技支撑 拓展油桐产业的“钱库”功能[J]. 中国农村科技, 2022(11): 58−60. CHEN Yicun. Strengthening scientific and technological support and expanding the “Qian Ku” function of tung oil industry[J]. China Rural Science & Technology, 2022(11): 58−60. [3] 方嘉兴, 何方, 姚小华. 中国油桐[M]. 2版. 北京: 中国林业出版社, 2017. FANG Jiaxing, HE Fang, YAO Xiaohua. Chinese Tung Oil Tree[M]. 2nd ed. Beijing: China Forestry Publishing House, 2017. [4] SUISSA J S, LI F W, MOREAU C S. Convergent evolution of fern nectaries facilitated independent recruitment of ant-bodyguards from flowering plants[J]. Nature Communications, 2024, 15: 4392. DOI: 10.1038/s41467-024-48646-x. [5] 胡书婧, 张汝民. 挥发性有机化合物在植物适应胁迫及生理生态中的作用[J]. 浙江农林大学学报, 2022, 39(6): 1378−1387. HU Shujing, ZHANG Rumin. Roles of volatile organic compounds in plant adaptation to stress and physiological ecology[J]. Journal of Zhejiang A&F University, 2022, 39(6): 1378−1387. DOI: 10.11833/j.issn.2095-0756.20220180. [6] HEIL M. Extrafloral nectar at the plant-insect interface: a spotlight on chemical ecology, phenotypic plasticity, and food webs[J]. Annual Review of Entomology, 2015, 60: 213−232. DOI: 10.1146/annurev-ento-010814-020753. [7] MARAZZI B, BRONSTEIN J L, KOPTUR S. The diversity, ecology and evolution of extrafloral nectaries: current perspectives and future challenges[J]. Annals of Botany, 2013, 111(6): 1243−1250. DOI: 10.1093/aob/mct109. [8] LIU Jingxin, CHEN Jin. Preliminary investigation of extrafloral nectaried plants in the tropical rainforests in Xishuangbanna, China[J]. Acta Botanica Yunnanica, 2008, 30(2): 173−182. DOI: 10.3969/j.issn.2095-0845.2008.02.008. [9] JONES I M, KOPTUR S, VON WETTBERG E J. The use of extrafloral nectar in pest management: overcoming context dependence[J]. Journal of Applied Ecology, 2017, 54(2): 489−499. DOI: 10.1111/1365-2664.12778. [10] BLÜTHGEN N, FIEDLER K. Preferences for sugars and amino acids and their conditionality in a diverse nectar-feeding ant community[J]. Journal of Animal Ecology, 2004, 73(1): 155−166. DOI: 10.1111/j.1365-2656.2004.00789.x. [11] TILNEY P M, NEL M, VAN WYK A E. Foliar secretory structures in Ekebergia capensis (Meliaceae)[J]. Heliyon, 2018, 4(2): e00541. DOI: 10.1016/j.heliyon.2018.e00541. [12] MAXIMO D, FERREIRA M J P, DEMARCO D. Inaugural description of extrafloral nectaries in Sapindaceae: structure, diversity and nectar composition[J]. Plants, 2023, 12(19): 3411. DOI: 10.3390/plants12193411. [13] PAIVA É A S, ANDRADE BUONO R, NEVES DELGADO M. Distribution and structural aspects of extrafloral nectaries in Cedrela fissilis (Meliaceae)[J]. Flora-Morphology, Distribution, Functional Ecology of Plants, 2007, 202(6): 455−461. DOI: 10.1016/j.flora.2006.11.001. [14] de FREITAS-SILVA L, de ARAÚJO H H, MEIRA R M S A, et al. Morphoanatomy, histochemical and secretions process of extrafloral nectaries in Joannesia princeps Vell. (Euphorbiaceae)[J]. Flora, 2023, 306: 152354. DOI: 10.1016/j.flora.2023.152354. [15] LONG Lu, ZHANG Zhennan, XU Fuchun, et al. The GhANT-GoPGF module regulates pigment gland development in cotton leaves[J]. Cell Reports, 2025, 44(1): 115112. DOI: 10.1016/j.celrep.2024.115112. [16] WANG Hongxing, REN Jie, ZHOU Shiyun, et al. Molecular regulation of oil gland development and biosynthesis of essential oils in Citrus spp.[J]. Science, 2024, 383(6683): 659−666. DOI: 10.1126/science.adl2953. [17] CHEN Shifu, ZHOU Yanqing, CHEN Yaru, et al. Fastp: an ultra-fast all-in-one FASTQ preprocessor[J]. Bioinformatics, 2018, 34(17): i884−i890. DOI: 10.1093/bioinformatics/bty560. [18] BOLGER A M, LOHSE M, USADEL B. Trimmomatic: a flexible trimmer for Illumina sequence data[J]. Bioinformatics, 2014, 30(15): 2114−2120. DOI: 10.1093/bioinformatics/btu170. [19] KIM D, LANGMEAD B, SALZBERG S L. HISAT: a fast spliced aligner with low memory requirements[J]. Nature Methods, 2015, 12(4): 357−360. DOI: 10.1038/nmeth.3317. [20] ZHANG Lin, LIU Meilan, LONG Hongxu, et al. Tung tree (Vernicia fordii) genome provides a resource for understanding genome evolution and improved oil production[J]. Genomics, Proteomics & Bioinformatics, 2019, 17(6): 558−575. DOI:10.1016/j.gpb.2019.03.006. [21] LIAO Yang, SMYTH G K, SHI Wei. The R package Rsubread is easier, faster, cheaper and better for alignment and quantification of RNA sequencing reads[J]. Nucleic Acids Research, 2019, 47(8): e47. DOI: 10.1093/nar/gkz114. [22] LI Xianhong, LI Jingru, ZHAO Qiancheng, et al. Physiological, biochemical, and genomic elucidation of the Ensifer adhaerens M8 strain with simultaneous arsenic oxidation and chromium reduction[J]. Journal of Hazardous Materials, 2023, 441: 129862. DOI: 10.1016/j.jhazmat.2022.129862. [23] CHEN Chengjie, WU Ya, LI Jiawei, et al. TBtools-II: a “one for all, all for one” bioinformatics platform for biological big-data mining[J]. Molecular Plant, 2023, 16(11): 1733−1742. DOI: 10.1016/j.molp.2023.09.010. [24] WANG Xiao, LIANG Shuang, YANG Wenqi, et al. MetMiner: a user-friendly pipeline for large-scale plant metabolomics data analysis[J]. Journal of Integrative Plant Biology, 2024, 66(11): 2329−2345. DOI: 10.1111/jipb.13774. [25] 李旭娟, 李纯佳, 刘洪博, 等. 甘蔗腋芽形成发育过程的转录组分析[J]. 生物技术通报, 2025, 41(3): 202−218. LI Xujuan, LI Chunjia, LIU Hongbo, et al. Transcriptome analysis of axillary bud formation and development in sugarcane[J]. Biotechnology Bulletin, 2025, 41(3): 202−218. DOI: 10.13560/j.cnki.biotech.bull.1985.2024-0755. [26] SZKLARCZYK D, MORRIS J H, COOK H, et al. The STRING database in 2017: quality-controlled protein-protein association networks, made broadly accessible[J]. Nucleic Acids Research, 2017, 45(D1): D362−D368. DOI: 10.1093/nar/gkw937. [27] SHANNON P, MARKIEL A, OZIER O, et al. Cytoscape: a software environment for integrated models of biomolecular interaction networks[J]. Genome Research, 2003, 13(11): 2498−2504. DOI: 10.1101/gr.1239303. [28] BADER G D, HOGUE C W. An automated method for finding molecular complexes in large protein interaction networks[J]. BMC Bioinformatics, 2003, 4(1): 2. DOI: 10.1186/1471-2105-4-2. [29] HAN Xiaojiao, LU Mengzhu, CHEN Yicun, et al. Selection of reliable reference genes for gene expression studies using real-time PCR in tung tree during seed development[J]. PLoS One, 2012, 7(8): e43084. DOI: 10.1371/journal.pone.0043084. [30] TAKEDA S, HANANO K, KARIYA A, et al. CUP-SHAPED COTYLEDON1 transcription factor activates the expression of LSH4 and LSH3 two members of the ALOG gene family, in shoot organ boundary cells[J]. The Plant Journal, 2011, 66(6): 1066−1077. DOI: 10.1111/j.1365-313X.2011.04571.x. [31] RAIMUNDO J, SOBRAL R, BAILEY P, et al. A subcellular tug of war involving three MYB-like proteins underlies a molecular antagonism in Antirrhinum flower asymmetry[J]. The Plant Journal, 2013, 75(4): 527−538. DOI: 10.1111/tpj.12225. [32] NOGUEIRA F C S, FARIAS A R B, TEIXEIRA F M, et al. Common features between the proteomes of floral and extrafloral nectar from the Castor plant (Ricinus communis) and the proteomes of exudates from carnivorous plants[J]. Frontiers in Plant Science, 2018, 9: 549. DOI: 10.3389/fpls.2018.00549. [33] HANCOCK J, LIVINGSTON S J, SAMUELS L. Building a biofactory: constructing glandular trichomes in Cannabis sativa[J]. Current Opinion in Plant Biology, 2024, 80: 102549. DOI: 10.1016/j.pbi.2024.102549. [34] JHU M Y, ICHIHASHI Y, FARHI M, et al. Lateral organ boundaries domain 25 functions as a key regulator of haustorium development in dodders[J]. Plant Physiology, 2021, 186(4): 2093−2110. DOI: 10.1093/plphys/kiab231. [35] KANNO Y, OIKAWA T, CHIBA Y, et al. AtSWEET13 and AtSWEET14 regulate gibberellin-mediated physiological processes[J]. Nature Communications, 2016, 7: 13245. DOI: 10.1038/ncomms13245. [36] 张计育, 王刚, 王涛, 等. SWEET蛋白在植物生长发育中的功能作用研究进展[J]. 植物资源与环境学报, 2023, 32(5): 1−15. ZHANG Jiyu, WANG Gang, WANG Tao, et al. Research progress on functional roles of SWEET proteins in plant growth and development[J]. Journal of Plant Resources and Environment, 2023, 32(5): 1−15. DOI: 10.3969/j.issn.1674-7895.2023.05.01. [37] HEIL M. Nectar: generation, regulation and ecological functions[J]. Trends in Plant Science, 2011, 16(4): 191−200. DOI: 10.1016/j.tplants.2011.01.003. [38] YAMASAKI E, KAWAKITA A, SAKAI S. Modified leaves with disk-shaped nectaries of Macaranga sinensis (Euphorbiaceae) provide reward for pollinators[J]. American Journal of Botany, 2013, 100(3): 628−632. DOI: 10.3732/ajb.1200600. [39] 李琳. 接骨草花外蜜腺特征及其对传粉效率的影响[D]. 雅安: 四川农业大学, 2022. LI Lin. Study on the Characteristics and Pollination Efficiency of the Extrafloral Nectaries in Sambucus javanica (Caprifoliaceae) [D]. Ya’an: Sichuan Agricultural University, 2022. [40] VILLAMIL N, BOEGE K, STONE G N. Testing the distraction hypothesis: do extrafloral nectaries reduce ant-pollinator conflict?[J]. Journal of Ecology, 2019, 107(3): 1377−1391. DOI: 10.1111/1365-2745.13135. [41] KOST C, HEIL M. Increased availability of extrafloral nectar reduces herbivory in lima bean plants (Phaseolus lunatus, Fabaceae)[J]. Basic and Applied Ecology, 2005, 6(3): 237−248. DOI: 10.1016/j.baae.2004.11.002. [42] 赵志礼, 赵汝能. 大戟属植物腺体的分类学意义[J]. 植物杂志, 1992(4): 38−39. ZHAO Zhili, ZHAO Runeng. Taxonomic significance of glands in Euphorbia[J]. Plants, 1992(4): 38−39. [43] ZHONG Jinshun, KELLOGG E A. Stepwise evolution of Corolla symmetry in CYCLOIDEA2-like and RADIALIS-like gene expression patterns in Lamiales[J]. American Journal of Botany, 2015, 102(8): 1260−1267. DOI: 10.3732/ajb.1500191. [44] ESCALANTE-PÉREZ M, JABORSKY M, LAUTNER S, et al. Poplar extrafloral nectaries: two types, two strategies of indirect defenses against herbivores[J]. Plant Physiology, 2012, 159(3): 1176−1191. DOI: 10.1104/pp.112.196014. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20250540






 下载:
下载: