-
种群结构是种群生态学的重要研究内容,其中年龄结构[1]、静态生命表和存活曲线是反映种群现状及存活、死亡过程的重要特征指标[2]。辽东栎Quercus wutaishanica是中国暖温带地带性植被和常见的落叶阔叶优势树种,分布范围较广,具有耐严寒、耐干旱、耐贫瘠的特点,主要分布在中国华北地区,其中,辽东栎天然次生林是六盘山区的顶级群落,辽东栎作为群落主要树种或优势树种,其生长状况和种群结构特征等可以帮助识别当地自然环境特征,因此,以往关于辽东栎的研究主要集中在辽东栎种群结构和空间分布格局等方面[3-8]。伊力塔等[3]通过分析不同群落类型下辽东栎的点格局发现:在辽东栎种群不断成长过程中,其分布特征由聚集分布变为随机分布。张育新等[4]研究表明:分析种群空间格局分布有助于准确认识种群生物学及生态学特性。MASAKI等[5]对群落中优势种的种群结构及空间分布进行了研究。胡尔查等[6]分析了乌拉山白桦Betula platyphylla的种群结构,认为在生存环境相似时,自身生物学和生态学特性是影响分布格局的最主要因素。王道亮等[7]通过研究黄龙山林区辽东栎天然次生林发现:格局分布与尺度大小密切相关。研究种群空间结构能够反映群落的生境条件和种群本身生物学特性之间的相互影响,同时揭示森林的天然更新机制以及发展方向[6]。以往只有对六盘山辽东栎林的空间分布特征、林分结构、生长发育以及天然更新情况有研究[8],缺少对六盘山辽东栎天然林种群结构以及种内各龄级之间的关系研究。鉴于此,本研究对六盘山区辽东栎天然林的径级结构以及不同径级阶段个体的空间分布以及相关性进行分析,研究其动态特征和影响因素,有助于掌握六盘山辽东栎的生长发育现状并深入认识其群落发展过程,为维护六盘山及周边地区辽东栎林的稳定空间分布格局提供理论基础。
-
研究区位于宁夏六盘山南部的香水河小流域(35°27′22.5″~35°33′29.7″N,106°12′10.6″~106°16′30.5″E),该区处于暖温带半湿润区向半干旱区过渡带,土壤以灰褐土为主,水分条件较好。小流域森林覆盖率高达82.91%,天然次生林占小流域面积的58.51%,主要树种有华山松Pinus armandii、辽东栎和白杨Populus alba等;人工林占小流域面积的24.00%,主要树种有华北落叶松Larix principis-rupprechtii等;灌木林占小流域面积的12.01%,灌木主要有峨眉蔷薇Rosa omeiensis、虎榛子Ostryopsis davidiana、野李子Prunus salicina等;草地零星分布在沟底,草本主要有狼针茅Stipa baicalensis、早熟禾Poa annua、艾蒿Artemisia argyi等;草甸占小流域面积的4.64%,草甸组成植物主要有蕨Pteridium和紫苞风毛菊Sanssurea iodostegia等[9]。从表1可见:辽东栎林分布在海拔1 900~2 280 m的山坡上,分布坡向主要为半阴坡、半阳坡和阴坡;坡度主要为陡坡;坡位上、中、下均有分布,常伴生有少量山杨Populus davidiana等。
表 1 六盘山辽东栎样地信息
Table 1. Location factors of Q. wutaishanica in Liupan Mountain
样地编号 样地位置 株数/株 林分密度/(株·hm−2) 郁闭度 海拔/m 坡度/(°) 坡位 坡向 林型 优势种 其他树种 1 秋千架林场 43 717 0.50 1 910 30 上 东北 阔叶纯林 辽东栎 无 2 挂马沟林场 27 450 0.35 2 170 35 下 东北 阔叶纯林 辽东栎 山杨 3 卧羊川林场 74 1 230 0.60 2 024 34 下 西 阔叶纯林 辽东栎 杨树、杏 4 卧羊川林场 62 1 030 0.58 1 944 35 上 西北 阔叶纯林 辽东栎 白桦等 5 卧羊川林场 71 1 180 0.60 1 959 28 中 西 阔叶纯林 辽东栎 山杨等 6 秋千架林场 64 1 067 0.58 1 900 32 中 东南 阔叶纯林 辽东栎 榆树、丁香 7 卧羊川林场 108 1 800 0.75 2 185 27 上 西北 阔叶纯林 辽东栎 山杨 8 秋千架林场 69 1 150 0.59 2 100 35 中 东 阔叶纯林 辽东栎 山杨、山楂、白桦 9 东山坡林场 70 1 167 0.62 2 184 25 下 东北 阔叶纯林 辽东栎 山杨、椴树 10 秋千架林场 66 1 100 0.57 2 180 30 上 东北 阔叶纯林 辽东栎 白桦、山杨 11 秋千架林场 64 1 067 0.55 2 040 33 中 西北 阔叶纯林 辽东栎 其他硬阔类 12 西峡林场 58 967 0.50 2 280 38 上 东南 阔叶纯林 辽东栎 山杨、椴树 说明:杏Armeniaca vulgaris;榆树Ulmus pumila;丁香Syringa oblata;山楂Crataegus pinnatifida;椴树Tilia tuan -
本研究采用2015年调查的12块样地,面积为24 m×24 m。调查样地内辽东栎及其他树种胸径DBH≥5 cm的树高、胸径、冠幅及枝下高、郁闭度、林分密度、坐标位置等指标,样地内辽东栎多有丛生,株数按1丛为1株,并从基部往上数确定枝条数。标准地的边界使用罗盘仪测角、皮尺量距,用布鲁莱斯测高仪测得树高,用胸径尺测量胸径,用测距仪确定每株树的坐标位置,并用手持全球定位系统(GPS)记下每个样地的经纬度、海拔等,林分密度通过株数除以样地面积得出,郁闭度采用步测法[10]。
-
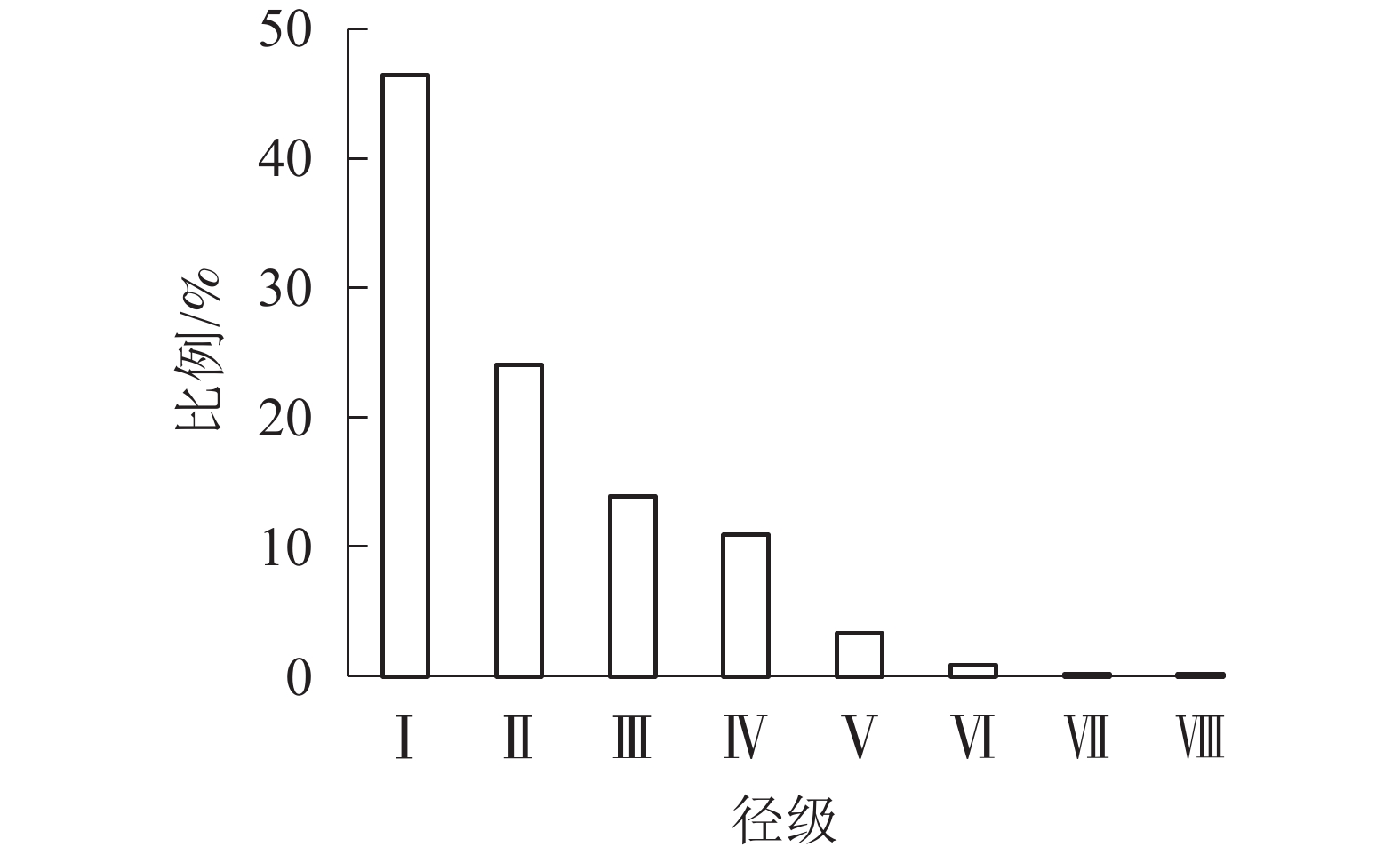
根据样地调查及文献[11-12],确定起测胸径为5 cm,径级划分为:Ⅰ级(5 cm≤DBH<10 cm)、Ⅱ级(10 cm≤DBH<15 cm)、Ⅲ级(15 cm≤DBH<20 cm)、Ⅳ级(20 cm≤DBH<25 cm)、Ⅴ级(25 cm≤DBH<30 cm)、Ⅵ级(30 cm≤DBH<35 cm)、Ⅶ级(35 cm≤DBH<40 cm)、Ⅷ级(DBH≥40 cm)。并以径级为横坐标,各径级内个体所占比例为纵坐标,绘制辽东栎径级结构图。
-
统计各径级内辽东栎个体数,根据函数关系式计算各函数值,绘制六盘山辽东栎种群的静态生命表。然后,根据静态生命表,以径级为横坐标,绘制辽东栎种群的存活系数(
$\ln {l_x}$ )、死亡率(${q_x}$ )和消失率(${K_x}$ )图[13]。$${l_x} = ({a_x}/{a_1}) \times 1\;000;$$ (1) $${d_x} = {l_x} - {l_{x + 1}};$$ (2) $${q_x} = ({d_x}/{l_x}) \times 100\% ;$$ (3) $${L_x} = ({l_x} + {l_{x + 1}})/2;$$ (4) $${T} = \sum\limits_{x = 1}^8 {{L_x}} ;$$ (5) $${E_x} = {T}/{l_x};$$ (6) $${K_x} = \ln {l_x} - \ln {l_{x + 1}}\text{。}$$ (7) 式(1)~(7)中:x为径级,取值1、2、
$\cdots $ 、8;${l_x}$ 为标准化存活个体数;${a_x}$ 为辽东栎存活株数;$ a_{1} $ 为辽东栎第1径级存活株数;${d_x}$ 为径级间隔期内的标准化死亡数;${q_x}$ 为径级间隔期内的死亡率;${L_x}$ 为区间寿命;${T}$ 为总寿命;${E_x}$ 为期望寿命[14],${K_x}$ 为消失率。 -
以径级为横坐标,分别绘制辽东栎种群存活率
${S_{(x)}}$ 和积累死亡率${F_{(x)}}$ 、死亡密度${f_{(x)}}$ 和危险率${\lambda _{(x)}}$ 图[15]。$${S_{(x)}} = {S_1} \; {S_2} \; {S_3} \; \cdots \; {S_x};$$ (8) $${F_{(x)}} = 1 - {S_{(x)}};$$ (9) $${f_{(x)}} = (2{S_x} - 1)/{h_x};$$ (10) $${\lambda _{(x)}} = 2(1 - {S_x})/\left[ {{h_x}(1 + {S_{x}})} \right]\text{。}$$ (11) 式(8)~(11)中:x为径级;
${S_{x}}$ 为存活率;${h_x}$ 为径级宽度。 -
对辽东栎纯林的空间格局,使用成对相关函数
$g(r)$ 进行描述,用尺度$r$ 作为横坐标,上下包迹线作为纵坐标,进行绘图。即:$$g(r) = {{{{\left( {2{\text{π}} r} \right)}^{ - 1}}{\rm{d}} K(r)}/{{\rm{d}} r}}\text{。}$$ (12) 式(12)中:函数
$K(r)$ 是从种群内随机抽取的个体落在以定点为圆心、$r$ 为半径的圆内期望值;$g(r)$ 函数是基于成对个体间距离的关联性函数,用种群实际分布数据计算不同研究尺度下的$g(r)$ 值,若在上下包迹线之间,符合随机分布;若在上包迹线以外,则呈聚集分布;若在下包迹线以外,则呈均匀分布[16]。采用先决条件零假设模型,进行双变量空间关联分析,依据Monte Carlo模拟结果,如$g(r)$ 在上下包迹线之间,表明两者空间上相互独立;如${\rm{g}}(r)$ 在上包迹线以上,则两者空间上为正相关;如在下包迹线以下,则两者空间上负相关。数据分析使用Programita软件完成,通过99次Monte Carlo模拟,得到99%的置信区间。数据处理采用Excel以及Origin软件完成。
-
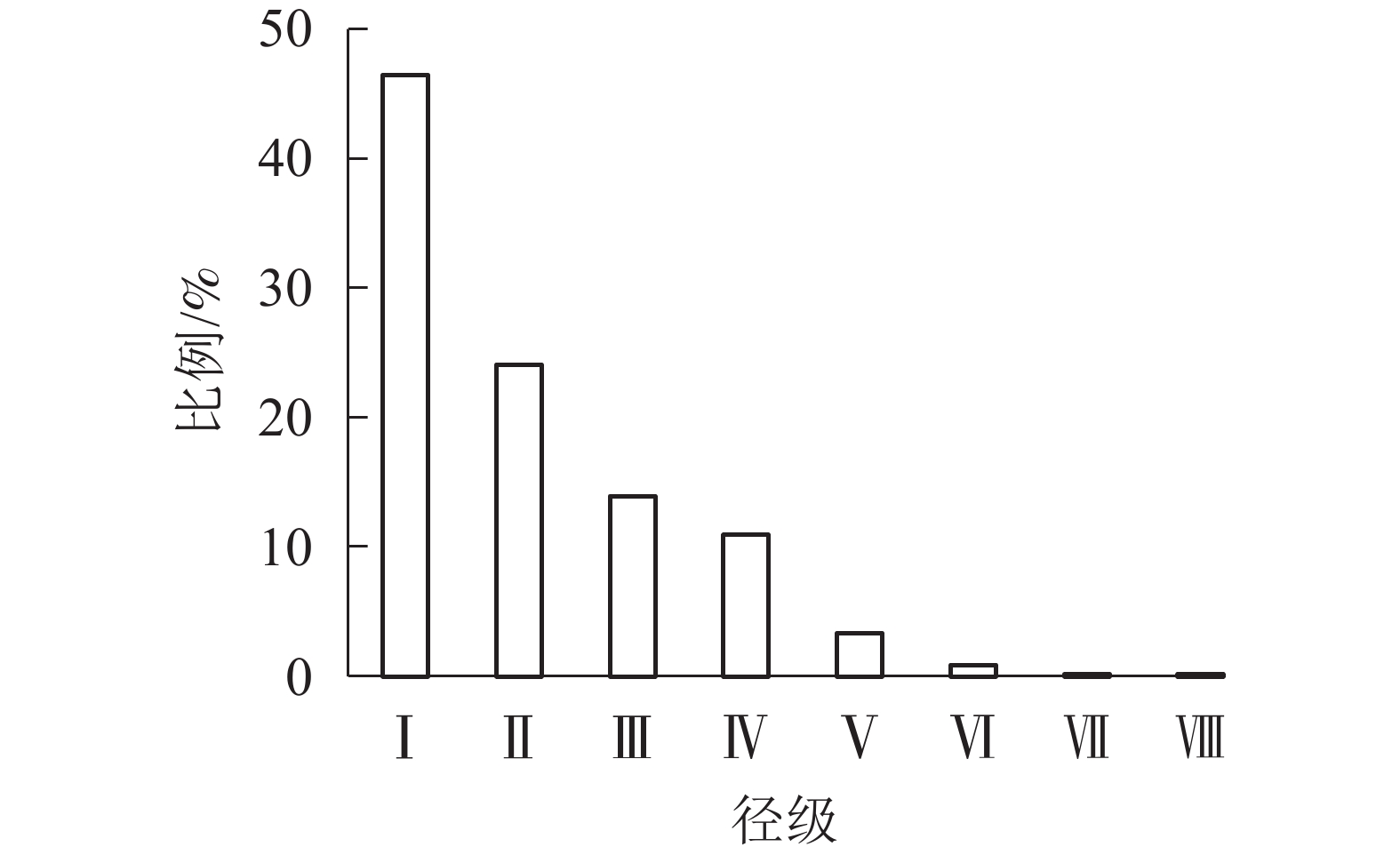
由图1表明:从第Ⅰ径级到第Ⅷ径级,辽东栎各径级所占比例逐渐减小,依次为46.48%、24.12%、13.91%、10.92%、3.36%、0.88%、0.18%、0.18%,从第Ⅲ到第Ⅵ径级所占比例减少,速度减慢。种群径级结构分布比例整体上为倒J型。
-
从表2可见:辽东栎种群的个体数量随径级增大而减少,同时标准化存活个体数(
${l_x}$ )也随径级增大而减少。辽东栎种群期望寿命(${E_x}$ )在第Ⅱ径级最高,为1.72;而在第Ⅰ径级个体数量最大,在第Ⅵ到第Ⅶ径级,${E_x}$ 又开始增大至1.50。在第Ⅷ径级,${E_x}$ 突然降到0.50,说明这时辽东栎种群已进入衰退阶段。辽东栎种群的存活率(${S_x}$ )在第Ⅲ径级达到最高,而在第Ⅶ径级又达到存活高峰。表 2 辽东栎种群静态生命表
Table 2. Static life table of Q. wutaishanica population
径级 胸径(DBH)/cm ${a_x}$/株 ${l_x}$ ${d_x}$ ${q_x}$ ${L_x}$ ${T}$ ${E_x}$ $\ln {l_x}$ ${K_x}$ ${S_{x} }$ Ⅰ 5≤DBH<10 264 1 000.00 481.06 0.48 759.47 1 651.52 1.65 6.91 0.66 0.52 Ⅱ 10≤DBH<15 137 518.94 219.70 0.42 409.09 892.05 1.72 6.25 0.55 0.58 Ⅲ 15≤DBH<20 79 299.24 64.39 0.22 267.05 482.95 1.61 5.70 0.24 0.78 Ⅳ 20≤DBH<25 62 234.85 162.88 0.69 153.41 215.91 0.92 5.46 1.18 0.31 Ⅴ 25≤DBH<30 19 71.97 53.03 0.74 45.45 62.50 0.87 4.28 1.34 0.26 Ⅵ 30≤DBH<35 5 18.94 15.15 0.80 11.36 17.05 0.90 2.94 1.61 0.20 Ⅶ 35≤DBH<40 1 3.79 0 0 3.79 5.68 1.50 1.33 0 1.00 Ⅷ DBH≥40 1 3.79 3.79 1.00 1.89 1.89 0.50 1.33 1.33 0 -
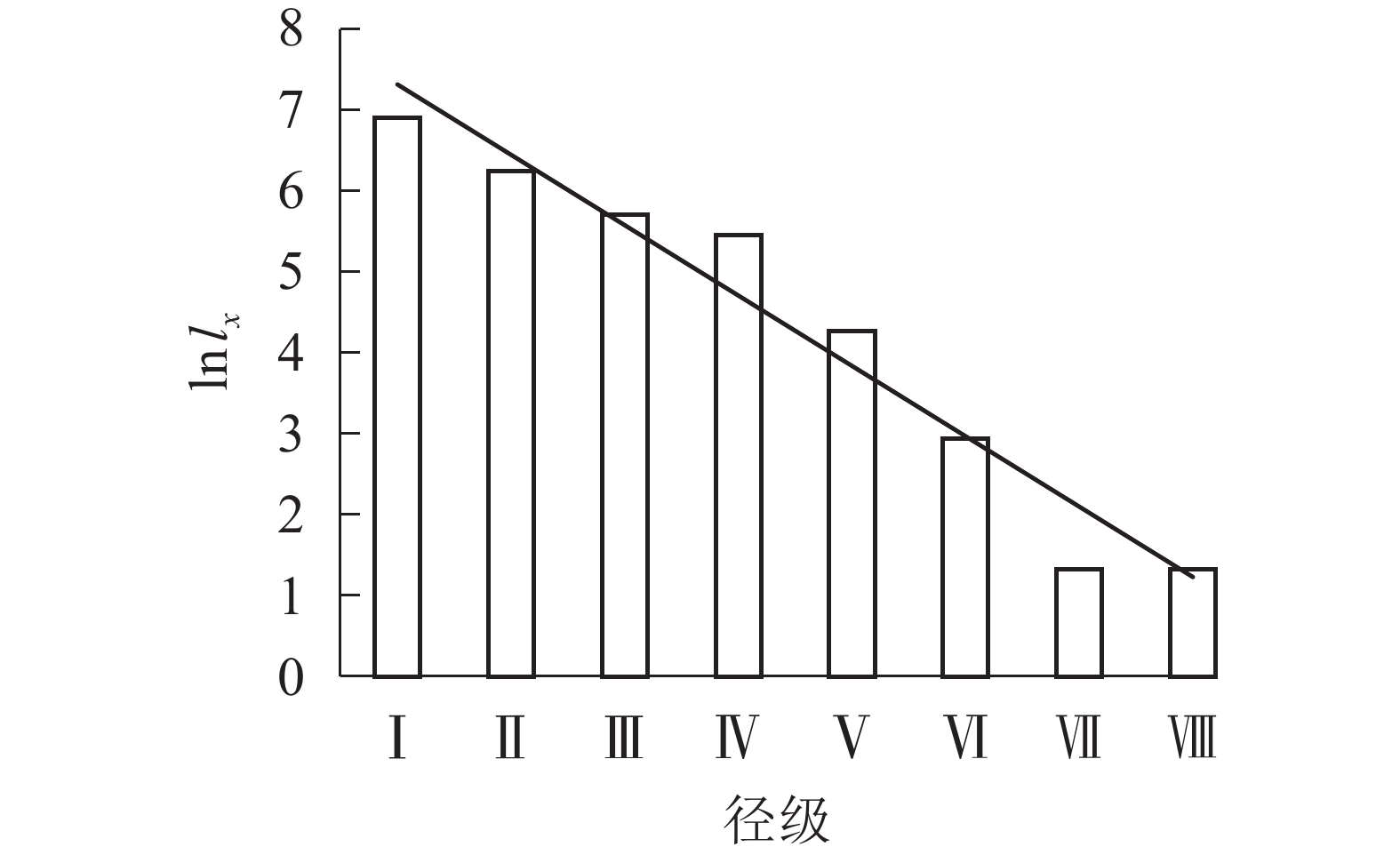
根据Deevey的划分,存活曲线被分为3种类型:Deevey-Ⅰ型、Deevey-Ⅱ型、Deevey-Ⅲ型[17]。从图2可看出:六盘山辽东栎存活趋势线趋于Deevey-Ⅱ型(斜线型),因第Ⅰ到第Ⅳ径级的存活系数逐渐下降,第Ⅳ第Ⅶ径级的存活系数近似相等,所以辽东栎种群存活趋势线在径级Ⅶ前大致呈直线。在第Ⅶ径级,存活系数突然下降,仅有33.36%的第Ⅵ径级的辽东栎个体可通过此筛选进入第Ⅶ径级。
-
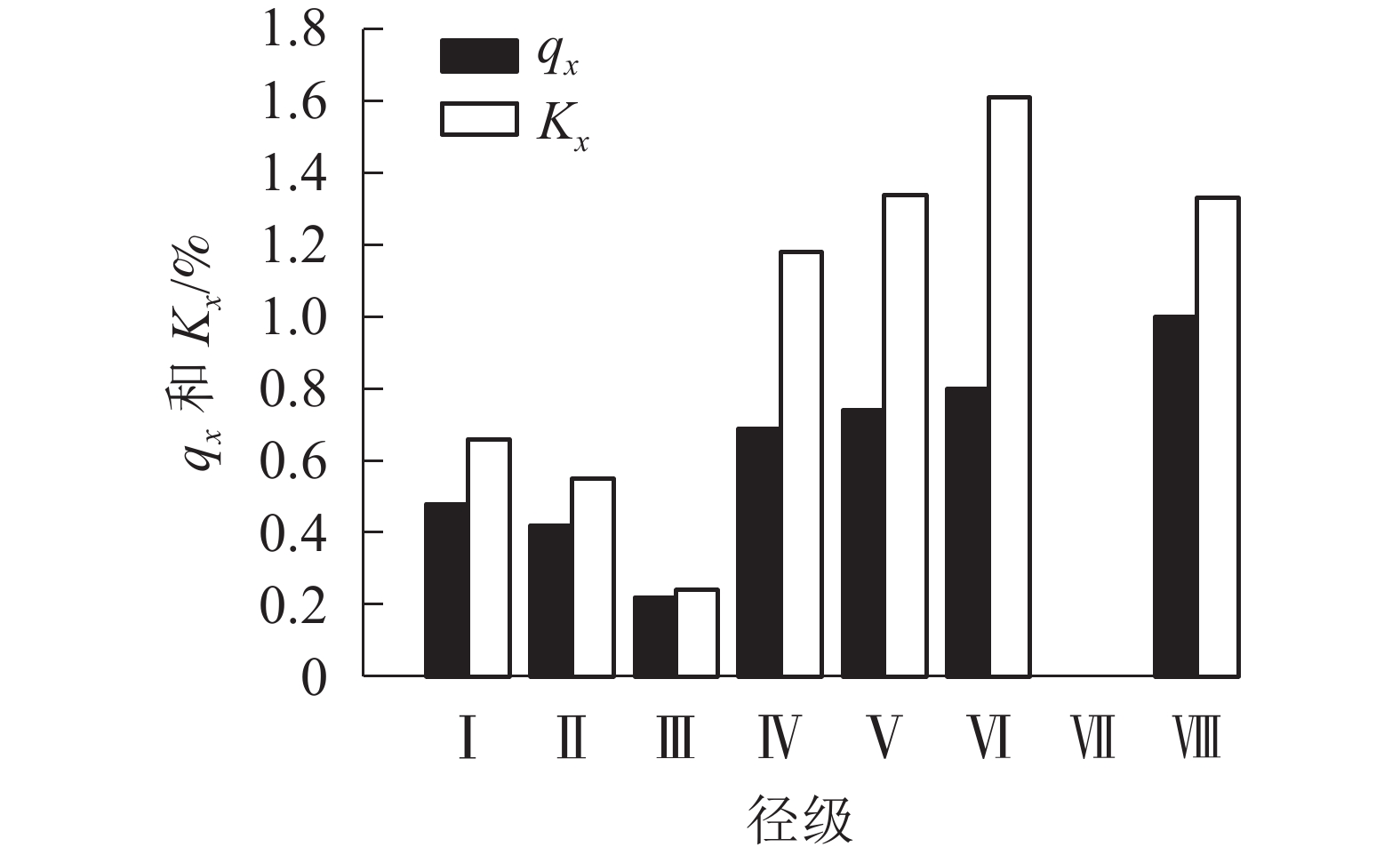
由图3可看出:种群的死亡率和消失率总体上均随径级增加先减后增,变化趋势一致,两者仅在第Ⅲ和Ⅶ径级出现波动,呈下降趋势,第Ⅶ径级死亡率和消失率突然降至为0。均出现了2个最大值,第1个最大值在第Ⅵ径级,这时死亡率为0.80,由于此阶段种内竞争加剧,环境压力下消失率达到顶峰,为1.61;第2个最大值出现在第Ⅷ径级。
-
由图4可看出:在第Ⅰ到第Ⅵ径级阶段,随龄级增大,辽东栎种群的生存率逐渐减小,而积累死亡率逐步增大;在第Ⅵ到第Ⅷ径级阶段,生存率与积累死亡率呈平稳状态。
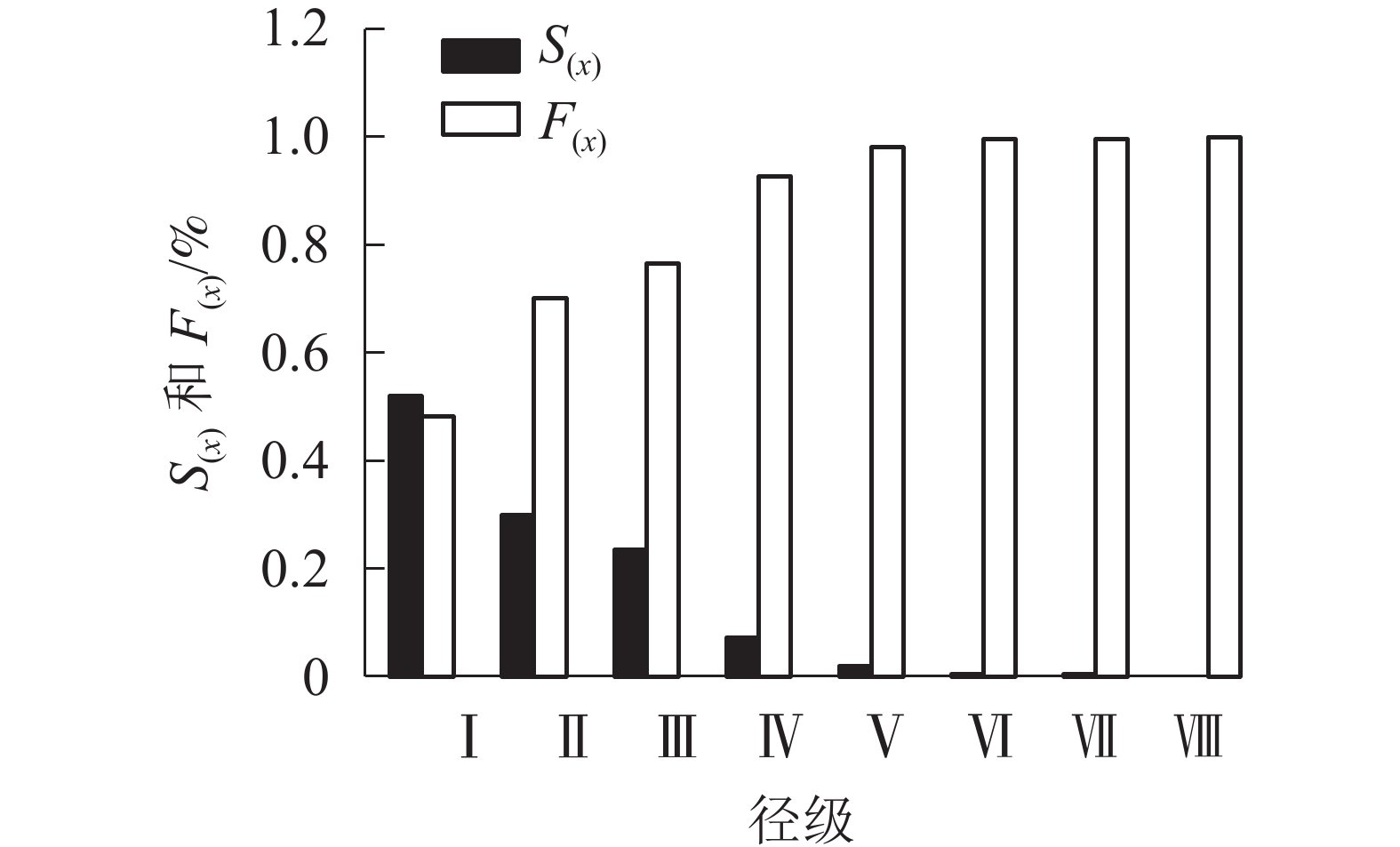
图 4 辽东栎种群的生存率[S(x)]与积累死亡率[F(x)]
Figure 4. Survival [S(x)] and accumulated mortality [F(x)] of Q. wutaishanica population
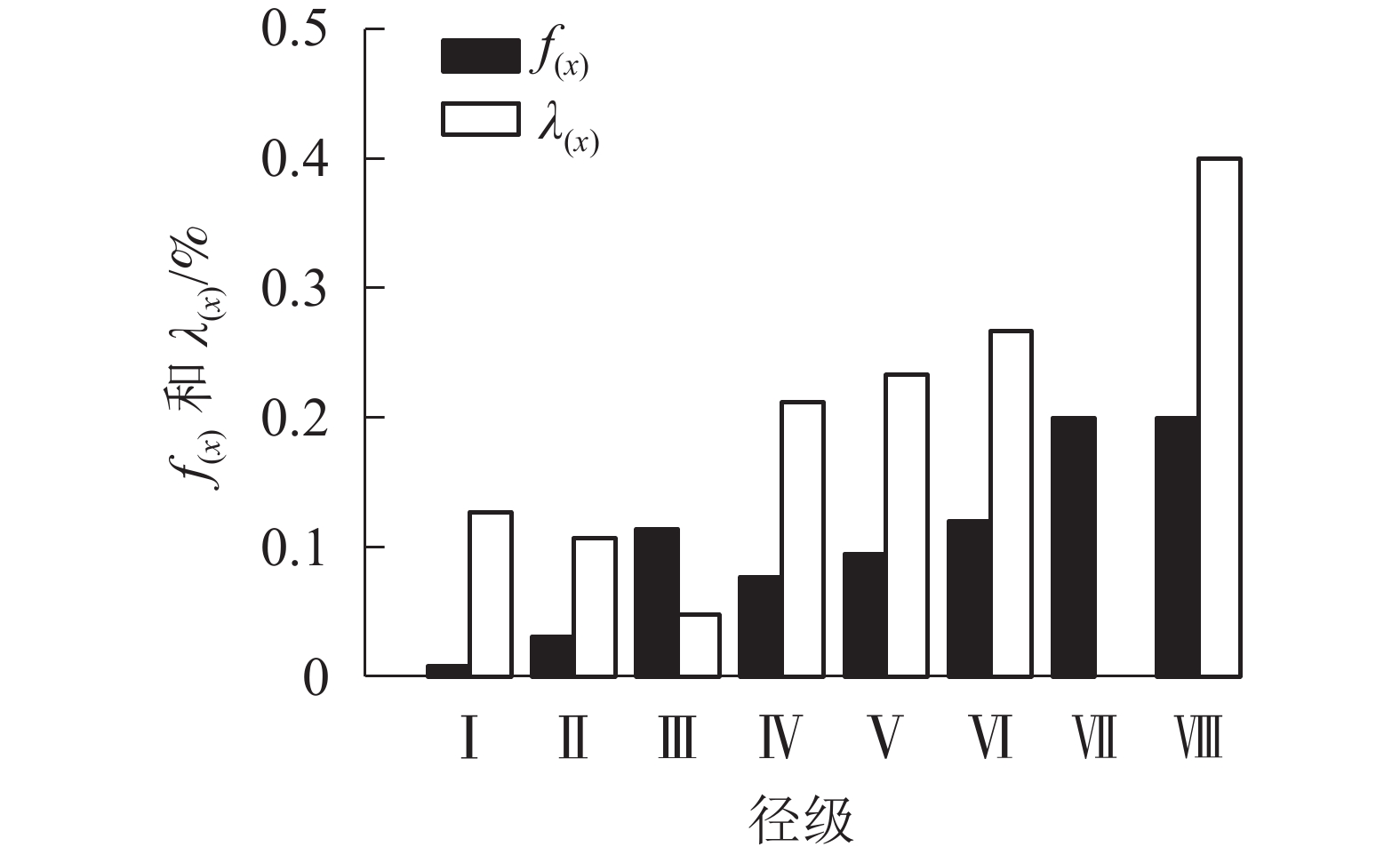
由图5可看出:辽东栎种群的死亡密度在第Ⅲ径级出现第1个峰值,在第Ⅶ到第Ⅷ径级阶段,死亡密度达到最高并不再变化。辽东栎种群的危险率在第Ⅷ径级达到最大值,此时的死亡密度也最大。
-
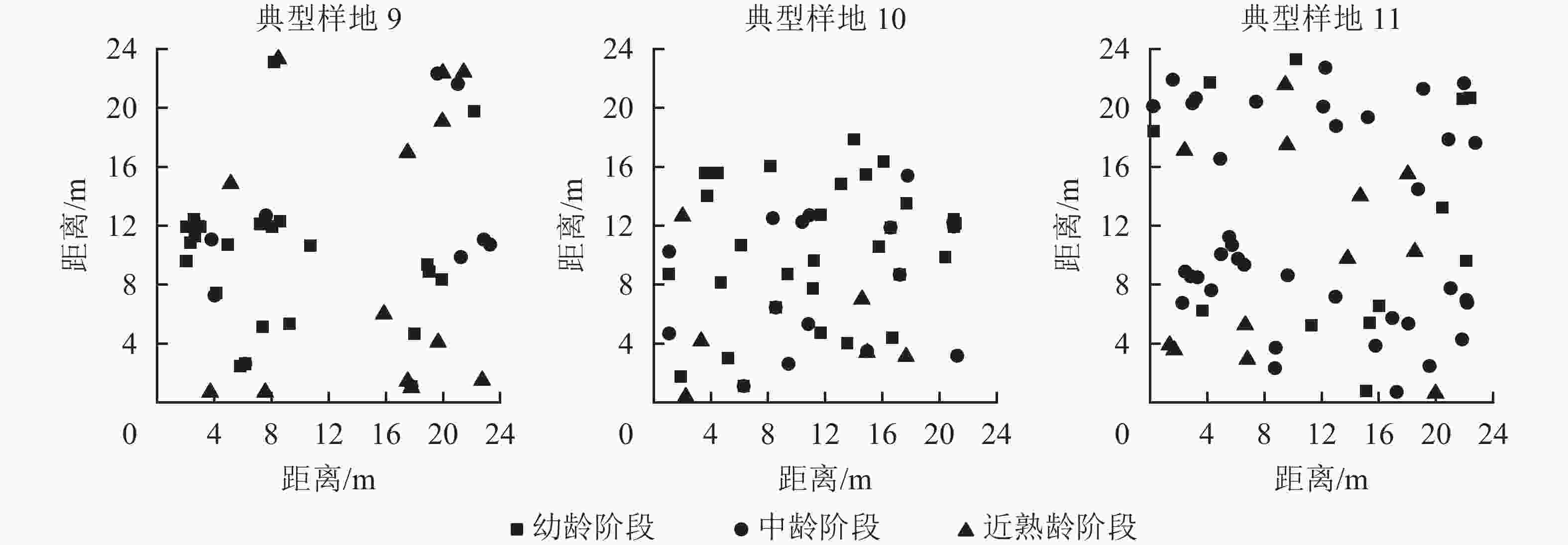
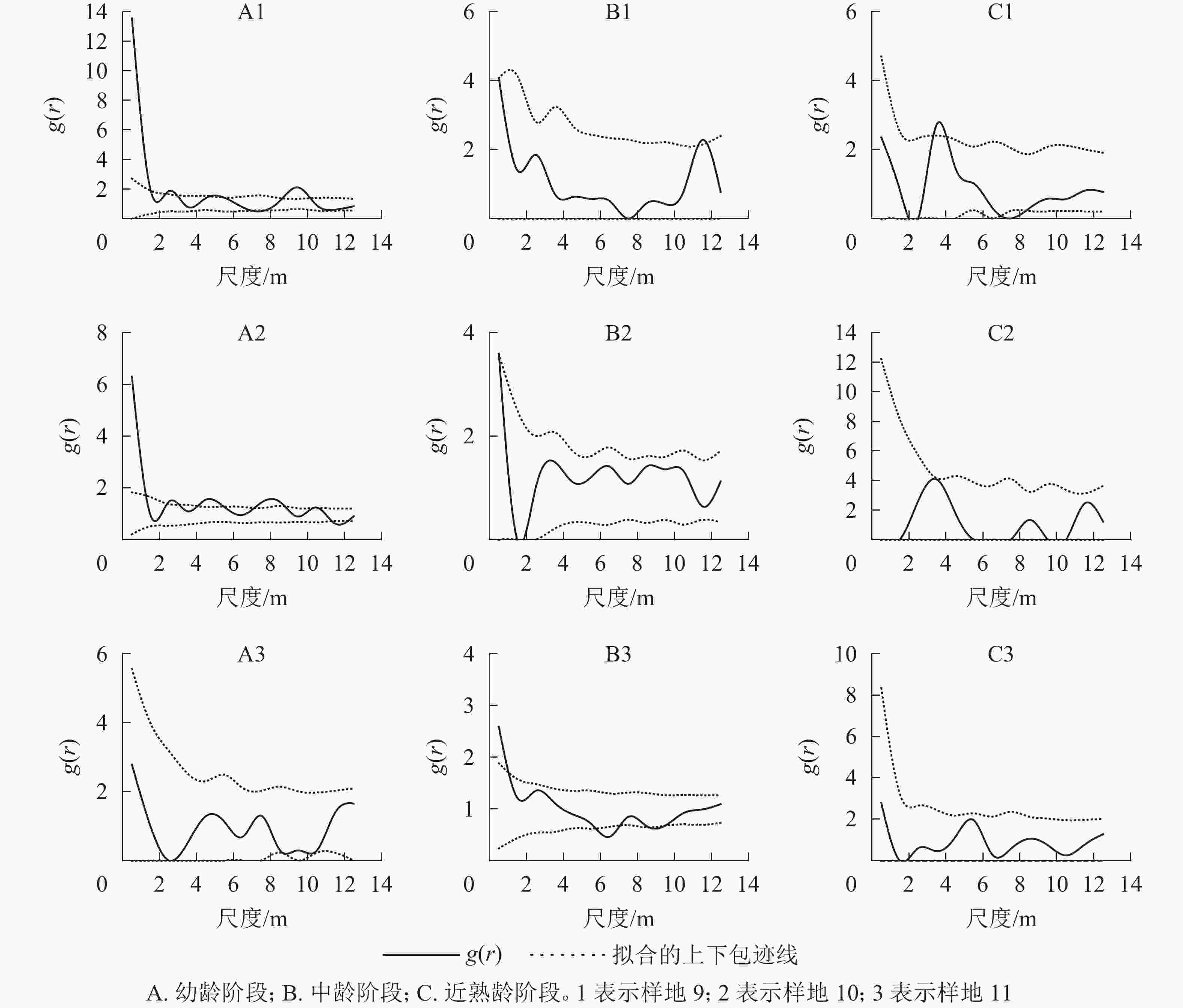
从12个样地中选择有代表意义的3个典型样地(第9、10、11号样地),把辽东栎分为4个生长阶段:幼龄阶段(5 cm≤DBH<10 cm)、中龄阶段(10 cm≤DBH<20 cm)、近熟龄阶段(20 cm≤DBH<30 cm)、成过熟龄阶段(DBH≥30 cm)。因为样地中辽东栎处于成过熟龄阶段的个体数特别少,因此本研究只考虑前3个生长阶段,从图6可以看出:典型样地9的辽东栎个体数从大到小依次为幼龄树、近熟龄树、中龄树,多为聚集分布;典型样地10的个体数从大到小依次为幼龄树、中龄树、近熟龄树,各生长阶段个体分布均匀;典型样地11的中龄树最多,个体呈随机分布。
取尺度r的间隔为1~14 m,对3个典型样地的幼龄、中龄、近熟龄辽东栎生长阶段的点格局进行了分析。由图7看出:典型样地9中,幼龄阶段在0~1 m和9~10 m尺度上为聚集分布,在其他尺度上为随机分布;中龄、近熟龄个体大致都为随机分布。典型样地10的幼龄和中龄个体在小尺度上为聚集分布,随着尺度变大,幼龄个体呈随机性聚集分布;近熟龄阶段在小尺度上出现均匀分布趋向,中龄个体在尺度14 m以内为随机分布。样地9和10内胸径大于20 cm的近熟龄个体,在尺度1~14 m都为随机分布。典型样地11内所有个体在1~14 m都为随机分布,在0~10 m上都呈聚集分布。
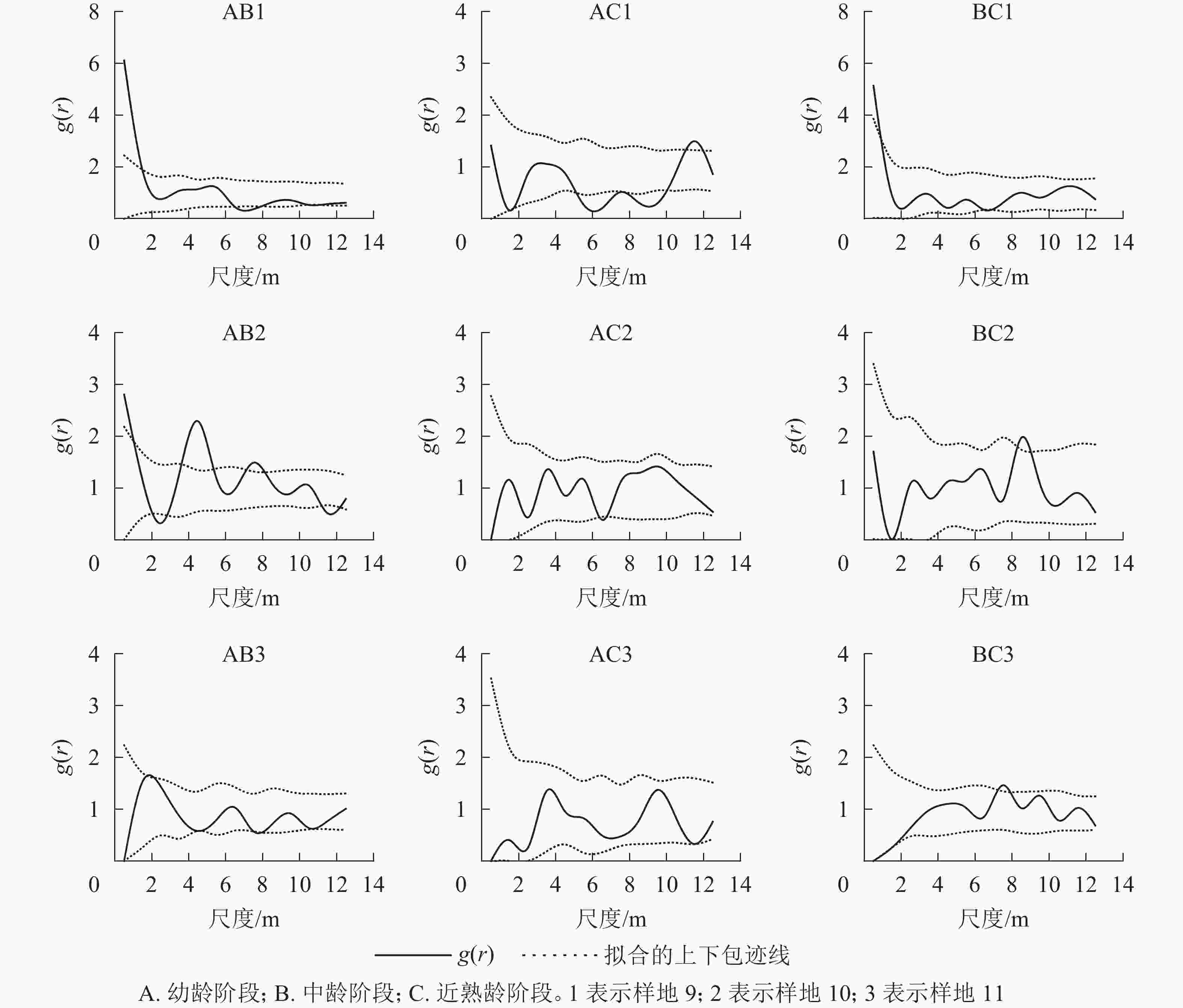
对各典型样地各年龄阶段进行双因素分析(图8)表明:典型样地9的幼龄与中龄个体间在小尺度上呈正相关,幼龄与近熟龄个体在尺度5~10 m呈负相关,中龄和近熟龄个体在0~14 m相关不显著。典型样地10的幼龄与中龄个体在2~6 m尺度上呈正相关,幼龄与近熟龄个体在0~14 m尺度上无相关,中龄和近熟龄个体之间无相关。典型样地11的辽东栎各生长阶段之间在0~2 m尺度上呈负相关,随尺度增大的相关性越来越不明显,呈相互独立状态。
-
种群结构是物种自身生物学特征、环境因素及植物种内和种间关系综合作用的结果[11]。静态生命表和生存分析可准确地反映种群在特定时间和空间范围内的动态规律[12]。种群的分布格局是由植物自身的生物学特性和环境因子共同决定的,可表明种群变化特征和群落的发展走向[18-19]。以往的辽东栎种群点格局研究[17, 20]认为:辽东栎种群中幼树主要呈聚集分布,随生长发育趋向于随机分布。
本研究得出:辽东栎种群在前期时,死亡率随龄级增加而减小,这是因为种群顺利度过了幼苗到幼树的瓶颈期,使辽东栎个体对环境的适应能力不断加强;在中期时,死亡率随龄级增加而升高,并趋于稳定,辽东栎种群的期望寿命在第Ⅱ径级达到最高,而第Ⅰ径级的个体数量最大;原因可能是第Ⅰ径级的辽东栎种群竞争强度大,个体间竞争增强,产生“自疏”,为第Ⅱ龄级的辽东栎生长提供了更多水热资源[21],使辽东栎在此期间生长旺盛,种群存活率最高。在第Ⅵ到第Ⅶ径级,期望寿命又开始增大,表明这个阶段辽东栎种群竞争强度逐渐减小。在第Ⅷ径级,期望寿命突然下降,表明辽东栎种群已进入衰退阶段。本研究生存分析发现:辽东栎群落生存曲线基本属于Deevey-Ⅱ型,这是因随径级增大,生存能力逐渐下降。辽东栎是地带性植被,各地的辽东栎并没固定的生存线型,凸线型[22]和凹线型[23]在以往研究中都存在。六盘山地区的辽东栎种群具有前期和中期稳定、后期衰退的生存过程。
本研究表明:在辽东栎种群中,幼龄和中龄个体在小尺度范围内呈聚集分布,随尺度不断增大,由聚集分布转为随机分布,这与伊力塔等[3]、王道亮等[7]的研究结论大致相同。在0~14 m尺度内,辽东栎种群中的幼树在小尺度上主要呈聚集分布,这是因辽东栎常出现幼苗簇生群落,且林内生态环境有利于幼苗发育[24]和辽东栎萌蘖更新、桩蘖更新。中龄树或近熟龄树占辽东栎种群较大比例时呈随机分布,这是因为随着径级增大,种群个体因争夺光照、土壤养分和水分等资源,出现恶性竞争,个体数量减少,聚集程度不断减弱,所以逐渐表现为随机分布格局。对3个典型样地的幼、中、近熟龄个体进行的双因素分析表明:小尺度上,样地9和10的幼龄和中、近熟龄个体都有一定正相关,这是因为在样地9和10的辽东栎个体之间存在良好竞争;大尺度上样地9、10、11的辽东栎个体之间大致都为无明显相关,这与王道亮等[7]的研究结果一致。由于种群空间格局是由个体生物学特性和环境条件相互作用所决定的[6],研究尺度也会影响研究结果,在未来的研究中可以扩大样地面积范围,进行六盘山辽东栎纯林的种群格局分析。
本研究认为:六盘山辽东栎林乔木种群处于相对稳定状态,更新状态良好,为保持辽东栎纯林结构稳定,应加强人为保护,维持辽东栎林种群更新的稳定环境条件,提高第Ⅱ径级的存活率。同时加强人工正面干预,使种群个体间保持良性竞争。
Population structure and spatial distribution pattern of Quercus wutaishanica in Liupan Mountains
-
摘要:
目的 辽东栎Quercus wutaishanica是组成六盘山森林植被的主要树种,分析六盘山辽东栎种群的空间分布格局和关联性,有助于掌握六盘山辽东栎的生长发育现状及种群发展过程。 方法 基于六盘山12个辽东栎纯林样地,通过静态生命表、种群径级结构、存活系数、死亡率、消失率以及生存分析,对辽东栎种群结构和动态进行了分析;采用点格局分析了六盘山辽东栎林种群空间格局分布规律以及空间关联性。 结果 ①样地内辽东栎种群径级结构分布近似于倒J型,更新状况良好,结构稳定。②辽东栎种群的存活曲线接近于Deevey-Ⅱ型曲线。③辽东栎种群整体呈前期和中期稳定、后期衰退的动态特征。④辽东栎幼龄、中龄级个体在小尺度范围内呈聚集分布,随着尺度增大,由聚集分布变为随机分布;近熟龄个体在小尺度上趋向于均匀分布,在大尺度上呈随机分布。 结论 六盘山辽东栎种群处于相对稳定状态,更新状况良好。辽东栎幼龄、中龄级个体在小尺度呈聚集分布,中龄与近熟龄个体在大尺度上关联性不明显,呈相互独立状态。为保持辽东栎林结构稳定,应加强人为调控,确保辽东栎林种群更新的稳定环境条件。图8表2参24 Abstract:Objective Quercus wutaishanica is the main tree species in Liupan Mountains. This study aims to analyze the spatial distribution pattern and correlation of Q. wutaishanica population in Liupan Mountains, so as to understand the growth and development status and population development process of Q. wutaishanica community in this area. Method Based on 12 pure forest plots of Q. wutaishanica in Liupan Mountains, the population structure and dynamics of Q. wutaishanica were studied by static life table, diameter class structure, survival coefficient, mortality rate, disappearance rate and survival analysis. Point pattern was used to analyze the spatial pattern and spatial correlation of Q. wutaishanica population in Liupan Mountain area. Result (1) The distribution of diameter class structure of Q. wutaishanica in the sample plots was close to the inverted J type, with good renewal status and stable structure. (2) The survival curve of Q. wutaishanica population was close to the deevey-Ⅱcurve. (3) The population of Q. wutaishanica was stable in the early and middle stages and declined in the late stage. (4) The young and middle age individuals of Q. wutaishanica showed aggregation distribution in small scale, which changed from aggregation distribution to random distribution with the increase of scale. Individuals of near maturity tended to distribute evenly on small scale and randomly on large scale. Conclusion The tree population of Q. wutaishanica in Liupan Mountains is relatively stable and in good regeneration condition. The young and middle age individuals of Q. wutaishanica show aggregation distribution in small scale, and the correlation between middle age and near mature individuals is not obvious in large scale, independent of each other. In order to keep the structure of Q. wutaishanica forest stable, human regulation should be strengthened to ensure the stable environmental conditions for population regeneration of Q. wutaishanica forest. [Ch, 8 fig. 2 tab. 24 ref.] -
表 1 六盘山辽东栎样地信息
Table 1. Location factors of Q. wutaishanica in Liupan Mountain
样地编号 样地位置 株数/株 林分密度/(株·hm−2) 郁闭度 海拔/m 坡度/(°) 坡位 坡向 林型 优势种 其他树种 1 秋千架林场 43 717 0.50 1 910 30 上 东北 阔叶纯林 辽东栎 无 2 挂马沟林场 27 450 0.35 2 170 35 下 东北 阔叶纯林 辽东栎 山杨 3 卧羊川林场 74 1 230 0.60 2 024 34 下 西 阔叶纯林 辽东栎 杨树、杏 4 卧羊川林场 62 1 030 0.58 1 944 35 上 西北 阔叶纯林 辽东栎 白桦等 5 卧羊川林场 71 1 180 0.60 1 959 28 中 西 阔叶纯林 辽东栎 山杨等 6 秋千架林场 64 1 067 0.58 1 900 32 中 东南 阔叶纯林 辽东栎 榆树、丁香 7 卧羊川林场 108 1 800 0.75 2 185 27 上 西北 阔叶纯林 辽东栎 山杨 8 秋千架林场 69 1 150 0.59 2 100 35 中 东 阔叶纯林 辽东栎 山杨、山楂、白桦 9 东山坡林场 70 1 167 0.62 2 184 25 下 东北 阔叶纯林 辽东栎 山杨、椴树 10 秋千架林场 66 1 100 0.57 2 180 30 上 东北 阔叶纯林 辽东栎 白桦、山杨 11 秋千架林场 64 1 067 0.55 2 040 33 中 西北 阔叶纯林 辽东栎 其他硬阔类 12 西峡林场 58 967 0.50 2 280 38 上 东南 阔叶纯林 辽东栎 山杨、椴树 说明:杏Armeniaca vulgaris;榆树Ulmus pumila;丁香Syringa oblata;山楂Crataegus pinnatifida;椴树Tilia tuan 表 2 辽东栎种群静态生命表
Table 2. Static life table of Q. wutaishanica population
径级 胸径(DBH)/cm ${a_x}$/株 ${l_x}$ ${d_x}$ ${q_x}$ ${L_x}$ ${T}$ ${E_x}$ $\ln {l_x}$ ${K_x}$ ${S_{x} }$ Ⅰ 5≤DBH<10 264 1 000.00 481.06 0.48 759.47 1 651.52 1.65 6.91 0.66 0.52 Ⅱ 10≤DBH<15 137 518.94 219.70 0.42 409.09 892.05 1.72 6.25 0.55 0.58 Ⅲ 15≤DBH<20 79 299.24 64.39 0.22 267.05 482.95 1.61 5.70 0.24 0.78 Ⅳ 20≤DBH<25 62 234.85 162.88 0.69 153.41 215.91 0.92 5.46 1.18 0.31 Ⅴ 25≤DBH<30 19 71.97 53.03 0.74 45.45 62.50 0.87 4.28 1.34 0.26 Ⅵ 30≤DBH<35 5 18.94 15.15 0.80 11.36 17.05 0.90 2.94 1.61 0.20 Ⅶ 35≤DBH<40 1 3.79 0 0 3.79 5.68 1.50 1.33 0 1.00 Ⅷ DBH≥40 1 3.79 3.79 1.00 1.89 1.89 0.50 1.33 1.33 0 -
[1] 范忆, 楼一恺, 库伟鹏, 等. 天目山紫楠种群年龄结构与点格局分析[J]. 浙江农林大学学报, 2020, 37(6): 1027 − 1035. FAN Yi, LOU Yikai, KU Weipeng, et al. Age structure and spatial point pattern of Phoebe sheareri population in Mount Tianmu [J]. J Zhejiang A&F Univ, 2020, 37(6): 1027 − 1035. [2] 周赛霞, 高浦新, 潘福兴, 等. 狭果秤锤树自然种群分布格局[J]. 浙江农林大学学报, 2020, 37(2): 220 − 227. ZHOU Saixia, GAO Puxin, PAN Fuxing, et al. Natural population distribution pattern of Sinojackia rehderiana in an evergreen broadleaf forest [J]. J Zhejiang A&F Univ, 2020, 37(2): 220 − 227. [3] 伊力塔, 韩海荣, 程小琴, 等. 灵空山林区辽东栎种群空间分布格局[J]. 生态学报, 2008, 28(7): 3254 − 3261. Yilita, HAN Hairong, CHENG Xiaoqin, et al. Spatial distribution pattern of Quercus liaotungensis population in Lingkong Mountains [J]. Acta Ecol Sin, 2008, 28(7): 3254 − 3261. [4] 张育新, 马克明, 祁建, 等. 北京东灵山海拔梯度上辽东栎种群结构和空间分布[J]. 生态学报, 2009, 29(6): 2789 − 2796. ZHANG Yuxin, MA Keming, QI Jian, et al. Size structure and spatial pattern of Quercus liaotungensis population along elevation gradient in Dongling Mountain, Beijing [J]. Acta Ecol Sin, 2009, 29(6): 2789 − 2796. [5] MASAKI T, OTA T, SUGITA H, et al. Structure and dynamics of tree populations within unsuccessful conifer plantations near the Shirakami mountains, a snowy region of Japan [J]. For Ecol Manage, 2004, 194(1/3): 389 − 401. [6] 胡尔查, 王晓江, 刘永宏, 等. 乌拉山自然保护区油松种群结构与分布格局研究[J]. 林业科学研究, 2011, 24(3): 363 − 369. HU Ercha, WANG Xiaojiang, LIU Yonghong, et al. Population structure and distribution pattern of Pinus tabulaeform in Wulashan Nature Reserve of Inner Mongolia [J]. For Res, 2011, 24(3): 363 − 369. [7] 王道亮, 李卫忠, 曹铸, 等. 黄龙山天然次生林辽东栎种群空间格局[J]. 生态学报, 2016, 36(9): 2677 − 2685. WANG Daoliang, LI Weizhong, CAO Zhu, et al. Spatial patterns of Quercus wutaishanica in natural secondary forest of Huanglong mountain [J]. Acta Ecol Sin, 2016, 36(9): 2677 − 2685. [8] 王占印, 于澎涛, 王双贵, 等. 宁夏六盘山区辽东栎林的空间分布及林分特征[J]. 林业科学研究, 2011, 24(1): 97 − 102. WANG Zhanyin, YU Pengtao, WANG Shuanggui, et al. The characteristics of stand structure and spatial distribution of Quercus liaotungensis forests in Liupan mountains [J]. For Res, 2011, 24(1): 97 − 102. [9] 刘泽彬, 王彦辉, 徐丽宏, 等. 六盘山华北落叶松林坡面的土壤水分时间稳定性[J]. 水土保持学报, 2017, 31(1): 153 − 159, 165. LIU Zebin, WANG Yanhui, XU Lihong, et al. Temporal stability of soil moisture on a slope surface of Larix principis-rupprechtii plantation in Liupan mountains [J]. Res Soil Water Conserv, 2017, 31(1): 153 − 159, 165. [10] 孟宪宇. 测树学[M]. 北京: 中国林业出版社, 2006: 63. [11] 郭薇. 灵空山天然油松、辽东栎种群动态与空间格局分析[D]. 太原: 山西大学, 2013. GUO Wei. Study on Population Dynamics and Spatial Pattern of Pinus tabulaeformis and Quercus wutaishanica in Lingkong Mountain[D]. Taiyuan: Shanxi University, 2013. [12] HE Fangliang, LEGENDRE P, LAFRANKIE J V. Distribution patterns of tree species in a Malaysian tropical rain forest [J]. J Veg Sci, 1997, 8(1): 105 − 114. [13] 张志永, 杨晓晖, 张晓, 等. 浑善达克沙地榆树种群结构和动态特征[J]. 中国沙漠, 2018, 38(3): 524 − 534. ZHANG Zhiyong, YANG Xiaohui, ZHANG Xiao, et al. Structure and dynamic characteristics of Ulmus pumila population in the Otingdag sandy land [J]. J Desert Res, 2018, 38(3): 524 − 534. [14] ABELI T, CAUZZI P, ROSSI G, et al. Restoring population structure and dynamics in translocated species: learning from wild populations [J]. Plant Ecol, 2016, 217(2): 183 − 192. [15] 张志录, 刘中华, 陈明辉, 等. 河南伏牛山区天然红豆杉种群结构与动态研究[J]. 水土保持研究, 2016, 23(3): 262 − 268. ZHANG Zhilu, LIU Zhonghua, CHEN Minghui, et al. Research on the population structure and dynamics of natural Taxus chinensis in Funiu mountain area of Henan Province [J]. Res Soil Water Conserv, 2016, 23(3): 262 − 268. [16] KANG Di, GUO Yaoxin, REN Chengjie, et al. Population structure and spatial pattern of main tree species in secondary Betula platyphylla forest in Ziwuling mountains, China [J]. Sci Rep, 2014, 4: 6873. doi: 10.1038/srep06873. [17] SOMANATHAN H, BORGES R M. Influence of exploitation on population structure, spatial distribution and reproductive success of dioecious species in afragmented cloud forest in India [J]. Biol Conserv, 2000, 94(2): 243 − 256. [18] 郝少英. 山西庞泉沟自然保护区辽东栎种群生命表研究[J]. 山西林业科技, 2019, 48(1): 1 − 5, 33. HAO Shaoying. Study on life table of Quercus liaotungensis population in Pangquangou Nature Reserve of Shanxi Province [J]. Shanxi For Sci Technol, 2019, 48(1): 1 − 5, 33. [19] 杨慧, 娄安如, 高益军, 等. 北京东灵山地区白桦种群生活史特征与空间分布格局[J]. 植物生态学报, 2007, 31(2): 272 − 282. YANG Hui, LOU Anru, GAO Yijun, et al. Life history characteristics and spatial distribution of the Betula platyphylla population in the Dongling mountain region, Beijing, China [J]. J Plant Ecol, 2007, 31(2): 272 − 282. [20] 李立, 陈建华, 任海保, 等. 古田山常绿阔叶林优势树种甜槠和木荷的空间格局分析[J]. 植物生态学报, 2010, 34(3): 241 − 252. LI Li, CHEN Jianhua, REN Haibao, et al. Spatial patterns of Castanopsis eyrei and Schima superba in mid-subtropical broadleaved evergreen forest in Gutian Mountain National Reserve, China [J]. Chin J Plant Ecol, 2010, 34(3): 241 − 252. [21] 段桂芳, 单立山, 李毅, 等. 甘肃中西部地区红砂种群结构及空间格局特征[J]. 水土保持研究, 2016, 23(1): 67 − 74. DUAN Guifang, SHAN Lishan, LI Yi, et al. Population structure and spatial pattern of Reaumuria soongorica population in midwest region of Gansu [J]. Res Soil Water Conserv, 2016, 23(1): 67 − 74. [22] 胡秀娟, 程积民, 杨晓梅, 等. 黄土高原子午岭林区辽东栎种群分布格局及群落特征研究[J]. 西北林学院学报, 2010, 25(5): 1 − 6. HU Xiujuan, CHENG Jimin, YANG Xiaomei, et al. Spatial distribution pattern and the community characteristic of Quercus wutaishanica forest in the Ziwuling region [J]. J Northwest For Univ, 2010, 25(5): 1 − 6. [23] 张健, 郝占庆, 宋波, 等. 长白山阔叶红松林中红松与紫椴的空间分布格局及其关联性[J]. 应用生态学报, 2007, 18(8): 1681 − 1687. ZHANG Jian, HAO Zhanqing, SONG Bo, et al. Spatial distribution patterns and associations of Pinus koraiensis and Tilia amurensis in broad-leaved Korean pine mixed forest in Changbai mountains [J]. Chin J Appl Ecol, 2007, 18(8): 1681 − 1687. [24] WU Xiaopu, ZHENG Yu, MA Keping. Population distribution and dynamics of Quercus wutaishanica, Fraxinus rhynchophylla and Acer mono in Dongling mountain, Beijing [J]. Acta Bot Sin, 2002, 44(2): 212 − 223. -

-
链接本文:
https://zlxb.zafu.edu.cn/article/doi/10.11833/j.issn.2095-0756.20200707






 下载:
下载: