-
秀珍菇Pleurotus pulmonarius学名为肺形侧耳,又名小平菇、袖珍菇、姬平菇,隶属真菌界Mycota担子菌门Basidiomycota伞菌亚纲Agaricomycetidae伞菌目Agaricales侧耳科Pleurotaceae侧耳属Pleurotus。秀珍菇富含人体必需的氨基酸、蛋白质、多糖、微量元素等多种生理活性物质[1],具有免疫调节[2]、抗肿瘤[3]、抗氧化[4]、降血糖血脂[5]等功效。在工厂栽培时,多次扩大培养易导致秀珍菇菌种退化,降低其子实体的产量和质量,致使其生物学效率和经济效益大幅下降。已经发生退化的菌种,必须经过复壮后才能投入生产,通常利用组织分离、尖端分离、原生质体再生等技术实现菌种复壮[6−8]。
氨基酸是含有碱性氨基和酸性羧基的有机化合物,参与机体物质合成、分解代谢和能量平衡等生命活动过程。氨基酸可作为有机氮源促进食用菌的生长,也可作为功能性物质调节机体生命活动[9]。马元伟等[10]研究发现:在培养基中添加一定浓度的组氨酸和赖氨酸,能够延缓或恢复丝状真菌的退化。孔梓璇等[11]通过外源添加丝氨酸,有效复壮了草菇Volvariella volvacea退化菌种的菌丝特性。常婷婷等[12]筛选出丙氨酸(Ala)、天冬酰胺(Asn)和丝氨酸(Ser)复配氨基酸培养基,可有效促进香菇Lentinus edodes菌丝生长。然而,氨基酸在秀珍菇的退化和复壮中的作用未见相关报道。基于氨基酸在微生物代谢与抗逆性中的重要作用,外源添加特定氨基酸可能延缓菌种退化或增强复壮效果。本研究通过比较生理特性、营养代谢及氧化应激水平等关键指标,探究氨基酸对秀珍菇菌种复壮的影响,旨在寻找能够延缓秀珍菇菌种退化或提高复壮效果的方法,为拓展食用菌菌种维护技术提供理论依据与实践参考。
-
秀珍菇菌株JX-2由福建农林大学菌物研究中心提供。JX-2菌株在90 mm平板上25 ℃培养,满板后转至新的90 mm平板进行第2代培养,以此类推,连续培养至10代获得JX-2第10代菌株(JX-2-10th)。在显微镜下挑取退化菌株JX-2-10th菌丝尖端至新的培养基中得到JX-2第10代复壮菌株(JX-2-10th-TP)。
-
对照组为马铃薯葡萄糖琼脂培养基(PDA,ck),处理组培养基为Ser-PDA、Ala-PDA,参考陈长兰等[13]的方法,Ser与Ala添加量为2 g·L−1。
-
菌丝生长速度的测定参考安学明等[14]的方法。将待测菌株活化后用直径8 mm打孔器打孔,接种至90 mm平板,在黑暗中25 ℃培养并观察菌落形态,同时记录菌丝的萌发时间,通过十字划线法测量菌丝生长速度。用打孔器取8个直径8 mm菌块接入三角瓶中,放入摇床,25 ℃、120 r·min−1培养7 d,倒掉瓶中液体,用滤纸吸干菌丝上的水分,置于平板放入烘箱60 ℃烘干2 d,得到菌体干质量,计算菌体生物量。
-
菌丝粗多糖的提取采用热水浸提法[15],测定采用苯酚-硫酸法。菌丝总蛋白采用总蛋白检测试剂盒(南京建成生物工程研究所,南京),按照说明书测定。
-
氧化应激指标包括超氧阴离子产生速率、过氧化氢(H2O2)质量摩尔浓度、过氧化物酶(POD)活性、超氧化物歧化酶(SOD)活性和过氧化氢酶(CAT)活性。超氧阴离子产生速率采用羟胺反应法测定[16],过氧化氢测定参考刘欣芊等[17]的方法,过氧化物酶活性测定参考王杰等[18]的方法,超氧化物歧化酶活性的测定采用SOD活性检测试剂盒(购于北京索莱宝科技有限公司,货号BC0175;酶活性单位定义:在25 ℃下,在黄嘌呤氧化酶偶联反应体系中抑制率为50%时,反应体系中的SOD酶活力定义为1个酶活力单位),过氧化氢酶活性测定参考邹优花等[19]的方法。
-
数据分析采用Excel和SPSS;每个处理3个重复,结果以平均值±标准差表示。
-
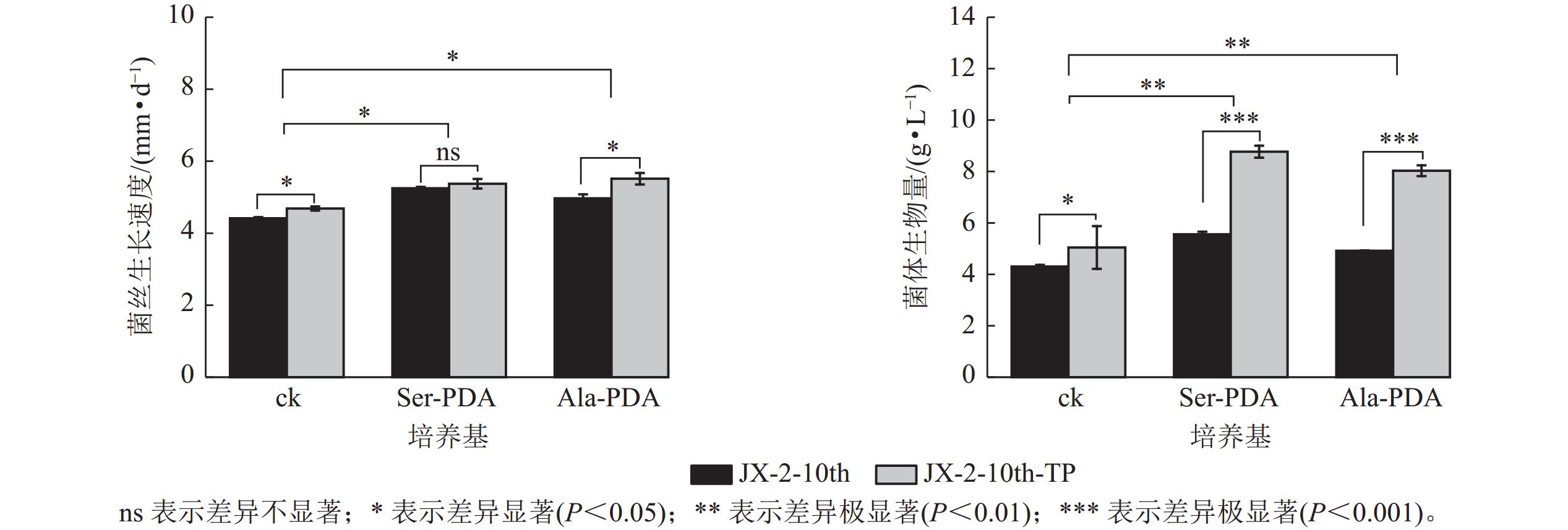
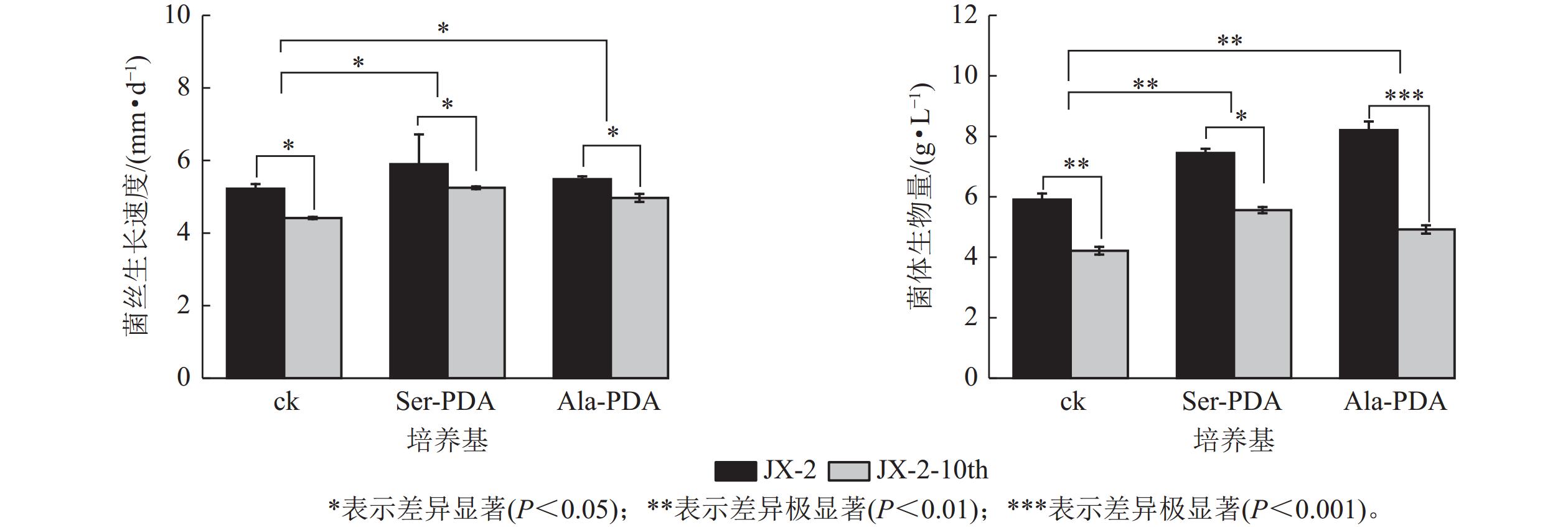
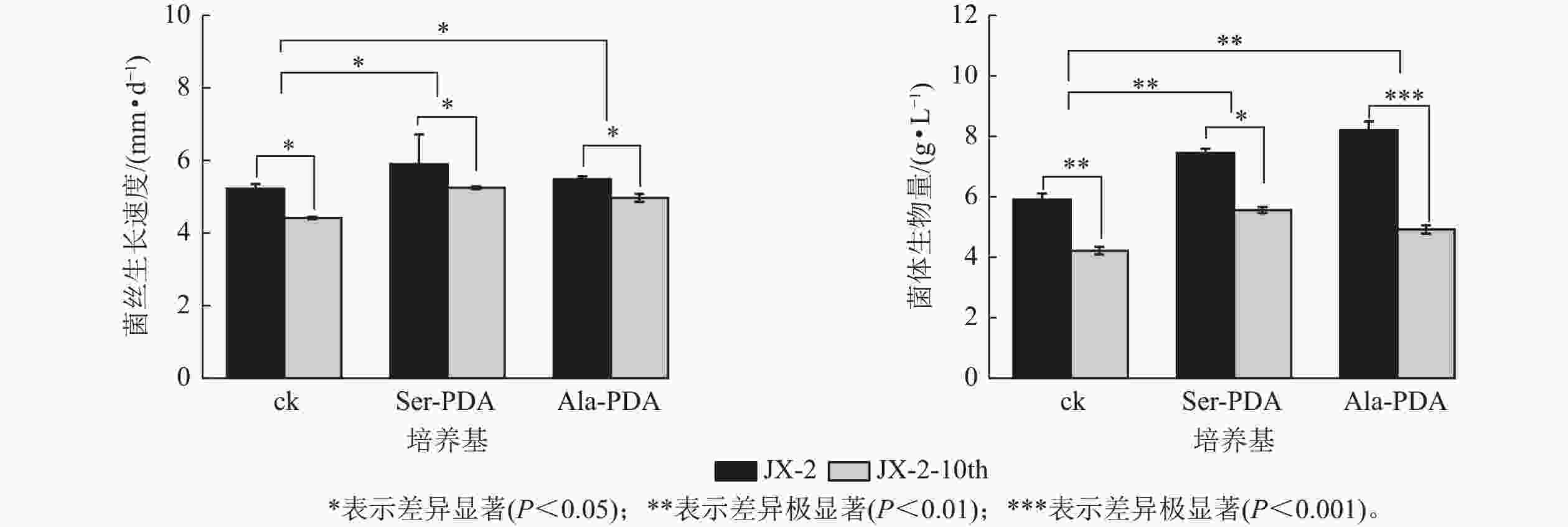
将菌株JX-2分别在PDA(ck)、Ser-PDA、Ala-PDA中继代培养10代,获得多次传代菌株JX-2-10th,比对JX-2与JX-2-10th的生长速度、生物量,结果如图1所示。在PDA中继代培养10代菌株后,菌丝生长速度、生物量显著下降(P<0.05),分别降低了15.45%、28.67%。在添加Ser、Ala的培养基中进行继代培养的JX-2-10th菌株的菌丝生长速度和生物量较JX-2虽有所降低,但优于ck,菌丝生长速度分别提高7.14%、4.76%,生物量提高37.50%、22.50%,均达到差异显著水平(P<0.05)。上述结果表明多次传代后秀珍菇菌株的菌丝体生理指标出现退化特征,但Ser、Ala的添加,能够一定程度上减缓菌株传代过程中的退化现象。
-
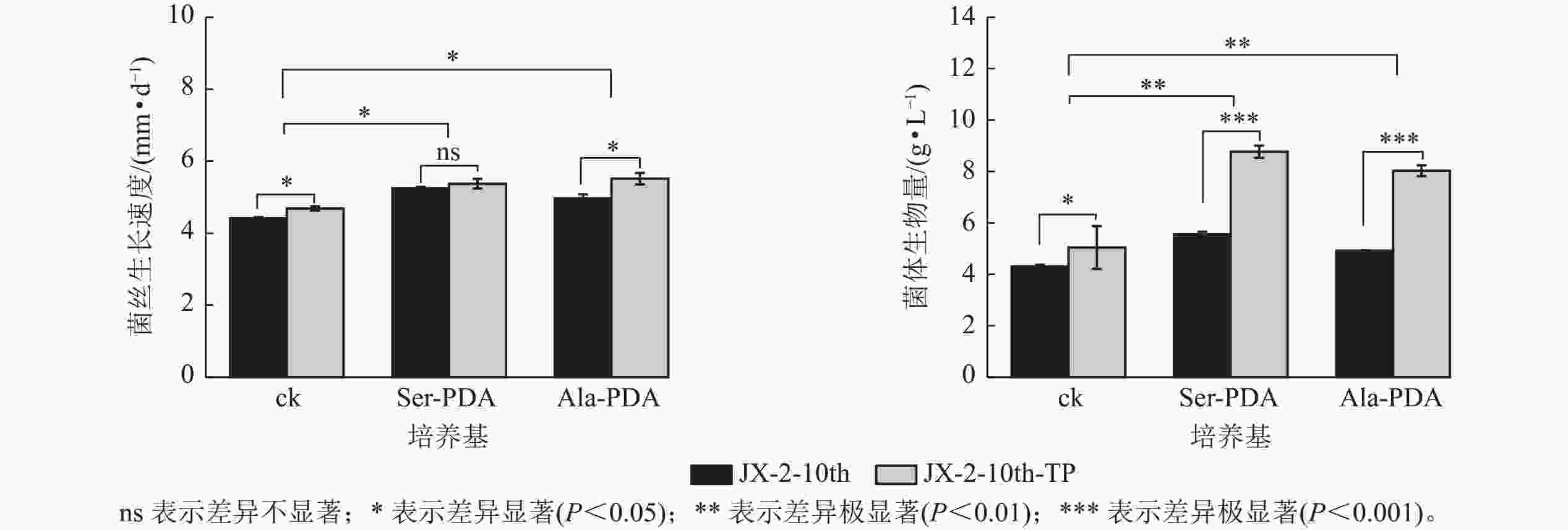
对JX-2-10th进行尖端纯化获得复壮菌株JX-2-10th-TP。由图2可知:在PDA培养基(ck)中纯化菌株菌丝的生长速度及生物量分别提高了6.12%、17.17%;在Ser+PDA培养基中菌丝生物量较纯化前提高了57.77% (P<0.01);在Ala-PDA培养基中纯化菌株菌丝生长速度及生物量较JX-2-10th均显著提高(P<0.05),分别提高了10.98%、63.26%。在Ser-PDA和Ala-PDA培养基中,菌丝生长速度分别是ck的1.18、1.23倍,生物量是ck的1.69、1.57倍。由此可见,尖端纯化能够在一定程度上恢复退化菌株菌丝生长速度和生物量,添加Ser或Ala的培养基恢复效果优于ck,且在Ala-PDA培养基中效果最佳。
-
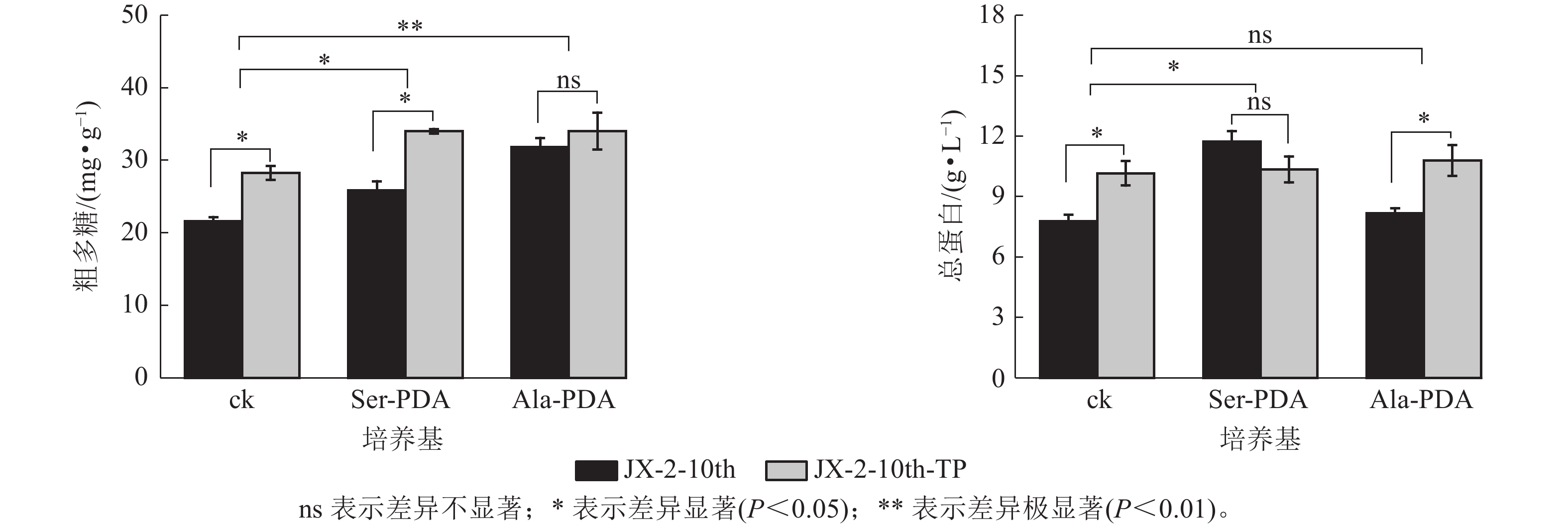
如图3所示:在PDA培养基(ck)中,复壮后菌株JX-2-10th-TP菌丝粗多糖质量分数比复壮前菌株JX-2-10th提高30.66% (P<0.05);在Ser+PDA培养基中,JX-2-10th-TP菌丝的粗多糖质量分数较复壮前提高31.52%(P<0.05);在Ala+PDA培养基中,复壮后菌丝的粗多糖质量分数虽然有所提升,但未达到显著水平。表明尖端纯化有助于改善退化秀珍菇菌株粗多糖质量分数降低的现象,且Ser能够促进尖端纯化效果,有效提高秀珍菇菌株中粗多糖。
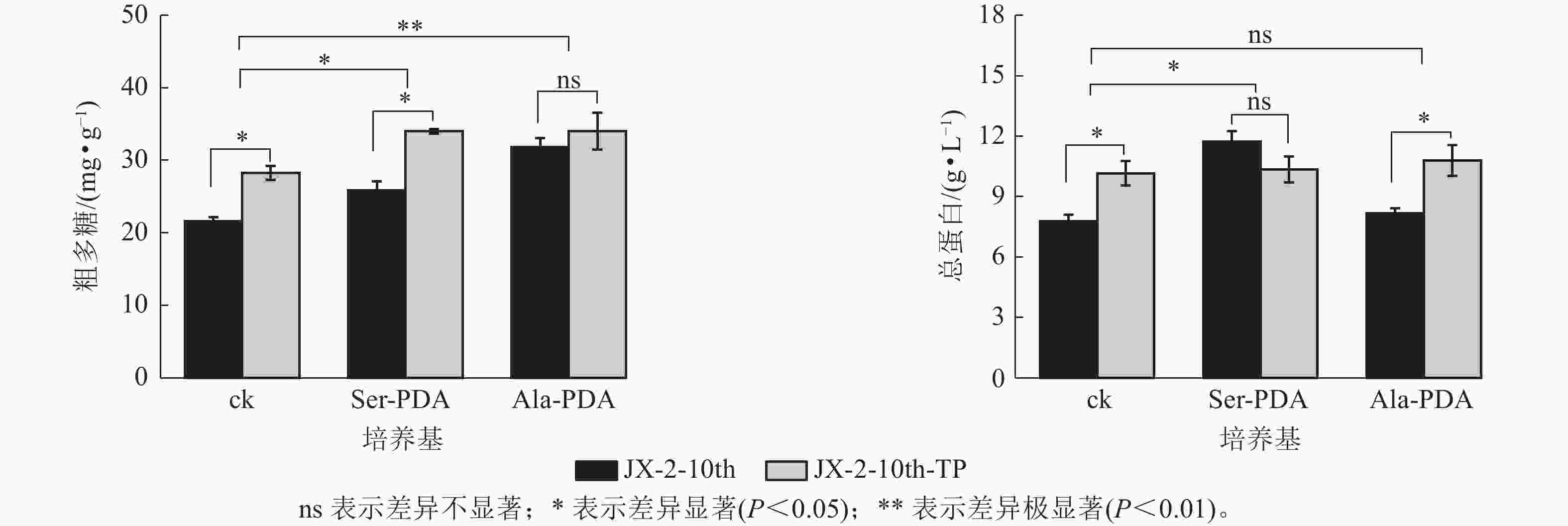
Figure 3. Effects of Ser or Ala on crude polysaccharide and total protein contents of mycelia after tip-purified
如图3所示:JX-2-10th-TP在PDA培养的菌丝总蛋白质量浓度是JX-2-10th的1.31倍(P<0.05);在Ala-PDA培养基中,JX-2-10th-TP的总蛋白质量浓度是复壮前的1.32倍(P<0.05)。Ser-PDA培养基中JX-2-10th-TP总蛋白质量浓度略低于纯化前菌株,但未达到显著水平。说明尖端纯化可能恢复退化秀珍菇菌株总蛋白质量浓度,添加Ala后纯化效果更明显。
-
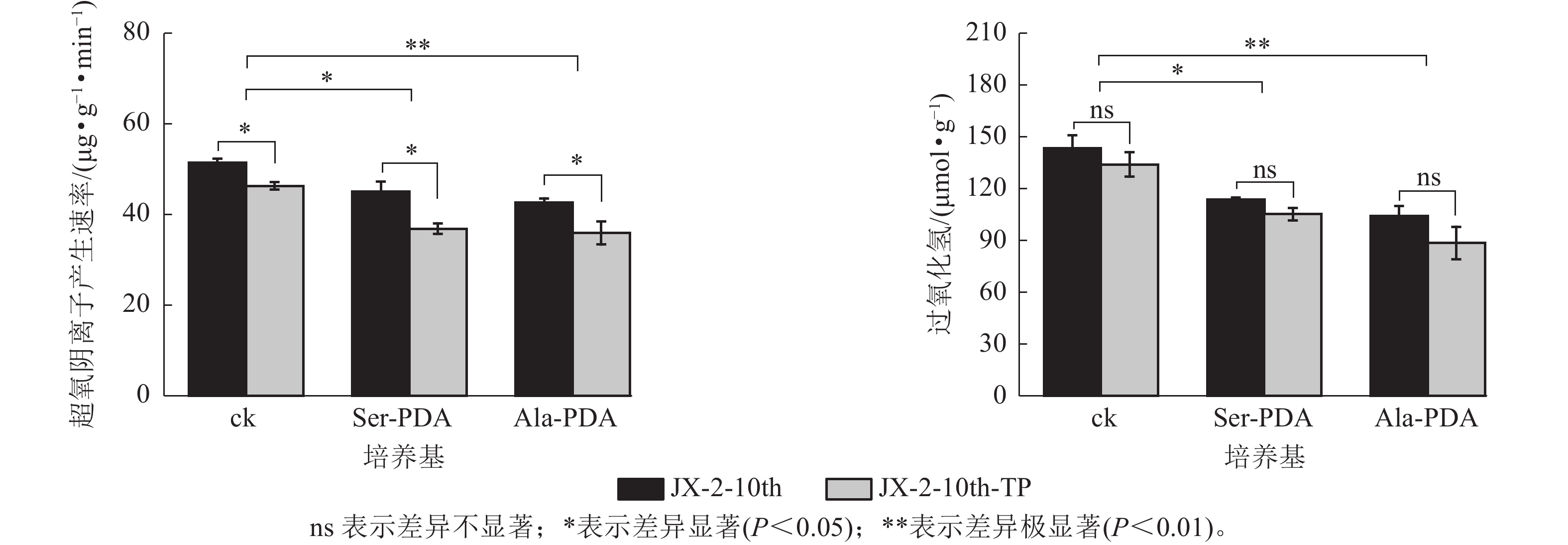
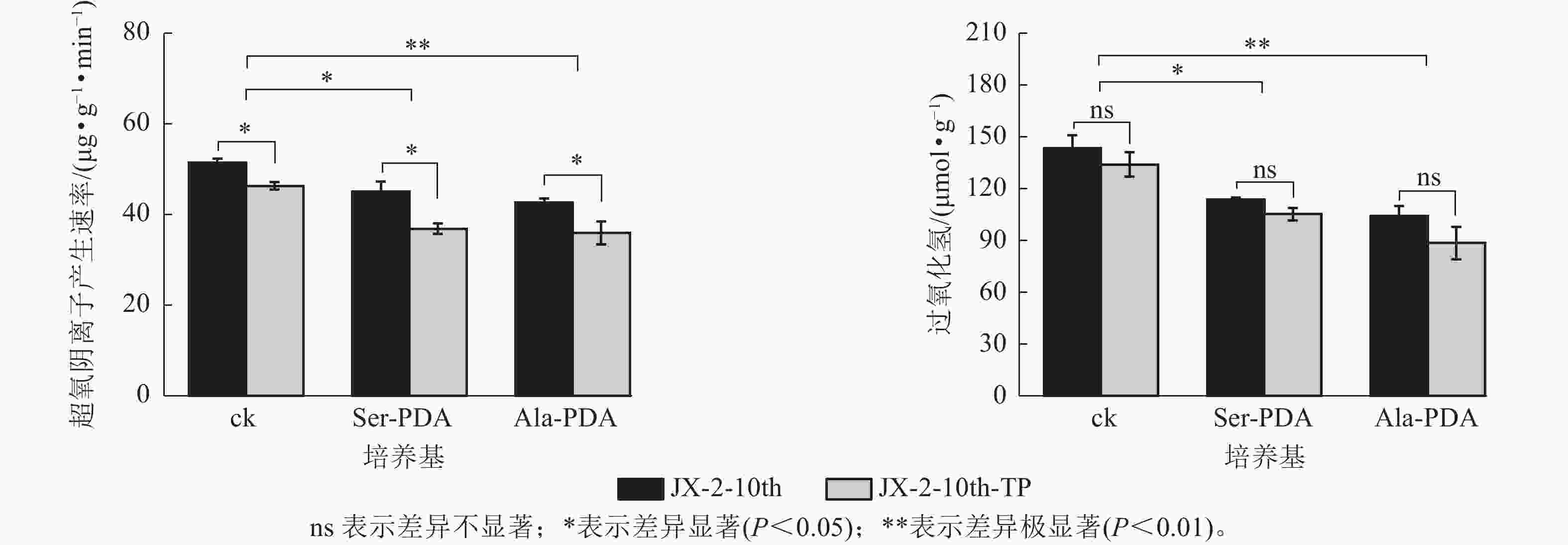
如图4所示:在PDA培养基(ck)中,JX-2-10th-TP的菌丝的超氧阴离子产生速率降低了9.90%,显著低于纯化前(P<0.05)。菌丝的H2O2质量摩尔浓度较JX-2-10th降低了6.51%;在Ser-PDA或Ala-PDA培养基中JX-2-10th-TP菌丝的超氧阴离子产生速率较JX-2-10th均显著降低(P<0.05),分别降低18.26%、15.80%。H2O2质量摩尔浓度较JX-2-10th分别降低7.56%、14.89%。说明尖端纯化能够有效改善退化秀珍菇菌株中超氧阴离子和H2O2的积累,且Ser、Ala处理后效果更佳。
-
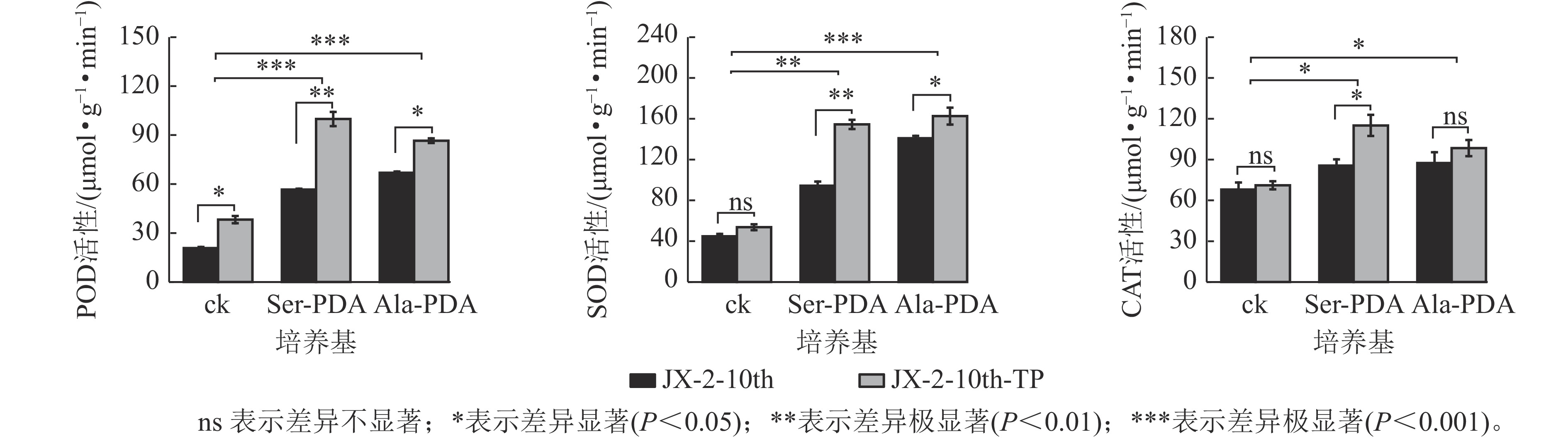
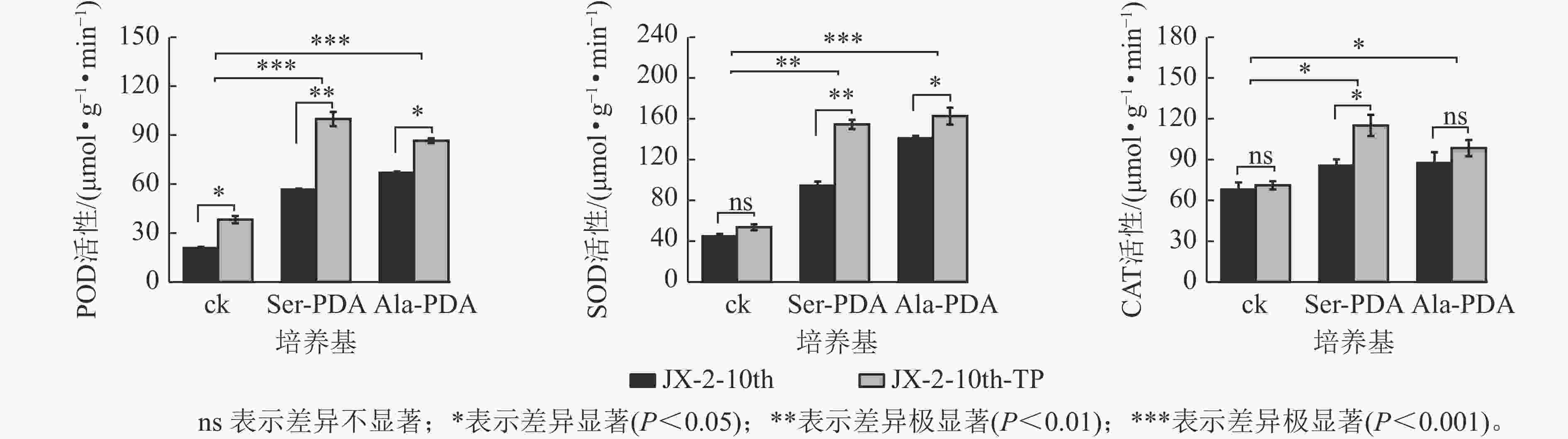
如图5所示:POD通过催化机体内过氧化氢发生氧化还原反应,清除体内H2O2。JX-2-10th-TP在PDA (ck)、Ser-PDA和Ala-PDA中培养的菌丝的POD活性均显著提高(P<0.05),分别比纯化前提高了84.20%、78.09%、29.41%。SOD主要通过催化超氧阴离子发生歧化反应,清除机体内积累的超氧阴离子。JX-2-10th-TP在ck的菌丝SOD活性较JX-2-10th提高了20.07%,在PDA+ Ser和PDA+Ala的培养基中,JX-2-10th-TP的SOD活性均显著提高(P<0.05),分别提高了63.70%、15.41%。CAT是主要承担机体内过氧化氢的分解,抑制过氧化氢堆积。JX-2-10th-TP在ck中培养的菌丝的CAT活性较JX-2-10th有所提高;在Ser-PDA培养基中,JX-2-10th-TP的SOD活性显著提高(P<0.05),比JX-2-10th提高34.56%;而在Ala-PDA培养基中,JX-2-10th-TP的SOD活性较JX-2-10th提高了12.56%,但未达显著差异。由上可知,尖端纯化能有效恢复退化秀珍菇菌株的抗氧化酶POD、SOD和CAT活性,且在Ser-PDA或Ala-PDA培养基中恢复效果更佳。
-
菌种质量在很大程度上决定了食用菌产量和品质。在工厂栽培时,退化菌种表现出菌丝稀疏、生长速率降低、子实体产量下降、优良性状丢失等现象[20−21],严重影响食用菌的经济效益。本研究发现:秀珍菇菌株JX-2连续传代过程中,随传代次数增加,菌丝生长速度减缓,证明多次的继代培养会引起秀珍菇种性的退化。退化菌种不可直接用于生产,改良培养基配方或外源物质的添加,可以在一定程度上延缓菌种退化或恢复已退化性状。许修宏等[22]发现:在液体培养基中添加磷酸二氢钾、维生素B1(VB1)、硫酸镁等外源物质可有效缓解黑木耳Auricularia auricula菌丝老化现象;王静等[23]发现:外源添加硫酸锰可恢复草菇退化菌种的菌丝生长速率和ROS清除能力;张凡红等[24]发现:外源丝氨酸可恢复草菇退化菌株的出菇能力,同时提高生长性状与营养物质含量。本研究通过前期预实验选择对退化秀珍菇菌株生理性状恢复效果最显著的Ser、Ala作为外源添加物质,发现多次传代后菌株退化特征有所缓解,菌丝生长速度、生物量较对照均显著提高,且Ser的提高效果更明显,证明Ser、Ala的添加可以延缓秀珍菇菌株生理性状的退化。此外也发现尖端纯化能够有效恢复退化秀珍菇菌株的生理指标,且在培养基中添加Ser、Ala后秀珍菇复壮菌株的生长速度及生物量的恢复效果更佳,纯化效果更明显。
食用菌中含有丰富的营养物质,菌种退化在一定程度上影响其营养物质含量[25]。多糖、蛋白是秀珍菇主要营养成分,秀珍菇菌丝体多糖对酒精性肝损伤有预防和保护效果[26];食用菌菌丝体蛋白质含量可与肉类媲美,且菌类蛋白在生产速度与经济效益上更具优势[27]。本研究表明:尖端纯化能够恢复秀珍菇菌株粗多糖及总蛋白含量,且在Ser-PDA培养基中,尖端纯化菌丝的粗多糖含量恢复效果更佳。Ser可以作为糖代谢途径中的中间产物或调节因子发挥作用。Ser可能参与磷酸戊糖途径,为多糖合成提供了重要的前体物质,如核糖-5-磷酸等[28]。这些前体物质进一步转化为合成多糖所需的单糖,从而促进粗多糖的合成。在Ala-PDA培养基中,尖端纯化菌丝的总蛋白含量恢复效果更佳。Ala是组成蛋白质的基本氨基酸之一,直接参与蛋白质的生物合成过程。培养基中添加Ala为蛋白质合成提供了充足的原料,有利于提高蛋白质含量。此外,Ala在细胞代谢中还可以调节代谢流,为蛋白质合成提供有利的代谢环境。Ala可以通过参与转氨基作用,将氨基转移给其他酮酸,生成新的氨基酸,从而维持细胞内氨基酸的平衡,保证各种氨基酸都能充足供应,以满足蛋白质合成的需要。同时,Ala代谢产生的能量和中间产物也可为蛋白质合成过程提供能量和物质支持。
ROS堆积是造成菌种退化的关键因素之一,随菌种退化程度增加,ROS在菌体内积累量上升,对菌株造成生理性毒害,致使菌种发生退化,优良性状丢失。LI等[29]发现在丝状真菌中,菌种多次继代培养后线粒体中ROS积累,造成氧化损伤是菌种退化的重要原因之一。抗氧化酶是ROS清除系统的重要部分,当ROS含量打破机体动态平衡时,抗氧化酶活性提高,清除体内积累的ROS,同时催化有毒物质分解,降低机体受到的氧化损伤[30]。本研究发现:尖端纯化后,有效提高菌株的SOD、POD和CAT活性,ROS含量明显下降;且在Ser-PDA培养基中纯化效果更为明显。Ser和Ala自身具有一定的氧化还原性,可以直接或间接参与细胞内的氧化还原反应。Ser的羟基和Ala的氨基等基团可以与ROS等自由基发生反应,将其转化为相对稳定的物质,从而减轻氧化应激对细胞的损伤。同时,它们的代谢产物也可能参与到细胞内的抗氧化防御网络中,间接提高抗氧化酶的活性[31−33]。由此推断,2种氨基酸的添加提供机体抗氧化性,提高ROS清除系统的清除效率,维持体内ROS处于低水平、动态平衡状态。
-
本研究证实连续多次的继代培养会引起秀珍菇种性的退化,菌株JX-2连续继代培养至第10代时,与初代菌株相比,其菌丝生长速度显著下降15.45%,生物量降低28.67%。Ser、Ala能够一定程度延缓菌种退化,在添加2 g·L−1 Ser或Ala的培养基中继代培养的菌株,相比于对照,菌丝生长速度分别提高7.14%、4.76%,生物量提高37.50%、22.50%。此外,本研究证实尖端纯化能够恢复退化菌株生理指标。在PDA培养基中进行尖端纯化后,菌丝生物量提升17.17%,粗多糖和总蛋白含量分别增加30.66%、30.50%,抗氧化指标也得到显著改善,其中POD活性提高84.20%,SOD活性提升20.07%。在Ser-PDA培养基中,复壮效果更为突出,生物量提升幅度高达57.77%,SOD活性提高63.70%;而在Ala-PDA培养基中,总蛋白含量增加32.01%。本研究可为后续解决秀珍菇菌种稳定性差、易退化的问题提供参考。
Effect of serine and alanine on degeneration and rejuvenation of Pleurotus pulmonarius spawn
doi: 10.11833/j.issn.2095-0756.20250216
- Received Date: 2025-03-20
- Accepted Date: 2025-09-10
- Rev Recd Date: 2025-05-12
-
Key words:
- subculturing /
- hyphal tip purification /
- nutritional components /
- reactive oxygen species (ROS) /
- antioxidant enzymes
Abstract:
| Citation: | YE Liyun, FENG Haiying, WU Xiaoping. Effect of serine and alanine on degeneration and rejuvenation of Pleurotus pulmonarius spawn[J]. Journal of Zhejiang A&F University, 2025, 42(X): 1−8 doi: 10.11833/j.issn.2095-0756.20250216 |









 DownLoad:
DownLoad: